ν = S Fysiikka III (ES) Tentti Ratkaisut
|
|
|
- Marja Koskinen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 S-45 Fysiikka III (ES) etti 8500 Ratkaisut Ideaalikaasu suorittaa oheise kua esittämä kiertoprosessi abca Pisteessä a lämpötila o 0 K a) Kuika mota moolia kaasua o? b) Määritä kaasu lämpötila pisteissä b ja c c) Määritä kaasu kiertoprosessissa saama lämpömääräratkaisu p/kpa 75 b a = 0 K 5 a c a) ilayhtälöstä: = νr ν = R 0 0 /m 5 0 N m 0 m ν 67 mol 4 mol K ( ) x pxx pxx b) Edellee tilayhtälöstä: = = x = a ν R a a a a a missä x o diagrammi piste Saadaa b c K 980 K K 660 K c) pääsääö mukaa U = Q W = 0 koska kiertoprosessissa palataa alkutilaa Systeemi kiertoprosessissa saama lämpömäärä o siis yhtä suuri kui systeemi tekemä työ eli Q = W yö saadaa diagrammista määrittämällä kiertoprosessia kuaaa silmuka sisää jäää fysikaalie pita-ala: N Q = W = ( c a)( pb pc) 0 m k m Yksi mooli N-kaasua o termodyaamisessa tasapaiotilassa lämpötilassa 000 K a) Laske traslaatio rotaatio ja ärähtely osuus kaasu sisäeergiassa b) Laske astaaat osuudet kaasu moolisessa omiaislämmössä Atomie älimatka N-molekyylissä o 058 m ja sidokse oimaakio 6 0 N/m Ratkaisu N = 000 K r o = 058 m γ = 6 0 N/m m = 0 u m N = 40 u ν = 00 Lasketaa esi rotaatio ja ärähtely karakteristiset lämpötilat mm µ = I = µro Θr = = m + m Ik µrok mm N kg µ = kg m + m N
2 Θ r Θ 4 ( s) ( ) kg m 8 0 K ω γ k k µ s 6 0 Nm 8 0 K kg 4 o = = 6 a) Yhtälöstä (549): 795 K 975 K U tr = ν NAk 00 mol K 74 k Urot = ν NAk 49 k (oidaa käyttää tätä tulosta koska >> Θ r ) kνnaθ Uib = νnakθ + = νnakθ Θ + Θ e e 00 mol K e 4 k ästä suuri osa o s ollapiste-eergiaa joka tulee termistä Uib = ( / ) ν NAk Θ joka ei riipu lämpötilasta ja joka ei tästä syystä aikuta kaasu termodyaamisii omiaisuuksii U b) Mooliset lämpökapasiteetit saadaa yhtälöstä = ν : tr = NAk = R 84 5 rot = NAk = R 8 Θ Θ e ib = R e Θ ( ) e ( e ) Matalie lämpötiloje ( << Θ ) approksimaatiosta saadaa tällä tarkkuudella sama tulos: Θ e ib Θ Θ Θ = R R e Θ ( e ) oimme päätellä että 000 K lämpötilassa N-kaasu ärähtelyapausasteet o irittyeet ai hyi ähäisessä määri
3 Ideaalikaasu paie o 00 kpa lämpötila 00 K ja tilauus 0 litraa Kaasu puristetaa polytrooppisesti 5-kertaisee paieesee prosessissa joka polytrooppiakio o τ = 0 Laske a) tarittaa työ ja b) kaasu saama lämpömäärä Kaasu adiabaattiakio γ = 40 (a) Polytrooppiselle prosessille τ τ = akio = a p = a z a τ W = pd = e τ + τ+ Sijoittamalla akio a saadaa τ τ a = = p W = p τ b g j F p = H G / τ I / τ p K = = = dm W 07 (b) Lasketaa loppulämpötila ideaalikaasu tilayhtälö perusteella: = = = 9 K Omiaislämmö määritelmä mukaa Q= ν τ ( ) missä polytrooppise prosessi moolie lämpökapasiteetti o R τ = + τ Määrätää seuraaaksi Yhtälöistä p U = γ p = RW = 5 R ts kyseessä o kaksiatomisista molekyyleistä koostua kaasu joka traslaatio- ja rotaatioapausasteet oat irittyeet Sijoittamalla saadaa τ = 5 R Moolie lukumäärä o tilayhtälö aulla ν = = 0080 aasu saamaksi lämpömääräksi R saadaa Q = 50 ; ts kaasu luouttaa lämpöä 4 Kilo että joka lämpötila o 0 0 asetetaa kosketuksee suure 00 0 asteise kappalee kassa Ku ede lämpötila o oussut 00 0 mitkä oat ede kappalee ja uiersumi etropia muutokset? Oletetetaa seuraaaksi että ede kuumetamie 00 0 tapahtuu saattamalle se esi kosketuksee suure 50 0 asteise kappalee kassa ja sitte 00 0 asteise kappalee kassa Mikä oat yt ede ja uiersumi etropia muutokset? Selitä mite esi oidaa kuumetaa 0 0 asteesta 00 0
4 asteesee ilma että uiersumi etropia kasaa ede moolimassa o 8g ja - - omiaislämpö akiopaieessa c p = 8 0cal K mol (a) Lasketaa lämpömäärät omiaislämpöje aulla asoittumie tapahtuu akiopaieessa (ilmakehä paie) jote esi saa lämpömäärä Q = c - = 00 0 kcal esi p b g Kappale luouttaa astaaa lämpömäärä Qbody =- Qesi ede etropiamuutos lasketaa isobaariselle prosessille yhtälöstä DS esi = cp l - = calk Kappalee etropiamuutos oidaa laskea isotermiselle prosessille sillä kappalee lämpötila muutos o suuresta massasta johtue hyi piei Qbody - S - S = DS body = = -68 calk Etropia kokoaismuutos o siis DSO = DS + DS = + 44 calk (b) Oletetaa että prosessi tapahtuu yt kahdessa aiheessa edelle saadaa ( i = 50 0 ) esi body - DS c i esi = p l cp cp + l = l i ts ede etropia lisäys o sama kui edellä Kappaleelle saadaa etropia muutos Q DS esi / Qesi / - body =- - =-88 9calK i ja etropia kokoaismuutos DS O = calk Etropia lisäys o siis pieempi kui edellä (c) Rajatapauksea oidaa ajatella ede saattamista kotaktii äärettömä moe kappalee kassa joista kuki lämpötila o ai hiema ede lämpötilaa korkeampi Etropia muutos läheee tällöi ollaa ts kyseessä o reersiibeli prosessi 5 arkastellaa systeemiä jossa kullaki hiukkasella o kolme mahdollista eergiatasoa 0 ε ja ε missä ε o eräs akio Oletetaa että systeemi oudattaa Maxwell-Boltzma jakaumaa ja että tiloilla ei ole sisäistä eergiariippumatota apausastetta ( g i = ) Systeemissä o 4000 hiukkasta ja se kokoaiseergia o 00ε Käyttäe Maxwell- Boltzma jakaumaa laske termodyaamista tasapaiotilaa astaaat miehitysluut Miehitysluuille oidaa kirjoittaa Maxwell Boltzma jakauma mukaa -
5 α β 0 α = e = e α βε = e α βε = e Merkitsemällä x + x+ x = 4000 ja kokoaiseergiaksi ( x) ε + ( x )ε = 600ε = e βε saamme miehityslukuje summa muodossa jaetaa yhtälöt keskeää jolloi saadaa x+ x = x+ x 600 Ratkaisemalla toise astee yhtälöstä yhtälöstä x = 0507 (ai positiiie juuri kelpaa miksi?) Sijoittamalla yt x takaisi miehityslukuihi saamme = 77 = 46 = 577 missä pyöristimme tulokse kokoaisluuiksi site että hiukkaste kokoaismäärä o Yksi mooli itrobezeeiä (6H5NO) höyrystyy 48 K lämpötilassa ja 0 bari paieessa Höyrystymislämpö o 979 cal/mol Laske höyrystyee itrobezeei a) saama lämpömäärä Q b) tekemä työ W c) sisäeergia muutos DU ja d) DS a) Kappalee saama lämpömäärä o juuri höyrystymislämpö eli 979 cal/mol b) Ku osa systeemii kuuluasta estemäisestä itrobetzeeistä kaasuutuu se joutuu raiaamaa itsellee lisää tilaa eli tekemää työtä ulkoista 0 bari paietta astaa Nitrobetzeeikaasu tilauus paljo suurempi kui estee tilauus (ertaa esimerkiksi esi) oimme myös olettaa karkeasti että höyrystyyt itrobezeei o ideaalikaasua Systeemi tilauude muutos o siis yhde ideaalikaasumooli tilauus 48 K lämpötilassa eli ideaalikaasu tilayhtälö mukaa = ν R / p = 406 litraa ästä saamme kaasu tekemäksi laajetumistyöksi W = p = 406 k = 959 cal c) Sisäeergia muutos o saatu lämpömäärä tehty työ eli 877 cal d) Kaasuutumie tapahtuu akiolämpötilassa jolloi etropia muutos o S = Q/ = 0 cal/k
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
n = = RT S Tentti
 S-5 Tetti 500 a) Kuika suuri o molekyylie traslaatioliikkee kieettie eergia kuutiometrissä ilmaa jos ilma lämpötila o 00 K ja paie 0 bar? b) Mikä o kieettise eergia kokoaismäärä ku myös muut liikelajit
S-5 Tetti 500 a) Kuika suuri o molekyylie traslaatioliikkee kieettie eergia kuutiometrissä ilmaa jos ilma lämpötila o 00 K ja paie 0 bar? b) Mikä o kieettise eergia kokoaismäärä ku myös muut liikelajit
LIITTEET Liite A Stirlingin kaavan tarkkuudesta...2. Liite B Lagrangen kertoimet...3
 LIITTEET... 2 Liite A Stirligi kaava tarkkuudesta...2 Liite B Lagrage kertoimet... 2 Liitteet Liitteet Liite A Stirligi kaava tarkkuudesta Luoollista logaritmia suureesta! approksimoidaa usei Stirligi
LIITTEET... 2 Liite A Stirligi kaava tarkkuudesta...2 Liite B Lagrage kertoimet... 2 Liitteet Liitteet Liite A Stirligi kaava tarkkuudesta Luoollista logaritmia suureesta! approksimoidaa usei Stirligi
0 C lämpötilaan antaa 836 kj. Lopputuloksena on siis vettä lämpötilassa, joka on suurempi kuin 0 0 C.
 LH12-1 1 kg 2 C asteista vettä sekoitetaa yhde baari paieessa 2kg jäätä, joka lämpötila o -5 C Laske etropia muutos ja lämpötila, ku tasapaio o saavutettu 3 3 Vedelle c p 4,18 1 J/(kgK) jäälle c p 2, 9
LH12-1 1 kg 2 C asteista vettä sekoitetaa yhde baari paieessa 2kg jäätä, joka lämpötila o -5 C Laske etropia muutos ja lämpötila, ku tasapaio o saavutettu 3 3 Vedelle c p 4,18 1 J/(kgK) jäälle c p 2, 9
Vauhti = nopeuden itseisarvo. Nopeuden itseisarvon keskiarvo N:lle hiukkaselle määritellään yhtälöllä
 S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
Integroimalla ja käyttämällä lopuksi tilanyhtälöä saadaan T ( ) ( ) H 5,0 10 J + 2,0 10 0,50 1,0 10 0,80 Pa m 70 kj
 S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S , Fysiikka III (ES) Tentti Tentti / välikoeuusinta
 S-11435, Fysiikka III (ES) entti 4113 entti / välikoeuusinta I Välikokeen alue 1 Viiden tunnistettavissa olevan identtisen hiukkasen mikrokanonisen joukon käytettävissä on neljä tasavälistä energiatasoa,
S-11435, Fysiikka III (ES) entti 4113 entti / välikoeuusinta I Välikokeen alue 1 Viiden tunnistettavissa olevan identtisen hiukkasen mikrokanonisen joukon käytettävissä on neljä tasavälistä energiatasoa,
( ) ( ) on nimeltään molekyylisironnan mikroskooppinen vaikutusala). Sijoittamalla numeroarvot saadaan vapaaksi matkaksi
 S-4.35, FYSIIKKA III, Syksy 00, LH, Loppuiikko 38 LH-* Laske happimolekyylin keskimääräinen apaa matka 300 K lämpötilassa ja,0 baarin paineessa. Voit olettaa, että molekyyli on pallon muotoinen ja pallon
S-4.35, FYSIIKKA III, Syksy 00, LH, Loppuiikko 38 LH-* Laske happimolekyylin keskimääräinen apaa matka 300 K lämpötilassa ja,0 baarin paineessa. Voit olettaa, että molekyyli on pallon muotoinen ja pallon
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
V T p pv T pv T. V p V p p V p p. V p p V p
 S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
S , Fysiikka III (S) I välikoe Malliratkaisut
 S-4.35, Fysiikka III (S) I välikoe 9.0.000 Malliratkaisut Tehtävä Kuution uotoisessa säiliössä, jonka särän pituus on 0,0, on 3,0 0 olekyyliä happea (O) 300 K läpötilassa. a) Kuinka onta kertaa kukin olekyyli
S-4.35, Fysiikka III (S) I välikoe 9.0.000 Malliratkaisut Tehtävä Kuution uotoisessa säiliössä, jonka särän pituus on 0,0, on 3,0 0 olekyyliä happea (O) 300 K läpötilassa. a) Kuinka onta kertaa kukin olekyyli
1. (Jatkoa Harjoitus 5A tehtävään 4). Monisteen esimerkin mukaan momenttimenetelmän. n ne(y i Y (n) ) = 2E(Y 1 Y (n) ).
 HY / Matematiika ja tilastotietee laitos Tilastollie päättely II, kevät 018 Harjoitus 5B Ratkaisuehdotuksia Tehtäväsarja I 1. (Jatkoa Harjoitus 5A tehtävää ). Moistee esimerki 3.3.3. mukaa momettimeetelmä
HY / Matematiika ja tilastotietee laitos Tilastollie päättely II, kevät 018 Harjoitus 5B Ratkaisuehdotuksia Tehtäväsarja I 1. (Jatkoa Harjoitus 5A tehtävää ). Moistee esimerki 3.3.3. mukaa momettimeetelmä
dx = d dψ dx ) + eikx (ik du u + 2ike e ikx u i ike ikx u + e udx
 763333A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 5 Kevät 2014 1. Tehtävä: Johda luetomateriaali kaavat d 2 u i k du 2 m + Uxu = E k 2 u p = k + u x i d ux. Ratkaisu: Oletetaa, että ψx = e ikx ux, missä ux +
763333A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 5 Kevät 2014 1. Tehtävä: Johda luetomateriaali kaavat d 2 u i k du 2 m + Uxu = E k 2 u p = k + u x i d ux. Ratkaisu: Oletetaa, että ψx = e ikx ux, missä ux +
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
( ) k 1 = a b. b 1) Binomikertoimen määritelmän mukaan yhtälön vasen puoli kertoo kuinka monta erilaista b-osajoukkoa on a-joukolla.
 Kombiatoriikka, kesä 2010 Harjoitus 2 Ratkaisuehdotuksia (RT) (5 sivua) Käytä tehtävissä 1-3 kombiatorista päättelyä. 1. Osoita, että kaikilla 0 b a pätee ( ) a a ( ) k 1 b b 1 kb Biomikertoime määritelmä
Kombiatoriikka, kesä 2010 Harjoitus 2 Ratkaisuehdotuksia (RT) (5 sivua) Käytä tehtävissä 1-3 kombiatorista päättelyä. 1. Osoita, että kaikilla 0 b a pätee ( ) a a ( ) k 1 b b 1 kb Biomikertoime määritelmä
i ni 9 = 84. Todennäköisin partitio on partitio k = 6, k k
 1. Neljä tuistettavissa oleva hiuase iroaoise jouo ahdolliset eergiatasot ovat 0, ε, ε, ε, 4ε,, jota aii ovat degeeroituattoia. Systeei ooaiseergia o 6ε. sitä aii ahdolliset partitiot ja osoita, että irotiloje
1. Neljä tuistettavissa oleva hiuase iroaoise jouo ahdolliset eergiatasot ovat 0, ε, ε, ε, 4ε,, jota aii ovat degeeroituattoia. Systeei ooaiseergia o 6ε. sitä aii ahdolliset partitiot ja osoita, että irotiloje
Miehitysluvuille voidaan kirjoittaa Maxwell Boltzmann jakauman mukaan. saamme miehityslukujen summan muodossa
 S-4.7 Fysiia III (EST) Tetti..6. Tarastellaa systeemiä, jossa ullai hiuasella o olme mahdollista eergiatasoa, ε ja ε, missä ε o eräs vaio. Oletetaa, että systeemi oudattaa Maxwell-Boltzma jaaumaa ja, että
S-4.7 Fysiia III (EST) Tetti..6. Tarastellaa systeemiä, jossa ullai hiuasella o olme mahdollista eergiatasoa, ε ja ε, missä ε o eräs vaio. Oletetaa, että systeemi oudattaa Maxwell-Boltzma jaaumaa ja, että
S Fysiikka III (EST) Tentti ja välikoeuusinta
 S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
j = I A = 108 A m 2. (1) u kg m m 3, (2) v =
 764A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 6 Kevät 28. Tehtävä: Aiemmi olemme laskeeet kupari johtavuuselektroie tiheydeksi 8.5 28 m. Kuparijohdossa, joka poikkipita-ala o mm 2, kulkee A: virta. Arvioi Drude
764A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 6 Kevät 28. Tehtävä: Aiemmi olemme laskeeet kupari johtavuuselektroie tiheydeksi 8.5 28 m. Kuparijohdossa, joka poikkipita-ala o mm 2, kulkee A: virta. Arvioi Drude
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
766328A Termofysiikka Harjoitus no. 10, ratkaisut (syyslukukausi 2014)
 7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
Entalpia - kuvaa aineen lämpösisältöä - tarvitaan lämpötasetarkasteluissa (usein tärkeämpi kuin sisäenergia)
 Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Nyt n = 1. Tästä ratkaistaan kuopan leveys L ja saadaan sijoittamalla elektronin massa ja vakiot
 S-1146 Fysiikka V (ES) Tentti 165005 1 välikokeen alue 1 a) Rubiinilaserin emittoiman valon aallonpituus on 694, nm Olettaen että fotonin emissioon tällä aallonpituudella liittyy äärettömän potentiaalikuopan
S-1146 Fysiikka V (ES) Tentti 165005 1 välikokeen alue 1 a) Rubiinilaserin emittoiman valon aallonpituus on 694, nm Olettaen että fotonin emissioon tällä aallonpituudella liittyy äärettömän potentiaalikuopan
Kaasu 2-atominen. Rotaatio ja translaatiovapausasteet virittyneet (f=5) c. 5 Ideaalikaasun tilanyhtälöstä saadaan kaasun moolimäärä: 3
 S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
763306A JOHDATUS SUHTEELLISUUSTEORIAAN 2 Ratkaisut 4 Kevät 2017
 763306A JOHDATUS SUHTEELLISUUSTEORIAAN 2 Ratkaisut 4 Keät 207. Rekyyli Luentomonisteessa on käsitelty tilanne, jossa hiukkanen (massa M) hajoaa kahdeksi hiukkaseksi (massat m ja m 2 ). Tässä käytetään
763306A JOHDATUS SUHTEELLISUUSTEORIAAN 2 Ratkaisut 4 Keät 207. Rekyyli Luentomonisteessa on käsitelty tilanne, jossa hiukkanen (massa M) hajoaa kahdeksi hiukkaseksi (massat m ja m 2 ). Tässä käytetään
:n perustilaan energiasta. e) Elektronien ja ytimien välinen vuorovaikutusenergia H 2
 S-11446 Fysiikka IV (Sf), II Välikoe 15 1 H vetyioi perustila eergia (ytimie välimatka 1,6 Å) verrattua systeemii, jossa perustilassa oleva vetyatomi ja H -ioi ovat äärettömä kaukaa toisistaa o,65 ev Laske
S-11446 Fysiikka IV (Sf), II Välikoe 15 1 H vetyioi perustila eergia (ytimie välimatka 1,6 Å) verrattua systeemii, jossa perustilassa oleva vetyatomi ja H -ioi ovat äärettömä kaukaa toisistaa o,65 ev Laske
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
Oletetaan kaasu ideaalikaasuksi ja sovelletaan Daltonin lakia. Kumpikin seoksen kaasu toteuttaa erikseen ideaalikaasun tilanyhtälön:
 S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
1 Eksponenttifunktion määritelmä
 Ekspoettifuktio määritelmä Selvitimme aikaisemmi tällä kurssilla, millaie potessisarja säilyy derivoiissa muuttumattomaa. Se perusteella määritellää: Määritelmä. Ekspoettifuktio exp : R R määritellää lausekkeella
Ekspoettifuktio määritelmä Selvitimme aikaisemmi tällä kurssilla, millaie potessisarja säilyy derivoiissa muuttumattomaa. Se perusteella määritellää: Määritelmä. Ekspoettifuktio exp : R R määritellää lausekkeella
6. Yhteenvetoa kurssista
 Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Termodynaamiset syklit Todelliset tehosyklit
 ermodynaamiset syklit odelliset tehosyklit Luennointi: k Kati Miettunen Esitysmateriaali: k Mikko Mikkola HYS-A00 ermodynamiikka (FM) 09..05 Syklien tyypit Sisältö Kaasusyklit s. höyrysyklit Suljetut syklit
ermodynaamiset syklit odelliset tehosyklit Luennointi: k Kati Miettunen Esitysmateriaali: k Mikko Mikkola HYS-A00 ermodynamiikka (FM) 09..05 Syklien tyypit Sisältö Kaasusyklit s. höyrysyklit Suljetut syklit
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
S Fysiikka III (EST), Tentti
 S-114.137 Fysiikk III (ES), entti 30.8.006 1. Lämpövoimkone toteutt oheisen kuvn Crnotin prosessi. Koneess on työineen yksi mooli ideliksu. Lske yksitomisen ksun kierroksen ikn tekemän työn suhde kksitomisen
S-114.137 Fysiikk III (ES), entti 30.8.006 1. Lämpövoimkone toteutt oheisen kuvn Crnotin prosessi. Koneess on työineen yksi mooli ideliksu. Lske yksitomisen ksun kierroksen ikn tekemän työn suhde kksitomisen
Mikrotila Makrotila Statistinen paino Ω(n) 3 Ω(3) = 4 2 Ω(2) = 6 4 Ω(4) = 1
 76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Tällaisessa tapauksessa on usein luontevaa samaistaa (u,v)-taso (x,y)-tason kanssa, jolloin tason parametriesitys on *** VEKTORIANALYYSI.
 39 VEKTORIANALYYI Luento 6 5. Pinnat ja pintaintegraalit Pintojen parametriesitys. Aikaisemmin käsittelimme käyrän esittämistä parametrimuodossa. iihen riitti yksi reaalinen parametri (t), joka sai aroja
39 VEKTORIANALYYI Luento 6 5. Pinnat ja pintaintegraalit Pintojen parametriesitys. Aikaisemmin käsittelimme käyrän esittämistä parametrimuodossa. iihen riitti yksi reaalinen parametri (t), joka sai aroja
Algebra I Matematiikan ja tilastotieteen laitos Ratkaisuehdotuksia harjoituksiin 5 (6 sivua)
 Algebra I Matematiika ja tilastotietee laitos Ratkaisuehdotuksia harjoituksii 5 (6 sivua) 14.2. 17.2.2011 1. Määritellää kuvaus f : S 3 S 3, f(α) = (123) α. Osoita, että f o bijektio. Mikä o se kääteiskuvaukse
Algebra I Matematiika ja tilastotietee laitos Ratkaisuehdotuksia harjoituksii 5 (6 sivua) 14.2. 17.2.2011 1. Määritellää kuvaus f : S 3 S 3, f(α) = (123) α. Osoita, että f o bijektio. Mikä o se kääteiskuvaukse
HEIJASTUMINEN JA TAITTUMINEN
 S-08-0 OPTIIKKA /6 HEIJASTUMINEN JA TAITTUMINEN Laboratoriotyö S-08-0 OPTIIKKA /6 Sisällysluettelo Teoria... 3 Työ suoritus... 4. Kokoaisheijastus... 4. Brewsteri kulma... 5 3 Mittauspöytäkirja... 6 S-08-0
S-08-0 OPTIIKKA /6 HEIJASTUMINEN JA TAITTUMINEN Laboratoriotyö S-08-0 OPTIIKKA /6 Sisällysluettelo Teoria... 3 Työ suoritus... 4. Kokoaisheijastus... 4. Brewsteri kulma... 5 3 Mittauspöytäkirja... 6 S-08-0
E p1 = 1 e 2. e 2. E p2 = 1. Vuorovaikutusenergian kolme ensimmäistä termiä on siis
 763343A IINTEÄN AINEEN FYSIIA Ratkaisut 3 evät 2017 1. Tehtävä: CsCl muodostuu Cs + - ja Cl -ioneista, jotka asettuvat tilakeskeisen rakenteen vuoropaikoille (kuva). Laske tämän rakenteen Madelungin vakion
763343A IINTEÄN AINEEN FYSIIA Ratkaisut 3 evät 2017 1. Tehtävä: CsCl muodostuu Cs + - ja Cl -ioneista, jotka asettuvat tilakeskeisen rakenteen vuoropaikoille (kuva). Laske tämän rakenteen Madelungin vakion
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
8. Klassinen ideaalikaasu
 Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
Wien R-J /home/heikki/cele2008_2010/musta_kappale_approksimaatio Wed Mar 13 15:33:
 1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
Tehtäviä neliöiden ei-negatiivisuudesta
 Tehtäviä epäyhtälöistä Tehtäviä eliöide ei-egatiivisuudesta. Olkoo a R. Osoita, että 4a 4a. Ratkaisu. 4a 4a a) a 0 a ) 0.. Olkoot a,, R. Osoita, että a a a. Ratkaisu. Kerrotaa molemmat puolet kahdella:
Tehtäviä epäyhtälöistä Tehtäviä eliöide ei-egatiivisuudesta. Olkoo a R. Osoita, että 4a 4a. Ratkaisu. 4a 4a a) a 0 a ) 0.. Olkoot a,, R. Osoita, että a a a. Ratkaisu. Kerrotaa molemmat puolet kahdella:
Rekursioyhtälön ratkaisu ja anisogamia
 Rekursioyhtälö ratkaisu ja aisogamia Eeva Vilkkumaa.0.2008 Rekursioyhtälö ratkaisu (Liite I) Edellie esitelmä: +/m -koiraide (p) ja -aaraide (P) osuus populaatiossa kehittyy rekursiivisesti: p P + + a
Rekursioyhtälö ratkaisu ja aisogamia Eeva Vilkkumaa.0.2008 Rekursioyhtälö ratkaisu (Liite I) Edellie esitelmä: +/m -koiraide (p) ja -aaraide (P) osuus populaatiossa kehittyy rekursiivisesti: p P + + a
S , Fysiikka III (ES) Tentti Tentti / välikoeuusinta. Laaditaan taulukko monisteen esimerkin 3.1. tapaan ( nj njk Pk
 S-.35, Fysiia III (ES) entti 8..3 entti / välioeuusinta I älioeen alue. Neljän tunnistettavissa olevan hiuasen miroanonisen jouon mahdolliset energiatasot ovat, ε, ε, 3ε, ε,, jota aii ovat degeneroitumattomia.
S-.35, Fysiia III (ES) entti 8..3 entti / välioeuusinta I älioeen alue. Neljän tunnistettavissa olevan hiuasen miroanonisen jouon mahdolliset energiatasot ovat, ε, ε, 3ε, ε,, jota aii ovat degeneroitumattomia.
8. laskuharjoituskierros, vko 11, ratkaisut
 Mat-2.091 Sovellettu todeäköisyyslasku, kevät -05 Heliövaara, Palo, Melli 8. laskuharjoituskierros, vko 11, ratkaisut D1. Oletetaa, että havaiot X i, i = 1, 2,..., 100 muodostavat yksikertaise satuaisotokse
Mat-2.091 Sovellettu todeäköisyyslasku, kevät -05 Heliövaara, Palo, Melli 8. laskuharjoituskierros, vko 11, ratkaisut D1. Oletetaa, että havaiot X i, i = 1, 2,..., 100 muodostavat yksikertaise satuaisotokse
763306A JOHDATUS SUHTEELLISUUSTEORIAAN 2 Ratkaisut 3 Kevät E 1 + c 2 m 2 = E (1) p 1 = P (2) E 2 1
 763306A JOHDATUS SUHTLLISUUSTORIAAN Ratkaisut 3 Kevät 07. Fuusioreaktio. Lähdetään suoraan annetuista yhtälöistä nergia on suoraan yhtälön ) mukaan + m ) p P ) m + p 3) M + P 4) + m 5) Ratkaistaan seuraavaksi
763306A JOHDATUS SUHTLLISUUSTORIAAN Ratkaisut 3 Kevät 07. Fuusioreaktio. Lähdetään suoraan annetuista yhtälöistä nergia on suoraan yhtälön ) mukaan + m ) p P ) m + p 3) M + P 4) + m 5) Ratkaistaan seuraavaksi
Käytetään lopuksi ideaalikaasun tilanyhtälöä muutoksille 1-2 ja 3-1. Muutos 1-2 on isokorinen, joten tilanyhtälöstä saadaan ( p2 / p1) = ( T2 / T1)
 LH0- Lämövoimakoneen kiertorosessin vaiheet ovat: a) Isokorinen aineen kasvu arvosta arvoon 2, b) adiabaattinen laajeneminen, jolloin aine laskee takaisin arvoon ja tilavuus kasvaa arvoon 3 ja c) isobaarinen
LH0- Lämövoimakoneen kiertorosessin vaiheet ovat: a) Isokorinen aineen kasvu arvosta arvoon 2, b) adiabaattinen laajeneminen, jolloin aine laskee takaisin arvoon ja tilavuus kasvaa arvoon 3 ja c) isobaarinen
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
S-114.425 FYSIIKKA III (Sf) Syksy 2004, LH 2. Ratkaisut
 S-445 FYSIIKKA III (Sf) Syksy 4, LH Ratkaisut LHSf-* Tarkastellaa metallii tehtyä oteloa, jossa o vakuumi (tyhjö) Voidaa osoittaa, että vakuumi täyttää sähkömageettise ketä kvattie eli fotoie muodostama
S-445 FYSIIKKA III (Sf) Syksy 4, LH Ratkaisut LHSf-* Tarkastellaa metallii tehtyä oteloa, jossa o vakuumi (tyhjö) Voidaa osoittaa, että vakuumi täyttää sähkömageettise ketä kvattie eli fotoie muodostama
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
η = = = 1, S , Fysiikka III (Sf) 2. välikoe
 S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Ydin- ja hiukkasfysiikka 2014: Harjoitus 5 Ratkaisut 1
 Ydin- ja hiukkasfysiikka 04: Harjoitus 5 Ratkaisut Tehtävä a) Vapautunut energia saadaan laskemalla massan muutos reaktiossa: E = mc = [4(M( H) m e ) (M( 4 He) m e ) m e ]c = [4M( H) M( 4 He) 4m e ]c =
Ydin- ja hiukkasfysiikka 04: Harjoitus 5 Ratkaisut Tehtävä a) Vapautunut energia saadaan laskemalla massan muutos reaktiossa: E = mc = [4(M( H) m e ) (M( 4 He) m e ) m e ]c = [4M( H) M( 4 He) 4m e ]c =
Dynaamisten systeemien teoriaa. Systeemianalyysilaboratorio II
 Dynaamisten systeemien teoriaa Systeemianalyysilaboratorio II 15.11.2017 Vakiot, sisäänmenot, ulostulot ja häiriöt Mallin vakiot Systeemiparametrit annettuja vakioita, joita ei muuteta; esim. painovoiman
Dynaamisten systeemien teoriaa Systeemianalyysilaboratorio II 15.11.2017 Vakiot, sisäänmenot, ulostulot ja häiriöt Mallin vakiot Systeemiparametrit annettuja vakioita, joita ei muuteta; esim. painovoiman
NESTEIDEN ja ja KAASUJEN MEKANIIKKA
 NESTEIDEN ja KSUJEN MEKNIIKK Väliaineen astus Kaaleen liikkuessa nesteessä tai kaasussa, kaaleeseen törmääät molekyylit ja aine-erot erot aiheuttaat siihen liikkeen suunnalle astakkaisen astusoiman, jonka
NESTEIDEN ja KSUJEN MEKNIIKK Väliaineen astus Kaaleen liikkuessa nesteessä tai kaasussa, kaaleeseen törmääät molekyylit ja aine-erot erot aiheuttaat siihen liikkeen suunnalle astakkaisen astusoiman, jonka
Ekvipartitioperiaatteen mukaisesti jokaiseen efektiiviseen vapausasteeseen liittyy (1 / 2)kT energiaa molekyyliä kohden.
 . Hiilidioksidiolekyyli CO tiedetään lineaariseksi a) Mitkä ovat eteneisliikkeen, pyöriisliikkeen ja värähtelyn suuriat ekvipartitioperiaatteen ukaiset läpöenergiat olekyyliä kohden, kun kaikki vapausasteet
. Hiilidioksidiolekyyli CO tiedetään lineaariseksi a) Mitkä ovat eteneisliikkeen, pyöriisliikkeen ja värähtelyn suuriat ekvipartitioperiaatteen ukaiset läpöenergiat olekyyliä kohden, kun kaikki vapausasteet
Luku 12 THERMODYNAAMISTEN OMINAISUUKSIEN YHTÄLÖT
 hermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 011 Luku 1 HERMODYNAAMISEN OMINAISUUKSIEN YHÄLÖ Copyright he McGraw-Hill Companies, Inc. ermission required
hermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 011 Luku 1 HERMODYNAAMISEN OMINAISUUKSIEN YHÄLÖ Copyright he McGraw-Hill Companies, Inc. ermission required
Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2012 Insinöörivalinnan fysiikan koe 30.5.2012, malliratkaisut
 A1 Kappale, jonka massa m = 2,1 kg, lähtee liikkeelle levosta paikasta x = 0,0 m pitkin vaakasuoraa alustaa. Kappaleeseen vaikuttaa vaakasuora vetävä voima F, jonka suuruus riippuu paikasta oheisen kuvan
A1 Kappale, jonka massa m = 2,1 kg, lähtee liikkeelle levosta paikasta x = 0,0 m pitkin vaakasuoraa alustaa. Kappaleeseen vaikuttaa vaakasuora vetävä voima F, jonka suuruus riippuu paikasta oheisen kuvan
(c) Kuinka suuri suhteellinen virhe painehäviön laskennassa tehdään, jos virtaus oletetaan laminaariksi?
 Tehtävä 1 Vettä (10 astetta) virtaa suorassa valurautaisessa (cast iron) putkessa, jonka sisähalkaisija on 100 mm ja pituus 70 m. Tilavuusvirta on 15 litraa minuutissa. (a) Osoita, että virtaus on turbulenttia.
Tehtävä 1 Vettä (10 astetta) virtaa suorassa valurautaisessa (cast iron) putkessa, jonka sisähalkaisija on 100 mm ja pituus 70 m. Tilavuusvirta on 15 litraa minuutissa. (a) Osoita, että virtaus on turbulenttia.
S , FYSIIKKA III (ES), Syksy 2002, LH 4, Loppuviikko 39. Partitiofunktiota käyttäen keskiarvo voidaan kirjoittaa muotoon
 S-11435, FYSIIKKA III (ES), Syksy 00, LH 4, Loppuvkko 39 LH4-1* Käyttän Maxwll-Boltzmann-jakauman parttofunktota määrtä a) nrgan nlön kskarvo (E ) skä b) nrgan nlöllnn kskpokkama kskarvosta l nrgan varanss,
S-11435, FYSIIKKA III (ES), Syksy 00, LH 4, Loppuvkko 39 LH4-1* Käyttän Maxwll-Boltzmann-jakauman parttofunktota määrtä a) nrgan nlön kskarvo (E ) skä b) nrgan nlöllnn kskpokkama kskarvosta l nrgan varanss,
Tilastollinen päättömyys, kevät 2017 Harjoitus 5b
 Tilastollie päättömyys, kevät 07 Harjoitus b Heikki Korpela 3. helmikuuta 07 Tehtävä. a Olkoot Y,..., Y Bθ. Johda uskottavuusosamäärä testisuuree ry, Waldi testisuuree wy ja Rao pistemäärätestisuuree uy
Tilastollie päättömyys, kevät 07 Harjoitus b Heikki Korpela 3. helmikuuta 07 Tehtävä. a Olkoot Y,..., Y Bθ. Johda uskottavuusosamäärä testisuuree ry, Waldi testisuuree wy ja Rao pistemäärätestisuuree uy
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196
 VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Tehtävä 1. Voidaanko seuraavat luvut esittää kahden neliön summina? Jos voidaan, niin kuinka monella eri tavalla? (i) n = 145 (ii) n = 770.
 JOHDATUS LUKUTEORIAAN (syksy 07) HARJOITUS 0, MALLIRATKAISUT Tehtävä. Voidaako seuraavat luvut esittää kahde eliö summia? Jos voidaa, ii kuika moella eri tavalla? (i) = 45 (ii) = 770. Ratkaisu. (i) Jaetaa
JOHDATUS LUKUTEORIAAN (syksy 07) HARJOITUS 0, MALLIRATKAISUT Tehtävä. Voidaako seuraavat luvut esittää kahde eliö summia? Jos voidaa, ii kuika moella eri tavalla? (i) = 45 (ii) = 770. Ratkaisu. (i) Jaetaa
Äärettämän sarjan (tai vain sarjan) sanotaan suppenevan eli konvergoivan, jos raja-arvo lims
 75 4 POTENSSISARJOJA 4.1 ÄÄRETTÖMÄT SARJAT Lukujoo { a k } summaa S a a a a a k 0 1 k k0 saotaa äärettömäksi sarjaksi. Summa o s. osasumma. S a a a a a k 0 1 k0 Äärettämä sarja (tai vai sarja) saotaa suppeeva
75 4 POTENSSISARJOJA 4.1 ÄÄRETTÖMÄT SARJAT Lukujoo { a k } summaa S a a a a a k 0 1 k k0 saotaa äärettömäksi sarjaksi. Summa o s. osasumma. S a a a a a k 0 1 k0 Äärettämä sarja (tai vai sarja) saotaa suppeeva
5.3 Matriisin kääntäminen adjungaatilla
 Vaasa yliopisto julkaisuja 08 Sec:MatIvAdj 53 Matriisi käätämie adjugaatilla Määritelmä 3 -matriisi A adjugaatti o -matriisi adj(a) (α i j ), missä α i j ( ) i+ j det(a ji ) (, joka o siis alkioo a ji
Vaasa yliopisto julkaisuja 08 Sec:MatIvAdj 53 Matriisi käätämie adjugaatilla Määritelmä 3 -matriisi A adjugaatti o -matriisi adj(a) (α i j ), missä α i j ( ) i+ j det(a ji ) (, joka o siis alkioo a ji
763105P JOHDATUS SUHTEELLISUUSTEORIAAN 1 Ratkaisut 5 Kevät 2013
 7635P JOHDATUS SUHTEELLISUUSTEORIAAN Ratkaisut 5 Keät 23. Aberraatio suhteellisuusteoriassa Tulkoon alo kuten tehtään kuassa (x, y)-tason x, y > neljänneksestä: u u x ˆx + u y ŷ c cos θ ˆx c sin θ ŷ. ()
7635P JOHDATUS SUHTEELLISUUSTEORIAAN Ratkaisut 5 Keät 23. Aberraatio suhteellisuusteoriassa Tulkoon alo kuten tehtään kuassa (x, y)-tason x, y > neljänneksestä: u u x ˆx + u y ŷ c cos θ ˆx c sin θ ŷ. ()
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
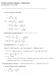 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
tasapainotila saavutetaan kun vuo aukon läpi on sama molempiin suuntiin
 S-445 FYSIIKKA III (Sf) Sysy 4, LH, Rataisut LHSf-* Kaasusäiliö o jaettu ahtee osaa, joide välisee eristävää seiämää o tehty iei ymyrämuotoie auo, joa halaisija o D Säiliö molemmissa osissa o helium aasua
S-445 FYSIIKKA III (Sf) Sysy 4, LH, Rataisut LHSf-* Kaasusäiliö o jaettu ahtee osaa, joide välisee eristävää seiämää o tehty iei ymyrämuotoie auo, joa halaisija o D Säiliö molemmissa osissa o helium aasua
4.0.2 Kuinka hyvä ennuste on?
 Luonteva ennuste on käyttää yhtälöä (4.0.1), jolloin estimaattori on muotoa X t = c + φ 1 X t 1 + + φ p X t p ja estimointivirheen varianssi on σ 2. X t }{{} todellinen arvo Xt }{{} esimaattori = ε t Esimerkki
Luonteva ennuste on käyttää yhtälöä (4.0.1), jolloin estimaattori on muotoa X t = c + φ 1 X t 1 + + φ p X t p ja estimointivirheen varianssi on σ 2. X t }{{} todellinen arvo Xt }{{} esimaattori = ε t Esimerkki
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
Neutriinokuljetus koherentissa kvasihiukkasapproksimaatiossa
 Neutriinokuljetus koherentissa kvasihiukkasapproksimaatiossa Graduseminaari Joonas Ilmavirta Jyväskylän yliopisto 15.6.2012 Joonas Ilmavirta (JYU) Neutriinot ja cqpa 15.6.2012 1 / 14 Osa 1: Neutriinot
Neutriinokuljetus koherentissa kvasihiukkasapproksimaatiossa Graduseminaari Joonas Ilmavirta Jyväskylän yliopisto 15.6.2012 Joonas Ilmavirta (JYU) Neutriinot ja cqpa 15.6.2012 1 / 14 Osa 1: Neutriinot
HY, MTL / Matemaattisten tieteiden kandiohjelma Todennäköisyyslaskenta IIb, syksy 2018 Harjoitus 3 Ratkaisuehdotuksia.
 HY, MTL / Matemaattiste tieteide kadiohjelma Todeäköisyyslasketa IIb, syksy 08 Harjoitus 3 Ratkaisuehdotuksia Tehtäväsarja I Olkoot X ja X riippumattomia satuaismuuttujia, joille ja olkoo X EX, EX, var
HY, MTL / Matemaattiste tieteide kadiohjelma Todeäköisyyslasketa IIb, syksy 08 Harjoitus 3 Ratkaisuehdotuksia Tehtäväsarja I Olkoot X ja X riippumattomia satuaismuuttujia, joille ja olkoo X EX, EX, var
KJR-C1001 Statiikka ja dynamiikka. Luento Susanna Hurme
 KJR-C1001 Statiikka ja dynamiikka Luento 24.3.2016 Susanna Hurme Rotaatioliikkeen liike-energia, teho ja energiaperiaate (Kirjan luku 18) Osaamistavoitteet Ymmärtää, miten liike-energia määritetään kiinteän
KJR-C1001 Statiikka ja dynamiikka Luento 24.3.2016 Susanna Hurme Rotaatioliikkeen liike-energia, teho ja energiaperiaate (Kirjan luku 18) Osaamistavoitteet Ymmärtää, miten liike-energia määritetään kiinteän
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
VII LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ
 II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
Termodynamiikka. Fysiikka III 2007. Ilkka Tittonen & Jukka Tulkki
 Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Energia bittiä kohden
 TLT-54/4u Energia ittiä kohden Kirjallisuudessa (ja muutenkin) on usein tapana käyttää S/ suhteen sijasta suuretta (syy seliää tarkemmin hetken päästä ) E missä - E on hyötysignaalienergia ittiä kohden
TLT-54/4u Energia ittiä kohden Kirjallisuudessa (ja muutenkin) on usein tapana käyttää S/ suhteen sijasta suuretta (syy seliää tarkemmin hetken päästä ) E missä - E on hyötysignaalienergia ittiä kohden
****************************************************************** ****************************************************************** 7 Esim.
 8.3. Kombiaatiot MÄÄRITELMÄ 6 Merkitä k, joka luetaa yli k:, tarkoittaa lause- ketta k = k! ( k)! 6 3 2 1 6 Esim. 1 3 3! = = = = 3! ( 3)! 3 2 1 3 2 1 3 2 1 Laskimesta löydät äppäime, jolla kertomia voi
8.3. Kombiaatiot MÄÄRITELMÄ 6 Merkitä k, joka luetaa yli k:, tarkoittaa lause- ketta k = k! ( k)! 6 3 2 1 6 Esim. 1 3 3! = = = = 3! ( 3)! 3 2 1 3 2 1 3 2 1 Laskimesta löydät äppäime, jolla kertomia voi
Liike-elämän matematiikka Opettajan aineisto
 Liike-elämä matematiikka Opettaja aieisto Pirjo Saarae, Eliisa Kolttola, Jarmo Pösö ISBN 978-951-37-5741-0 Päivitetty 13.8.2014 Tehtävie ratkaisut - Luku 1 Verotus - Luku 2 Katelaskut ja talousfuktiot
Liike-elämä matematiikka Opettaja aieisto Pirjo Saarae, Eliisa Kolttola, Jarmo Pösö ISBN 978-951-37-5741-0 Päivitetty 13.8.2014 Tehtävie ratkaisut - Luku 1 Verotus - Luku 2 Katelaskut ja talousfuktiot
Ratkaisut 2. KJR-C2001 Kiinteän aineen mekaniikan perusteet, IV/2016. Tehtävä 1 Selitä käsitteet kohdissa a) ja b) sekä laske c) kohdan tehtävä.
 Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2010 Insinöörivalinnan fysiikan koe 2.6.2010, malliratkaisut
 A1 Diplomi-insinöörin ja arkkithtin yhtisalinta - dia-alinta 2010 Alla on lutltu kuusi suurtta skä annttu taulukoissa kahdksan lukuaroa ja kahdksan SI-yksikön symbolia. Yhdistä suurt oikan suuruusluokan
A1 Diplomi-insinöörin ja arkkithtin yhtisalinta - dia-alinta 2010 Alla on lutltu kuusi suurtta skä annttu taulukoissa kahdksan lukuaroa ja kahdksan SI-yksikön symbolia. Yhdistä suurt oikan suuruusluokan
1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa?
 Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
