m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
|
|
|
- Maija-Leena Tamminen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T ,15 K paineessa P 1 atm Pa. Veden ominaislämpökapasiteetti c 4190 J/kg K), höyrystymislämpö l h 56 kj/kg ja normaali kiehumislämpötila T ,15 K. Veden lämpötilan laskiessa siitä vapautuva lämpömäärä on Q mc T mct 1 T ) 0,00 kg 4190 J kg 1 K 1 383,15 373,15 K) 8380 J. Tämä lämpömäärä kuluu veden höyrystymiseen, Q m h l h. Muodostuneen höyryn massa on m h Q l h 8380 J J kg 1 0, kg 3,71 g. Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0, kg 0,00 kg 0, ,86 %. Lasketaan vielä muodostuneen höyryn tilavuus ideaalikaasun tilanyhtälön avulla V nrt P m hrt M m P 0, kg 8,31447 J mol 1 K 1 373,15 K 18, kg mol Pa 6, m 3 6,31 l.. Veden höyrynpaine lämpötiloissa 16, 0 ja 30 on P 16 1,81 kpa, P 0,34 kpa ja P 30 4,5 kpa. Veden moolimassa M m 18,0 g/mol ja lämpötiloissa 100, 37 ja 5 höyrystymislämpö l kj/kg numeroarvo kappaleen 8 taulukosta 1), l kj/kg numeroarvo harjoituksen 1 tehtävästä 6) ja l kj/kg numeroarvo laskettu harjoituksen 8 tehtävästä 6). Clausius-Clapeyronin yhtälöstä saadaan höyrystymiskäyrän 1
2 approksimatiivinen yhtälö 8.7), josta P T ) Ae lm RT Ae lmm RT ln P T ) ln Ae lmm RT ) A ln e lmm RT ln A lm m R Saatu yhtälö esittää suoraa ln P T ) b + kt 1, missä vakiotermi b ln A ja kulmakerroin k lm m /R on suoraan verrannollinen höyrystymislämpöön l. Kulmakerroin saadaan selville sovittamalla suora pistejoukkoon T 1, ln P T )). Lämpötilan käänteisluvut ja paineen luonnolliset logaritmit, joita sovituksessa tarvitaan, on esitetty seuraavassa taulukossa. ) 1 T. T ) T K) T 1 K 1 ) P Pa) ln P 16 89,15 0, , ,15 0, , ,15 0, , ,5 ln P 8,0 7,5 3,30 3,35 3,40 3,45 1/T 1/K) 10 3 Kuva 1: Pistejoukkoon sovitetun suoran 5, ,98/T kuvaaja. Suoran sovitus kuva 1) voidaan tehdä esimerkiksi pienimmän neliösumman menetelmällä likiarvojen käyttö vaikuttaa lopputulokseen hieman, esimerkiksi edellä esitetyn taulukon arvoja käytettäessä noin 10 kj/kg). Kulmakertoimeksi saadaan k 5336,98 K ± 31,64 K ±0,59 %), jonka avulla edelleen höyrystymislämmöksi k lm m R l kr M m 5336,98 K 8,31447 J mol 1 K 1 18, kg mol ,603 J kg 1 46 kj kg 1. Havaitaan, että tulos on sopusoinnussa vertailuarvojen l 100, l 37 ja l 5 kanssa.
3 3. Tarkasteltava ideaalikaasu koostuu kahdesta identtisestä molekyylistä, joista kumpikin voi olla tilassa r 1,, 3 tai 4. a) Identtisiä hiukkasia ei voida erottaa toisistaan, joten tilat r, s) toinen molekyyli tilassa r ja toinen tilassa s) ja s, r) ovat sama asia. Tiloja, joilla r s, on neljä kappaletta. Jos k molekyyliä voi esiintyä n 4 eri tilassa ja s r, on kyseisten tilojen lukumäärä ) n n! k k!n k)! 4!!4 )! 4 3!!! 6. Kaasulla on siis yhteensä mahdollista tilaa. b) Kaasun mahdolliset tilat on lueteltu alla muodossa r, s). 1, 1) 1, ) 1, 3) 1, 4), ), 3), 4) 3, 3, 4) 4, 4) c) Kohdassa b) mainitut tilat voidaan esittää myös miehityslukujen n r avulla muodossa n 1, n, n 3, n 4 ) missä kukin miehitysluku on 1, tai 0 riippuen siitä, onko kyseisen tilan r miehittänyt molekyyleistä toinen, molemmat, vai ei kumpikaan. Tällä tavalla esitetyt tilat on lueteltu alla., 0, 0, 0) 1, 1, 0, 0) 1, 0, 1, 0) 1, 0, 0, 1) 0,, 0, 0) 0, 1, 1, 0) 0, 1, 0, 1) 0, 0,, 0) 0, 0, 1, 1) 0, 0, 0, ) d) Kaasun tilan R energia on ɛ R ɛ r + ɛ s. Kohdassa b) lueteltujen tilojen avulla kaasun partitiofunktio on Z R e βɛ R e βɛ 1+ɛ 1 ) + e βɛ 1+ɛ ) + e βɛ 1+ɛ 3 ) + e βɛ 1+ɛ 4 ) + e βɛ +ɛ ) + e βɛ +ɛ 3 ) + e βɛ +ɛ 4 ) + e βɛ 3+ɛ 3 ) + e βɛ 3+ɛ 4 ) + e βɛ 4+ɛ 4 ). 3
4 e) Partitiofunktio voidaan esittää myös rajoitettuna kaksinkertaisena summauksena yli kaikkien mahdollisten yksihiukkastilojen, ZT, V, ) r1 s1 }{{} s r s e βɛr+ɛs) e βɛ 1+ɛ s) + s e βɛ 3+ɛ s) + s3 e βɛ +ɛ s) s4 e βɛ 4+ɛ s) mikä nähdään joko kirjoittamalla kaikki termit auki tai yksinkertaisesti vertaamalla suoraan kohdan d) tulokseen, jossa selvästi jälkimmäinen summaus muuttujan s yli juoksee ensimmäisen summan muuttujan arvosta r arvoon neljä. f) Partitiofunktio voidaan esittää myös rajoitettuna nelinkertaisena summauksena yli miehityslukujen n r kaikkien mahdollisten arvojen, ZT, V, ) n 1 0 n 0 n 3 0 n 4 0 } {{ } n 1 +n +n 3 +n 4 n 0 n 3 0 n n 0 n 3 0 n 4 0 e βn 1ɛ 1 +n ɛ +n 3 ɛ 3 +n 4 ɛ 4 ) e βn ɛ +n 3 ɛ 3 +n 4 ɛ 4 ) n 0 n 3 0 n 4 0 e βɛ 1+n ɛ +n 3 ɛ 3 +n 4 ɛ 4 ) e βɛ 1+n ɛ +n 3 ɛ 3 +n 4 ɛ 4 ) Miehityslukusummauksen nähdään olevan yhtäpitävä aiempien esitysten kanssa kirjoittamalla kaikki summaukset auki, rajoitus huomioiden. Esimerkiksi yllä viimeisessä kolminkertaisessa summassa jää tällöin jäljelle vain yksi termi, e βɛ 1, sillä kun n 1, muiden miehityslukujen on rajoituksen perusteella oltava nollia. Toinen tapa on verrata nelinkertaisen summauksen lauseketta kohdan c) ja d) tuloksiin kirjoittamalla kohdan d) tulos muotoon Z r e βɛr e βɛ 1+0ɛ +0ɛ 3 +0ɛ 4 ) + e β1ɛ 1+1ɛ +0ɛ 3 +0ɛ 4 ) + e β1ɛ 1+0ɛ +1ɛ 3 +0ɛ 4 ) + e β1ɛ 1+0ɛ +0ɛ 3 +1ɛ 4 ) + e β0ɛ 4+ɛ +0ɛ 3 +0ɛ 4 ) + e β0ɛ 1+1ɛ +1ɛ 3 +0ɛ 4 ) + e β0ɛ 1+1ɛ +0ɛ 3 +1ɛ 4 ) + e β0ɛ 1+0ɛ +ɛ 3 +0ɛ 4 ) + e β0ɛ 1+0ɛ +1ɛ 3 +1ɛ 4 ) + e β0ɛ 1+0ɛ +0ɛ 3 +ɛ 4 ). 4
5 4. Lämpötilassa T 0 93,15 K ja paineessa P 1 atm Pa olevan hapen moolimassa M m 31,99 g/mol ja perustilan s 0 translaatioenergia ɛ tr s ɛ tr 0 0. Olettamalla happi ideaalikaasuksi saadaan tilanyhtälöstä Yhden happimolekyylin massa on N V P kt. m O M m N A 31, kg mol 1 6, mol 1 5, kg. Alimman translaatiotilan miehitysluvun keskiarvoksi saadaan luentojen yhtälön 9.7) avulla n 0 N V h πmkt / e ɛtr 0 kt P ) h 3/ e 0 kt kt πm O kt Pa 1, J K 1 93,15 K [ ] 6, J s) 3/ π 5, , J K ,15 K 1, , Koska n 0 1, happi käyttäytyy näissä olosuhteissa klassisen ideaalikaasun tavoin. 5. Normaaliolosuhteissa lämpötila T ,15 K ja paine P 0 1 atm Pa. Tehtävässä tulee tarkastella, missä lämpötilassa luentojen klassisuusehto 9.8) ei enää toteudu, kun aluksi normaaliolosuhteissa olevaa vetyä jäähdytetään. Vedyn H moolimassa M m,016 g/mol lukuarvo luentojen kappaleen 9 esimerkistä). Asetetaan yhtälössä 9.8) N V h πmkt / 1. 1) Vetymolekyylin massa on m H M m N A, kg mol 1 6, mol 1 3, kg. a) Jäähdytys tapahtuu vakiotilavuudessa, jolloin P V NkT N V P kt vakio. 5
6 Ratkaistaan lämpötila yhtälöstä 1), ) /3 ) N h T V πm H k ) /3 ) P0 h kt 0 πm H k ) / Pa 1, J K 1 73,15 K 6, J s) π 3, kg 1, J K 1 0, K 0,136 K. b) Jäähdytys tapahtuu vakiopaineessa, jolloin N/V P/kT ) ei ole vakio. Yhtälö 1) saadaan tällöin muotoon ) ) P0 h 3/ 1, kt πmkt mistä ratkaistaan lämpötila ) /5 ) P0 h 3/5 T k πm H k ) / Pa 1, J K 1 6, J s) π 3, kg 1, J K 1, K,84 K. 6. Alumiinin tiheys ρ a 700 kg/m 3 ja moolimassa M m,a 7,0 g/mol. Lämpötilassa T a 300 K alumiinin elektroneja, joiden massa on m e 9, kg, käsitellään elektronikaasuna. Kiehumispisteessä 4, K nestemäisen heliumin tiheys on ρ h 1 kg/m 3 ja moolimassa M m,h 4,00 g/mol. Klassisuusehto voidaan lausua vaatimalla, että perustilan keskimääräinen miehitysluku on hyvin pieni eli yhtälön 9.8) mukaan muodossa /5 n 0 N V h πmkt 1. Vaihtoehtoisesti voidaan vaatia, että molekyylien de Broglie- eli materia-aallonpituus 9.30) on pieni niiden välimatkoihin verrattuna, λ 3 l 3, missä aallonpituus ja molekyylien välisen keskimääräisen etäisyyden kuutio ovat λ l 3 V N. h 3mkT 6
7 a) Lämpötilassa T a 300 K alumiini esiintyy kiinteänä metallina, jonka valenssielektroneja voidaan käsitellä vapaaelektronimallin avulla eli olettamalla kiderakenteen koostuvan positiivisesti varautuneista atomisydämistä ja lähes vapaasti liikkuvasta elektronikaasusta. Jokainen alumiiniatomi luovuttaa elektronikaasuun kolme johde-elektronia, jolloin elektronitiheydeksi saadaan N V Nρ a m a 3ρ an A M m,a, missä N A 6, /mol on Avogadron luku. Perustilan keskimääräiseksi miehitysluvuksi saadaan siten n 0 3ρ an A M m,a h πm e kt a kg m 3 6, mol 1 0,07 kg mol 1 6, J s) π 9, kg 1, J K K 14397, , joten klassisuusehto ei toteudu. Toisaalta voidaan myös laskea de Broglie-aallonpituus λ 3 h 3me kt 6, J s 3 9, kg 1, J K K, m 3 ja verrata sitä keskimääräiseen molekyylien väliseen etäisyyteen l 3 V N M m,a 3ρ a N A 0,07 kg mol kg m 3 6, mol 1 5, m 3. Nähdään, että λ 3 > l 3 eli klassisuusehto ei toteudu. b) Nestemäisen heliumin tapauksessa m M m,h /N A ja lämpötilassa T h 4 K perustilan 7
8 keskimääräiseksi miehitysluvuksi saadaan n 0 ρ hn A h N A M m,h πm m,h kt h ρ h NA M m,h ) 5 h πkt h 6, kg m 3 3 mol 1 0,004 kg mol 1 6, J s) π 1, J K 1 4 K 1, > 1, joten klassisuusehto ei toteudu. Myös vertaamalla de Broglie-aallonpituutta λ 3 h 3mkT h N A 3Mm,h kt h ) 5 6, J s 6, mol 1 3 0,004 kg mol 1 1, J K 1 4 K, m 3 keskimääräiseen molekyylien väliseen etäisyyteen l 3 V N M m,h ρ h N A 0,004kg mol 1 1 kg mol 1 6, mol 1 5, m 3 nähdään, että λ 3 > l 3 eli klassisuusehto ei toteudu. 8
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
Z 1 = Np i. 2. Sähkömagneettisen kentän värähdysliikkeen energia on samaa muotoa kuin molekyylin värähdysliikkeen energia, p 2
 766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 10, ratkaisut (syyslukukausi 2014)
 7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Mikrotila Makrotila Statistinen paino Ω(n) 3 Ω(3) = 4 2 Ω(2) = 6 4 Ω(4) = 1
 76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
9 Klassinen ideaalikaasu
 111 9 Klassinen ideaalikaasu 9-1 Klassisen ideaalikaasun patitiofunktio Ideaalikaasu on eaalikaasun idealisaatio, jossa molekyylien väliset keskimäääiset etäisyydet oletetaan hyvin suuiksi molekyylien
111 9 Klassinen ideaalikaasu 9-1 Klassisen ideaalikaasun patitiofunktio Ideaalikaasu on eaalikaasun idealisaatio, jossa molekyylien väliset keskimäääiset etäisyydet oletetaan hyvin suuiksi molekyylien
Käyttämällä annettua kokoonpuristuvuuden määritelmää V V. = κv P P = P 0 = P. (b) Lämpölaajenemisesta johtuva säiliön tilavuuden muutos on
 766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
Ilman suhteellinen kosteus saadaan, kun ilmassa olevan vesihöyryn osapaine jaetaan samaa lämpötilaa vastaavalla kylläisen vesihöyryn paineella:
 ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
766328A Termofysiikka Harjoitus no. 12, ratkaisut (syyslukukausi 2014)
 7668A Termofysiikk Hrjoitus no 1, rtkisut (syyslukukusi 14) 1 Lämpötilss T K elektronien energit eivät ylitä Fermin energi (ɛ i ɛ F ), lämpötilprmetri β j kemillinen potentili vst Fermin energi (µ() ɛ
7668A Termofysiikk Hrjoitus no 1, rtkisut (syyslukukusi 14) 1 Lämpötilss T K elektronien energit eivät ylitä Fermin energi (ɛ i ɛ F ), lämpötilprmetri β j kemillinen potentili vst Fermin energi (µ() ɛ
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
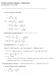 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
S Fysiikka III (EST) Tentti ja välikoeuusinta
 S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
Integroimalla ja käyttämällä lopuksi tilanyhtälöä saadaan T ( ) ( ) H 5,0 10 J + 2,0 10 0,50 1,0 10 0,80 Pa m 70 kj
 S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
ψ(x) = A cos(kx) + B sin(kx). (2) k = nπ a. (3) E = n 2 π2 2 2ma 2 n2 E 0. (4)
 76A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 4 Kevät 214 1. Tehtävä: Yksinkertainen malli kovalenttiselle sidokselle: a) Äärimmäisen yksinkertaistettuna mallina elektronille atomissa voidaan pitää syvää potentiaalikuoppaa
76A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 4 Kevät 214 1. Tehtävä: Yksinkertainen malli kovalenttiselle sidokselle: a) Äärimmäisen yksinkertaistettuna mallina elektronille atomissa voidaan pitää syvää potentiaalikuoppaa
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
S , Fysiikka III (S) I välikoe Malliratkaisut
 S-4.35, Fysiikka III (S) I välikoe 9.0.000 Malliratkaisut Tehtävä Kuution uotoisessa säiliössä, jonka särän pituus on 0,0, on 3,0 0 olekyyliä happea (O) 300 K läpötilassa. a) Kuinka onta kertaa kukin olekyyli
S-4.35, Fysiikka III (S) I välikoe 9.0.000 Malliratkaisut Tehtävä Kuution uotoisessa säiliössä, jonka särän pituus on 0,0, on 3,0 0 olekyyliä happea (O) 300 K läpötilassa. a) Kuinka onta kertaa kukin olekyyli
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
Kvanttifysiikan perusteet 2017
 Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Nyt n = 1. Tästä ratkaistaan kuopan leveys L ja saadaan sijoittamalla elektronin massa ja vakiot
 S-1146 Fysiikka V (ES) Tentti 165005 1 välikokeen alue 1 a) Rubiinilaserin emittoiman valon aallonpituus on 694, nm Olettaen että fotonin emissioon tällä aallonpituudella liittyy äärettömän potentiaalikuopan
S-1146 Fysiikka V (ES) Tentti 165005 1 välikokeen alue 1 a) Rubiinilaserin emittoiman valon aallonpituus on 694, nm Olettaen että fotonin emissioon tällä aallonpituudella liittyy äärettömän potentiaalikuopan
Työ 3: Veden höyrystymislämmön määritys
 Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Ekvipartitioperiaatteen mukaisesti jokaiseen efektiiviseen vapausasteeseen liittyy (1 / 2)kT energiaa molekyyliä kohden.
 . Hiilidioksidiolekyyli CO tiedetään lineaariseksi a) Mitkä ovat eteneisliikkeen, pyöriisliikkeen ja värähtelyn suuriat ekvipartitioperiaatteen ukaiset läpöenergiat olekyyliä kohden, kun kaikki vapausasteet
. Hiilidioksidiolekyyli CO tiedetään lineaariseksi a) Mitkä ovat eteneisliikkeen, pyöriisliikkeen ja värähtelyn suuriat ekvipartitioperiaatteen ukaiset läpöenergiat olekyyliä kohden, kun kaikki vapausasteet
1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa?
 Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
η = = = 1, S , Fysiikka III (Sf) 2. välikoe
 S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
11 Kvantti-ideaalikaasu
 35 Kvantti-ideaalikaasu - Kvanttistatistiikka Kappaleessa 9 tarkasteltiin klassisissa olosuhteissa esiintyvää ideaalikaasua. Tällaisessa kaasussa molekyylien tavoitettavissa on niin paljon yksihiukkastiloja,
35 Kvantti-ideaalikaasu - Kvanttistatistiikka Kappaleessa 9 tarkasteltiin klassisissa olosuhteissa esiintyvää ideaalikaasua. Tällaisessa kaasussa molekyylien tavoitettavissa on niin paljon yksihiukkastiloja,
1240eV nm. 410nm. Kun kappaleet saatetaan kontaktiin jännite-ero on yhtä suuri kuin työfunktioiden erotus ΔV =
 S-47 ysiikka III (ST) Tentti 88 Maksimiaallonpituus joka irroittaa elektroneja metallista on 4 nm ja vastaava aallonpituus metallille on 8 nm Mikä on näiden metallien välinen jännite-ero? Metallin työfunktio
S-47 ysiikka III (ST) Tentti 88 Maksimiaallonpituus joka irroittaa elektroneja metallista on 4 nm ja vastaava aallonpituus metallille on 8 nm Mikä on näiden metallien välinen jännite-ero? Metallin työfunktio
1 WKB-approksimaatio. Yleisiä ohjeita. S Harjoitus
 S-114.1427 Harjoitus 3 29 Yleisiä ohjeita Ratkaise tehtävät MATLABia käyttäen. Kirjoita ratkaisut.m-tiedostoihin. Tee tuloksistasi lyhyt seloste, jossa esität laskemasi arvot sekä piirtämäsi kuvat (sekä
S-114.1427 Harjoitus 3 29 Yleisiä ohjeita Ratkaise tehtävät MATLABia käyttäen. Kirjoita ratkaisut.m-tiedostoihin. Tee tuloksistasi lyhyt seloste, jossa esität laskemasi arvot sekä piirtämäsi kuvat (sekä
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
S , Fysiikka III (ES) Tentti Tentti / välikoeuusinta
 S-11435, Fysiikka III (ES) entti 4113 entti / välikoeuusinta I Välikokeen alue 1 Viiden tunnistettavissa olevan identtisen hiukkasen mikrokanonisen joukon käytettävissä on neljä tasavälistä energiatasoa,
S-11435, Fysiikka III (ES) entti 4113 entti / välikoeuusinta I Välikokeen alue 1 Viiden tunnistettavissa olevan identtisen hiukkasen mikrokanonisen joukon käytettävissä on neljä tasavälistä energiatasoa,
Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin.
 1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
Bensiiniä voidaan pitää hiilivetynä C8H18, jonka tiheys (NTP) on 0,703 g/ml ja palamislämpö H = kj/mol
 Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Luento 8. Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli. Sähkönjohtavuus Druden malli
 Luento 8 Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli Sähkönjohtavuus Druden malli Klassiset C V -mallit Termodynamiikka kun Ei ennustetta arvosta! Klassinen
Luento 8 Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli Sähkönjohtavuus Druden malli Klassiset C V -mallit Termodynamiikka kun Ei ennustetta arvosta! Klassinen
Vauhti = nopeuden itseisarvo. Nopeuden itseisarvon keskiarvo N:lle hiukkaselle määritellään yhtälöllä
 S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
Fysikaalinen kemia II kaavakokoelma, osa 1
 Fysikaalinen kemia II kaavakokoelma, osa 1 Wienin siirtymälaki: T λ max = 0.2898 cm K (1) Stefan Boltzmanin laki: M = σt 4 σ = 5.67 10 8 W m 2 K 4 (2) Planckin jakauma ρ = 8πkT λ 4 ( 1 ) e hc/λkt 1 (3)
Fysikaalinen kemia II kaavakokoelma, osa 1 Wienin siirtymälaki: T λ max = 0.2898 cm K (1) Stefan Boltzmanin laki: M = σt 4 σ = 5.67 10 8 W m 2 K 4 (2) Planckin jakauma ρ = 8πkT λ 4 ( 1 ) e hc/λkt 1 (3)
( ) ( ) on nimeltään molekyylisironnan mikroskooppinen vaikutusala). Sijoittamalla numeroarvot saadaan vapaaksi matkaksi
 S-4.35, FYSIIKKA III, Syksy 00, LH, Loppuiikko 38 LH-* Laske happimolekyylin keskimääräinen apaa matka 300 K lämpötilassa ja,0 baarin paineessa. Voit olettaa, että molekyyli on pallon muotoinen ja pallon
S-4.35, FYSIIKKA III, Syksy 00, LH, Loppuiikko 38 LH-* Laske happimolekyylin keskimääräinen apaa matka 300 K lämpötilassa ja,0 baarin paineessa. Voit olettaa, että molekyyli on pallon muotoinen ja pallon
Teddy 1. harjoituksen malliratkaisu kevät 2011
 Teddy 1. harjoituksen malliratkaisu kevät 2011 1. Dipolimomentti voidaan määritellä pistevarauksille seuraavan vektoriyhtälön avulla: µ = q i r i, (1) i missä q i on i:nnen varauksen suuruus ja r i = (x
Teddy 1. harjoituksen malliratkaisu kevät 2011 1. Dipolimomentti voidaan määritellä pistevarauksille seuraavan vektoriyhtälön avulla: µ = q i r i, (1) i missä q i on i:nnen varauksen suuruus ja r i = (x
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
8 Aineen olomuodot. 8-1 Olomuodon muutokset
 96 8 Aineen olomuodot 8-1 Olomuodon muutokset Vesi voi esiintyä eri lämpötiloissa hyvin erilaisissa tiloissa jäänä, nestemäisenä vetenä ja höyrynä. Tällaisia tiloja sanotaan aineen olomuodoiksi (engl.
96 8 Aineen olomuodot 8-1 Olomuodon muutokset Vesi voi esiintyä eri lämpötiloissa hyvin erilaisissa tiloissa jäänä, nestemäisenä vetenä ja höyrynä. Tällaisia tiloja sanotaan aineen olomuodoiksi (engl.
Wien R-J /home/heikki/cele2008_2010/musta_kappale_approksimaatio Wed Mar 13 15:33:
 1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma
 KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma Sekä A- että B-osiosta tulee saada vähintään 10 pistettä. Mikäli A-osion pistemäärä on vähemmän kuin 10 pistettä,
KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma Sekä A- että B-osiosta tulee saada vähintään 10 pistettä. Mikäli A-osion pistemäärä on vähemmän kuin 10 pistettä,
MATEMATIIKAN KOE, LYHYT OPPIMÄÄRÄ HYVÄN VASTAUKSEN PIIRTEITÄ
 MATEMATIIKAN KOE, LYHYT OPPIMÄÄRÄ 24.9.2019 HYVÄN VASTAUKSEN PIIRTEITÄ Alustavat hyvän vastauksen piirteet on suuntaa-antava kuvaus kokeen tehtäviin odotetuista vastauksista ja tarkoitettu ensisijaisesti
MATEMATIIKAN KOE, LYHYT OPPIMÄÄRÄ 24.9.2019 HYVÄN VASTAUKSEN PIIRTEITÄ Alustavat hyvän vastauksen piirteet on suuntaa-antava kuvaus kokeen tehtäviin odotetuista vastauksista ja tarkoitettu ensisijaisesti
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
8. Klassinen ideaalikaasu
 Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2012 Insinöörivalinnan fysiikan koe 30.5.2012, malliratkaisut
 A1 Kappale, jonka massa m = 2,1 kg, lähtee liikkeelle levosta paikasta x = 0,0 m pitkin vaakasuoraa alustaa. Kappaleeseen vaikuttaa vaakasuora vetävä voima F, jonka suuruus riippuu paikasta oheisen kuvan
A1 Kappale, jonka massa m = 2,1 kg, lähtee liikkeelle levosta paikasta x = 0,0 m pitkin vaakasuoraa alustaa. Kappaleeseen vaikuttaa vaakasuora vetävä voima F, jonka suuruus riippuu paikasta oheisen kuvan
n = = RT S Tentti
 S-5 Tetti 500 a) Kuika suuri o molekyylie traslaatioliikkee kieettie eergia kuutiometrissä ilmaa jos ilma lämpötila o 00 K ja paie 0 bar? b) Mikä o kieettise eergia kokoaismäärä ku myös muut liikelajit
S-5 Tetti 500 a) Kuika suuri o molekyylie traslaatioliikkee kieettie eergia kuutiometrissä ilmaa jos ilma lämpötila o 00 K ja paie 0 bar? b) Mikä o kieettise eergia kokoaismäärä ku myös muut liikelajit
Luvun 12 laskuesimerkit
 Luvun 12 laskuesimerkit Esimerkki 12.1 Mikä on huoneen sisältämän ilman paino, kun sen lattian mitat ovat 4.0m 5.0 m ja korkeus 3.0 m? Minkälaisen voiman ilma kohdistaa lattiaan? Oletetaan, että ilmanpaine
Luvun 12 laskuesimerkit Esimerkki 12.1 Mikä on huoneen sisältämän ilman paino, kun sen lattian mitat ovat 4.0m 5.0 m ja korkeus 3.0 m? Minkälaisen voiman ilma kohdistaa lattiaan? Oletetaan, että ilmanpaine
Oletetaan kaasu ideaalikaasuksi ja sovelletaan Daltonin lakia. Kumpikin seoksen kaasu toteuttaa erikseen ideaalikaasun tilanyhtälön:
 S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
S Fysiikka III (Est), 2 VK Malliratkaisut (Arvosteluperusteita täydennetään vielä)
 S-.7 Fysiikka III (st), VK 8.5.008 Malliratkaisut (Arvosteluperusteita täydennetään vielä). Näytä, että sekä symmetrinen aaltofunktio ψn( x ) ψn ( x) + ψn( x) ψn, että antisymmetrinen aaltofunktioψn( x)
S-.7 Fysiikka III (st), VK 8.5.008 Malliratkaisut (Arvosteluperusteita täydennetään vielä). Näytä, että sekä symmetrinen aaltofunktio ψn( x ) ψn ( x) + ψn( x) ψn, että antisymmetrinen aaltofunktioψn( x)
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
c) Missä ajassa kappale selvittää reitin b-kohdan tapauksessa? [3p]
![c) Missä ajassa kappale selvittää reitin b-kohdan tapauksessa? [3p] c) Missä ajassa kappale selvittää reitin b-kohdan tapauksessa? [3p]](/thumbs/50/26318972.jpg) Fysiikan valintakoe 11.5.2016 klo 9-12 1. Kappale lähtee levosta liikkeelle pisteessä A (0,3) ja liukuu kitkattomasti, ensin kaltevaa tasoa pitkin pisteeseen B (x,0) ja siitä edelleen vaakaatasoa pitkin
Fysiikan valintakoe 11.5.2016 klo 9-12 1. Kappale lähtee levosta liikkeelle pisteessä A (0,3) ja liukuu kitkattomasti, ensin kaltevaa tasoa pitkin pisteeseen B (x,0) ja siitä edelleen vaakaatasoa pitkin
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-445, Fysiikka III (Sf) tentti/välikoeuusinta 43 välikokeen alue ristetyssä astiassa, jonka lämötila idetään, kelvinissä, on nestemäistä heliumia tasaainossa helium kaasun kanssa Se on erotettu toisesta
S-445, Fysiikka III (Sf) tentti/välikoeuusinta 43 välikokeen alue ristetyssä astiassa, jonka lämötila idetään, kelvinissä, on nestemäistä heliumia tasaainossa helium kaasun kanssa Se on erotettu toisesta
Kaasu 2-atominen. Rotaatio ja translaatiovapausasteet virittyneet (f=5) c. 5 Ideaalikaasun tilanyhtälöstä saadaan kaasun moolimäärä: 3
 S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
TKK, TTY, LTY, OY, ÅA, TY ja VY insinööriosastojen valintakuulustelujen fysiikan koe 31.5.2006, malliratkaisut ja arvostelu.
 1 Linja-autoon on suunniteltu vauhtipyörä, johon osa linja-auton liike-energiasta siirtyy jarrutuksen aikana Tätä energiaa käytetään hyväksi kun linja-autoa taas kiihdytetään Linja-auto, jonka nopeus on
1 Linja-autoon on suunniteltu vauhtipyörä, johon osa linja-auton liike-energiasta siirtyy jarrutuksen aikana Tätä energiaa käytetään hyväksi kun linja-autoa taas kiihdytetään Linja-auto, jonka nopeus on
Ohjeellinen pituus: 2 3 sivua. Vastaa joko tehtävään 2 tai 3
 PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
0. perusmääritelmiä. Lukutyypit Laskusäännöt Laskujärjestys
 0. perusmääritelmiä Lukutyypit Laskusäännöt Laskujärjestys Luonnolliset luvut (N): 1, 2, 3, 4 Kokonaisluvut (Z):... 4, 3, 2, 1, 0, 1, 2, 3, 4... RaConaaliluvut (Q): kaikki luvut, jotka voidaan esieää kahden
0. perusmääritelmiä Lukutyypit Laskusäännöt Laskujärjestys Luonnolliset luvut (N): 1, 2, 3, 4 Kokonaisluvut (Z):... 4, 3, 2, 1, 0, 1, 2, 3, 4... RaConaaliluvut (Q): kaikki luvut, jotka voidaan esieää kahden
a) Oletetaan, että happi on ideaalikaasu. Säiliön seinämiin osuvien hiukkasten lukumäärä saadaan molekyylivuon lausekkeesta = kaava (1p) dta n =
 S-, ysiikka III (S) välikoe 7000 Laske nopeuden itseisarvon keskiarvo v ja nopeuden neliöllinen keskiarvo v rs seuraaville 6 olekyylien nopeusjakauille: a) kaikkien vauhti 0 / s, b) kolen vauhti / s ja
S-, ysiikka III (S) välikoe 7000 Laske nopeuden itseisarvon keskiarvo v ja nopeuden neliöllinen keskiarvo v rs seuraaville 6 olekyylien nopeusjakauille: a) kaikkien vauhti 0 / s, b) kolen vauhti / s ja
Kojemeteorologia (53695) Laskuharjoitus 1
 Kojemeteorologia (53695) Laskuharjoitus 1 Risto Taipale 20.9.2013 1 Tehtävä 1 Erään lämpömittarin vertailu kalibrointistandardiin antoi keskimääräiseksi eroksi standardista 0,98 C ja eron keskihajonnaksi
Kojemeteorologia (53695) Laskuharjoitus 1 Risto Taipale 20.9.2013 1 Tehtävä 1 Erään lämpömittarin vertailu kalibrointistandardiin antoi keskimääräiseksi eroksi standardista 0,98 C ja eron keskihajonnaksi
Shrödingerin yhtälön johto
 Shrödingerin yhtälön johto Tomi Parviainen 4. maaliskuuta 2018 Sisältö 1 Schrödingerin yhtälön johto tasaisessa liikkeessä olevalle elektronille 1 2 Schrödingerin yhtälöstä aaltoyhtälöön kiihtyvässä liikkeessä
Shrödingerin yhtälön johto Tomi Parviainen 4. maaliskuuta 2018 Sisältö 1 Schrödingerin yhtälön johto tasaisessa liikkeessä olevalle elektronille 1 2 Schrödingerin yhtälöstä aaltoyhtälöön kiihtyvässä liikkeessä
a) Piirrä hahmotelma varjostimelle muodostuvan diffraktiokuvion maksimeista 1, 2 ja 3.
 Ohjeita: Tee jokainen tehtävä siististi omalle sivulleen/sivuilleen. Merkitse jos tehtävä jatkuu seuraavalle konseptille. Kirjoita ratkaisuihin näkyviin tarvittavat välivaiheet ja perustele lyhyesti käyttämästi
Ohjeita: Tee jokainen tehtävä siististi omalle sivulleen/sivuilleen. Merkitse jos tehtävä jatkuu seuraavalle konseptille. Kirjoita ratkaisuihin näkyviin tarvittavat välivaiheet ja perustele lyhyesti käyttämästi
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka. Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU
 MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
MAB3 - Harjoitustehtävien ratkaisut:
 MAB3 - Harjoitustehtävien ratkaisut: 1 Funktio 1.1 Piirretään koordinaatistoakselit ja sijoitetaan pisteet: 1 1. a) Funktioiden nollakohdat löydetään etsimällä kuvaajien ja - akselin leikkauspisteitä.
MAB3 - Harjoitustehtävien ratkaisut: 1 Funktio 1.1 Piirretään koordinaatistoakselit ja sijoitetaan pisteet: 1 1. a) Funktioiden nollakohdat löydetään etsimällä kuvaajien ja - akselin leikkauspisteitä.
0. perusmääritelmiä. Lukutyypit Laskusäännöt Laskujärjestys
 Lukutyypit Laskusäännöt Laskujärjestys 0. perusmääritelmiä Luonnolliset luvut (N): 1, 2, 3, 4 Kokonaisluvut (Z):... 4, 3, 2, 1, 0, 1, 2, 3, 4... RaFonaaliluvut (Q): kaikki luvut, jotka voidaan esihää kahden
Lukutyypit Laskusäännöt Laskujärjestys 0. perusmääritelmiä Luonnolliset luvut (N): 1, 2, 3, 4 Kokonaisluvut (Z):... 4, 3, 2, 1, 0, 1, 2, 3, 4... RaFonaaliluvut (Q): kaikki luvut, jotka voidaan esihää kahden
Luku 13 KAASUSEOKSET
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2010 Luku 13 KAASUSEOKSET Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2010 Luku 13 KAASUSEOKSET Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Betonimatematiikkaa
 Betonimatematiikkaa.11.017 Kiviaineksen rakeisuusesimerkki Laske seuraavan seulontatuloksen rakeisuusluku ja piirrä rakeisuuskäyrä Seula # mm Seulalle jäänyt Läpäisyarvo % g % Pohja 60 9,0-0,15 30 4,5
Betonimatematiikkaa.11.017 Kiviaineksen rakeisuusesimerkki Laske seuraavan seulontatuloksen rakeisuusluku ja piirrä rakeisuuskäyrä Seula # mm Seulalle jäänyt Läpäisyarvo % g % Pohja 60 9,0-0,15 30 4,5
Fysiikan laboratoriotyöt 1, työ nro: 2, Harmoninen värähtelijä
 Fysiikan laboratoriotyöt 1, työ nro: 2, Harmoninen värähtelijä Tekijä: Mikko Laine Tekijän sähköpostiosoite: miklaine@student.oulu.fi Koulutusohjelma: Fysiikka Mittausten suorituspäivä: 04.02.2013 Työn
Fysiikan laboratoriotyöt 1, työ nro: 2, Harmoninen värähtelijä Tekijä: Mikko Laine Tekijän sähköpostiosoite: miklaine@student.oulu.fi Koulutusohjelma: Fysiikka Mittausten suorituspäivä: 04.02.2013 Työn
TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT
 TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT (lukuun ottamatta tehtävää 12, johon kukaan ei ollut vastannut) RATKAISU TEHTÄVÄ 1 a) Vesi haihtuu (höyrystyy) ja ottaa näin ollen energiaa ympäristöstä
TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT (lukuun ottamatta tehtävää 12, johon kukaan ei ollut vastannut) RATKAISU TEHTÄVÄ 1 a) Vesi haihtuu (höyrystyy) ja ottaa näin ollen energiaa ympäristöstä
Matematiikkaa kemisteille, kevät 2012 Ylimääräinen laskuharjoitus Palautus 7.5. klo (suositellaan kuitenkin tekemään ennen välikoetta 30.4!
 Matematiikkaa kemisteille, kevät 2012 Ylimääräinen laskuharjoitus Palautus 7.5. klo 16.00 (suositellaan kuitenkin tekemään ennen välikoetta 30.4! Tämä laskuharjoitus ei ole pakollinen, eikä sen pisteitä
Matematiikkaa kemisteille, kevät 2012 Ylimääräinen laskuharjoitus Palautus 7.5. klo 16.00 (suositellaan kuitenkin tekemään ennen välikoetta 30.4! Tämä laskuharjoitus ei ole pakollinen, eikä sen pisteitä
Pituuden lämpötilalaajeneminen ja -kutistuminen
 8 Lämpölaajeneminen Lämpölaajeneminen tarkoittaa, että kun kappaleen lämpötila kasvaa, kasvaa myös sen koko. Vastaavasti lämpötilan laskeminen pienentää kappaleen kokoa. Kiinteiden kappaleiden pituuden
8 Lämpölaajeneminen Lämpölaajeneminen tarkoittaa, että kun kappaleen lämpötila kasvaa, kasvaa myös sen koko. Vastaavasti lämpötilan laskeminen pienentää kappaleen kokoa. Kiinteiden kappaleiden pituuden
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
