RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
|
|
|
- Olivia Leppänen
- 10 vuotta sitten
- Katselukertoja:
Transkriptio
1 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa. c) Kappaleen (systeemin) sisäenergia on rakenneosasten liike- ja potentiaalienergiaa. d) Aineeseen tai aineesta siirtyvä lämpö eli lämpömäärä on cmδ T, jossa c on aineen ominaislämpö. e) Faasi on aineen olomuotoalue. f) Kiehuminen tapahtuu lämpötilassa, jossa nesteen sisäinen höyrynpaine on yhtä suuri kuin ulkoinen paine. Jos höyrynpaine on yhtä suuri tai suurempi kuin ulkoinen paine, höyryä muodostuu kaikkialla nesteessä, eli neste kiehuu. g) Jos nesteen sisäinen höyrynpaine on matala, haihtumista tapahtuu ainoastaan nesteen pinnasta. h) Kolmoispisteen lämpötilassa ja paineessa kaikki kolme olomuotoa ovat tasapainossa keskenään. i) Entropia kuvaa systeemin järjestyksen astetta, ja se liittyy aineen mikroskooppisten rakenteiden järjestykseen. Systeemin entropia on sitä suurempi, mitä pienempi systeemin järjestys on. Luonnollisissa prosesseissa systeemin epäjärjestys kasvaa ja samalla entropia kasvaa. j) Termodynamiikan pääsäännöt: Lämpöopin nollaspääsääntö Eristetyssä systeemissä lämpötilaerot tasoittuvat. Lämpöopin ensimmäinen pääsääntö Sisäenergian muutos on Δ U + W, jossa on systeemiin/systeemistä siirtyvä lämpö ja W on systeemin tekemä/systeemiin tehtävä työ. Systeemiin siirtyvät energiat tulkitaan positiivisiksi. Lämpöopin toinen pääsääntö Sellaista lämpövoimakonetta, joka muuttaisi kaiken ottamansa lämmön työksi, ei voida rakentaa. Termodynaamisissa prosesseissa yhä vähemmän energiaa on käytettävissä työksi. Kaikki termodynaamiset prosessit suuntautuvat kohti tasapainoa. Termodynaamisissa prosesseissa entropia kasvaa. Lämpöopin kolmas pääsääntö Absoluuttista nollapistettä, 0 K, ei voi saavuttaa. k) Carnot-hyötysuhde on lämpövoimakoneen maksimihyötysuhde.
2 Physica 9 1. painos 2(7) 12.2 veden massa m 1 0,150 kg alumiinikappaleen massa m 2 0,100 kg veden ominaislämpökapasiteetti c 1 4,19 /(kg C) alumiinin ominaislämpökapasiteetti c 2? veden ja astian alkulämpötila t 1 20,0 C alumiinin alkulämpötila t 2 68 C loppulämpötila t 26 C Koska systeemi on eristetty, luovutettu lämpömäärä on yhtä suuri kuin vastaanotettu lämpömäärä. luovutettu vastaanotettu Vesi lämpenee ja alumiini jäähtyy, joten cm ( t t ) c m ( t t ), josta ratkaistaan cm 1 1( t t1) c2 m ( t t) 2 2 4,19 0,150 kg 6,0 C 0,100 kg 42 C 0,8979 0,90 kg C. kg C Vastaus: Alumiinin ominaislämpökapasiteetti on 0,90. kg C 12.3 Jääpalan massa on m j 1,00 kg ja alkulämpötila t a 20 C. Lämmitysteho on P 0,1 kw. Ratkaistaan tehon avulla jään lämpenemiseen, sulamiseen ja veden lämpenemiseen kuluvat ajat. Teho on P, Δ t josta saadaan aika Δ t. P Jään lämpeneminen jl c jmj( ta tjs ) 2, 06 1, 00kg 20 o 41,2 41, 2 0,1 kw jl Δ tjl 412 s 6,9 min P
3 Physica 9 1. painos 3(7) Jään sulaminen s sm 333 1,00 kg 333 kg s 333 Δ ts 3330 s. P 0,1 kw Jään sulamiseen ja lämmitykseen kulunut aika: Δ + Δ t s 412 s s 62,4 min. t jl Veden lämpeneminen vl cvm( tl tjs ) 4,19 1,00 kg 100 C o ,1 kw l Δ tl P Kokonaisaika Δ + Δ ts + t jl Δ tl 4190 s 412 s s s 132,3 min Piirretään lämpötilan kuvaaja Veden alkulämpötila on t v 22 C ja loppulämpötila t 1 37 C. Veden massa on m v 6,5 kg ja kivien massa m k 2,7 kg Kivien ominaislämpökapasiteetti on c k 0,83 /kg C Oletetaan, että kivi on kauttaaltaan alkulämpötilassa ja lopussa se on kokonaan loppulämpötilassa. Kivien luovuttama lämpömäärä on yhtä suuri kuin veden vastaanottama lämpömäärä. luovutettu vastaanotettu eli cm( t t) cm( t t) k k k l v v l v cm( t t) k k k k k l v v l v + cm( t t) k k k k k l v v l v Ratkaistaan kivien alkulämpötila t k k k l + cm v v( tl tv) cm k k 0,83 2,7 kg 37 C + 4,19 6,5 kg (37 C 22 C) 0,83 2,7 kg 219,2959 C 220 C. Vastaus: Kivien alkulämpötila oli 220 C.
4 Physica 9 1. painos 4(7) 12.5 veden massa m v 10,0 kg ja jään massa m j 3,0 kg jäätä. Veden alkulämpötila t v 20 C ja loppulämpötila t l 0 C. Jäätä sulaa m s, jolloin jääksi jää m j m s. veden massa m v Vesi luovuttaa lämpöä ja osa jäästä sulaa ja osa jää jääksi. Loppulämpötila on 0 C. luovutetettu vastaanotettu cm( t t) sm v v v l s Sulavan jään massa on cm v v( tv tl) ms s 4,19 10,0 kg 20 C kg 333 C 2,5165 kg 2,5 kg. Jääksi jää 3,0 kg 2,5165kg 0,4835 kg 0,50 kg. Vastaus: Jäätä jää jääksi (sulamatta) 0,50 kg a) Paineen lisäys nostaa kiehumispistettä, koska kiehumispistekäyrä (oikeanpuoleinen käyrä) nousee. b) 1 2: Ensin höyryn lämpötila laskee paineen pysyessä vakiona. Käyrällä höyry tiivistyy, sitten neste jäähtyy. 1 3: Ensin höyryn lämpötila pysyy vakiona ja höyryn paine kasvaa. Höyry tiivistyy nesteeksi lämpötilan pysyessä vakiona. c) Vallitsee tasapainotila: Vesi on sekä kaasumaisena että kiinteänä a) Jään sulamiseen kuluu energiaa. Energia otetaan vedestä, jolloin veden lämpötila laskee. b) Suihku kastelee ihoa. Iholta haihtuva vesi sitoo lämpöenergiaa ja jäähdyttää ihoa. c) Ei ole. Vesi höyrystyy kiukaalla. Höyrystyminen sitoo huomattavasti enemmän energiaa kuin veden lämmittäminen. d) Höyrystyminen sitoo energiaa. Pullossa on nestettä, joka höyrystyy paineen pienetessä, kun kaasua käytetään. e) Ilmassa oleva vesihöyry tiivistyy kylmään pintaan, sillä kylmään ilmaan mahtuu vähemmän vettä Veden massa on m 1 0,300 kg, messinki astian massa m 2 0,255 kg ja lyijyn massa m 3 0,200 kg. Veden ominaislämpökapasiteetti on c 1 4,19 /(kg C), messingin ominaislämpökapasiteetti c 2 0,380 /(kg C) ja
5 Physica 9 1. painos 5(7) lyijyn ominaislämpökapasiteetti c 3 0,128 /(kg C). Veden ja astian alkulämpötila on t 1 21,3 C ja lyijyn alkulämpötila t C. Astia ja vesi lämpenevät ja lyijy jäähtyy. luovutettu vastaanotettu eli cm ( t t ) + c m ( t t ) c m ( t t) c2m2t c2m2t1 c3m3t3 c3m3t Loppulämpötila on + + t cm + cm + cm ,19 0,300 kg 21,3 C + 0,380 0,255 kg 21,3 C + 0,128 0,200 kg 100 C 4,19 0,300 kg + 0,380 0,255 kg + 0,128 0,200 kg 22,7605 C 22,8 C. Vastaus: Loppulämpötila oli 22,8 C Astian lämpökapasiteetti C 40 J/ C, veden massa m 79 g vettä. Alkulämpötila θ 1 81 C. a) Koska lämpötilaerot pyrkivät tasoittumaan, lämpötilan kuvaaja lähenee asymptoottisesti ympäristön lämpötilaa. Ekstrapoloimalla jäähtymiskäyrää voidaan arvioida ympäristön lämpötilan olevan noin 30 C. b) Sekä vesi että astia luovuttavat jäähtyessään lämpöä ympäristöön. Kuvaajasta todetaan, että ensimmäisen 2000 sekunnin aikana systeemi on jäähtynyt lämpötilasta 81 C lämpötilaan 40 C. Täten ympäristöön siirtynyt lämpömäärä on c m( θ θ ) + C( θ θ ) v J 4,19 0, 079 kg (81 C 40 C) + 40 (81 C 40 C) C J 15.
6 Physica 9 1. painos 6(7) c) Hetkellinen lämpöteho d dθ dθ P cvm + C. dt dt dt Jäähtymisnopeus d θ hetkellä 350 s saadaan kuvaajan tangentin fysikaalisena dt kulmakertoimena. Kuviosta saadaan Δ θ 67 C C 0, Δt 2150 s s Sijoittamalla tehon P lausekkeeseen saadaan P C J C 4,19 0,079 kg 0, ,0312 s + C 11,6 W 12 W. s Vastaus: a) Ympäristön lämpötila on noin 30 C. b) Lämpöä on siirtynyt ympäristöön 15. c) Systeemistä poistuva lämpöteho hetkellä 350 s on 12 W Oletetaan, että virvoitusjuoman ominaisuudet ovat kuten veden c limu 4,19 /kg C, c jää 2,09 /kg C, s 333 /kg Olkoon loppulämpötila t x. Jään massa saadaan tiheyden ja tilavuuden tulona kg 3 3 mjää ρv 917 4,5 10 m 0, kg. 3 m Luovutetut energiat: Limonaati jäähtyy 10 C 0 C limu1 climumlim uδ tlim u 4,19 0,05kg 10 C 2,095. Limonaati jäätyy lim u2 smlim u 333 0,05kg kg 16,65. Jäätynyt limonaati jäähtyy 0 C -> t x lim u3 cjäämlim uδ tlim u jää 2,09 0,05 kg (0 C tx ) Vastaanotettu energia jää cjäämjääδ tjää 2,09 0,41265 kg ( t x ( 30 C)) Luovutetut energiat ovat yhteensä yhtä paljon kuin vastaanotettu energia + + lim u1 lim u2 lim u3 jää
7 Physica 9 1. painos 7(7) 2, ,65 + 2,09 0,05 kg (0 C tx) 2,09 0,41265 kg ( tx + 30 C) 7,3719 C -7,4 C Vastaus: Loppulämpötila on 7,4 C. t x
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöopin pääsäännöt
 Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa?
 Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Lämpöopin pääsäännöt. 0. pääsääntö. I pääsääntö. II pääsääntö
 Lämpöopin pääsäännöt 0. pääsääntö Jos systeemit A ja C sekä B ja C ovat termisessä tasapainossa, niin silloin myös A ja B ovat tasapainossa. Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta
Lämpöopin pääsäännöt 0. pääsääntö Jos systeemit A ja C sekä B ja C ovat termisessä tasapainossa, niin silloin myös A ja B ovat tasapainossa. Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta
Lämmityksen lämpökerroin: Jäähdytin ja lämmitin ovat itse asiassa sama laite, mutta niiden hyötytuote on eri, jäähdytyksessä QL ja lämmityksessä QH
 Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
Muita lämpökoneita. matalammasta lämpötilasta korkeampaan. Jäähdytyksen tehokerroin: Lämmityksen lämpökerroin:
 Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
VASTAUKSIA YO-KYSYMYKSIIN KURSSISTA FY2: Lämpö
 VASTAUKSIA YO-KYSYMYKSIIN KURSSISTA FY2: Lämpö 1. Selitä fysikaalisesti, miksi: a) sateessa kastuneet vaatteet tuntuvat kylmältä, b) pyykit kuivuvat myös pakkasessa, c) uunista pudonneen hehkuvan hiilenpalan
VASTAUKSIA YO-KYSYMYKSIIN KURSSISTA FY2: Lämpö 1. Selitä fysikaalisesti, miksi: a) sateessa kastuneet vaatteet tuntuvat kylmältä, b) pyykit kuivuvat myös pakkasessa, c) uunista pudonneen hehkuvan hiilenpalan
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
Aineen olomuodot ja olomuodon muutokset
 Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
4 Aineen olomuodot. 4.2 Höyrystyminen POHDI JA ETSI
 4 Aineen olomuodot 4.2 Höyrystyminen POHDI JA ETSI 4-1. a) Vesi asettuu astiassa vaakatasoon Maan vetovoiman ja veden herkkäliikkeisyyden takia. Painovoima tekee työtä, kunnes veden potentiaalienergia
4 Aineen olomuodot 4.2 Höyrystyminen POHDI JA ETSI 4-1. a) Vesi asettuu astiassa vaakatasoon Maan vetovoiman ja veden herkkäliikkeisyyden takia. Painovoima tekee työtä, kunnes veden potentiaalienergia
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT
 TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT (lukuun ottamatta tehtävää 12, johon kukaan ei ollut vastannut) RATKAISU TEHTÄVÄ 1 a) Vesi haihtuu (höyrystyy) ja ottaa näin ollen energiaa ympäristöstä
TERMODYNAMIIKAN KURSSIN FYS 2 KURS- SIKOKEEN RATKAISUT (lukuun ottamatta tehtävää 12, johon kukaan ei ollut vastannut) RATKAISU TEHTÄVÄ 1 a) Vesi haihtuu (höyrystyy) ja ottaa näin ollen energiaa ympäristöstä
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Oikeasta vastauksesta (1p): Sulamiseen tarvittavat lämmöt sekä teräksen suurin mahdollinen luovutettu lämpö:
 A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa eräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808 C
A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa eräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808 C
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka
 Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Alkudemonstraatio Käsi lämpömittarina Laittakaa kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä. 1) Pitäkää
Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Alkudemonstraatio Käsi lämpömittarina Laittakaa kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä. 1) Pitäkää
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA Copyright The McGraw-Hill Companies, Inc. Permission required
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA Copyright The McGraw-Hill Companies, Inc. Permission required
Työ 3: Veden höyrystymislämmön määritys
 Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Ilman suhteellinen kosteus saadaan, kun ilmassa olevan vesihöyryn osapaine jaetaan samaa lämpötilaa vastaavalla kylläisen vesihöyryn paineella:
 ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 / 14.11.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Vielä vähän entropiasta... Termodynamiikan 2. pääsääntö Entropian rooli 2. pääsäännön yhteydessä
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 / 14.11.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Vielä vähän entropiasta... Termodynamiikan 2. pääsääntö Entropian rooli 2. pääsäännön yhteydessä
LÄMPÖPUMPUN ANTOTEHO JA COP Täytä tiedot vihreisiin ruutuihin Mittauspäivä ja aika LASKE VIRTAAMA, JOS TIEDÄT TEHON JA LÄMPÖTILAERON
 LÄMPÖPUMPUN ANTOTEHO JA COP Täytä tiedot vihreisiin ruutuihin Täytä tiedot Mittauspäivä ja aika Lähdön lämpötila Paluun lämpötila 32,6 C 27,3 C Meno paluu erotus Virtaama (Litraa/sek) 0,32 l/s - Litraa
LÄMPÖPUMPUN ANTOTEHO JA COP Täytä tiedot vihreisiin ruutuihin Täytä tiedot Mittauspäivä ja aika Lähdön lämpötila Paluun lämpötila 32,6 C 27,3 C Meno paluu erotus Virtaama (Litraa/sek) 0,32 l/s - Litraa
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Lämpötila ja lämpöenergia
 Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila ja lämpöenergia Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila ja lämpöenergia Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
Luku 20. Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde
 Luku 20 Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde Uutta: Termodynamiikan 2. pääsääntö Jäähdytyskoneen hyötykerroin ja lämpöpumpun lämpökerroin Entropia Tilastollista termodynamiikkaa
Luku 20 Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde Uutta: Termodynamiikan 2. pääsääntö Jäähdytyskoneen hyötykerroin ja lämpöpumpun lämpökerroin Entropia Tilastollista termodynamiikkaa
Peruslaskutehtävät fy2 lämpöoppi kurssille
 Peruslaskutehtävät fy2 lämpöoppi kurssille Muista että kurssissa on paljon käsitteitä ja ilmiöitä, jotka on myös syytä hallita. Selvitä itsellesi kirjaa apuna käyttäen mitä tarkoittavat seuraavat fysiikan
Peruslaskutehtävät fy2 lämpöoppi kurssille Muista että kurssissa on paljon käsitteitä ja ilmiöitä, jotka on myös syytä hallita. Selvitä itsellesi kirjaa apuna käyttäen mitä tarkoittavat seuraavat fysiikan
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
Aineopintojen laboratoriotyöt 1. Veden ominaislämpökapasiteetti
 Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Kiiännö!! b) Fysiikan tunnilla tutkittiin lääkeruiskussa olevan ilman paineen riippuvuutta lämpötilasta vakiotilavuudessa ruiskuun kiinnitetyn
 FYSKKA (FY02l: 2. KURSS: Lämpö vasraa KUUTEEN (6) TEHnÄVÄÄN il KOE 21.02.2013 1. a) Suuren matkustajalentokoneen lentokorkeus maahan nähden on 10,5 km, vauhti980 km/h ja massa 310 000 kg. Laske lentokoneen
FYSKKA (FY02l: 2. KURSS: Lämpö vasraa KUUTEEN (6) TEHnÄVÄÄN il KOE 21.02.2013 1. a) Suuren matkustajalentokoneen lentokorkeus maahan nähden on 10,5 km, vauhti980 km/h ja massa 310 000 kg. Laske lentokoneen
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Oikeat vastaukset: Tehtävän tarkkuus on kolme numeroa. Sulamiseen tarvittavat lämmöt sekä teräksen suurin mahdollinen luovutettu lämpö:
 A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
Lämpötila, lämpö energiana
 Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila, lämpö energiana Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila, lämpö energiana Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 4.12. ja tiistai 5.12. Metallilangan venytys Metallilankaan tehty työ menee atomien välisten
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 4.12. ja tiistai 5.12. Metallilangan venytys Metallilankaan tehty työ menee atomien välisten
LÄMPÖOPPIA: lämpöenergia, lämpömäärä (= lämpö Q) Aineen lämpötila t aineen saaman lämpömäärän Q funktiona; t = t(q)
 LÄMPÖOPPIA: lämpöenergia, lämpömäärä (= lämpö ) Aineen lämpöila aineen saaman lämpömäärän funkina; = () C F 5 D 4 E 3 B 2 C 1 A E N E R G I A A S I T O U T U U E N E R G I A A V A P A U T U U AB: Kiineä
LÄMPÖOPPIA: lämpöenergia, lämpömäärä (= lämpö ) Aineen lämpöila aineen saaman lämpömäärän funkina; = () C F 5 D 4 E 3 B 2 C 1 A E N E R G I A A S I T O U T U U E N E R G I A A V A P A U T U U AB: Kiineä
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Luvun 12 laskuesimerkit
 Luvun 12 laskuesimerkit Esimerkki 12.1 Mikä on huoneen sisältämän ilman paino, kun sen lattian mitat ovat 4.0m 5.0 m ja korkeus 3.0 m? Minkälaisen voiman ilma kohdistaa lattiaan? Oletetaan, että ilmanpaine
Luvun 12 laskuesimerkit Esimerkki 12.1 Mikä on huoneen sisältämän ilman paino, kun sen lattian mitat ovat 4.0m 5.0 m ja korkeus 3.0 m? Minkälaisen voiman ilma kohdistaa lattiaan? Oletetaan, että ilmanpaine
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka
 Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
Kuivauksen fysiikkaa. Hannu Sarkkinen
 Kuivauksen fysiikkaa Hannu Sarkkinen 28.11.2013 Kuivatusmenetelmiä Auringon säteily Mikroaaltouuni Ilmakuivatus Ilman kosteus Ilman suhteellinen kosteus RH = ρ v /ρ vs missä ρ v = vesihöyryn tiheys (g/m
Kuivauksen fysiikkaa Hannu Sarkkinen 28.11.2013 Kuivatusmenetelmiä Auringon säteily Mikroaaltouuni Ilmakuivatus Ilman kosteus Ilman suhteellinen kosteus RH = ρ v /ρ vs missä ρ v = vesihöyryn tiheys (g/m
Tarvittavat välineet: Kalorimetri, lämpömittari, jännitelähde, kaksi yleismittaria, sekuntikello
 1 LÄMPÖOPPI 1. Johdanto Työssä on neljä eri osiota, joiden avulla tutustutaan lämpöopin lakeihin ja ilmiöihin. Työn suoritettuaan opiskelijan on tarkoitus ymmärtää lämpöopin keskeiset käsitteet, kuten
1 LÄMPÖOPPI 1. Johdanto Työssä on neljä eri osiota, joiden avulla tutustutaan lämpöopin lakeihin ja ilmiöihin. Työn suoritettuaan opiskelijan on tarkoitus ymmärtää lämpöopin keskeiset käsitteet, kuten
FY9 Fysiikan kokonaiskuva
 FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196
 VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
Kaasu Neste Kiinteä aine Plasma
 Olomuodot Kaasu: atomeilla/molekyyleillä suuri nopeus, vuorovaikuttavat vain törmätessään toisiinsa Neste: atomit/molekyylit/ionit liukuvat toistensa lomitse, mutta pysyvät yhtenä nestetilavuutena (molekyylien
Olomuodot Kaasu: atomeilla/molekyyleillä suuri nopeus, vuorovaikuttavat vain törmätessään toisiinsa Neste: atomit/molekyylit/ionit liukuvat toistensa lomitse, mutta pysyvät yhtenä nestetilavuutena (molekyylien
Ohjeellinen pituus: 2 3 sivua. Vastaa joko tehtävään 2 tai 3
 PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma
 KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma Sekä A- että B-osiosta tulee saada vähintään 10 pistettä. Mikäli A-osion pistemäärä on vähemmän kuin 10 pistettä,
KOE 3, A-OSIO Agroteknologia Agroteknologian pääsykokeessa saa olla mukana kaavakokoelma Sekä A- että B-osiosta tulee saada vähintään 10 pistettä. Mikäli A-osion pistemäärä on vähemmän kuin 10 pistettä,
LUKION FYSIIKKAKILPAILU PERUSSARJA
 PERUSSARJA Vastaa huolellisesti ja siististi! Kirjoita tekstaten koepaperiin oma nimesi, kotiosoitteesi, sähköpostiosoite, opettajasi nimi sekä koulusi nimi. Kilpailuaikaa on 100 minuuttia. Sekä tehtävä-
PERUSSARJA Vastaa huolellisesti ja siististi! Kirjoita tekstaten koepaperiin oma nimesi, kotiosoitteesi, sähköpostiosoite, opettajasi nimi sekä koulusi nimi. Kilpailuaikaa on 100 minuuttia. Sekä tehtävä-
Ch 19-1&2 Lämpö ja sisäenergia
 Ch 19-1&2 Lämpö ja sisäenergia Esimerkki 19-1 Olet syönyt liikaa täytekakkua ja havaitset, että sen energiasisältö oli 500 kcal. Arvioi kuinka korkealle mäelle sinun pitää pitää kiivetä, jotta kuluttaisit
Ch 19-1&2 Lämpö ja sisäenergia Esimerkki 19-1 Olet syönyt liikaa täytekakkua ja havaitset, että sen energiasisältö oli 500 kcal. Arvioi kuinka korkealle mäelle sinun pitää pitää kiivetä, jotta kuluttaisit
TUTKIMUS IKI-KIUKAAN ENERGIASÄÄSTÖISTÄ YHTEISKÄYTTÖSAUNOISSA
 TUTKIMUS IKI-KIUKAAN ENERGIASÄÄSTÖISTÄ YHTEISKÄYTTÖSAUNOISSA IKI-Kiuas Oy teetti tämän tutkimuksen saatuaan taloyhtiöiltä positiivista palautetta kiukaistaan. Asiakkaat havaitsivat sähkölaskujensa pienentyneen,
TUTKIMUS IKI-KIUKAAN ENERGIASÄÄSTÖISTÄ YHTEISKÄYTTÖSAUNOISSA IKI-Kiuas Oy teetti tämän tutkimuksen saatuaan taloyhtiöiltä positiivista palautetta kiukaistaan. Asiakkaat havaitsivat sähkölaskujensa pienentyneen,
Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2011 Insinöörivalinnan fysiikan koe 1.6.2011, malliratkaisut
 A1 Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2011 Täydennä kuhunkin kohtaan yhtälöstä puuttuva suure tai vakio alla olevasta taulukosta. Anna vastauksena kuhunkin kohtaan ainoastaan
A1 Diplomi-insinöörien ja arkkitehtien yhteisvalinta - dia-valinta 2011 Täydennä kuhunkin kohtaan yhtälöstä puuttuva suure tai vakio alla olevasta taulukosta. Anna vastauksena kuhunkin kohtaan ainoastaan
SISÄLLYSLUETTELO SYMBOLILUETTELO 4
 1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
Kryogeniikan termodynamiikkaa DEE Kryogeniikka Risto Mikkonen 1
 DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa 4.3.05 DEE-54030 Kryogeniikka Risto Mikkonen Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold
DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa 4.3.05 DEE-54030 Kryogeniikka Risto Mikkonen Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
Tämän päivän ohjelma: ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
Energia-alan keskeisiä termejä. 1. Energiatase (energy balance)
 Energia-alan keskeisiä termejä 1. Energiatase (energy balance) Energiataseet perustuvat energian häviämättömyyden lakiin. Systeemi rajataan ja siihen meneviä ja sieltä tulevia energiavirtoja tarkastellaan.
Energia-alan keskeisiä termejä 1. Energiatase (energy balance) Energiataseet perustuvat energian häviämättömyyden lakiin. Systeemi rajataan ja siihen meneviä ja sieltä tulevia energiavirtoja tarkastellaan.
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
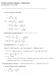 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
Palautus yhtenä tiedostona PDF-muodossa viimeistään torstaina
 PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
Entalpia - kuvaa aineen lämpösisältöä - tarvitaan lämpötasetarkasteluissa (usein tärkeämpi kuin sisäenergia)
 Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Transistori. Vesi sisään. Jäähdytyslevy. Vesi ulos
 Nesteiden lämmönjohtavuus on yleensä huomattavasti suurempi kuin kaasuilla, joten myös niiden lämmönsiirtokertoimet sekä lämmönsiirtotehokkuus ovat kaasujen vastaavia arvoja suurempia Pakotettu konvektio:
Nesteiden lämmönjohtavuus on yleensä huomattavasti suurempi kuin kaasuilla, joten myös niiden lämmönsiirtokertoimet sekä lämmönsiirtotehokkuus ovat kaasujen vastaavia arvoja suurempia Pakotettu konvektio:
Lämpöoppi 2. Energia lämpöopin kautta
 DFCL3 HAHMOTTAVA KOKEELLISUUS Kirjallinen esitys Aihekokonaisuus 9: Lämpöoppi 2. Energia lämpöopin kautta 03.11.2002 Kaisa Friman Titta Kosunen DFCL3 1 ENERGIAN PERUSHAHMOJEN ILMENEMINEN LÄMPÖOPISSA...
DFCL3 HAHMOTTAVA KOKEELLISUUS Kirjallinen esitys Aihekokonaisuus 9: Lämpöoppi 2. Energia lämpöopin kautta 03.11.2002 Kaisa Friman Titta Kosunen DFCL3 1 ENERGIAN PERUSHAHMOJEN ILMENEMINEN LÄMPÖOPISSA...
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
Fysiikan maailmankuva 2015 Luento 8. Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa?
 Fysiikan maailmankuva 2015 Luento 8 Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa? Ajan nuoli Aika on mukana fysiikassa niinkuin jokapäiväisessä
Fysiikan maailmankuva 2015 Luento 8 Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa? Ajan nuoli Aika on mukana fysiikassa niinkuin jokapäiväisessä
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KATTILAN VESIHÖYRYPIIRIN SUUNNITTELU Höyrykattilan on tuotettava höyryä seuraavilla arvoilla.
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KATTILAN VESIHÖYRYPIIRIN SUUNNITTELU Höyrykattilan on tuotettava höyryä seuraavilla arvoilla.
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus HÖYRYTEKNIIKKA 1. Vettä (0 C) höyrystetään 2 bar paineessa 120 C kylläiseksi höyryksi. Laske
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus HÖYRYTEKNIIKKA 1. Vettä (0 C) höyrystetään 2 bar paineessa 120 C kylläiseksi höyryksi. Laske
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Termodynaamisten tasapainotarkastelujen tulokset esitetään usein kuvaajina, joissa:
 Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
Kaksi yleismittaria, tehomittari, mittausalusta 5, muistiinpanot ja oppikirjat. P = U x I
 Pynnönen 1/3 SÄHKÖTEKNIIKKA Kurssi: Harjoitustyö : Tehon mittaaminen Pvm : Opiskelija: Tark. Arvio: Tavoite: Välineet: Harjoitustyön tehtyäsi osaat mitata ja arvioida vastukseen jäävän tehohäviön sähköisessä
Pynnönen 1/3 SÄHKÖTEKNIIKKA Kurssi: Harjoitustyö : Tehon mittaaminen Pvm : Opiskelija: Tark. Arvio: Tavoite: Välineet: Harjoitustyön tehtyäsi osaat mitata ja arvioida vastukseen jäävän tehohäviön sähköisessä
Aineen olomuodot. Fysiikka 2 tiivistelmä. Lämpö. Nimityksiä: systeemit. Paine. Lämpötila F A
 http://www.foxitsoftware.com For evaluation only. 7..0 Aineen olomuodot Fysiikka tiivistelmä Juhani Kaukoranta Raahen lukio 0 Kiinteä Pitää oman muotonsa astiassa Neste Saa astian muodon Kaasu Jos kansi,
http://www.foxitsoftware.com For evaluation only. 7..0 Aineen olomuodot Fysiikka tiivistelmä Juhani Kaukoranta Raahen lukio 0 Kiinteä Pitää oman muotonsa astiassa Neste Saa astian muodon Kaasu Jos kansi,
0 C lämpötilaan antaa 836 kj. Lopputuloksena on siis vettä lämpötilassa, joka on suurempi kuin 0 0 C.
 LH12-1 1 kg 2 C asteista vettä sekoitetaa yhde baari paieessa 2kg jäätä, joka lämpötila o -5 C Laske etropia muutos ja lämpötila, ku tasapaio o saavutettu 3 3 Vedelle c p 4,18 1 J/(kgK) jäälle c p 2, 9
LH12-1 1 kg 2 C asteista vettä sekoitetaa yhde baari paieessa 2kg jäätä, joka lämpötila o -5 C Laske etropia muutos ja lämpötila, ku tasapaio o saavutettu 3 3 Vedelle c p 4,18 1 J/(kgK) jäälle c p 2, 9
