Termodynamiikan toinen pääsääntö
|
|
|
- Niina Mäkelä
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 Termodynamiikan toinen pääsääntö Fysikaalisen ja kemiallisen tapahtuman spontaanisuus eli mihin suuntaan tapahtuma etenee spontaanisesti. Systeemin termodynaaminen ominaisuus, joka kertoo tapahtuman (prosessin) spontaanisuudesta, on Gibbs:in energia (tilanfuntio). Spontaaneja (suunta): Kaasun laajeneminen tilavuuteen, kuuma kappale luovuttaa lämmön ympäristöön, kemiallinen reaktio etenee tiettyyn suuntaan, Jos edellisiä tapahtumia viedään vastakkaiseen suuntaan tarvitaan työtä. Huom.: Spontaanisuus tarkoittaa siis luonnollista taipumusta asioiden etenemiseen johonkin suuntaan. Kuitenkin toteutuuko se, voi riippua muista seikoista (reaktiokinetiikka aktivoitumisenergia ; termodynamikka ei kerro, miten nopeasti spontaani prosessi tapahtuu ja mitä tietä).
2 2. PS (Kelvin) 2. Pääsääntö Kelvinin esittämässä muodossa: Mikään prosessi ei ole mahdollinen siten, että ainoa tapahtuma prosessissa olisi lämmön käyttäminen jostakin lämpölähteestä täydellisesti työksi. Osa lämmöstä menee aina lämpönä ympäristöön eikä täydellisesti työksi, siis kuvan Esittämä työ ei ole mahdollinen. (Työtä ei voi tehdä ilman energiaa.)
3 Spontaanin muutoksen suunta Mikä määrää suunnan? 1.PS esitti energian säilymisen, siis onko U? Ei! (ei systeemin kokonaisenergia U; eristetylle systeemille se on vakio) Väite: Systeemin energia pyrkii minimiin ja prosessi, joka johtaa siihen on spontaani.? Ei päde, sillä ideaalikaasun laajenemisessa energia ei muutu. Jos systeemin energia laskee prosessissa, niin ympäristön lisääntyy saman verran (1.PS). Ympäristön tapahtuma on samoin spontaani kuin systeeminkin, vaikka sen energia lisääntyy tässä prosessissa. Eristetyn systeemin kokonaisenergia on prosessissa vakio, mutta energia prosessissa jakautuu eri tavoin. Spontaanin prosessin suunta riippuukin energian jakautumisesta.
4 Energian jakautuminen Spontaanissa muutoksessa eristetyn systeemin energia jakautuu sattumanvaraisesti systeemin hiukkasten lämpöliikkeeksi. Kuvassa 3.2 pallo (systeemi) pomppii lattialla (ympäristö). Kullakin kosketuksella pallo menettää energiaa lattiaan ja sen oma liike-energia vähenee. Energia leviää lattiaan (ja ilmaan) niiden molekyylien liike-energiaksi. Lopuksi pallon liike-energia on muuttunut lattian (ja ilman) molekyylien satunnaiseksi liike-energiaksi ja pallo on paikallaan lattialla.
5 Järjestynyt järjestymätön liike Jos pallo alkaisi pomppia itsekseen pysähdyttyään edellä esitetysti lattialle, se vaatisi energian spontaania keskittymistä juuri pallon alle, eikä pelkkä lattian yleinen lämmittäminen saa sitä aikaan. Energian keskittymisen lisäksi molekyylien liikesuunta pitäisi olla sama eikä sattumanvarainen (Brownin liike). Kuva 3.3 a) pallo lattialla. b) ylöspäin ponnahtava pallo: lämpöliikkeen värähdysten pitäisi siis järjestyä samansuuntaisiksi, jotta pallo ponnahtaa.
6 Entropia 1. PS: Energian säilyminen - U (sisäenergia) osoittaa mahdolliset muutokset. 2. PS: Spontaanin prosessin suunta - S (Entropia) osoittaa spontaanit muutokset mahdollisista muutoksista. 2. PS. voidaan esittää entropian avulla: Eristetyn systeemin entropia lisääntyy spontaanissa muutoksessa: S tot > 0 S tot on systeemin ja sen ympäristön kokonaisentropia. Esim. systeemin jäähtyminen ympäristön lämpötilaan tai kaasun vapaa laajeneminen ovat spontaaneja prosesseja, joissa kokonaisentropia kasvaa.
7 Entropia termodynamiikassa Lämpö aiheuttaa satunnaisen molekyylien liikkeen lisääntymisen ympäristössä, kun systeemin energia siirtyy lämpönä. Jos energia siirtyy työnä, niin se aiheuttaa molekyylien järjestyneen liikkeen ympäristössä. Entropian määritellään: ds = dq rev /T (3.1) q rev reversiibelisti (T:n tasapainotilassa: T s = T y ) siirtynyt lämpö. Mitattava entropian muutos: S = i f dq rev /T (3.2) (yksikkö J/K ja moolientropialle (laatusuure) J K -1 mol -1 ; sama yksikkö kuin R:lla ja moolisella lämpökapasiteetilla)
8
9
10 V i = nrt/p i ja V f = nrt/p f V f /V i = p i /p f tulos (sijoitus edelliseen; ideaalikaasun Isoterminen laajeneminen)
11 Ympäristön entropia Kun pieni lämpömäärä dq sur siirtyy systeemistä ympäristöön, ympäristön entalpia muuttuu S sur. Jos ympäristö koostuu vakiotilavuudesta, niin du sur = dq sur. (Jos taas ympäristö on vakiopaineessa, niin dh sur = dq sur.) du sur (dh sur ) on tilanfunktio ja eksaktidifferentiaali ja siten riippumaton polusta (reversiibeli tai irreversiibeli). Koska du sur = dq sur (vakiotilavuus), niin siirtyvälle lämmölle pätee sama kuin sisäenergialle ja saadaan (3.1 ja 3.2): ds sur = dq sur,rev /T sur = dq sur /T sur (3.3a) S sur = dq sur /T sur (3.3b) Esimerkiksi adiabaattiselle prosessille q sur = 0 ja S sur = 0 (Kun ympäristö pysyy sisäisessä tasapainossa ei lämpötilaeroja sen tilavuuden sisällä.)
12
13 Tilastollinen näkemys entropiasta Boltzmannin jakaumalain mukaan systeemin molekyylit (atomit) voivat olla vain tietyissä energiatiloissa (Niillä on siis vain tietty energia.) eli ne voidaan jaotella tilansa mukaan kullekin energiatilalle kuuluvaksi (jakaumalaki) sen mukaan millainen lämpöenergiatila (lämpötila) niillä on. Boltzmann: Yhteys systeemin molekyylien jakaumien (energiatiloille) ja systeemin entropian välillä: S = k lnw (3.5) jossa Boltzmannin vakio k = x JK -1 ja W on mikrotilojen lukumäärä (tapojen lukumäärä, jolla molekyylit voivat asettua energiatiloille tuottamaan saman kokonaisenergian). (Kukin mikrotila kestää vain hetken dynaamisessa molekyylisysteemissä ja mitatessamme systeemin ominaisuuksia saamme keskiarvoja, joissa ovat mukana monet mikrotilat.)
14 Mikrotilat - epäjärjestys Mikrotilojen lukuisa joukko ja nopeat tilojen muutokset tuottavat käsitteet: epäjärjestys, satunnainen ja energian ja aineen jakaumat. Aineen ja energian epäjärjestynyttä jakautumista (epäjärjestyksen lisääntymistä)käytetään usein kuvaamaan entropiaa. Yhtälöä (3.5) ns. Boltzmannin kaavaa sanotaan myös tilastolliseksi entropiaksi. Kun W = 1, vastaten yhtä mikrotilaa (vain yksi tapa saavuttaa annettu energia kaikki molekyylit samassa tilassa), S = 0.
15 Mikrotilat - tilatiheys Jos on olemassa useampia tiloja, missä systeemi voi olla W > 1, S > 0. Mitä enemmän tiloja (suurempi tilatiheys), joille molekyylit miehittyvät, sitä useampia tapoja on saavuttaa koko molekyylijoukon haluttu (sama) kokonaisenergia (eli on olemassa suurempi mikrotilojen joukko kyseistä kokonaisenergiaa kohti). Tällöin W ja S ovat suurempia kuin jos mikrotilojen määrä on pienempi. (energian jakautuminen tasaisesti kaikkialle)
16 Tilavuuden muutos - tilatiheys Kuva 3.4 Hiukkanen laatikossa Kaasumolekyylien törmäily, kun tilavuus kasvaa: Keskimääräinen törmäysmatka (vapaamatka) molekyyleillä kasvaa, energiatilatiheys kasvaa [Vrt. hiukkanen laatikossa malli: E n = n 2 h 2 /(8mL 2 ), L on laatikon leveys], jolloin W ja siten S kasvavat.
17 Entropia 1/T:n funktio Boltzmannin tilastollinen käsittely selventää myös entropian käänteistä riippuvuutta lämpötilasta. Kun T on suuri mikrotilojen joukko on suuri ja tietty lämpötilan lisäys lisää mikrotilojen määrää tunnetun määrän verran. Kun T on pieni mikrotilojen joukko on pieni (T = 0 K, vain yksi mikrotila) ja sama lämpötilan lisäys kuin edellä lisää mikrotilojen määrää saman verran kuin edellä, mutta MILLÄ OLETUKSELLA? Tilatiheys on molempien lämpötilojen alueella sama!). Tällöin suhteellinen mikrotilojen lukumäärä on matalassa lämpötilassa suurempi kuin korkeassa ja S:n määritelmä ottaa sen huomioon (1/T).
18 S tilanfunktio Entropia on tilafunktio ei riipu siitä, miten tila saavutetaan. Osoitus: Jos yhtälön 3.1 integraali satunnaisen tapahtumasyklin ympäri takaisin lähtötilaan (merkintä ) on nolla, niin S on tilanfunktio (ds eksaktidifferentiaali) dq rev /T rev = 0 (3.6) 1.Osoitetaan todeksi ideaalikaasun Carnot syklille 2. Osoitetaan, että tulos on totta mille tahansa aineelle. 3. Osoitetaan, että se on tosi mille tahansa syklille.
19 Termodynaaminen sykli Kuva 3.5: Tilasta i tilaan f ja takaisin (i) muodostaa syklin, jonka tilafunktion kokonaismuutos on nolla.
20 Carnot-syklin rakenne (1.) Kuva 3.6: 1. A B reversiibeli, isoterminen laajeneminen T h :ssa, 2. B C reversiibeli, adiabaattinen laajeneminen, 3. C D reversiibeli, isoterminen kokoonpuristus T c :ssa, 4. D A reversiibeli, adiabaattinen puristuminen
21 Carnot-sykli Carnot-sykli muodostuu 4 reversiibelistä askeleesta, joissa entropian muutokset S ovat: 1. A B reversiibeli, isoterminen laajeneminen T h :ssa: S = q h /T h, jossa q h systeemiin tuotu lämpö kuumasta lämpölähteestä (h) 2. B C reversiibeli, adiabaattinen laajeneminen: q = 0 eli S = 0, jolloin T h T c [kylmä lämmön poistajan lämpötila, (c)] 3. C D reversiibeli, isoterminen kokoonpuristus T c :ssa:energia siirtyy kylmään lämmön poistajaan (q c, negatiivinen) ja S = q c /T c 4. D A reversiibeli, adiabaattinen kokoonpuristuminen: q = 0 eli S = 0, jolloin T c T h. Näistä saadaan: ds = q h /T h + q c /T c, jossa osoitetaan, että q h /q c = T h /T c, (3.7) jolloin ds = 0.
22 Carnot-sykli: q h /q c = T h /T c :n perustelu Syklin ominaispiirteet: (Huom. Ideaalikaasun (IK) reversiibeli, adiabaattinen ja isoterminen muutos, käsitelty aiemmin ) 1. Sama adiabaatti (q = 0 ks. esim. kuvat 2.18 ja 2.21) kulkee A:n ja D:n sekä B:n ja C:n [A (T h ) ja D (T c ) sekä B (T h ) ja C (T c )] kautta (kuva 3.6). 2. Energian siirto q:na IK:n isotermisissä askeleissa on: q h = nrt h ln (V B /V A ) ja q c = nrt c ln (V D /V C )
23
24 Edellinen pätee mille tahansa aineelle (2.) Lämpökoneen tehokkuus * hyötysuhde (positiivinen luku), määritelmä]: η =Tehty työ/lämpölähteestä saatu lämpö = w / q h (3.8) Kuva 3.7: η = ( q h q c )/ q h = 1 q c / q h (3.9) Yhtälöstä 3.7 (1. todistus) seuraa: η = 1 T c /T h (3.10) (= Carnot-hyötysuhde) Osoitus: Kaikkilla reversiibeleillä koneilla on sama tehokkuus riippumatta niiden rakenteesta. [Kahden reversiibelin koneen vertailu (Kuva 3.8)]
25 Koneiden tehokkuus vertailu (Atkins s.101) Kuva 3.8: Ajattelemalla kone A tehokkaammaksi kuin B tekemään työtä samassa lämpötilassa (T h ja T c ) olevien lämpövarastojen välillä johtaa ristiriitaan 2. pääsäännön (Kelvin) kanssa. (Atkins s.101) Siten koneet ovat yhtä tehokkaita ja yhtälö 3.10 pätee Carnotsyklin kaikille aineille.
26 Tosi mille tahansa syklille (3.) Väite: dq rev /T rev = 0 kaikille sykleille: Perustelu: Arvio mistä tahansa reversiibelistä syklistä voidaan laskea summan avulla joukosta Carnot-syklejä. Kuva 3.9 Tämä arvio paranee, kun Carnot-syklit pienennetään infinidesimaalisiksi (siirrytään summasta integraaliin). Koska kunkin Carnot-syklin ds = 0, on niiden summakin nolla ja väite on tosi. SIIS 1, 2 ja 3 ovat totta ja S on tilanfunktio
27 Termodynaaminen lämpötila Kone toimii reversiibelisti kahden lämpötilan välillä T h (lämmönlähde) ja T (kylmä lämmönpoistaja). Yhtälöstä 3.10 saadaan: T = (1 η) T h (3.11) Tällä yhtälöllä Kelvin määritteli termodynaamisen lämpötila-asteikon lämpökoneen hyötysuhteen avulla: Lämpölähde on korkeassa lämpötilassa T h ja tarkastelemme T:tä. Kelvinin asteikossa T h = K, veden triplettipiste. Jos esimerkiksi jonkin koneen η = 0.20, silloin kylmän lämmönpoistajan lämpötila on T = (1 0.2) K = 220 K. Tämä arvo ei riipu aineesta.
28 Clausiuksen epäyhtälö Reversiibeli työ on suurempi (tai yhtä suuri) kuin irreversiibeli: dw rev dw (negatiivisia systeemin kannalta) joten edellinen on sama kuin: - dw rev - dw eli dw - dw rev 0* Tilanfunktiona U on sama reversiibelille ja irreversiibelille muutokselle: du = dq + dw = dq rev + dw rev. Siten dq rev - dq = dw - dw rev 0 (*ks. edellä) tai dq rev dq ja dq rev /T dq/t eli ds = dq rev /T dq/t (Clausiuksen epäyhtälö) (3.12) Jos systeemi on eristetty, dq = 0 ja ds 0 (ed. perusteella): Eristetyssä systeemissä S ei voi pienentyä spontaanissa prosessissa.
29 Lämmönsiirto kuumasta kylmään Kuva 3.10: Energia siirtyy T h lähteestä lämpönä S pienenee (1/T h ). Kun sama energia siirtyy T c jäähdyttäjään S lisääntyy suuremmalla määrällä (1/T c ). Kokonaisentropia kasvaa eli prosessi on spontaani.
30 Lämmönsiirto kuumasta kylmään
31 Tekniset sovellutukset (Jähdyttäjän teho (hyötysuhde) samoin kuin aiemmin. ) Jäähdytys: Energia q c siirtyy T c jäähdyttäjästä huoneeseen (T h ): S = - q c /T c + q c /T h < 0 (3.14) Prosessi ei ole spontaani (jälkimmäinen tekijä pienempi) eli lämpimässä huoneessa entropia ei kasva riittävästi, jotta olisi suurempi kuin entropian pieneneminen kylmässä energialähteessä. Määritellään termodynaaminen hyötysuhde (coefficient of performance): c = lämpönä siirtynyt energia/työnä siirtynyt energia = q c / w (3.15)
32 Kuva 3.11: Jääkaapin toiminta a) Energiavirta kylmästä energialähteestä kuumaan luovutustilaan ei ole spontaani. Entropian lisäys kuumassa on pienempi kuin sen väheneminen kylmässä. Summa on negatiivinen. b) b) Jos lisätään energiaa työnä korvaamaan entropiaero, niin kokonaisentropia saadaan positiiviseksi ja prosessi voi tapahtua (tulee spontaaniksi).
33
34
35 Erityisprosessien entropianmuutos a) Ideaalikaasun isotermisen laajenemisen entropianmuutos b) Entropianmuutos aineen tilan (faasin) muutokselle muutoslämpötilassa (faasimuutosentropia) c) Aineen lämpenemisen entropianmuutos (lämpökapasiteetin avulla) d) Aineen entropianmuutos lämpötilamuutoksessa, joka sisältää myös faasimuutoksen ( kokonaismuutos ) a) Ideaalikaasun isotermisen laajeneminen: (Esim. 3.1) S = nr ln (V f /V i ) (3.17)
36 Ideaalikaasun isotermisen laajeneminen (V i V f ) S on tilafunktio ja S systeemille ei liity siirtymätiehen tilojen välillä eli ei riipu siitä tapahtuuko siirtymä reversiibelisti tai irreversiibelistä. Kuva 3.12: S = nr ln (V f /V i ) (3.17) Ideaalikaasun isotermisen laajeneminen on irreversiibeli tapahtuma, jossa tarkastelemme sekä systeemin, että ympäristön entropian muutosta.
37 Kokonaisentropia S tot riippuu siitä miten laajeneminen tapahtuu. Kaikille tapahtumille ympäristö ottaa vastaan lämpönä systeemin energian: dq sur = dq. * Reversiibelille muutokselle (esimerkki 3.1): q rev = nrt ln (V f /V i ), josta yhtälön 3.3b mukaan: S sur = q sur /T = q rev /T = nr ln (V f /V i ) (3.18) Systeemille muutos on negatiivinen (vastakkaismerkkinen), jolloin S tot = 0. * Toisaalta, jos ideaalikaasun vapaa laajeneminen (w = 0), niin q = 0 (koska U = 0). Siten S sur = 0 ja S tot saadaan yhtälöstä 3.17: S tot > 0 S tot = nr ln (V f /V i ) (3.19) (irreversiibeli)
38 Faasimuutoksen entropia Kun aine nesteytyy tai kiinteytyy, niin moolekyylien liike muuttuu ja samalla aineen ja energian jakautuminen systeemissä muuttuu ja myös entropia muuttuu: Nesteen höyrystyessä kaasuksi (tai kiinteän nesteytyessä), molekyylien vapausasteet lisääntyvät eli entropia kasvaa. Systeemi ja ympäristö ovat normaalissa faasisiirtymän lämpötilassa (kaksi faasia tasapainossa) esim. 0 o C (273 K) vesi/jää tasapainolle ja 100 o C (373 K) vesihöyry/vesi (neste) tasapainossa, kun p = 1 atm molemmissa tasapainoissa. Paine on vakio tasapainoille energian siirtyminen systeemin ja ympäristön välillä on lämmön siirto q = trs H ja molaarinen systeemin entropian muutos trs S = trs H/T trs (3.20)
39 Faasimuutoksen standardientropioita Eksotermiselle muutokselle trs H/T trs < 0 (systeemi luovuttaa energiaa, kun se kondensoituu) ja systeemin järjestys lisääntyy. Jos trs H/T trs > 0 (endoterminen), järjestys vähenee (esim. höyrystyminen). Ympäristön entropia vähenee saman verran kuin systeemin lisääntyy, joten trs S tot = 0
40 Standardihöyrystymisentropia Monien nesteiden standardihöyrystymisentropia on noin 85 JK -1 mol -1 (Troutonin sääntö; kokeellinen tulos samankaltainen tilavuuden muutos nesteille).
41
42 Yhtälöstä 3.2 saadaan: Lämmitys S(T f ) = S(T i ) + Ti Tf dq rev /T (3.21) Vakio paineessa dq rev = C p dt (yht. 2.22) ja S(T f ) = S(T i ) + Ti Tf C p dt/t (3.22) Vakio tilavuudessa: S(T f ) = S(T i ) + Ti Tf C V dt/t. Jos esim. C p ei riipu T:sta: S(T f ) = S(T i ) + C p Ti Tf dt/t = S(T i ) + C p ln(t f /T i ) (3.23) on samanlainen kuin lämmitykselle V vakiona. (kuva 3.13)
43 Kuva 3.13: Entropian logaritminen lisäys lämmitettäessä ainetta V vakiona. Eri käyrät vastaavat eri C V :n arvoja (C V,m /R). S/nR vs T f /T i
44
45
46
47 Entropian mittaukset Yhtälön 3.22 avulla voidaan S(T) liittää S(T = 0) mittaamalla aineen C p eri lämpötiloissa ja lisäämällä faasimuutosentropiat kussakin faasimuutos lämpötilassa. Muut suureet paitsi S m (0) voidaan mitata kalorimetrisesti ja integrointi lämpötilojen välillä joko graafisesti tai sovittamalla mittaustietoon polynoomi (Taulukko 2.2: C = a + bt +ct 2 ), jonka integrointi voidaan tehdä analyyttisesti (esimerkki).
48 Entropia mittausten avulla Kuva 3.14 esittää menettelyn: Pinta-ala käyrän (C p,m /T vs. T) alla on vaadittu integraali. Vaihtoehtoisesti voidaan laskea vastaava pinta-ala käyrälle C p,m vs. lnt, koska dt /T = lnt. Lämpötiloissa T f (sulaminen) ja T b (kiehuminen) tapahtuu faasisiirtymä (kaksi faasia tasapainossa). Muissa lämpötiloissa yksi faasi (kaasu, neste tai kiinteä) lämpenee. (Jos aine hajoaa ennen jotain em. faasimuutoksista, systeemissä täytyy hajoamisentropia huomioida ja tämän lämpötilan yläpuolella systeemi entropian määräävät hajoamistuotteiden entropiat.) Lähellä T = 0 K: C p = at 3 (perustelu luvussa 7, Debyen extrapolointi).
49
50
51
52 3. Termodynamiikan pääsääntö T = 0 :ssa täydellisessä kiteessä aineen rakenne on täysin järjestäytynyt ja siten sen entropia voidaan ajatella nollaksi. (S = 0, jos on olemassa vain yksi mahdollinen miehitystapa eli yksi mikrotila; Boltzmannin yhtälö 3.5: W = 1) Nerstin lämpöteoreema: Kaikkien fysikaalisten ja kemiallisten tapahtumien entropianmuutos lähestyy nollaa, kun T 0. ( S 0, kun T 0, jolloin aineella on täydellinen järjestys) Nerstin teoreema Jos alkuaineilla on täydellinen kidetila T = 0:ssa ja asetamme niille S = 0, niin kaikille täydellisille kiteille S = 0, kun T = termodynamiikan pääsääntö: Aineen täydellisen kidemuodon entropia on 0, kun T = 0. (Tämä helpottaa asian käsittelyä)
53
54 Molekyylien liittyminen aineeksi T = 0:ssa Esimerkiksi molekyyli AB voi (T = 0) muodostaa aineelle kaksi kiderakennetta: ABABABAB tai BABABABA, jolloin W > 1 ja S > 0 aineella on jäännösentropia T = 0:ssa. Vesijään jäännösentropia on 3.4 JK -1 mol -1 : Jäässä vetysidokset ovat sitomassa molekyylejä yhteen ja kukin O- atomi on sitoutunut kahdella lyhyellä sidoksella kahteen vetyyn ja (noin?) kahdella pitkällä sidoksella kahteen muuhun vetyyn (naapurimolekyylissä). Nämä vuorovaikutukset voinevat vaihdella satunnaisesti vielä T = 0:ssa jäännösentropia.
55 3. pääsäännön entropiaksi nimitetään entropioita, jotka perustuvat määritelmään: = 0, kun T = 0. Kun aine on standarditilassaan lämpötilassa T, merkitään (3. pääsäännön) standardientropia = S Θ (T). Reaktioentropia määritellään: r S Θ = Tuotteet νs mθ Lähtöaineet νs m Θ tai r S Θ = J ν J S mθ (J) 3. Pääsäännön entropia (3.25a) S (3.25b)
56 x69.9 ( x205.1) JK-1mol-1
57 Ionien standardientropia Kationeja ei voi tuottaa neutraalissa vesiliuoksessa ilman anioneja (vrt. Kappale 2.8), joten määritellään H + :lle S Θ (H +, aq) = 0 (3.26) Muita ioneja voidaan verrata tähän ja määräys aiheuttaa sen, että ionien standardientropiat voivat olla joko positiivisia tai negatiivisia. Esimerkiksi: Cl - (aq) = + 57 JK -1 mol -1 ja Mg 2+ (aq) = JK -1 mol -1 (eli Cl - :n entropia on korkeampi kuin H + :n vedessä) Riippuu: ionien koosta ja varauksesta pieni koko ja suuri varaus vaikuttaa liuottinmolekyylien järjestykseen enemmän kuin yksinkertaisesti varattu suuri ioni.
58 Kiinteän aineen hilavirheet 3. lain mukaan täydelliselle kidehilalle T=0:ssa S = 0. Aineen ominaisuuksien muuttamiseksi (kovuus, sähkönjohtavuus, väri ) kidehilaan halutaan kuitenkin usein täydellistä kiderakennetta häiritsevä epäpuhtaus tai muu kiderakenteellinen muutos (hiili raudassa, seospuolijohteet, korukivi, raudan karkaisu ). Hilan pistevirhe (point defect, void, lattice vacancy, substitutional impurity atom, interstitial impurity atom, dopand site ) syntyy tyhjästä atomipaikasta tai muusta epäsäännöllisyydestä rakenteessa. Hilavirheet vaikuttavat entropiaan.
59 Kuva 3.15: Hilavirheenä H 2 ja D 2 niobiumissa vaikuttavat (lämpökapasiteettiin ja) entropiaan. Kuten aiemmin (3.22) havaittiin, käyrän ( C p /T T:n funktiona) avulla saadaan entropia laskettua tietyssä lämpötilamuutoksessa integroimalla alku- ja loppulämpötilojen välillä. Niobium (puhdas) on tärkeä metalli matalan lämpötilan superjohteissa Vaikutus materiaalikemiaan
Spontaanissa prosessissa Energian jakautuminen eri vapausasteiden kesken lisääntyy Energia ja materia tulevat epäjärjestyneemmäksi
 KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
Lämmityksen lämpökerroin: Jäähdytin ja lämmitin ovat itse asiassa sama laite, mutta niiden hyötytuote on eri, jäähdytyksessä QL ja lämmityksessä QH
 Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Muita lämpökoneita. matalammasta lämpötilasta korkeampaan. Jäähdytyksen tehokerroin: Lämmityksen lämpökerroin:
 Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
Luku Pääsääntö (The Second Law)
 Luku 3 2. Pääsääntö (he Second Law) Some things happen naturally, some things don t Spontaneous must be interpreted as a natural tendency that may or may not be realized in prac=ce. hermodynamics is silent
Luku 3 2. Pääsääntö (he Second Law) Some things happen naturally, some things don t Spontaneous must be interpreted as a natural tendency that may or may not be realized in prac=ce. hermodynamics is silent
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luku 20. Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde
 Luku 20 Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde Uutta: Termodynamiikan 2. pääsääntö Jäähdytyskoneen hyötykerroin ja lämpöpumpun lämpökerroin Entropia Tilastollista termodynamiikkaa
Luku 20 Kertausta: Termodynamiikan 2. pääsääntö Lämpövoimakoneen hyötysuhde Uutta: Termodynamiikan 2. pääsääntö Jäähdytyskoneen hyötykerroin ja lämpöpumpun lämpökerroin Entropia Tilastollista termodynamiikkaa
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
6. Yhteenvetoa kurssista
 Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
1 Clausiuksen epäyhtälö
 1 PHYS-C0220 ermodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Clausiuksen epäyhtälö Carnot n koneen syklissä lämpötilassa H ja L vastaanotetuille lämmöille Q H ja Q L pätee oisin ilmaistuna,
1 PHYS-C0220 ermodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Clausiuksen epäyhtälö Carnot n koneen syklissä lämpötilassa H ja L vastaanotetuille lämmöille Q H ja Q L pätee oisin ilmaistuna,
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 / 14.11.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Vielä vähän entropiasta... Termodynamiikan 2. pääsääntö Entropian rooli 2. pääsäännön yhteydessä
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 9 / 14.11.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Vielä vähän entropiasta... Termodynamiikan 2. pääsääntö Entropian rooli 2. pääsäännön yhteydessä
Ekvipartitioteoreema. Entropia MB-jakaumassa. Entropia tilastollisessa mekaniikassa
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
Lämpöopin pääsäännöt
 Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
7 Termodynaamiset potentiaalit
 82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
2. Termodynamiikan perusteet
 Statistinen fysiikka, osa A (FYSA241) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL249. Ei kiinteitä vastaanottoaikoja. kl 2013 2. Termodynamiikan perusteet 1 TD ja SM Statistisesta fysiikasta voidaan
Statistinen fysiikka, osa A (FYSA241) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL249. Ei kiinteitä vastaanottoaikoja. kl 2013 2. Termodynamiikan perusteet 1 TD ja SM Statistisesta fysiikasta voidaan
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 3: Lämpövoimakoneet ja termodynamiikan 2. pääsääntö Maanantai 13.11. ja tiistai 14.11. Milloin prosessi on adiabaattinen?
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 3: Lämpövoimakoneet ja termodynamiikan 2. pääsääntö Maanantai 13.11. ja tiistai 14.11. Milloin prosessi on adiabaattinen?
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
Ch 19-1&2 Lämpö ja sisäenergia
 Ch 19-1&2 Lämpö ja sisäenergia Esimerkki 19-1 Olet syönyt liikaa täytekakkua ja havaitset, että sen energiasisältö oli 500 kcal. Arvioi kuinka korkealle mäelle sinun pitää pitää kiivetä, jotta kuluttaisit
Ch 19-1&2 Lämpö ja sisäenergia Esimerkki 19-1 Olet syönyt liikaa täytekakkua ja havaitset, että sen energiasisältö oli 500 kcal. Arvioi kuinka korkealle mäelle sinun pitää pitää kiivetä, jotta kuluttaisit
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Entalpia - kuvaa aineen lämpösisältöä - tarvitaan lämpötasetarkasteluissa (usein tärkeämpi kuin sisäenergia)
 Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Kryogeniikan termodynamiikkaa DEE Kryogeniikka Risto Mikkonen 1
 DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa 4.3.05 DEE-54030 Kryogeniikka Risto Mikkonen Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold
DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa 4.3.05 DEE-54030 Kryogeniikka Risto Mikkonen Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
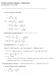 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
Lämpöopin pääsäännöt. 0. pääsääntö. I pääsääntö. II pääsääntö
 Lämpöopin pääsäännöt 0. pääsääntö Jos systeemit A ja C sekä B ja C ovat termisessä tasapainossa, niin silloin myös A ja B ovat tasapainossa. Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta
Lämpöopin pääsäännöt 0. pääsääntö Jos systeemit A ja C sekä B ja C ovat termisessä tasapainossa, niin silloin myös A ja B ovat tasapainossa. Eristetyssä systeemissä eri lämpöiset kappaleet asettuvat lopulta
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
IX TOINEN PÄÄSÄÄNTÖ JA ENTROPIA...208
 IX OINEN PÄÄSÄÄNÖ JA ENROPIA...08 9. ermodynaamisen systeemin pyrkimys tasapainoon... 08 9. ermodynamiikan toinen pääsääntö... 0 9.3 Entropia termodynamiikassa... 0 9.3. Entropian määritelmä... 0 9.3.
IX OINEN PÄÄSÄÄNÖ JA ENROPIA...08 9. ermodynaamisen systeemin pyrkimys tasapainoon... 08 9. ermodynamiikan toinen pääsääntö... 0 9.3 Entropia termodynamiikassa... 0 9.3. Entropian määritelmä... 0 9.3.
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA Copyright The McGraw-Hill Companies, Inc. Permission required
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 8 EXERGIA: TYÖPOTENTIAALIN MITTA Copyright The McGraw-Hill Companies, Inc. Permission required
Palautus yhtenä tiedostona PDF-muodossa viimeistään torstaina
 PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
Biofysiikka Luento Entropia, lämpötila ja vapaa energia. Shannonin entropia. Boltzmannin entropia. Lämpötila. Vapaa energia.
 Biofysiikka Luento 7 1 6. Entropia, lämpötila ja vapaa energia Shannonin entropia Boltzmannin entropia M I NK P ln P S k B j1 ln j j Lämpötila Vapaa energia 2 Esimerkkiprobleemoita: Miten DNA-sekvenssistä
Biofysiikka Luento 7 1 6. Entropia, lämpötila ja vapaa energia Shannonin entropia Boltzmannin entropia M I NK P ln P S k B j1 ln j j Lämpötila Vapaa energia 2 Esimerkkiprobleemoita: Miten DNA-sekvenssistä
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
Ohjeellinen pituus: 2 3 sivua. Vastaa joko tehtävään 2 tai 3
 PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
Tämän päivän ohjelma: ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics)
 2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
Termodynamiikka. Fysiikka III 2007. Ilkka Tittonen & Jukka Tulkki
 Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
PHYS-A0120 Termodynamiikka. Emppu Salonen
 PHYS-A0120 ermodynamiikka Emppu Salonen 1. joulukuuta 2016 ermodynamiikka 1 1 Lämpötila ja lämpö 1.1 ilanyhtälö arkastellaan kolmea yksinkertaista fluidisysteemiä 1, jotka koostuvat kukin vain yhdentyyppisistä
PHYS-A0120 ermodynamiikka Emppu Salonen 1. joulukuuta 2016 ermodynamiikka 1 1 Lämpötila ja lämpö 1.1 ilanyhtälö arkastellaan kolmea yksinkertaista fluidisysteemiä 1, jotka koostuvat kukin vain yhdentyyppisistä
Thermodynamics is Two Laws and a Li2le Calculus
 Thermodynamics is Two Laws and a Li2le Calculus Termodynamiikka on joukko työkaluja, joiden avulla voidaan tarkastella energiaan ja entropiaan lii2yviä ilmiötä kaikissa luonnonilmiöissä ja lai2eissa Voidaan
Thermodynamics is Two Laws and a Li2le Calculus Termodynamiikka on joukko työkaluja, joiden avulla voidaan tarkastella energiaan ja entropiaan lii2yviä ilmiötä kaikissa luonnonilmiöissä ja lai2eissa Voidaan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ
 I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 1: Lämpötila ja Boltzmannin jakauma Ke 24.2.2016 1 YLEISTÄ KURSSISTA Esitietovaatimuksena
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 1: Lämpötila ja Boltzmannin jakauma Ke 24.2.2016 1 YLEISTÄ KURSSISTA Esitietovaatimuksena
Integroimalla ja käyttämällä lopuksi tilanyhtälöä saadaan T ( ) ( ) H 5,0 10 J + 2,0 10 0,50 1,0 10 0,80 Pa m 70 kj
 S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
19.6-7 Harvan kaasun sisäenergia ja lämpökapasiteetit
 19.6-7 Harvan kaasun sisäenergia ja lämpökapasiteetit Kokeelliset havainnot ja teoria (mm. luku 18.4) Ainemäärän pysyessä vakiona harvan kaasun sisäenergia riippuu ainoastaan sen lämpötilasta eli U = U(T
19.6-7 Harvan kaasun sisäenergia ja lämpökapasiteetit Kokeelliset havainnot ja teoria (mm. luku 18.4) Ainemäärän pysyessä vakiona harvan kaasun sisäenergia riippuu ainoastaan sen lämpötilasta eli U = U(T
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196
 VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
VIII KIERTOPROSESSIT JA TERMODYNAAMISET KONEET 196 8.1 Kiertoprosessin ja termodynaamisen koneen määritelmä... 196 8.2 Termodynaamisten koneiden hyötysuhde... 197 8.2.1 Lämpövoimakone... 197 8.2.2 Lämpöpumpun
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
4. Termodynaamiset potentiaalit
 Statistinen fysiikka, osa A (FYSA241) uomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL249. Ei kiinteitä vastaanottoaikoja. kl 2013 4. ermodynaamiset potentiaalit 1 asapainotila Mikrokanoninen ensemble Eristetty
Statistinen fysiikka, osa A (FYSA241) uomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL249. Ei kiinteitä vastaanottoaikoja. kl 2013 4. ermodynaamiset potentiaalit 1 asapainotila Mikrokanoninen ensemble Eristetty
infoa tavoitteet E = p2 2m kr2 Klassisesti värähtelyn amplitudi määrää kokonaisenergian Klassisesti E = 1 2 mω2 A 2 E = 1 2 ka2 = 1 2 mω2 A 2
 infoa tavoitteet Huomenna keskiviikkona 29.11. ei ole luentoa. Oppikirjan lukujen 12-13.3. lisäksi kotisivulla laajennettu luentomateriaali itse opiskeltavaksi Laskarit pidetään normaalisti. Ymmärrät mitä
infoa tavoitteet Huomenna keskiviikkona 29.11. ei ole luentoa. Oppikirjan lukujen 12-13.3. lisäksi kotisivulla laajennettu luentomateriaali itse opiskeltavaksi Laskarit pidetään normaalisti. Ymmärrät mitä
Mikrotila Makrotila Statistinen paino Ω(n) 3 Ω(3) = 4 2 Ω(2) = 6 4 Ω(4) = 1
 76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 3: Lämpövoimakoneet ja termodynamiikan 2. pääsääntö Maanantai 14.11. ja tiistai 15.11. Kurssin aiheet 1. Lämpötila ja lämpö
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 3: Lämpövoimakoneet ja termodynamiikan 2. pääsääntö Maanantai 14.11. ja tiistai 15.11. Kurssin aiheet 1. Lämpötila ja lämpö
Luento 2: Lämpökemiaa, osa 1 Torstai klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Vauhti = nopeuden itseisarvo. Nopeuden itseisarvon keskiarvo N:lle hiukkaselle määritellään yhtälöllä
 S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
energian), systeemi on eristetty (engl. isolated). Tällöin sekä systeemiin siirtynyt
 14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
SISÄLLYSLUETTELO SYMBOLILUETTELO 4
 1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
Termodynaamiset syklit Todelliset tehosyklit
 ermodynaamiset syklit odelliset tehosyklit Luennointi: k Kati Miettunen Esitysmateriaali: k Mikko Mikkola HYS-A00 ermodynamiikka (FM) 09..05 Syklien tyypit Sisältö Kaasusyklit s. höyrysyklit Suljetut syklit
ermodynaamiset syklit odelliset tehosyklit Luennointi: k Kati Miettunen Esitysmateriaali: k Mikko Mikkola HYS-A00 ermodynamiikka (FM) 09..05 Syklien tyypit Sisältö Kaasusyklit s. höyrysyklit Suljetut syklit
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, Luku 7 ENTROPIA
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 7 ENTROPIA Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 7 ENTROPIA Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
DEE Kryogeniikka
 DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold tip tirling aim com mod.jpg Introduced about
DEE-54030 Kryogeniikka Kryogeniikan termodynamiikkaa Open ystem vs. Closed ystem Open system Melting Closed system Introduced about 900 Cryocooler Boiling Cold tip tirling aim com mod.jpg Introduced about
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Entrooppiset voimat. Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit
 Entrooppiset voimat Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Entrooppiset voimat Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
6. Entropia, lämpötila ja vapaa energia
 6. Entropia, lämpötila a vapaa energia 1 Luento 6 24.2.2017: Shannonin entropia M I NK P ln P 1 Boltzmannin entropia S k B ln Lämpötila Vapaa energia 2 Probleemoita: Miten DNA-sekvenssistä määräytyvän
6. Entropia, lämpötila a vapaa energia 1 Luento 6 24.2.2017: Shannonin entropia M I NK P ln P 1 Boltzmannin entropia S k B ln Lämpötila Vapaa energia 2 Probleemoita: Miten DNA-sekvenssistä määräytyvän
Luento 8 6.3.2015. Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit
 Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 4.12. ja tiistai 5.12. Metallilangan venytys Metallilankaan tehty työ menee atomien välisten
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 4.12. ja tiistai 5.12. Metallilangan venytys Metallilankaan tehty työ menee atomien välisten
η = = = 1, S , Fysiikka III (Sf) 2. välikoe
 S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
6-1 Hyötysuhde ja tehokerroin
 67 6 Lämpövoimakoneet ja jäähdyttimet 6-1 Hyötysuhde ja tehokerroin Lämpövoimakone (engl. heat engine) on laite, joka muuttaa lämpöenergiaa työksi. Tavallisesti laitteessa tapahtuu kiertoprosessi, jonka
67 6 Lämpövoimakoneet ja jäähdyttimet 6-1 Hyötysuhde ja tehokerroin Lämpövoimakone (engl. heat engine) on laite, joka muuttaa lämpöenergiaa työksi. Tavallisesti laitteessa tapahtuu kiertoprosessi, jonka
