Korkealämpötilakemia
|
|
|
- Annika Halonen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 Korkealämpötilakemia Binääriset tasapainopiirrokset To klo 8-10 SÄ114 Tavoite Oppia lukemaan ja tulkitsemaan binäärisiä tasapainopiirroksia 1
2 Sisältö Hieman kertausta - Gibbsin vapaaenergian pitoisuusriippuvuudesta Binääristen tasapainopiirrosten perustyypit - Aukoton liukoisuus - Eutektinen, peritektinen ja monotektinen tasapaino Välifaasit Vipusääntö Esimerkkejä ja tehtäviä Tasapainopiirrosten ja aktiivisuuksien suhteesta Tasapainopiirrosten määrityksestä Tasapainopiirrosten yksinkertaistaminen vakio-oletuksilla Vakioidaan paine, lämpötila tai jokin pitoisuusmuuttuja - Tuloksena helpommin luettava kuvaajat 2
3 Binääriset koostumuslämpötila-kuvaajat Tasapainopiirrokset (monimutkaisemmatkin) koostuvat tietyistä perustyypeistä - Aukoton liukoisuus - Eutektinen tasapaino - Peritektinen tasapaino - Monotektinen tasapaino - Välifaasit Kuvaajien lukemisessa ja tulkinnassa on tunnistettava nämä perustyypit sekä osattava käyttää ns. vipusääntöä Kertausta: Gibbsin vapaaenergia koostumuksen funktiona - Tarkastellaan kahdessa osassa: G = H 0 TS m - H 0 kuvaa systeemin atomien lämpösisältöä - S m on sekoittumisentropia - Vapaaenergian pitoisuusriippuvuuden muoto riippuu seoksen komponenttien välisistä vuorovaikutuksista - Sekoittumisentropia ja lämpötila ovat aina positiivisia - TS m termi on aina alaspäin kaareutuva käyrä/pinta - Komponenttien (esim. binäärisysteemin A ja B) väliset vuorovaikutusenergiat (merkitään V AA, V BB ja V AB ) vaihtelevat - H 0 -käyrä voi kaartua ylös- tai alaspäin - Vapaaenergiakäyrän tai pinnan muoto saadaan näiden kahden termin summana 3
4 Gibbsin vapaaenergia koostumuksen funktiona Vapaaenergian pitoisuusriippuvuuden muoto voi olla erilainen eri lämpötiloissa - Heijastuu lopulliseen tasapainopiirrokseen Tasapainotilan kahden eri koostumuksen välillä Kaksi eri koostumuksen omaavaa faasia/ainetta voivat olla tasapainossa keskenään, kun niillä on sama kemiallinen potentiaali - Graafisesti esitettynä: - Kuvataan Gibbsin vapaaenergian pitoisuusriippuvuus - Käyrälle piirretty tangetti tietyssä koostumuspisteessä on Gibbsin vapaaenergian ensimmäinen derivaatta pitoisuuden suhteen (ko. pisteessä) = Kemiallinen potentiaali - Jos kahdelle eri koostumuspisteelle voidaan piirtää yhteinen tangetti, on näiden koostumusten omaavilla systeemeillä sama kemiallinen potentiaali - ts. ko. koostumukset ovat tasapainossa keskenään - Yhteinen tangentti voidaan piirtää samaa faasia kuvaavan käyrän kahden eri pisteen kautta (ks. esimerkkikuvaaja) tai kahta eri faasia kuvaavien käyrien pisteiden kautta Kuva: K. Hack - FactSage -koulutusmateriaali. 4
5 Aukoton liukoisuus Tasapainossa keskenään olevien faasien (esim. sula ja kiinteä faasi) vapaaenergiakäyrät kaareutuvat alaspäin Komponenttien aukoton liukoisuus molemmissa faaseissa Aukoton liukoisuus Esiintyy, kun komponentit ovat samankaltaisia 5
6 Eutektinen tasapaino Aukoton liukoisuus sulassa tilassa Liukoisuusaukko kiinteässä tilassa Samalla käyrällä kaksi paikallista minimiä Kaksi käyrää, joilla omat minimit - Kiinteän olomuodon vapaaenergia kuvissa esitettyä muotoa - (a) Kaksi kiinteää faasia, joilla sama kidemuoto (yksi vapaaenergiakäyrä) - (b) Kaksi kiinteää faasia, joilla eri kidemuodot (molemmilla kidemuodoilla oma vapaaenergiakäyrä) Paikallisille minimeille yhteinen tangentti - Tangentti on vapaaenergiakäyrän ensimmäinen derivaatta pitoisuuden suhteen (l. kemiallinen potentiaali) - Pisteet, joiden kautta tangentti piirretään, rajaavat alueen, jossa kahdella ei koostumuksella on sama kemiallinen potentiaali - Leikkauspisteiden väliin jää alue, jossa kaksi eri koostumuksen omaavaa (kiinteää) faasia ovat tasapainossa keskenään = Liukoisuusaukko Eutektinen tasapaino Aukoton liukoisuus sulassa tilassa Liukoisuusaukko kiinteässä tilassa Piirretty lämpötilassa T 5 - Kiinteän olomuodon vapaaenergia kuvissa esitettyä muotoa - (a) Kaksi kiinteää faasia, joilla sama kidemuoto (yksi vapaaenergiakäyrä) - (b) Kaksi kiinteää faasia, joilla eri kidemuodot (molemmilla kidemuodoilla oma vapaaenergiakäyrä) Paikallisille minimeille yhteinen tangentti Eutektinen lämpötila ja koostumus a 1 a 2 - Tangentti on vapaaenergiakäyrän ensimmäinen derivaatta pitoisuuden suhteen (l. kemiallinen potentiaali) - Pisteet, joiden kautta tangentti piirretään, rajaavat alueen, jossa kahdella ei koostumuksella on sama kemiallinen potentiaali - Leikkauspisteiden väliin jää alue, jossa kaksi eri koostumuksen omaavaa (kiinteää) faasia ovat tasapainossa keskenään = Liukoisuusaukko 6
7 Eutektinen tasapaino Eutektisen tasapainon muodostuminen vapaaenergiakäyrien pohjalta Eutektinen tasapaino 7
8 Eutektoidinen tasapaino Eutektista tasapainoa vastaava tilanne, jossa kahden kiinteän ja yhden sulan faasin sijasta on kolme kiinteää faasia - Vasemmalla olevan kuvan esimerkkitapauksessa sekä aineella A että aineella B on kiinteän tilan faasitransformaatio ennen sulamista - Aineella A kiinteästä -faasista kiinteään -faasiin - Aineella B kiinteästä -faasista kiinteään -faasiin - Metallurgin kannalta erityisen kiinnostava eutektoidinen tasapaino liittyy Fe-C-systeemiin Kuvat: Frederick N Rhines: Phase diagrams in metallurgy, McGraw-Hill, Eutektoidinen tasapaino Fe-C-systeemissä esiintyvä eutektoidinen tasapaino - + -alueen ylärajaa kutsutaan A 3 -rajaksi tai -lämpötilaksi - + -alueen alarajaa kutsutaan A 1 -rajaksi tai lämpötilaksi (A2 on varattu kuvaamaan ferriitin Curie-pistettä) - Lämpötila, jonka yläpuolella ferromagnetismi häviää - +Fe 3 C alueen ylärajaa kutsutaan A CM -rajaksi - Hypoeutektoidinen koostumukseltaan eutektoidisen pisteen vasemmalla puolella olevat seokset - Hypereutektoidinen koostumukseltaan eutektoidisen pisteen oikealla puolella olevat seokset - Perliitti eutektoidinen rakenne, jossa ferriitin muodostaman yhtenäisen matriisin sisään on hautautunut erillisiä sementiittilamelleja 8
9 Fe-C-systeemissä esiintyvä eutektoidinen tasapaino - + -alueen ylärajaa kutsutaan A 3 -rajaksi tai -lämpötilaksi - + -alueen alarajaa kutsutaan A 1 -rajaksi tai lämpötilaksi (A2 on varattu kuvaamaan ferriitin Curie-pistettä) - Lämpötila, jonka yläpuolella ferromagnetismi häviää - +Fe 3 C alueen ylärajaa kutsutaan A CM -rajaksi - Hypoeutektoidinen koostumukseltaan eutektoidisen pisteen vasemmalla puolella olevat seokset - Hypereutektoidinen koostumukseltaan eutektoidisen pisteen oikealla puolella olevat seokset - Perliitti eutektoidinen rakenne, jossa ferriitin muodostaman yhtenäisen matriisin sisään on hautautunut erillisiä sementiittilamelleja Kuva: Frederick N Rhines: Phase diagrams in metallurgy, McGraw-Hill, Oulun yliopisto Peritektinen tasapaino Aukoton liukoisuus sulassa tilassa Liukoisuusaukko kiinteässä tilassa Ero eutektiseen tasapainoon Peritektinen lämpötila - Peritektisessä tasapainossa kiinteiden faasien käyrien minimit ovat samalla puolella sulakäyrän minimiä, kun taas eutektisessa tasapainossa kiinteäkäyrien minimit ovat eri puolilla sulakäyrän minimiä 9
10 Peritektinen tasapaino Peritektoidinen tasapaino Peritektista tasapainoa vastaava tilanne, jossa kahden kiinteän ja yhden sulan faasin sijasta on kolme kiinteää faasia - esimerkki Fe 2 O 3 -Al 2 O 3 -systeemistä 10
11 Monotektinen tasapaino Liukoisuusaukko kiinteän tilan lisäksi myös sulassa tilassa Kriittinen lämpötila Monotektinen lämpötila Kuva: Frederick N Rhines: Phase diagrams in metallurgy, McGraw-Hill, Monotektinen tasapaino 11
12 Monotektoidinen lämpötila Monotektista tasapainoa vastaava tilanne, jossa kahden kiinteän ja yhden sulan faasin sijasta on kolme kiinteää faasia - esimerkki Al-Zn-systeemistä Välifaaseja sisältävät systeemit L (s) L (s) L + (s) (s) Kaikki binäärisysteemit koostuvat edellä esitettyjen perustyyppien yhdistelmistä Välifaasit - Vakiokoostumuksellisia (tai lähes vakiokoostumuksellisia) yhdisteitä, joiden - koostumus on puhtaiden komponenttien välissä - kiderakenne poikkeaa puhtaiden komponenttien rakenteista - Voivat muodostua suoraan sulatteesta tai reaktion kautta Muodostuminen suoraan sulatteesta (Congruent) Muodostuminen reaktion kautta (Incongruent) 12
13 Eri faasien vapaaenergiakäyrät systeemille, jossa esiintyy suoraan sulatteesta muodostuva välifaasi Eri faasien vapaaenergiakäyrät systeemille, jossa esiintyy reaktion kautta muodostuva välifaasi 13
14 Välifaaseja sisältävät systeemit Välifaasit voivat olla vakiokoostumuksellisia tai olla stabiileja laajemmalla koostumusalueella Välifaaseja sisältävät systeemit Välifaasit voivat olla vakiokoostumuksellisia tai olla stabiileja laajemmalla koostumusalueella 14
15 Välifaaseja sisältävät systeemit Välifaasit voivat olla vakiokoostumuksellisia tai olla stabiileja laajemmalla koostumusalueella Välifaaseja sisältävät systeemit Monissa korkealämpötilaprosesseissa esiintyy spinelli-rakenteen omaavaa faasia, jolla on usein laaja stabiilisuusalue - Tulenkestävissä vuorausmateriaaleissa - Mg-Al-spinelli - Malmeissa/rikasteissa - Kromiitti, magnetiitti 15
16 Välifaaseja sisältävät systeemit Mittaukset korkeissa lämpötiloissa ovat haastavia - Joistain systeemeistä on esitetty vaihtoehtoisia, keskenään ristiriitaisia, versioita tasapainopiirroksista - esim. Al 2 O 3 -SiO 2 -systeemissä esiintyvä välifaasi - Muodostuuko suoraan sulatteesta vai reaktion kautta? - Stabiilisuusalueen laajuus? Faasiosuuksien määritys vipusäännön avulla Binäärisysteemi A-B, jossa - A kiteytyy -faasina - B kiteytyy -faasina - esiintyy liukoisuusaukko koostumusvälillä c 1 c 2 Tarkastellaan kaksifaasialueelle osuvaa koostumusta c - -faasin osuus (x): - -faasin osuus (1-x): c c1 x c c 2 c 1 x c c c 1 m l n l 16
17 Tehtävä: Fe-Psysteemi Vastaa oheisen Fe-P-systeemiä kuvaavan piirroksen pohjalta seuraaviin kysymyksiin: - Montako välifaasia esiintyy kuvan koostumusalueella? - Muodostuvatko ne reaktion kautta vai suoraan sulatteesta? - Mitkä ovat välifaasien koostumukset? - Mitä faaseja esiintyy systeemissä, joka koostuu sulasta, joska on jäähdytetty 900 C:een, ja jonka kokonaiskoostumus on 90 p-% Fe ja loput P? - Mitkä ovat tässä systeemissä esiintyvien faasien osuudet ja koostumukset? Sulaminen päättyy Sulaminen alkaa Esimerkki 2-faasialueella sulan koostumus seuraa likvidusta Materiaali on täysin sulanut 2-faasialueella 2-faasialueella kiinteän faasin koostumus seuraa solidusta Monikomponenttisysteemin sulamisen tarkastelu faasipiirroksia hyödyntäen: Tarkastellaan binääristä FeO-MgO-systeemiä, jossa on 30 % FeO ja 70 % MgO - Millä lämpötilavälillä sulaminen tapahtuu? - Mitkä ovat faasien osuudet ja koostumukset puuroalueella? Faasien osuudet 2-faasialueella määritetään vipusäännön avulla Sulan osuus = (83-70)/(83-52) = 0,42 (42%) Kiinteä osuus = (70-52)/(83-52) = 0,58 (58%) Monikomponenttisysteemien jähmettymistä voidaan tarkastella vastaavalla tavalla 1. sulapisaran koostumus Viimeisenä sulavan kiinteän faasin koostumus 17
18 Aktiivisuudet ja tasapainopiirrokset Tasapainopiirrokset kuvaavat systeemissä esiintyvien faasien stabiilisuuksia eri olosuhteissa Stabiilisuus on riippuvainen tarkastelun kohteena olevien aineiden reaktiivisuuksista (ts. aktiivisuuksista) Tasapainopiirrosten ja aktiivisuuksien välillä havaitaan tiettyjä riippuvuuksia Aktiivisuudet ja tasapainopiirrokset Tasapainopiirrosten ja aktiivisuuksien välillä havaitaan tiettyjä riippuvuuksia - Voimakkaan negatiivinen poikkeama Raoultin laista Merkki voimakkaista vetovoimista Yhdisteiden muodostuminen todennäköistä Välifaaseja sisältävät systeemit 18
19 Aktiivisuudet ja tasapainopiirrokset Tasapainopiirrosten ja aktiivisuuksien välillä havaitaan tiettyjä riippuvuuksia - Liuoksen käyttäytyminen lähes ideaalista Liuoksen osaslajit toistensa kaltaisia Laajat liukoisuusalueet (mahdollinen aukoton liukoisuus) Aktiivisuudet ja tasapainopiirrokset Tasapainopiirrosten ja aktiivisuuksien välillä havaitaan tiettyjä riippuvuuksia - Koostumusalue, jossa aineen aktiivisuus on yksi Aine esiintyy puhtaana 19
20 Lämpötila Aktiivisuudet ja tasapainopiirrokset Tasapainopiirrosten ja aktiivisuuksien välillä havaitaan tiettyjä riippuvuuksia - Koostumusalue, jossa aineen aktiivisuus on yksi Aine esiintyy puhtaana Tasapainopiirrosten kokeellinen määritys Aiemmin todettiin, että faasipiirrosten määritys kokeellisesti tasapainomenetelmällä on erittäin hidasta, koska tarvitaan suuri määrä kokeita - Jokainen lämpötila ja koostumus erikseen T X Käytännössä kaksifaasialueelle (tai yleisemmin monifaasialueelle) osuvasta kokeesta saadaan muutakin kuin tätä pistettä koskevaa tietoa Näytettä, jonka koostumus on X A, hehkutettiin lämpötilassa T X tasapainoon asti ja jäähdytettiin nopeasti. Havaittiin kaksi faasia: - Kiteinen, jonka koostumus X S - Lasifaasi, jonka koostumus X L (lasifaasi on nopeasti jähmettynyttä sulaa) X S A = 0 % B = 100 % X A X L A = 100 % B = 0 % Pitoisuus Piste (X A,T X ) osuu kaksifaasialueelle (puuroalue), jonka rajat ko. lämpötilassa ovat X S ja X L Ts. mittaus kertoo tietoa A-B-systeemistä myös muissa kuin koeolosuhteissa. 20
21 Lämpötila Lämpötila Tasapainopiirrosten kokeellinen määritys Aiemmin todettiin, että faasipiirrosten määritys kokeellisesti tasapainomenetelmällä on erittäin hidasta, koska tarvitaan suuri määrä kokeita - Jokainen lämpötila ja koostumus erikseen T Y X A A = 0 % X S X L B = 100 % A = 100 % B = 0 % Käytännössä kaksifaasialueelle (tai yleisemmin monifaasialueelle) osuvasta kokeesta saadaan muutakin kuin tätä pistettä koskevaa tietoa Pitoisuus Toista näytettä, jolla on sama koostumus X A, hehkutettiin matalammassa lämpötilassa T Y tasapainoon asti ja jäähdytettiin nopeasti. Havaittiin edelleen 2 faasia: - Kiteinen, jonka koostumus X S - Lasifaasi, jonka koostumus X L Piste (X A,T Y ) osuu edelleen kaksifaasialueelle (puuroalue), jonka rajat ovat nyt X S ja X L Tasapainopiirrosten kokeellinen määritys Aiemmin todettiin, että faasipiirrosten määritys kokeellisesti tasapainomenetelmällä on erittäin hidasta, koska tarvitaan suuri määrä kokeita - Jokainen lämpötila ja koostumus erikseen Käytännössä kaksifaasialueelle (tai yleisemmin monifaasialueelle) osuvasta kokeesta saadaan muutakin kuin tätä pistettä koskevaa tietoa T Z Tarkastelu kolmannessa, matalammassa lämpötilassa T Z Havaittiin edelleen 2 faasia: - Kiteinen, jonka koostumus X S - Lasifaasi, jonka koostumus X L Pitoisuus Saadaan puuroalueen koostumusrajat kolmannessa lämpötilassa. A = 0 % B = 100 % X S X A X L A = 100 % B = 0 % 21
22 Lämpötila Tasapainopiirrosten kokeellinen määritys Aiemmin todettiin, että faasipiirrosten määritys kokeellisesti tasapainomenetelmällä on erittäin hidasta, koska tarvitaan suuri määrä kokeita - Jokainen lämpötila ja koostumus erikseen Käytännössä kaksifaasialueelle (tai yleisemmin monifaasialueelle) osuvasta kokeesta saadaan muutakin kuin tätä pistettä koskevaa tietoa Pitoisuus Yhdistämällä kokeiden tulokset nähdään, miten puuroalueen koostumusrajat muuttuvat lämpötilan funktiona. Voidaan hahmotella solidus- ja likviduskäyrät. Kokeita jatkamalla saadan selville mihin lämpötiloihin asti puuroalue yltää. A = 0 % B = 100 % A = 100 % B = 0 % Tasapainopiirrosten kokeellinen määritys Aiemmin todettiin, että faasipiirrosten määritys kokeellisesti tasapainomenetelmällä on erittäin hidasta, koska tarvitaan suuri määrä kokeita - Jokainen lämpötila ja koostumus erikseen Käytännössä kaksifaasialueelle (tai yleisemmin monifaasialueelle) osuvasta kokeesta saadaan muutakin kuin tätä pistettä koskevaa tietoa Yhdistämällä kokeiden tulokset nähdään, miten puuroalueen koostumusrajat muuttuvat lämpötilan funktiona. Voidaan hahmotella solidus- ja likviduskäyrät. Kokeita jatkamalla saadan selville mihin lämpötiloihin asti puuroalue yltää. 22
23 Yhteenveto Monimutkaisemmatkin binäärisysteemejä kuvaavat tasapainopiirrokset koostuvat tietyistä perustapauksista - Aukoton liukoisuus - Eutektinen ja eutektoidinen tasapaino - Peritektinen ja peritektoidinen tasapaino - Monotektinen ja monotektoidinen tasapaino - Systeemeissä voi esiintyä välifaaseja, jotka voivat muodostua - suoraan sulatteesta - reaktion kautta Kaksifaasialueella keskenään tasapainossa olevien faasien osuudet voidaan määrittää vipusäännön avulla 23
Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta
 Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 4 Tavoite Oppia tulkitsemaan 2-komponenttisysteemien faasipiirroksia 1 Binääriset
Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 4 Tavoite Oppia tulkitsemaan 2-komponenttisysteemien faasipiirroksia 1 Binääriset
Korkealämpötilakemia
 Korkealämpötilakemia Useamman komponentin tasapainopiirrokset To 7.12.2017 klo 8-10 SÄ114 Tavoite Oppia lukemaan ja tulkitsemaan ternäärisiä tasapainopiirroksia 1 Sisältö Ternääriset tasapainopiirrokset
Korkealämpötilakemia Useamman komponentin tasapainopiirrokset To 7.12.2017 klo 8-10 SÄ114 Tavoite Oppia lukemaan ja tulkitsemaan ternäärisiä tasapainopiirroksia 1 Sisältö Ternääriset tasapainopiirrokset
Korkealämpötilakemia
 Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä1-komponenttipiirrokset To 23.11.2017 klo 8-10 SÄ114 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä1-komponenttipiirrokset To 23.11.2017 klo 8-10 SÄ114 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
Tärkeitä tasapainopisteitä
 Tietoa tehtävistä Tasapainopiirrokseen liittyviä käsitteitä Tehtävä 1 rajojen piirtäminen Tehtävä 2 muunnos atomi- ja painoprosenttien välillä Tehtävä 3 faasien koostumus ja määrät Tehtävä 4 eutektinen
Tietoa tehtävistä Tasapainopiirrokseen liittyviä käsitteitä Tehtävä 1 rajojen piirtäminen Tehtävä 2 muunnos atomi- ja painoprosenttien välillä Tehtävä 3 faasien koostumus ja määrät Tehtävä 4 eutektinen
Korkealämpötilakemia
 Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä 1-komponenttipiirrokset Ti 13.11.2018 klo 8-10 AT115A Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä 1-komponenttipiirrokset Ti 13.11.2018 klo 8-10 AT115A Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
Faasipiirrokset, osa 3 Ternääristen ja monikomponenttipiirrosten tulkinta
 Faasipiirrokset, osa 3 Ternääristen ja monikomponenttipiirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 5 Tavoite Oppia tulkitsemaan 3-komponenttisysteemien faasipiirroksia
Faasipiirrokset, osa 3 Ternääristen ja monikomponenttipiirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 5 Tavoite Oppia tulkitsemaan 3-komponenttisysteemien faasipiirroksia
Chem-C2400 Luento 3: Faasidiagrammit Ville Jokinen
 Chem-C2400 Luento 3: Faasidiagrammit 16.1.2019 Ville Jokinen Oppimistavoitteet Faasidiagrammit ja mikrorakenteen muodostuminen Kahden komponentin faasidiagrammit Sidelinja ja vipusääntö Kolmen faasin reaktiot
Chem-C2400 Luento 3: Faasidiagrammit 16.1.2019 Ville Jokinen Oppimistavoitteet Faasidiagrammit ja mikrorakenteen muodostuminen Kahden komponentin faasidiagrammit Sidelinja ja vipusääntö Kolmen faasin reaktiot
Termodynaamisten tasapainotarkastelujen tulokset esitetään usein kuvaajina, joissa:
 Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
Dislokaatiot - pikauusinta
 Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1
 Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1 A B B Piirroksen alue 1: Sularajan yläpuolella on seos aina täysin sula => yksifaasialue (L). Alueet 2 ja 5: Nämä ovat
Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1 A B B Piirroksen alue 1: Sularajan yläpuolella on seos aina täysin sula => yksifaasialue (L). Alueet 2 ja 5: Nämä ovat
Sulamisen ja jähmettymisen tarkastelu faasipiirroksia hyödyntäen
 Sulamisen ja jähmettymisen tarkastelu faasipiirroksia hyödyntäen Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 6 Tavoite Oppia muutamien esimerkkien avulla tarkastelemaan monikomponenttisysteemien
Sulamisen ja jähmettymisen tarkastelu faasipiirroksia hyödyntäen Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 6 Tavoite Oppia muutamien esimerkkien avulla tarkastelemaan monikomponenttisysteemien
Faasipiirrokset, osa 1: Laatiminen sekä 1-komponenttipiirrosten tulkinta
 Faasipiirrokset, osa 1: Laatiminen sekä 1-komponenttipiirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 3 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen
Faasipiirrokset, osa 1: Laatiminen sekä 1-komponenttipiirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 3 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen
Korkealämpötilakemia
 1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
Standarditilat. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 2 - Luento 2. Tutustua standarditiloihin
 Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Kon Teräkset Viikkoharjoitus 1. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka
 Kon-67.3110 Teräkset Viikkoharjoitus 1. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka Luennolta: Perustieto eri ilmiöistä Kirjoista: Syventävä tieto eri ilmiöistä
Kon-67.3110 Teräkset Viikkoharjoitus 1. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka Luennolta: Perustieto eri ilmiöistä Kirjoista: Syventävä tieto eri ilmiöistä
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Korkealämpötilakemia
 Korkealämpötilakemia Metallurgiset liuosmallit Yleistä To 15.11.218 klo 8-1 PR126A Tavoite Tutustua ideaali- ja reaaliliuosten käsitteisiin Tutustua liuosmalleihin yleisesti - Jaottelu - Hyvän liuosmallin
Korkealämpötilakemia Metallurgiset liuosmallit Yleistä To 15.11.218 klo 8-1 PR126A Tavoite Tutustua ideaali- ja reaaliliuosten käsitteisiin Tutustua liuosmalleihin yleisesti - Jaottelu - Hyvän liuosmallin
Kellogg-diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 1
 Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy 6 Teema - Luento Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy 6 Teema - Luento Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
Ellinghamin diagrammit
 Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
Rauta-hiili tasapainopiirros
 Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
Korkealämpötilakemia
 Korkealämpötilakemia Ellingham-diagrammit To 9.11.2017 klo 8-10 SÄ114 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Sisältö Mikä on Ellinghamin diagrammi?
Korkealämpötilakemia Ellingham-diagrammit To 9.11.2017 klo 8-10 SÄ114 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Sisältö Mikä on Ellinghamin diagrammi?
Kellogg-diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2012 Teema 1 - Luento 1
 Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy Teema - Luento Eetu-Pekka Heikkinen, Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Eetu-Pekka
Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy Teema - Luento Eetu-Pekka Heikkinen, Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Eetu-Pekka
KJR-C2004 materiaalitekniikka. Harjoituskierros 3
 KJR-C2004 materiaalitekniikka Harjoituskierros 3 Tänään ohjelmassa 1. Tasapainopiirros 1. Tulkinta 2. Laskut 2. Faasimuutokset 3. Ryhmätyöt 1. Esitehtävän yhteenveto (palautetaan harkassa) 2. Ryhmätehtävä
KJR-C2004 materiaalitekniikka Harjoituskierros 3 Tänään ohjelmassa 1. Tasapainopiirros 1. Tulkinta 2. Laskut 2. Faasimuutokset 3. Ryhmätyöt 1. Esitehtävän yhteenveto (palautetaan harkassa) 2. Ryhmätehtävä
Luento 1 Rauta-hiili tasapainopiirros Austeniitin hajaantuminen perliittimekanismilla
 Luento 1 Rauta-hiili tasapainopiirros Austeniitin hajaantuminen perliittimekanismilla Vapaa energia ja tasapainopiirros Allotropia - Metalli omaksuu eri lämpötiloissa eri kidemuotoja. - Faasien vapaat
Luento 1 Rauta-hiili tasapainopiirros Austeniitin hajaantuminen perliittimekanismilla Vapaa energia ja tasapainopiirros Allotropia - Metalli omaksuu eri lämpötiloissa eri kidemuotoja. - Faasien vapaat
CHEM-C2400 MATERIAALIT SIDOKSESTA RAKENTEESEEN (5 op) Laskuharjoitus 1
 CHEM-C2400 MATERIAALIT SIDOKSESTA RAKENTEESEEN (5 op) Laskuharjoitus 1 Kristallografiaa 1. Suunnan millerin indeksit (ja siten siis suunta) lasketaan vähentämällä loppupisteen koordinaateista alkupisteen
CHEM-C2400 MATERIAALIT SIDOKSESTA RAKENTEESEEN (5 op) Laskuharjoitus 1 Kristallografiaa 1. Suunnan millerin indeksit (ja siten siis suunta) lasketaan vähentämällä loppupisteen koordinaateista alkupisteen
Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä.
 FAASIDIAGRAMMIT Määritelmiä Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä. Esimerkkejä: (a) suolaliuos (P=1),
FAASIDIAGRAMMIT Määritelmiä Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä. Esimerkkejä: (a) suolaliuos (P=1),
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin
 Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 27.10.2016 klo 14-16 Luennon tavoite Tutustua eri tapoihin määrittää termodyn. tasapaino laskennallisesti Tutustua termodynaamisten
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 27.10.2016 klo 14-16 Luennon tavoite Tutustua eri tapoihin määrittää termodyn. tasapaino laskennallisesti Tutustua termodynaamisten
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin
 Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 7.9.2017 klo 8-10 Prosessimetallurgian tutkimusyksikkö Eetu-Pekka Heikkinen, 2017 Luennon tavoite Tutustua eri tapoihin määrittää
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 7.9.2017 klo 8-10 Prosessimetallurgian tutkimusyksikkö Eetu-Pekka Heikkinen, 2017 Luennon tavoite Tutustua eri tapoihin määrittää
Ratkaisu. Tarkastellaan aluksi Fe 3+ - ja Fe 2+ -ionien välistä tasapainoa: Nernstin yhtälö tälle reaktiolle on:
 Esimerkki Pourbaix-piirroksen laatimisesta Laadi Pourbaix-piirros, jossa on esitetty metallisen ja ionisen raudan sekä raudan oksidien stabiilisuusalueet vesiliuoksessa 5 C:een lämpötilassa. Ratkaisu Tarkastellaan
Esimerkki Pourbaix-piirroksen laatimisesta Laadi Pourbaix-piirros, jossa on esitetty metallisen ja ionisen raudan sekä raudan oksidien stabiilisuusalueet vesiliuoksessa 5 C:een lämpötilassa. Ratkaisu Tarkastellaan
Binäärinen tasapaino, ei täyttä liukoisuutta
 Tasapainopiirrokset Binäärinen tasapaino, ei täyttä liukoisuutta Binäärinen tasapaino Kiinteässä tilassa koostumuksesta riippuen kahta faasia Eutektisella koostumuksella ei puuroaluetta Faasiosuudet muuttuvat
Tasapainopiirrokset Binäärinen tasapaino, ei täyttä liukoisuutta Binäärinen tasapaino Kiinteässä tilassa koostumuksesta riippuen kahta faasia Eutektisella koostumuksella ei puuroaluetta Faasiosuudet muuttuvat
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
Aineen olomuodot ja olomuodon muutokset
 Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
(l) B. A(l) + B(l) (s) B. B(s)
 FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Metallit 2005. juha.nykanen@tut.fi
 Metallit 2005 juha.nykanen@tut.fi Aikataulu Pe 2.9.2005 Pe 9.9.2005 Pe 16.9.2005 Pe 23.9.2005 Pe 10.9.2005 Pe 8.10.2005 Valurauta Valurauta ja teräs Teräs Teräs ja alumiini Magnesium ja titaani Kupari,
Metallit 2005 juha.nykanen@tut.fi Aikataulu Pe 2.9.2005 Pe 9.9.2005 Pe 16.9.2005 Pe 23.9.2005 Pe 10.9.2005 Pe 8.10.2005 Valurauta Valurauta ja teräs Teräs Teräs ja alumiini Magnesium ja titaani Kupari,
Metallurgian perusteita
 Metallurgian perusteita Seija Meskanen, Teknillinen korkeakoulu Pentti Toivonen, Teknillinen korkeakoulu Korkean laadun saavuttaminen edellyttää sekä rauta että teräsvalujen tuotannossa tiukkaa prosessikuria
Metallurgian perusteita Seija Meskanen, Teknillinen korkeakoulu Pentti Toivonen, Teknillinen korkeakoulu Korkean laadun saavuttaminen edellyttää sekä rauta että teräsvalujen tuotannossa tiukkaa prosessikuria
Faasimuutokset ja lämpökäsittelyt
 Faasimuutokset ja lämpökäsittelyt Yksinkertaiset lämpökäsittelyt Pehmeäksihehkutus Nostetaan lämpötilaa Diffuusio voi tapahtua Dislokaatiot palautuvat Materiaali pehmenee Rekristallisaatio Ei ylitetä faasirajoja
Faasimuutokset ja lämpökäsittelyt Yksinkertaiset lämpökäsittelyt Pehmeäksihehkutus Nostetaan lämpötilaa Diffuusio voi tapahtua Dislokaatiot palautuvat Materiaali pehmenee Rekristallisaatio Ei ylitetä faasirajoja
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
ja piirrä sitä vastaavat kaksi käyrää ja tarkista ratkaisusi kuvastasi.
 Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
Sähkökemialliset tarkastelut HSC:llä
 Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA
 ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa
 Rikasta pohjoista 10.4.2019 Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa Lapin alueen yritysten uudet teräsmateriaalit Nimi Numero CK45 / C45E (1.1191) 19MnVS6 / 20MnV6 (1.1301) 38MnV6 /
Rikasta pohjoista 10.4.2019 Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa Lapin alueen yritysten uudet teräsmateriaalit Nimi Numero CK45 / C45E (1.1191) 19MnVS6 / 20MnV6 (1.1301) 38MnV6 /
Alieutektoidisen teräksen normalisointi
 Alieutektoidisen teräksen normalisointi Hiili (C) ja rauta (Fe) Hiili ja rauta voivat muodostaa yhdessä monia erilaisia mikrorakenteita, olipa kyseessä sitten teräs (hiiltä maksimissaan 2.1p.% C, eli hiiltä
Alieutektoidisen teräksen normalisointi Hiili (C) ja rauta (Fe) Hiili ja rauta voivat muodostaa yhdessä monia erilaisia mikrorakenteita, olipa kyseessä sitten teräs (hiiltä maksimissaan 2.1p.% C, eli hiiltä
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Puhtaat aineet ja seokset
 Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
Kon Teräkset Viikkoharjoitus 2. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikan laitos
 Kon-67.3110 Teräkset Viikkoharjoitus 2. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikan laitos Luennolta: Perustieto eri ilmiöistä Kirjoista: Syventävä tieto eri
Kon-67.3110 Teräkset Viikkoharjoitus 2. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikan laitos Luennolta: Perustieto eri ilmiöistä Kirjoista: Syventävä tieto eri
Oikeat vastaukset: Tehtävän tarkkuus on kolme numeroa. Sulamiseen tarvittavat lämmöt sekä teräksen suurin mahdollinen luovutettu lämpö:
 A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
3.3 Paraabeli toisen asteen polynomifunktion kuvaajana. Toisen asteen epäyhtälö
 3.3 Paraabeli toisen asteen polynomifunktion kuvaajana. Toisen asteen epäyhtälö Yhtälön (tai funktion) y = a + b + c, missä a 0, kuvaaja ei ole suora, mutta ei ole yhtälökään ensimmäistä astetta. Funktioiden
3.3 Paraabeli toisen asteen polynomifunktion kuvaajana. Toisen asteen epäyhtälö Yhtälön (tai funktion) y = a + b + c, missä a 0, kuvaaja ei ole suora, mutta ei ole yhtälökään ensimmäistä astetta. Funktioiden
HSC-ohje laskuharjoituksen 1 tehtävälle 2
 HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
Lisätehtäviä. Rationaalifunktio. x 2. a b ab. 6u x x x. kx x
 MAA6 Lisätehtäviä Laske lisätehtäviä omaan tahtiisi kurssin aikan Palauta laskemasi tehtävät viimeistään kurssikokeeseen. Tehtävät lasketaan ilman laskint Rationaalifunktio Tehtäviä Hyvitys kurssiarvosanassa
MAA6 Lisätehtäviä Laske lisätehtäviä omaan tahtiisi kurssin aikan Palauta laskemasi tehtävät viimeistään kurssikokeeseen. Tehtävät lasketaan ilman laskint Rationaalifunktio Tehtäviä Hyvitys kurssiarvosanassa
Rak Betonitekniikka 2 Harjoitus Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys
 Rak-82.3131 Betonitekniikka 2 Harjoitus 2 23.9.2010 Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys Portlandsementti Portlandsementin kemiallinen koostumus KOMPONENTTI LYHENNE PITOISUUS
Rak-82.3131 Betonitekniikka 2 Harjoitus 2 23.9.2010 Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys Portlandsementti Portlandsementin kemiallinen koostumus KOMPONENTTI LYHENNE PITOISUUS
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
Tina-vismutti juotosmetallin binäärinen seos Tekijä: Lassi Vuorela Yhteystiedot:
 Tina-vismutti juotosmetallin binäärinen seos Tekijä: Lassi Vuorela Yhteystiedot: lassi.vuorela@aalto.fi Juottaminen Juottamisessa on tarkoitus liittää kaksi materiaalia tai osaa niin, että sähkövirta kykenee
Tina-vismutti juotosmetallin binäärinen seos Tekijä: Lassi Vuorela Yhteystiedot: lassi.vuorela@aalto.fi Juottaminen Juottamisessa on tarkoitus liittää kaksi materiaalia tai osaa niin, että sähkövirta kykenee
Metallien plastinen deformaatio on dislokaatioiden liikettä
 Metallien plastinen deformaatio on dislokaatioiden liikettä Särmädislokaatio 2 Ruuvidislokaatio 3 Dislokaation jännitystila Dislokaatioiden vuorovaikutus Jännitystila aiheuttaa dislokaatioiden vuorovaikutusta
Metallien plastinen deformaatio on dislokaatioiden liikettä Särmädislokaatio 2 Ruuvidislokaatio 3 Dislokaation jännitystila Dislokaatioiden vuorovaikutus Jännitystila aiheuttaa dislokaatioiden vuorovaikutusta
Matematiikan tukikurssi
 Matematiikan tukikurssi Kurssikerta 8 1 Funktion kuperuussuunnat Derivoituva funktio f (x) on pisteessä x aidosti konveksi, jos sen toinen derivaatta on positiivinen f (x) > 0. Vastaavasti f (x) on aidosti
Matematiikan tukikurssi Kurssikerta 8 1 Funktion kuperuussuunnat Derivoituva funktio f (x) on pisteessä x aidosti konveksi, jos sen toinen derivaatta on positiivinen f (x) > 0. Vastaavasti f (x) on aidosti
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
b) Määritä/Laske (ei tarvitse tehdä määritelmän kautta). (2p)
 Matematiikan TESTI, Maa7 Trigonometriset funktiot RATKAISUT Sievin lukio II jakso/017 VASTAA JOKAISEEN TEHTÄVÄÄN! MAOL/LIITE/taulukot.com JA LASKIN ON SALLITTU ELLEI TOISIN MAINITTU! TARKISTA TEHTÄVÄT
Matematiikan TESTI, Maa7 Trigonometriset funktiot RATKAISUT Sievin lukio II jakso/017 VASTAA JOKAISEEN TEHTÄVÄÄN! MAOL/LIITE/taulukot.com JA LASKIN ON SALLITTU ELLEI TOISIN MAINITTU! TARKISTA TEHTÄVÄT
Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty Vastaus: Määrittelyehto on x 1 ja nollakohta x = 1.
 Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 4..6 Kokoavia tehtäviä ILMAN TEKNISIÄ APUVÄLINEITÄ. a) Funktion f( ) = määrittelyehto on +, eli. + Ratkaistaan funktion nollakohdat. f(
Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 4..6 Kokoavia tehtäviä ILMAN TEKNISIÄ APUVÄLINEITÄ. a) Funktion f( ) = määrittelyehto on +, eli. + Ratkaistaan funktion nollakohdat. f(
Kertaus. x x x. K1. a) b) x 5 x 6 = x 5 6 = x 1 = 1 x, x 0. K2. a) a a a a, a > 0
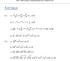 Juuri 8 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 8.9.07 Kertaus K. a) 6 4 64 0, 0 0 0 0 b) 5 6 = 5 6 = =, 0 c) d) K. a) b) c) d) 4 4 4 7 4 ( ) 7 7 7 7 87 56 7 7 7 6 6 a a a, a > 0 6 6 a
Juuri 8 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 8.9.07 Kertaus K. a) 6 4 64 0, 0 0 0 0 b) 5 6 = 5 6 = =, 0 c) d) K. a) b) c) d) 4 4 4 7 4 ( ) 7 7 7 7 87 56 7 7 7 6 6 a a a, a > 0 6 6 a
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Palautus yhtenä tiedostona PDF-muodossa viimeistään torstaina
 PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
MT Erikoismateriaalit tuotantoprosesseissa (3 op)
 MT-0.6101 Erikoismateriaalit tuotantoprosesseissa (3 op) 6. Luento - Ke 11.11.2015 Reaktiotermodynamiikan käyttö tulenkestävien valinnassa Marko Kekkonen MT-0.6101 Erikoismateriaalit tuotantoprosesseissa
MT-0.6101 Erikoismateriaalit tuotantoprosesseissa (3 op) 6. Luento - Ke 11.11.2015 Reaktiotermodynamiikan käyttö tulenkestävien valinnassa Marko Kekkonen MT-0.6101 Erikoismateriaalit tuotantoprosesseissa
LUKU 16 KEMIALLINEN JA FAASITASAPAINO
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 LUKU 16 KEMIALLINEN JA FAASITASAPAINO Copyright The McGraw-Hill Companies, Inc. Permission required
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 LUKU 16 KEMIALLINEN JA FAASITASAPAINO Copyright The McGraw-Hill Companies, Inc. Permission required
1. a. Ratkaise yhtälö 8 x 5 4 x + 2 x+2 = 0 b. Määrää joku toisen asteen epäyhtälö, jonka ratkaisu on 2 x 1.
 ABIKertaus.. a. Ratkaise yhtälö 8 5 4 + + 0 b. Määrää joku toisen asteen epäyhtälö, jonka ratkaisu on. 4. Jaa polynomi 8 0 5 ensimmäisen asteen tekijöihin ja ratkaise tämän avulla 4 epäyhtälö 8 0 5 0.
ABIKertaus.. a. Ratkaise yhtälö 8 5 4 + + 0 b. Määrää joku toisen asteen epäyhtälö, jonka ratkaisu on. 4. Jaa polynomi 8 0 5 ensimmäisen asteen tekijöihin ja ratkaise tämän avulla 4 epäyhtälö 8 0 5 0.
Tina-vismutti seos juotosmetallina
 Tina-vismutti seos juotosmetallina Miikka Martikainen Juottaminen Juottaminen on metallien liitosmenetelmä, jossa kappaleet liitetään toisiinsa sulattamalla niiden väliin juotosainetta, eli juotetta. Juotteena
Tina-vismutti seos juotosmetallina Miikka Martikainen Juottaminen Juottaminen on metallien liitosmenetelmä, jossa kappaleet liitetään toisiinsa sulattamalla niiden väliin juotosainetta, eli juotetta. Juotteena
MS-A0204 Differentiaali- ja integraalilaskenta 2 (ELEC2) Luento 6: Ääriarvojen luokittelu. Lagrangen kertojat.
 MS-A0204 Differentiaali- ja integraalilaskenta 2 (ELEC2) Luento 6: Ääriarvojen luokittelu. Lagrangen kertojat. Antti Rasila Matematiikan ja systeemianalyysin laitos Aalto-yliopisto Kevät 2016 Antti Rasila
MS-A0204 Differentiaali- ja integraalilaskenta 2 (ELEC2) Luento 6: Ääriarvojen luokittelu. Lagrangen kertojat. Antti Rasila Matematiikan ja systeemianalyysin laitos Aalto-yliopisto Kevät 2016 Antti Rasila
4. Kertausosa. 1. a) 12
 . Kertausosa. a kun, : b kun, tai 8 . Paraabeli y a bc c aukeaa ylöspäin, jos a alaspäin, jos a a Funktion g kuvaaja on paraabeli, jolle a. Se aukeaa ylöspäin. b Funktion g kuvaaja on paraabeli, jolle
. Kertausosa. a kun, : b kun, tai 8 . Paraabeli y a bc c aukeaa ylöspäin, jos a alaspäin, jos a a Funktion g kuvaaja on paraabeli, jolle a. Se aukeaa ylöspäin. b Funktion g kuvaaja on paraabeli, jolle
Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty
 Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 14..016 Kertaus K1. a) b) x 18 ( x 9) ( x ) ( x+ ) lim = lim = lim x+ x+ ( x + ) x x x = lim (x 6) = ( ) 6 = 1 x x + 6 ( ) + 6 0 lim = =
Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 14..016 Kertaus K1. a) b) x 18 ( x 9) ( x ) ( x+ ) lim = lim = lim x+ x+ ( x + ) x x x = lim (x 6) = ( ) 6 = 1 x x + 6 ( ) + 6 0 lim = =
Luento 2. Kon Teräkset DI Timo Kiesi Koneenrakennuksen materiaalitekniikka Aalto-yliopisto
 Luento 2 Kon-67.3110 Teräkset DI Timo Kiesi Koneenrakennuksen materiaalitekniikka Aalto-yliopisto Rauta-hiili -tasapainopiirros Honeycombe & Bhadeshia s. 30-41. Uudistettu Miekk oj s. 268-278. Rauta (Fe)
Luento 2 Kon-67.3110 Teräkset DI Timo Kiesi Koneenrakennuksen materiaalitekniikka Aalto-yliopisto Rauta-hiili -tasapainopiirros Honeycombe & Bhadeshia s. 30-41. Uudistettu Miekk oj s. 268-278. Rauta (Fe)
Valurauta ja valuteräs
 Valurauta ja valuteräs Seija Meskanen Teknillinen korkeakoulu Tuula Höök Tampereen teknillinen yliopisto Valurauta ja valuteräs ovat raudan (Fe), hiilen (C), piin (Si) ja mangaanin (Mn) sekä muiden seosaineiden
Valurauta ja valuteräs Seija Meskanen Teknillinen korkeakoulu Tuula Höök Tampereen teknillinen yliopisto Valurauta ja valuteräs ovat raudan (Fe), hiilen (C), piin (Si) ja mangaanin (Mn) sekä muiden seosaineiden
Mak Materiaalitieteen perusteet
 Mak-45.310 tentit Mak-45.310 Materiaalitieteen perusteet 1. välikoe 24.10.2000 1. Vertaile ionisidokseen ja metalliseen sidokseen perustuvien materiaalien a) sähkönjohtavuutta b) lämmönjohtavuutta c) diffuusiota
Mak-45.310 tentit Mak-45.310 Materiaalitieteen perusteet 1. välikoe 24.10.2000 1. Vertaile ionisidokseen ja metalliseen sidokseen perustuvien materiaalien a) sähkönjohtavuutta b) lämmönjohtavuutta c) diffuusiota
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
Matematiikan taito 9, RATKAISUT. , jolloin. . Vast. ]0,2] arvot.
![Matematiikan taito 9, RATKAISUT. , jolloin. . Vast. ]0,2] arvot. Matematiikan taito 9, RATKAISUT. , jolloin. . Vast. ]0,2] arvot.](/thumbs/61/46046056.jpg) 7 Sovelluksia 90 a) Koska sin saa kaikki välillä [,] olevat arvot, niin funktion f ( ) = sin pienin arvo on = ja suurin arvo on ( ) = b) Koska sin saa kaikki välillä [0,] olevat arvot, niin funktion f
7 Sovelluksia 90 a) Koska sin saa kaikki välillä [,] olevat arvot, niin funktion f ( ) = sin pienin arvo on = ja suurin arvo on ( ) = b) Koska sin saa kaikki välillä [0,] olevat arvot, niin funktion f
781611S KIINTEÄN OLOMUODON KEMIA (4 op)
 781611S KIINTEÄN OLOMUODON KEMIA (4 op) ma ti ke to pe 12.9. klo 12-14 19.9. klo 12-14 26.9. klo 12-14 3.10. klo 12-14 KE351 10.10. klo 12-14 17.10. klo 12-14 24.10. klo 12-14 31.10. klo 12-14 KE351 14.9.
781611S KIINTEÄN OLOMUODON KEMIA (4 op) ma ti ke to pe 12.9. klo 12-14 19.9. klo 12-14 26.9. klo 12-14 3.10. klo 12-14 KE351 10.10. klo 12-14 17.10. klo 12-14 24.10. klo 12-14 31.10. klo 12-14 KE351 14.9.
Esimerkiksi ammoniakin valmistus typestä ja vedystä on tyypillinen teollinen tasapainoreaktio.
 REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
Matematiikan tukikurssi
 Matematiikan tukikurssi Kurssikerta 10 1 Funktion monotonisuus Derivoituva funktio f on aidosti kasvava, jos sen derivaatta on positiivinen eli jos f (x) > 0. Funktio on aidosti vähenevä jos sen derivaatta
Matematiikan tukikurssi Kurssikerta 10 1 Funktion monotonisuus Derivoituva funktio f on aidosti kasvava, jos sen derivaatta on positiivinen eli jos f (x) > 0. Funktio on aidosti vähenevä jos sen derivaatta
Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen
 KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
17. Tulenkestävät aineet
 17. Tulenkestävät aineet Raimo Keskinen Peka Niemi - Tampereen ammattiopisto Alkuaineiden oksidit voidaan jakaa kemiallisen käyttäytymisensä perusteella luonteeltaan happamiin, emäksisiin ja neutraaleihin
17. Tulenkestävät aineet Raimo Keskinen Peka Niemi - Tampereen ammattiopisto Alkuaineiden oksidit voidaan jakaa kemiallisen käyttäytymisensä perusteella luonteeltaan happamiin, emäksisiin ja neutraaleihin
Korkealämpötilakemia
 ..7 Korkealämötilakemia Teema Luento Kellogg-diagrammit To..7 klo 8- SÄ4 Tavoite Oia tulkitsemaan ja laatimaan ns. Kelloggdiagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
..7 Korkealämötilakemia Teema Luento Kellogg-diagrammit To..7 klo 8- SÄ4 Tavoite Oia tulkitsemaan ja laatimaan ns. Kelloggdiagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
MAA2.3 Koontitehtävät 2/2, ratkaisut
 MAA.3 Koontitehtävät /, ratkaisut. (a) 3x 5x 4 = 0 x = ( 5) ± ( 5) 4 3 ( 4) 6 (b) (x 4) = (x 4)(x + 4) (x 4)(x 4) = (x 4)(x + 4) x 8x + 6 = x 6 x 6 8x = 3 : 8 x = 4 = 5 ± 73 6 (c) 4 x + x + = 0 4 x + 4x
MAA.3 Koontitehtävät /, ratkaisut. (a) 3x 5x 4 = 0 x = ( 5) ± ( 5) 4 3 ( 4) 6 (b) (x 4) = (x 4)(x + 4) (x 4)(x 4) = (x 4)(x + 4) x 8x + 6 = x 6 x 6 8x = 3 : 8 x = 4 = 5 ± 73 6 (c) 4 x + x + = 0 4 x + 4x
l 1 2l + 1, c) 100 l=0
 MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
Termiikin ennustaminen radioluotauksista. Heikki Pohjola ja Kristian Roine
 Termiikin ennustaminen radioluotauksista Heikki Pohjola ja Kristian Roine Maanpintahavainnot havaintokojusta: lämpötila, kostea lämpötila (kosteus), vrk minimi ja maksimi. Lisäksi tuulen nopeus ja suunta,
Termiikin ennustaminen radioluotauksista Heikki Pohjola ja Kristian Roine Maanpintahavainnot havaintokojusta: lämpötila, kostea lämpötila (kosteus), vrk minimi ja maksimi. Lisäksi tuulen nopeus ja suunta,
1. a) b) Nollakohdat: 20 = c) a b a b = + ( a b)( a + b) Derivaatan kuvaajan numero. 1 f x x x g x x x x. 3. a)
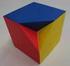 Pitkä matematiikka YO-koe 9..04. a) b) 7( x ) + = x ( x ) x(5 8 x) > 0 7x + = x x + 8x + 5x > 0 7x = 0 Nollakohdat: 0 8x + 5x = 0 x = 7 x(8x 5) = 0 5 5 x = 0 tai x = Vastaus: 0 < x < 8 8 c) a+ b) a b)
Pitkä matematiikka YO-koe 9..04. a) b) 7( x ) + = x ( x ) x(5 8 x) > 0 7x + = x x + 8x + 5x > 0 7x = 0 Nollakohdat: 0 8x + 5x = 0 x = 7 x(8x 5) = 0 5 5 x = 0 tai x = Vastaus: 0 < x < 8 8 c) a+ b) a b)
Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille
 Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille 25.1.2018 Kemian tehtävät Kirjoita nimesi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin
Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille 25.1.2018 Kemian tehtävät Kirjoita nimesi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin
Mat Dynaaminen optimointi, mallivastaukset, kierros Vaimennetun heilurin tilanyhtälöt on esitetty luennolla: θ = g sin θ r θ
 Mat-48 Dynaaminen optimointi, mallivastaukset, kierros Vaimennetun heilurin tilanyhtälöt on esitetty luennolla: θ = g sin θ r θ L ẋ = x ẋ = g L sin x rx Epälineaarisen systeemin tasapainotiloja voidaan
Mat-48 Dynaaminen optimointi, mallivastaukset, kierros Vaimennetun heilurin tilanyhtälöt on esitetty luennolla: θ = g sin θ r θ L ẋ = x ẋ = g L sin x rx Epälineaarisen systeemin tasapainotiloja voidaan
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
PAINOPISTE JA MASSAKESKIPISTE
 PAINOPISTE JA MASSAKESKIPISTE Kappaleen painopiste on piste, jonka kautta kappaleeseen kohdistuvan painovoiman vaikutussuora aina kulkee, olipa kappale missä asennossa tahansa. Jos ajatellaan kappaleen
PAINOPISTE JA MASSAKESKIPISTE Kappaleen painopiste on piste, jonka kautta kappaleeseen kohdistuvan painovoiman vaikutussuora aina kulkee, olipa kappale missä asennossa tahansa. Jos ajatellaan kappaleen
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
2 Pistejoukko koordinaatistossa
 Pistejoukko koordinaatistossa Ennakkotehtävät 1. a) Esimerkiksi: b) Pisteet sijaitsevat pystysuoralla suoralla, joka leikkaa x-akselin kohdassa x =. c) Yhtälö on x =. d) Sijoitetaan joitain ehdon toteuttavia
Pistejoukko koordinaatistossa Ennakkotehtävät 1. a) Esimerkiksi: b) Pisteet sijaitsevat pystysuoralla suoralla, joka leikkaa x-akselin kohdassa x =. c) Yhtälö on x =. d) Sijoitetaan joitain ehdon toteuttavia
Preliminäärikoe Tehtävät A-osio Pitkä matematiikka kevät 2016 Sivu 1 / 4
 Preliminäärikoe Tehtävät A-osio Pitkä matematiikka kevät 06 Sivu / 4 Laske yhteensä enintään 0 tehtävää. Kaikki tehtävät arvostellaan asteikolla 0-6 pistettä. Osiossa A EI SAA käyttää laskinta. Osiossa
Preliminäärikoe Tehtävät A-osio Pitkä matematiikka kevät 06 Sivu / 4 Laske yhteensä enintään 0 tehtävää. Kaikki tehtävät arvostellaan asteikolla 0-6 pistettä. Osiossa A EI SAA käyttää laskinta. Osiossa
