|
|
|
- Riitta Kouki
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1
2
3
4
5
6
7
8
9
10
11 mak37135 MAK Materiaalien ja prosessien termodynaamis-kineettiset perusteet Tentti Vastaa 7:ään kysymykseen 1. Sinun olisi arvioitava hiilettyykö teräs, jonka hiilipitoisuus on 0.35% vai tapahtuuko hiilenkato ja miten nopeasti teräksen hiilipitoisuus muuttuu teräskappaleen pintakerroksissa. Lämpökäsittelyuunin suojakaasuna on N2-CH4-H2-seos ja lämpötila on tunnettu. Mitä ilmiöitä sinun tulisi ottaa huomioon ja mitä asioita selvittää saadaksesi käsityksen siitä mitä tulee tapahtumaan ja miten nopeasti ilmiöt etenevät? 2. Oheisessa piirroksessa (piirros puuttuu)on esitetty binäärisen korvausliuoksen A-B integraalinen moolinen Gibbsin sekoitusenergia (Gmix, DGmixm etc.) 1000 C:ssa. Tsekkaa onko seos (liuos) ideaalinen vaiko ei! 3. Mitä tapahtuu a) oheisen kuvan (niinpä niin...) A pisteissä 1 ja 2 kun lämpötila laskee ja b) mitkä faasit ovat stabiilit kuvan B pisteissä 1,2 ja 3 ja c) arvioi karkeasti miä on faasien ainemääräsuhde kuvan B pisteessä 3? 4. Oheisessa kuvassa on esitetty hapen osapaine (logaritmi) kun Me-Au sulaseos on tasapainossa metallioksidin Me2O kanssa. Mikä on metallin Me aktiivisuus sulaseoksessa 1100 C:ssa, kun kullan mooliosuus on 0.4 ja 0.7? Kyseisen oksidin Gibbsin muodostumisenergia ko. lämpötilassa on annettu ohessa. Vihje: muodosta kyseisen oksidin muodostumisreaktio, ja ratkaise sen tasapainoehdosta Me:n aktiivisuus Tieto: DfH (Me2O) DfG (Me2O) kj/mol kj/mol Mikä on edellä mainitun oksidin muodostumisentropia 1100 C:ssa? 6. Missä lämpötilassa magnesiumkarbonaatti hajoaa spontaanisti, eli sen hajoamispaine saavuttaa yhden ilmakehän paineen (= 1 bar). Seuraava tieto on käytettävissä: Hajoamisreaktio: MgO + CO2(g) = MgCO3(s); Tieto: DfH (J) DfS (J/mol-1*K-1) MgO CO file:///c /Documents%20and%20Settings/Jani%20Jansson/Desktop/Tentit/mak37135.htm (1 of 5) :15:51
12 mak37135 MgCO Sinkin pitoisuus Bi-pohjaisessa elektroniikan komponenttien liittämiseen tarkoitetussa juotteessa on 3.6 mol% ja sinkin aktiivisuuskerroin (Raoultin aktiivisuukerroin siis mooliosuuteen suhteutettu) on Hapettuuko sinkki juotteesta sinkkimonoksidiksi, kun suojaukseen käytetään kaasuseosta: 80%N2(g) + 20%H2(g) + 10 ppm (= 0.001%) H2O(g) Seuraava tieto on käytettävissä: DfG (T) = ZnO *T J/mol Vihje: Kirjoita hapettumisreaktio ja laske sen tasapainoehdosta H2O(g) *T J/mol hapettuuko sinkki (onkozno stabiili eli aktiivisuus 1) 8. Kupari-rikki seos syttyy helposti itsestään, jos aineet ovat kovin hienojakoisia. Arvioi adiabaattisen reaktiolämpötilan kautta, minkä luokan lämpötila reaktiossa syntyy ja pyrkiikö muodostuva kuparisulfidi sulamaan! Seuraava tieto on käytettävissä: DfH (298); kj/mol Cp(T) J/(mol-1*K-1) Ts l Cu2S *10-3*T 1403 K Välikoe I/ Vastaa kuuteen (6) kysymykseen! 1. Mikä on lyijykloridin muodostumisentalpia (DfH ) 700K:ssa? Ohessa laskentaan tarvittava termodynaaminen tieto. Cp = A + B*10-3*T + C*105*T-2 HSER(298) A B C J/mol J/(mol*K) PbCl2(s) Pb Cl2(g) Apuja: Mikä tahansa muodostumissuure on kyseisen tilasuureen muutos, kun standarditilaiset (puhtaat) alkuaineet muodostavat standarditilaisen puhtaan tuotteen. Jos et ehdi laskea esitä miten olisit laskenut! 2. file:///c /Documents%20and%20Settings/Jani%20Jansson/Desktop/Tentit/mak37135.htm (2 of 5) :15:51
13 mak37135 a) Miten stoikiometrinen yhdistefaasi ja liuosfaasi eroavat mielestäsi termodynaamisesti toisistaan? b) Mitä tarkoittaa aineen A termodynaaminen aktiivisuus, aktiivisuuskerroin ja partiaalinen moolinen Gibbsin eksessienergia? 3. Soveltuuko yksinkertainen säännöllisen liuoksen Redlich-Kister formalismi, jossa siis vain yksi vuorovaikutusparametri L, (joka vastaa Margulesin a - parametria eli Hildebrandtin nab-parametriä) mielestäsi kuvaamaan hyvin oheisen liuoksen käyttäytymistä? Perustele arviosi! Kiinteälle Cu-Ni liuokselle on määrätty 973K:ssa seuraavat integraalisen moolisen Gibbsin sekoitusenergian arvot xni DGmix/cal Vihje: Erottele toisistaan ideaalinen ja eksessi Gibbsin sekoitusenergia ja testaa miten hyvin ko. arvoilla toteutuu säännöllisen liuoksen yksi vakioparametri ( LCuNi eli ncuni)! Ratkaisu DmixG = DmixGid + DmixGxs = RT(xNilnxNi + xculnxcu) + LxCuxNi 4. a) Mitä tapahtuu oheisen tasapainopiirroksen (kuva puuttuu) pisteissä 1, 2 ja 3 sekä 4 ja 5, kun lämpötila pyrkii laskemaan edelleen nuolten suunnan mukaisesti? b) Mitkä faasit ovat stabiilit erilaisilla symboleille (räjähdys, äijänpää, tähti, sydän ja kuu) ilmaistuissa pisteissä? 5. Päättele Le Chatelier in periaatteeseen nojautuen tahi muutoin, mihin suuntaan reaktion SiC(s) + 2O2(g) = SiO2(s) + CO2(g) (1) tasapainon asema muuttuu 1000 C:ssa (so. eteneekö reaktio jompaan kumpaan suuntaan?), kun a) lämpötila nousee, b) paine laskee? Tarvittava termodynaaminen tieto: DRH (1273) = kj; (DRG (1273) = ) 6. file:///c /Documents%20and%20Settings/Jani%20Jansson/Desktop/Tentit/mak37135.htm (3 of 5) :15:51
14 mak37135 Onko kulta termodynaamisesti stabiili faasi huoneenlämpötilassa ilmassa yhden ilmakehän paineessa vai pyrkiikö se hapettumaan Au2O3:ksi? Seuraava tieto on käytettävissä: DfH 298(Au2O3) = J/mol, S 298(Au) = 47.3 J*mol-1*K-1, S 298(O2) = J*mol-1*K-1, S 298(Au2O3) = J*mol-1*K-1 Vihje: Laske ensin kultaoksidin standardimuodostumis Gibbs in energia, kirjoita kultaoksidin muodostumisreaktio, päättele sen tasapainoehdosta, onko kultaoksidi stabiili huoneenlämpötilassa, ilmassa yhden ilmakehän paineessa! 7. Mikä on stökiömetrisen Cr2N:n aktiivisuus Cr2+dN-faasissa lämpötilassa 1235 C, oheisen kuvan (Yllätys, yllätys, kuva puuttuu) pisteessä B, jossa Cr2+dN-faasin kanssa tasapainoisen a-kromin typpipitoisuus on 0.22 p-% (painoprosenttia). Tieto: 1. MN = 14, MCr = DfG (Cr2N) = J/mol (1235 C:ssa) 3. a-cr-faasi on kromin suhteen ideaalinen eli Raoultin aktiivisuuskerroin kromille gcr = 1 Apuja: Kirjoita nitridin muodostumisreaktion tasapainoehto, sijoita siihen edellä annettu ja oheisesta kuvasta saatava tieto ja ratkaise siitä stökiömetrisen nitridin aktiivisuus! Ratkaisu: Tasapainoehto reaktiolle 2[Cr] +0.5N2(g) = [Cr2N]Cr2+dN on K = a[cr2n]a2[cr]*(pn2/p )0.5 = expìî-dfg (Cr2N) = -( )RTüþ josta delleen a[cr2n] = K * a2[cr] * (pn2/p )0.5 = 3.992* * = [Cr2N]Cr2+dN viittaa siihen, että epästökiömetrinen krominitridi voidaan käsittää stökiömetrisen krominitridin ja kromin muodostamaksi kiinteäksi liuokseksi. Riippumatta siitä, miksikä ko. faasi käsitetään stökiömetrisellä krominitridillä on jokaisessa systeemin faasissa (myöskin kromifaasissa) sama aktiivisuus, joka voidaan laskea kyseisen reaktion tasapainoehdosta jos kromin ja typen aktiivisuudet ovat tunnetut! file:///c /Documents%20and%20Settings/Jani%20Jansson/Desktop/Tentit/mak37135.htm (4 of 5) :15:51
15 mak37135 file:///c /Documents%20and%20Settings/Jani%20Jansson/Desktop/Tentit/mak37135.htm (5 of 5) :15:51
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Termodynaamisten tasapainotarkastelujen tulokset esitetään usein kuvaajina, joissa:
 Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
Lämpötila (Celsius) Luento 9: Termodynaamisten tasapainojen graafinen esittäminen, osa 1 Tiistai 17.10. klo 8-10 Termodynaamiset tasapainopiirrokset Termodynaamisten tasapainotarkastelujen tulokset esitetään
Ellinghamin diagrammit
 Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
Chem-C2400 Luento 3: Faasidiagrammit Ville Jokinen
 Chem-C2400 Luento 3: Faasidiagrammit 16.1.2019 Ville Jokinen Oppimistavoitteet Faasidiagrammit ja mikrorakenteen muodostuminen Kahden komponentin faasidiagrammit Sidelinja ja vipusääntö Kolmen faasin reaktiot
Chem-C2400 Luento 3: Faasidiagrammit 16.1.2019 Ville Jokinen Oppimistavoitteet Faasidiagrammit ja mikrorakenteen muodostuminen Kahden komponentin faasidiagrammit Sidelinja ja vipusääntö Kolmen faasin reaktiot
SISÄLLYSLUETTELO SYMBOLILUETTELO 4
 1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
Tehtävä 1. Tasapainokonversion laskenta Χ r G-arvojen avulla Alkyloitaessa bentseeniä propeenilla syntyy kumeenia (isopropyylibentseeniä):
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
CHEM-A1110 Virtaukset ja reaktorit. Laskuharjoitus 9/2016. Energiataseet
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
Korkealämpötilakemia
 1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
Korkealämpötilakemia
 Korkealämpötilakemia Ellingham-diagrammit To 9.11.2017 klo 8-10 SÄ114 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Sisältö Mikä on Ellinghamin diagrammi?
Korkealämpötilakemia Ellingham-diagrammit To 9.11.2017 klo 8-10 SÄ114 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Sisältö Mikä on Ellinghamin diagrammi?
Mak Materiaalitieteen perusteet
 Mak-45.310 tentit Mak-45.310 Materiaalitieteen perusteet 1. välikoe 24.10.2000 1. Vertaile ionisidokseen ja metalliseen sidokseen perustuvien materiaalien a) sähkönjohtavuutta b) lämmönjohtavuutta c) diffuusiota
Mak-45.310 tentit Mak-45.310 Materiaalitieteen perusteet 1. välikoe 24.10.2000 1. Vertaile ionisidokseen ja metalliseen sidokseen perustuvien materiaalien a) sähkönjohtavuutta b) lämmönjohtavuutta c) diffuusiota
Tärkeitä tasapainopisteitä
 Tietoa tehtävistä Tasapainopiirrokseen liittyviä käsitteitä Tehtävä 1 rajojen piirtäminen Tehtävä 2 muunnos atomi- ja painoprosenttien välillä Tehtävä 3 faasien koostumus ja määrät Tehtävä 4 eutektinen
Tietoa tehtävistä Tasapainopiirrokseen liittyviä käsitteitä Tehtävä 1 rajojen piirtäminen Tehtävä 2 muunnos atomi- ja painoprosenttien välillä Tehtävä 3 faasien koostumus ja määrät Tehtävä 4 eutektinen
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
MAK tentti Vastaa 5:een kysymykseen
 MAK-37.130 tentti 17.4.2000 Vastaa 5:een kysymykseen 1. Onko vedyn käyttö pelkistimenä järkevä vaihtoehto molybdenin valmistukseen molybdenioksidista, MoO2 1200 C:ssa vakiopaineessa (1 bar)? Päättele pelkistyksessä
MAK-37.130 tentti 17.4.2000 Vastaa 5:een kysymykseen 1. Onko vedyn käyttö pelkistimenä järkevä vaihtoehto molybdenin valmistukseen molybdenioksidista, MoO2 1200 C:ssa vakiopaineessa (1 bar)? Päättele pelkistyksessä
Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta
 Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 4 Tavoite Oppia tulkitsemaan 2-komponenttisysteemien faasipiirroksia 1 Binääriset
Faasipiirrokset, osa 2 Binääristen piirrosten tulkinta Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 4 Tavoite Oppia tulkitsemaan 2-komponenttisysteemien faasipiirroksia 1 Binääriset
Standarditilat. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 2 - Luento 2. Tutustua standarditiloihin
 Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Mak Sovellettu materiaalitiede
 .106 tentit Tentti 21.5.1997 1. Rekristallisaatio. 2. a) Mitkä ovat syyt metalliseosten jähmettymisen yhteydessä tapahtuvalle lakimääräiselle alijäähtymiselle? b) Miten lakimääräinen alijäähtyminen vaikuttaa
.106 tentit Tentti 21.5.1997 1. Rekristallisaatio. 2. a) Mitkä ovat syyt metalliseosten jähmettymisen yhteydessä tapahtuvalle lakimääräiselle alijäähtymiselle? b) Miten lakimääräinen alijäähtyminen vaikuttaa
Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen
 KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Korkealämpötilakemia
 Korkealämpötilakemia Binääriset tasapainopiirrokset To 30.10.2017 klo 8-10 SÄ114 Tavoite Oppia lukemaan ja tulkitsemaan binäärisiä tasapainopiirroksia 1 Sisältö Hieman kertausta - Gibbsin vapaaenergian
Korkealämpötilakemia Binääriset tasapainopiirrokset To 30.10.2017 klo 8-10 SÄ114 Tavoite Oppia lukemaan ja tulkitsemaan binäärisiä tasapainopiirroksia 1 Sisältö Hieman kertausta - Gibbsin vapaaenergian
Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä.
 FAASIDIAGRAMMIT Määritelmiä Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä. Esimerkkejä: (a) suolaliuos (P=1),
FAASIDIAGRAMMIT Määritelmiä Faasi: Aineen tila, jonka kemiallinen koostumus ja fysikaalinen ominaisuudet ovat homogeeniset koko näytteessä. P = näytteen faasien lukumäärä. Esimerkkejä: (a) suolaliuos (P=1),
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Luku 2. Kemiallisen reaktion tasapaino
 Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Sähkökemialliset tarkastelut HSC:llä
 Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
Korkealämpötilakemia
 Korkealämpötilakemia Metallurgiset liuosmallit Yleistä To 15.11.218 klo 8-1 PR126A Tavoite Tutustua ideaali- ja reaaliliuosten käsitteisiin Tutustua liuosmalleihin yleisesti - Jaottelu - Hyvän liuosmallin
Korkealämpötilakemia Metallurgiset liuosmallit Yleistä To 15.11.218 klo 8-1 PR126A Tavoite Tutustua ideaali- ja reaaliliuosten käsitteisiin Tutustua liuosmalleihin yleisesti - Jaottelu - Hyvän liuosmallin
Kellogg-diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 1 - Luento 1
 Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy 6 Teema - Luento Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy 6 Teema - Luento Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Aluksi tutustutaan yleisesti tasaainoiirroksiin
Luento 2: Lämpökemiaa, osa 1 Torstai klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin
 Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 27.10.2016 klo 14-16 Luennon tavoite Tutustua eri tapoihin määrittää termodyn. tasapaino laskennallisesti Tutustua termodynaamisten
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 27.10.2016 klo 14-16 Luennon tavoite Tutustua eri tapoihin määrittää termodyn. tasapaino laskennallisesti Tutustua termodynaamisten
Kellogg-diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2012 Teema 1 - Luento 1
 Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy Teema - Luento Eetu-Pekka Heikkinen, Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Eetu-Pekka
Kellogg-diagrammit Ilmiömallinnus rosessimetallurgiassa Syksy Teema - Luento Eetu-Pekka Heikkinen, Tavoite Oia tulkitsemaan ja laatimaan ns. Kellogg-diagrammeja eli vallitsevuusaluekaavioita Eetu-Pekka
MT Erikoismateriaalit tuotantoprosesseissa (3 op)
 MT-0.6101 Erikoismateriaalit tuotantoprosesseissa (3 op) 6. Luento - Ke 11.11.2015 Reaktiotermodynamiikan käyttö tulenkestävien valinnassa Marko Kekkonen MT-0.6101 Erikoismateriaalit tuotantoprosesseissa
MT-0.6101 Erikoismateriaalit tuotantoprosesseissa (3 op) 6. Luento - Ke 11.11.2015 Reaktiotermodynamiikan käyttö tulenkestävien valinnassa Marko Kekkonen MT-0.6101 Erikoismateriaalit tuotantoprosesseissa
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Dislokaatiot - pikauusinta
 Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Liitetaulukko 1/11. Tutkittujen materiaalien kokonaispitoisuudet KOTIMAINEN MB-JÄTE <1MM SAKSAN MB- JÄTE <1MM POHJAKUONA <10MM
 Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin
 Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 7.9.2017 klo 8-10 Prosessimetallurgian tutkimusyksikkö Eetu-Pekka Heikkinen, 2017 Luennon tavoite Tutustua eri tapoihin määrittää
Johdanto laskennalliseen termodynamiikkaan ja mikroluokkaharjoituksiin Torstai 7.9.2017 klo 8-10 Prosessimetallurgian tutkimusyksikkö Eetu-Pekka Heikkinen, 2017 Luennon tavoite Tutustua eri tapoihin määrittää
Spontaanissa prosessissa Energian jakautuminen eri vapausasteiden kesken lisääntyy Energia ja materia tulevat epäjärjestyneemmäksi
 KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
781611S KIINTEÄN OLOMUODON KEMIA (4 op)
 781611S KIINTEÄN OLOMUODON KEMIA (4 op) ma ti ke to pe 12.9. klo 12-14 19.9. klo 12-14 26.9. klo 12-14 3.10. klo 12-14 KE351 10.10. klo 12-14 17.10. klo 12-14 24.10. klo 12-14 31.10. klo 12-14 KE351 14.9.
781611S KIINTEÄN OLOMUODON KEMIA (4 op) ma ti ke to pe 12.9. klo 12-14 19.9. klo 12-14 26.9. klo 12-14 3.10. klo 12-14 KE351 10.10. klo 12-14 17.10. klo 12-14 24.10. klo 12-14 31.10. klo 12-14 KE351 14.9.
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
KEMA221 2009 KEMIALLINEN TASAPAINO ATKINS LUKU 7
 KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
Käsitteitä. Hapetusluku = kuvitteellinen varaus, jonka atomi saa elektronin siirtyessä
 Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Sähkökemian perusteita, osa 1
 Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
HSC-ohje laskuharjoituksen 1 tehtävälle 2
 HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1
 Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1 A B B Piirroksen alue 1: Sularajan yläpuolella on seos aina täysin sula => yksifaasialue (L). Alueet 2 ja 5: Nämä ovat
Faasialueiden nimeäminen/tunnistaminen (eutek1sessa) tasapainopiirroksessa yleises1 A B B Piirroksen alue 1: Sularajan yläpuolella on seos aina täysin sula => yksifaasialue (L). Alueet 2 ja 5: Nämä ovat
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa
 Rikasta pohjoista 10.4.2019 Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa Lapin alueen yritysten uudet teräsmateriaalit Nimi Numero CK45 / C45E (1.1191) 19MnVS6 / 20MnV6 (1.1301) 38MnV6 /
Rikasta pohjoista 10.4.2019 Lapin alueen yritysten uudet teräsmateriaalit Raimo Ruoppa Lapin alueen yritysten uudet teräsmateriaalit Nimi Numero CK45 / C45E (1.1191) 19MnVS6 / 20MnV6 (1.1301) 38MnV6 /
Raerajalujittuminen LPK / Oulun yliopisto
 Raerajalujittuminen 1 Erkautuslujittuminen Epäkoherentti erkauma: kiderakenne poikkeaa matriisin rakenteesta dislokaatiot kaareutuvat erkaumien väleistä TM teräksissä tyypillisesti mikroseosaineiden karbonitridit
Raerajalujittuminen 1 Erkautuslujittuminen Epäkoherentti erkauma: kiderakenne poikkeaa matriisin rakenteesta dislokaatiot kaareutuvat erkaumien väleistä TM teräksissä tyypillisesti mikroseosaineiden karbonitridit
KE Prosessien perusteet
 KE-40.2500 Prosessien perusteet Tentiss2i saa kiiyttia1 materiaalina vain fysikaalisen kemian taulukoita kirjaa sek?i kemian laitetekniikan taulukoita ja piinoksia kirjaa' TENTT 10.3.20088-13. 1. Selit8
KE-40.2500 Prosessien perusteet Tentiss2i saa kiiyttia1 materiaalina vain fysikaalisen kemian taulukoita kirjaa sek?i kemian laitetekniikan taulukoita ja piinoksia kirjaa' TENTT 10.3.20088-13. 1. Selit8
Firan vesilaitos. Laitosanalyysit. Lkm keski- maksimi Lkm keski- maksimi
 Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
KJR-C2004 materiaalitekniikka. Harjoituskierros 3
 KJR-C2004 materiaalitekniikka Harjoituskierros 3 Tänään ohjelmassa 1. Tasapainopiirros 1. Tulkinta 2. Laskut 2. Faasimuutokset 3. Ryhmätyöt 1. Esitehtävän yhteenveto (palautetaan harkassa) 2. Ryhmätehtävä
KJR-C2004 materiaalitekniikka Harjoituskierros 3 Tänään ohjelmassa 1. Tasapainopiirros 1. Tulkinta 2. Laskut 2. Faasimuutokset 3. Ryhmätyöt 1. Esitehtävän yhteenveto (palautetaan harkassa) 2. Ryhmätehtävä
Sähkökemia. Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali
 Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Molekyylibiotieteet/Bioteknologia Etunimet valintakoe Tehtävä 3 Pisteet / 30
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Rauta-hiili tasapainopiirros
 Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
(l) B. A(l) + B(l) (s) B. B(s)
 FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
Palautus yhtenä tiedostona PDF-muodossa viimeistään torstaina
 PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
PHYS-A0120 Termodynamiikka, syksy 2018 Kotitentti Vastaa tehtäviin 1/2/3, 4, 5/6, 7/8, 9 (yhteensä viisi vastausta). Tehtävissä 1, 2, 3 ja 9 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
Top Analytica Oy Ab. XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio
 XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio Röntgenfluoresenssi Röntgensäteilyllä irroitetaan näytteen atomien sisäkuorilta (yleensä K ja L kuorilta) elektroneja. Syntyneen vakanssin paikkaa
XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio Röntgenfluoresenssi Röntgensäteilyllä irroitetaan näytteen atomien sisäkuorilta (yleensä K ja L kuorilta) elektroneja. Syntyneen vakanssin paikkaa
Normaalipotentiaalit
 Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
Lkm keski- maksimi Lkm keski- maksimi. Lkm keski- maksimi Lkm keski- maksimi
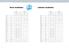 Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Tutkimuskohteen sijainti: Eli järvi 1 :
 Tutkimuskohteen sijainti: K E M I Eli järvi 1 : 400 000 OUTOKUMPU Oy - Malminetsinta HUMUSTUTKIMUSKOKEILU KEMI, ELIJARVI Tutkimusalueen sijainti Tutkimuksen tarkoitus Näytteenoton suoritus Preparointi
Tutkimuskohteen sijainti: K E M I Eli järvi 1 : 400 000 OUTOKUMPU Oy - Malminetsinta HUMUSTUTKIMUSKOKEILU KEMI, ELIJARVI Tutkimusalueen sijainti Tutkimuksen tarkoitus Näytteenoton suoritus Preparointi
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka. Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU
 MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
Sukunimi: Etunimi: Henkilötunnus:
 K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Kon Teräkset Harjoituskierros 7. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka
 Kon-67.3110 Teräkset Harjoituskierros 7. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka Hammaspyörät Suunnittelustandardit Euroopassa esimerkiksi: ISO 6336-1 5
Kon-67.3110 Teräkset Harjoituskierros 7. Timo Kiesi Koneenrakennuksen materiaalitekniikan tutkimusryhmä Koneenrakennustekniikka Hammaspyörät Suunnittelustandardit Euroopassa esimerkiksi: ISO 6336-1 5
7 Termodynaamiset potentiaalit
 82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
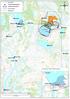 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
luku2 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen
 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
17VV VV 01021
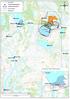 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
HEVOSENLANNAN PIENPOLTTOHANKKEEN TULOKSIA. Erikoistutkija Tuula Pellikka
 HEVOSENLANNAN PIENPOLTTOHANKKEEN TULOKSIA Erikoistutkija Tuula Pellikka TUTKIMUKSEN TAUSTA Tavoitteena oli tutkia käytännön kenttäkokeiden avulla hevosenlannan ja kuivikkeen seoksen polton ilmaan vapautuvia
HEVOSENLANNAN PIENPOLTTOHANKKEEN TULOKSIA Erikoistutkija Tuula Pellikka TUTKIMUKSEN TAUSTA Tavoitteena oli tutkia käytännön kenttäkokeiden avulla hevosenlannan ja kuivikkeen seoksen polton ilmaan vapautuvia
:TEKES-hanke. 40121/04 Leijukerroksen kuplien ilmiöiden ja olosuhteiden kokeellinen ja laskennallinen tutkiminen
 FB-kupla :TEKES-hanke 40121/04 Leijukerroksen kuplien ilmiöiden ja olosuhteiden kokeellinen ja laskennallinen tutkiminen Ryhmähankkeen osapuolet: Tampereen teknillinen yliopisto Osahanke: Biopolttoaineiden
FB-kupla :TEKES-hanke 40121/04 Leijukerroksen kuplien ilmiöiden ja olosuhteiden kokeellinen ja laskennallinen tutkiminen Ryhmähankkeen osapuolet: Tampereen teknillinen yliopisto Osahanke: Biopolttoaineiden
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
Ruostumattoman teräksen valmistaminen loppupään terässulattoprosessit.
 Ruostumattoman teräksen valmistaminen loppupään terässulattoprosessit www.outokumpu.com Johdanto Tuotantokaavio AOD-konvertteri AOD Senkka-asema SA Yhteenveto Ruostumaton teräs Ruostumaton teräs koostuu
Ruostumattoman teräksen valmistaminen loppupään terässulattoprosessit www.outokumpu.com Johdanto Tuotantokaavio AOD-konvertteri AOD Senkka-asema SA Yhteenveto Ruostumaton teräs Ruostumaton teräs koostuu
kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin?
 Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Korkealämpötilakemia
 Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä1-komponenttipiirrokset To 23.11.2017 klo 8-10 SÄ114 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
Korkealämpötilakemia Gibbsin faasisääntö, kuvaajien laadinta sekä1-komponenttipiirrokset To 23.11.2017 klo 8-10 SÄ114 Tavoite Tutustua faasipiirrosten kokeelliseen ja laskennalliseen laadintaan ja siten
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Valitse seuraavista joko tehtävä 1 tai 2
 PHYS-A0120 Termodynamiikka, syksy 2016 Kotitentti Vastaa tehtäviin 1/2, 3, 4/5, 6/7, 8 ja 9 (yhteensä kuusi vastausta). Tehtävissä 1 ja 2 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
PHYS-A0120 Termodynamiikka, syksy 2016 Kotitentti Vastaa tehtäviin 1/2, 3, 4/5, 6/7, 8 ja 9 (yhteensä kuusi vastausta). Tehtävissä 1 ja 2 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Teollinen kaivostoiminta
 Teollinen kaivostoiminta Jouni Pakarinen Kuva: Talvivaara 2007 -esite Johdanto Lähes kaikki käyttämämme tavarat tai energia on tavalla tai toisella sijainnut maan alla! Mineraali = on luonnossa esiintyvä,
Teollinen kaivostoiminta Jouni Pakarinen Kuva: Talvivaara 2007 -esite Johdanto Lähes kaikki käyttämämme tavarat tai energia on tavalla tai toisella sijainnut maan alla! Mineraali = on luonnossa esiintyvä,
Luku 15 KEMIALLISET REAKTIOT
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 15 KEMIALLISET REAKTIOT Copyright The McGraw-Hill Companies, Inc. Permission required for
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 15 KEMIALLISET REAKTIOT Copyright The McGraw-Hill Companies, Inc. Permission required for
- Termodynaamiset edellytykset - On olemassa ajava voima prosessin tapahtumiselle - Perusta - Kemiallinen potentiaali
 Luento 1: Yleistä kurssista ja sen suorituksesta Tiistai 9.10. klo 10-12 Kemiallisten prosessien edellytykset - Termodynaamiset edellytykset - On olemassa ajava voima prosessin tapahtumiselle - Perusta
Luento 1: Yleistä kurssista ja sen suorituksesta Tiistai 9.10. klo 10-12 Kemiallisten prosessien edellytykset - Termodynaamiset edellytykset - On olemassa ajava voima prosessin tapahtumiselle - Perusta
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Prosessi- ja ympäristötekniikan perusta
 Prosessi- ja ympäristötekniikan perusta Aihe 2: Materiaalitaseet Tavoite Tavoitteena on oppia tasetarkastelun käsite ja oppia tuntemaan, miten materiaalitaseita voidaan hyödyntää kokonaisprosessien sekä
Prosessi- ja ympäristötekniikan perusta Aihe 2: Materiaalitaseet Tavoite Tavoitteena on oppia tasetarkastelun käsite ja oppia tuntemaan, miten materiaalitaseita voidaan hyödyntää kokonaisprosessien sekä
Pellettien pienpolton haasteet TUOTEPÄÄLLIKKÖ HEIKKI ORAVAINEN VTT EXPERT SERVICES OY
 Pellettien pienpolton haasteet TUOTEPÄÄLLIKKÖ HEIKKI ORAVAINEN VTT EXPERT SERVICES OY Esityksen sisältö Ekopellettien ja puupellettien vertailua polttotekniikan kannalta Koetuloksia ekopellettien poltosta
Pellettien pienpolton haasteet TUOTEPÄÄLLIKKÖ HEIKKI ORAVAINEN VTT EXPERT SERVICES OY Esityksen sisältö Ekopellettien ja puupellettien vertailua polttotekniikan kannalta Koetuloksia ekopellettien poltosta
EPÄORGAANINEN KEMIA HARJOITUKSIA. Jaksollinen järjestelmä
 EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
