CHEM-A1110 Virtaukset ja reaktorit. Laskuharjoitus 9/2016. Energiataseet
|
|
|
- Annika Aro
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla tai vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin energiatase Ammoniakkia tuotetaan reaktioyhtälön N2(g) + 3 H2(g) 2 NH3(g) mukaisesti reaktorissa ilmanpaineessa käyttäen syöttönä seosta, jossa on stoikiometrinen määrä typpeä ja vetyä. Typen konversio on 25 % ja tuotevirran lämpötila 480 C. Missä lämpötilassa seos on syötettävä reaktoriin, jotta reaktori toimisi adiabaattisesti? Aineiden ominaisarvoja: Yhdiste J/(mol K) fh 0 (25 C) kj/mol Typpi 34 0 Vety 34 0 Ammoniakki 46-46,191 Vinkit tehtävän ratkaisemiseen: Tee energiatase adiabaattiselle reaktorille ja mieti mitä oletuksia voidaan tehdä (adiabaattista reaktoria ei lämmitetä tai jäähdytetä vaan reaktorin lämpötilan annetaan muuttua vapaasti reaktion edetessä) Laske reaktioentalpia referenssilämpötilassa (25 C) Laske DCp Laske reaktioentalpia reaktiolämpötilassa (480 C) Voit olettaa typpeä syötettävän 1 mol/h Ratkaise energiataseesta syötön lämpötila (V: 273 C) RATKAISU REAKTIOYHTÄLÖ: N2(g) + 3 H2(g) 2 NH3(g)
2 ENERGIATASE: Perustase, kun reaktorissa tapahtuu useita samanaikaisia reaktioita: (Tämä tapa pätee, kun komponenttien Cp:t eivät ole lämpötilasta riippuvia ja entalpia on annettu reaktiolämpötilassa) ( ) () Oletukset: Steady state (=> de/dt=0), systeemi ei tee työtä ( =0), adiabaattinen ( =0) Nyt saadaan yllä oleva yhtälö muotoon: ( ) () =0 Laskennan perusta N2,0 = 1 mol/h, jolloin H2,0 = 3 mol/h Jotta saadaan laskettua reaktioentalpia reaktiolämpötilassa T yhtälöllä () Tarvitaan ensin reaktioentalpia referenssilämpötilassa (Tref = 25 C) (25 ) () () = 2 46, ,382 Ja DCp: () () = Joista edelleen reaktioentalpia reaktiolämpötilassa (T = 480 C): (480 ) 92,382 0,044 (480 25) 112,402 Ratkaistaan syötön lämpötila ( ) () =0 + () = 273,4 = , ,402 0, ,034 Tehtävä 2. Isoterminen virtausreaktori, 2 reaktiota Keteeni (CH2CO) on tärkeä teollinen välituote, joka valmistetaan krakkaamalla etikkahappoa:
3 CH3COOH(g) fi CH2CO(g) + H2O(g) DrH(700 C) = 178,87 kj/mol Samanaikaisesti etikkahappo hajoaa termisesti metaaniksi ja hiilidioksidiksi. Mikä on krakkausuunin lämmitystarve, kun etikkahapposyöttö on 1000 mol/h lämpötilassa 300 C ja kun krakkauslämpötila on 700 C? Etikkahapon konversio on 30% ja selektiivisyys keteeniksi on 80%. Sivureaktion reaktiolämpö on DrH(700 C) = 12,68 kj/(mol etikkahappoa). Aineiden ominaisarvoja:, = 121,9, = 39,0, = 77,5, = 63,7, = 51,5 Vinkit tehtävän ratkaisemiseen: Isotermistä reaktoria lämmitetään/jäähdytetään siten, että reaktorin lämpötila pysyy vakiona Etikkahapon selektiivisyys keteeniksi on 80%, joten loput 20% reagoineesta etikkahaposta reagoi sivureaktion CH3COOH fi CH4 + CO2 mukaan Kun reaktiolämmöt on annettu reaktiolämpötilassa, niin lämmitystarve = syötön lämmitykseen tarvittava energiamäärä + reaktioista vapautuva/sitoutuva energiamäärä (V: ~92 MJ/h) RATKAISU REAKTIOYHTÄLÖT: (1) CH3COOH fi CH2CO + H2O DrH = 181,03 kj/mol (2) CH3COOH fi CH4 + CO2 DrH = 15,36 kj/mol ENERGIATASE: Perustase, kun reaktorissa tapahtuu useita samanaikaisia reaktioita: (Tämä tapa pätee, kun komponenttien Cp:t eivät ole lämpötilasta riippuvia ja entalpia on annettu reaktiolämpötilassa) = ( ) () Oletukset: Steady state (=> de/dt=0), systeemi ei tee työtä (W & =0) Nyt saadaan yllä oleva yhtälö muotoon: = ( ) + () Eli reaktorin jäähdytys tai lämmitystarve (Q) on sama kuin syötön lämmitykseen tarvittu lämpömäärä + reaktiolämpö
4 Huomaa: Reaktiolämpö on positiivinen endotermiselle ja negatiivinen eksotermiselle reaktiolle. Syöttö puhdasta etikkahappoa ( ) = ,9 () ( ) = Reaktorissa reagoivan A:n kokonaismäärä saadaan kun huomioidaan molemmat reaktiot. Helpoiten tämä tapahtuu kun käytetään selektiivisyyttä S Lisäksi S = 1eli tässä tapauksessa S1+S2 = 1 => S2 = 1- S1 i () + ( ) [ + ( ) ] = 0, = Reaktorin lämmitystarve on siis ( ) 92 0,8 178,87 + ( 0,8) 12,68 () = = Tehtävä 3. Adiabaattinen CSTR, energiataseen ja mitoitusyhtälön yhdistäminen Nestefaasireaktiossa A reagoi B:ksi adiabaattisessa sekoitussäiliöreaktorissa A B. Reaktio on toista kertalukua A:n suhteen. Komponenttia A ja liuotinta S syötetään 10 l/min lämpötilassa 50 C (CA0 = CS0 = 4 mol/l). Kuinka suuri konversio saavutetaan ja minkä kokoinen CSTR tarvitaan, kun tuotteen lämpötila on 143 C? Lähtöarvoja: (50 ) 15,32 = 66,9 = 66,9 = 75,3 (143 ) = 1,102 Vinkit tehtävän ratkaisemiseen: Adiabaattista reaktoria ei lämmitetä tai jäähdytetä vaan reaktorin lämpötilan annetaan muuttua vapaasti reaktion edetessä Ratkaise konversio yleisestä energiataseesta Laske reaktorin tilavuus CSTR:n mitoitusyhtälöstä
5 (V: 86 %, 105 dm 3 ) RATKAISU Energiatase adiabaattiselle reaktorille (Q=0) ( ) =0 ( ) => = Nestefaasireaktio vakiovirtauksella ( ) = 10 4 = 40 = 10 4 = = 0, ,0753 (143 50) 40 15,32 +0 (143 50) =0,8632 = 86,3 % CSTR:n mitoitusyhtälö = Reaktionopeusyhtälö, toista kertalukua A:n suhteen Stoikiometria () Yhdistetään = = = [ ()] = 10 0,863 () 1,102 4 ( 0,863) = 104, Tehtävä 4. Isoterminen vs. adiabaattinen panosreaktori, energiataseen ja mitoitusyhtälön yhdistäminen Panosreaktorissa tutkitaan ksyleenin isomeroitumista nestefaasissa. Reaktioyhtälö on muotoa A B.
6 Reaktio on ensimmäistä kertalukua ksyleenin (A) suhteen. Reaktorin tilavuus on 2 dm 3 ja reaktoriin panostetaan alussa 20 moolia ksyleeniä 25 C:ssa. Reaktion aktivoitumisenergia on 50 kj/mol ja frekvenssitekijä /s. Laske kauan kestää saavuttaa 50 %:n konversio, kun reaktio suoritetaan a) isotermisesti b) adiabaattisesti Lähtöarvoja: (25 ) 20,00, = 100, = 100 Vinkit tehtävän ratkaisemiseen: Isotermisessä tapauksessa laske konversio panosreaktorin mitoitusyhtälöstä (isotermisessä tapauksessa reaktorin lämpötila pidetään koko ajan 25 C:ssa jäähdyttämällä reaktoria) Adiabaattisessa tapauksessa johda yhtälö konversion muuttumiselle ajan funktiona (adiabaattisessa tapauksessa reaktorin lämpötilan annetaan nousta vapaasti) Laske reaktorin loppulämpötila adiabaattisen reaktorin energiataseesta eri konversion arvoilla (esim. 0,1:n askeleen välein nollasta 0,5:een) Laske reaktionopeusvakio jokaisessa loppulämpötilassa Laske termi dt jokaisella konversiolla ja integroi numeerisesti käyttäen vaikkapa puolisuunnikassääntöä: () 2 ( ), ä (V: a) 64 min, b) 9,3 min) RATKAISU a) Isoterminen Ensimmäisen kertaluvun nestefaasireaktio, joka tehdään vakiolämpötilassa ja vakiopaineessa: = = Sijoitetaan nopeusyhtälö taseyhtälöön: =
7 Integroidaan (alkuehto: t=0 ja ca=ca0): = 1 Lasketaan reaktionopeusvakio (298) = /( = 1, Lasketaan ca0 ja ca = = 20 = 10 ()= 10 ( 0,5) =5 Sijoitetaan 1 1 1, b) Adiabaattinen Panosreaktorin mitoitusyhtälö Ensimmäisen kertaluvun reaktio Stoikiometria () Yhdistämällä saadaan ()= () 5 10 = Ylläoleva yhtälö riippuu konversion lisäksi myös reaktiolämpötilasta, koska reaktionopeusvakio k riippuu lämpötilasta. Yhtälöä ei voi siis suoraan integroida, koska reaktiolämpötilaa ei tunneta. Konversio ja reaktiolämpötila saadaan yhdistettyä toisiinsa energiataseella. Reaktoreiden energiataseet -prujussa on johdettu panosreaktorille adiabaattinen lämpötilannousu: = missä
8 DT = T T0 DcA = ca ca0 x reaktion etenemisaste = = = 2000 = =0 Numeerista integrointia varten tehdään taulukko eri konversion arvoille (esim. askelpituudella h = 0,1), konversioiden avulla lasketaan ca ja T (adiabaattisen lämmönnousun avulla), sitten k lämpötilassa T (k lasketaan tehtävässä annetulla korrelaatiolla) ja lopuksi dt: X CA T(K) k(1/s) (mol/dm 3 ) = (1 ) , ,6 = y0 0, , ,7 = y1 0, , ,1 = y2 0, , ,2 = y3 0, , ,3 = y4 0, , ,0 = y5 Käyttämällä puolisuunnikassääntöä saadaan ajaksi = 2 ( ) = 0,1 (5814, , , , ,3 + 73,0) = 584,41 9,7 2 Annettaessa reaktorin toimia adiabaattisesti (eli ilman jäähdytystä) haluttu konversio saavutetaan huomattavasti lyhyemmässä ajassa kuin isotermisessä ajossa. Huomataan, että adiabaattisessa tapauksessa 50 %:n konversio saavutetaan huomattavasti nopeammin kuin isotermisessä tapauksessa. Adiabaattisessa reaktorissa lämpötila nousee 100 C, minkä takia reaktionopeusvakion arvo kasvaa Arrheniuksen yhtälön mukaisesti yli 100-kertaiseksi.
Tehtävä 1. Tasapainokonversion laskenta Χ r G-arvojen avulla Alkyloitaessa bentseeniä propeenilla syntyy kumeenia (isopropyylibentseeniä):
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
HSC-ohje laskuharjoituksen 1 tehtävälle 2
 HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
Luku 21. Kemiallisten reaktioiden nopeus
 Luku 21. Kemiallisten reaktioiden nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista tasapainoreaktiota:
Luku 21. Kemiallisten reaktioiden nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista tasapainoreaktiota:
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
Luku 8. Reaktiokinetiikka
 Luku 8 Reaktiokinetiikka 234 8.1 Reaktion nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista
Luku 8 Reaktiokinetiikka 234 8.1 Reaktion nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista
Reaktiotekniikka. Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää
 Reaktiotekniikka Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää Luennon sisältö Johdanto ja termejä Reaktiotekniikka Kemiallinen prosessitekniikka Kemialliset reaktiot Reaktioiden jaottelu
Reaktiotekniikka Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää Luennon sisältö Johdanto ja termejä Reaktiotekniikka Kemiallinen prosessitekniikka Kemialliset reaktiot Reaktioiden jaottelu
Luku 2. Kemiallisen reaktion tasapaino
 Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
1 Di erentiaaliyhtälöt
 Taloustieteen mat.menetelmät syksy 2017 materiaali II-5 1 Di erentiaaliyhtälöt 1.1 Skalaariyhtälöt Määritelmä: ensimmäisen kertaluvun di erentiaaliyhtälö on muotoa _y = F (y; t) oleva yhtälö, missä _y
Taloustieteen mat.menetelmät syksy 2017 materiaali II-5 1 Di erentiaaliyhtälöt 1.1 Skalaariyhtälöt Määritelmä: ensimmäisen kertaluvun di erentiaaliyhtälö on muotoa _y = F (y; t) oleva yhtälö, missä _y
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Termodynamiikka. Fysiikka III 2007. Ilkka Tittonen & Jukka Tulkki
 Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Puun termiset aineominaisuudet pyrolyysissa
 1 Puun termiset aineominaisuudet pyrolyysissa V Liekkipäivä Otaniemi, Espoo 14.1.2010 Ville Hankalin TTY / EPR 14.1.2010 2 Esityksen sisältö TTY:n projekti Biomassan pyrolyysin reaktiokinetiikan tutkimus
1 Puun termiset aineominaisuudet pyrolyysissa V Liekkipäivä Otaniemi, Espoo 14.1.2010 Ville Hankalin TTY / EPR 14.1.2010 2 Esityksen sisältö TTY:n projekti Biomassan pyrolyysin reaktiokinetiikan tutkimus
kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin?
 Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Kaasu 2-atominen. Rotaatio ja translaatiovapausasteet virittyneet (f=5) c. 5 Ideaalikaasun tilanyhtälöstä saadaan kaasun moolimäärä: 3
 S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
KJR-C2002 Kontinuumimekaniikan perusteet
 KJR-C2002 Kontinuumimekaniikan perusteet Luento 25.11.2015 Susanna Hurme, Yliopistonlehtori, TkT Tämän päivän luento Aiemmin ollaan johdettu palkin voimatasapainoyhtälöt differentiaaligeometrisella tavalla
KJR-C2002 Kontinuumimekaniikan perusteet Luento 25.11.2015 Susanna Hurme, Yliopistonlehtori, TkT Tämän päivän luento Aiemmin ollaan johdettu palkin voimatasapainoyhtälöt differentiaaligeometrisella tavalla
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Molekyylibiotieteet/Bioteknologia Etunimet valintakoe Tehtävä 3 Pisteet / 30
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
2v 1 = v 2, 2v 1 + 3v 2 = 4v 2.. Vastaavasti ominaisarvoa λ 2 = 4 vastaavat ominaisvektorit toteuttavat. v 2 =
 TKK, Matematiikan laitos Pikkarainen/Tikanmäki Mat-1.1320 Matematiikan peruskurssi K2 Harjoitus 12, A=alku-, L=loppuviikko, T= taulutehtävä, P= palautettava tehtävä, W= verkkotehtävä 21. 25.4.2008, viikko
TKK, Matematiikan laitos Pikkarainen/Tikanmäki Mat-1.1320 Matematiikan peruskurssi K2 Harjoitus 12, A=alku-, L=loppuviikko, T= taulutehtävä, P= palautettava tehtävä, W= verkkotehtävä 21. 25.4.2008, viikko
12. Differentiaaliyhtälöt
 1. Differentiaaliyhtälöt 1.1 Johdanto Differentiaaliyhtälöitä voidaan käyttää monilla alueilla esimerkiksi tarkasteltaessa jonkin kohteen lämpötilan vaihtelua, eksponentiaalista kasvua, sähkölatauksen
1. Differentiaaliyhtälöt 1.1 Johdanto Differentiaaliyhtälöitä voidaan käyttää monilla alueilla esimerkiksi tarkasteltaessa jonkin kohteen lämpötilan vaihtelua, eksponentiaalista kasvua, sähkölatauksen
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
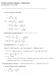 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
KEMA221 2009 KEMIALLINEN TASAPAINO ATKINS LUKU 7
 KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
SISÄLLYSLUETTELO SYMBOLILUETTELO 4
 1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
2. Viikko. CDH: luvut (s ). Matematiikka on fysiikan kieli ja differentiaaliyhtälöt sen yleisin murre.
 2. Viikko Keskeiset asiat ja tavoitteet: 1. Peruskäsitteet: kertaluku, lineaarisuus, homogeenisuus. 2. Separoituvan diff. yhtälön ratkaisu, 3. Lineaarisen 1. kl yhtälön ratkaisu, CDH: luvut 19.1.-19.4.
2. Viikko Keskeiset asiat ja tavoitteet: 1. Peruskäsitteet: kertaluku, lineaarisuus, homogeenisuus. 2. Separoituvan diff. yhtälön ratkaisu, 3. Lineaarisen 1. kl yhtälön ratkaisu, CDH: luvut 19.1.-19.4.
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
 mak37135 MAK-37.135 Materiaalien ja prosessien termodynaamis-kineettiset perusteet Tentti 22.2.2001 Vastaa 7:ään kysymykseen 1. Sinun olisi arvioitava hiilettyykö teräs, jonka hiilipitoisuus on 0.35% vai
mak37135 MAK-37.135 Materiaalien ja prosessien termodynaamis-kineettiset perusteet Tentti 22.2.2001 Vastaa 7:ään kysymykseen 1. Sinun olisi arvioitava hiilettyykö teräs, jonka hiilipitoisuus on 0.35% vai
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka. Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU
 MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
(a) Järjestellään yhtälöitä siten, että vasemmalle puolelle jää vain y i ja oikealle puolelle muut
 BM0A5830 Differentiaalihtälöiden peruskurssi Harjoitus 7, Kevät 07 Päivitksiä: Tehtävän b tehtävänantoa korjattu, tehtävän 5 vastaus korjattu. b tehtävänantoa sujuvoitettu. Vastauksia lisätt.. Monasti
BM0A5830 Differentiaalihtälöiden peruskurssi Harjoitus 7, Kevät 07 Päivitksiä: Tehtävän b tehtävänantoa korjattu, tehtävän 5 vastaus korjattu. b tehtävänantoa sujuvoitettu. Vastauksia lisätt.. Monasti
1.1 Homogeeninen kemiallinen tasapaino
 1.1 Homogeeninen kemiallinen tasapaino 1. a) Mitä tarkoittaa käsite kemiallinen tasapaino? b) Miten kemiallinen tasapaino ilmaistaan reaktioyhtälössä? c) Mistä tekijöistä tasapainossa olevan reaktioseoksen
1.1 Homogeeninen kemiallinen tasapaino 1. a) Mitä tarkoittaa käsite kemiallinen tasapaino? b) Miten kemiallinen tasapaino ilmaistaan reaktioyhtälössä? c) Mistä tekijöistä tasapainossa olevan reaktioseoksen
Numeeriset menetelmät TIEA381. Luento 12. Kirsi Valjus. Jyväskylän yliopisto. Luento 12 () Numeeriset menetelmät / 33
 Numeeriset menetelmät TIEA381 Luento 12 Kirsi Valjus Jyväskylän yliopisto Luento 12 () Numeeriset menetelmät 25.4.2013 1 / 33 Luennon 2 sisältö Tavallisten differentiaaliyhtälöiden numeriikasta Rungen
Numeeriset menetelmät TIEA381 Luento 12 Kirsi Valjus Jyväskylän yliopisto Luento 12 () Numeeriset menetelmät 25.4.2013 1 / 33 Luennon 2 sisältö Tavallisten differentiaaliyhtälöiden numeriikasta Rungen
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Differentiaali- ja integraalilaskenta 1 Ratkaisut 5. viikolle /
 MS-A8 Differentiaali- ja integraalilaskenta, V/7 Differentiaali- ja integraalilaskenta Ratkaisut 5. viikolle / 9..5. Integroimismenetelmät Tehtävä : Laske osittaisintegroinnin avulla a) π x sin(x) dx,
MS-A8 Differentiaali- ja integraalilaskenta, V/7 Differentiaali- ja integraalilaskenta Ratkaisut 5. viikolle / 9..5. Integroimismenetelmät Tehtävä : Laske osittaisintegroinnin avulla a) π x sin(x) dx,
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta Insinöörivalinnan kemian koe MALLIRATKAISUT
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
2 Yhtälöitä ja epäyhtälöitä
 2 Yhtälöitä ja epäyhtälöitä 2.1 Ensimmäisen asteen yhtälö ja epäyhtälö Muuttujan x ensimmäisen asteen yhtälöksi sanotaan yhtälöä, joka voidaan kirjoittaa muotoon ax + b = 0, missä vakiot a ja b ovat reaalilukuja
2 Yhtälöitä ja epäyhtälöitä 2.1 Ensimmäisen asteen yhtälö ja epäyhtälö Muuttujan x ensimmäisen asteen yhtälöksi sanotaan yhtälöä, joka voidaan kirjoittaa muotoon ax + b = 0, missä vakiot a ja b ovat reaalilukuja
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
LAPPEENRANNAN TEKNILLINEN YLIOPISTO KEMIANTEKNIIKAN OSASTO PERMUURAHAISHAPON VALMISTAMINEN PUTKIREAKTORISSA
 LAPPEENRANNAN TEKNILLINEN YLIOPISTO KEMIANTEKNIIKAN OSASTO PERMUURAHAISHAPON VALMISTAMINEN PUTKIREAKTORISSA Työn tarkastajana ja ohjaajana toimi DI Eero Kolehmainen Lappeenrannassa 26.3.2008 Jukka Räsänen
LAPPEENRANNAN TEKNILLINEN YLIOPISTO KEMIANTEKNIIKAN OSASTO PERMUURAHAISHAPON VALMISTAMINEN PUTKIREAKTORISSA Työn tarkastajana ja ohjaajana toimi DI Eero Kolehmainen Lappeenrannassa 26.3.2008 Jukka Räsänen
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Luento 3: Liikkeen kuvausta, differentiaaliyhtälöt
 Luento 3: Liikkeen kuvausta, differentiaaliyhtälöt Suoraviivainen liike integrointi Digress: vakio- vs. muuttuva kiihtyvyys käytännössä Kinematiikkaa yhdessä dimensiossa taustatietoa ELEC-A3110 Mekaniikka
Luento 3: Liikkeen kuvausta, differentiaaliyhtälöt Suoraviivainen liike integrointi Digress: vakio- vs. muuttuva kiihtyvyys käytännössä Kinematiikkaa yhdessä dimensiossa taustatietoa ELEC-A3110 Mekaniikka
Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: b) 0 e x + 1
 Tehtävä : Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: a) a) x b) e x + Integraali voisi ratketa muuttujanvaihdolla. Integroitava on muotoa (a x ) n joten sopiva muuttujanvaihto voisi olla
Tehtävä : Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: a) a) x b) e x + Integraali voisi ratketa muuttujanvaihdolla. Integroitava on muotoa (a x ) n joten sopiva muuttujanvaihto voisi olla
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
KE5 Kurssikoe Kastellin lukio 2012 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko.
 KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
MS-C1340 Lineaarialgebra ja differentiaaliyhtälöt
 MS-C1340 Lineaarialgebra ja differentiaaliyhtälöt Differentiaaliyhtälöt, osa 1 Riikka Kangaslampi Matematiikan ja systeemianalyysin laitos Aalto-yliopisto 2015 1 / 20 R. Kangaslampi Matriisihajotelmista
MS-C1340 Lineaarialgebra ja differentiaaliyhtälöt Differentiaaliyhtälöt, osa 1 Riikka Kangaslampi Matematiikan ja systeemianalyysin laitos Aalto-yliopisto 2015 1 / 20 R. Kangaslampi Matriisihajotelmista
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
Luento 2: Lämpökemiaa, osa 1 Torstai klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
ax + y + 2z = 0 2x + y + az = b 2. Kuvassa alla on esitetty nesteen virtaus eräässä putkistossa.
 BM20A5800 Funktiot, lineaarialgebra ja vektorit Harjoitus 7, Syksy 206 Tutkitaan yhtälöryhmää x + y + z 0 2x + y + az b ax + y + 2z 0 (a) Jos a 0 ja b 0 niin mikä on yhtälöryhmän ratkaisu? Tulkitse ratkaisu
BM20A5800 Funktiot, lineaarialgebra ja vektorit Harjoitus 7, Syksy 206 Tutkitaan yhtälöryhmää x + y + z 0 2x + y + az b ax + y + 2z 0 (a) Jos a 0 ja b 0 niin mikä on yhtälöryhmän ratkaisu? Tulkitse ratkaisu
y + 4y = 0 (1) λ = 0
 Matematiikan ja tilastotieteen osasto/hy Differentiaaliyhtälöt I Laskuharjoitus 6 mallit Kevät 2019 Tehtävä 1. Ratkaise yhtälöt a) y + 4y = x 2, b) y + 4y = 3e x. Ratkaisu: a) Differentiaaliyhtälön yleinen
Matematiikan ja tilastotieteen osasto/hy Differentiaaliyhtälöt I Laskuharjoitus 6 mallit Kevät 2019 Tehtävä 1. Ratkaise yhtälöt a) y + 4y = x 2, b) y + 4y = 3e x. Ratkaisu: a) Differentiaaliyhtälön yleinen
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä
 LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä. Diffuusio yksiulotteisessa epäjärjestäytyneessä hilassa E J ii, J ii, + 0 E b, i E i i i i+ x Kuva.:
LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä. Diffuusio yksiulotteisessa epäjärjestäytyneessä hilassa E J ii, J ii, + 0 E b, i E i i i i+ x Kuva.:
KE Prosessien perusteet
 KE-40.2500 Prosessien perusteet Tentiss2i saa kiiyttia1 materiaalina vain fysikaalisen kemian taulukoita kirjaa sek?i kemian laitetekniikan taulukoita ja piinoksia kirjaa' TENTT 10.3.20088-13. 1. Selit8
KE-40.2500 Prosessien perusteet Tentiss2i saa kiiyttia1 materiaalina vain fysikaalisen kemian taulukoita kirjaa sek?i kemian laitetekniikan taulukoita ja piinoksia kirjaa' TENTT 10.3.20088-13. 1. Selit8
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
Prosessitekniikka Taseet
 Oppimistavoite, osa 1 Prosessitekniikka Taseet Ville lopaeus Kemian laitetekniikan tutkimusryhmä Saada peruskäsitys tyypillisestä kemiallisesta prosessista ja sen osista Tunnistaa yksikköprosessit ja yksikköoperaatiot
Oppimistavoite, osa 1 Prosessitekniikka Taseet Ville lopaeus Kemian laitetekniikan tutkimusryhmä Saada peruskäsitys tyypillisestä kemiallisesta prosessista ja sen osista Tunnistaa yksikköprosessit ja yksikköoperaatiot
Selvitetään kaasujen yleisen tilanyhtälön avulla yhdisteen moolimassa.
 Diploi-insinööri ja arkkitehtikoulutuksen yhteisvalinta 2016 DI-keian valintakoe 1.6.2016 alliratkaisut 1. a) ääritetään ensin yhdisteen epiirinen kaava. Oletetaan, että yhdistettä on 100 g. Yhdiste sisältää
Diploi-insinööri ja arkkitehtikoulutuksen yhteisvalinta 2016 DI-keian valintakoe 1.6.2016 alliratkaisut 1. a) ääritetään ensin yhdisteen epiirinen kaava. Oletetaan, että yhdistettä on 100 g. Yhdiste sisältää
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Algoritmit 1. Demot Timo Männikkö
 Algoritmit 1 Demot 1 31.1.-1.2.2018 Timo Männikkö Tehtävä 1 (a) Algoritmi, joka tutkii onko kokonaisluku tasan jaollinen jollain toisella kokonaisluvulla siten, että ei käytetä lainkaan jakolaskuja Jaettava
Algoritmit 1 Demot 1 31.1.-1.2.2018 Timo Männikkö Tehtävä 1 (a) Algoritmi, joka tutkii onko kokonaisluku tasan jaollinen jollain toisella kokonaisluvulla siten, että ei käytetä lainkaan jakolaskuja Jaettava
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Esimerkiksi ammoniakin valmistus typestä ja vedystä on tyypillinen teollinen tasapainoreaktio.
 REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
HY, MTO / Matemaattisten tieteiden kandiohjelma Todennäköisyyslaskenta IIa, syksy 2018 Harjoitus 3 Ratkaisuehdotuksia.
 HY, MTO / Matemaattisten tieteiden kandiohjelma Todennäköisyyslaskenta IIa, syksy 8 Harjoitus Ratkaisuehdotuksia Tehtäväsarja I. Mitkä seuraavista funktioista F, F, F ja F 4 ovat kertymäfunktioita? Mitkä
HY, MTO / Matemaattisten tieteiden kandiohjelma Todennäköisyyslaskenta IIa, syksy 8 Harjoitus Ratkaisuehdotuksia Tehtäväsarja I. Mitkä seuraavista funktioista F, F, F ja F 4 ovat kertymäfunktioita? Mitkä
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Ei välttämättä, se voi olla esimerkiksi Reuleaux n kolmio:
 Inversio-ongelmista Craig, Brown: Inverse problems in astronomy, Adam Hilger 1986. Havaitaan oppositiossa olevaa asteroidia. Pyörimisestä huolimatta sen kirkkaus ei muutu. Projisoitu pinta-ala pysyy ilmeisesti
Inversio-ongelmista Craig, Brown: Inverse problems in astronomy, Adam Hilger 1986. Havaitaan oppositiossa olevaa asteroidia. Pyörimisestä huolimatta sen kirkkaus ei muutu. Projisoitu pinta-ala pysyy ilmeisesti
Luento 2: Liikkeen kuvausta
 Luento 2: Liikkeen kuvausta Suoraviivainen liike integrointi Kinematiikkaa yhdessä dimensiossa Luennon sisältö Suoraviivainen liike integrointi Kinematiikkaa yhdessä dimensiossa Liikkeen ratkaisu kiihtyvyydestä
Luento 2: Liikkeen kuvausta Suoraviivainen liike integrointi Kinematiikkaa yhdessä dimensiossa Luennon sisältö Suoraviivainen liike integrointi Kinematiikkaa yhdessä dimensiossa Liikkeen ratkaisu kiihtyvyydestä
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Hapot, Emäkset ja pk a Opettava tutkija Pekka M Joensuu Jokaisella hapolla on: Arvo, joka kertoo meille kuinka hapan kyseinen protoni on. Helpottaa valitsemaan
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Hapot, Emäkset ja pk a Opettava tutkija Pekka M Joensuu Jokaisella hapolla on: Arvo, joka kertoo meille kuinka hapan kyseinen protoni on. Helpottaa valitsemaan
8 Yritys kilpailullisilla markkinoilla (Mankiw & Taylor, Ch 14)
 8 Yritys kilpailullisilla markkinoilla (Mankiw & Taylor, Ch 14) Markkinat ovat kilpailulliset silloin, kun siellä on niin paljon yrityksiä, että jokainen pitää markkinoilla määräytyvää hintaa omista toimistaan
8 Yritys kilpailullisilla markkinoilla (Mankiw & Taylor, Ch 14) Markkinat ovat kilpailulliset silloin, kun siellä on niin paljon yrityksiä, että jokainen pitää markkinoilla määräytyvää hintaa omista toimistaan
KE5 Kurssikoe Kastellin lukio 2014
 KE5 Kurssikoe Kastellin lukio 014 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heterogeeninen tasapaino
KE5 Kurssikoe Kastellin lukio 014 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heterogeeninen tasapaino
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Oletetaan kaasu ideaalikaasuksi ja sovelletaan Daltonin lakia. Kumpikin seoksen kaasu toteuttaa erikseen ideaalikaasun tilanyhtälön:
 S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
S-445, ysiikka III (Sf) entti 653 Astiassa on, µmol vetyä (H ) ja, µg tyeä ( ) Seoksen lämötila on 373 K ja aine,33 Pa Määritä a) astian tilavuus, b) vedyn ja tyen osaaineet ja c) molekyylien lukumäärä
Matemaattinen Analyysi
 Vaasan yliopisto, kevät 01 / ORMS1010 Matemaattinen Analyysi. harjoitus, viikko 1 R1 ke 1 16 D11 (..) R to 10 1 D11 (..) 1. Määritä funktion y(x) MacLaurinin sarjan kertoimet, kun y(0) = ja y (x) = (x
Vaasan yliopisto, kevät 01 / ORMS1010 Matemaattinen Analyysi. harjoitus, viikko 1 R1 ke 1 16 D11 (..) R to 10 1 D11 (..) 1. Määritä funktion y(x) MacLaurinin sarjan kertoimet, kun y(0) = ja y (x) = (x
TKK, TTY, LTY, OY, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 31.5.2006
 TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
7 Termodynaamiset potentiaalit
 82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
Insinöörimatematiikka D
 Insinöörimatematiikka D Demonstraatio 7, 6.7... Ratkaise dierentiaalihtälöpari = = Vastaus: DY-pari voidaan esittää muodossa ( = Matriisin ominaisarvot ovat i ja i ja näihin kuuluvat ominaisvektorit (
Insinöörimatematiikka D Demonstraatio 7, 6.7... Ratkaise dierentiaalihtälöpari = = Vastaus: DY-pari voidaan esittää muodossa ( = Matriisin ominaisarvot ovat i ja i ja näihin kuuluvat ominaisvektorit (
Bensiiniä voidaan pitää hiilivetynä C8H18, jonka tiheys (NTP) on 0,703 g/ml ja palamislämpö H = kj/mol
 Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Normaaliryhmä. Toisen kertaluvun normaaliryhmä on yleistä muotoa
 Normaaliryhmä Toisen kertaluvun normaaliryhmä on yleistä muotoa x = u(t,x,y), y t I, = v(t,x,y), Funktiot u = u(t,x,y), t I ja v = v(t,x,y), t I ovat tunnettuja Toisen kertaluvun normaaliryhmän ratkaisu
Normaaliryhmä Toisen kertaluvun normaaliryhmä on yleistä muotoa x = u(t,x,y), y t I, = v(t,x,y), Funktiot u = u(t,x,y), t I ja v = v(t,x,y), t I ovat tunnettuja Toisen kertaluvun normaaliryhmän ratkaisu
2 dy dx 1. x = y2 e x2 2 1 y 2 dy = e x2 xdx. 2 y 1 1. = ex2 2 +C 2 1. y =
 BM20A5830 Differentiaaliyhtälöiden peruskurssi Harjoitus 2, Kevät 207 Päivityksiä: Tehtävän 4b tehtävänanto korjattu ja vastauksia lisätty.. Ratkaise y, kun 2y x = y 2 e x2. Jos y () = 0 niin mikä on ratkaisu
BM20A5830 Differentiaaliyhtälöiden peruskurssi Harjoitus 2, Kevät 207 Päivityksiä: Tehtävän 4b tehtävänanto korjattu ja vastauksia lisätty.. Ratkaise y, kun 2y x = y 2 e x2. Jos y () = 0 niin mikä on ratkaisu
2. Uusiutuvat luonnonvarat: Kalastuksen taloustiede
 YLE5 / YET-09 Luonnonvarataloustieteen jatkokurssi. Uusiutuvat luonnonvarat: alastuksen taloustiede Marko Lindroos & Maija Holma Uusiutuvat luonnonvarat alastuksen taloustiede: Luentoteemat.1 Johdanto.
YLE5 / YET-09 Luonnonvarataloustieteen jatkokurssi. Uusiutuvat luonnonvarat: alastuksen taloustiede Marko Lindroos & Maija Holma Uusiutuvat luonnonvarat alastuksen taloustiede: Luentoteemat.1 Johdanto.
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
Insinöörimatematiikka D, laskuharjoituksien esimerkkiratkaisut
 Insinöörimatematiikka D, 406 6 laskuharjoituksien esimerkkiratkaisut Ratkaistaan differentiaaliyhtälö y = y () Tässä = d dy eli kyseessä on lineaarinen kertaluvun differentiaaliyhtälö: Yhtälön () homogenisoidulle
Insinöörimatematiikka D, 406 6 laskuharjoituksien esimerkkiratkaisut Ratkaistaan differentiaaliyhtälö y = y () Tässä = d dy eli kyseessä on lineaarinen kertaluvun differentiaaliyhtälö: Yhtälön () homogenisoidulle
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
k=0 saanto jokaisen kolmannen asteen polynomin. Tukipisteet on talloin valittu
 LIS AYKSI A kirjaan Reaalimuuttujan analyysi 1.6. Numeerinen integrointi: Gaussin kaavat Edella kasitellyt numeerisen integroinnin kaavat eli kvadratuurikaavat Riemannin summa, puolisuunnikassaanto ja
LIS AYKSI A kirjaan Reaalimuuttujan analyysi 1.6. Numeerinen integrointi: Gaussin kaavat Edella kasitellyt numeerisen integroinnin kaavat eli kvadratuurikaavat Riemannin summa, puolisuunnikassaanto ja
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos

