BECS-C2101 Biofysiikka
|
|
|
- Kristiina Keskinen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 BECS-C2101 Biofysiikka 1 Luento Solujen sisustan koostumus Biomolekyylien vuorovaikutukset ja rakenne Veden ominaisuudet
2 Chapter 2. What s Inside Cells 2 Biologinen kysymys: Miten solut toteuttavat ja hoitavat niissä jatkuvasti käynnissä olevan valtavan määrän kemiallisia prosesseja ja reaktioihin osallistuvia aineita? Fysikaalisia ideoita: 1. Solukalvot järjestyvät spontaanisti rakenneosistaan ja muodostavat kompartmentteja. 2. Solut käyttävät aktiivista kuljetusta. 3. Biokemialliset prosessit ovat spesifejä (usein entsyymivälitteisiä).
3 What s Inside Cells 3 Eri organismien koostumus:
4 Erilaisilla eliöillä on hyvin samanlainen koostumus atomitasolla: 4 Koostumus molekyylitasolla:
5 Biologisesti tärkeiden alkuaineiden sijainti jaksollisessa järjestelmässä: 5 molekyyleissä Pieniä atomeja: Vahvat kovalenttiset sidokset Myös kaksois- ja kolmoissidoksia (esim. Si ei, vaikka 4 elektronia uloimmalla kuorella kuten C)
6 Skaaloista 6 Dimensiot aika energia: Suuruusluokkien sisäistäminen Dimensiot:
7 Skaaloista 7 Dimensiot: Molekyylejä HIV Bakteeri Bakteriofagi (virus)
8 Skaaloista 8 Dimensiot, edellisen kuvan molekyylit: a. Hiiliatomi b. Glukoosi c. ATP d. Klorofylli e. Siirtäjä-RNA (trna) f. Vasta-ainemolekyyli g. Ribosomi h. Poliovirus i. Myosiini j. DNA k. F-aktiini l. Entsyymejä m. Pyruvaattidehydrogenaasi
9 Skaaloista Dimensiot: ATP 9 1 Å = 0.1 nm = m
10 10 Dimensiot: Glukoosi sokerit Hemoglobiini proteiinit Ribosomi pienet soluorganellit Useimmat virukset Å Solut > 1 mm vrt. mikroelektrodin kärki Φ < 100 nm
11 Biologiset makromolekyylit voivat olla tosi makroja! 11 DNA:
12 Aikaskaalat: 12 Useimmat entsyymit: Substraatti tuote: 10-3 s Jotkut entsyymit jopa 10-6 s Useat konformaatiomuutokset nopeita DNA:n kaksoiskierteen oikeneminen: ms Molekyylin osan rotaatio toisen suhteen: ns Fotoreseptorimolekyylin konfiguraatiomuutos: < ps Proteiinin elinikä voi olla vain tunteja! Sidos katkeaa
13 13 Nopeiden reaktioiden tutkimus ekstralyhyillä ( jopa < 10 fs) valopulsseilla 10 fs: valon kulkema matka m = 3 mm!
14 Energiaskaalat: 14 1 J = cal Primaarinen energialähde: aurinko Fotonin energia (500 nm): 2.5 ev 57 kcal/mol Terminen energia (25 ºC): ev 0.6 kcal/mol Keskim. energia per vapausaste molekyylissä Kovalenttinen sidos n. 100 kcal/mol C-C 83 kcal/mol Stabiili Tarvitaan entsyymejä katkaisemaan sidokset spesifiset katkaisukohdat Ei-kovalenttiset (fysikaaliset) sidokset muutama kcal/mol Terminen energia riittää katkomaan
15 Molekyylinsisäiset sidokset 15 Kovalenttiset sidokset Kemiallinen sidos Vahvoja sidoksia Biomolekyylien sidokset n kj/mol (1,7 10,4 ev) Molekyylien rakennesidoksia, suuntaavia
16 Eri atomien väliset sidokset polaarisia ryhmiä (dipolimomentti) 16 Elektronegatiivisuus Kasvaa järjestysluvun kasvaessa samassa jaksossa Kasvaa siirryttäessä ryhmässä ylöspäin Esimerkiksi: C-C: ei-polaarinen O-H: voimakkaasti polaarinen
17 Biomolekyyleissä reversiibeleitä vuorovaikutuksia välittävät sidokset Molekyylien välillä Molekyylien sisällä Ionisidokset Ionien välinen attraktio (ei suuntariippuva) Kutsutaan myös Molekyyleissä: suolasilta ( salt linkage, salt bridge ) Voima F liuoksessa: ionipari (varaukset q 1 ja q 2 etäisyydellä r) F qq Dr Vedessä r 80, tyhjössä r = 1 Hiilivety-ympäristössä (lipidi) r 2 Tyypillien ionisidos biomolekyylien välillä: COO -...NH 3 + D 1 2, r Tyhjön permittiivisyys r = riippuen, onko vettä vai muuta väliainetta ionien ympärillä
18 Ionisidoksen energia: Ytimien tasapainoetäisyys = van der Waals säteiden summa Atomien etäisyyksistä kiteessä NaCl-tyyppinen kide (FCC = face-centered cubic) Tasapainoetäisyydet useista eri ionikiteistä ja vertailemalla: Esim. NaCl KCl ja NaOH KOH Kationisäteet < vast. atomisäteet Anionisäteet > vast. atomisäteet Esim. NaCl x e = 2.79 Å (kide), mutta 2.36 Å (kaasu) Sidosenergia viemällä toinen ioni äärettömän kauas: Esim. NaCl r q1q 2 2 Dr q q E dx J J 5.31eV 498kJ mol Dr ( )
19 Koordinaatiosidokset Metallikomplekseissa Keskusatomi (usein ioni) Ligandit ympäröivät keskusatomia (symmetria) Ligandien vapaat elektroniparit keskeisiä, sitova elektronipari yhdeltä atomilta Keskusatomina yleensä siirtymäalkuaine (vajaa d-kuori) Esim 1. Hemoglobiinin hemiryhmä: 4 pyrrolirengasta Fe 2+ :lla 4 sidosta N-atomeihin
20 Fe yleensä oktaedraalisesti ligandoitu: 6 mahdollista sidossuuntaa ligandeille Porfyriinissa 4 ligandia Hemiryhmässä 1 sidos histidiiniin, 1 mahdollinen O 2 :een
21 21 Esim. 2. Kalsiumsensoriproteiinit Kalsiumin sitoutuminen EF-käsirakenteisiin ( EF hand ) Tyypillisesti 4 kalsiumsidospaikkaa/sensoriproteiini
22 Vetysidos Varattujen ja myös neutraalien molekyylien välillä Kaksi elektronegatiivista atomia jakaa vetyatomin: (vety)donori ja (vety)akseptori Donori voimakkaasti elektronegatiivinen dipoli, jossa vedyllä positiivista varausta Akseptorilla negatiivista varausta (vapaa elektronipari) attraktoi H Biologisissa systeemeissä: Donori = O tai N, jossa H kovalenttisesti Akseptori = O tai N
23 Sidosenergia kj/mol mev (vrt. kt 25 mev huoneenlämmössä) Vetysidoksen voimakkuus riippuu sidossuunnasta Lineaarinen sidos matalaenergisin: H kahden negat. varausjakauman välissä Sidospituudet suurempia kuin kovalenttisessa sidoksessa:
24 Biologisesti tärkeitä vetysidoksia: Vedessä ja biomolekyylien ryhmien ja vesimolekyylien välillä: Esim. OH-ryhmät, karbonyyliryhmät (C=O) Proteiinien aminohappojen välillä: DNA-ketjujen nukleotidien emästen välillä:
25 van der Waals vuorovaikutukset Dipolivuorovaikutuksia (pysyviä tai indusoitu); attraktiivinen Repulsio elektroniverhojen päällekkäisyydestä (Paulin kieltosääntö) Aina vaikuttamassa Heikko (~ 4 kj/mol) Jyrkkä etäisyysriippuvuus Merkittävä kahden molekyylin välillä vain, jos iso joukko atomeja vuorovaikuttamassa molekyylien 3-D rakenteen vastattava toisiaan (steerinen komplementaarisuus) spesifisyyttä, vaikka vdw-vuorovaikutus luonteeltaan epäspesifinen
26 Solujen molekulaariset rakennuspalikat 26 Ionit Vesi Lipidit Sokerit Na +
27 Vesi ja sen ominaisuudet 27 Vedellä anomaalisia ominaisuuksia Vetysidoksista O voimakkaasti elektronegatiivinen vetyatomielektronit kohti happea vedyistä vetysidosdonoreita Vapaat elektroniparit vetysidosakseptoreita Mahdollista 4 vetysidosta/molekyyli! Suuntariippuva Optimaalinen sidos ~ 5,5 kcal/mol H 2 O O: 6 elektronia 2 x H: 2 elektronia sp3-hybridisaatio 2 vapaata elektroniparia
28 Veden ominaisuudet 28 Vetysidos ko-operatiivinen Vetysidoksen muodostuminen alentaa toisen vetysidoksen muodostumiskynnystä
29 Veden fysikaalisia ominaisuuksia 29 Korkea dielektrisyysvakio, erittäin polaarinen liuotin; erottelee helposti varautuneet partikkelit Korkea sulamis- ja kiehumispiste sekä höyrystymislämpö jää < vesi (sama T ) Suuri pintajännitys Tiheyden lämpötilariippuvuus Maksimi n. 4 C:ssa Suuri johtavuus (likimain sama nesteenä ja kiinteänä!)
30 Kiinteä vesi: Jää 30 Jään rakenne lähellä 0 ºC Tetraedrirakenne kullakin H 2 O 4.0 lähinaapuria Hyvin pieni tilatäyttösuhde kiinteäksi aineeksi Harva rakenne onteloita, joihin mahtuu muita pieniä molekyylejä OH-sidospituus Å, jäässä O-O -etäisyys 2.76 Å
31 11.3 Nestemäinen vesi 31 Nesteet: Yleensä tiheys 5-15 % pienempi kuin kiinteässä faasissa Paine ei juuri vaikuta: p 2p pienentää tilavuutta vain n % Lämpötila: 1 K nosto kasvattaa tilavuutta 0.1 % molekyylien fluktuaatio voimakasta Rakennetietoa: Röntgendiffraktiomittaukset Neutronisirontamittaukset Radiaalinen jakaumafunktio g(r): ( r) N g( r) V Vesi 4 C, röntgendiffraktiomittaukset : Huippu r O-O = 2.82 Å:ssa: 4.4 lähinaapuria vrt. jää 4.0, nesteet yleensä 8-10 r O-O,vesi = 2.82 Å hiukan suurempi kuin r O-O,jää = 2.76 Å Huippu r = 3.7 Å? Huippu 4.5 Å: Kosinilause: c 2 a c 2 b abcos cos Å 4.5 Å
32 Solujen molekulaariset rakennuspalikat 32 Proteiinit DNA, RNA ATP, GTP
33 Nukleotidit, DNA 33 OH-ryhmä: ketjuttava sidos tähän Solussa yksittäisillä nukleotideilla usein 3 fosfaattiryhmää energiaa DNA/RNAsynteesiin Negatiivisia varauksia tasavälein: vastaionit!
34 DNA-rakenne vs. RNA-rakenne 34 DNA:lla kaksoiskierre, RNA:lla yksöiskierre
35 ATP, solujen energiavarasto 35 AMP, ADP, ATP (adenosiinimono-, -di-, -trifosfaatti) ATP-hydrolyysi vapauttaa noin 20 k B T fysiologisissa olosuhteissa Ihmisen ATP-tuotto päivässä n. 40 kg
36 Informaation kulku soluissa; solukalvo 36 Muodostaa kompartmentteja Keskeinen signaaliprosesseissa
37 Informaation kulku soluissa 37 Usein takaisinkytkentä geeniekspressioon
38 Informaation kulku soluissa; mrna-synteesi 38 Molekulaarinen moottori: RNA-polymeraasi RNA-polymeraasi ympäröi DNA-kaksoiskierteen Avaa DNA-kaksoiskierteen Liikkuu askel kerrallaan Syntetisoi lähetti-rna:n (mrna) Energia nukleotidien trifosfaatista
39 Informaation kulku soluissa; proteiinisynteesi 39 Translaatio ribosomeissa: 3 nukleotidia 1 aminohappo N. 50 eri proteiinia osallistuu, laskostuminen, kuljetus
40 Chapter 3. The Molecular Dance 40 Solut: Korkeasti järjestyneitä systeemeitä Terminen energia: Molekyylien satunnaisliike tuhoaa järjestystä Johtopäätös: Solut toimivat paremmin kylmässä? Biologinen kysymys: Miten nanomaailma poikkeaa makromaailmasta?
41 Chapter 3. The Molecular Dance 41 Solut: Korkeasti järjestyneitä systeemeitä Terminen energia: Molekyylien satunnaisliike tuhoaa järjestystä Johtopäätös: Solut toimivat paremmin kylmässä? Biologinen kysymys: Miten nanomaailma poikkeaa makromaailmasta? Fysikaalinen idea: Kaikki on termisessä liikkeessä
42 Jakaumista 42 Diskreetti jakauma: Muuttuja x saa diskreettejä arvoja x 1, x 2,... N riippumatonta tapausta: N 1 kpl x = x 1 N 2 kpl x = x 2 jne. Todennäköisyys tapaukselle x i on P(x i ), missä N N i Additiivisuus: Todennäköisyys tapaukselle, että havaitaan joko x i tai x j N i N N Normiointi: i Px j P( x ) suurilla N i P( x ) P( x ), x x i j i j N N... N N N 1 2 ( i) 1
43 Jatkuva jakauma: Muuttuja x jatkuva Todennäköisyys tapaukselle, että dn(x 0 ) mittausta saa arvon välillä [x 0, x 0 + dx], on 43 dn( x0) N P( x ) dx suurille 0 N Normiointi: P ( x ) dx 1 Normaalijakauma: 1 x x 2 2 P( x) e = 0,2 = 0,5 = 1
44 Muuttujan x odotusarvo (keskiarvo): x ( ) diskreetti xip xi i xp( x) dx jatkuva Funktion f(x) odotusarvo: ( ) ( ) diskreetti f xi P xi i f( x) f ( x) P( x) dx jatkuva 44 Muuttujan x varianssi: Keskihajonta: varianssi( ) x x x x x x x 2 keskihajonta (RMS)
45 Terminen liike: kineettinen kaasuteoria 45 Ideaalikaasulaki: pv Nk T nrt k T J pn nm N ideaalikaasupartikkelia kuutiossa (harva kaasu): mv Liikemäärä muuttuu törmäyksissä seinään: Törmäysten välinen aika (samaan seinään) per molekyyli: Seinään voima: (yhdestä molekyylistä) N molekyyliä: 21 B ( ) B r 4,1 10 4,1 vauhti jakautunut f ( mv ) 2mv mv t 2L L v 2 x x x x x mv x t 2L v x f p A 2 2 Nm vx Nm vx k 2 BT L L V m v 2 x
46 x y z ja 3 x v v v v v 46 kin E m v k T B Ideaalikaasupartikkelin keskim. kineettinen energia on 3 2 kt B Ei riipu (ideaali)kaasumolekyylien lajista eikä koosta Esim. N 2 huoneenlämmössä M(N 2 ) 28 g/mol v ,1 10 m 0,028 kg / mol / mol 21 kbt J m s
47 Esim. Minkä kokoiset (ideaalikaasu)partikkelit alkavat leijua huoneenlämmössä ilmassa, jos niiden tiheys on sama kuin veden? 47
48 Esim. Minkä kokoiset (ideaalikaasu)partikkelit alkavat leijua huoneenlämmössä ilmassa, jos niiden tiheys on sama kuin veden? 48 Potentiaalienergiaero lattian ja katon välillä U mg Vg k T 21 (3m) (3m) B r 4,1 10 J 4,1 10 J 4 V 3 r 1,4 10 m kg m ,81 3m 3 2 m s r 3nm Vrt. Vesimolekyylin r = 0,135 nm
49 Esim. Molekyylien liike solukalvossa 49 Translaatio 2-dim. Keskim. translaatioenergia / molekyyli = kt Molekyyleillä eri massa ja siten eri keskim. vauhti Ei ideaalikaasu: vuorovaikutuksia molekyylien välillä B
50 Molekyylien vauhtijakauma 50 Tähän asti vain keskimääräinen v 2 ; mikä on vauhtijakauma? Voidaan mitata: Tyhjiö: höyrystyneet metalliatomit eivät koe törmäyksiä kaasuatomeihin Höyrystetty metalli Thallium-höyry: 944 K ja 870 K redusoitu nopeus skaalaa T:n u u m kt 4 B
51 Boltzmann-jakauma 51 Ideaalikaasun molekyylien vauhdit normaalijakautuneet: Tasapainossa v 0 (muuten nettovirtaus) x kt m B 2 2 x vx vx x vx y z P( v ) x m 2 kt 2 x mv 2k T m P( vx, v y, vz ) e 2 kt B B v 2 x vx x P( vx) e todennäk. että x-suunt. v v 2 x e B mv 2k T B x
52 Boltzmann-jakauma 52 N toisistaan riippumattomasti liikkuvaa ideaalikaasumolekyyliä: N 1 2 N mv mv mv ½ m( v v... v ) 2kBT 2kBT 2kBT kbt ( 1, 2,..., N )... P v v v e e e e Ideaalikaasumolekyylit eivät vuorovaikuta: vain kineettistä energiaa E kbt P( tila) Boltzmann-jakauma e Pätee myös yleisesti, kun potentiaalienergiatermit U(x i ) tunnetaan Kun T 0, P(alin energiatila) 1
53 Aktivaatioenergiavalli 53 Aktivaatioon tarvitaan usein jokin minimienergia Esim. veden haihdutus: Nopeusjakauma kattilassa Aluksi tasapainossa kansi suljettuna ja eristettynä Kannen avaus: karannut jakaumaosa: e E k T Kannen sulkemisen jälkeen uusi tasapaino (katkoviiva) Yksinkert. kemiallisten reaktioiden nopeuden T-riippuvuus barrier B e E k T barrier B
54 Relaksaatio tasapainoon: 54 Kokonaisenergia ei muutu Energian jakautuminen partikkeleille muuttuu Törmäysten kautta Liikkeen järjestyksen aste muuttuu Mekaaninen energia termiseksi energiaksi: KITKA Järjestynyt liike satunnaisliikkeeksi Esim. Suihku korkeaenergisiä vesimolekyylejä veteen:
55 Molekyylien terminen liike 55 Translaatiot, värähtelyt, rotaatiot Värähtelyt: Atomit tasapainoasemansa ympärillä Rotaatiot: Koko molekyyli Molekyylin sisäiset -sidosten ympäri Molekyylin konformaatioenergia riippuu sidoskulmista Esim. Etaani CH 3 -CH 3
Luento Pääteemat: Vetysidos Veden ominaisuudet Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely
 Luento 0.1.017 1 Pääteemat: Vetysidos Veden ominaisuudet Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely Vetysidos Varattujen ja myös neutraalien molekyylien välillä Kaksi elektronegatiivista
Luento 0.1.017 1 Pääteemat: Vetysidos Veden ominaisuudet Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely Vetysidos Varattujen ja myös neutraalien molekyylien välillä Kaksi elektronegatiivista
Chapter 3. The Molecular Dance. Luento Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely
 Chapter 3. The Molecular Dance 1 Luento 15.1.016 Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely Chapter 3. The Molecular Dance Solut: Korkeasti järjestyneitä systeemeitä Terminen
Chapter 3. The Molecular Dance 1 Luento 15.1.016 Terminen liike Kineettinen kaasuteoria Boltzmann-jakauma Satunnaiskävely Chapter 3. The Molecular Dance Solut: Korkeasti järjestyneitä systeemeitä Terminen
NBE-C.2101 Biofysiikka
 NBE-C.2101 Biofysiikka Luennoitsija: Ari Koskelainen ari.koskelainen@aalto.fi puh. 050-3673768 Assistentit: Teemu Turunen, Ossi Kaikkonen etunimi.sukunimi@aalto.fi Kurssin tiedotus: MyCourses Oppimateriaali:
NBE-C.2101 Biofysiikka Luennoitsija: Ari Koskelainen ari.koskelainen@aalto.fi puh. 050-3673768 Assistentit: Teemu Turunen, Ossi Kaikkonen etunimi.sukunimi@aalto.fi Kurssin tiedotus: MyCourses Oppimateriaali:
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET
 HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
DNA:n informaation kulku, koostumus
 DNA:n informaation kulku, koostumus KOOSTUMUS Elävien bio-organismien koostumus. Vety, hiili, happi ja typpi muodostavat yli 99% orgaanisten molekyylien rakenneosista. Biomolekyylit voidaan pääosin jakaa
DNA:n informaation kulku, koostumus KOOSTUMUS Elävien bio-organismien koostumus. Vety, hiili, happi ja typpi muodostavat yli 99% orgaanisten molekyylien rakenneosista. Biomolekyylit voidaan pääosin jakaa
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
Luento 8 6.3.2015. Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit
 Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Nesteen sisäinen kitka ja diffuusio
 Nesteen sisäinen kitka ja diffuusio 1 Luento.1.016 (oppikirjan luku 4) Nesteen sisäinen kitka Satunnaiskävelyilmiöitä Diffuusio Diffuusio kalvon läpi Diffuusiotensorikuvaus: Magneettiresonanssi (MR) Hermoratojen
Nesteen sisäinen kitka ja diffuusio 1 Luento.1.016 (oppikirjan luku 4) Nesteen sisäinen kitka Satunnaiskävelyilmiöitä Diffuusio Diffuusio kalvon läpi Diffuusiotensorikuvaus: Magneettiresonanssi (MR) Hermoratojen
Entrooppiset voimat. Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit
 Entrooppiset voimat Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Entrooppiset voimat Entrooppiset voimat Vapaan energian muunnoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Kiteinen aine. Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne.
 Kiteinen aine Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne. Kiteinen aine on hyvä erottaa kiinteästä aineesta, johon kuuluu myös
Kiteinen aine Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne. Kiteinen aine on hyvä erottaa kiinteästä aineesta, johon kuuluu myös
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
, m s ) täytetään alimmasta energiatilasta alkaen. Alkuaineet joiden uloimmalla elektronikuorella on samat kvanttiluvut n,
 S-114.6, Fysiikka IV (EST),. VK 4.5.005, Ratkaisut 1. Selitä lyhyesti mutta mahdollisimman täsmällisesti: a) Keskimääräisen kentän malli ja itsenäisten elektronien approksimaatio. b) Monen fermionin aaltofunktion
S-114.6, Fysiikka IV (EST),. VK 4.5.005, Ratkaisut 1. Selitä lyhyesti mutta mahdollisimman täsmällisesti: a) Keskimääräisen kentän malli ja itsenäisten elektronien approksimaatio. b) Monen fermionin aaltofunktion
Alikuoret eli orbitaalit
 Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Luku 2: Atomisidokset ja ominaisuudet
 Luku 2: Atomisidokset ja ominaisuudet Käsiteltävät aiheet: Mikä aikaansaa sidokset? Mitä eri sidostyyppejä on? Mitkä ominaisuudet määräytyvät sidosten kautta? Chapter 2-1 Atomirakenne Atomi elektroneja
Luku 2: Atomisidokset ja ominaisuudet Käsiteltävät aiheet: Mikä aikaansaa sidokset? Mitä eri sidostyyppejä on? Mitkä ominaisuudet määräytyvät sidosten kautta? Chapter 2-1 Atomirakenne Atomi elektroneja
Luento 1: Sisältö. Vyörakenteen muodostuminen Molekyyliorbitaalien muodostuminen Atomiketju Energia-aukko
 Luento 1: Sisältö Kemialliset sidokset Ionisidos (suolat, NaCl) Kovalenttinen sidos (timantti, pii) Metallisidos (metallit) Van der Waals sidos (jalokaasukiteet) Vetysidos (orgaaniset aineet, jää) Vyörakenteen
Luento 1: Sisältö Kemialliset sidokset Ionisidos (suolat, NaCl) Kovalenttinen sidos (timantti, pii) Metallisidos (metallit) Van der Waals sidos (jalokaasukiteet) Vetysidos (orgaaniset aineet, jää) Vyörakenteen
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia
 Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Luento Sähköstaattiset vuorovaikutukset. Veden ominaisuudet Hydrofobinen vuorovaikutus. x = 0
 Luento 9 11.3.016 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
Luento 9 11.3.016 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Luento Sähköstaattiset vuorovaikutukset. Veden ominaisuudet Hydrofobinen vuorovaikutus. x = 0
 Luento 9 17.3.017 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
Luento 9 17.3.017 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
Kertausta 1.kurssista. KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä. Hiilen isotoopit
 KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 2: Kaasujen kineettistä teoriaa Pe 26.2.2016 1 AIHEET 1. Maxwellin-Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 2: Kaasujen kineettistä teoriaa Pe 26.2.2016 1 AIHEET 1. Maxwellin-Boltzmannin
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Orgaaninen reaktio Opettava tutkija Pekka M Joensuu Orgaaniset reaktiot Syyt Pelkkä törmäys ei riitä Varaukset (myös osittaisvaraukset) houkuttelevat molekyylejä
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Orgaaninen reaktio Opettava tutkija Pekka M Joensuu Orgaaniset reaktiot Syyt Pelkkä törmäys ei riitä Varaukset (myös osittaisvaraukset) houkuttelevat molekyylejä
Orgaanisten yhdisteiden rakenne ja ominaisuudet
 Orgaanisten yhdisteiden rakenne ja ominaisuudet 1 2 KOVALENTTISET SIDOKSET ORGAANISISSA YHDISTEISSÄ 3 4 5 6 7 Orgaanisissa molekyyleissä hiiliatomit muodostavat aina neljä kovalenttista sidosta Hiiliketju
Orgaanisten yhdisteiden rakenne ja ominaisuudet 1 2 KOVALENTTISET SIDOKSET ORGAANISISSA YHDISTEISSÄ 3 4 5 6 7 Orgaanisissa molekyyleissä hiiliatomit muodostavat aina neljä kovalenttista sidosta Hiiliketju
Chapter 4. Random Walks, Friction and Diffusion
 Chapter 4. Random Walks, Friction and Diffusion 1 Luento3 6.1.017 Diffuusiotensorikuvaus: Magneettiresonanssi (MR) Hermoratojen kuvantaminen Chapter 4. Random Walks, Friction and Diffusion Dissipaatio:
Chapter 4. Random Walks, Friction and Diffusion 1 Luento3 6.1.017 Diffuusiotensorikuvaus: Magneettiresonanssi (MR) Hermoratojen kuvantaminen Chapter 4. Random Walks, Friction and Diffusion Dissipaatio:
Sukunimi: Etunimi: Henkilötunnus:
 K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
Määritelmä, metallisidos, metallihila:
 ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
Biofysiikka Luento Entropia, lämpötila ja vapaa energia. Shannonin entropia. Boltzmannin entropia. Lämpötila. Vapaa energia.
 Biofysiikka Luento 7 1 6. Entropia, lämpötila ja vapaa energia Shannonin entropia Boltzmannin entropia M I NK P ln P S k B j1 ln j j Lämpötila Vapaa energia 2 Esimerkkiprobleemoita: Miten DNA-sekvenssistä
Biofysiikka Luento 7 1 6. Entropia, lämpötila ja vapaa energia Shannonin entropia Boltzmannin entropia M I NK P ln P S k B j1 ln j j Lämpötila Vapaa energia 2 Esimerkkiprobleemoita: Miten DNA-sekvenssistä
Kvanttimekaaninen atomimalli. "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman
 Kvanttimekaaninen atomimalli "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman Tunnin sisältö 1. 2. 3. 4. 5. 6. 7. Kvanttimekaaninen atomimalli Orbitaalit Kvanttiluvut Täyttymisjärjestys
Kvanttimekaaninen atomimalli "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman Tunnin sisältö 1. 2. 3. 4. 5. 6. 7. Kvanttimekaaninen atomimalli Orbitaalit Kvanttiluvut Täyttymisjärjestys
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
HEIKOT SIDOKSET. Heikot sidokset ovat rakenneosasten välisiä sidoksia.
 HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
Luento 8. Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli. Sähkönjohtavuus Druden malli
 Luento 8 Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli Sähkönjohtavuus Druden malli Klassiset C V -mallit Termodynamiikka kun Ei ennustetta arvosta! Klassinen
Luento 8 Lämpökapasiteettimallit Dulong-Petit -laki Einsteinin hilalämpömalli Debyen ääniaaltomalli Sähkönjohtavuus Druden malli Klassiset C V -mallit Termodynamiikka kun Ei ennustetta arvosta! Klassinen
Vanilliini (karbonyyliyhdiste) Etikkahappo (karboksyyliyhdiste)
 1 a) Määrittele karbonyyliyhdiste. Piirrä esimerkkirakennekaava ja nimeä se. Samoin määrittele karboksyyliyhdiste, piirrä esimerkkirakennekaava ja nimeä se. Toisen esimerkin tulee olla rakenteeltaan avoketjuinen,
1 a) Määrittele karbonyyliyhdiste. Piirrä esimerkkirakennekaava ja nimeä se. Samoin määrittele karboksyyliyhdiste, piirrä esimerkkirakennekaava ja nimeä se. Toisen esimerkin tulee olla rakenteeltaan avoketjuinen,
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
Biomolekyylit ja biomeerit
 Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Solun perusrakenne I Solun perusrakenne. BI2 I Solun perusrakenne 3. Solujen kemiallinen rakenne
 Solun perusrakenne I Solun perusrakenne 3. Solujen kemiallinen rakenne 1. Avainsanat 2. Solut koostuvat molekyyleistä 3. Hiilihydraatit 4. Lipidit eli rasva-aineet 5. Valkuaisaineet eli proteiinit rakentuvat
Solun perusrakenne I Solun perusrakenne 3. Solujen kemiallinen rakenne 1. Avainsanat 2. Solut koostuvat molekyyleistä 3. Hiilihydraatit 4. Lipidit eli rasva-aineet 5. Valkuaisaineet eli proteiinit rakentuvat
Voima ja potentiaalienergia II Energian kvantittuminen
 Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita
 Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita 10. Valkuaisaineiden valmistaminen solussa 1. Avainsanat 2. Perinnöllinen tieto on dna:n emäsjärjestyksessä 3. Proteiinit koostuvat
Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita 10. Valkuaisaineiden valmistaminen solussa 1. Avainsanat 2. Perinnöllinen tieto on dna:n emäsjärjestyksessä 3. Proteiinit koostuvat
Kemian opiskelun avuksi
 Kemian opiskelun avuksi Ilona Kuukka Mukana: Petri Järvinen Matti Koski Euroopan Unionin Kotouttamisrahasto osallistuu hankkeen rahoittamiseen. AINE JA ENERGIA Aine aine, nominatiivi ainetta, partitiivi
Kemian opiskelun avuksi Ilona Kuukka Mukana: Petri Järvinen Matti Koski Euroopan Unionin Kotouttamisrahasto osallistuu hankkeen rahoittamiseen. AINE JA ENERGIA Aine aine, nominatiivi ainetta, partitiivi
KE2 Kemian mikromaailma
 KE2 Kemian mikromaailma 30. maaliskuuta 2017/S.H. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Kopioi vastauspaperisi ensimmäisen sivun ylälaitaan seuraava taulukko. Kokeen pisteet
KE2 Kemian mikromaailma 30. maaliskuuta 2017/S.H. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Kopioi vastauspaperisi ensimmäisen sivun ylälaitaan seuraava taulukko. Kokeen pisteet
Kvanttifysiikan perusteet 2017
 Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Ionisidos ja ionihila:
 YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
Mitä elämä on? Astrobiologian luento 15.9.2015 Kirsi
 Mitä elämä on? Astrobiologian luento 15.9.2015 Kirsi Määritelmän etsimistä Lukemisto: Origins of Life and Evolution of the Biosphere, 2010, issue 2., selaile kokonaan Perintteisesti: vaikeasti määriteltävä
Mitä elämä on? Astrobiologian luento 15.9.2015 Kirsi Määritelmän etsimistä Lukemisto: Origins of Life and Evolution of the Biosphere, 2010, issue 2., selaile kokonaan Perintteisesti: vaikeasti määriteltävä
Tehtävä 2. Selvitä, ovatko seuraavat kovalenttiset sidokset poolisia vai poolittomia. Jos sidos on poolinen, merkitse osittaisvaraukset näkyviin.
 KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
1. a) Selitä kemian käsitteet lyhyesti muutamalla sanalla ja/tai piirrä kuva ja/tai kirjoita kaava/symboli.
 Kemian kurssikoe, Ke1 Kemiaa kaikkialla RATKAISUT Maanantai 14.11.2016 VASTAA TEHTÄVÄÄN 1 JA KOLMEEN TEHTÄVÄÄN TEHTÄVISTÄ 2 6! Tee marinaalit joka sivulle. Sievin lukio 1. a) Selitä kemian käsitteet lyhyesti
Kemian kurssikoe, Ke1 Kemiaa kaikkialla RATKAISUT Maanantai 14.11.2016 VASTAA TEHTÄVÄÄN 1 JA KOLMEEN TEHTÄVÄÄN TEHTÄVISTÄ 2 6! Tee marinaalit joka sivulle. Sievin lukio 1. a) Selitä kemian käsitteet lyhyesti
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 7: Ekvipartitioteoreema, partitiofunktio ja ideaalikaasu Ke 16.3.2016 1 KURSSIN
Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin.
 1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
Luku 8. Mekaanisen energian säilyminen. Konservatiiviset ja eikonservatiiviset. Potentiaalienergia Voima ja potentiaalienergia.
 Luku 8 Mekaanisen energian säilyminen Konservatiiviset ja eikonservatiiviset voimat Potentiaalienergia Voima ja potentiaalienergia Mekaanisen energian säilyminen Teho Tavoitteet: Erottaa konservatiivinen
Luku 8 Mekaanisen energian säilyminen Konservatiiviset ja eikonservatiiviset voimat Potentiaalienergia Voima ja potentiaalienergia Mekaanisen energian säilyminen Teho Tavoitteet: Erottaa konservatiivinen
782630S Pintakemia I, 3 op
 782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
Siirtymämetallien erityisominaisuuksia
 Siirtymämetallien erityisominaisuuksia MATERIAALIT JA TEKNOLOGIA, KE4 Sivuryhmien metallien kemiaa: Jaksojen (vaakarivit) 4 ja 5 sivuryhmien metalleista käytetään myös nimitystä d-lohkon alkuaineet, koska
Siirtymämetallien erityisominaisuuksia MATERIAALIT JA TEKNOLOGIA, KE4 Sivuryhmien metallien kemiaa: Jaksojen (vaakarivit) 4 ja 5 sivuryhmien metalleista käytetään myös nimitystä d-lohkon alkuaineet, koska
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
VESI JA VESILIUOKSET
 VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
kertausta edellisestä seuraa, että todennäköisimmin systeemi löydetään sellaisesta mikrotilasta, jollaisia on
 tavoitteet kertausta Tiedät mitä on Boltzmann-jakauma ja osaat soveltaa sitä Ymmärrät miten päädytään kaasumolekyylien nopeusjakaumaan Ymmärrät kuinka voidaan arvioida hiukkasen vapaa matka Kaikki mikrotilat,
tavoitteet kertausta Tiedät mitä on Boltzmann-jakauma ja osaat soveltaa sitä Ymmärrät miten päädytään kaasumolekyylien nopeusjakaumaan Ymmärrät kuinka voidaan arvioida hiukkasen vapaa matka Kaikki mikrotilat,
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 22.1.2015 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 22.1.2015 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
MUUTOKSET ELEKTRONI- RAKENTEESSA
 MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
1. Materiaalien rakenne
 1. Materiaalien rakenne 1.1 Johdanto 1. Luento 2.11.2010 1.1 Johdanto Materiaalit voidaan luokitella useilla eri tavoilla Kemiallisen sidoksen mukaan: metallit, keraamit, polymeerit Käytön mukaan: komposiitit,
1. Materiaalien rakenne 1.1 Johdanto 1. Luento 2.11.2010 1.1 Johdanto Materiaalit voidaan luokitella useilla eri tavoilla Kemiallisen sidoksen mukaan: metallit, keraamit, polymeerit Käytön mukaan: komposiitit,
ATOMIN JA IONIN KOKO
 ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
Molekyylit. Helsinki University of Technology, Laboratory of Computational Engineering, Micro- and Nanosciences Laboratory. Atomien väliset sidokset
 Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
Nimi sosiaaliturvatunnus. Vastaa lyhyesti, selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
Ydinfysiikkaa. Tapio Hansson
 3.36pt Ydinfysiikkaa Tapio Hansson Ydin Ydin on atomin mittakaavassa äärimmäisen pieni. Sen koko on muutaman femtometrin luokkaa (10 15 m), kun taas koko atomin halkaisija on ångströmin luokkaa (10 10
3.36pt Ydinfysiikkaa Tapio Hansson Ydin Ydin on atomin mittakaavassa äärimmäisen pieni. Sen koko on muutaman femtometrin luokkaa (10 15 m), kun taas koko atomin halkaisija on ångströmin luokkaa (10 10
Wien R-J /home/heikki/cele2008_2010/musta_kappale_approksimaatio Wed Mar 13 15:33:
 1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
Reaktiolämpö KINEETTINEN ENERGIA POTENTIAALI- ENERGIA
 POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
Chapter 7. Entropic forces at work
 Chapter 7. Entropic forces at work 1 Luento 8 4.3.2016 Osmoottinen paine Pintajännitys Tyhjennysvuorovaikutus MIKSI? Vapaa energia F a = E a -TS a voi pienentyä 1. Pienentämällä energiaa 2. Kasvattamalla
Chapter 7. Entropic forces at work 1 Luento 8 4.3.2016 Osmoottinen paine Pintajännitys Tyhjennysvuorovaikutus MIKSI? Vapaa energia F a = E a -TS a voi pienentyä 1. Pienentämällä energiaa 2. Kasvattamalla
Johdatus biofysiikkaan 15.1.2013 Introduction to biophysics 15.1.2013
 Johdatus biofysiikkaan 15.1.2013 Introduction to biophysics 15.1.2013 2nd lecture: Biophysics of biomolecules, by Marja Hyvönen please preferably contact me by email marja.hyvonen@oulu.fi p. 0294 481119
Johdatus biofysiikkaan 15.1.2013 Introduction to biophysics 15.1.2013 2nd lecture: Biophysics of biomolecules, by Marja Hyvönen please preferably contact me by email marja.hyvonen@oulu.fi p. 0294 481119
6. Entropia, lämpötila ja vapaa energia
 6. Entropia, lämpötila a vapaa energia 1 Luento 6 24.2.2017: Shannonin entropia M I NK P ln P 1 Boltzmannin entropia S k B ln Lämpötila Vapaa energia 2 Probleemoita: Miten DNA-sekvenssistä määräytyvän
6. Entropia, lämpötila a vapaa energia 1 Luento 6 24.2.2017: Shannonin entropia M I NK P ln P 1 Boltzmannin entropia S k B ln Lämpötila Vapaa energia 2 Probleemoita: Miten DNA-sekvenssistä määräytyvän
Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan?
 2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
YLEINEN KEMIA. Alkuaineiden esiintyminen maailmassa. Alkuaineet. Alkuaineet koostuvat atomeista. Atomin rakenne. Copyright Isto Jokinen
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
Biofysiikka, Luento
 Biofysiikka, Luento 4 3..017 1 Diffuusio eri geometrioissa ja sovelluksia Varattujen partikkelien diffuusio (elektrodiffuusio) Johdatus matalien Reynolds-lukujen maailmaan Aikariippuvat diffuusioprosessit
Biofysiikka, Luento 4 3..017 1 Diffuusio eri geometrioissa ja sovelluksia Varattujen partikkelien diffuusio (elektrodiffuusio) Johdatus matalien Reynolds-lukujen maailmaan Aikariippuvat diffuusioprosessit
ULKOELEKTRONIRAKENNE JA METALLILUONNE
 ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
11. MOLEKYYLIT. Kvanttimekaniikka on käyttökelpoinen molekyyleille, jos se pystyy selittämään atomien välisten sidosten syntymisen.
 11. MOLEKYYLIT Vain harvat alkuaineet esiintyvät luonnossa atomeina (jalokaasut). Useimmiten alkuaineet esiintyvät yhdisteinä: pieninä tai isoina molekyyleinä, klustereina, nesteinä, kiinteänä aineena.
11. MOLEKYYLIT Vain harvat alkuaineet esiintyvät luonnossa atomeina (jalokaasut). Useimmiten alkuaineet esiintyvät yhdisteinä: pieninä tai isoina molekyyleinä, klustereina, nesteinä, kiinteänä aineena.
Chem-C2400 Luento 2: Kiderakenteet Ville Jokinen
 Chem-C2400 Luento 2: Kiderakenteet 11.1.2019 Ville Jokinen Oppimistavoitteet Metalli-, ioni- ja kovalenttinen sidos ja niiden rooli metallien ja keraamien kiderakenteissa. Metallien ja keraamien kiderakenteen
Chem-C2400 Luento 2: Kiderakenteet 11.1.2019 Ville Jokinen Oppimistavoitteet Metalli-, ioni- ja kovalenttinen sidos ja niiden rooli metallien ja keraamien kiderakenteissa. Metallien ja keraamien kiderakenteen
SÄHKÖMAGNETISMI: kevät 2017
 SÄHKÖMAGNETISMI: kevät 2017 Viikko Aihe kirjan luku Viikko 1 Sähköken>ä, pistevaraukset 14 Viikko 2 Varausjakauman sähköken>ä 16 Viikko 2 Sähköinen poteniaalienergia ja poteniaali 17 Viikko 3 Sähköken>ä
SÄHKÖMAGNETISMI: kevät 2017 Viikko Aihe kirjan luku Viikko 1 Sähköken>ä, pistevaraukset 14 Viikko 2 Varausjakauman sähköken>ä 16 Viikko 2 Sähköinen poteniaalienergia ja poteniaali 17 Viikko 3 Sähköken>ä
8. Klassinen ideaalikaasu
 Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
Statistinen fysiikka, osa B (FYSA242) Tuomas Lappi tuomas.v.v.lappi@jyu.fi Huone: FL240. Ei kiinteitä vastaanottoaikoja. kl 2016 8. Klassinen ideaalikaasu 1 Fysikaalinen tilanne Muistetaan: kokeellisesti
L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA
 MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle Oppimistavoitteet
CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle Oppimistavoitteet
Luento 10. Potentiaali jatkuu, voiman konservatiivisuus, dynamiikan ja energiaperiaatteen käyttö, reaalinen jousi
 Luento 10 Potentiaali jatkuu, voiman konservatiivisuus, dynamiikan ja energiaperiaatteen käyttö, reaalinen jousi Tällä luennolla tavoitteena: Gravitaatio jatkuu Konservatiivinen voima Mitä eroa on energia-
Luento 10 Potentiaali jatkuu, voiman konservatiivisuus, dynamiikan ja energiaperiaatteen käyttö, reaalinen jousi Tällä luennolla tavoitteena: Gravitaatio jatkuu Konservatiivinen voima Mitä eroa on energia-
TASASUUNTAUS JA PUOLIJOHTEET
 TASASUUNTAUS JA PUOLIJOHTEET (YO-K06+13, YO-K09+13, YO-K05-11,..) Tasasuuntaus Vaihtovirran suunta muuttuu jaksollisesti. Tasasuuntaus muuttaa sähkövirran kulkemaan yhteen suuntaan. Tasasuuntaus toteutetaan
TASASUUNTAUS JA PUOLIJOHTEET (YO-K06+13, YO-K09+13, YO-K05-11,..) Tasasuuntaus Vaihtovirran suunta muuttuu jaksollisesti. Tasasuuntaus muuttaa sähkövirran kulkemaan yhteen suuntaan. Tasasuuntaus toteutetaan
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Hapot, Emäkset ja pk a Opettava tutkija Pekka M Joensuu Jokaisella hapolla on: Arvo, joka kertoo meille kuinka hapan kyseinen protoni on. Helpottaa valitsemaan
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Hapot, Emäkset ja pk a Opettava tutkija Pekka M Joensuu Jokaisella hapolla on: Arvo, joka kertoo meille kuinka hapan kyseinen protoni on. Helpottaa valitsemaan
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
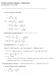 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
