Reaktiolämpö KINEETTINEN ENERGIA POTENTIAALI- ENERGIA
|
|
|
- Onni Karjalainen
- 6 vuotta sitten
- Katselukertoja:
Transkriptio
1 POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa, vapautuu energiaa varastointi tai käyttö (liikkuminen, ajattelu jne.). Kemiallisten reaktioiden kautta tuotettu lämpö- ja sähköenergia (jopa yli 90%) on peräisin kemiallisista reaktioista. Kemiallisen reaktion energian muutoksia tutkivaa osa-aluetta sanotaan termokemiaksi koska energia havaitaan yleensä lämmön siirtymisenä. Termokemia on osa termodynamiikkaa (kreikka: therme = lämpö ja dynamis = voima). Huom! Tarkasti ottaen käsitteet lämpö ja lämpöenergia ovat kaksi eri asiaa ja ne sekoitetaan usein keskenään. Lämpö( sisä)energia on tilasuure, lämpö ei. Lämpö on energia, joka siirtyy systeemin ja ympäristön välillä lämpötilaerojen seurauksena (atomitason törmäykset). Lämpöenergialla eli lämpömäärällä tarkoitetaan atomitason energiaa (molekyylien liike ja sidoksiin varastoitunut potentiaalienergia). Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli kineettistä energiaa. Kun kemiallinen reaktio tapahtuu eli aineet muuttuvat toisiksi aineiksi, liittyy siihen aina energiamuutoksia, jotka havaitaan: valona, lämpönä, entropian kasvuna. Sisäenergialla tarkoitetaan kaikkea mikrotason energiaa ja potentiaalienergialla kemiallista energiaa. 1
2 Määritelmä, kemiallinen reaktio: Kemiallinen reaktio on tapahtuma, jossa lähtöaineiden sisäiset sidokset katkeavat ja uusia sidoksia syntyy samalla, kun atomit järjestyvät uudelleen. Toisin sanoen syntyvät tuotteet ovat eri aineita kuin lähtöaineet. Ovatko olomuodon muutokset kemiallisia reaktioita? Vertaa heikkojen ja vahvojen sidosten katkeamisia ja uusien syntymisiä. Aineen rakenneosilla on sekä vahvoista että heikoista sidoksista aiheutuvaa potentiaalienergiaa että lämpöliikkeestä aiheutuvaa liike-energiaa (yht lämpöenergia). Koska reaktioissa sidoksia katkeaa ja uusia muodostuu, niin kemiassa usein riittää, että tarkastellaan vain rakenneosien heikkoihin ja vahvoihin sidoksiin varastoitunutta potentiaalienergiaa. Kemiallisessa reaktiossa ainetta ei häviä Aineen häviämättömyyden laki. Määritelmä, kemiallinen energia (kemiallisiin sidoksiin varastoitunut energia): Edellä esiteltyä potentiaalienergiaa kutsutaan kemialliseksi energiaksi ja se voi muuttua reaktioissa muiksi energian muodoiksi. Vahvat sidokset Ionisidos Metallisidos Kovalenttinen sidos Heikot sidokset Ioni-dipoli-sidos Dipoli-dipoli-sidos (vetysidos erikoistapauksena) Dispersiovoimat (van Der Waals, Londonin voimat) 2
3 Rakenneosien sidoksiin varastoitunut energia Energian muutoksia havainnollistetaan energiakaavioilla. Niihin piirretään lähtöaineiden ja reaktiotuotteiden energiatasot. Tasojen korkeusero kuvaa vapautuvan tai sitoutuvan energian määrän. Nuoli alaspäin kuvaa energian vapautumista ja nuoli ylöspäin energian sitoutumista. Jännittyneet molekyylit Palamisessa vapautuvan lämpöenergian määrän riippuvuus CH 2 -yksikköön varastoituneesta energiasta. 3
4 Molekyylien konformaatiot Jännitetyn jousen energia on potentiaalienergiaa. Jännittyneillä molekyyleillä on vastaavasti kemiallista energiaa. Rakenneosien liike-energia lämpöliike Jään molekyylihilassa vesimolekyylit värähtelevät. Vetysidokset pitävät molekyylit tiukasti kiinni toisissaan. Vedessä molekyylien väliset vetysidosverkostot muuttuvat jatkuvasti, kun vesimolekyylit liukuvat toistensa ohi. Vesihöyryssä vetysidokset ovat purkautuneet. Vesimolekyylit liikkuvat vapaasti. 4
5 ympäristö ympäristö Nesteen ja kaasun rakenneosilla on myös pyörimisestä johtuvaa liikeenergiaa (kaksois- ja kolmoissidokset ovat jäykkiä). Rakenneosilla on sidosten venytys- ja taivutusvärähtelystä johtuvaa liike- ja potentiaalienergiaa. Molekyylit myös keinahtelevat. Määritelmä, ekso- ja endoterminen reaktio: Jos kemiallinen reaktio vapauttaa lämpöä ympäristöön, sitä sanotaan eksotermiseksi reaktioksi. Havaitaan esimerkiksi reaktioastian lämpenemisenä. Vastaavasti, jos kemiallinen reaktio sitoo lämpöä ympäristöstä, sitä sanotaan endotermiseksi reaktioksi. Havaitaan reaktioastian kylmenemisenä. Kemiallisella systeemillä tarkoitetaan kemiallisen reaktion lähtöaineita ja reaktiotuotteita. Ympäristön muodostaa tällöin reaktioastia, vesiliuoksissa vesi, ilma jne. Sidosten katkeaminen on aina energiaa sitova eli endoterminen vaihe. Uusien sidosten muodostuminen puolestaan aina vapauttaa energiaa eli tämä on eksoterminen vaihe. Kemialliseen reaktioon liittyvä kokonaisenergian muutos voidaan siis ajatella näiden kahden vaiheen summana. 5
6 Käytännössä on mahdotonta mitata sidosten aukaisemiseen tarvittavaa tai muodostuvien sidosten vapauttamaa energiamäärää. Tämän vuoksi kemiallisten reaktioiden energiamuutoksia kuvataan entalpian muutoksella. Määritelmä, entalpia H lämpösisältö : Entalpia kuvaa aineen sisäenergiaa vakiopaineessa. Entalpia koostuu sidosten potentiaalienergiasta ja hiukkasten liike-energiasta. Reaktion entalpiamuutoksella eli lämpösisällön muutoksella, merkitään H, tarkoitetaan reaktiotuotteiden ja lähtöaineiden entalpia-arvojen erotusta, eli H = H reaktiotuotteet H lähtöaineet = H lopputila H alkutila Tietyn reaktion lähtöaineiden ja reaktiotuotteiden entalpian todellisia lukuarvoja ei voida mitata eikä laskea, mutta muutos H voidaan mitata kalorimetrillä. Kalorimetri on reaktioastia, joka on mahdollisimman hyvin eristetty, jotta systeemistä ei pääse karkaamaan lämpöä ympäristöön eikä ympäristöstä sitoudu lämpöä systeemiin. Eksotermisissä reaktioissa muodostuvien reaktiotuotteiden entalpia on pienempi kuin lähtöaineiden, jolloin energiaa siis vapautuu lämpönä ympäristöön. Entalpiamuutoksen arvo merkitään tällöin negatiivisena, eli H < 0. Endotermisissä reaktioissa tapahtuu toisinpäin eli energiaa sitoutuu ja tällaisille reaktioille H :n arvo merkitään positiivisena lukuna eli H > 0. Monet endotermiset reaktiot tapahtuvat vain jos systeemiä lämmitetään koko prosessin ajan! Näitä kuvataan usein energiakaavioilla. Huomaa, ettei pystyakselilla ole arvoja. 6
7 Esimerkki 2, käänteisten prosessien entalpian muutokset: Yleisesti aineiden (veden) höyrystyminen ja tiivistyminen sekä sulaminen ja jähmettyminen ovat käänteisiä prosesseja. Energian säilymislaista ja merkkisopimuksista seuraa, että käänteisten prosessien entalpioiden muutokset ovat lukuarvoltaan samat, mutta vastakkaismerkkiset. a) Veden höyrystymisentalpia 100 :ssa on +40,7 kj/mol ja tiivistymisentalpia 40,7 kj/mol. Sulamisentalpia 0 :ssa on +6,01 kj/mol ja jähmettymisentalpia 6,01 kj/mol. b) Magnesiumin palaminen 2 Mg s + O 2 g 2 MgO s, H = 1204 kj on eksoterminen reaktio, joten käänteisreaktio on endoterminen 2 MgO s 2 Mg s + O 2 g, H = kj c) Kidevedellisen natriumsulfaatin liukeneminen veteen Na 2 SO 4 H 2 O s 2 Na + aq + SO 4 2 aq, H = +79 kj on endoterminen reaktio, joten sen kiteytyminen on eksoterminen reaktio 2 Na + aq + SO 4 2 aq Na 2 SO 4 H 2 O s, H = 79 kj 7
8 Mistä entalpian muutos delta H riippuu? Tarkoilla mittauksilla on voitu osoittaa, että entalpian muutos H on kullekkin lämpökemialliselle muutokselle ominainen vakio, jonka lukuarvo riippuu seuraavista asioista: 1. Mittauslämpötilasta ja paineesta 2. Lähtöaineiden ja reaktiotuotteiden määristä 3. Lähtöaineiden ja reaktiotuotteiden olomuodoista 1. Mittauslämpötilasta ja paineesta Entalpian muutokset mitataan tavallisesti samassa lämpötilassa ja paineessa (25 = 298,15 K, 101,325 kpa) eli vertailu(standardi)olosuhteissa. Tämä helpottaa eri prosessien entalpiamuutosten vertaamista keskenään. Vertailuolosuhteissa mitatut entalpian muutokset ilmoitetaan kirjoittamalla H:n yläindeksiksi astemerkki H. Taulukkokirjoissa esitetyt entalpia-arvot ovat mitattu standardiolosuhteissa 25 = 298,15 K, 101,325 kpa, liuosten konsentraatiot 1,0 mol/l. Tämä merkitään tunnuksella H Lähtöaineiden ja reaktiotuotteiden määristä Entalpian muutokset ilmoitetaan yleensä reaktioyhtälön ilmoittamia ainemääriä kohti. Esimerkiksi vedyn palamista kuvaavasta reaktioyhtälöstä 2 H 2 g + O 2 g 2 H 2 O l, H = 572 kj voidaan lukea seuraavaa: Kun vertailuolosuhteissa 2 moolia kaasumaista vetyä ja 1 mooli kaasumaista happea reagoivat keskenään, syntyy 2 moolia nestemäistä vettä ja vapautuu 572 kj lämpöenergiaa. Laske entalpian muutos, kun 120 ml vetykaasua ja 150 ml happikaasua saatetaan reagoimaan keskenään NTP- olosuhteissa. Ratkaisu: Vedyn ja hapen ainemäärät: n H 2 = V V m = 0,120 l 22,41 l/mol = 5, mol Reaktioyhtälön perusteella n O 2 = V V m = 0,150 l 22,41 l/mol = 6, mol n H 2 n O 2 = 2 1 = 2. 8
9 Laskettujen ainemäärien suhde on n H 2 n O 2 = 5, mol 6, ,80 < 2, mol joten vety on rajoittava tekijä. Muodostuvan veden ainemäärä lasketaan vedyn ainemäärän kautta: n H 2 n H 2 O = 2 2 = 1 n H 2O = 5, mol. Entalpia-arvo oli kuitenkin annettu reaktiolle, jossa vettä muodostuu kaksi moolia. Näin ollen kysytyn reaktion entalpiamuutokseksi tulee H = 5, mol 572 kj 2,0 mol = 1,5315 kj 1,53 kj 3. Lähtöaineiden ja reaktiotuotteiden olomuodoista Myös olomuodon muutoksissa sitoutuu tai vapautuu lämpöenergiaa. Tämän takia reaktioyhtälöön pitää merkitä lähtöaineiden ja reaktiotuotteiden olomuodot. 2 H 2 g + O 2 g 2 H 2 O g, H = 484 kj 2 H 2 O g 2 H 2 O l, H = 88 kj 2 H 2 g + O 2 g 2 H 2 O l, H = 572 kj Ylimmässä palamisreaktiossa syntyy kaasuuntunutta vettä ja vapautuu 484 kj lämpöenergiaa. Alimmassa palamisreaktiossa syntyy nestemäistä vettä ja vapautuu 572 kj lämpöenergiaa. Erotus 88 kj johtuu siitä, että alimman reaktion reaktioentalpiassa on mukana myös veden tiivistyessä höyrystä nesteeksi vapautuva lämpöenergia (keskimmäinen reaktioyhtälö). Energiakaaviosta nähdään, miten vedyn palamisreaktion reaktioentalpia riippuu reaktiossa syntyvän veden olomuodosta. Jos reaktiossa syntyvä vesi on höyrynä, kahden kaasuuntuneen vesimoolin tiivistyessä vapautuva energia 88 kj ei ole mukana reaktioentalpian arvossa. 9
10 Esimerkki: Mitä tietoja seuraava lämpökemiallinen reaktioyhtälö välittää? Metaani CH 4 on maakaasun pääkomponentti. CH 4 g + 2 O 2 g CO 2 g + 2 H 2 O l, H = 890 kj Ratkaisu: 1) Kun 1 mooli (= 16,0 g) metaanikaasua palaa täydellisesti puhtaassa hapessa, se kuluttaa 2 moolia (= 64,0 g) happikaasua ja syntyy 1 mooli (= 44,0 g) kaasumaista hiilidioksidia ja 2 moolia (= 36,0 g) nestemäistä vettä. 2) Reaktio on eksoterminen. Lämpöä vapautuu 890 kj reaktioyhtälön ilmoittamia ainemääriä kohti. Reaktioentalpia on ilmoitettu standardiolosuhteissa. 3) Reaktio on eksoterminen, joten reaktiotuotteiden sidosten syntyessä vapautuu enemmän energiaa kuin lähtöaineiden sidosten purkautuessa. 4) Olomuodot on merkitty reaktioyhtälöön, koska myös olomuodon muutoksissa sitoutuu tai vapautuu merkittäviä lämpömääriä. Hessin laki eli Hessin sykli Energian säilymislain mukaan kemiallisessa reaktiossa energiaa ei häviä eikä sitä voi syntyä tyhjästä. Entalpialaskuissa tämä tunnetaan Hessin lakina. Määritelmä, Hessin laki: Kokonaisreaktion reaktioentalpia on osareaktioiden reaktioentalpioiden summa (suunnat huomioiden). Eli Hessin lain mukaan kemiallisen reaktion entalpiamuutos on aina sama riippumatta siitä, kuinka monen vaiheen kautta reaktiotuotteet ovat muodostuneet. Esimerkki: Tarkastellaan natriumvetykarbonaatin hajoamista natriumkarbonaatiksi, hiilidioksidiksi ja vedeksi: 1. 2 NaHCO 3 s Na 2 CO 3 s + CO 2 g + H 2 O l Tämän reaktion entalpiamuutosta H 1 ei voida suoraan määrittää, joten hyödynnetään Hessin lakia. 10
11 Tarvitaan seuraavat reaktiot syklin muodostamiseksi 2. Na 2 CO 3 s + 2 HCl aq 2 NaCl aq + CO 2 g + H 2 O l 3. NaHCO 3 s + HCl aq NaCl aq + CO 2 g + H 2 O l Nyt siis reaktiot 2. ja 3. antavat 1. :n, kun 3. kerrotaan kahdella ja otetaan 2. käänteisenä. Sykliksi tulee Ja H 1 = 2 H 3 H 2 TAI Nuolien suunnat huomioiden 2 H 3 = H 1 + H 2 josta H 1 = 2 H 3 H 2 Eli 2 NaHCO 3 s + 2 HCl aq 2 NaCl aq + 2 CO 2 g + 2 H 2 O l 2 NaCl aq + CO 2 g + H 2 O l Na 2 CO 3 s + 2 HCl aq 2 NaHCO 3 s Na 2 CO 3 s + CO 2 g + H 2 O l Nyt jos esimerkiksi ollaan punnittu natriumkarbonaattia 2,0757 g ja liuotettu se 2 M vetykloridihappoon V HCl = 30 ml 0,030 kg, jolloin T = 4,6 K, niin reaktion 2. reaktiolämmöksi tulee (käytetään veden ominaislämpökap.) H 2 = 4,19 kj 0,030 kg 4,6 K = 0,5782 kj kg K Ja entalpiamuutos yhtä natriumkarbonaattimoolia, M Na 2 CO 3 = 105,99 g/mol n Na 2 CO 3 = 0,019 mol, kohti on 0,5782 kj kj = 29,52 0, mol mol 11
12 Reaktio on eksoterminen, lämpöä vapautui ja H 2 30 kj mol. Ja jos ollaan punnittu natriumvetykarbonaattia 2,1064 g ja liuotettu se 2 M vetykloridihappoon V HCl = 30 ml 0,030 kg, jolloin T = 4,5 K, niin reaktion 3. reaktiolämmöksi tulee (käytetään veden ominaislämpökap.) H 3 = 4,19 kj 0,030 kg 4,5 K = 0,5657 kj kg K entalpiamuutos yhtä natriumvetykarbonaattimoolia, M NaHCO 3 = 84,008 g/mol n NaHCO 3 = 0,0250 mol, kohti on 0,5782 kj kj = 22,5613 0,02507 mol mol Koska reaktio on endoterminen, lämpöä sitoutui ja H kj mol. 12
13 Nyt voidaan Hessin syklin avulla määrittää reaktion 1. entalpiamuutos. Koska H 1 = 2 H 3 H 2 niin H 1 = 2 mol H 3 1 mol H 2 = 2 mol 22,561 kj mol 1 mol kj 29,52 mol Reaktio on siis endoterminen! = +74,64 kj 74 kj 13
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Bensiiniä voidaan pitää hiilivetynä C8H18, jonka tiheys (NTP) on 0,703 g/ml ja palamislämpö H = kj/mol
 Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Perjantai VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN
 Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
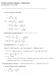 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
Törmäysteoria. Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa
 Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Reaktiosarjat
 Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Kohti entalpiamuutoksiin liittyviä laskuja
 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Kohti entalpiamuutoksiin liittyviä laskuja Ilona Linnavuori Kemian opettajankoulutusyksikkö, Helsingin yliopisto ilona.linnavuori@helsinki.fi Tiivistelmä
KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Kohti entalpiamuutoksiin liittyviä laskuja Ilona Linnavuori Kemian opettajankoulutusyksikkö, Helsingin yliopisto ilona.linnavuori@helsinki.fi Tiivistelmä
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta Insinöörivalinnan kemian koe MALLIRATKAISUT
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET
 HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
1. a) Selitä kemian käsitteet lyhyesti muutamalla sanalla ja/tai piirrä kuva ja/tai kirjoita kaava/symboli.
 Kemian kurssikoe, Ke1 Kemiaa kaikkialla RATKAISUT Maanantai 14.11.2016 VASTAA TEHTÄVÄÄN 1 JA KOLMEEN TEHTÄVÄÄN TEHTÄVISTÄ 2 6! Tee marinaalit joka sivulle. Sievin lukio 1. a) Selitä kemian käsitteet lyhyesti
Kemian kurssikoe, Ke1 Kemiaa kaikkialla RATKAISUT Maanantai 14.11.2016 VASTAA TEHTÄVÄÄN 1 JA KOLMEEN TEHTÄVÄÄN TEHTÄVISTÄ 2 6! Tee marinaalit joka sivulle. Sievin lukio 1. a) Selitä kemian käsitteet lyhyesti
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus KEMIALLISIIN REAKTIOIHIN PERUSTUVA POLTTOAINEEN PALAMINEN Voimalaitoksessa käytetään polttoaineena
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin?
 Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Vesi. Pintajännityksen Veden suuremman tiheyden nesteenä kuin kiinteänä aineena Korkean kiehumispisteen
 Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
KE03. Kurssikalvot. Tuomas Hentunen. Kevät Tuomas Hentunen KE03 Kevät / 26
 KE03 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE03 Kevät 2016 1 / 26 Reaktioyhtälöt ja niiden tasapainottaminen Kemiallista reaktiota kuvataan reaktioyhtälöllä reaktioyhtälöstä selviää:
KE03 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE03 Kevät 2016 1 / 26 Reaktioyhtälöt ja niiden tasapainottaminen Kemiallista reaktiota kuvataan reaktioyhtälöllä reaktioyhtälöstä selviää:
Kemia s2011 ratkaisuja. Kemian koe s 2011 lyhennettyjä ratkaisuja
 Kemian koe s 2011 lyhennettyjä ratkaisuja 1. a) Veden autoprotolyysin 2H 2 O(l) H 3 O + (aq) + OH (aq) seurauksena vedessä on pieni määrä OH ja H 3 O + ioneja, jotka toimivat varauksen kuljettajina. Jos
Kemian koe s 2011 lyhennettyjä ratkaisuja 1. a) Veden autoprotolyysin 2H 2 O(l) H 3 O + (aq) + OH (aq) seurauksena vedessä on pieni määrä OH ja H 3 O + ioneja, jotka toimivat varauksen kuljettajina. Jos
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Osa2. Kemiallinen reaktio
 Osa2. Kemiallinen reaktio 1. Kertoimien määrittäminen 2. Määrälliset laskut - massasuhdemenetelmä - moolimenetelmä 3. Palamisreaktiot 4. Lämpöenergia reaktioissa 5. Reaktionopeuteen vaikuttavia tekijöitä
Osa2. Kemiallinen reaktio 1. Kertoimien määrittäminen 2. Määrälliset laskut - massasuhdemenetelmä - moolimenetelmä 3. Palamisreaktiot 4. Lämpöenergia reaktioissa 5. Reaktionopeuteen vaikuttavia tekijöitä
Määritelmä, metallisidos, metallihila:
 ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Ainemäärien suhteista laskujen kautta aineiden määriin
 REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Lukion kemia 3, Reaktiot ja energia. Leena Piiroinen Luento 2 2015
 Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan?
 2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
HEIKOT SIDOKSET. Heikot sidokset ovat rakenneosasten välisiä sidoksia.
 HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Esimerkiksi ammoniakin valmistus typestä ja vedystä on tyypillinen teollinen tasapainoreaktio.
 REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot
 REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot Kertausta: Alun perin hapot luokiteltiin aineiksi, jotka maistuvat happamilta. Toisaalta karvaalta maistuvat
REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot Kertausta: Alun perin hapot luokiteltiin aineiksi, jotka maistuvat happamilta. Toisaalta karvaalta maistuvat
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka
 Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
MAOL:n pistesuositus kemian reaalikokeen tehtäviin syksyllä 2011.
 MAL:n pistesuositus kemian reaaikokeen tehtäviin syksyä 2011. - Tehtävän eri osat arvosteaan 1/3 pisteen tarkkuudea ja oppusumma pyöristetään kokonaisiksi pisteiksi. Tehtävän sisää pieniä puutteita voi
MAL:n pistesuositus kemian reaaikokeen tehtäviin syksyä 2011. - Tehtävän eri osat arvosteaan 1/3 pisteen tarkkuudea ja oppusumma pyöristetään kokonaisiksi pisteiksi. Tehtävän sisää pieniä puutteita voi
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Luku 2. Kemiallisen reaktion tasapaino
 Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
MUUTOKSET ELEKTRONI- RAKENTEESSA
 MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
YLEINEN KEMIA. Alkuaineiden esiintyminen maailmassa. Alkuaineet. Alkuaineet koostuvat atomeista. Atomin rakenne. Copyright Isto Jokinen
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
KE2 Kemian mikromaailma
 KE2 Kemian mikromaailma 30. maaliskuuta 2017/S.H. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Kopioi vastauspaperisi ensimmäisen sivun ylälaitaan seuraava taulukko. Kokeen pisteet
KE2 Kemian mikromaailma 30. maaliskuuta 2017/S.H. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Kopioi vastauspaperisi ensimmäisen sivun ylälaitaan seuraava taulukko. Kokeen pisteet
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Kertausta 1.kurssista. KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä. Hiilen isotoopit
 KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
Kaikki ympärillämme oleva aine koostuu alkuaineista.
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
ULKOELEKTRONIRAKENNE JA METALLILUONNE
 ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
1. Kemialliset reaktiot Kemiallisessa reaktiossa tapahtuu energiamuutoksia, kun sidoksia katkeaa ja uusia sidoksia muodostuu. Kemiallinen reaktio voi
 1. Kemialliset reaktiot Kemiallisessa reaktiossa tapahtuu energiamuutoksia, kun sidoksia katkeaa ja uusia sidoksia muodostuu. Kemiallinen reaktio voi tapahtua, kun lähtöaineiden molekyylit ja atomit törmäävät
1. Kemialliset reaktiot Kemiallisessa reaktiossa tapahtuu energiamuutoksia, kun sidoksia katkeaa ja uusia sidoksia muodostuu. Kemiallinen reaktio voi tapahtua, kun lähtöaineiden molekyylit ja atomit törmäävät
Kemian koe, KE3 Reaktiot ja energia RATKAISUT Maanantai VASTAA YHTEENSÄ VIITEEN TEHTÄVÄÄN
 Kemian koe, KE3 Reaktiot ja eneria RATKAISUT Sievin ukio Maanantai 9.1.2017 VASTAA YHTEENSÄ VIITEEN TEHTÄVÄÄN 1. A. Seitä käsitteet ja määritemät (yhyesti), isää tarvittaessa kemiainen merkintätapa: a)
Kemian koe, KE3 Reaktiot ja eneria RATKAISUT Sievin ukio Maanantai 9.1.2017 VASTAA YHTEENSÄ VIITEEN TEHTÄVÄÄN 1. A. Seitä käsitteet ja määritemät (yhyesti), isää tarvittaessa kemiainen merkintätapa: a)
Reaktioyhtälö. Sähköisen oppimisen edelläkävijä www.e-oppi.fi. Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava
 Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
W el = W = 1 2 kx2 1
 7.2 Elastinen potentiaalienergia Paitsi gravitaatioon, myös materiaalien deformaatioon (muodonmuutoksiin) liittyy systeemin rakenneosasten keskinäisiin paikkoihin liittyvää potentiaalienergiaa Elastinen
7.2 Elastinen potentiaalienergia Paitsi gravitaatioon, myös materiaalien deformaatioon (muodonmuutoksiin) liittyy systeemin rakenneosasten keskinäisiin paikkoihin liittyvää potentiaalienergiaa Elastinen
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus
 Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus HÖYRYTEKNIIKKA 1. Vettä (0 C) höyrystetään 2 bar paineessa 120 C kylläiseksi höyryksi. Laske
Mamk / Tekniikka ja liikenne / Sähkövoimatekniikka / Sarvelainen 2015 T8415SJ ENERGIATEKNIIKKA Laskuharjoitus HÖYRYTEKNIIKKA 1. Vettä (0 C) höyrystetään 2 bar paineessa 120 C kylläiseksi höyryksi. Laske
2. Reaktioyhtälö 3) CH 3 CH 2 COCH 3 + O 2 CO 2 + H 2 O
 2. Reaktioyhtälö 11. a) 1) CH 3 CH 2 OH + O 2 CO 2 + H 2 O Tasapainotetaan CH 3 CH 2 OH + O 2 CO 2 + H 2 O C, kpl 1+1 1 kerroin 2 CO 2 :lle CH 3 CH 2 OH + O 2 2 CO 2 + H 2 O H, kpl 3+2+1 2 kerroin 3 H
2. Reaktioyhtälö 11. a) 1) CH 3 CH 2 OH + O 2 CO 2 + H 2 O Tasapainotetaan CH 3 CH 2 OH + O 2 CO 2 + H 2 O C, kpl 1+1 1 kerroin 2 CO 2 :lle CH 3 CH 2 OH + O 2 2 CO 2 + H 2 O H, kpl 3+2+1 2 kerroin 3 H
Aineen olomuodot ja olomuodon muutokset
 Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
Aineen olomuodot ja olomuodon muutokset Jukka Sorjonen sorjonen.jukka@gmail.com 8. helmikuuta 2017 Jukka Sorjonen (Jyväskylän Normaalikoulu) Aineen olomuodot ja olomuodon muutokset 8. helmikuuta 2017 1
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Kemia s10 Ratkaisut. b) Kloorin hapetusluvun muutos: +VII I, Hapen hapetusluvun muutos: II 0. c) n(liclo 4 ) = =
 1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
Yhdisteiden nimeäminen
 Yhdisteiden nimeäminen Binääriyhdisteiden nimeäminen 1. Ioniyhdisteet 2. Epämetallien väliset yhdisteet Kompleksiyhdisteiden nimeäminen Kemiallinen reaktio 1. Reaktioyhtälö 2. Määrälliset laskut 3. Reaktionopeuteen
Yhdisteiden nimeäminen Binääriyhdisteiden nimeäminen 1. Ioniyhdisteet 2. Epämetallien väliset yhdisteet Kompleksiyhdisteiden nimeäminen Kemiallinen reaktio 1. Reaktioyhtälö 2. Määrälliset laskut 3. Reaktionopeuteen
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Molekyylibiotieteet/Bioteknologia Etunimet valintakoe Tehtävä 3 Pisteet / 30
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - hakukohde Sukunimi Molekyylibiotieteet/Bioteknologia Etunimet valintakoe 20.5.2013 Tehtävä 3 Pisteet / 30 3. Osa I: Stereokemia a) Piirrä kaikki
Luento 2: Lämpökemiaa, osa 1 Torstai klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
Alkuaineita luokitellaan atomimassojen perusteella
 IHMISEN JA ELINYMPÄRISTÖN KEMIAA, KE2 Alkuaineen suhteellinen atomimassa Kertausta: Isotoopin määritelmä: Saman alkuaineen eri atomien ytimissä on sama määrä protoneja (eli sama alkuaine), mutta neutronien
IHMISEN JA ELINYMPÄRISTÖN KEMIAA, KE2 Alkuaineen suhteellinen atomimassa Kertausta: Isotoopin määritelmä: Saman alkuaineen eri atomien ytimissä on sama määrä protoneja (eli sama alkuaine), mutta neutronien
ATOMIN JA IONIN KOKO
 ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia
 Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
7 Termodynaamiset potentiaalit
 82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
Näiden aihekokonaisuuksien opetussuunnitelmat ovat luvussa 8.
 9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
VESI JA VESILIUOKSET
 VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
Tehtävä 1. Tasapainokonversion laskenta Χ r G-arvojen avulla Alkyloitaessa bentseeniä propeenilla syntyy kumeenia (isopropyylibentseeniä):
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin.
 1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
Tehtävä 2. Selvitä, ovatko seuraavat kovalenttiset sidokset poolisia vai poolittomia. Jos sidos on poolinen, merkitse osittaisvaraukset näkyviin.
 KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
Kemialliset reaktiot. Yo-tehtäviä ratkaisuineen, Pietarsaaren lukio. 2.9.2009 Kemia 3
 2.9.2009 Kemia 3 Kemialliset reaktiot Yo-tehtäviä ratkaisuineen, Pietarsaaren lukio 2 Kemialliset reaktiot Yo-tehtäviä ratkaisuineen, Pietarsaaren lukio Sisältö Yo-kemia K07 t 2... 3 a) Kirjoita palamisreaktion
2.9.2009 Kemia 3 Kemialliset reaktiot Yo-tehtäviä ratkaisuineen, Pietarsaaren lukio 2 Kemialliset reaktiot Yo-tehtäviä ratkaisuineen, Pietarsaaren lukio Sisältö Yo-kemia K07 t 2... 3 a) Kirjoita palamisreaktion
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
