Kromatografian perusteet
|
|
|
- Niilo Aho
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 Kromatografian perusteet P Biokemian menetelmät I ja Juha Kerätär / BMTK Päivän aiheet Mitä on kromatografia? Taso- ja pylväskromatografian yleiset sovellukset biokemiassa. Opiskelija tietää ja osaa kertoa, mitä tarkoittavat kromatografiset menetelmät. Opiskelija ymmärtää kromatografisten menetelmien biokemiallisen taustan, ja osaa kertoa, mihin niitä voidaan käyttää. Kromatografiset menetelmät kromatografia Laboratoriotekniikoita, joilla seoksen aineet saadaan eroteltua toisistaan jonkin niiden ominaisuuden perusteella. Preparatiiviset kromatografiamenetelmät: aineiden erottelu toisistaan uusia kokeita varten. Analyyttiset kromatografiamenetelmät: aineiden erottelua jonkin ominaisuuden perusteella käytetään aineiden tutkimisen välineenä. Molekyylin tunnistaminen vertailemalla tuntematonta ainetta standardinäytteeseen. Eivät sulje toisiaan pois menetelmässä, jossa erotellaan seoksen aineet toisistaan ja kerätään ne talteen, voidaan saada myös analyyttista tietoa. 1
2 Esimerkki: proteiinin puhdistus kromatografialla Tutkittavaa proteiinia on tuotettu yhdistelmä- DNA:n avulla bakteerisoluissa. Bakteerisoluissa on tuotetun proteiinin lisäksi tuhansia erilaisia proteiineja. Rekombinanttiproteiinissa usein merkkihäntä (esim. His-tag) Proteiinit ominaisuuksiltaan yksilöitä: Aminohapposekvenssi, koko Kolmiulotteinen rakenne Pintavaraus ja sen riippuvuus liuoksen ph:sta Hydrofobisuus tai hydrofiilisyys Kyky tarttua spesifisesti kohdemolekyyliin (substraatti, toinen proteiini) Proteiinit toimivat usein komplekseina muiden proteiinien kanssa. Kullekin proteiinille on etsittävä yhdistelmä erilaisia (kromatografisia) menetelmiä, joilla muut proteiinit saadaan erotettua ja puhdistettava proteiini pysymään aktiivisena. Viimeisen puhdistusvaiheen jälkeen proteiinin tulee olla riittävän puhdas siihen käyttöön mihin se on tuotettu, ja sitä on oltava riittävästi tätä käyttöä varten. Esimerkiksi proteiinin tuotossa rakennetutkimukseen (kiteytykseen ja röntgenkristallografiaan): vähintään 10 mg erittäin puhdasta proteiinia. Kromatografian yleinen periaate Kromatografiassa tutkittava näyte on vuorovaikutuksessa kahden fysikaalisesti erilaisen materiaalin kanssa samanaikaisesti. Liikkuva faasi (mobile phase) Stationäärifaasi (stationary phase) eli paikallaan pysyvä faasi Tutkittava näyte lisätään liikkuvaan faasiin. Liikkuva faasi kuljettaa näytettä stationäärifaasin läheisyydessä. Kromatografian yleinen periaate Näytemolekyylien erilaiset vuorovaikutukset stationäärifaasin ja liikkuvan faasin kanssa ovat kromatografian perusta. Näytteen eri molekyyleillä voi olla erilainen affiniteetti stationäärifaasiin. (Affiniteetti = molekyylien taipumus olla vuorovaikutuksessa stationäärifaasin kanssa.) Jos molekyyli vuorovaikuttaa voimakkaasti stationäärifaasin kanssa liike kromatografiasysteemin läpi hidastuu. Jos molekyylin vuorovaikutus stationäärifaasin kanssa on heikko poistuu kromatografiasysteemistä eli eluoituu nopeammin. 2
3 ajosuunta Kromatografian tyypit Kromatografisia menetelmiä voidaan luokitella useilla eri perusteilla: Stationääri- ja liikkuvan faasin fysikaalinen olomuoto esim. este-neste, kiinteä-neste, neste-kaasu Erottumisen periaate adsorptio, partitio Stationääri- ja liikkuvan faasin kemialliset ominaisuudet esim. polaarinen, pooliton Stationäärifaasin muoto esim. taso, pylväs Menetelmän tarkoitus preparatiivinen, analyyttinen Stationäärifaasin fysikaalinen tai kemiallinen luonne ominaisuus, johon näytteen erottuminen perustuu Sama menetelmä voidaan luokitella usealla eri tavalla. Tällä kurssilla pääpaino taso- ja pylväskromatografiassa, sekä pylväskromatografian eri muotoihin stationäärifaasin ominaisuuksien perusteella jaoteltuna. Tasokromatografia (planar chromatography) Tyypillisesti paperi- ja ohutlevykromatografiaa (thin layer chromatography, TLC). Perustuu partitioon eli molekyylien väliseen sitoutumisvuorovaikutukseen. Molekyylit erottuvat, koska eri molekyyleillä on eri jakautumisperuste liikkuvan ja stationäärifaasin välillä. Näytemolekyylit jakautuvat kahden liuosfaasin välillä: stationäärifaasi on päällystetty nestemäisellä adsorbentilla. Paperikromatografiassa stationäärifaasina on selluloosaan sitoutunut vesi. Ohutlevykromatografiassa stationäärifaasina on liuos, jota on käytetty pintamateriaalin valmistukseen (usein vesi). Liikkuvan faasin polaariset molekyylit voivat sitoutua stationäärifaasiin. Näytteiden erottuminen perustuu niiden liukoisuuteen stationäärifaasin ja nestemäisen liikkuvan faasin välillä. Paperi- ja ohutlevykromatografian suoritus Tyypillisesti silikageelillä päällystetty lasilevy. Levylle voi piirtää lyijykynällä apuviivan ja pisteet pipetoimiseen noin 2 cm levyn alareunasta. Käsittele ohutlevyä suojakäsineet kädessä ja vain reunoihin koskien! Näyte on yleensä liuotettu helposti haihtuvaan liuottimeen. Pipetoidaan pieni määrä kerrallaan levyn alareunaan, annetaan liuottimen haihtua lisäysten välissä. Erotuskyky paras, kun näyte mahdollisimman pienellä alueella. Liikkuvia faaseja (ajoliuoksia) on olemassa useita erilaisia. Käytettävän ajoastian tulee olla tarpeeksi tiivis, jotta kaasuuntuva ajoliuos kyllästää ilman astian sisällä. Ajoastian pohjalla ei saa olla niin paljon ajoliuosta, että se koskettaisi (= liuottaisi) näytepisteet. 3
4 R f = ajoliuoksen kulkema matka näytepisteiden kulkemat matkat näytepisteen kulkema matka ajoliuoksen kulkema matka Ajoliuos kulkee ylöspäin ohutlevyllä kapillaari-ilmiön avulla. Erilaiset näytepisteeseen pipetoidut molekyylit liikkuvat eri nopeudella ohutlevyllä, riippuen levyn materiaalista ja ajoliuoksesta (= stationääri- ja liikkuvasta faasista) Ajo täytyy lopettaa ennen kuin ajoliuos saavuttaa ohutlevyn huipun. Merkitse ajoliuksen kulkema matka heti levylle. Jos näytemolekyylit eivät ole värillisiä, ohutlevy täytyy värjätä tai muuten visualisoida tutkittavat molekyylit (esim. lipidejä tutkittaessa kuivuneen levyn värjäys jodikammiossa). Ohutlevyllä kulkeutuneille näytepisteille lasketaan suhteellinen liikkuvuus R f (relative mobility, myös retention factor ): pisteen keskikohdasta laskettu kuljettu matka jaettuna ajoliuksen kulkemalla matkalla. Mihin paperi- ja ohutlevykromatografiaa käytetään? Tuntemattomien molekyylien tunnistaminen. Ajetaan tuntematon näyte yhtä aikaa erilaisten standardimolekyylien kanssa. Verrataan saatuja R f-arvoja kirjallisuudesta saatuihin arvoihin samalla kromatografiamenetelmällä. Molekyylin eristäminen näyteseoksesta. Tasokromatografiamenetelmien etuja: Tarvittava näytemäärä on pieni. Analyysin tekeminen on halpaa ja nopeaa. Näytteiden havainnointi kromatogrammilta suoraviivaista. Pienten molekyylien tunnistamiseen: erityisesti aminohappojen, sokerien ja rasvahappojen erottelu ja tunnistaminen. BMTK:ssa käytetään lähinnä harjoitustöissä. Tyhjä gravity flow pylväs (Bio-Rad) Pylväskromatografia Superdexgeelisuodatuspylväs (GE) HisTrap FF IMAC-pylväs (GE) Pylväskromatografiassa kiinteä stationäärifaasi on pakattu lasi-, muovi- tai metallipylvääseen ja nestemäisen liikkuvan faasin annetaan virrata pylvään läpi. Menetelmä perustuu yleensä näytemolekyylin adsorptioon stationäärifaasiin, eli suhteellisen spesifisiin, reversiibeleihin vuorovaikutuksiin näytemolekyylin ja stationäärifaasin välillä. Biokemiassa usein käytettyjä pylväskromatografian sovelluksia: - Ioninvaihtokromatografia (ion-exchange) - Affiniteettikromatografia (affinity chromatography) - Immobilisoitu metalli-ioni affiniteettikromatografia (IMAC) - Hydrofobinen vuorovaikutus kromatografia (HIC) - Geelisuodatus (gel filtration) Stationäärifaasi koostuu huokoisista, pienikokoisista pallomaisista partikkeleista, joita kutsutaan matriksiksi. - Matriksilla suuri pinta-ala enemmän mahdollisuutta vuorovaikuttaa liikkuvan faasin kanssa. 4
5 Pylväskromatografian suoritus Pylvään pakkaaminen Voidaan pakata itse kaupallisesta matriksista. Tutkimuksessa käytetään usein valmiiksi pakattua, kaupallista pylvästä. Tasapainotus Pylväs tasapainotetaan valuttamalla käytettävää liikkuvaa faasia (eluenttia, eluointipuskuria) sen läpi. Näytteen lataaminen Konsentroitu näyte siirretään pylvään yläpäähän ja annetaan näytteen sekä eluentin vuorovaikuttaa matriksin eli stationäärifaasin kanssa. Pylvään pesu Matriksiin epäspesifisesti sitoutuneet molekyylit irtoavat liikkuvan faasin mukana. Voidaan käyttää myös ominaisuuksiltaan poikkeavaa pesupuskuria. Näytteen eluointi Näytteen molekyyleillä erilainen vuorovaikutus matriksiin ja eluenttiin voivat ajautua pois pylväästä eri hetkillä ja siten fraktioida pieniin eriin. HPLC-laitteisto (high performance liquid chromatography). Tietokoneen kautta hallittavassa järjestelmässä, jossa on esimerkiksi pumppu, spektrofotometri ja fraktionkerääjä voidaan käyttää erilaisia kaupallisia tai käsin pakattuja pylväitä. Eluentti voi virrata pylvään läpi joko painovoiman avulla, tai voidaan käyttää pumppujärjestelmää. Näytteiden eluointiin pylväästä on erilaisia tapoja: Jatkuva eluutio: eluointipuskuri on koko ajan sama. Portaittainen eluutio: puskurin jotain ominaisuutta (esim. ph tai, komponentin konsentraatio) muutetaan portaittain. Asteittainen eluutio (gradientti): kaksi eluointiliuosta, joista toisen suhteellinen osuus kasvaa lineaarisesti. Fraktiot kerätään fraktionkerääjällä tai käsin omiin putkiinsa. - Esimerkki: Pylväs on pakattu 20 ml:lla matriksia. Pylvääseen ladataan pumpulla 1 ml näytettä, ja sen jälkeen näyte eluoidaan 40 ml:lla eluointipuskuria. Eluointipuskuri kerätään 1 ml fraktioina (= 40 x 1 ml putkea). Fraktioista ei juuri koskaan näe paljaalla silmällä näytemolekyylejä. Kromatografian etenemistä on seurattava jollain tapaa, tai näyte on muuten visualisoitava fraktioista. Spektrofotometria: Fraktioista mitataan absorbanssi halutulla aallonpituudella, tai eluoituva neste voi kulkea ennen fraktiokeräystä spektrofotometrin läpi. Esimerkiksi proteiinin puhdistumisen seuranta aallonpituudella 280 nm. Geelielektroforeesi: Näytteet (kiinnostavista) fraktioista tutkitaan tarkemmin geelielektroforeesilla. Entsyymiaktiivisuus: Fraktiot, joissa esimerkiksi puhdistettava, aktiivinen entsyymi esiintyy voidaan tunnistaa. Paperi- tai ohutlevykromatografia. Jos tarvitaan vain pieni määrä (µg) puhdistettua näytettä, pylväskromatografia voidaan tehdä myös ns. batchpuhdistuksena eppendorf-putkessa. - Matriksia µl. - Pesut ja eluutiot tehdään sentrifugoimalla. 5
6 Ioninvaihtokromatografia The Principle of Ion Exchange Chromatograpy (GE Life Sciences) Adsorptiokromatografian muoto, joka soveltuu varauksellisten molekyylien puhdistamiseen. Pylvääseen pakattu stationäärifaasi on synteettista materiaalia, johon on kovalenttisesti liitetty ionisia toiminnallisia ryhmiä. Liikkuvan faasin ja näytteen varaukselliset molekyylit muodostavat reversiibeleitä elektrostaattisia vuorovaikutuksia varautuneen stationäärifaasin kanssa. - Erimerkkisten varausten väliset vuorovaikutukset. - Dipoliset vuorovaikutukset. Matriksi, jossa on negatiivisesti varautuneita ryhmiä, sitoo positiivisesti varautuneita molekyylejä eli kationeja = kationinvaihtaja. Ioninvaihtajan eli stationäärifaasin valitseminen Stationäärifaasin valinta on yksinkertaista, jos tutkittavassa molekyylissä on vain yhdenlaisia varauksellisia ryhmiä. Biologisissa molekyyleissä kuitenkin usein sekä positiivisesti että negatiivisesti varautuneita ryhmiä. Proteiinille voidaan laskea sen aminohapposekvenssin perusteella isoelektrinen piste (pi). Jos ph = pi, proteiinimolekyylin nettovaraus on nolla. Jos liuoksen ph > pi: proteiini on negatiivisesti varautunut sitoutuu anioninvaihtajaan. Jos liuoksen ph < pi: proteiini on positiivisesti varautunut sitoutuu kationinvaihtajaan. Huomioitava kuitenkin, että proteiini on stabiili vain tietyllä ph-alueella! Puskurin eli liikkuvan faasin valitseminen Näytettä matriksiin sitoessa puskurin ioneilla tulisi olla sama varaus kuin matriksilla, jotta ne eivät tartu matriksiin ja laske sen sitomiskapasiteettia. Puskurin ionivahvuus ei saa olla liian suuri, koska korkeat ionivahvuudet häiritsevät puhdistettavan molekyylin ja pylväsmateriaalin välisiä vuorovaikutuksia. Puskurin ph valitaan alueelta, jossa erotettava molekyyli, esimerkiksi proteiini, on stabiili ja varautunut niin, että se sitoutuu matriksiin. Eluointi tapahtuu häiritsemällä matriksin ja sitoutuneen molekyylin vuorovaikutusta: Puskurin suolapitoisuuden nosto toistettavin tapa. ph:n muuttaminen tapauskohtaista, stabiilius! Usein käytetään gradienttieluutiota. 6
7 Ioninvaihtokromatografian periaate: anioninvaihtaja 1. Positiivisesti varautuneeseen matriksiin sitoutunut puskuriliuoksen negatiivisesti varautuneita ioneja. 2. Näyte ladataan pylvääseen. Näytteen molekyylit varautuneet positiivisesti, neutraalisti ja negatiivisesti. Varaus riippuu olosuhteista, mm. ph:sta. 3. Molekyylit, joilla on vastakkainen varaus matriksin kanssa, sitoutuvat stationäärifaasiin. Sitoutumisen voimakkuus riippuu varauksen suuruudesta. Neutraalit ja saman varauksen omaavat eivät sitoudu, vaan eluoituvat. Epäspesifisesti tai heikosti sitoutuneet molekyylit pestään pois. 4. Matriksi pestään puskurilla, jossa on suurempi ionivahvuus tai eri ph kuin näytettä sidottaessa. 5. Molekyylit, joiden varaus on nyt suurempi, syrjäyttävät sitoutuneen molekyylin matriksissa. Affiniteettikromatografia The Principle of Affinity Chromatograpy (GE Life Sciences) Affiniteettikromatografiassa molekyylien erottelu perustuu spesifisiin vuorovaikutuksiin stationäärifaasin ja näytemolekyylin välillä. Käytetään stationäärifaasia, johon puhdistettavan molekyylin ligandi on kovalenttisesti sidottu eli immobilisoitu. Jos molekyyli B saa molekyyli A:han spesifisesti sitoutuessaan aikaan biologisen vasteen sanotaan biokemiassa että molekyyli B on molekyyli A:n ligandi. (A + B A:B biologinen vaste) Käytetään mm. nukleiinihappojen ja erilaisten proteiinien (entsyymien, vastaaineiden, rekombinanttiproteiinien) eristämiseen ja puhdistamiseen. Pylväät tyypillisesti melko pieniä näytteen kokoon verrattuna vain murto-osa näytteen molekyyleistä sitoutuu pylvääseen. Affiniteettimatriksin valinta Affiniteettikromatografiassa käytetään kaupallisia matrikseja, joissa Valmis ligandi TAI Aktiivinen toiminnallinen ryhmä, johon oma ligandi voidaan liittää. Eivät sido epäspesifisiä molekyylejä. Fysikaalisesti ja kemiallisesti stabiileja erilaisissa olosuhteissa. Ligandi voidaan valita vasta kun tiedetään jotain tutkittavasta molekyylistä! Vuorovaikutuksen on oltava voimakas ja spesifinen, mutta reversiibeli tutkittavaan molekyyliin. Sisältää reaktiivisen ryhmän, joka voidaan sitoa matriksiin. Esimerkkejä: Vasta-aine + antigeeni Entsyymi + substraatti, inhibiittori, kofaktori tai substraattianalogi Lähetti-RNA + oligo (dt) 25 7
8 Ligandi ja siihen sitoutunut molekyyli vuorovaikuttavat vetysidosten sekä hydrofobisten ja kovalenttisten vuorovaikutusten kautta. Ligandin ja sitoutuneen molekyylin välisiä vuorovaikutuksia häiritään eluoinnin aikana: Epäspesifinen eluutio: ph:n muutos Ionivahvuuden muutos Molekyylin heikko denaturointi Spesifinen eluutio: Eluutiopuskuriin lisätään molekyyliä, joka kilpailee ligandin kanssa näytemolekyyliin sitoutumisesta tai näytemolekyylin kanssa ligandiin sitoutumisesta. Eluointi affiniteettipylväästä Affiniteettikromatografian suoritus 1. Ligandi sidotaan stationäärifaasiin 2. Molekyyli ladataan ja se sitoutuu ligandiinsa. 3. Molekyyli irrotetaan ligandista sitoutumisesta kilpailevalla molekyylillä. Affiniteettimatriksi (stationäärifaasi) pakataan pylvääksi (tai käytetään valmiiksi pakattua, kaupallista pylvästä). Näyte ladataan pylvääseen ja ajetaan sen läpi. Matriksin ligandien kanssa vuorovaikuttavat molekyylit sitoutuvat pylvääseen. Muut molekyylit tulevat ulos pylväästä. Pylvääseen kiinnittynyt molekyyli eluoidaan pylväästä häiritsemällä ligandin ja sitoutuneen molekyylin välisiä vuorovaikutuksia lisäämällä molekyyli, joka kilpailee ligandeista tai näytemolekyylistä. 6xHis Immobilisoitu metalliioni-affiniteettikromatografia (IMAC) PDB-rakenne 2BV9 rekombinanttiproteiinista, jossa histidiinihäntä. (Clostridium thermocellumin lichenaasi-entsymi). Affiniteettikromatografian alatyyppi, jossa proteiinija tai peptideitä erotellaan niiden erilaisen metalli-ioniin kohdistuvan affiniteetin perusteella. Kahdenarvoisia metalli-ioneja (Ni 2 +, Zn 2 +, Cu 2 +, jne.) immobilisoidaan pylvääseen kelaation avulla. Tietyt aminohapot (histidiini, kysteiini, tryptofaani) voivat muodostaa komplekseja kelatoitujen metalli-ionien kanssa neutraalissa ph:ssa. Proteiini eluoidaan laskemalla ph:ta, lisäämällä sitoutumisen kanssa kilpailevan molekyylin konsentraatiota, tai lisäämällä EDTA:ta. 8
9 IMAC:n käyttö IMAC:iaa käytetään yleisesti etenkin histidiinihännän sisältävien rekombinanttiproteiinien puhdistamisessa. Neljä nikkeli-ionin kuudesta sitoutumiskohdasta sitoutuneina matriksimateriaaliin. Jäljelle jäävät kaksi ovat vapaita sitoutumaan rekombinanttiproteiinin histidiinihäntään. Proteiinin eluointi: Imidatsolin lisääminen: natiivi eluointi, imidatsoli kilpailee sitoutumisesta histidiinin kanssa. ph:n lasku: denaturoiva eluointi Hydrofobinen vuorovaikutus kromatografia (HIC) The Principle of Hydrophobic Interaction Chromatograpy (GE Life Sciences) Hydrofobinen vuorovaikutuskromatografia (hydrophobic interaction chromatography) perustuu molekyylien, yleensä proteiinin, erotteluun hydrofobisten eli vesipakoisten vuorovaikutusten perusteella. Laskostuneen proteiinin pinnan rakenteet ovat tyypillisesti hydrofiilisiä (pääasiassa solulimassa olevat proteiinit ts. ei kalvoproteiinit). Niiden pinnalla on kuitenkin myös joitain hydrofobisia ryhmiä, ja HIC perustuu niiden vuorovaikutukseen matriksiin sidottujen hydrofobisten ryhmien kanssa. Proteiinin pinnan hydrofobiset alueet johtuvat ei-polaarisista aminohapoista (Ala, Phe, Val, Trp, Leu, Ile, Met), niiden määrä ja luonne on kullekin proteiinille ominainen. HIC:n käyttö Proteiininäyte laitetaan pylvääseen korkeassa suolapitoisuudessa (vertaa miten ioninvaihtokromatografiassa!). Korkea suolapitoisuus (esim. Na 2 SO 4, NaCl tai (NH 4 ) 2 SO 4 ) syrjäyttää proteiinin hydrofobisten alueiden ja matriksin hydrofobisten ryhmien ympärillä järjestyneitä vesimolekyylejä, kasvattaen hydrofobisia vuorovaikutuksia. Proteiinit eluoidaan pylväästä: Laskemalla suolapitoisuutta Muuttamalla jollain muulla tavalla liikkuvan faasin polaarisuutta (detergentit, orgaaniset liuottimet) Muuttamalla ph:ta HIC on mieto puhdistusmenetelmä proteiini säilyy natiivimuodossaan. Käytetään usein rekombinanttiproteiinien puhdistamisessa rakennetutkimuksia varten. 9
10 Geelisuodatuskromatografia poikkeaa muista kromatografiamenetelmistä siinä, että näytteen molekyylien erottelu perustuu ainoastaan niiden kokoon. The Principle of Gel Filtration Chromatography (GE Life Sciences) Ei biokemiallisia vuorovaikutuksia molekyylien, liikkuvan faasin ja stationäärifaasin välillä. Kirjallisuudessa useita nimiä: gel filtration, gel exclusion, molecular sieve, gel permeation chromatography (GPC). Soveltuu laajalle kirjolle erikokoisia molekyylejä kymmenistä useisiin miljooniin Da. Voidaan käyttää proteiinien, nukleiinihappojen, polysakkaridien ja muiden biomolekyylien puhdistamiseen. Geelisuodatuskromatografia Geelisuodatuksen suoritus Stationäärifaasi koostuu pienistä, inerteistä varauksettomista partikkeleista, joissa on kontrolloidun kokoisia reikiä. Mikroskooppikuvassa näyttävät pesusieneltä. Liikkuva faasi on koko ajan samanlainen, eikä kromatografiassa ole pesuvaihetta. Liikkuvan faasin ainoa tehtävä on kuljettaa näyte pylvään läpi. Molekyylien eluutiotilavuus (missä eluutiopuskurin tilavuudessa ne tulevat ulos pylväästä) on suoraan suhteessa niiden molekyylipainoon ja muotoon. Molekyylit, joiden koko on suurempi kuin partikkelien reiät, kulkeutuvat nopeammin pylvään läpi, ja siten niiden eluutiotilavuus on pienempi. Pienemmät molekyylit pääsevät matriksin partikkelin sisään, mikä hidastaa niiden kulkeutumista, jolloin niiden eluutiotilavuus on suurempi. Geelisuodatuksen käyttötarkoituksia Suolan poisto (desalting). Geelisuodatuksella voidaan poistaa näytteessä olevat epäorgaaniset suolot, orgaaniset liuottimet tai muut pienet molekyylit. Voivat esimerkiksi haitata seuraavaa työvaihetta tai jatkotutkimuksia. Voidaan käyttää valmiiksi pakattuja, pieniä pylväitä, joiden läpi näyte eluoidaan painovoimalla tai sentrifugilla. Biomolekyylien puhdistaminen Käytetyin geelisuodatuksen sovellutus. Usein proteiinien puhdistuksen viimeinen vaihe, jolla saadaan homogeeninen näyte esimerkiksi rakennetutkimukseen (esim. dimeerisen proteiinin aktiivinen muoto). 10
11 A) hemoglobiini Da B) ovalbumiini Da C) kymotrypsinogeeni Da D) myoglobiini Da E) sytokromi c Da Standardit eluoidaan pylväästä. Jakaantumiskertoimen avulla piirretty standardisuora Eluutiotilavuus vs molekyylipaino Molekyylipainon (M r) määrittäminen: Molekyylin eluutiotilavuus on suhteessa vain molekyylin kokoon. Standardimolekyylit ajetaan ensin pylvään läpi, jolloin saadaan eluutiotilavuudet V e tietyn kokoisille molekyyleille. Blue dextraanin (M w=2 MDa) avulla määritetään pylvään tyhjätilavuus V 0. Pylvään kokonaistilavuus V t lasketaan matemaattisesti. Kunkin standardimolekyylin eluutiotilavuudelle määritetään jakaantumiskerroin K: K = (V e-v 0)/(V t-v 0) Jakaantumiskerroin K kuvaa sitä osuutta matriksista, jonka sisällä näytemolekyyli kykenee liikkumaan. Standardimolekyylien jakaantumiskertoimien ja molekyylikokojen perusteella piirretään standardikuvaaja, jolta voi määrittää tutkittavan näytteen eluutiotilavuutta vastaavan jakautumiskertoimen perusteella sen molekyylikoon. 11
Kromatografian perusteet
 Kromatografian perusteet 740151P Biokemian menetelmät I 2.10. ja 9.10. Juha Kerätär / BMTK Päivän aiheet Mitä on kromatografia? Taso- ja pylväskromatografian yleiset sovellukset biokemiassa. Opiskelija
Kromatografian perusteet 740151P Biokemian menetelmät I 2.10. ja 9.10. Juha Kerätär / BMTK Päivän aiheet Mitä on kromatografia? Taso- ja pylväskromatografian yleiset sovellukset biokemiassa. Opiskelija
Seosten erotusmenetelmiä
 Seosten erotusmenetelmiä KEMIAA KAIKKIALLA, KE1 Kemiassa on usein tarve erottaa niin puhtaita aineita kuin myös seoksia toisistaan. Seoksesta erotetaan sen komponentteja (eli seoksen muodostavia aineita)
Seosten erotusmenetelmiä KEMIAA KAIKKIALLA, KE1 Kemiassa on usein tarve erottaa niin puhtaita aineita kuin myös seoksia toisistaan. Seoksesta erotetaan sen komponentteja (eli seoksen muodostavia aineita)
KROMATOGRAFIAN PERUSTEET
 KROMATOGRAFIAN PERUSTEET Outi Itkonen Sairaalakemisti, dos. HUSLAB 5.2.2015 O. Itkonen 1 KROMATOGRAFIA χρῶμα chroma väri" γράφειν graphein kirjoittaa alan uranuurtajat Archer John Porter Martin ja Richard
KROMATOGRAFIAN PERUSTEET Outi Itkonen Sairaalakemisti, dos. HUSLAB 5.2.2015 O. Itkonen 1 KROMATOGRAFIA χρῶμα chroma väri" γράφειν graphein kirjoittaa alan uranuurtajat Archer John Porter Martin ja Richard
Tenttipäivät. Tentti TI :30-17:30 1. uusinta MA :30-17:30 2. uusinta MA :30-17:30
 Tenttipäivät Tentti TI 14.11. 14:30-17:30 1. uusinta MA 11.12. 14:30-17:30 2. uusinta MA 30.1.2018 14:30-17:30 Jos on joku iso päällekkäisyys (= tutkinnon pakollisen kurssin pakollinen läsnäolo, esimerkiksi
Tenttipäivät Tentti TI 14.11. 14:30-17:30 1. uusinta MA 11.12. 14:30-17:30 2. uusinta MA 30.1.2018 14:30-17:30 Jos on joku iso päällekkäisyys (= tutkinnon pakollisen kurssin pakollinen läsnäolo, esimerkiksi
Biokemian labrameiningit I harjoitustyöosuus. Arne Raasakka, 20.10.2007 Työ suoritettu: 12. 13.10.2007 arne.raasakka@oulu.fi
 Työ 1. Rekömbinanttipröteiinin puhdistaminen Ni-NTA affiniteettikrömatögrafialla seka pröteiinin mölekyylipainön ma a ritys elektröföreesilla ja geelisuödatuskrömatögrafialla Biokemian labrameiningit I
Työ 1. Rekömbinanttipröteiinin puhdistaminen Ni-NTA affiniteettikrömatögrafialla seka pröteiinin mölekyylipainön ma a ritys elektröföreesilla ja geelisuödatuskrömatögrafialla Biokemian labrameiningit I
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET
 HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1)
 MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
ALKOHOLIT SEKAISIN KOHDERYHMÄ:
 ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
ALKOHOLIT SEKAISIN TAUSTAA
 ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
10.9.2015 Pipetointi, sentrifugointi ja spektrofotometria
 BIOKEMIAN MENETELMÄT I, SYKSY 2015 VASTAUKSET LUENTOMATERIAALIN TEHTÄVIIN: 10.9.2015 Pipetointi, sentrifugointi ja spektrofotometria Pesukoneen g-voimat: RCF (x g) = 1,119 10-5 (rpm)2 r = roottorin säde
BIOKEMIAN MENETELMÄT I, SYKSY 2015 VASTAUKSET LUENTOMATERIAALIN TEHTÄVIIN: 10.9.2015 Pipetointi, sentrifugointi ja spektrofotometria Pesukoneen g-voimat: RCF (x g) = 1,119 10-5 (rpm)2 r = roottorin säde
ROMUMETALLIA OSTAMASSA (OSA 1)
 ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA
 ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
L10 Polyelektrolyytit pinnalla
 CHEM-2230 Pintakemia L10 Polyelektrolyytit pinnalla Monika Österberg Polyelektrolyyttiadsorptio (mg/m 1 0.5 2 ) C Muistatteko kemisorption ja fysisorption ero? Adsorptiota kuvataan adsorptioisotermin avulla
CHEM-2230 Pintakemia L10 Polyelektrolyytit pinnalla Monika Österberg Polyelektrolyyttiadsorptio (mg/m 1 0.5 2 ) C Muistatteko kemisorption ja fysisorption ero? Adsorptiota kuvataan adsorptioisotermin avulla
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia)
 ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan?
 2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
CHEM-A1310 Biotieteen perusteet 2018
 CHEM-A1310 Biotieteen perusteet 2018 Laboratoriodemojen teoriaosuus Huomaa: Jokaisesta suorittamatta jääneestä demokerrasta vähennetään 0.75 pistettä tentin kokonaispisteistä. Rästikertojen jälkeen suoritukset
CHEM-A1310 Biotieteen perusteet 2018 Laboratoriodemojen teoriaosuus Huomaa: Jokaisesta suorittamatta jääneestä demokerrasta vähennetään 0.75 pistettä tentin kokonaispisteistä. Rästikertojen jälkeen suoritukset
Proteiinipuhdistus. Johdanto. www.edu.fi/biogeeni
 Proteiinipuhdistus Johdanto Proteiinien jälkikäsittely on monimuotoinen, usein myös vaikeahko ja kalliskin laji. Haastetta hommassa riittääkin jos esimerkiksi E.Colin tuottamista tuhansista proteiineista
Proteiinipuhdistus Johdanto Proteiinien jälkikäsittely on monimuotoinen, usein myös vaikeahko ja kalliskin laji. Haastetta hommassa riittääkin jos esimerkiksi E.Colin tuottamista tuhansista proteiineista
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
Ionisidos ja ionihila:
 YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
Henkilötunnus - Biokemian/bioteknologian valintakoe. Sukunimi Etunimet Tehtävä 1 Pisteet / 20
 elsingin yliopisto/tampereen yliopisto enkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24. 5. 2004 Etunimet Tehtävä 1 Pisteet / 20 Solujen kalvorakenteet rajaavat solut niiden ulkoisesta ympäristöstä
elsingin yliopisto/tampereen yliopisto enkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24. 5. 2004 Etunimet Tehtävä 1 Pisteet / 20 Solujen kalvorakenteet rajaavat solut niiden ulkoisesta ympäristöstä
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA TAUSTAA Pehmeä vesi on hyvän pesutuloksen edellytys. Tavallisissa pesupulvereissa fosfori esiintyy polyfosfaattina, joka suhteellisen nopeasti hydrolisoituu vedessä ortofosfaatiksi.
FOSFORIPITOISUUS PESUAINEESSA TAUSTAA Pehmeä vesi on hyvän pesutuloksen edellytys. Tavallisissa pesupulvereissa fosfori esiintyy polyfosfaattina, joka suhteellisen nopeasti hydrolisoituu vedessä ortofosfaatiksi.
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
Kasvien piilotetut väriaineet
 KOHDERYHMÄ: Työ sopii parhaiten lukioon kursseille KE1 tai KE2. Työn voi tehdä myös yläkoululaisten kanssa kurssilla raaka-aineet ja tuotteet, jolloin keskitytään poolittomuuden sijaan erotusmenetelmiin.
KOHDERYHMÄ: Työ sopii parhaiten lukioon kursseille KE1 tai KE2. Työn voi tehdä myös yläkoululaisten kanssa kurssilla raaka-aineet ja tuotteet, jolloin keskitytään poolittomuuden sijaan erotusmenetelmiin.
EPIONEN Kemia 2015. EPIONEN Kemia 2015
 EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
METABOLISTEN SAIRAUKSIEN ANALYTIIKAN JÄRJESTÄMINEN NORDLAB OULUSSA. Marja-Kaisa Koivula Sairaalakemisti, FT, dosentti
 METABOLISTEN SAIRAUKSIEN ANALYTIIKAN JÄRJESTÄMINEN NORDLAB OULUSSA Marja-Kaisa Koivula Sairaalakemisti, FT, dosentti Esityksen sisältö Johdanto Kromatografiset menetelmät Entsymaattinen määritysmenetelmä
METABOLISTEN SAIRAUKSIEN ANALYTIIKAN JÄRJESTÄMINEN NORDLAB OULUSSA Marja-Kaisa Koivula Sairaalakemisti, FT, dosentti Esityksen sisältö Johdanto Kromatografiset menetelmät Entsymaattinen määritysmenetelmä
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo
 Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo 15.3.2017 Kationinvaihtokapasiteetti Ca 2+ K + Mg 2+ Kationi = Positiivisesti varautunut ioni Kationinvaihtokapasiteetti
Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo 15.3.2017 Kationinvaihtokapasiteetti Ca 2+ K + Mg 2+ Kationi = Positiivisesti varautunut ioni Kationinvaihtokapasiteetti
Puhtaat aineet ja seokset
 Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Solun perusrakenne I Solun perusrakenne. BI2 I Solun perusrakenne 3. Solujen kemiallinen rakenne
 Solun perusrakenne I Solun perusrakenne 3. Solujen kemiallinen rakenne 1. Avainsanat 2. Solut koostuvat molekyyleistä 3. Hiilihydraatit 4. Lipidit eli rasva-aineet 5. Valkuaisaineet eli proteiinit rakentuvat
Solun perusrakenne I Solun perusrakenne 3. Solujen kemiallinen rakenne 1. Avainsanat 2. Solut koostuvat molekyyleistä 3. Hiilihydraatit 4. Lipidit eli rasva-aineet 5. Valkuaisaineet eli proteiinit rakentuvat
POHDITTAVAKSI ENNEN TYÖTÄ
 MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
Alikuoret eli orbitaalit
 Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Biomolekyylit ja biomeerit
 Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biokemian menetelmät I kurssi, työselostukset, kevät 2016.
 Biokemian menetelmät I kurssi, työselostukset, kevät 2016. DEADLINET: työselostus tulostettuna paperille Työ 3: To 24.3.2016 klo 15:00 KE1132:n palautuspiste tai BMTK:n Työ 2: Pe 1.4.2016 klo 16:00 KE1132:n
Biokemian menetelmät I kurssi, työselostukset, kevät 2016. DEADLINET: työselostus tulostettuna paperille Työ 3: To 24.3.2016 klo 15:00 KE1132:n palautuspiste tai BMTK:n Työ 2: Pe 1.4.2016 klo 16:00 KE1132:n
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt
 KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
ELEC-C2210 Molekyyli- ja solubiologia
 ELEC-C2210 Molekyyli- ja solubiologia Entsyymikatalyysi Vuento & Heino ss. 66-75 ECB: Luku 3, s. 90-93 & luku 4, s. 144- Dos. Tuomas Haltia, Biotieteiden laitos, biokemia ja biotekniikka Miten entsyymit
ELEC-C2210 Molekyyli- ja solubiologia Entsyymikatalyysi Vuento & Heino ss. 66-75 ECB: Luku 3, s. 90-93 & luku 4, s. 144- Dos. Tuomas Haltia, Biotieteiden laitos, biokemia ja biotekniikka Miten entsyymit
VESI JA VESILIUOKSET
 VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä. FT Satu Ikonen, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola
 Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Luento 8 6.3.2015. Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit
 Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
SÄHKÖ KÄSITTEENÄ. Yleisnimitys suurelle joukolle ilmiöitä ja käsitteitä:
 FY6 SÄHKÖ Tavoitteet Kurssin tavoitteena on, että opiskelija ymmärtää sähköön liittyviä peruskäsitteitä, tutustuu mittaustekniikkaan osaa tehdä sähköopin perusmittauksia sekä rakentaa ja tutkia yksinkertaisia
FY6 SÄHKÖ Tavoitteet Kurssin tavoitteena on, että opiskelija ymmärtää sähköön liittyviä peruskäsitteitä, tutustuu mittaustekniikkaan osaa tehdä sähköopin perusmittauksia sekä rakentaa ja tutkia yksinkertaisia
CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017
 CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017 Tenttikysymysten aihealueita eli esimerkkejä mistä aihealueista ja minkä tyyppisiä tehtäviä kokeessa
CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017 Tenttikysymysten aihealueita eli esimerkkejä mistä aihealueista ja minkä tyyppisiä tehtäviä kokeessa
Integrointi ja sovellukset
 Integrointi ja sovellukset Tehtävät:. Muodosta ja laske yläsumma funktiolle fx) x 5 välillä [, 4], kun väli on jaettu neljään yhtä suureen osaan.. Määritä integraalin x + ) dx likiarvo laskemalla alasumma,
Integrointi ja sovellukset Tehtävät:. Muodosta ja laske yläsumma funktiolle fx) x 5 välillä [, 4], kun väli on jaettu neljään yhtä suureen osaan.. Määritä integraalin x + ) dx likiarvo laskemalla alasumma,
α-amylaasi α-amylaasin eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Tärkkelys Oligosakkaridit Maltoosi + glukoosi
 n eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Työssä eristetään ja puhdistetaan merkittävä ja laajalti käytetty teollisuusentsyymi syljestä. pilkkoo tärkkelystä ensin oligosakkarideiksi
n eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Työssä eristetään ja puhdistetaan merkittävä ja laajalti käytetty teollisuusentsyymi syljestä. pilkkoo tärkkelystä ensin oligosakkarideiksi
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
Laskuharjoitus 3 palautus 11. 11. 2003 mennessä. Entsyymillä on seuraavanlainen reaktiomekanismi (katso oheista kuvaa):
 Laskuharjoitus 3 palautus 11. 11. 2003 mennessä Tehtävä 1: Entsyymikinetiikkaa Entsyymillä on seuraavanlainen reaktiomekanismi (katso oheista kuvaa): 1. A:n sitoutuminen saa konformaatiossa aikaan muutoksen,
Laskuharjoitus 3 palautus 11. 11. 2003 mennessä Tehtävä 1: Entsyymikinetiikkaa Entsyymillä on seuraavanlainen reaktiomekanismi (katso oheista kuvaa): 1. A:n sitoutuminen saa konformaatiossa aikaan muutoksen,
Plasmidi-DNA:n eristys bakteerisoluista DNA:n geelielektroforeesi (Proteiinien geelielektroforeesi)
 Plasmidi-DNA:n eristys bakteerisoluista DNA:n geelielektroforeesi (Proteiinien geelielektroforeesi) CHEM-A1310 Biotieteen perusteet Heli Viskari 2017 DNA-harjoitustöiden aikataulu, valitse yksi näistä
Plasmidi-DNA:n eristys bakteerisoluista DNA:n geelielektroforeesi (Proteiinien geelielektroforeesi) CHEM-A1310 Biotieteen perusteet Heli Viskari 2017 DNA-harjoitustöiden aikataulu, valitse yksi näistä
Dislokaatiot - pikauusinta
 Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Vastaa lyhyesti selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
CHEM-A1310 Biotieteen perusteet 2019
 CHEM-A1310 Biotieteen perusteet 2019 Laboratoriodemojen teoriaosuus Huomaa: Jokaisesta suorittamatta jääneestä demokerrasta vähennetään 0.75 pistettä tentin kokonaispisteistä. Rästikertojen jälkeen suoritukset
CHEM-A1310 Biotieteen perusteet 2019 Laboratoriodemojen teoriaosuus Huomaa: Jokaisesta suorittamatta jääneestä demokerrasta vähennetään 0.75 pistettä tentin kokonaispisteistä. Rästikertojen jälkeen suoritukset
Seminar 24.1.2014. Wet chemistry alliance Synthetic chemistry
 *not as active students 24.1.2014 Kaivosvesiasioiden verkostoitumistilaisuus UEF Farmasia Wet Chemistry Alliance Seminar 24.1.2014 Wet chemistry alliance Synthetic chemistry Prof. J. Vepsäläinen (UEF)
*not as active students 24.1.2014 Kaivosvesiasioiden verkostoitumistilaisuus UEF Farmasia Wet Chemistry Alliance Seminar 24.1.2014 Wet chemistry alliance Synthetic chemistry Prof. J. Vepsäläinen (UEF)
Vinkkejä opettajille ja odotetut tulokset SIVU 1
 Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia
 Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella
 Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella Tarvittavat ennakkotiedot ja käsitteet: Atomi, anioni, kationi, atomien yleisimmät hapetustilat, metallien jännitesarja,
Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella Tarvittavat ennakkotiedot ja käsitteet: Atomi, anioni, kationi, atomien yleisimmät hapetustilat, metallien jännitesarja,
Määritelmät. Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin
 Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Heikot sidokset voimakkuusjärjestyksessä: -Sidos poolinen, kun el.neg.ero on 0,5-1,7. -Poolisuus merkitään osittaisvarauksilla
 Heikot sidokset voimakkuusjärjestyksessä: 1. Ioni-dipoli sidokset 2. Vetysidokset 3. 4. Dipoli-dipoli sidokset Dispersiovoimat -Sidos poolinen, kun el.neg.ero on 0,5-1,7 -Poolisuus merkitään osittaisvarauksilla
Heikot sidokset voimakkuusjärjestyksessä: 1. Ioni-dipoli sidokset 2. Vetysidokset 3. 4. Dipoli-dipoli sidokset Dispersiovoimat -Sidos poolinen, kun el.neg.ero on 0,5-1,7 -Poolisuus merkitään osittaisvarauksilla
ALKOHOLIPITOISUUDEN MÄÄRITYS OLUESTA KAASUKROMATOGRAFIL- LA
 (1) ALKOHOLIPITOISUUDEN MÄÄRITYS OLUESTA KAASUKROMATOGRAFIL- LA 1. Standardiliuosten teko etanolista Arvioi, mikä on näytteen alkoholipitoisuus Valitse sen mukaan 3-4 standardiliuosta, jotka ovat näytteen
(1) ALKOHOLIPITOISUUDEN MÄÄRITYS OLUESTA KAASUKROMATOGRAFIL- LA 1. Standardiliuosten teko etanolista Arvioi, mikä on näytteen alkoholipitoisuus Valitse sen mukaan 3-4 standardiliuosta, jotka ovat näytteen
Kondensaatio ja hydrolyysi
 Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA. Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva
 GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva Gluteenittomuus Gluteenittomia tuotteita koskevan standardin on asettanut Codex Alimentarius
GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva Gluteenittomuus Gluteenittomia tuotteita koskevan standardin on asettanut Codex Alimentarius
AMINOTRANSAMINAASI-ENTSYYMIN PUHDISTUS JA KITEYTYS
 AMINOTRANSAMINAASI-ENTSYYMIN PUHDISTUS JA KITEYTYS Saara Sipola 2011 Oulun seudun ammattikorkeakoulu AMINOTRANSAMINAASI-ENTSYYMIN PUHDISTUS JA KITEYTYS Saara Sipola Opinnäytetyö Kevät 2011 Laboratorioalan
AMINOTRANSAMINAASI-ENTSYYMIN PUHDISTUS JA KITEYTYS Saara Sipola 2011 Oulun seudun ammattikorkeakoulu AMINOTRANSAMINAASI-ENTSYYMIN PUHDISTUS JA KITEYTYS Saara Sipola Opinnäytetyö Kevät 2011 Laboratorioalan
Tehtävä 2. Selvitä, ovatko seuraavat kovalenttiset sidokset poolisia vai poolittomia. Jos sidos on poolinen, merkitse osittaisvaraukset näkyviin.
 KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
joka voidaan määrittää esim. värinmuutosta seuraamalla tai lukemalla
 REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Kiteet kimpaleiksi (Veli-Matti Ikävalko)
 Kiteet kimpaleiksi (Veli-Matti Ikävalko) VINKKEJÄ OPETTAJALLE: Työ voidaan suorittaa 8 luokalla ionisidosten yhteydessä. Teoria ja kysymysosa osa voidaan suorittaa kotitehtävänä. Kirjallisuudesta etsimiseen
Kiteet kimpaleiksi (Veli-Matti Ikävalko) VINKKEJÄ OPETTAJALLE: Työ voidaan suorittaa 8 luokalla ionisidosten yhteydessä. Teoria ja kysymysosa osa voidaan suorittaa kotitehtävänä. Kirjallisuudesta etsimiseen
Limsan sokeripitoisuus
 KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
KaiHali & DROMINÄ hankkeiden loppuseminaari
 KaiHali & DROMINÄ hankkeiden loppuseminaari Kaivosvesien muuttamien vesistöjen aktiiviset puhdistusmenetelmät Esther Takaluoma / Kimmo Kemppainen, KAMK 04.12.2018 Aktiiviset puhdistusmenetelmät 1. Luontainen
KaiHali & DROMINÄ hankkeiden loppuseminaari Kaivosvesien muuttamien vesistöjen aktiiviset puhdistusmenetelmät Esther Takaluoma / Kimmo Kemppainen, KAMK 04.12.2018 Aktiiviset puhdistusmenetelmät 1. Luontainen
PULLEAT VAAHTOKARKIT
 PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
KALKINPOISTOAINEET JA IHOMME
 KALKINPOISTOAINEET JA IHOMME Martta asuu kaupungissa, jossa vesijohtovesi on kovaa 1. Yksi kovan veden Martalle aiheuttama ongelma ovat kalkkisaostumat (kalsiumkarbonaattisaostumat), joita syntyy kylpyhuoneeseen
KALKINPOISTOAINEET JA IHOMME Martta asuu kaupungissa, jossa vesijohtovesi on kovaa 1. Yksi kovan veden Martalle aiheuttama ongelma ovat kalkkisaostumat (kalsiumkarbonaattisaostumat), joita syntyy kylpyhuoneeseen
Spektrofotometria ja spektroskopia
 11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Nimi sosiaaliturvatunnus. Vastaa lyhyesti, selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
LABORATORIOTYÖ: AGAROOSIGEELIELEKTROFOREESI
 LABORATORIOTYÖ: AGAROOSIGEELIELEKTROFOREESI Agaroosigeelielektroforeesi (AGE) on yksinkertainen ja tehokas menetelmä erikokoisten DNAjaksojen erottamiseen, tunnistamiseen ja puhdistamiseen. Eri valmistajien
LABORATORIOTYÖ: AGAROOSIGEELIELEKTROFOREESI Agaroosigeelielektroforeesi (AGE) on yksinkertainen ja tehokas menetelmä erikokoisten DNAjaksojen erottamiseen, tunnistamiseen ja puhdistamiseen. Eri valmistajien
BIOMOLEKYYLEJÄ. fruktoosi
 BIMLEKYYLEJÄ IMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Ihminen on käyttänyt luonnosta saatavia, kasveissa ja eläimissä esiintyviä polymeerejä eli biopolymeerejä jo pitkään arkipäivän tarpeisiinsa. Biomolekyylit
BIMLEKYYLEJÄ IMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Ihminen on käyttänyt luonnosta saatavia, kasveissa ja eläimissä esiintyviä polymeerejä eli biopolymeerejä jo pitkään arkipäivän tarpeisiinsa. Biomolekyylit
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
PULLEAT JA VALTAVAT VAAHTOKARKIT
 sivu 1/6 PULLEAT JA VALTAVAT VAAHTOKARKIT LUOKKA-ASTE/KURSSI Soveltuu ala-asteelle, mutta myös yläkouluun syvemmällä teoriataustalla. ARVIOTU AIKA n. 1 tunti TAUSTA Ilma on kaasua. Se on yksi kolmesta
sivu 1/6 PULLEAT JA VALTAVAT VAAHTOKARKIT LUOKKA-ASTE/KURSSI Soveltuu ala-asteelle, mutta myös yläkouluun syvemmällä teoriataustalla. ARVIOTU AIKA n. 1 tunti TAUSTA Ilma on kaasua. Se on yksi kolmesta
Teknologia jalostusasteen työkaluna. FENOLA OY Harri Latva-Mäenpää Toimitusjohtaja 14.5.2014 Seinäjoki
 Teknologia jalostusasteen työkaluna FENOLA OY Harri Latva-Mäenpää Toimitusjohtaja 14.5.2014 Seinäjoki Fenola Oy Fenola Oy on suomalainen yritys, jonka liikeideana on valmistaa ainutlaatuisia ja aitoja
Teknologia jalostusasteen työkaluna FENOLA OY Harri Latva-Mäenpää Toimitusjohtaja 14.5.2014 Seinäjoki Fenola Oy Fenola Oy on suomalainen yritys, jonka liikeideana on valmistaa ainutlaatuisia ja aitoja
L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
MUUTOKSET ELEKTRONI- RAKENTEESSA
 MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
Peptidi ---- F ----- K ----- V ----- R ----- H ----- A ---- A. Siirtäjä-RNA:n (trna:n) (3 ) AAG UUC CAC GCA GUG CGU (5 ) antikodonit
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 3 Pisteet / 20 Osa 1: Haluat selvittää -- F -- K -- V -- R -- H -- A peptidiä
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 3 Pisteet / 20 Osa 1: Haluat selvittää -- F -- K -- V -- R -- H -- A peptidiä
Biodiesel Tuotantomenetelmien kemiaa
 Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Biopolymeerit. Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä.
 Biopolymeerit Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä. Tärkeimpiä biopolymeerejä ovat hiilihydraatit, proteiinit ja nukleiinihapot. 1 Hiilihydraatit Hiilihydraatit jaetaan mono
Biopolymeerit Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä. Tärkeimpiä biopolymeerejä ovat hiilihydraatit, proteiinit ja nukleiinihapot. 1 Hiilihydraatit Hiilihydraatit jaetaan mono
Työ 2324B 4h. VALON KULKU AINEESSA
 TURUN AMMATTIKORKEAKOULU TYÖOHJE 1/5 Työ 2324B 4h. VALON KULKU AINEESSA TYÖN TAVOITE Työssä perehdytään optisiin ilmiöihin tutkimalla valon kulkua linssisysteemeissä ja prismassa. Tavoitteena on saada
TURUN AMMATTIKORKEAKOULU TYÖOHJE 1/5 Työ 2324B 4h. VALON KULKU AINEESSA TYÖN TAVOITE Työssä perehdytään optisiin ilmiöihin tutkimalla valon kulkua linssisysteemeissä ja prismassa. Tavoitteena on saada
Luento Sähköstaattiset vuorovaikutukset. Veden ominaisuudet Hydrofobinen vuorovaikutus. x = 0
 Luento 9 11.3.016 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
Luento 9 11.3.016 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
DEE-11110: SÄHKÖTEKNIIKAN PERUSTEET
 DEE-11110: SÄHKÖTEKNIIKAN PERUSTEET Kurssin esittely Sähkömagneettiset ilmiöt varaus sähkökenttä magneettikenttä sähkömagneettinen induktio virta potentiaali ja jännite sähkömagneettinen energia teho Määritellään
DEE-11110: SÄHKÖTEKNIIKAN PERUSTEET Kurssin esittely Sähkömagneettiset ilmiöt varaus sähkökenttä magneettikenttä sähkömagneettinen induktio virta potentiaali ja jännite sähkömagneettinen energia teho Määritellään
Solun kemiallinen peruskoostumus eläinsolu. Solun kemia. Solun kemiallinen peruskoostumus bakteerisolu. Vesi 1
 Solun kemiallinen peruskoostumus eläinsolu Solun kemia paino-% Vesi 75-90 proteiinit 10-20 Lipidit 2 Hiilihydraatit 1 RNA/DNA 0,7/0,4 Epäorg. 1,5 Solun kemiallinen peruskoostumus bakteerisolu Vesi 1 paino-%
Solun kemiallinen peruskoostumus eläinsolu Solun kemia paino-% Vesi 75-90 proteiinit 10-20 Lipidit 2 Hiilihydraatit 1 RNA/DNA 0,7/0,4 Epäorg. 1,5 Solun kemiallinen peruskoostumus bakteerisolu Vesi 1 paino-%
Liike ja voima. Kappaleiden välisiä vuorovaikutuksia ja niistä aiheutuvia liikeilmiöitä
 Liike ja voima Kappaleiden välisiä vuorovaikutuksia ja niistä aiheutuvia liikeilmiöitä Tasainen liike Nopeus on fysiikan suure, joka kuvaa kuinka pitkän matkan kappale kulkee tietyssä ajassa. Nopeus voidaan
Liike ja voima Kappaleiden välisiä vuorovaikutuksia ja niistä aiheutuvia liikeilmiöitä Tasainen liike Nopeus on fysiikan suure, joka kuvaa kuinka pitkän matkan kappale kulkee tietyssä ajassa. Nopeus voidaan
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Metsäpatologian laboratorio tuhotutkimuksen apuna. Metsätaimitarhapäivät 23. 24.1.2014 Anne Uimari
 Metsäpatologian laboratorio tuhotutkimuksen apuna Metsätaimitarhapäivät 23. 24.1.2014 Anne Uimari Metsäpuiden vaivat Metsäpuiden eloa ja terveyttä uhkaavat monet taudinaiheuttajat: Bioottiset taudinaiheuttajat
Metsäpatologian laboratorio tuhotutkimuksen apuna Metsätaimitarhapäivät 23. 24.1.2014 Anne Uimari Metsäpuiden vaivat Metsäpuiden eloa ja terveyttä uhkaavat monet taudinaiheuttajat: Bioottiset taudinaiheuttajat
kemiallisesti puhdas vesi : tislattua vettä käytetään mm. höyrysilitysraudoissa (saostumien ehkäisy)
 Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA
 ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
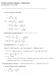 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
Liuottimien analytiikka. MUTKU-päivät 2016, 16.3.2016 Jarno Kalpala, ALS Finland Oy
 Liuottimien analytiikka MUTKU-päivät 2016, 16.3.2016 Jarno Kalpala, ALS Finland Oy RIG H T S O L U T I O N S R IGH T PA RT N ER Sisältö Terminologia Näytteenoton ja analysoinnin suurimmat riskit ja niiden
Liuottimien analytiikka MUTKU-päivät 2016, 16.3.2016 Jarno Kalpala, ALS Finland Oy RIG H T S O L U T I O N S R IGH T PA RT N ER Sisältö Terminologia Näytteenoton ja analysoinnin suurimmat riskit ja niiden
Käyttöohjeet IVD Matrix HCCA-portioned
 8290200 Käyttöohjeet IVD Matrix HCCA-portioned Matriisiavusteisen laserdesorptio/ionisaatio-lentoaikamassaspektrometrian (MALDI-TOF-MS) puhdistettu matriisiaine. CARE-tuotteet ovat korkealaatuisia kulutustuotteita,
8290200 Käyttöohjeet IVD Matrix HCCA-portioned Matriisiavusteisen laserdesorptio/ionisaatio-lentoaikamassaspektrometrian (MALDI-TOF-MS) puhdistettu matriisiaine. CARE-tuotteet ovat korkealaatuisia kulutustuotteita,
Luento Sähköstaattiset vuorovaikutukset. Veden ominaisuudet Hydrofobinen vuorovaikutus. x = 0
 Luento 9 17.3.017 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
Luento 9 17.3.017 1 Sähköstaattiset vuorovaikutukset Poissonoltzmann yhtälö Varatut pinnat nesteessä Varatut pallomaiset partikkelit nesteessä Veden ominaisuudet Hydrofobinen vuorovaikutus = 0 Sähköstaattiset
