ALKUPERÄISTUTKIMUS. Luuytimensiirrosta veren kantasolujen. kokemukset sadan ensimmäisen potilaan autologisesta kantasolujen siirrosta Turussa
|
|
|
- Martta Korhonen
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 ALKUPERÄISTUTKIMUS Luuytimensiirrosta veren kantasolujen siirtoon kokemukset sadan ensimmäisen potilaan autologisesta kantasolujen siirrosta Turussa Kari Remes, Allan Rajamäki, Seija Grenman, Maija Itälä, Marjut Kauppila, Jukka Nikoskelainen, Tarja-Terttu Pelliniemi, Raija Ristamäki, Toivo T. Salmi, Tuula Salmi, Eeva Salminen, Riitta Vanharanta ja Auli Toivanen Hematopoieettisten kantasolujen siirto mahdollistaa syövän suuriannoksiset hoidot ja voi parantaa näin hoitotuloksia lääkitykseen ja sädehoitoon reagoivissa syöpätaudeissa. Autologiset kantasolujen siirrot ovat viime vuosien aikana yleistyneet hematologian ja onkologian piirissä, ja veri on syrjäyttänyt luuytimen kantasolujen lähteenä. TYKS:n luuytimensiirtoyksikössä aloitettiin autologiset siirrot vuonna Olemme analysoineet sadan ensimmäisen potilaamme siirtotulokset. Autologisen kantasolujen siirron avulla intensiivihoidon siedettävyys on hyvä samoin kuin hoidon välitön teho, mutta taudin myöhempi uusiutumistaipumus on suuri. Suurelta osin syövän intensiivihoito on edelleen kokeellista, ja potilaat pitäisi ottaa mukaan hoitomuodon lopullista asemaa selvittäviin tutkimuksiin. Lääkitykseen reagoivissa syöpätaudeissa on yritetty parantaa hoitotuloksia annosten lisäämisellä. Näin on tehty erityisesti pahanlaatuisissa veritaudeissa mutta myös monen kiinteän syöpäkasvaimen hoidossa. Suuriannoksisimmat hoidot aiheuttavat merkittävän luuydinvaurion ja vaativat tuekseen hematopoieettisen kantasolukon siirron. Kantasolulähde voi olla luuydin tai veri, ja se voi olla peräisin vieraasta yksilöstä (allogeeninen siirto) tai omaa kudosta (autologinen siirto). Allogeenisista luuytimensiirroista on kokemuksia 1970-luvun puolivälistä lähtien: suuriannoksinen lääkitys ja allogeeninen luuytimensiirto on monessa hematologisessa syövässä potentiaalisesti parantava hoitomuoto, mutta siihen liittyy huomattava toimenpidekuolleisuus. Saatujen siirtokokemusten perusteella ryhdyttiin pian analogisiin suuriannoshoitoihin autologisen luuytimensiirron (ABMT) avulla. Viime aikoina on veri tullut suosituksi autologisten kantasolujen lähteeksi. Autologisen kantasolujen siirron (autologous stem cell transplantation, ASCT) etuna on pieni toimenpidekuolleisuus, ja suhteellisen vähäisen toksisuuden vuoksi sen käyttö voidaan ulottaa vuotiaisiin saakka. Siihen liittyy kuitenkin suuri taudin uusiutumisen riski. ASCT:n asema eri tautien hoidossa on suurelta osin selvittämättä, sillä toistaiseksi on julkaistu vain hyvin harvoja satunnaistettuja, prospektiivisia tutkimuksia intensiivihoidon hyödystä tavanomaiseen hoitoon verrattuna. TYKS:n sisätautien klinikassa aloitettiin ASCT:t vuonna 1991, aluksi luuytimensiirtoina, mutta pian yhä laajemmalti veren kantasolujen siirtoina (autologous blood cell transplantation, ABCT). Viimeisten kolmen vuoden aikana ABCT on ollut ensisijainen valinta ja tarvittaessa sitä on tuettu myös ABMT:llä. Suuriannoshoitoa ja ASCT:tä käytetään hematologisten käyttöaiheiden lisäksi myös kiinteiden kasvainten hoidossa. Näin on tehty myös TYKS:ssa, missä kantasolujen siirtoyksikköön kuuluvat sisätautien ja lasten- Duodecim 113: ,
2 Aineisto ja menetelmät Ensimmäiset sata potilasta hoidettiin ASCT:llä aikavälillä Ensimmäiset kaksi siirtoa toteutettiin ABMT:llä, mutta jo vuoden 1992 alussa ryhdyttiin käyttämään ABCT:tä, alkuun ABMT:n tukemana mutta vuoden 1993 alusta ensisijaisesti yksinään. ABMT-tukea käytetään edelleen, jos verestä ei saada kerätyksi riittävästi kantasoluja. ASCT-toiminnan kehitys TYKS:ssa on esitetty taulukossa 1. Aineistomme potilaista 96 on aikuisia ja neljä lapsia (5 15-vuotiaita). Yleisimmät ASCT:n aiheet ovat olleet multippeli myelooma ja non-hodgkin-lymfooma, joiden osuus siirroista on ollut 70 %. Viidennes siirroista on liittynyt kiinteiden kasvainten intensiivihoitoon. Ensimmäisten sadan potilaamme siirtoaiheet ja muut tiedot siirtoa edeltäneeltä ajalta on esitetty taulukossa 2. Kolmelle potilaalle on tehty kaksoissiirto eli kaksi peräkkäistä intensiivihoitoa ASCT-tuella, joten siirtojen kokonaismäärä on 103. K a n t a s o l u j e n k e r ä ä m i n e n. Luuytimen keruu on tehty ilman granulosyyttikasvutekijöiden (G-/GM-CSF) käyttöä. Veren kantasolujen keruuta on edeltänyt kantasolujen mobilisaatio kohtalaisen sytopenian aiheuttavan solunsalpaajahoidon ja sitä seuraavan G- tai GM-CSF-stimulaation yhdistelmällä. Vain yksi lymfooma- ja yksi rintasyöpäpotilas saivat pelkän kasvutekijämobilisaation. Yleisin solunsalpaajahoito mobilisaatiossa on ollut suuriannoksinen (4 g/m 2 ) syklofosfamidilääkitys (63 potilasta). Pienempiannoksisen ( g/m 2 ) syklofosfamidihoidon sai kuusi potilasta. Myös erilaisia tautikohtaisia yhdistelmähoitoja solunsalpaajilla käytettiin kantasolujen mobilisoimiseksi erityisesti lymfoomia ja muita kiinteitä kasvaimia hoidettaessa. Veren kantasolut kerättiin Fenwal CS-3000 Plus -afereesilaitteella (Baxter, Ill., USA). Käsitelty kertatilavuus on ollut noin 10 litraa ja keruuaika 2 3 tuntia. Aluksi afereesit aloitettiin veren leukosyyttimäärän alkaessa kasvaa solunsalpaajahoidon jälkeen (> x 10 9 /l) ja saaliin määrää arvioitiin mononukleaarisolujen (MNC) määrällä (tavoite >2 x 10 8 MNC/saajan painokilo). Ensimmäiset potilaat saivat varmuuden vuoksi veren kantasolujen ohella myös luuytimen siirron. Vuoden 1993 alusta siirtoon on käytetty pelkkiä veren kantasoluja, jos MNC-määrä on ollut vähintään 2x10 8 /kg. Sittemmin veren kantasolujen keruun aloitus on perustunut veren CD34-positiivisten (CD34+) solujen määrän seurantaan veren leukosyyttimäärän kasvuvaiheessa: aluksi afereesit aloitettiin veren CD34+-solujen määrän ylittäessä arvon 10 x 10 6 /l, mutta nyttemmin raja-arvona on ollut noin 20 x 10 6 /l. Havaintojemme mukaan CD34+-solujen keruusaalis on varsin tarkasti arvioitavissa keruuaamu- Taulukko 1. Autologiset kantasolujen siirrot TYKS:ssa elokuusta 1991 maaliskuuhun 1996 (potilasmäärä vuosittain). Vuosi ABMT ABMT+ ABCT selabct Yht. ABCT / Kahdelle potilaalle intensiivihoito + ABCT kahdesti ABMT = autologinen luuytimensiirto, ABCT = autologinen veren kantasolujen siirto, selabct = autologinen veren kantasolujen siirto eristetyillä (selektoiduilla) kantasoluilla. tautien klinikoiden (siirtojen suorituspaikat) lisäksi naistentautien ja onkologian klinikat sekä keskuslaboratorion hematologian osasto (siirteiden käsittely ja tallennus sekä kantasolujen viljely ja laskenta). Kuvaamme kokemuksemme TYKS:n sadasta ensimmäisestä potilaasta, jotka ovat saa- neet ASCT:llä tuetun suuriannoshoidon. na veren CD34+-solupitoisuuden avulla: kun pitoisuus on <20x10 6 /l, saalis on niukka, kun taas pitoisuuden ylittäessä arvon 100 x 10 6 /l riittävä solusaalis saadaan yhdellä afereesilla (Remes ym. 1996). Keruutavoitteena on ollut vähintään 4 x 10 6 CD34+-solua/kg; hyväksytty minimimäärä pelkän ABCT:n suorittamiselle on ollut 1.5 x 10 6 /kg. K a n t a s o l u j e n e r i s t y s ( s e l e k t o i n t i ). Laitteisto CD34+-solujen eristämiseen (CellPro Ceprate SC, Wa, USA) saatiin tammikuussa 1995, ja sittemmin eristäminen on ollut tavoitteena myelooma-, lymfooma- ja munasarjasyöpäpotilailla. Eristämisen edellytyksenä on ollut, että kahdella peräkkäisella afereesilla on saatu yhteensä vähintään 5x10 6 CD34+-solua/kg. Tässä aineistossa ABCT on tehty eristetyillä kantasoluilla 24 potilaalle. CD34+-solujen kvantifiointi. Veren CD34+-solumääritys tehtiin kantasolut tunnistavan monoklonaalisen CD34-vasta-aineen (HPCA-2PE, Becton- Dickinson, USA) avulla. Kvantifiointi tehtiin FACS-virtaussytometrilla (Becton-Dickinson). Afereesituotteen CD34+solupitoisuus analysoitiin punasolujen hajottamisen jälkeen (Ortho lysing solution, Ortho Diagnostics, USA) edellä kuvatulla vasta-ainevärjäyksellä pohjoismaisen suosituksen mukaisesti (Johnsen 1995). Puolikiinteää viljelymenetelmää käytettiin hematopoieettisten solujen kasvun pesäkelaskentaan Iscoven ym. (1974) menettelyä mukaillen. Veren ja afereesituotteen MNC kvantifioitiin käyttäen Technicon H2 -analysaattoria (Technicon, Tarrytown, NY, USA). K a n t a s o l u j e n s ä i l y t y s. Keruun tai eristämisen jälkeen kantasolut jäädytettiin ohjelmoitavalla solujen pakastuslaitteella (Planer KRYO Series II Cryofreezer, MI, USA) ja siirrettiin nestetyppisäiliön nestefaasiin ( 196 o C). I n t e n s i i v i h o i t o o n ryhtymisen edellytyksenä on useimmiten ollut se, että tauti on reagoinut suotuisasti solunsalpaajahoitoon. Osalla potilaista ryhdyttiin intensiivihoitoyritykseen taudin ollessa stabiilissa, hoitoon reagoimattomassa tai etenevässä vaiheessa (11 myeloomaa, kaksi lymfoomaa, neljä kiinteää kasvainta). Intensiivihoidon laatu on määräytynyt taudin mukaisesti. Myeloomassa hoitona on ollut suuriannoksinen melfalaani (140 mg/m 2 ) ja kokokehon sädetys (12 Gy viitenä fraktiona, keuhkoannos 9.6 Gy) alle 220 K. Remes ym.
3 Taulukko 2. Ensimmäiset sata autologisen kantasolujen siirron saanutta potilasta diagnoosiryhmittäin (mediaanit ja vaihteluväli ellei toisin ilmoitettu). Diagnoosi Potilaita Ikä, v Taudin kesto, kk Potilaita 1 Aiempien solun- Hoitovaste 2 hoitolinjoilla salpaajakuurien ennen siirtoa määrä Myelooma (37 66) 9 (4 151) (2 37) CR(2), VGPR(10) PR(16), SD(9), PD(2) Lymfoomat (19 64) 22.5 (6 174) (4 26) CR1(6), CR2(17) PR(11), PD(2) Leukemiat (12 53) 23 (7 53) (2 14) CR1/2(3), PR(3) Rintasyöpä 4 43 (37 53) 4 (4 5) 4 2 (2 3) CR(4) Munasarjasyöpä 9 48 (40 57) 9 (7 35) (7 32) CRpat(5) PR(2), PD(2) Muut (4 32) 16.5 (6 32) (5 24) CR1(3), CR2(1) PR(1), PD(1) 1 Potilas saanut yhtä (hoitolinja 1), kahta (hoitolinja 2) tai kolmea (hoitolinja 3) erilaista solunsalpaajayhdistelmää 2 Hoitovasteet (potilaiden lukumäärä): CR = täydellinen remissio, CR1/2 = 1. tai 2. täydellinen remissio, CRpat = patologisesti varmistettu CR, VGPR = erittäin hyvä osittainen remissio (myelooma: muutoin CR, mutta elektroforeesissa M-komponentti; CLL: muutoin CR, mutta CLL-soluja osoitettavissa pintamerkkitutkimuksella), PR = osittainen remissio, SD = vakaa tauti, PD = etenevä tauti 3 Lymfoomat: non-hodgkin-lymfooma 32, Hodgkinin tauti 4 4 Leukemiat: KLL 4, KML 1, ALL 1 5 Muut kasvaimet: sarkoomat 3, kiveskarsinooma 1, neuroblastooma 1, Wilmsin tuumori 1 60-vuotiaille ja pelkkä melfalaanihoito (200 mg/m 2 ) yli 60 vuotta täyttäneille. Lymfoomapotilaiden intensiivihoitona on ollut BEAM (karmustiini 300 mg/m 2, etoposidi 800 mg/m 2, sytarabiini mg/m 2 ja melfalaani 140 mg/m 2 ) lukuun ottamatta kahta potilasta, jotka saivat suuriannoksisen syklofosfamidilääkityksen (120 mg/kg) ja edellä mainitun koko kehon sädetyksen. Viimeksi mainittua esihoitoa on käytetty myös kroonisessa lymfaattisessa leukemiassa (KLL). Munasarjasyövän intensiivihoitoon annettiin kaikille yhdeksälle potilaalle karboplatiinia ( mg/m 2 ) ja syklofosfamidia ( mg/m 2 ). Kolmantena solunsalpaajana hoitoon liitettiin etoposidi ( mg/m 2 ) seitsemälle potilaalle ja doksorubisiini (120 mg/m 2 ) tai paklitakseli (300 mg/m 2 ) kahdelle. Rintasyövässä käytettiin pohjoismaisen liitännäishoito-ohjelman mukaan CTCb-hoitoa (syklofosfamidi 6 g/m 2, tiotepa 500 mg/m 2 ja karboplatiini 800 mg/m 2 ). Useimpien muiden kiinteiden tuumorien hoidon perustana on ollut suuriannoksinen melfalaanilääkitys. KML-potilas sai esihoidokseen suuriannoksisen busulfaanilääkityksen (16 mg/kg) ja akuuttia lymfaattista leukemiaa (ALL) sairastanut lapsi busulfaania (16 mg/kg) ja syklofosfamidia (120 mg/kg). K a n t a s o l u j e n s i i r t o tunnin kuluttua intensiivihoidon jälkeen kantasolut kuljetettiin nestetyppiastiassa osastolle, sulatettiin +37 o C:n vesihauteessa ja ruiskutettiin heti potilaaseen keskuslaskimokatetrin kautta. Pahoinvoinnin, oksentelun ja vatsakouristusten ehkäisemiseksi potilaat saivat metoklopramidia, difenhydramiinia ja deksametasonia. Siirron jälkeisestä päivästä lähtien potilaat (poikkeuksena KML) saivat granulosyyttikasvutekijää 5 µg/kg/vrk ihon alle, kunnes veren neutrofiilimäärä oli yli 1.0 x 10 9 /l kolmena peräkkäisenä päivänä. Veriarvojen ja yleiskunnon parannuttua myeloomapotilaille on pyritty aloittamaan ylläpitohoito alfainterferonilla (3 MU kolmesti viikossa ihon alle). T u l o s t e n a n a l y s o i n t i. Tässä raportissa on keskitytty mobilisaatiohoidon, CD34+-solujen eristämisen, intensiivihoidon jälkeisen hematologisen toipumisen, hoitovasteiden ja taudin uusiutumisten tarkasteluun. Seuranta ulottuu asti. Tulokset Kantasolujen mobilisaatio. Yleisimmin käytetyn mobilisaatiohoidon eli suuriannoksisen syklofosfamidilääkityksen ja G-/GM-CSF:n ominaispiirteet on esitetty taulukossa 3. Kantasolujen keruu aloitettiin keskimäärin 11 päivän kuluttua em. hoidosta, ja tavoitesaalis saatiin kerätyksi keskimäärin kolmella afereesilla. Kolmannekselle mobilisaatiohoidon saaneista ilmaantui neutropeeninen kuume. Kantasolujen mobilisaatio voi epäonnistua: erityisesti aiempien solunsalpaajakuurien lukumäärä (>10) ja trombosyyttimäärän hidas kasvu mobilisaatiohoidon jälkeen ennakoivat CD34+-solujen huonoa ilmaantumista vereen. Kantasolujen eristäminen. CD34+-solujen eristäminen 24 potilaalla onnistui siten, että eristyksen jälkeinen solusaalis oli keskimäärin 42 % Luuytimensiirrosta veren kantasolujen siirtoon 221
4 T a u l u k k o 3. Kantasolumobilisaatio suuriannoksisen (4 g/m 2 ) syklofosfamidin ja kasvutekijän (G-/GM-CSF 5 µg/ kg/vrk) yhdistelmällä (potilailla, joista CD34+-solutiedot käytettävissä; mediaanit ja vaihteluvälit). Tauti Potilaita Afereesien Korkein CD34+- CD34+- Afereesien Kuume aloitus, vrk pitoisuus veressä, saalis, määrä neutropeniassa x 10 6 /l x 10 6 /kg n % Myelooma (9 19) 72.3 ( ) 6.9 ( ) 3 (1 5) 9 26 Lymfooma (8 19) 62.7 ( ) 8.0 ( ) 3 (2 5) 7 32 (vaihteluväli %) lähtötilanteen CD34+-solumäärästä ja eristetyn saaliin keskimääräinen puhtausaste CD34+-solujen suhteen oli 86 % (69 96 %). Hematologinen toipuminen intensiivihoidosta. Veren neutrofiilien ja trombosyyttien elpyminen ABCT:n jälkeen on selvästi nopeampaa kuin ABMT:n jälkeen (taulukko 4). Tämä heijastuu lyhyempänä sairaalahoitona. Kun veren kantasolujen siirtoa on tuettu myös luuytimensiirrolla, veren neutrofiilit elpyvät nopeasti, mutta trombosyyttimäärän kasvu on hidasta. Tämä heijastaa sitä ilmeistä seikkaa, että veren kantasolusaaliin jäädessä niukaksi myös luuydin on»huonolaatuista». Käytettäessä eristettyjä CD34+-soluja siirtoon hematologinen toipuminen on ollut yhtä nopeata kuin tavanomaisen ABCT:n jälkeen. Intensiivihoidon sivuvaikutukset. Kolme potilasta (3 %) on kuollut intensiivihoidon jälkeisessä neutropeenisessa sepsiksessä. Yksi näistä potilaista oli ABMT:llä hoidettu akuuttia lymfaattista leukemiaa sairastanut lapsi, ja kaksi potilasta (myelooma, lymfooma) menehtyi ABCT:n jälkeen. Molemmilla jälkimmäisistä potilaista oli komplikaatioiden sietoa huonontava lisätauti: toisella oli LED:n vaurioittama sydän ja toisella myeloomamunuaisen aiheuttama dialyysihoitoa vaativa munuaisten vajaatoiminta. Ensimmäinen autologisen siirron elokuussa 1991 saanut potilaamme menehtyi suuriannoshoidon (syklofosfamidi ja koko kehon sädetys) myöhäissivuvaikutukseen pneumoniittiin ja perikardiittiin 41 kuukauden kuluttua siirrosta perustaudin ollessa remissiossa. Muutoin intensiivihoidon siedettävyys oli kohtalaisen hyvä. Pahimmat sivuvaikutukset esiintyivät maha-suolikanavan oireina (suun mukosiitti, ripuli/pahoinvointi) ja kuumeiluna. Vaikea-asteista (WHO:n aste 3 4) mukosiittia, muuta maha-suolikanavan oireilua sekä yli 38 o C:n kuumeilua (WHO:n aste 3 4) esiintyi käytetyimpien intensiivihoitojen yhteydessä seuraavasti: BEAMhoidossa (34 potilasta) 26, 35 ja 12 %:lla; suuriannoksisessa melfalaanihoidossa + koko kehon sädetyksessä (18 potilasta) 39, 11 ja 0 %:lla sekä pelkässä melfalaanihoidossa (19 potilasta) 11, 21 ja 0 %:lla. Vasteet intensiivihoitoon. Intensiivihoito on lisännyt hyvien vasteiden määrää kaikissa diagnoosiryhmissä (taulukko 5). Erityisen selvä vasteiden paraneminen on todettu siirron aikaan osittaisen hoitovasteen saaneilla potilailla, joista huomattava osa saa täydellisen remission tai erittäin hyvän osittaisen hoitovasteen. Analysointiajankohtana keskimääräinen seuranta-aika oli 13 kuukautta (1 50 kk), mikä ei vielä salli hoidon pitkäaikaistulosten tarkastelua. Seuranta-aikana tauti on edennyt seuraavasti: myelooma 11 potilaalla (28 %), lymfooma seitsemällä (19 %), sarkooma kahdella (67 %), rintasyöpä yhdellä (25 %) ja munasarjasyöpä viidellä (56 %) (taulukko 6). Kahdella potilaalla (rabdomyosarkooma ja kiveskarsinooma) intensiivihoito ei tehonnut lainkaan taudin etenemisvaiheessa. Pohdinta Viime vuosien kokemukset osoittavat selvästi, että ASCT on intensiivihoidon käyttökelpoinen tuki. Erityisesti ABCT:n jälkeinen hematologinen toipuminen on nopeaa ja hoidon toksisuus vähäistä (Holoyake ja Franklin 1994, Remes ja Rajamäki 1996). Kuolleisuus toimenpiteeseen on vain noin 2 %. Niinpä ASCT voidaan toteuttaa ikävuoteen saakka. Autologiset siirrot ovatkin nykyisin yleisempiä kuin allogeeniset. 222 K. Remes ym.
5 Taulukko 4. Hematologinen toipuminen intensiivihoidon jälkeen. Veriarvojen paranemista kuvastavat luvut ovat päiviä (mediaani ja vaihteluväli) siirron jälkeen. Siirto- Potilaita Neutrofiilit, Trombosyytit Hemoglobiini Sairaalahoitotapa 1.0 x 10 9 /l, 20 x 10 9 /l, 50 x 10 9 /l, 100 g/l, aika, vrk vrk vrk vrk vrk ABMT (10 40) 32 (20 571) 47 (24 571) 51 (15 571) 26 (17 40) ABMT+ABCT (10 45) 42 (10 584) 154 (15 458) 81 (13 504) 22 (14 53) ABCT (9 45) 1 12 (6 359) 1 16 (10 359) 1 17 (0 361) 1 14 (11 41) 1 ABCTsel (9 18) 1 13 (9 27) 1 17 (10 34) 1 16 (0 73) 1 15 (12 27) 1 1 p < 0.001; eron merkitsevyys verrattaessa ryhmiä ABCT ja ABCTsel ABMT-ryhmään (Mann Whitneyn U-testi). Vuonna 1994 oli Euroopan siirtorekisterin tiedossa 306 hematopoieettisia solujensiirtoja tekevää yksikköä 30 eri maasta ja raportoituja siirtoja , joista allogeenisia ja autologisia (Gratwohl ym. 1996a). Veren suosio kantasolulähteenä on kasvanut, ja omassakin toiminnassamme vuonna % siirroista tehtiin veren kantasoluilla. ABCT:n edellytys on, että kantasolujen mobilisaatio vereen onnistuu ja niitä saadaan kerätyksi riittävästi. Vaikka kantasolut ovat mobilisoitavissa vereen sekä ohimenevän luuytimen laman aiheuttavalla solunsalpaajahoidolla että pelkästään kasvutekijällä, näiden kahden yhdistelmä on tehokkain (Gianni ym. 1989). Käytetyin mobilisaatiosolunsalpaaja erityisesti lymfoproliferatiivisissa taudeissa on ollut suuriannoksinen syklofosfamidi (1.2 7 g/m 2 ), joka mobilisaatiokykynsä lisäksi vaikuttaa myös hoidettavaan tautiin. Kokemukset osoittavat, että siirrettäessä vähintään 2.5 5x10 6 CD34+-solua/kg veriarvot paranevat nopeasti: neutrofiilimäärä 1.0 x 10 9 /l ja trombosyyttiarvo 20 x 10 9 /l saavutetaan vuorokaudessa siirron jälkeen (Schwartzberg ym. 1993, Bensinger ym. 1994), mikä on 1 2 viikkoa nopeampaa kuin käytettäessä luuydintä kantasolujen lähteenä. Luuytimen toiminnan hitaampi elpyminen erityisesti trombosyyttien osalta on odotettavissa, jos vähimmäismäärä siirrettäviä CD34+-soluja on 1 x 10 6 /kg (Bensinger ym. 1994). Afereesein kerättävä CD34+-solusaalis on hyvin ennustettavissa veren CD34+-solupitoisuuden avulla (Haas ym. 1994, Remes ym. 1996). Lymfoproliferatiiviset taudit ovat merkittävimmät aikuispotilaiden autologisen siirron aiheet (Gratwohl ym. 1996b). Viime vuosien aikana kokeellisen intensiivihoidon piiriin ovat tulleet myös kiinteät tuumorit, jotka alusta alkaen ovat olleet lapsipotilailla tärkein siirtoaihe. Lapsilla on kiinteitä kasvaimia yritetty hoitaa suuriannoksisella solunsalpaajalääkityksellä ja ASCT:lla jo yli 20 vuoden ajan, mutta lukuun ottamatta eräitä suu- T a u l u k k o 5. Hoitovasteiden lukumäärä tautiryhmittäin: vaste ennen intensiivihoitoa (E) ja paras vaste (3 6 kk) sen jälkeen (J). Diagnoosi Potilaita CR1/2 VGPR PR SD PD NE Kuollut E J E J E J E J E J E J Myelooma Lymfooma Leukemiat Munasarjasyöpä Rintasyöpä Muut CR1/2 = 1.tai 2. täydellinen remissio, VGPR = erittäin hyvä osittainen remissio, PR = osittainen remissio, SD = vakaa tauti, PD = etenevä tauti, NE = ei arvioitavissa Luuytimensiirrosta veren kantasolujen siirtoon 223
6 T a u l u k k o 6. Taudin uusiutuminen intensiivihoidon jälkeen (mediaanit ja vaihteluvälit). Diagnoosi Potilaita Relapsien Relapsiaika Elossa pysyminen määrä siirrosta, kk siirron jälkeen, kk n % Myelooma (2 36) 31 (9 50+) Lymfooma (3 12) 15 (8 28) Kiinteät kasvaimet (4 11) 12 (6 21+) ren riskin neuroblastooma- ja sarkoomapotilaita hoidon hyödyllisyys on edelleen epäselvä (Ladenstein ym. 1993, Atra ja Pinkerton 1996). Niin aikuisilla kuin lapsilla hoitoaiheiden arviointia vaikeuttaa kontrolloitujen tutkimusten vähäisyys. Multippeli myelooma. Myelooma on omassa aineistossamme ollut yleisin siirtoaihe. Siirroista 17 tehtiin taudin myöhemmässä kuin ensihoitovaiheessa, ja näistä potilaista seitsemällä tauti on siirron jälkeen edennyt. Ensihoitovaiheessa siirron saaneiden (22 potilasta) joukossa tauti on edennyt toistaiseksi vain neljällä. Seuranta-ajat ovat toki vielä lyhyet, keskimäärin 16 kuukautta. Tuore prospektiivinen, satunnaistettu ranskalainen monikeskustutkimus, joka tehtiin 200 myeloomapotilaalla, osoitti ABMT:lla tuetun intensiivihoidon hyödyn ensihoitona tavanomaiseen hoitoon nähden: hyviä vasteita esiintyi merkitsevästi enemmän, ja arvioitu viiden vuoden elossaolo-osuus satunnaistamisen jälkeen oli 52 % intensiivihoitoa saaneilla ja keskimäärin 12 % tavanomaisen hoidon ryhmässä (p = 0.03) (Attal ym. 1996). Nykyisin intensiivihoitoa ja ASCT:tä voidaan pitää ensisijaisena valintana alle 65-vuotiailla myeloomapotilailla. Täydellisen remission saavuttaminen on pitkäkestoisen hoitovasteen merkittävä ennustekijä myeloomassa (Björkstrand ym. 1994, Harousseau ym. 1995, Attal ym. 1996), ja siihen pääsemiseksi intensiivihoito on tehokkain käytettävissä oleva menetelmä. Omassa aineistossamme täydellisten vasteiden määrä lisääntyi kahdesta 16:een intensiivihoidolla. Muita merkittäviä kestävän hoitotuloksen ennustekijöitä ovat vähäinen tautimassa diagnoosivaiheessa, seerumin pieni β 2 - mikroglobuliinipitoisuus ja taudin vastaaminen lääkehoitoon ennen siirtoa (Björkstrand ym. 1994). Interferoniylläpitohoidon merkitys on epäselvä (Björkstrand ym. 1994, Harousseau ym. 1995). Myelooma uusii tai etenee intensiivihoidon jälkeenkin niin, ettei elossapysymiskäyrään ilmaannu selvää tasannetta (Attal ym. 1996). Jäännöstaudin hoitostrategioiden parantaminen on ajankohtainen haaste. Intensiivihoidon jälkeen uusiutunut tauti on useimmiten hillittävissä tavanomaisin hoidoin (Tricot ym. 1995). Intensiivihoidon teho edenneessä myeloomassa ei ole yhtä hyvä kuin varhaisessa taudissa, mutta myös muuhun hoitoon reagoimaton tauti voi vastata intensiivihoitoon, ja vaste saattaa säilyä kohtalaisen pitkään (Gertz ym. 1995, Harousseau ym. 1995). Koska allogeeninen kantasolujen siirto tarjonnee edelleen ainoan mahdollisuuden pysyvään paranemiseen myeloomasta, sen mahdollisuus on pidettävä mielessä nuorehkoja (alle vuotiaita) potilaita hoidettaessa (Barlogie 1991, Anderson 1995, Gahrton ym. 1995). Koska myelooman hoidossa näyttää pitävän paikkansa periaate»mitä enemmän hoitoa, sen parempi», sen loogisena seurauksena on ollut yrittää kahta peräkkäistä kantasolujen siirroin tuettua intensiivihoitoa. Alustavat tulokset ovatkin olleet lupaavia, parempia kuin aiemmilla hoidoilla (Vesole ym. 1994, Björkstrand ym. 1995). Lymfoomat. Intensiivihoidon ja ASCT:n tehosta lymfoomissa on jonkin verran tutkimusnäyttöä. Ensimmäinen kontrolloitu tutkimus toistaiseksi ainoa Hodgkinin taudissa käsitteli intensiivihoidon tehoa uusiutuneessa ja hoitoresistentissä Hodgkinin taudissa 40 potilaalla (Linch ym. 1993). Intensiivihoito (BEAM) tuotti enemmän täydellisiä vasteita ja pidemmän elossa pysymisen kuin pieniannoksinen (mini-) BEAM. Tähänastinen kokemus intensiivihoidosta Hodgkinin taudissa puoltaa tätä hoitoa seuraa- 224 K. Remes ym.
7 vissa tilanteissa: kun ensilinjan lääkityksellä ei saavuteta täydellistä remissiota tai kun tauti uusii kuuden kuukauden kuluessa hoidon päättymisestä tai toisen hoitolinjan jälkeen (Vandenberghe ja Goldstone 1996). Selvä näyttö intensiivihoidon hyödystä tavanomaiseen lääkitykseen nähden on saatu uusiutuneen ja solunsalpaajahoitoon vastanneen kohtalaisen tai erittäin nopeakasvuisen non-hodgkinlymfooman hoidossa ns. PARMA-monikeskustutkimuksessa (Philip ym. 1995). Siinä viiden vuoden elossaolo-osuus intensiivihoidon ja ABMT:n jälkeen oli 53 % ja taudin etenemättömyys 46 %, kun vastaavat luvut tavanomaisen solunsalpaajalääkityksen jälkeen olivat 32 ja 12 % (p = ja 0.001). Tämän perusteella intensiivihoitoa ja ASCT:tä voidaan pitää ensisijaisena vaihtoehtona solunsalpaajahoidolle vastaavassa uusiutuneessa non-hodgkin-lymfoomassa kyseisessä potilasryhmässä. Intensiivihoidon asema kohtalaisen tai erittäin nopeakasvuisen non-hodgkin-lymfooman ensilinjan hoitona on edelleen epäselvä. Ranskalaisessa monikeskustutkimuksessa selvitettiin intensiivihoidon ja ABMT:n tehoa kohtalaisen voimakkaaseen sekventiaaliseen solunsalpaajalääkitykseen nähden potilailla, jotka oli saatu induktiohoidolla täydelliseen remissioon (Haouin ym. 1994). Merkitsevää eroa elossa pysymisessä ei ollut viiden vuoden kuluttua. Kuitenkin niillä potilailla, jotka kuuluivat kansainvälisen ennusteluokittelun mukaan huonon ennusteen ryhmiin, saatiin suuntaa-antava ero intensiivihoidon hyväksi: remissiossa pysyneiden osuudet olivat kolmen vuoden kuluttua 60 vs 41 % (p = 0.07). Hollantilaistutkimuksessa intensiivihoidolla ja ABMT:llä ei ollut parempaa tehoa tavanomaiseen hoitoon nähden potilailla, jotka eivät kolmella induktiokuurilla olleet saavuttaneet remissiota (Verdonck ym. 1995). Remission hidas saavuttaminen ei kuitenkaan ole yleisesti hyväksytty huonon ennusteen merkki. Intensiivihoidon tuloksia arvioitaessa oleellisin seikka lienee potilaiden valinta ensilinjan hoitovaiheessa hyödyn voisivat saada huonoennusteisimmat potilaat. Lisävalaistusta tähän saadaan aikanaan monesta meneillään olevasta huonon ennusteen potilaisiin kohdistuvasta tutkimuksesta. Intensiivihoidon asema on vielä epäselvä myös hidaskasvuisissa lymfoomissa (Armitage 1993, Lazarus 1995). Kuten myeloomassa, myös huonoennusteista non-hodgkin-lymfoomaa sairastavan nuoren potilaan tapauksessa allogeeninen kantasolujen siirto tarjoaa perustellun vaihtoehdon (Chopra ym. 1992, Ratanatharathorn ym. 1994). Myös lymfoomissa intensiivihoidon välitön teho on hyvä. Siirron aikaan osittaisen hoitovasteen saaneista potilaistamme kaikki saavuttivat intensiivihoidolla täydellisen remission, minkä odottaisi parantavan ennustetta. Sama odotus kohdistuu toisen remission aikaan hoidettuihin potilaisiin, joiden ennuste tavanomaisia solunsalpaajahoitoja käytettäessä olisi hyvin huono. Kun autologisen siirron jälkeen ilmaantuu lymfooman relapsi, ennuste on nopeakasvuisissa tautimuodoissa huono: keskimääräinen elinaika on selvästi alle vuoden (Vose ym. 1992). Lyhyt elinaika relapsin jälkeen tuli esiin omillakin potilaillamme: keskimääräinen elinaika oli runsas puoli vuotta. Rintasyöpä. Kiinteiden kasvainten intensiivihoito on tullut aikuisillakin merkittäväksi ASCT:n aiheeksi, vaikka tämä hoitomuoto ei ole standardihoito toistaiseksi yhdessäkään kiinteässä syövässä (Schmitz ym. 1996). Vuonna 1994 jo lähes kolmannes Euroopassa tehdyistä autologisista siirroista kohdistui kiinteisiin kasvaimiin, eniten rintasyöpään (Gratwohl ym. 1996a). Pohjois-Amerikassa rintasyöpä on tullut yleisimmäksi ASCT:n aiheeksi. Rintasyövän ASCT:t aloitettiin Suomessa vuonna 1993 (Joensuu ja Remes 1994). Ensimmäinen satunnaistettu tutkimus intensiivihoidosta ja ASCT:stä ja toistaiseksi ainut kiinteiden kasvainten alueella on tehty metastasoituneen tai levinneen rintasyövän ensihoidosta (Bezwoda ym. 1995). Intensiivihoito tuotti enemmän hyviä vasteita ja pidemmän keskimääräisen eliniän kuin tavanomainen solunsalpaajalääkitys (90 ja 45 viikkoa). Tutkimusraporttia seuranneessa pääkirjoituksessa katsottiin kuitenkin tutkimustuloksen antavan toistaiseksi pienehkön potilasmäärän ja lyhyen seurannan takia aiheen lähinnä jatkotutkimusten suunnitteluun mutta ei lopullisiin hoitokäytäntöjä koskeviin päätelmiin (Kennedy 1995). Niinpä intensiivihoito ja ASCT on edelleenkin tutkimuksellinen hoito, jossa potilaat pitäisi niin liitännäishoidossa Luuytimensiirrosta veren kantasolujen siirtoon 225
8 kuin metastaattisen taudin hoidossakin kanavoida prospektiivisiin kliinisiin tutkimuksiin. Tällaisia käynnissä olevia tutkimuksia ovat Pohjoismaiden rintasyöpäryhmän organisoima kainaloon laajalti levinneen huonon ennusteen rintasyövän laaja satunnaistettu tutkimus, jossa potilaat jaetaan intensiivihoitoon ja tavanomaiseen hoitoon (Joensuu 1996), ja Suomessa aloitettu pienen tuumoritaakan metastasoitunutta rintasyöpää sairastavien vastaava hoitovertailu. Nykytiedon perusteella myös rintasyövässä intensiivihoidon käyttö on rajattava tauteihin, jotka vastaavat solunsalpaajiin. Munasarjasyöpä. Prospektiiviset tutkimukset intensiivihoidon ja tavanomaisen hoidon mahdollisen tehoeron selvittämiseksi on käynnistetty myös huonoennusteisen munasarjasyövän osalta. Kontrolloimattomien tutkimusten valossa intensiivihoidon tulokset ovat olleet lupaavia, kun hoito on annettu osana ensihoitoa potilaille, joilla on ollut siirron aikaan vain vähän jäännöstuumoria (Murakami ym. 1994, Benedetti-Panici ym. 1995, Grenman ym. 1996). Molemmat taudin uusiutumisen vuoksi hoitamamme potilaat, joilla hoitoa edeltäneessä leikkauksessa todettiin makroskooppista tuumoria, ovat menehtyneet tautiinsa vuoden kuluessa siirrosta. Niistä seitsemästä potilaasta, joilla todettiin joko histologisesti varmistettu remissio (viisi potilasta) tai mikroskooppista tuumoria imusolmukkeissa (kaksi potilasta), yksi on kuollut (12 kuukaudessa) ja kolmella on todettu taudin uusiutuminen 6 11 kuukauden kuluttua hoidosta. Kolme potilasta on pysynyt kliinisesti oireettomina (5 20 kuukautta siirrosta). Täten vähäinen kasvainmassa hoidon aikaan ei taannut hyvää vastetta, ja onkin pyrittävä löytämään myös muita potilaiden valintaan vaikuttavia ennustekijöitä. Myös optimaalinen solunsalpaajayhdistelmä on vielä avoin (Grenman ym. 1996). Siirteen puhdistus. Taudin uusimisen esto ASCT:n jälkeen on nykyään keskeisiä kysymyksiä. Uusimisen syynä lienee useimmiten intensiivihoidon jälkeinen jäännöstauti, mutta siirteeseen keruuvaiheessa tulleet syöpäsolut voivat myös edistää taudin uusimista (Brenner ym. 1993). Syöpäsolukontaminaation esiintyminen siirteissä on yleistä, joskin verestä kerätyissä tuotteissa sitä esiintyy vähemmän kuin luuytimessä (Gribben ym. 1991, Mariette ym. 1994, Witzig ym. 1995). Syöpäsoluja voidaan vähentää siirteistä mm. fysikaalis-kemiallisin ja immunologisin keinoin, esimerkiksi syöpäsoluihin kohdistettuja monoklonaalisia vasta-aineita käyttäen, sekä kantasolujen eristyksen avulla (Kvalheim 1996). On saatu viitteitä siitä, että käytettäessä puhdistettuja kantasoluja taudin uusiutuminen siirtojen jälkeen on vähäisempää kuin käsittelemättömien kantasolujen siirron jälkeen (Gribben ym. 1991). Alkuvuodesta 1995 lähtien olemme pyrkineet ensisijaisesti eristettyjen kantasolujen siirtoihin non- Hodgkin-lymfoomissa, myeloomassa ja osassa kiinteitä kasvaimia. Tulevaisuus näyttää, onko siirteen puhtausasteella merkitystä niin kauan kuin jäännöstaudin ongelma säilyy nykyisellään. Lopuksi ASCT mahdollistaa syövän suuriannoksisen hoidon. Verestä kerättyjen kantasolujen käyttöön liittyy lyhyt sytopeniavaihe, lyhentynyt sairaalahoidon tarve ja vähäinen kuolleisuus. Suuriannoksinen solunsalpaajahoito on vakiinnuttanut asemansa myelooman ja kohtalaisen tai erittäin nopeakasvuisen uusiutuneen non-hodgkin-lymfooman hoidossa; muut aiheet muotoutuvat kontrolloidun tutkimusnäytön lisääntyessä. Tulevaisuudelta odotetaan tehokkaampia suuriannoshoitoja ja keinoja taudin uusimisen vähentämiseen. Tällaisia keinoja voivat olla siirteiden puhdistus ja suuriannoksisiin lääkityksiin liitettävät immunologiset hoidot. Vakiintuneet autologisten kantasolujen siirron aiheet merkitsevät Suomessa noin 250:tä ASCT-hoitoa vuodessa, ja määrä lisääntynee tulevaisuudessa. Ainakin toistaiseksi yliopistosairaaloiden kapasiteetti riittää tähän hyvin. Intensiivihoidon piiriin kuuluva alle vuotias potilas on heti diagnoosivaiheessa ennen hoitoihin ryhtymistä lähetettävä intensiivihoitoyksikköön hoitosuunnitelman laatimiseksi. Näin vältetään hoidot (esim. alkyloivat solunsalpaajat, kuten melfalaani, ja sädetykset), jotka vaarantaisivat mahdollisen myöhemmän kantasolujen keruun ja siirron. 226 K. Remes ym.
9 Kirjallisuutta Anderson K C: Who benefits from high-dose therapy for multiple myeloma? J Clin Oncol 13: , 1995 Armitage J O: Bone marrow transplantation for indolent lymphomas. Semin Oncol 20: , 1993 Atra A, Pinkerton C R: Autologous stem cell transplantation in solid tumours of childhood. Ann Med 28: , 1996 Attal M, Harousseau J-L, Stoppa A-M, ym.: A prospective, randomized trial of autologous bone marrow transplantation and chemotherapy in multiple myeloma. N Engl J Med 335: 91 97, 1996 Barlogie B: Toward a cure for multiple myeloma? N Engl J Med 325: , 1991 Benedetti-Panici P, Greggi S, Scambia G, ym.: High-dose chemotherapy with autologous peripheral stem cell support in advanced ovarian cancer. Ann Med 27: , 1995 Bensinger W I, Longin K, Appelbaum F, ym.: Peripheral blood stem cells (PBSCs) collected after recombinant granulocyte colony stimulating factor (rhg-csf): an analysis of factors correlating with the tempo of engraftment after transplantation. Br J Haematol 87: , 1994 Bezwoda W R, Seymour L, Dansey R D: High-dose chemotherapy with hematopoietic rescue as primary treatment for metastatic breast cancer: a randomized trial. J Clin Oncol 13: , 1995 Björkstrand B, Goldstone A H, Ljungman P, ym.: Prognostic factors in autologous stem cell transplantation for multiple myeloma: an EBMT registry study. Leuk Lymphoma 15: , 1994 Björkstrand B, Ljungman P, Bird J M, ym.: Double high-dose chemoradiotherapy with autologous stem cell transplantation can induce molecular remissions in multiple myeloma. Bone Marrow Transplant 15: , 1995 Brenner M K, Rill D R, Moen R C, ym.: Gene-marking to trace origin of relapse after autologous bone-marrow transplantation. Lancet 341: 85 86, 1993 Chopra R, Goldstone A H, Philip T, ym.: Autologous versus allogeneic bone marrow transplantation for non-hodgkin s lymphoma: a case-controlled analysis of the European Bone Marrow Transplant Group registry data. J Clin Oncol 10: , 1992 Gahrton G, Tura S, Ljungman P, ym.: Prognostic factors in allogeneic bone marrow transplantation for multiple myeloma. J Clin Oncol 13: , 1995 Gertz M A, Pineda A A, Chen M G, ym.: Refractory and relapsing multiple myeloma treated by blood stem cell transplantation. Am J Med Sci 309: , 1995 Gianni A M, Siena S, Bregni M, ym.: Granulocyte-macrophage colony-stimulating factor to harvest circulating haemopoietic stem cells for autotransplantation. Lancet 2: , 1989 Gratwohl A, Hermans J, Baldomero H: Hematopoietic precursor cell transplants in Europe: activity in Report from the European Group for Blood and Marrow Transplantation (EBMT). Bone Marrow Transplant 17: , 1996(a) Gratwohl A, Hermans J, Baldomero H, ym.: Indications for haemopoietic precursor cell transplants in Europe. Br J Haematol 92: 35 43, 1996(b) Grenman S E, Rantanen V T, Salmi T A: High-dose chemotherapy with autologous stem cell support in advanced ovarian cancer. Ann Med 28: , 1996 Gribben J G, Freedman A S, Neuberg D, ym.: Immunologic purging of marrow assessed by PCR before autologous bone marrow transplantation for B-cell lymphoma. N Engl J Med 325: , 1991 Haas R, Möhle R, Murea S, ym.: Characterization of peripheral blood progenitor cells mobilized by cytotoxic chemotherapy and recombinant human granulocyte colony-stimulating factor. J Hematother 3: , 1994 Haouin C, Lepage E, Gisselbrecht C, ym.: Comparison of autologous bone marrow transplantation with sequential chemotherapy for intermediate-grade and high-grade non-hodgkin s lymphoma in first complete remission: a study of 464 patients. J Clin Oncol 12: , 1994 Harousseau J L, Attal M, Divine M, ym.: Autologous stem cell transplantation after first remission induction treatment in multiple myeloma: a report of the French Registry on autologous transplantation in multiple myeloma. Blood 85: , 1995 Holyoake T L, Franklin I M: Bone marrow transplants from peripheral blood. Set to transform medical oncology. BMJ 309: 4 5, 1994 Iscove N N, Sieber F, Winterhalter K H: Erythroid colony formation in cultures of mouse and human bone marrow: analysis of the requirement for erythropoietin by gel filtration and affinity chromatography on agarose-concanavalin A. J Cell Physiol 83: , 1974 Joensuu H: Autologous stem cell transplantation in breast cancer. Ann Med 28: , 1996 Joensuu H, Remes K: Autologinen kantasolusiirto rintasyövässä. Duodecim 110: , 1994 Johnsen H E for the Nordic Myeloma Study Group laboratories: Report from a Nordic workshop on CD34+ cell analysis: technical recommendations for progenitor cell enumeration in leukapheresis from multiple myeloma patients. J Hematother 4: 21 28, 1995 Kennedy M J: High-dose chemotherapy of breast cancer: is the question answered? J Clin Oncol 13: , 1995 Kvalheim G: Purging of autografts: methods and clinical significance. Ann Med 28: , 1996 Ladenstein R, Hartmann O, Pinkerton C R: The role of megatherapy with autologous bone marrow rescue in solid tumours of childhood. Ann Oncol 4 [Suppl1]: 45 58, 1993 Lazarus H M: Bone marrow transplantation in low-grade non- Hodgkin s lymphoma. Leuk Lymphoma 17: , 1995 Linch D C, Winfield D, Goldstone A H, ym.: Dose intensification with autologous bone-marrow transplantation in relapsed and resistant Hodgkin s disease: results of a BNLI randomised trial. Lancet 341: , 1993 Mariette X, Fermand J-P, Brouet J-C: Myeloma cell contamination of peripheral blood stem cell grafts in patients with multiple myeloma treated by high-dose therapy. Bone Marrow Transplant 14: 47 50, 1994 Murakami M, Shinozuka T, Kuroshima Y, ym.: High-dose chemotherapy with autologous bone marrow transplantation for the treatment of malignant ovarian tumours. Semin Oncol 21 [Suppl]: 29 32, 1994 Philip T, Guglielmi C, Hagenbeek A, ym.: Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-hodgkin s lymphoma. N Engl J Med 333: , 1995 Ratanatharathorn V, Uberti J, Karanes C, ym.: Prospective comparative trial of autologous versus allogeneic bone marrow transplantation in patients with non-hodgkin s lymphoma. Blood 84: , 1994 Remes K, Rajamäki A: Autologous stem cell transplantations. Ann Med 28: 79 81, 1996 Remes K, Matinlauri I, Grenman S, ym.: Daily measurements of blood CD34+ cells after stem cell mobilization predict stem cell yield and post-transplant hematopoietic recovery. J Hematother 6: 13 19, 1997 Schmitz N, Gratwohl A, Goldman J M for Accrediation Sub Committee of the EBMT: Allogeneic and autologous transplantation for haematological diseases, solid tumours and immune disorders. Current practice in Europe in 1996 and proposals for an operational classification. Bone Marrow Transplant 17: , 1996 Schwartzberg L, Birch R, Blanco R, ym: Rapid and sustained hematopoietic reconstitution by peripheral blood stem cell infusion alone following high-dose chemotherapy. Bone Marrow Transplant 11: , 1993 Tricot G, Jagannath S, Vesole D H, ym.: Relapse of multiple myeloma after autologous transplantation: survival after salvage therapy. Bone Marrow Transplant 16: 7 11, 1995 Vandenberghe E A, Goldstone A H: Autologous stem cell transplants in lymphomas. Ann Med 28: , 1996 Luuytimensiirrosta veren kantasolujen siirtoon 227
10 Verdonck L F, van Putten W L J, Hagenbeek A, ym.: Comparison of CHOP chemotherapy with autologous bone marrow transplantation for slowly responding patients with aggressive non- Hodgkin s lymphoma. N Engl J Med 332: , 1995 Vesole D H, Barlogie B, Jagannath S, ym.: High-dose therapy for refractory multiple myeloma: improved prognosis with better supportive care and double transplants. Blood 84: , 1994 Vose J M, Bierman P J, Anderson J R, ym.: Progressive disease after high-dose therapy and autologous transplantation for lymphoid malignancy: clinical course and patient follow-up. Blood 80: , 1992 Witzig T E, Gertz M A, Lust J A, ym.: Serial studies of peripheral blood myeloma cells in patients with multiple myeloma: when is the optimal time for stem cell harvest? Leuk Lymphoma 19: , 1995 KARI REMES, dosentti, erikoislääkäri MAIJA ITÄLÄ, LL, (väit.) erikoislääkäri MARJUT KAUPPILA, LL, erikoislääkäri JUKKA NIKOSKELAINEN, apulaisprofessori AULI TOIVANEN, professori TYKS:n sisätautien klinikka, Turku ALLAN RAJAMÄKI, dosentti, osaston ylilääkäri TARJA-TERTTU PELLINIEMI, dosentti, erikoislääkäri RIITTA VANHARANTA, FM, sairaalakemisti TYKS:n keskuslaboratorion hematologian osasto Turku SEIJA GRENMAN, dosentti, erikoislääkäri TUULA SALMI, dosentti, osastonylilääkäri TYKS:n naistentautien klinikka, Turku RAIJA RISTAMÄKI, LT, erikoislääkäri EEVA SALMINEN, professori TYKS:n syöpätautien klinikka, Turku TOIVO T. SALMI, dosentti, tutkimusjohtaja TYKS:n lastentautien klinikka, Turku Jätetty toimitukselle Hyväksytty julkaistavaksi
Autologiset kantasolusiirrot. aiheet non-hodgkin-lymfoomissa. Esa Jantunen, Taru Kuittinen, Eija Mahlamäki ja Tapio Nousiainen
 Alkuperäistutkimus Autologiset kantasolusiirrot non-hodgkin-lymfoomissa Esa Jantunen, Taru Kuittinen, Eija Mahlamäki ja Tapio Nousiainen Non-Hodgkin-lymfoomat ovat yleisin autologisella kantasolusiirrolla
Alkuperäistutkimus Autologiset kantasolusiirrot non-hodgkin-lymfoomissa Esa Jantunen, Taru Kuittinen, Eija Mahlamäki ja Tapio Nousiainen Non-Hodgkin-lymfoomat ovat yleisin autologisella kantasolusiirrolla
KATSAUS. Suuriannoshoidon ja kantasolusiirtojen aiheet. Tapani Ruutu
 KATSAUS Suuriannoshoidon ja kantasolusiirtojen aiheet Tapani Ruutu Kantasolusiirron avulla voidaan lisätä pahanlaatuisen veritaudin solunsalpaaja- ja sädehoidon voimakkuutta ja suurentaa taudin paranemistodennäköisyyttä.
KATSAUS Suuriannoshoidon ja kantasolusiirtojen aiheet Tapani Ruutu Kantasolusiirron avulla voidaan lisätä pahanlaatuisen veritaudin solunsalpaaja- ja sädehoidon voimakkuutta ja suurentaa taudin paranemistodennäköisyyttä.
Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö)
 Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö) SISÄLLYS Käytetyt lyhenteet... 2 Yksikön esittely... 3 Konventionaalinen syöpähoito... 3 1. Yleiset tunnusluvut... 3 2. Leukemiat...
Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö) SISÄLLYS Käytetyt lyhenteet... 2 Yksikön esittely... 3 Konventionaalinen syöpähoito... 3 1. Yleiset tunnusluvut... 3 2. Leukemiat...
Myelooman muuttuva hoito
 Katsaus Esa Jantunen Myelooman muuttuva hoito Viime vuosina autologinen kantasolusiirto on vakiinnuttanut asemansa nuorempien myeloomapotilaiden hoidossa, ja talidomidia käytetään entistä useammin osana
Katsaus Esa Jantunen Myelooman muuttuva hoito Viime vuosina autologinen kantasolusiirto on vakiinnuttanut asemansa nuorempien myeloomapotilaiden hoidossa, ja talidomidia käytetään entistä useammin osana
Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö)
 Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö) SISÄLLYS Käytetyt lyhenteet... Yksikön esittely... Kansainväliset/pohjoismaiset tutkimus- ja hoito-ohjelmat, joissa olemme jo
Koonneet: Mervi Taskinen Jaana Vettenranta Kim Vettenranta (vastuuhenkilö) SISÄLLYS Käytetyt lyhenteet... Yksikön esittely... Kansainväliset/pohjoismaiset tutkimus- ja hoito-ohjelmat, joissa olemme jo
Neuroendokriinisten syöpien lääkehoito
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen
 Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Transplant eligible ensilinjan hoito
 Transplant eligible ensilinjan hoito Ohje koskee hyväkuntoisia 70-75-vuotiaita potilaita Sytogenetiikka kaikilta Korkean riskin sytogenetiikka: del17p ( 20%), t(4;14),+1q, t(14;16), t(14;20) Potilaat pyritään
Transplant eligible ensilinjan hoito Ohje koskee hyväkuntoisia 70-75-vuotiaita potilaita Sytogenetiikka kaikilta Korkean riskin sytogenetiikka: del17p ( 20%), t(4;14),+1q, t(14;16), t(14;20) Potilaat pyritään
Krooninen lymfaattinen leukemia (KLL) on
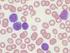 KATSAUS Kroonisen lymfaattisen leukemian nykyhoito Maija Itälä Krooninen lymfaattinen leukemia on länsimaiden yleisin leukemia, ja sitä on totuttu hoitamaan kaikilla terveydenhuollon tasoilla. Alkyloiva
KATSAUS Kroonisen lymfaattisen leukemian nykyhoito Maija Itälä Krooninen lymfaattinen leukemia on länsimaiden yleisin leukemia, ja sitä on totuttu hoitamaan kaikilla terveydenhuollon tasoilla. Alkyloiva
Uudet lääkkeet pidentävät myeloomapotilaiden elinaikaa
 Tieteessä alkuperäistutkimus Maria Salminen LK TY, lääketieteellinen tiedekunta Tommi Kauko VTM, biostatistikko Turun yliopisto, lääketieteellinen tiedekunta, kliininen laitos, biostatistiikka Mervi Putkonen
Tieteessä alkuperäistutkimus Maria Salminen LK TY, lääketieteellinen tiedekunta Tommi Kauko VTM, biostatistikko Turun yliopisto, lääketieteellinen tiedekunta, kliininen laitos, biostatistiikka Mervi Putkonen
WALDENSTRÖ MIN MAKRÖGLÖBULINEMIAN HÖITÖ- ÖHJELMIA
 WALDENSTRÖ MIN MAKRÖGLÖBULINEMIAN HÖITÖ- ÖHJELMIA Waldenströmin taudin kansallinen hoito-ohje löytyy www.hematology.fi sivustolta: https://www.hematology.fi/fi/hoito-ohjeet/veritaudit/plasmasolutaudit/waldenstromin-tauti
WALDENSTRÖ MIN MAKRÖGLÖBULINEMIAN HÖITÖ- ÖHJELMIA Waldenströmin taudin kansallinen hoito-ohje löytyy www.hematology.fi sivustolta: https://www.hematology.fi/fi/hoito-ohjeet/veritaudit/plasmasolutaudit/waldenstromin-tauti
ALL2000_Amendment_2014
 ALL2000_Amendment_2014 Hoito-ohjelmaa voidaan käyttää yli 15-vuotiaiden T- tai B-ALL-potilaiden hoidossa. ALL2000_amendement_2014 koostuu induktiohoidosta, viidestä konsolidaatiohoidosta ja ylläpitohoidosta.
ALL2000_Amendment_2014 Hoito-ohjelmaa voidaan käyttää yli 15-vuotiaiden T- tai B-ALL-potilaiden hoidossa. ALL2000_amendement_2014 koostuu induktiohoidosta, viidestä konsolidaatiohoidosta ja ylläpitohoidosta.
Allogeenisten kantasolujensiirtojen kehityssuunnat ja niiden heijastuminen Turun siirtokeskuksen toimintaan ja tuloksiin
 Katsaus KARI REMES, SINI LUOMA, TOIVO T. SALMI, TARJA-TERTTU PELLINIEMI, MAIJA ITÄLÄ, MARJUT KAUPPILA, JUKKA NIKOSKELAINEN, MERVI PUTKONEN, VELI KAIRISTO, ALLAN RAJAMÄKI, ANRI TIENHAARA, SEPPO PYRHÖNEN
Katsaus KARI REMES, SINI LUOMA, TOIVO T. SALMI, TARJA-TERTTU PELLINIEMI, MAIJA ITÄLÄ, MARJUT KAUPPILA, JUKKA NIKOSKELAINEN, MERVI PUTKONEN, VELI KAIRISTO, ALLAN RAJAMÄKI, ANRI TIENHAARA, SEPPO PYRHÖNEN
Granulosyyttikasvutekijöiden käyttöaiheet. Erkki Elonen
 LÄÄKEVAAKA Granulosyyttikasvutekijöiden käyttöaiheet Erkki Elonen Vaikea neutropenia altistaa vaarallisille infektioille. Granulosyyttikasvutekijät ovat parantaneet granulosytopeniapotilaiden elämänlaatua
LÄÄKEVAAKA Granulosyyttikasvutekijöiden käyttöaiheet Erkki Elonen Vaikea neutropenia altistaa vaarallisille infektioille. Granulosyyttikasvutekijät ovat parantaneet granulosytopeniapotilaiden elämänlaatua
MYELOOMAN HOITO-OHJE. Sisällysluettelo. Suomen myeloomaryhmän (FMG) hoitosuositus 11/2017
 MYELOOMAN HOITO-OHJE Suomen myeloomaryhmän (FMG) hoitosuositus 11/2017 Sisällysluettelo 1. Kantasolusiirtoon soveltuvat ensilinjan hoito... 2 1.1. Induktiohoito... 2 1.2. Omien kantasolujen mobilisaatio...
MYELOOMAN HOITO-OHJE Suomen myeloomaryhmän (FMG) hoitosuositus 11/2017 Sisällysluettelo 1. Kantasolusiirtoon soveltuvat ensilinjan hoito... 2 1.1. Induktiohoito... 2 1.2. Omien kantasolujen mobilisaatio...
MITÄ UUTTA SARKOOMIEN HOIDOSSA?
 MITÄ UUTTA SARKOOMIEN HOIDOSSA? O S A S T O N Y L I L Ä Ä K Ä R I M A I J A T A R K K A N E N H Y K S S Y Ö P Ä K E S K U S LUENNON SISÄLTÖ luu- ja pehmytkudossarkoomat ei pediatrisia tutkimuksia ei gynekologisia
MITÄ UUTTA SARKOOMIEN HOIDOSSA? O S A S T O N Y L I L Ä Ä K Ä R I M A I J A T A R K K A N E N H Y K S S Y Ö P Ä K E S K U S LUENNON SISÄLTÖ luu- ja pehmytkudossarkoomat ei pediatrisia tutkimuksia ei gynekologisia
Syövän solunsalpaajahoidon keskeisimpiä
 Syöpäpotilaan infektiot Valkosolukasvutekijät pahanlaatuisten tautien tukihoitona Pekka Riikonen, Erkki Elonen ja Lasse Teerenhovi Solunsalpaajat ovat keskeinen osa monen syövän hoitoa. Niiden vaikutus
Syöpäpotilaan infektiot Valkosolukasvutekijät pahanlaatuisten tautien tukihoitona Pekka Riikonen, Erkki Elonen ja Lasse Teerenhovi Solunsalpaajat ovat keskeinen osa monen syövän hoitoa. Niiden vaikutus
MYELOOMAN HOITO-OHJE. Sisällysluettelo. Suomen myeloomaryhmän (FMG) hoitosuositus 2019
 MYELOOMAN HOITO-OHJE Suomen myeloomaryhmän (FMG) hoitosuositus 2019 Sisällysluettelo 1. Kantasolusiirtoon soveltuvat ensilinjan hoito... 2 1.1. Induktiohoito...3 1.2. Omien kantasolujen mobilisaatio...4
MYELOOMAN HOITO-OHJE Suomen myeloomaryhmän (FMG) hoitosuositus 2019 Sisällysluettelo 1. Kantasolusiirtoon soveltuvat ensilinjan hoito... 2 1.1. Induktiohoito...3 1.2. Omien kantasolujen mobilisaatio...4
ISLABin kantasolulaboratorio Autologisia kantasolusiirteitä intensiivihoidon tueksi
 ISLABin kantasolulaboratorio Autologisia kantasolusiirteitä intensiivihoidon tueksi Eija Mahlamäki erikoislääkäri Itä-Suomen laboratoriokeskuksen liikelaitoskuntayhtymä 23.10.2013 Hematopoieettisten kantasolujen
ISLABin kantasolulaboratorio Autologisia kantasolusiirteitä intensiivihoidon tueksi Eija Mahlamäki erikoislääkäri Itä-Suomen laboratoriokeskuksen liikelaitoskuntayhtymä 23.10.2013 Hematopoieettisten kantasolujen
Radioimmunoterapia B-solulymfoomien hoidossa
 Sirpa Leppä ja Tuula Lehtinen KATSAUS Radioimmunoterapia B-solulymfoomien hoidossa B-lymfosyytin CD20-pinta-antigeenin tunnistavat radioaktiiviset monoklonaaliset vasta-aineet ovat osoittautuneet tehokkaiksi
Sirpa Leppä ja Tuula Lehtinen KATSAUS Radioimmunoterapia B-solulymfoomien hoidossa B-lymfosyytin CD20-pinta-antigeenin tunnistavat radioaktiiviset monoklonaaliset vasta-aineet ovat osoittautuneet tehokkaiksi
Follikulaarisen lymfooman nykyhoito
 Follikulaarisen lymfooman nykyhoito Follikulaariseen lymfoomaan sairastui Suomen syöpärekisterin tuoreimpien tilastojen mukaan vuonna 2014 kaikkiaan 228 potilasta. 1 Tämä tarkoittaa noin viidesosaa kaikista
Follikulaarisen lymfooman nykyhoito Follikulaariseen lymfoomaan sairastui Suomen syöpärekisterin tuoreimpien tilastojen mukaan vuonna 2014 kaikkiaan 228 potilasta. 1 Tämä tarkoittaa noin viidesosaa kaikista
Läpimurto ms-taudin hoidossa?
 Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Esa Jantunen, professori Itä-Suomen yliopisto ja Siunsote Erikoistuvien päivät Kuopio
 Esa Jantunen, professori Itä-Suomen yliopisto ja Siunsote Erikoistuvien päivät Kuopio 12.04.2019 SYNNINTUNNUSTUKSET Advisory board: Genzyme/Sanofi, Amgen, Takeda, TEVA International meetings: Celgene,
Esa Jantunen, professori Itä-Suomen yliopisto ja Siunsote Erikoistuvien päivät Kuopio 12.04.2019 SYNNINTUNNUSTUKSET Advisory board: Genzyme/Sanofi, Amgen, Takeda, TEVA International meetings: Celgene,
kertomus 2 Hematologi Aino Lepän
 Toiminta015 kertomus 2 skus e k ä p ö y S S HYK a Hematologi talo Aino Lepän SISÄLLYS Toiminta 2 Toiminnan tulokset 5 Laadunhallinta ja potilasturvallisuus 7 Kehittämisprojektit 8 Käynnissä olevat tutkimukset
Toiminta015 kertomus 2 skus e k ä p ö y S S HYK a Hematologi talo Aino Lepän SISÄLLYS Toiminta 2 Toiminnan tulokset 5 Laadunhallinta ja potilasturvallisuus 7 Kehittämisprojektit 8 Käynnissä olevat tutkimukset
Lymfoomapotilaiden allogeeniset kantasolujensiirrot
 Esa Jantunen, Sirkku Jyrkkiö, Outi Kuittinen, Tuula Lehtinen, Rita Janes, Erkki Elonen ja Liisa Volin Lymfoomapotilaiden allogeeniset kantasolujensiirrot Monien lymfoomatyyppien hoitotulokset ovat parantuneet.
Esa Jantunen, Sirkku Jyrkkiö, Outi Kuittinen, Tuula Lehtinen, Rita Janes, Erkki Elonen ja Liisa Volin Lymfoomapotilaiden allogeeniset kantasolujensiirrot Monien lymfoomatyyppien hoitotulokset ovat parantuneet.
Valtakunnallinen koulutuskoordinaattori: dosentti Päivi Lähteenmäki. Koulutusohjelman vastuuhenkilö ja kuulustelija: Dosentti Päivi Lähteenmäki
 LASTENHEMATOLOGIAN JA -ONKOLOGIAN LISÄKOULUTUSOHJELMA Valtakunnallinen koulutuskoordinaattori: dosentti Päivi Lähteenmäki Koulutusohjelman vastuuhenkilö ja kuulustelija: Dosentti Päivi Lähteenmäki Koulutusohjelman
LASTENHEMATOLOGIAN JA -ONKOLOGIAN LISÄKOULUTUSOHJELMA Valtakunnallinen koulutuskoordinaattori: dosentti Päivi Lähteenmäki Koulutusohjelman vastuuhenkilö ja kuulustelija: Dosentti Päivi Lähteenmäki Koulutusohjelman
Kantasolusiirrot vaikeiden autoimmuunitautien hoitona
 Katsaus Kantasolusiirrot vaikeiden autoimmuunitautien hoitona Esa Jantunen, Riitta Myllykangas-Luosujärvi, Oili Kaipiainen-Seppänen, Eija Mahlamäki ja Tapio Nousiainen Autoimmuunitaudit ovat vaikeusasteeltaan
Katsaus Kantasolusiirrot vaikeiden autoimmuunitautien hoitona Esa Jantunen, Riitta Myllykangas-Luosujärvi, Oili Kaipiainen-Seppänen, Eija Mahlamäki ja Tapio Nousiainen Autoimmuunitaudit ovat vaikeusasteeltaan
Iäkkäiden potilaiden pahanlaatuisten veritautien hoito
 Esa Jantunen, Taru Kuittinen ja Erkki Elonen KATSAUS Iäkkäiden potilaiden pahanlaatuisten veritautien hoito Suuri ja yhä lisääntyvä osa pahanlaatuisiin veritauteihin sairastuvista on iäkkäitä, mutta hoitotutkimuksia
Esa Jantunen, Taru Kuittinen ja Erkki Elonen KATSAUS Iäkkäiden potilaiden pahanlaatuisten veritautien hoito Suuri ja yhä lisääntyvä osa pahanlaatuisiin veritauteihin sairastuvista on iäkkäitä, mutta hoitotutkimuksia
KEUHKOSYÖVÄN SEULONTA. Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema
 KEUHKOSYÖVÄN SEULONTA Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema Seulonta on tiettyyn väestöryhmään kohdistuva tutkimus, jolla pyritään
KEUHKOSYÖVÄN SEULONTA Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema Seulonta on tiettyyn väestöryhmään kohdistuva tutkimus, jolla pyritään
Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku
 1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP
 Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
Kenelle täsmähoitoja ja millä hinnalla?
 Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Kivessyövän hoidossa tapahtuu
 Kivessyövän hoidossa tapahtuu S. Jyrkkiö, Tyks Onkologiapäivät 30.8.2014 Kivessyöpä yleistyy Nordcan database/ylönen O. 1 ST I kivessyöpä: seuranta tai adj hoito? 2 Seminoma ST I SWENOTECA tulokset V 2007-2010
Kivessyövän hoidossa tapahtuu S. Jyrkkiö, Tyks Onkologiapäivät 30.8.2014 Kivessyöpä yleistyy Nordcan database/ylönen O. 1 ST I kivessyöpä: seuranta tai adj hoito? 2 Seminoma ST I SWENOTECA tulokset V 2007-2010
Ei- klassinen nodulaarinen lymfosyyttivaltainen Hodgkinin lymfooma (NLPHL):
 HODGKININ LYMFOOMA Hoitosuositus 12/2013 Suomen Lymfoomaryhmä/ työryhmä: Aromaa- Häyhä Annikka (KYS), Auvinen Päivi (KYS), Böhm Jan (KSKS), Hernberg Micaela (HUS), Jantunen Esa (KYS), Jyrkkiö Sirkku (TYKS),
HODGKININ LYMFOOMA Hoitosuositus 12/2013 Suomen Lymfoomaryhmä/ työryhmä: Aromaa- Häyhä Annikka (KYS), Auvinen Päivi (KYS), Böhm Jan (KSKS), Hernberg Micaela (HUS), Jantunen Esa (KYS), Jyrkkiö Sirkku (TYKS),
Tavallisimmat lymfaattiset sairaudet
 Tavallisimmat lymfaattiset sairaudet Syöpäpäivä 10.5.2016 Mirja Vapaatalo Verisolut Lymfosyytti immunologinen solu, joka osallistuu elimistön puolustukseen infektioita vastaan 20-40% verenkierron valkosoluista
Tavallisimmat lymfaattiset sairaudet Syöpäpäivä 10.5.2016 Mirja Vapaatalo Verisolut Lymfosyytti immunologinen solu, joka osallistuu elimistön puolustukseen infektioita vastaan 20-40% verenkierron valkosoluista
KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito. Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen
 KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen www.hematology.fi KLL:n diagnostiikka, seuranta ja hoito-ohjeet löytyvät täältä: -> Hoito-ohjeet
KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen www.hematology.fi KLL:n diagnostiikka, seuranta ja hoito-ohjeet löytyvät täältä: -> Hoito-ohjeet
AML hoitotutkimuksia. AML-työryhmäkokous
 AML hoitotutkimuksia AML-työryhmäkokous 27.09.2017 Tutkimuskysymyksiä Induktiohoito Remissioiden määrä Hoidon toksisuus Konsolidaatiohoito Relapsin esto (RFS, OS) Hoidon toksisuus AraC annos Antrasykliini
AML hoitotutkimuksia AML-työryhmäkokous 27.09.2017 Tutkimuskysymyksiä Induktiohoito Remissioiden määrä Hoidon toksisuus Konsolidaatiohoito Relapsin esto (RFS, OS) Hoidon toksisuus AraC annos Antrasykliini
Lupaava ensivaiheen syövän hoidon tutkimustulos Lymfoomapotilaiden tautivapaa elinaika voi kaksinkertaistua
 Lupaava ensivaiheen syövän hoidon tutkimustulos Lymfoomapotilaiden tautivapaa elinaika voi kaksinkertaistua Maailman suurimmassa onkologian alan vuosittaisessa kokouksessa ASCOssa Chicagossa on esitetty
Lupaava ensivaiheen syövän hoidon tutkimustulos Lymfoomapotilaiden tautivapaa elinaika voi kaksinkertaistua Maailman suurimmassa onkologian alan vuosittaisessa kokouksessa ASCOssa Chicagossa on esitetty
Seminoman hoito ja seuranta. S. Jyrkkiö
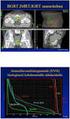 Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka
 Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka Pehmytkudos- ja luusarkoomissa eri hoito-ohjelmat pehmytkudossarkoomissa yleensä kirurgia ensin Onkologinen
Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka Pehmytkudos- ja luusarkoomissa eri hoito-ohjelmat pehmytkudossarkoomissa yleensä kirurgia ensin Onkologinen
HEMATOLOGISTA SYÖPÄÄ SAIRASTAVAN JA KANTASOLUSIIRTEEN SAANEEN POTILAAN KUNTOUTUMINEN
 Opinnäytetyö (AMK) Hoitotyön koulutusohjelma Sairaanhoitaja 2012 Jenny Kultanen & Lilli Mustonen HEMATOLOGISTA SYÖPÄÄ SAIRASTAVAN JA KANTASOLUSIIRTEEN SAANEEN POTILAAN KUNTOUTUMINEN OPINNÄYTETYÖ (AMK)
Opinnäytetyö (AMK) Hoitotyön koulutusohjelma Sairaanhoitaja 2012 Jenny Kultanen & Lilli Mustonen HEMATOLOGISTA SYÖPÄÄ SAIRASTAVAN JA KANTASOLUSIIRTEEN SAANEEN POTILAAN KUNTOUTUMINEN OPINNÄYTETYÖ (AMK)
Pitkävaikutteinen injektiolääke helpottaa psykoosipotilaan hoitoon sitoutumista - Sic!
 Page 1 of 5 JULKAISTU NUMEROSSA 2/2016 TEEMAT Pitkävaikutteinen injektiolääke helpottaa psykoosipotilaan hoitoon sitoutumista Hannu Koponen / Kirjoitettu 8.4.2016 / Julkaistu 3.6.2016 Psykoosipotilaiden
Page 1 of 5 JULKAISTU NUMEROSSA 2/2016 TEEMAT Pitkävaikutteinen injektiolääke helpottaa psykoosipotilaan hoitoon sitoutumista Hannu Koponen / Kirjoitettu 8.4.2016 / Julkaistu 3.6.2016 Psykoosipotilaiden
KATSAUS. Interferonit veritautien hoidossa. Esa Jantunen ja Tapio Nousiainen
 KATSAUS Esa Jantunen ja Tapio Nousiainen Interferonit kuuluvat ns. biologisiin vasteenmuuntajiin, joilla on muun muassa antiproliferatiivisia ja solujen erilaistumista indusoivia ominaisuuksia. Näihin
KATSAUS Esa Jantunen ja Tapio Nousiainen Interferonit kuuluvat ns. biologisiin vasteenmuuntajiin, joilla on muun muassa antiproliferatiivisia ja solujen erilaistumista indusoivia ominaisuuksia. Näihin
Arviointien hyödyntäminen käytännön työssä Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue
 Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Aikuisten akuutti lymfaattinen leukemia 20 vuoden hoitotulokset TYKS:ssa
 Rami Nylund, Maija Itälä-Remes, Tommi Kauko, Marjut Kauppila, Mervi Putkonen, Urpu Salmenniemi, Tommi Salmi ja Kari Remes 20 vuoden hoitotulokset TYKS:ssa 714 Aikuisten akuuttia lymfaattista leukemiaa
Rami Nylund, Maija Itälä-Remes, Tommi Kauko, Marjut Kauppila, Mervi Putkonen, Urpu Salmenniemi, Tommi Salmi ja Kari Remes 20 vuoden hoitotulokset TYKS:ssa 714 Aikuisten akuuttia lymfaattista leukemiaa
Rautaisannos tietoa myeloomapotilaille
 Lukijalle: Multippeli myelooma informaatiopäivä järjestettiin Tampereella 30.10.2010. Informaatiopäivän tarkoituksena oli antaa vertaistukea ja ajankohtaista tietoa myelooma-potilaille, heidän läheisilleen,
Lukijalle: Multippeli myelooma informaatiopäivä järjestettiin Tampereella 30.10.2010. Informaatiopäivän tarkoituksena oli antaa vertaistukea ja ajankohtaista tietoa myelooma-potilaille, heidän läheisilleen,
Levinneen suolistosyövän hoito
 Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 11.5.2016 Fludarabin Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Vaikka kroonisen lymfaattisen leukemian (KLL) esiintyvyys
11.5.2016 Fludarabin Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Vaikka kroonisen lymfaattisen leukemian (KLL) esiintyvyys
Noin kolmasosa non-hodgkin-lymfoomista
 Katsaus MARTINE VORNANEN, MARKKU HEIKKINEN JA ESA JANTUNEN Maha-suolikanava on ekstranodaalisten lymfoomien tavallisin ilmenemispaikka. Valtaosa näistä kasvaimista sijaitsee mahalaukussa. Histologisesti
Katsaus MARTINE VORNANEN, MARKKU HEIKKINEN JA ESA JANTUNEN Maha-suolikanava on ekstranodaalisten lymfoomien tavallisin ilmenemispaikka. Valtaosa näistä kasvaimista sijaitsee mahalaukussa. Histologisesti
Uusin tieto vahvistaa biologisen reumalääkkeen ja. metotreksaatin yhdistelmähoidon tehokkuuden
 Lehdistötiedote 10.6.2004 (julkaistavissa kello 11.15) Uusin tieto vahvistaa biologisen reumalääkkeen ja metotreksaatin yhdistelmähoidon tehokkuuden Kansainvälisen TEMPO- nivelreumatutkimuksen toisen vuoden
Lehdistötiedote 10.6.2004 (julkaistavissa kello 11.15) Uusin tieto vahvistaa biologisen reumalääkkeen ja metotreksaatin yhdistelmähoidon tehokkuuden Kansainvälisen TEMPO- nivelreumatutkimuksen toisen vuoden
Matalamman riskin AML. Ei uusia täsmälääkkeitä Onko hoitotuloksia siten mahdollista saada paremmaksi
 Matalamman riskin AML Ei uusia täsmälääkkeitä Onko hoitotuloksia siten mahdollista saada paremmaksi 1. AI-induktio Nykyinen hoito 2. Mito-HDAraC induktio Mitoksantoni 4 pv + HDAraC 16 g/m2 8 g/m2 4 g/m2
Matalamman riskin AML Ei uusia täsmälääkkeitä Onko hoitotuloksia siten mahdollista saada paremmaksi 1. AI-induktio Nykyinen hoito 2. Mito-HDAraC induktio Mitoksantoni 4 pv + HDAraC 16 g/m2 8 g/m2 4 g/m2
Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
PET-tutkimusten vaikuttavuus ja kustannukset. Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala
 PET-tutkimusten vaikuttavuus ja kustannukset Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala ISI Web of Science: hakusana PET/CT N = 4974, 27.4.2010 Mihin diagnostisia menetelmiä tarvitaan?
PET-tutkimusten vaikuttavuus ja kustannukset Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala ISI Web of Science: hakusana PET/CT N = 4974, 27.4.2010 Mihin diagnostisia menetelmiä tarvitaan?
Uutta lääkkeistä: Vemurafenibi
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Syövän lääkkeet muuttuvat eläviksi CAR-Tsolut
 Page 1 of 7 JULKAISTU NUMEROSSA 3/2018 BIOLOGISET LÄÄKKEET Syövän lääkkeet muuttuvat eläviksi CAR-Tsolut tulevat Olli Tenhunen, Piia Rannanheimo, Heli Suila / Kirjoitettu 12.11.2018 / Julkaistu 13.11.2018
Page 1 of 7 JULKAISTU NUMEROSSA 3/2018 BIOLOGISET LÄÄKKEET Syövän lääkkeet muuttuvat eläviksi CAR-Tsolut tulevat Olli Tenhunen, Piia Rannanheimo, Heli Suila / Kirjoitettu 12.11.2018 / Julkaistu 13.11.2018
Lapsuusiän syövän hoitotulokset TAYS-piirin alueella
 Laura Palonkoski, Olli Lohi, Mikko Arola ja Kim Vettenranta ALKUPERÄISTUTKIMUS Lapsuusiän syövän hoitotulokset TAYS-piirin alueella Johdanto: Lapsuusiän syövän hoitotulokset ovat parantuneet merkittävästi
Laura Palonkoski, Olli Lohi, Mikko Arola ja Kim Vettenranta ALKUPERÄISTUTKIMUS Lapsuusiän syövän hoitotulokset TAYS-piirin alueella Johdanto: Lapsuusiän syövän hoitotulokset ovat parantuneet merkittävästi
Jukka Hytönen Kliinisen mikrobiologian erikoislääkäri UTULab Bakteeriserologia
 Bordetella pertussis Laboratorion näkökulma Jukka Hytönen Kliinisen mikrobiologian erikoislääkäri UTULab Bakteeriserologia SIDONNAISUUDET Asiantuntija Labquality Ammatinharjoittaja Mehiläinen Apurahoja:
Bordetella pertussis Laboratorion näkökulma Jukka Hytönen Kliinisen mikrobiologian erikoislääkäri UTULab Bakteeriserologia SIDONNAISUUDET Asiantuntija Labquality Ammatinharjoittaja Mehiläinen Apurahoja:
KATSAUS. Soluterapia. Kari Remes
 KATSAUS Kari Remes on osa nykyaikaista hematologista hoitovalikoimaa. Se on nopeasti kehittyvä ala, jolla on paljon yhteyksiä solu- ja molekyylibiologiaan, virologiaan, immunologiaan sekä solulaskennan
KATSAUS Kari Remes on osa nykyaikaista hematologista hoitovalikoimaa. Se on nopeasti kehittyvä ala, jolla on paljon yhteyksiä solu- ja molekyylibiologiaan, virologiaan, immunologiaan sekä solulaskennan
Oppimistavoitteet. Syöpien esiintyvyys, ennuste, hoito ja tutkimus. Syöpien esiintyvyys. Suomen syöpärekisteri. Lisäksi
 Oppimistavoitteet Syöpien esiintyvyys, ennuste, hoito ja tutkimus Sirpa Leppä, professori Syöpätautien klinikka Hankkia yleiskäsitys syövän yleisyydestä, yleisimpien syöpien sairastavuudesta ja kuolleisuudesta
Oppimistavoitteet Syöpien esiintyvyys, ennuste, hoito ja tutkimus Sirpa Leppä, professori Syöpätautien klinikka Hankkia yleiskäsitys syövän yleisyydestä, yleisimpien syöpien sairastavuudesta ja kuolleisuudesta
Lapsi ja nuori syöpäpotilaana. Carea, Kymenlaakson Syöpäyhdistys, Sylva Toivo Salmi 20.3.2014
 Lapsi ja nuori syöpäpotilaana Carea, Kymenlaakson Syöpäyhdistys, Sylva Toivo Salmi 20.3.2014 Lasten ja nuorten syöpä, lukumäärät 0-14 vuotiaat n.150 uutta tapausta vuosittain 15-24 vuotiaat n. 140 uutta
Lapsi ja nuori syöpäpotilaana Carea, Kymenlaakson Syöpäyhdistys, Sylva Toivo Salmi 20.3.2014 Lasten ja nuorten syöpä, lukumäärät 0-14 vuotiaat n.150 uutta tapausta vuosittain 15-24 vuotiaat n. 140 uutta
Diagnostiikka. Non-Hodgkin-lymfoomat. Hoito. Follikulaarinen lymfooma. Kasvainkuorman ja levinneisyyden selvittely
 Lymfoomat Non-Hodgkin-lymfoomat n. 1000/v Hodgkin-lymfooma n. 120/v Noin 5 % kaikista syövistä Lymfoomien etiologia Tuntematon Immuunipuutos synnynnäiset immuunipuutostaudit elimensiirrot HIV EB-virus
Lymfoomat Non-Hodgkin-lymfoomat n. 1000/v Hodgkin-lymfooma n. 120/v Noin 5 % kaikista syövistä Lymfoomien etiologia Tuntematon Immuunipuutos synnynnäiset immuunipuutostaudit elimensiirrot HIV EB-virus
Mitä uutta lymfoomien hoitokäytännöissä? S. Jyrkkiö, TYKS Onkologiapäivät 30.8.13
 Mitä uutta lymfoomien hoitokäytännöissä? S. Jyrkkiö, TYKS Onkologiapäivät 30.8.13 N=549 FU 45 kk PFS 69 vs 31 kk R-B R-CHOP Alopecia 0 % 100 % Hematol toksisuus 30 68 Infektiot 37 50 Neuropatia 7 29 Stomatiitti
Mitä uutta lymfoomien hoitokäytännöissä? S. Jyrkkiö, TYKS Onkologiapäivät 30.8.13 N=549 FU 45 kk PFS 69 vs 31 kk R-B R-CHOP Alopecia 0 % 100 % Hematol toksisuus 30 68 Infektiot 37 50 Neuropatia 7 29 Stomatiitti
Uutta melanoomasta. Pia Vihinen TYKS/Syöpäklinikka. Tutkimukset kun epäilet melanooman leviämistä
 Uutta melanoomasta Pia Vihinen TYKS/Syöpäklinikka Tutkimukset kun epäilet melanooman leviämistä Vartalon TT tutkimus tai PET-TT Verikokeet; Hb, maksa-arvot, krea Korkea LDH huonon ennusteen merkki PAD:
Uutta melanoomasta Pia Vihinen TYKS/Syöpäklinikka Tutkimukset kun epäilet melanooman leviämistä Vartalon TT tutkimus tai PET-TT Verikokeet; Hb, maksa-arvot, krea Korkea LDH huonon ennusteen merkki PAD:
Fer$litee$n säästävä munasarjasyöpäkirurgia. Erikoislääkäri, LT Annika Auranen TYKS Naistenklinikka GKS koulutuspäivät 27.9.2013
 Fer$litee$n säästävä munasarjasyöpäkirurgia Erikoislääkäri, LT Annika Auranen TYKS Naistenklinikka GKS koulutuspäivät 27.9.2013 Sidonnaisuudet kahden viimeisen vuoden ajalta LT, naistentau$en ja synnytysten
Fer$litee$n säästävä munasarjasyöpäkirurgia Erikoislääkäri, LT Annika Auranen TYKS Naistenklinikka GKS koulutuspäivät 27.9.2013 Sidonnaisuudet kahden viimeisen vuoden ajalta LT, naistentau$en ja synnytysten
Tervekudosten huomiointi rinnan sädehoidossa
 Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
TerveysInfo. GIST potilaan opas Oppaassa kerrotaan GISTin hoidosta, täsmälääkehoidosta sekä siitä mistä ja miten sairastunut saa apua.
 TerveysInfo Cancerpatientens sociala förmåner Syöpäpotilaan sosiaalietuudet pähkinänkuoressa. Maksuton yksityishenkilöille, yhteisöille 2 e/kpl, A5, 44 sivua http:///@bin/270880/sosedut netti_ru. Hakusanat:
TerveysInfo Cancerpatientens sociala förmåner Syöpäpotilaan sosiaalietuudet pähkinänkuoressa. Maksuton yksityishenkilöille, yhteisöille 2 e/kpl, A5, 44 sivua http:///@bin/270880/sosedut netti_ru. Hakusanat:
Diffuusin suurisoluisen B-solulymfooman (DLBCL) hoitosuositus Versio II
 Suomen lymfoomaryhmä Versio I 9.5.2007 Versio II 12.5.2014 Diffuusin suurisoluisen B-solulymfooman (DLBCL) hoitosuositus Versio II Sisältö sivu Diagnostiikka 2 Levinneisyysselvittely 2 Ennustetekijät 4
Suomen lymfoomaryhmä Versio I 9.5.2007 Versio II 12.5.2014 Diffuusin suurisoluisen B-solulymfooman (DLBCL) hoitosuositus Versio II Sisältö sivu Diagnostiikka 2 Levinneisyysselvittely 2 Ennustetekijät 4
Hodgkinin taudin hoidon myöhäiset sivuvaikutukset. Marjo Pajunen
 Tapausselostus Hodgkinin taudin hoidon myöhäiset sivuvaikutukset Marjo Pajunen Sädehoidon aiheuttamat myöhäiset, vakavat sivuvaikutukset ovat suhteellisen harvinaisia. Hodgkinin taudissa hoitotulokset
Tapausselostus Hodgkinin taudin hoidon myöhäiset sivuvaikutukset Marjo Pajunen Sädehoidon aiheuttamat myöhäiset, vakavat sivuvaikutukset ovat suhteellisen harvinaisia. Hodgkinin taudissa hoitotulokset
LIITE I LUETTELO LÄÄKEVALMISTEEN NIMISTÄ, LÄÄKEMUODOSTA, VAHVUUDESTA, ANTOREITISTÄ, HAKIJASTA JA MYYNTILUVAN HALTIJASTA JÄSENVALTIOISSA
 LIITE I LUETTELO LÄÄKEVALMISTEEN NIMISTÄ, LÄÄKEMUODOSTA, VAHVUUDESTA, ANTOREITISTÄ, HAKIJASTA JA MYYNTILUVAN HALTIJASTA JÄSENVALTIOISSA 1 Jäsenvaltio EU/ETA Itävalta Belgia Tanska Suomi Ranska Irlanti
LIITE I LUETTELO LÄÄKEVALMISTEEN NIMISTÄ, LÄÄKEMUODOSTA, VAHVUUDESTA, ANTOREITISTÄ, HAKIJASTA JA MYYNTILUVAN HALTIJASTA JÄSENVALTIOISSA 1 Jäsenvaltio EU/ETA Itävalta Belgia Tanska Suomi Ranska Irlanti
TerveysInfo. GIST potilaan opas Oppaassa kerrotaan GISTin hoidosta, täsmälääkehoidosta sekä siitä mistä ja miten sairastunut saa apua.
 TerveysInfo Cancerpatientens sociala förmåner Syöpäpotilaan sosiaalietuudet pähkinänkuoressa. Maksuton yksityishenkilöille, yhteisöille 2 e/kpl, A5, 44 sivua http:///@bin/270880/sosedut netti_ru. Hakusanat:
TerveysInfo Cancerpatientens sociala förmåner Syöpäpotilaan sosiaalietuudet pähkinänkuoressa. Maksuton yksityishenkilöille, yhteisöille 2 e/kpl, A5, 44 sivua http:///@bin/270880/sosedut netti_ru. Hakusanat:
LYMFOSYTOOSIT SANOIN JA KUVIN. Pentti Mäntymaa TAYS, Laboratoriokeskus
 LYMFOSYTOOSIT SANOIN JA KUVIN Pentti Mäntymaa TAYS, Laboratoriokeskus Lymfosytoosin määritelmä veren lymfosyyttien määrä >3.5 x 10 9 /l lymfosyyttien kohonnut %-osuus erittelyjakaumassa voi johtua joko
LYMFOSYTOOSIT SANOIN JA KUVIN Pentti Mäntymaa TAYS, Laboratoriokeskus Lymfosytoosin määritelmä veren lymfosyyttien määrä >3.5 x 10 9 /l lymfosyyttien kohonnut %-osuus erittelyjakaumassa voi johtua joko
Uutta lääkkeistä: Palbosiklibi
 Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
AML-2018 (päivitetty AML-2012 hoito-ohjelma) Päivitetty AML:n hoito-ohjelma pohjautuu AML 2012-hoito-ohjelmaan. Merkittävimmät muutokset:
 AML-2018 (päivitetty AML-2012 hoito-ohjelma) Päivitetty AML:n hoito-ohjelma pohjautuu AML 2012-hoito-ohjelmaan. Merkittävimmät muutokset: - riskiluokitus ELN 2017 ja luokitus WHO:n 2017 mukaisia - AML-
AML-2018 (päivitetty AML-2012 hoito-ohjelma) Päivitetty AML:n hoito-ohjelma pohjautuu AML 2012-hoito-ohjelmaan. Merkittävimmät muutokset: - riskiluokitus ELN 2017 ja luokitus WHO:n 2017 mukaisia - AML-
 Hoitotehoa ennustavat RAS-merkkiaineet Tärkeä apuväline kolorektaalisyövän lääkehoidon valinnassa Tämän esitteen tarkoitus Tämä esite auttaa ymmärtämään paremmin kolorektaalisyövän erilaisia lääkehoitovaihtoehtoja.
Hoitotehoa ennustavat RAS-merkkiaineet Tärkeä apuväline kolorektaalisyövän lääkehoidon valinnassa Tämän esitteen tarkoitus Tämä esite auttaa ymmärtämään paremmin kolorektaalisyövän erilaisia lääkehoitovaihtoehtoja.
E-vitamiini saattaa lisätä ja vähentää kuolemia
 E-vitamiini saattaa lisätä ja vähentää kuolemia Harri Hemilä Duodecim-lehti Kommentti / Keskustelua Sanoja 386 Tarjottu Duodecim lehteen julkaistavaksi 24.10.2013 Hylätty 29.10.2013 Julkaistu mielipiteenä
E-vitamiini saattaa lisätä ja vähentää kuolemia Harri Hemilä Duodecim-lehti Kommentti / Keskustelua Sanoja 386 Tarjottu Duodecim lehteen julkaistavaksi 24.10.2013 Hylätty 29.10.2013 Julkaistu mielipiteenä
Syöpä lapsella. Kim Vettenranta, dos. Osastonylilääkäri Lasten veri- ja syöpätautien sekä kantasolusiirtoklinikka HYKS
 Syöpä lapsella Kim Vettenranta, dos. Osastonylilääkäri Lasten veri- ja syöpätautien sekä kantasolusiirtoklinikka HYKS Lasten syöpätaudit Leukemiat (30%) Aivotuumorit (28%) Lymfoomat (Hodgkin, NHL) (11%)
Syöpä lapsella Kim Vettenranta, dos. Osastonylilääkäri Lasten veri- ja syöpätautien sekä kantasolusiirtoklinikka HYKS Lasten syöpätaudit Leukemiat (30%) Aivotuumorit (28%) Lymfoomat (Hodgkin, NHL) (11%)
Mitä onkologi toivoo patologilta?
 Mitä onkologi toivoo patologilta? Mikä PAD-lausunnossa vaikuttaa kilpirauhassyövän hoitoon Hanna Mäenpää, dos HUS, Syöpätautien klinikka Onkologian trendejä Entiteetit pirstoutuvat pienemmiksi: lisää tietoa
Mitä onkologi toivoo patologilta? Mikä PAD-lausunnossa vaikuttaa kilpirauhassyövän hoitoon Hanna Mäenpää, dos HUS, Syöpätautien klinikka Onkologian trendejä Entiteetit pirstoutuvat pienemmiksi: lisää tietoa
INFLECTRA SEULONTAKORTTI
 Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
TERVEYS ALKAA TIEDOSTA NAINEN PIDÄ HUOLTA ITSESTÄSI
 TERVEYS ALKAA TIEDOSTA NAINEN PIDÄ HUOLTA ITSESTÄSI 1 RINTAOIREET JA RINTOJEN SEURANTA Jokaisen naisen on syytä pitää huolta rintojensa terveydestä. Rintakuvauksiin tullaan yleensä joko oireettomille tehdyn
TERVEYS ALKAA TIEDOSTA NAINEN PIDÄ HUOLTA ITSESTÄSI 1 RINTAOIREET JA RINTOJEN SEURANTA Jokaisen naisen on syytä pitää huolta rintojensa terveydestä. Rintakuvauksiin tullaan yleensä joko oireettomille tehdyn
Paksunsuolen stenttihoito siltahoito ja palliaatio
 Paksunsuolen stenttihoito siltahoito ja palliaatio Heikki Huhtinen, LT TYKS, vatsaelinkirurgian ja urologian klinikka Gastroenterologiayhdistyksen syyskokous 20.9.2013, Kuopio Sidonnaisuudet Tutkimusrahoitusta
Paksunsuolen stenttihoito siltahoito ja palliaatio Heikki Huhtinen, LT TYKS, vatsaelinkirurgian ja urologian klinikka Gastroenterologiayhdistyksen syyskokous 20.9.2013, Kuopio Sidonnaisuudet Tutkimusrahoitusta
Liite IV. Tieteelliset päätelmät
 Liite IV Tieteelliset päätelmät 1 Tieteelliset päätelmät Euroopan komissiolle ilmoitettiin 10. maaliskuuta 2016, että riippumaton seurantaryhmä (IDMC) oli havainnut, että idelalisibia saaneilla potilailla
Liite IV Tieteelliset päätelmät 1 Tieteelliset päätelmät Euroopan komissiolle ilmoitettiin 10. maaliskuuta 2016, että riippumaton seurantaryhmä (IDMC) oli havainnut, että idelalisibia saaneilla potilailla
Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa
 Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa 2007-2013 1 Sisältö Imukudoksen ja verta muodostavan kudoksen kasvaimien pääryhmät 2 Uudet tapaukset koko maassa sukupuolittain
Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa 2007-2013 1 Sisältö Imukudoksen ja verta muodostavan kudoksen kasvaimien pääryhmät 2 Uudet tapaukset koko maassa sukupuolittain
bukkaalinen fentanyylitabletti Effentora_ohjeet annostitrausta varten opas 6.indd :04:58
 10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
LAPSENA SAIRASTETUN SYÖVÄN (VAKAVAN SAIRAUDEN) MYÖHÄISVAIKUTUKSET
 LAPSENA SAIRASTETUN SYÖVÄN (VAKAVAN SAIRAUDEN) MYÖHÄISVAIKUTUKSET Päivi Lähteenmäki, dosentti, oyl lastentautien ja lasten hematologian el TYKS lastentautien klinikka 27.10.2011 Katsauksen sisältö Tilastotietoja
LAPSENA SAIRASTETUN SYÖVÄN (VAKAVAN SAIRAUDEN) MYÖHÄISVAIKUTUKSET Päivi Lähteenmäki, dosentti, oyl lastentautien ja lasten hematologian el TYKS lastentautien klinikka 27.10.2011 Katsauksen sisältö Tilastotietoja
Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa
 Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa 2008-2014 1 Sisältö Imukudoksen ja verta muodostavan kudoksen kasvaimien pääryhmät 3 Uudet tapaukset koko maassa sukupuolittain
Leukemioiden, lymfoomien ja muiden pahanlaatuisten veritautien ilmaantuvuus Suomessa 2008-2014 1 Sisältö Imukudoksen ja verta muodostavan kudoksen kasvaimien pääryhmät 3 Uudet tapaukset koko maassa sukupuolittain
POTILAAN OSALLISTAMINEN
 POTILAAN OSALLISTAMINEN TUTKIMUKSEN EDISTÄMISTÄ JA HOIDON JATKUVAA LAADUN PARANTAMISTA, CASE HYKS SYÖPÄKESKUS Tuula Helander Kehittämispäällikkö, Hyks Syöpäkeskus, HUS Asiamies, Suomen Syöpäinstituutti
POTILAAN OSALLISTAMINEN TUTKIMUKSEN EDISTÄMISTÄ JA HOIDON JATKUVAA LAADUN PARANTAMISTA, CASE HYKS SYÖPÄKESKUS Tuula Helander Kehittämispäällikkö, Hyks Syöpäkeskus, HUS Asiamies, Suomen Syöpäinstituutti
Ei-klassinen nodulaarinen lymfosyyttivaltainen Hodgkinin lymfooma (NLPHL):
 HODGKININ LYMFOOMA Hoitosuositus 9/2017 Suomen Lymfoomaryhmä/ työryhmä: Aromaa-Häyhä Annikki (KYS), Hernberg Micaela (HUS), Jyrkkiö Sirkku (TYKS), Karjalainen-Lindsberg Marja-Liisa (HUS), Kuittinen Outi
HODGKININ LYMFOOMA Hoitosuositus 9/2017 Suomen Lymfoomaryhmä/ työryhmä: Aromaa-Häyhä Annikki (KYS), Hernberg Micaela (HUS), Jyrkkiö Sirkku (TYKS), Karjalainen-Lindsberg Marja-Liisa (HUS), Kuittinen Outi
Mitä uutta kolorektaalisyövästä?
 Mitä uutta kolorektaalisyövästä? Tapio Salminen, TAYS Valtakunnalliset onkologiapäivät 2013 Metastasoineen taudin hoidon valinnan periaatteet kolorektaalisyövässä Ryhmä 0 R0 resekoitavissa oleva maksa
Mitä uutta kolorektaalisyövästä? Tapio Salminen, TAYS Valtakunnalliset onkologiapäivät 2013 Metastasoineen taudin hoidon valinnan periaatteet kolorektaalisyövässä Ryhmä 0 R0 resekoitavissa oleva maksa
Hoidetun rintasyöpäpotilaan seuranta
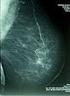 Hoidetun rintasyöpäpotilaan seuranta Tavoitteet Seurannassa pyritään rintasyövän mahdollisen paikallisen uusiutumisen ja vastakkaisen rinnan uuden syövän varhaiseen toteamiseen. Oireettomalle potilaalle
Hoidetun rintasyöpäpotilaan seuranta Tavoitteet Seurannassa pyritään rintasyövän mahdollisen paikallisen uusiutumisen ja vastakkaisen rinnan uuden syövän varhaiseen toteamiseen. Oireettomalle potilaalle
Paraneeko lymfooma vasta-ainehoidolla?
 Sirpa Leppä, Heidi Nyman ja Marja-Liisa Karjalainen-Lindsberg KATSAUS Non-Hodgkin-lymfoomien diagnostiikka on WHO:n luokituksen myötä monipuolistunut ja tarkentunut. Ennustetekijöitä on löytynyt, ja uusia
Sirpa Leppä, Heidi Nyman ja Marja-Liisa Karjalainen-Lindsberg KATSAUS Non-Hodgkin-lymfoomien diagnostiikka on WHO:n luokituksen myötä monipuolistunut ja tarkentunut. Ennustetekijöitä on löytynyt, ja uusia
Rintasyöpä Suomessa. Mammografiapäivät Tampere 26.6.2009. Risto Sankila. Ylilääkäri, Suomen Syöpärekisteri, Helsinki
 Rintasyöpä Suomessa Mammografiapäivät Tampere 26.6.2009 Risto Sankila Ylilääkäri, Suomen Syöpärekisteri, Helsinki Suomen Syöpärekisteri Syöpätautien tilastollinen ja epidemiologinen tutkimuslaitos... syöpärekisteri
Rintasyöpä Suomessa Mammografiapäivät Tampere 26.6.2009 Risto Sankila Ylilääkäri, Suomen Syöpärekisteri, Helsinki Suomen Syöpärekisteri Syöpätautien tilastollinen ja epidemiologinen tutkimuslaitos... syöpärekisteri
kertomus 2 Hematologi Aino Lepän
 Toiminta016 kertomus 2 skus e k ä p ö y S S HYK a Hematologi talo Aino Lepän SISÄLLYS Toiminta 2 Toiminnan tuloksia 5 Laadunhallinta ja potilasturvallisuus 7 Kehittämisprojektit 8 Käynnissä olevat tutkimukset
Toiminta016 kertomus 2 skus e k ä p ö y S S HYK a Hematologi talo Aino Lepän SISÄLLYS Toiminta 2 Toiminnan tuloksia 5 Laadunhallinta ja potilasturvallisuus 7 Kehittämisprojektit 8 Käynnissä olevat tutkimukset
Seminooman sädehoito. Paula Lindholm Tyks, syöpätaudit
 Seminooman sädehoito Paula Lindholm Tyks, syöpätaudit Miten seminooma leviää? 85% kliininen stage I ja 11% st II para-aortaali-imusolmukkeet Ipsilateraaliset parailiakaaliset Ipsilateraalinen munuaishilus
Seminooman sädehoito Paula Lindholm Tyks, syöpätaudit Miten seminooma leviää? 85% kliininen stage I ja 11% st II para-aortaali-imusolmukkeet Ipsilateraaliset parailiakaaliset Ipsilateraalinen munuaishilus
Gynekologisen karsinomakirurgian keskittämine. Eija Tomás, Tays LT, naistentautien ja gynekologisen sädehoidon el
 Gynekologisen karsinomakirurgian keskittämine Eija Tomás, Tays LT, naistentautien ja gynekologisen sädehoidon el Suomessa 5.2 miljoonaa asukasta 5 yliopistosairaalaa 16 keskusairaalaa aluesairaalat ja
Gynekologisen karsinomakirurgian keskittämine Eija Tomás, Tays LT, naistentautien ja gynekologisen sädehoidon el Suomessa 5.2 miljoonaa asukasta 5 yliopistosairaalaa 16 keskusairaalaa aluesairaalat ja
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Zarzio 30 MU/0,5 ml injektio-/infuusioneste, liuos, esitäytetyssä ruiskussa 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml liuosta sisältää 60 miljoonaa
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Zarzio 30 MU/0,5 ml injektio-/infuusioneste, liuos, esitäytetyssä ruiskussa 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml liuosta sisältää 60 miljoonaa
Veren kantasolujen määrää alentavan hoidon (myeloablatiivisen hoidon) jälkeen luuytimensiirron saaneet potilaat
 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Neupogenia voidaan käyttää: - lisäämään veren valkosolujen määrää solunsalpaajahoidon jälkeen infektioiden ehkäisemiseksi. - lisäämään
VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Neupogenia voidaan käyttää: - lisäämään veren valkosolujen määrää solunsalpaajahoidon jälkeen infektioiden ehkäisemiseksi. - lisäämään
Kansaneläkelaitoksen päätös
 Kansaneläkelaitoksen päätös lääketieteellisistä edellytyksistä, jotka sairauden tulee rajoitetusti erityiskorvattavan lääkkeen erityiskorvaamiseksi täyttää. Annettu Helsingissä 31.12.2004 Kansaneläkelaitos
Kansaneläkelaitoksen päätös lääketieteellisistä edellytyksistä, jotka sairauden tulee rajoitetusti erityiskorvattavan lääkkeen erityiskorvaamiseksi täyttää. Annettu Helsingissä 31.12.2004 Kansaneläkelaitos
Keuhkosyövän uudet lääkkeet
 Keuhkosyövän uudet lääkkeet Jarkko Ahvonen Syöpätautien erikoislääkäri Tampereen yliopistollinen sairaala Sidonnaisuudet Asiantuntijapalkkio Boehringer Ingelheim, Bristol-Myers Squibb, Lilly, MSD, Roche
Keuhkosyövän uudet lääkkeet Jarkko Ahvonen Syöpätautien erikoislääkäri Tampereen yliopistollinen sairaala Sidonnaisuudet Asiantuntijapalkkio Boehringer Ingelheim, Bristol-Myers Squibb, Lilly, MSD, Roche
