KEMA211 EPÄORGAANINEN KEMIA 1 (4 op)
|
|
|
- Jorma Ranta
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 KEMA211 EPÄORGAANINEN KEMIA 1 (4 op) Luennot , ti 1215 ja ke 1015, salissa YlistöKem 1 Loppukoe 6.5., klo , salissa MaA 103 Kirjallisuus C.E. Housecroft, A.G. Sharpe Inorganic Chemistry, kolmas painos, Pearson Education, Gosport, 2008 Kurssiin kuuluvat kirjan kappaleet 2, 4-7, 9 Lisäksi kemian nimistö-osio. Companion web site http// Luentomateriaali http//users.jyu.fi/~resillan/kema211 Kurssille ilmoittautumiset Korpin kautta http// Opiskelu Korppi 1
2 1. Peruskäsitteitä 1.1 Yleistä asiaa Jos orgaaninen kemia on hiilen kemiaa, silloin epäorgaaninen kemia on muiden alkuaineiden kemiaa. Raja on kuitenkin epäselvä. Atomien kemialliset ominaisuudet riippuvat niiden elektronirakenteesta. Kemiallisten yhdisteiden ominaisuuksia voidaan osittain ennustaa niiden rakennusosina olevien atomien perusteella. Fysikaalisen kemian tutkimusmenetelmät ovat keskeisessä asemassa kemian salaisuuksien selvittämisessä.
3 Epäorgaaninen kemia tutkii kokeellisesti ja selittää teoreettisesti kaikkien alkuaineiden kaikkien yhdisteiden ominaisuuksia ja reaktiota. Hiilivedyt ja niiden johdannaiset kuuluvat orgaanisen kemian tutkimusalaan, mutta fullereenit ja nanoputket kuuluvat myös epäorgaanisen kemian tutkimusalaan. Epäorgaanisen kemian ytimen muodostaa koordinaatiokemia, joka ulottuu klassisesta siirtymämetallien kompleksiyhdisteistä biologisesti tärkeisiin metallikomplekseihin ja kovalenttisiin organometalliyhdisteisiin.
4 Epäorgaanisen kemian monipuolisuus selviää alla olevasta kaaviosta, johon voidaan lisätä yhteyksiä uusiin tutkimusaloihin. Medicines metallo-oganic compounds New materials coordination polymers
5 2 Peruskäsitteitä Molekyylit 2.1 Sidosmallit Johdanto Historiaa Ennen elektroneja kerrannaisten painosuhteiden laki eli alkuaineet sitoutuvat keskenään tietyn valenssin mukaisesti. Kun elektronit oli keksitty G.N. Lewis ja I. Langmuir Ioniset yhdisteet syntyvät elektronien siirtyessä alkuaineilta toisille (ionisidos). Kovalenttiset yhdisteet syntyvät alkuaineiden keskenään jakamien yhteisten elektronien vaikutuksesta (kovalenttinen sidos). Eräissä tapauksissa yhteiset elektronit (elektronipari) tulevat vain toiselta alkuaineatomilta (koordinaatiosidos, identtinen "normaalin" kovalenttisen sidoksen kanssa). Nykyiset kemiallisen sitoutumisen mallit perustuvat kvanttimekaaniikkaan ja Schrödingerin aaltoyhtälön (likimääräisiin) ratkaisuihin. 2
6 Kaksi mallia on käytössä * Valenssisidosteoria (VB, Valence Bond, kehittäjinä Heitler ja Pauling) Atomit kohtaavat ja molekyyli muodostuu siten, että atomien alkuperäinen luonne (ja sen elektronit) säilyvät sitoutumisessa hyvin pitkälle. * Molekyyliorbitaaliteoria (MO, Molecular Orbital, kehittäjinä Hund ja Mulliken) Atomien orbitaalit menevät päällekkäin (overlap) ja niistä muodostuvat yli koko molekyylin vaikuttavat molekyyliorbitaalit, joille (sidos)elektronit sitten asettuvat. Silloin yksittäisen atomin luonne hämärtyy molekyylissä. Kemiallisen sitoutumisen syvälliseksi ymmärtämiseksi molempien, VB ja MO, teorioiden periaatteet pitää tuntea, koska usein sitoutuminen on selitettävissä näiden kahden teoria "välimaastossa" olevaksi, jolloin toinen näyttää olevan lähempänä "totuutta". "Malleja tulee käyttää, mutta niihin ei pidä uskoa!" Aluksi yksinkertaisin kovalenttisen sitoutumisen malli Lewisin malli 3
7 Lewisin rakenteet Yksinkertainen, mutta hyödyllinen, menetelmä kuvattaessa mille atomille valenssielektronit (eli sidos- ja vapaat elektroniparit) asettuvat molekyylissä. HO H Elektronit pisteillä Sidosel. parit valenssiviivoilla H O H N N N N O O O O Yksinkertaisuudessaan ei pysty kertomaan molekyylin muotoa! Onko HO H vai HO H???? (Tarvitaan lisää tietoa!) 2.2 Homonukleaariset kaksiatomiset molekyylit Valenssisidosteoria (VB, valence bond) Termin homonukleaarinen käyttö Homonukleaarinen kovalenttinen sidos muodostuu kahden samaa alkuainetta olevan atomin välille, esim. H-H sidos H 2 ssa, O=O sidos O 2 ssa ja O-O sidos H 2 O 2 ssa (kuva 2.1). 4
8 5
9 Homonukleaarinen molekyyli sisältää vain yhtä alkuainetta. Kaksiatomiset homonukleaariset molekyylit kuten esim. H 2, O 2, N 2 ja F 2. Kolmiatomiset esim. O 3 ja moniatomiset homonukleaariset molekyylit kuten esim. P 4 ja S 8 (kuva 2.2). 6
10 Kovalenttinen sidospituus, kovalenttinen säde ja van der Waalsin säde Atomien välinen etäisyys eli sidospituus d on perustavaa laatua oleva rakenneparametri. Määritetään spektroskooppisilla ja diffraktiomenetelmillä Kirjassa Box 1.2 ja 6.5 Röntgen- (X-ray) ja neutronidiffraktiot (s,l), elektronidiffraktio (g) On kätevää määritellä atomin kovalenttinen säde r cov Atomin X kovalenttinen säde, r cov, on puolet atomien välisestä etäisyydestä X X sidoksessa. Eri säde sidostyypistä (yksinkertainen, kaksois- vai kolmoissidos) riippuen (kuitenkin sama X!) Atomin X van der Waalsin säde, r v, on puolet kahden toisiaan lähinnä olevan sidokseen osallistumattoman (non-bonded) X atomin välisestä etäisyydestä. 7
11 Kuvan 2.1 pohjaa hyväksi käyttäen r cov (O, single) 2 x r v (H) d O O 8
12 Esim. rikki S 8 (s) pakkautuu kahdella eri tavalla, joista -muoto on tiiviimpi (tiheys = 2,07 g cm 3 ) kuin -muoto (tiheys = 1,94 g cm 3 ). Näissä muodoissa van der Waalsin voimat vaikuttavat molekyylien välillä, ja molekyylien välisten heikkojen van der Waalsin sidosten heikkous paljastuu siinä, että S 8 (s) haihtuu helposti ja S 8 -renkaat säilyvät kaasufaasissa. Siten atomin van der Waalsin säde r v (X) on aina suurempi kuin sen kovalenttinen säde r cov (X) sitoutumisen vahvuudesta johtuen. Säteiden arvoja on kirjan Liitteessä 6. H 2 molekyyli Sitoutumisen valenssisidosmallin (VB) mukainen kuvaus Atomit lähestyvät toisiaan, jolloin niiden välillä tapahtuu vuorovaikutusta. Kun vetyatomit (H A ja H B ) ovat kaukana toisistaan, kumpikin näkee vain oman elektroninsa (1 ja 2) eikä atomien välillä ole vuorovaikutusta. Tätä kuvaa aaltofunktio 1 1 9
13 Kun atomit ovat lähellä toisiaan, ei voida enää sanoa, kumpi elektroni, 1 vai 2, on lähinnä atomia H A tai H B, vaan ne muodostavat sidoselektroniparin vety-ytimien väliseen alueeseen. Tätä tilannetta kuvaa aaltofunktio 2. 2 Jotta molemmat tilanteet tulisivat otettua huomioon kovalenttisen sidoksen muodostuessa, otetaan sitoutumista kuvaava aaltofunktio cov aaltofunktioiden 1 ja 2 lineaarisena kombinaationa ("painotettu yhteenlasku") cov = + = N( ) (2.1) N c 1 1 c 2 N = normitustekijä c 1 ja c 2 ovat tilojen 1 ja 2 painokertoimet (eli kuinka paljon ko. tilaa tulee mukaan sitoumiseen) 10
14 MUTTA! Toinenkin lineaarinen kombinaation voidaan kirjoittaa = N( 1 2 ) (2.2) Elektronien 1 ja 2 spinien osalta + (yht. 2.1) vastaa spinien pariutumista ( ) ja (yht. 2.2) vastaa samansuuntaisia spinejä ( ). Laskemalla + ja kuvaamien tilojen energiat sidospituuden d funktiona saadaan tulokseksi, että n energia on aina voimakkaasti hylkivä (eli korkea, sidosta hajottava) kun taas + n energia saavuttaa minimin dn arvolla 87 pm, joka vastaa H H sidoksen dissosiaatioenergiaa, U = 303 kj mol 1. H 2 n sidosdissosiaatioenergia U määritellään prosessille H 2 (g) 2 H(g) Kokeelliset (so. ei lasketut, vaan mitatut) arvot ovat H 2 (g)lle d = 74 pm ja U = 358 kj mol 1 Eli malli antaa tässä vaiheessa oikeansuuntaisia tuloksia, mutta niissä on vielä (runsaasti) parantamisen varaa! 11
15 Yhtälöä (2.1) voidaan parantaa * kumpikin elektroni varjostaa jonkin verran kummankin ytimen varausta (Z korvataan tehollisella ydinvarauksella Z eff ) * lisätään mahdollisia tiloja molemmat el. voivat olla joko H A lla tai H B lla, eli ioniset tilat tilanne [H A ] + [H B ], jota kuvaa aaltofunktio 3 sekä tilanne [H A ] [H B ] +, jota kuvaa aaltofunktio 4. Aaltofunktio paranee, kun lisätään kovalenttiseen (homopolaariseen eli tasasähköiseen) kuvaukseen ioniset (heteropolaariset) vaikutukset Homonukleaarisissa kaksiatomisissa molekyyleissä molemmat päät ovat samanlaiset, joten 1 n ja 2 n kuvaamat tilanteet ovat yhtä todennäköiset (sama painoarvo), samoin 3 n ja 4 n kuvaamat tilanteet keskenään + = N[( ) + c ( )] (2.3) Merkitsemällä ensimmäistä sulkua kovalenttiseksi osaksi ja toista ioniseksi saadaan mol = N[ cov + c ( ionic )] (2.4) 12
16 Vielä kerran kuvallisesti esitettynä kovalenttinen + 1 H A (1)H B (2) mol = cov + c ion 2 H A (2)H B (1) Tällä mallilla kun c ~ 0,25 d(h H) = 75 pm U = 398 kj mol 1 ioninen Sidospituus ok. Energia vähän parempi, ei hyvä! [H A (1)(2)] H B + H A+ [H B (1)(2)] 13
17 Tilannetta voidaan parantaa tarkemmalla matemaattisella käsittelyllä, mutta kuvauksen havainnollisuus huononee. (VBn matemaattinen jatkokäsittely ei kuulu tämän kurssin piiriin!) H 2 lla tässä kuvauksessa kolme ääritapausta H + H H H H H + Tämä merkintä on molekyylin kovalenttisen sitoutumisen resonanssirakenne, mikään sen kanoninen osarakenne ei esiinny puhtaana, vaan ne sekoittuvat keskenään kukin omalla tietyllä painoarvollaan. Huomaa, että keskimmäinen ( H H ) kuvaa paikallistunutta 2-keskus-2-elektronisidosta. Kukin osarakenne kuvaa paikallistunutta tilannetta, jotka yhdessä johtavat koko molekyylin kattavaan ei-paikallistuneeseen sitoutumisen kuvaukseen. 14
18 Valenssisidosmalli (VB) ja molekyylit F 2, O 2 ja N 2 F 2 Fluoriatomin F perustilan elektronirakenne on [He]2s 2 2p 5 Fluoriatomien parittomat elektronit ennustavat yhden yksinkertaisen kovalenttisen sidoksen F F muodostumista. F 2 n resonanssirakenne F F F + F F F + Tässä kovalenttinen osarakenne on hallitseva. O 2 Happiatomin O perustilan elektronirakenne [He]2s 2 2p 4 ja Hundin säännöt johtavat siihen, että kummallakin happiatomilla on kaksi paritonta elektronia, joten VB ennustaa kaksoissidoksen O=O syntymisen. Koska VB malli lähtee siitä, että elektronit muodostavat pareja niin pitkälle kuin suinkin on mahdollista, se ennustaa, että O 2 olisi diamagneettinen. Diamagneettisessa yhdisteessä kaikki elektronit ovat pariutuneet, magneettikenttä hylkii diamagneettista ainetta. Paramagneettisessa yhdisteessä on yksi tai useampia parittomia elektroneja, magneettikenttä vetää puoleensa paramagneettista ainetta. 15
19 VB mallin yksi huomattavimmista heikkouksista on se, että se ei pysty ennustamaan sitä kokeellista tosiseikkaa, että dihappimolekyyli O 2 on paramagneettinen (2 paritonta el.) N 2 Typpiatomin N perustilan elektronirakenne [He]2s 2 2p 3 ja Hundin säännöt johtavat siihen, että kummallakin typpimatomilla on kolme paritonta elektronia, joten VB ennustaa kolmoissidoksen N N syntymisen. Kovalenttinen osarakenne on resonanssirakenteessa hallitseva ja tuottaa tyydyttävän kuvauksen N 2 n sitoutumiselle. 2.3 Kaksiatomiset homonukleaariset molekyylit Molekyyliorbitaaliteoria (MO) MO-teoria Yleistä Molekyyliorbitaaliteorian (MO) lähtökohtana on se, että laitamme ensin molekyylin atomien ytimet niiden tasapainoasemaan ja sitten muodostamme (laskemme) molekyyliorbitaalit (eli alueet, jotka ulottuvat avaruudessa yli koko molekyylin), joita yksittäinen elektroni voi miehittää (so. voi liikkua molekyyliorbitaalin määräämällä alueella). Kukin molekyyliorbitaali syntyy atomien atomiorbitaalien välisistä vuorovaikutuksista, jotka ovat 16
20 * sallittuja, jos atomiorbitaalien symmetriat ovat keskenään sopivia; * tehokkaita, jos atomiorbitaalien välinen keskinäinen peitto (overlap) on merkittävää; * tehokkaita, jos atomiorbitaalien energiat ovat lähellä toisiaan. Tärkeä perussääntö on se, että muodostettavien molekyyliorbitaalien (MO) lukumäärä pitää olla sama kuin molekyylissä olevien atomien tarkasteltavaksi otettujen atomiorbitaalien lukumäärä. Kutakin MOta vastaa tietty energia ja elektronit asettuvat perustilan energiatiloille aufbau-periaatteen mukaisesti elektronit asettuvat ensin alimmille MOille Hundin sääntöjä "kunnioittaen". Molekyylin kokonaisenergia saadaan molekyyliorbitaalien (elektroni-elektroni vuorovaikutuksella korjattujen) energioiden summana. H 2 molekyyli Sitoutumisen molekyyliorbitaaliteorian (MO) mukainen kuvaus H 2 n molekyyliorbitaalien likimääräinen kuvaus saadaan käsittelemällä niitä atomiorbitaalien lineaarisina kombinaatioina (LCAO, Linear Combination of Atomic Orbitals) Kummallakin vedyllä on yksi 1s atomiorbitaali, olkoon niiden aaltofunktiot 1 ja 2. 17
21 1s orbitaalin aaltofunktion etumerkki voi olla + tai. Kuten seisovassa aaltoliikkeessä samanmerkkiset aallot vahvistavat toisiaan (samassa vaiheessa olevat, in-phase), erimerkkiset (vastakkaisissa vaiheissa olevat, out-of-phase) sammuttavat toisensa, samanmerkkisinä orbitaalit sitovat (bonding), erimerkkisinä hajottavat (antibonding). in phase N ] MO MO MO [ 1 2 * * out of phase N ] MO [ 1 2 (2.5) (2.6) Normitustekijät sisältävät peittointegraalin S, joka kertoo kuinka paljon atomiorbitaalit menevät päällekkäin N 1 2(1 S) 1 2 (2.7) N * 1 2(1 S) 1 2 (2.8) 18
22 H 2 n MO-energiatasokaavio ensin piirretään MO-orbitaalien energiatasot matemaattisten yhdistelmien mukaiseen järjestykseen ja sen jälkeen elektronit sijoitetaan tasoille aufbau-periaatteiden mukaiseen järjestykseen. hajottava MO Punaisella on merkitty MOorbitaalien symmetrianimikointi. sitova MO 19
23 solmupinta 20
24 MOlla on -symmetria, jos se on symmetrinen ytimiä yhdistävän janan suhteen, so. jos orbitaalia pyöritetään yhdysjanan suhteen, sen faasissa (eli vaiheessa) ei tapahdu muutosta. Merkintä * jakaantuu kahteen osaan tarkoittaa, että yhdysjanan suhteen pyöritys ei muuta faasia ja * tarkoittaa, että ytimien välissä on ortogonaalinen solmutaso. Divetymolekyylin H 2 perustilan elektronikonfiguraatio on g (1s) 2 eli g (1s)-MOlla on kahden elektroni (yhden el.parin) miehitys. Kuvasta 2.3 (energiatasokaavio) voidaan päätellä seuraavia asioita 1.) vain el.pareja, joten H 2 n ennustetaan olevan diamagneettinen, kuten on kokeellisesti havaittukin. 2.) muodollinen sidoskertaluku voidaan laskea kaavasta 2.9, jolloin H 2 n sidoskertaluku on yksi (1). Sidoskertaluku = ½ (sidosel.lkm hajottavien el. lkm) (2.9) BO(H 2 ) = ½(2 0) = 1 21
25 Sidoskertalukua ei voida kokeellisesti mitata, mutta mitattujen sidospituuksien ja sidosenergioiden sekä sidoskertaluvun välille saadaan korrelaatiota. Hapettamalla (otetaan el. pois) ja pelkistämällä (lisäämällä el.) molekyyliä MO-diagrammin avulla nähdään miten sidoskertaluku muuttuu eli heikkeneekö vai vahvistuuko sidos. Esim. H 2 [H 2 ] + + e Sidoskertaluku 1 0,5 d(h 2 ) = 74 pm d(h 2+ ) = 105 pm Sidos pitenee U(H 2 ) = 458 kj mol 1 U(H 2+ ) = 269 kj mol 1 Sidos heikkenee Tämän kaltaisiin vertailuihin tulee kuitenkin suhtautua tietyllä varovaisuudella, koska laskettu sidoskertaluku tulee likimääräisestä teoriasta eikä siten ota huomioon kaikkia luonnossa vaikuttavia tekijöitä. Katso esim. M. Kaupp ja Riedel (2004) Inorganica Chimica Acta, vol. 357, s "On the lack of correlation between bond lengths, dissociation energies and force constants the fluorine-substituted ethane homologues" 22
26 Sitoutuminen He 2, Li 2 ja Be 2 molekyyleissä MO teoriaa voidaan soveltaa mille tahansa kaksiatomiselle homonukleaariselle molekyylille. Valenssiatomiorbitaalien lukumäärän kasvaessa MO-diagrammit käyvät mutkikkaammiksi. He 1s 2 He 2 g (1s) 2 * u (1s)2 BO(He 2 ) = ½(2 2 ) = 0 Ei sidosta, molekyyliä ei tunneta (non-existent!) 23
27 Li 2 Li [He]2s 1 (2s) 2 BO(Li 2 ) = ½ (2 0 ) = 1 yksi sigmasidos Li Li 24
28 Be 2 (2s) 2 *(2s) 2 Be 1s 2 2s 2 Tällä kantajoukolla (so. 1s 1, 1s 2, 2s 1 ja 2s 2 ) MO teoria ennustaa, että sidoskertaluku on nolla, ei sidosta, Be 2 ei muodostu! hajottaa sitoo On kuitenkin olemassa kokeellista tietoa Be 2 erittäin pysymätön, d(be-be) = 245 pm ja U = 10 kj mol 1 BO(Be 2 ) = ½ (2 2 ) = 0 25
29 Sitoutuminen F 2 ja O 2 molekyyleissä F atomin valenssikuorella on miehitettyjä 2s ja 2p atomiorbitaaleja, jotka pitää ottaa MO-tarkastelussa huomioon. F 2 ssa sitoutumiseen osallistuvat 2s-2s ja 2p-2p vuorovaikutukset (peitot). Ennen kuin pääsemme eteenpäin, pitää tarkastella millaisia 2p-2p vuorovaikutuksia voi esiintyä. 2p orbitaaleja on kolme kappaletta 2p x, 2p y ja 2p z joiden pallukat (lobes) ovat symmetrisesti asettuneet alaindeksinsä mukaisen koordinaattiakselin suhteen. X 2 -molekyyliä tarkasteltaessa on käytännöllistä asettaa atomi X jollekin koordinaattiakselille. Vaikka valinnassa on kolme vaihtoehtoa, yleensä valitaan z-akseli sidosakseliksi. X X z Tämä valinta määrää sen, miten p-orbitaalit jakautuvat sitoutumisen kannalta kahteen eri joukkoon, jotka johtavat MOden kahteen erilaiseen sidossymmetriaan 1) g (2p z ) sekä 2) u (2p x ) ja u (2p y ). Kuva
30 27
31 on asymmetrinen sidosakselin kierron suhteen (faasi muuttuu). *llä oltava kaksi ominaisuutta a) tarkoittaa, että kierrossa faasi muuttuu ja b) * tarkoitta, että ydinten välissä on toinen solmutaso. 28
32 F 2 B.O. = ½(8 6) = 1 (2s) 2 * (2s) 2 (2p z ) 2 (2p x ) 2 (2p y ) 2 * (2p x ) 2 * (2p y ) 2 29
33 O 2 kokeellista faktaa O 2 kaasu (298 K), 90 Kssa siniseksi nesteeksi. Paramagneettinen (diradikaali, 2 paritonta el.) O [He]2s 2 2p 4 siten O 2 12 valenssielektronia 2. O O eli. O O O Mutta Missä parittomat elektronit?? Yksinkertainen VB antaa saman (virheellisen) selityksen eli vain el. pareja O 2 ssa Mutta MO teoria antaa suoraan oikean selityksen!!!!!! 30
34 kaksi paritonta elektronia! B.O. = ½(8 4) = 2 (2s) 2 * (2s) 2 (2p z ) 2 (2p x ) 2 (2p y ) 2 * (2p x ) 1 * (2p y ) 1 31
35 Mitä tapahtuu, jos s p energiaero on pieni? Hapen ja fluorin tapauksessa ero on suuri, kuten kuvasta näkyy, ja edellä tehty likimääräistys (MOta muodostettaessa s ja p atomiorbitaalit eivät sekoitu keskenään). Boorilla ja hiilellä ero on pieni, joten saman symmetrian omaavat toisiaan energiassa lähellä olevat (MO) orbitaalit sekoittuvat keskenään, vaikutus esitetty kuvassa
36 g (2p)n energia painuu alemmaksi kuin pii-orbitaalien energiat kun siirrytään N 2 sta O 2 teen! (ns. - crossover) 33
37 Koska MO malli on teoreettinen malli, pitää kysyä mitä kokeellista todistusaineistoa on mallin ennustaman - crossover'in tueksi olemassa? Taulukko 2.1 Kaksiatomisten 2. jakson X 2 molekyylien kokeellisia tietoja. X 2 Sidospituus / pm Sidoksen diss. entalpia Sidoskertaluku / kj mol 1 Magneettiset ominaisuudet Li 2 Be 2 B 2 C 2 N 2 O 2 F Diamagneettinen -- Paramagneettinen Diamagneettinen Diamagneettinen Paramagneettinen Diamagneettinen O 2 n paramagneettisuus selittyy vain MOn avulla, VB "menee metsään" riippumatta siitä, tapahtuuko - crossover vai ei. Samoin Li 2 n, C 2 n, N 2 n ja F 2 n diamagneettisuudet ovat sopusoinnussa sekä MOn että VBn kanssa, riippumatta - crossover'ista. B 2 n paramagneettisuus selittyy vain MOlla kuvan 2.9 energiajärjestyksellä, jos - järjestys olisi toinen, B 2 n olisi diamagneettinen vastoin havaintoja. 34
38 Työstetty esimerkki 2.1 MO-teoria, kaksiatomisten molekyylien ominaisuuksien ennustaminen. N N sidoksen diss.entalpiat ovat N 2 ssa 945 kj mol 1 ja [N 2 ] ssa 765 kj mol 1. Selitä miksi näin MO-teoriaa käyttäen ja ennusta onko [N 2 ] dia- vai paramagneettinen. N [He]2s 2 2p 3 N 2 n MO-energiadiagrammi, olettaen, että vain 2s-2s ja 2p-2p vuorovaikutukset ovat merkittäviä, on esitetty kuvassa 2.9. Sen perusteella N 2 n sidoskertaluku on 3. [N 2 ] ssä, olettaen että N 2 n energiakaaviota voidaan käyttää tarkastelun pohjana, lisättävä (pelkistävä) elektroni menee seuraavalla tyhjälle MOlle, joka on hajottava * g (2p). Siten laskettu sidoskertaluku on 2,5 eli sidos on heikompi ja sen dissosiaatioentalpia on alempi kuin N 2 ssa, aivan kuten on kokeellisesti havaittu. [N 2 ] ssa on yksi pariton elektroni hajottavalla * g (2p) orbitaalilla, joten sen ennustetaan olevan paramagneettinen. 35
39 2.4 Oktettisääntö ja isoelektroniset yhdisteet Oktettisääntö 1. rivin p-lohkon alkuaineet Atomi noudattaa oktettisääntöä, jos se elektroneja luovuttamalla, vastaanottamalla tai jakamalla saavuttaa uloimmalle valenssikuorelleen jalokaasun kahdeksan elektronin oktetin eli konfiguraation ns 2 np 6. Ioniset yhdisteet, joissa on ioneja kuten esim. Na + (2s 2 2p 6 ), Mg 2+ (2s 2 2p 6 ), F (2s 2 2p 6 ), Cl (3s 2 3p 6 ) ja O 2 (2s 2 2p 6 ), näyttävät noudattavan oktettisääntöä, mutta niissä ionien väliset sähköstaattiset voimat kompensoivat ioninmuodostusenergiat (eli energiat jotka tarvitaan jotta atomista tulisi ioni), katso luku 6. Yleensä oktettisääntö onkin hyödyllisin sovellettaessa sitä kovalenttisesti sitoutuneisiin p-lohkon alkuaineiden yhdisteisiin. Oktettisääntö auttaa Lewisin kaavojen laadinnassa, esim. CH 4 C 4 val. el. (2s 2 2p 2 ) H 1 val. el. (1s 1 ) H H C H H [BH 4 ] B 4 val. el. (2s 2 2p 1 ) H 1 val. el. (1s 1 ) H H B H H 36
40 [NH 4 ] + N 5 val. el. (2s 2 2p 3 ) H 1 val. el. (1s 1 ) + H H N H H Edellä oktetin muodostukseen osallistuivat sidosel. parit, mutta myös vapaat el. parit voivat osallistua oktetin muodostumiseen, esim. Isoelektroniset yhdisteet H S H H F Jaksollisessa järjestelmässä B, C ja N ovat vierekkäin ja niillä on vastaavasti 3, 4 ja 5 valenssielektronia. Siten B lla, Cllä ja N + lla on kullakin 4 valenssielektronia, mistä johtuen [BH 4 ], CH 4 ja [NH 4 ] + ovat isoelektronisia yhdisteitä. Isoelektronisuus merkitsee usein "sama määrä valenssielektroneja", mutta oikeastaan pitäisi aina kertoa tarkasti mistä on kysymys. Edellä mainitut kolme yhdistettä ovat "isoelektronisia kokonaiselektronimäärän (sisäkuorien + valenssikuoren elektronit) suhteen" kun taas esim. HF, HCl ja HBr ovat "isoelektronisia vain valenssielektronien suhteen". Isoelektronisuus on yksinkertainen mutta tärkeä ja hyödyllinen periaate. Usein keskenään isoelektronisilla yhdisteillä on sama rakenne (isostructural), kuten on laita yhdisteillä [BH 4 ], CH 4 ja [NH 4 ] +. 37
41 Työstetty esimerkki 2.2 Isoelektroniset ionit ja molekyylit Osoita, että N 2 ja [NO] + ovat isoelektroniset. N ryhmässä 15 eli sillä on 5 valenssielektronia O ryhmässä 16 eli sillä on 6 valenssielektronia O + lla on 5 valenssielektronia kuten Nllä. Siten N 2 lla ja [NO] + lla on kummallakin 10 valenssielektronia, joten ne ovat valenssielektronien suhteen isoelektronisia. (Myös samanrakenteisia eli lineaarisia, kummassakin on kolmoissidos, BO = 3). Oktettisääntö raskaammat p-lohkon alkuaineet Mentäessä p-lohkon ryhmässä alaspäin koordinaatioluvut pyrkivät kasvamaan (atomien koko kasvaa ja d-orbitaalit tulevat energiassa edullisemmiksi, eli voivat osallistua sitoutumiseen). Esim. koordinaatioluku 6 esiintyy yhdisteissä SF 6, [PF 6 ] ja [SiF 6 ] 2, kun taas vastaavia yksinkertaisia yhdistetä ei esiinny 1. rivin alkuaineilla O, N ja C. Vastaavasti ryhmä 17 alkuaineiden yhdisteissä kuten ClF 3, BrF 5 ja IF 7 fluori on aina terminaaliatomina ja muodostaa yhden sidoksen. 38
42 ClF 3 n Lewisin (kovalenttinen) rakenne osoittaa, että Cln ympärillä on 10 valenssielektronia eli klooriatomi on "laajentanut oktettiaan". Tällaisia yhdisteitä kutsutaan hypervalenttiksi. F Cl F F F Cl F F Oktetin laajentamiselta vältytään ottamalla mukaan varaukset (ioniset osarakenteet) Cl-atomilla on yksi pariton elektroni (3s 2 3p 5 ) eli se pystyy muodostamaan yhden kovalenttisen sidoksen, kun taas Cl + (3s 2 3p 4 ) on kahden parittoman elektronin ioni, joka pystyy muodostamaan kaksi kovalenttista sidosta. + 2 F Cl + F Cl + F + F F Cl + F F Tämä on yksi VBmallin resonanssirakenteen kanoninen äärimuoto! F Cl + F F F Cl + F F F Cl + F F ClF 3 n VBresonanssirakenne. 39
MUUTOKSET ELEKTRONI- RAKENTEESSA
 MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
MUUTOKSET ELEKTRONI- RAKENTEESSA KEMIAA KAIK- KIALLA, KE1 Ulkoelektronit ja oktettisääntö Alkuaineen korkeimmalla energiatasolla olevia elektroneja sanotaan ulkoelektroneiksi eli valenssielektroneiksi.
ULKOELEKTRONIRAKENNE JA METALLILUONNE
 ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
ULKOELEKTRONIRAKENNE JA METALLILUONNE Palautetaan mieleen jaksollinen järjestelmä ja mitä siitä saa- Kertausta daan irti. H RYHMÄT OVAT SARAKKEITA Mitä sarakkeen numero kertoo? JAKSOT OVAT RIVEJÄ Mitä
Alikuoret eli orbitaalit
 Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Luento 1: Sisältö. Vyörakenteen muodostuminen Molekyyliorbitaalien muodostuminen Atomiketju Energia-aukko
 Luento 1: Sisältö Kemialliset sidokset Ionisidos (suolat, NaCl) Kovalenttinen sidos (timantti, pii) Metallisidos (metallit) Van der Waals sidos (jalokaasukiteet) Vetysidos (orgaaniset aineet, jää) Vyörakenteen
Luento 1: Sisältö Kemialliset sidokset Ionisidos (suolat, NaCl) Kovalenttinen sidos (timantti, pii) Metallisidos (metallit) Van der Waals sidos (jalokaasukiteet) Vetysidos (orgaaniset aineet, jää) Vyörakenteen
Ionisidos ja ionihila:
 YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
Kvanttimekaaninen atomimalli. "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman
 Kvanttimekaaninen atomimalli "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman Tunnin sisältö 1. 2. 3. 4. 5. 6. 7. Kvanttimekaaninen atomimalli Orbitaalit Kvanttiluvut Täyttymisjärjestys
Kvanttimekaaninen atomimalli "Voi hyvin sanoa, että kukaan ei ymmärrä kvanttimekaniikkaa. -Richard Feynman Tunnin sisältö 1. 2. 3. 4. 5. 6. 7. Kvanttimekaaninen atomimalli Orbitaalit Kvanttiluvut Täyttymisjärjestys
Atomin elektronikonfiguraatiot (1)
 Atomin elektronikonfiguraatiot (1) Atomiin sidotun elektronin tilaa kuvataan neljällä kvanttiluvulla: n pääkvattiluku - aaltofunktion eli orbitaalin energia, keskimääräinen etäisyys ytimestä, saa arvot
Atomin elektronikonfiguraatiot (1) Atomiin sidotun elektronin tilaa kuvataan neljällä kvanttiluvulla: n pääkvattiluku - aaltofunktion eli orbitaalin energia, keskimääräinen etäisyys ytimestä, saa arvot
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Orgaaninen reaktio Opettava tutkija Pekka M Joensuu Orgaaniset reaktiot Syyt Pelkkä törmäys ei riitä Varaukset (myös osittaisvaraukset) houkuttelevat molekyylejä
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen Orgaaninen reaktio Opettava tutkija Pekka M Joensuu Orgaaniset reaktiot Syyt Pelkkä törmäys ei riitä Varaukset (myös osittaisvaraukset) houkuttelevat molekyylejä
Kertausta 1.kurssista. KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä. Hiilen isotoopit
 KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
SIDOKSET. Palautetaan mieleen millaisia sidoksia kemia tuntee ja miten ne luokitellaan: Heikot sidokset ovat rakenneosasten välisiä sidoksia.
 SIDOKSET IHMISEN JA ELINYMPÄ- RISTÖN KEMIA, KE2 Palautetaan mieleen millaisia sidoksia kemia tuntee ja miten ne luokitellaan: Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
SIDOKSET IHMISEN JA ELINYMPÄ- RISTÖN KEMIA, KE2 Palautetaan mieleen millaisia sidoksia kemia tuntee ja miten ne luokitellaan: Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin.
 1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
1.2 Elektronin energia Käytetään nykyaikaista kvanttimekaanista atomimallia, Bohrin vetyatomi toimii samoin. -elektronit voivat olla vain tietyillä energioilla (pääkvanttiluku n = 1, 2, 3,...) -mitä kauempana
9. JAKSOLLINEN JÄRJESTELMÄ
 9. JAKSOLLINEN JÄRJESTELMÄ Jo vuonna 1869 venäläinen kemisti Dmitri Mendeleev muotoili ajatuksen alkuaineiden jaksollisesta laista: Jos alkuaineet laitetaan järjestykseen atomiluvun mukaan, alkuaineet,
9. JAKSOLLINEN JÄRJESTELMÄ Jo vuonna 1869 venäläinen kemisti Dmitri Mendeleev muotoili ajatuksen alkuaineiden jaksollisesta laista: Jos alkuaineet laitetaan järjestykseen atomiluvun mukaan, alkuaineet,
Luku 14: Elektronispektroskopia. 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi
 Luku 14: Elektronispektroskopia 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi 1 2-atomisen molekyylin elektronitilan termisymbolia muodostettaessa tärkeä ominaisuus on elektronien
Luku 14: Elektronispektroskopia 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi 1 2-atomisen molekyylin elektronitilan termisymbolia muodostettaessa tärkeä ominaisuus on elektronien
Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012
 Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Aine koostuu atomeista Nimitys tulee sanasta atomos = jakamaton (400 eaa, Kreikka) Atomin kuvaamiseen käytetään atomimalleja Pallomalli
Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Aine koostuu atomeista Nimitys tulee sanasta atomos = jakamaton (400 eaa, Kreikka) Atomin kuvaamiseen käytetään atomimalleja Pallomalli
Määritelmä, metallisidos, metallihila:
 ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
Kiteinen aine. Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne.
 Kiteinen aine Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne. Kiteinen aine on hyvä erottaa kiinteästä aineesta, johon kuuluu myös
Kiteinen aine Kide on suuresta atomijoukosta muodostunut säännöllinen ja stabiili, atomiseen skaalaan nähden erittäin suuri, rakenne. Kiteinen aine on hyvä erottaa kiinteästä aineesta, johon kuuluu myös
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia
 Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Kovalenttinen sidos ja molekyyliyhdisteiden ominaisuuksia 16. helmikuuta 2014/S.. Mikä on kovalenttinen sidos? Kun atomit jakavat ulkoelektronejaan, syntyy kovalenttinen sidos. Kovalenttinen sidos on siis
Luku 11: Molekyylien rakenne. Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H
 Luku 11: Molekyylien rakenne Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H + 2 ja muut kaksiatomiset molekyylit Hückel approksimaatio 1 Elektronien liike on hyvin
Luku 11: Molekyylien rakenne Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H + 2 ja muut kaksiatomiset molekyylit Hückel approksimaatio 1 Elektronien liike on hyvin
Orgaanisten yhdisteiden rakenne ja ominaisuudet
 Orgaanisten yhdisteiden rakenne ja ominaisuudet 1 2 KOVALENTTISET SIDOKSET ORGAANISISSA YHDISTEISSÄ 3 4 5 6 7 Orgaanisissa molekyyleissä hiiliatomit muodostavat aina neljä kovalenttista sidosta Hiiliketju
Orgaanisten yhdisteiden rakenne ja ominaisuudet 1 2 KOVALENTTISET SIDOKSET ORGAANISISSA YHDISTEISSÄ 3 4 5 6 7 Orgaanisissa molekyyleissä hiiliatomit muodostavat aina neljä kovalenttista sidosta Hiiliketju
Luku 13: Elektronispektroskopia. 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi
 Luku 13: Elektronispektroskopia 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi 1 2-atomisen molekyylin elektronitilan termisymbolia muodostettaessa tärkeä ominaisuus on elektronien
Luku 13: Elektronispektroskopia 2-atomiset molekyylit moniatomiset molekyylit Fluoresenssi ja fosforesenssi 1 2-atomisen molekyylin elektronitilan termisymbolia muodostettaessa tärkeä ominaisuus on elektronien
Molekyylit. Helsinki University of Technology, Laboratory of Computational Engineering, Micro- and Nanosciences Laboratory. Atomien väliset sidokset
 Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
Kertaus. Tehtävä: Kumpi reagoi kiivaammin kaliumin kanssa, fluori vai kloori? Perustele.
 Kertaus 1. Atomin elektronirakenteet ja jaksollinen järjestelmä kvanttimekaaninen atomimalli, atomiorbitaalit virittyminen, ionisoituminen, liekkikokeet jaksollisen järjestelmän rakentuminen alkuaineiden
Kertaus 1. Atomin elektronirakenteet ja jaksollinen järjestelmä kvanttimekaaninen atomimalli, atomiorbitaalit virittyminen, ionisoituminen, liekkikokeet jaksollisen järjestelmän rakentuminen alkuaineiden
Luku 2: Atomisidokset ja ominaisuudet
 Luku 2: Atomisidokset ja ominaisuudet Käsiteltävät aiheet: Mikä aikaansaa sidokset? Mitä eri sidostyyppejä on? Mitkä ominaisuudet määräytyvät sidosten kautta? Chapter 2-1 Atomirakenne Atomi elektroneja
Luku 2: Atomisidokset ja ominaisuudet Käsiteltävät aiheet: Mikä aikaansaa sidokset? Mitä eri sidostyyppejä on? Mitkä ominaisuudet määräytyvät sidosten kautta? Chapter 2-1 Atomirakenne Atomi elektroneja
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
, m s ) täytetään alimmasta energiatilasta alkaen. Alkuaineet joiden uloimmalla elektronikuorella on samat kvanttiluvut n,
 S-114.6, Fysiikka IV (EST),. VK 4.5.005, Ratkaisut 1. Selitä lyhyesti mutta mahdollisimman täsmällisesti: a) Keskimääräisen kentän malli ja itsenäisten elektronien approksimaatio. b) Monen fermionin aaltofunktion
S-114.6, Fysiikka IV (EST),. VK 4.5.005, Ratkaisut 1. Selitä lyhyesti mutta mahdollisimman täsmällisesti: a) Keskimääräisen kentän malli ja itsenäisten elektronien approksimaatio. b) Monen fermionin aaltofunktion
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
CHEM-A1250 Luento 3 Sidokset (jatkuu) + kemiallinen reaktio
 CHEM-A1250 Luento 3 Sidokset (jatkuu) + kemiallinen reaktio Eeva-Leena Rautama Elektronien vastaanottaminen, luovuttaminen ja jakaminen Pääsääntöisesti kemiallisten sidosten muodostumista Sitoutumisella
CHEM-A1250 Luento 3 Sidokset (jatkuu) + kemiallinen reaktio Eeva-Leena Rautama Elektronien vastaanottaminen, luovuttaminen ja jakaminen Pääsääntöisesti kemiallisten sidosten muodostumista Sitoutumisella
ATOMIN JA IONIN KOKO
 ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
Laskennalinen kemia. Menetelmien hierarkia: Molekyyligeometria Molekyylimekaniikka Molekyylidynamiikka
 Laskennalinen kemia Menetelmien hierarkia: Molekyyligeometria Molekyylimekaniikka Molekyylidynamiikka Molekyyligeometria ja elektronirakenteet Empiiriset menetelmät (Hückel, Extended Hückel) Semi-empiiriset
Laskennalinen kemia Menetelmien hierarkia: Molekyyligeometria Molekyylimekaniikka Molekyylidynamiikka Molekyyligeometria ja elektronirakenteet Empiiriset menetelmät (Hückel, Extended Hückel) Semi-empiiriset
Luku 10: Molekyylien rakenne. Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H
 Luku 10: Molekyylien rakenne Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H + 2 ja muut kaksiatomiset molekyylit Hückel approksimaatio 1 Molekyylien elektronirakennetta
Luku 10: Molekyylien rakenne Valenssisidosteoria Kaksiatomiset ja moniatomiset molekyylit Molekyyliorbitaaliteoria H + 2 ja muut kaksiatomiset molekyylit Hückel approksimaatio 1 Molekyylien elektronirakennetta
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
HEIKOT SIDOKSET. Heikot sidokset ovat rakenneosasten välisiä sidoksia.
 HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
HEIKOT SIDOKSET KEMIAN MIKRO- MAAILMA, KE2 Palautetaan mieleen (on tärkeää ymmärtää ero sisäisten ja ulkoisten voimien välillä): Vahvat sidokset ovat rakenneosasten sisäisiä sidoksia. Heikot sidokset ovat
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
Ionisidos syntyy, kun elektronegatiivisuusero on tarpeeksi suuri (yli 1,7). Yleensä epämetallin (suuri el.neg.) ja metallin (pieni el.neg.) välille.
 2.1 Vahvat sidokset 1. Ionisidokset 2. 3. Kovalenttiset sidokset Metallisidokset Ionisidos syntyy, kun elektronegatiivisuusero on tarpeeksi suuri (yli 1,7). Yleensä epämetallin (suuri el.neg.) ja metallin
2.1 Vahvat sidokset 1. Ionisidokset 2. 3. Kovalenttiset sidokset Metallisidokset Ionisidos syntyy, kun elektronegatiivisuusero on tarpeeksi suuri (yli 1,7). Yleensä epämetallin (suuri el.neg.) ja metallin
CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017
 CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017 Tenttikysymysten aihealueita eli esimerkkejä mistä aihealueista ja minkä tyyppisiä tehtäviä kokeessa
CHEM-C2210 Alkuainekemia ja epäorgaanisten materiaalien synteesi ja karakterisointi (5 op), kevät 2017 Tenttikysymysten aihealueita eli esimerkkejä mistä aihealueista ja minkä tyyppisiä tehtäviä kokeessa
d) Klooria valmistetaan hapettamalla vetykloridia kaliumpermanganaatilla. (Syntyy Mn 2+ -ioneja)
 Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
8. MONIELEKTRONISET ATOMIT
 8. MONIELEKTRONISET ATOMIT 8.1. ELEKTRONIN SPIN Epärelativistinen kvanttimekaniikka selittää vetyatomin rakenteen melko tarkasti, mutta edelleen kokeellisissa atomien energioiden mittauksissa oli selittämättömiä
8. MONIELEKTRONISET ATOMIT 8.1. ELEKTRONIN SPIN Epärelativistinen kvanttimekaniikka selittää vetyatomin rakenteen melko tarkasti, mutta edelleen kokeellisissa atomien energioiden mittauksissa oli selittämättömiä
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Jaksollinen järjestelmä ja sidokset
 Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
KE1 KERTAUSTA SIDOKSISTA VASTAUKSET 2013. a) K ja Cl IONISIDOS, KOSKA KALIUM ON METALLI JA KLOORI EPÄMETALLI.
 KE1 KERTAUSTA SIDOKSISTA VASTAUKSET 2013 Atomien väliset VAVAT sidokset: Molekyylien väliset EIKOT sidokset: 1. IOISIDOS 1. DISPERSIOVOIMAT 2. KOVALETTIE SIDOS 2. DIPOLI-DIPOLISIDOS 3. METALLISIDOS 3.
KE1 KERTAUSTA SIDOKSISTA VASTAUKSET 2013 Atomien väliset VAVAT sidokset: Molekyylien väliset EIKOT sidokset: 1. IOISIDOS 1. DISPERSIOVOIMAT 2. KOVALETTIE SIDOS 2. DIPOLI-DIPOLISIDOS 3. METALLISIDOS 3.
(Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen)
 KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
pääkiertoakseli #$%%ä 2C 2 C 2!"
 Tehtävä 1 Määritä seuraavien molekyylien pisteryhmät: (a) H 3 N H 3 N l o l NH 3 + NH 3 urataan lohkokaaviota: lineaari!"!" suuri symmetria 2s v #$%%ä 2v!" pääkiertoakseli #$%%ä 2 2 2!" s h Vastaavasti:
Tehtävä 1 Määritä seuraavien molekyylien pisteryhmät: (a) H 3 N H 3 N l o l NH 3 + NH 3 urataan lohkokaaviota: lineaari!"!" suuri symmetria 2s v #$%%ä 2v!" pääkiertoakseli #$%%ä 2 2 2!" s h Vastaavasti:
Kemian syventävät kurssit
 Kemian syventävät kurssit KE2 Kemian mikromaailma aineen rakenteen ja ominaisuuksien selittäminen KE3 Reaktiot ja energia laskuja ja reaktiotyyppejä KE4 Metallit ja materiaalit sähkökemiaa: esimerkiksi
Kemian syventävät kurssit KE2 Kemian mikromaailma aineen rakenteen ja ominaisuuksien selittäminen KE3 Reaktiot ja energia laskuja ja reaktiotyyppejä KE4 Metallit ja materiaalit sähkökemiaa: esimerkiksi
Kvanttifysiikan perusteet 2017
 Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Molekyylit. Atomien välisten sidosten muodostuminen
 Molekyylit. Johdanto. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit 6. Orgaaniset
Molekyylit. Johdanto. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit 6. Orgaaniset
11. MOLEKYYLIT. Kvanttimekaniikka on käyttökelpoinen molekyyleille, jos se pystyy selittämään atomien välisten sidosten syntymisen.
 11. MOLEKYYLIT Vain harvat alkuaineet esiintyvät luonnossa atomeina (jalokaasut). Useimmiten alkuaineet esiintyvät yhdisteinä: pieninä tai isoina molekyyleinä, klustereina, nesteinä, kiinteänä aineena.
11. MOLEKYYLIT Vain harvat alkuaineet esiintyvät luonnossa atomeina (jalokaasut). Useimmiten alkuaineet esiintyvät yhdisteinä: pieninä tai isoina molekyyleinä, klustereina, nesteinä, kiinteänä aineena.
Siirtymämetallien erityisominaisuuksia
 Siirtymämetallien erityisominaisuuksia MATERIAALIT JA TEKNOLOGIA, KE4 Sivuryhmien metallien kemiaa: Jaksojen (vaakarivit) 4 ja 5 sivuryhmien metalleista käytetään myös nimitystä d-lohkon alkuaineet, koska
Siirtymämetallien erityisominaisuuksia MATERIAALIT JA TEKNOLOGIA, KE4 Sivuryhmien metallien kemiaa: Jaksojen (vaakarivit) 4 ja 5 sivuryhmien metalleista käytetään myös nimitystä d-lohkon alkuaineet, koska
1. Materiaalien rakenne
 1. Materiaalien rakenne 1.1 Johdanto 1. Luento 2.11.2010 1.1 Johdanto Materiaalit voidaan luokitella useilla eri tavoilla Kemiallisen sidoksen mukaan: metallit, keraamit, polymeerit Käytön mukaan: komposiitit,
1. Materiaalien rakenne 1.1 Johdanto 1. Luento 2.11.2010 1.1 Johdanto Materiaalit voidaan luokitella useilla eri tavoilla Kemiallisen sidoksen mukaan: metallit, keraamit, polymeerit Käytön mukaan: komposiitit,
MOLEKYYLIT Johdanto Vetymolekyyli-ioni Kaksiatomiset molekyylit...239
 MOLEKYYLIT... 8 6.1 Johdanto...8 6. Vetymolekyyli-ioni...9 6.3 Kaksiatomiset molekyylit...39 6.4 Kaksiatomisten molekyylien elektronikonfiguraatioita...43 6.5 Moniatomiset molekyylit...5 6.6 Orgaaniset
MOLEKYYLIT... 8 6.1 Johdanto...8 6. Vetymolekyyli-ioni...9 6.3 Kaksiatomiset molekyylit...39 6.4 Kaksiatomisten molekyylien elektronikonfiguraatioita...43 6.5 Moniatomiset molekyylit...5 6.6 Orgaaniset
elektroni = -varautunut tosi pieni hiukkanen nukleoni = protoni/neutroni
 3.1 Atomin rakenneosat Kaikki aine matter koostuu alkuaineista elements. Jokaisella alkuaineella on omanlaisensa atomi. Mitä osia ja hiukkasia parts and particles atomissa on? pieni ydin, jossa protoneja
3.1 Atomin rakenneosat Kaikki aine matter koostuu alkuaineista elements. Jokaisella alkuaineella on omanlaisensa atomi. Mitä osia ja hiukkasia parts and particles atomissa on? pieni ydin, jossa protoneja
KEMIAN MIKROMAAILMA, KE2 Kvanttimekaaninen atomimalli
 KEMIAN MIKROMAAILMA, KE2 Kvanttimekaaninen atomimalli Aineen rakenteen teoria alkoi hahmottua, kun 1800-luvun alkupuolella John Dalton kehitteli teoriaa atomeista jakamattomina aineen perusosasina. Toki
KEMIAN MIKROMAAILMA, KE2 Kvanttimekaaninen atomimalli Aineen rakenteen teoria alkoi hahmottua, kun 1800-luvun alkupuolella John Dalton kehitteli teoriaa atomeista jakamattomina aineen perusosasina. Toki
Ydinfysiikkaa. Tapio Hansson
 3.36pt Ydinfysiikkaa Tapio Hansson Ydin Ydin on atomin mittakaavassa äärimmäisen pieni. Sen koko on muutaman femtometrin luokkaa (10 15 m), kun taas koko atomin halkaisija on ångströmin luokkaa (10 10
3.36pt Ydinfysiikkaa Tapio Hansson Ydin Ydin on atomin mittakaavassa äärimmäisen pieni. Sen koko on muutaman femtometrin luokkaa (10 15 m), kun taas koko atomin halkaisija on ångströmin luokkaa (10 10
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA
 MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
ψ(x) = A cos(kx) + B sin(kx). (2) k = nπ a. (3) E = n 2 π2 2 2ma 2 n2 E 0. (4)
 76A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 4 Kevät 214 1. Tehtävä: Yksinkertainen malli kovalenttiselle sidokselle: a) Äärimmäisen yksinkertaistettuna mallina elektronille atomissa voidaan pitää syvää potentiaalikuoppaa
76A KIINTEÄN AINEEN FYSIIKKA Ratkaisut 4 Kevät 214 1. Tehtävä: Yksinkertainen malli kovalenttiselle sidokselle: a) Äärimmäisen yksinkertaistettuna mallina elektronille atomissa voidaan pitää syvää potentiaalikuoppaa
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Kemia 3 op. Kirjallisuus: MaoL:n taulukot: kemian sivut. Kurssin sisältö
 Kemia 3 op Kirjallisuus: MaoL:n taulukot: kemian sivut Kurssin sisältö 1. Peruskäsitteet ja atomin rakenne 2. Jaksollinen järjestelmä,oktettisääntö 3. Yhdisteiden nimeäminen 4. Sidostyypit 5. Kemiallinen
Kemia 3 op Kirjallisuus: MaoL:n taulukot: kemian sivut Kurssin sisältö 1. Peruskäsitteet ja atomin rakenne 2. Jaksollinen järjestelmä,oktettisääntö 3. Yhdisteiden nimeäminen 4. Sidostyypit 5. Kemiallinen
Kiinteiden materiaalien magneettiset ominaisuudet
 Kiinteiden materiaalien magneettiset ominaisuudet Peruskäsite: Yhdisteessä elektronien orbtaaliliike ja spin vaikuttavat magneettisiin ominaisuuksiin (spinin vaikutus on merkittävämpi) Diamagnetismi Kaikki
Kiinteiden materiaalien magneettiset ominaisuudet Peruskäsite: Yhdisteessä elektronien orbtaaliliike ja spin vaikuttavat magneettisiin ominaisuuksiin (spinin vaikutus on merkittävämpi) Diamagnetismi Kaikki
Johdantoa/Kertausta. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Johdantoa/Kertausta MATERIAALIT JA TEKNOLOGIA, KE4 Mitä on kemia? Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen
Johdantoa/Kertausta MATERIAALIT JA TEKNOLOGIA, KE4 Mitä on kemia? Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Avaruus- eli stereoisomeria
 Avaruus- eli stereoisomeria KEMIAN MIKRO- MAAILMA, KE2 Kolme alalajia: 1) cis-trans-isomeria, 2) optinen isomeria ja 3) konformaatioisomeria, Puhtaiden stereoisomeerien valmistaminen ja erottaminen toisistaan
Avaruus- eli stereoisomeria KEMIAN MIKRO- MAAILMA, KE2 Kolme alalajia: 1) cis-trans-isomeria, 2) optinen isomeria ja 3) konformaatioisomeria, Puhtaiden stereoisomeerien valmistaminen ja erottaminen toisistaan
Chem-C2400 Luento 2: Kiderakenteet Ville Jokinen
 Chem-C2400 Luento 2: Kiderakenteet 11.1.2019 Ville Jokinen Oppimistavoitteet Metalli-, ioni- ja kovalenttinen sidos ja niiden rooli metallien ja keraamien kiderakenteissa. Metallien ja keraamien kiderakenteen
Chem-C2400 Luento 2: Kiderakenteet 11.1.2019 Ville Jokinen Oppimistavoitteet Metalli-, ioni- ja kovalenttinen sidos ja niiden rooli metallien ja keraamien kiderakenteissa. Metallien ja keraamien kiderakenteen
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
2. Alkaanit. Suoraketjuiset alkaanit: etuliite+aani Metaani, etaani... Dekaani (10), undekaani, dodekaani, tridekaani, tetradekaani, pentadekaani..
 2. Alkaanit SM -08 Kaikkein yksinkertaisimpia orgaanisia yhdisteitä. Sisältävät vain hiiltä ja vetyä ja vain yksinkertaisia - sidoksia. Yleinen molekyylikaava n 2n+2 Alkaanit voivat olla suoraketjuisia
2. Alkaanit SM -08 Kaikkein yksinkertaisimpia orgaanisia yhdisteitä. Sisältävät vain hiiltä ja vetyä ja vain yksinkertaisia - sidoksia. Yleinen molekyylikaava n 2n+2 Alkaanit voivat olla suoraketjuisia
Molekyylit. Helsinki University of Technology, Laboratory of Computational Engineering. Atomien väliset sidokset
 Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
Molekyylit. Atomien väliset sidokset. Vetymolekyyli-ioni 3. Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 4. Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 5. Moniatomiset molekyylit
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET
 HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
HEIKOT VUOROVAIKUTUKSET MOLEKYYLIEN VÄLISET SIDOKSET Tunnin sisältö 2. Heikot vuorovaikutukset Millaisia erilaisia? Missä esiintyvät? Biologinen/lääketieteellinen merkitys Heikot sidokset Dipoli-dipolisidos
766334A Ydin- ja hiukkasfysiikka
 1 766334A Ydin- ja hiukkasfysiikka Luentomonistetta täydentävää materiaalia: 4 Juhani Lounila Oulun yliopisto, Fysiikan laitos, 01 6 Radioaktiivisuus Kuva 1 esittää radioaktiivisen aineen ydinten lukumäärää
1 766334A Ydin- ja hiukkasfysiikka Luentomonistetta täydentävää materiaalia: 4 Juhani Lounila Oulun yliopisto, Fysiikan laitos, 01 6 Radioaktiivisuus Kuva 1 esittää radioaktiivisen aineen ydinten lukumäärää
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Massaspektrometria. magneetti negat. varautuneet kiihdytys ja kohdistus
 Massaspektrometria IHMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Määritelmä Massaspektrometria on tekniikka-menetelmä, jota käytetään 1) mitattessa orgaanisen molekyylin molekyylimassaa ja 2) määritettäessä
Massaspektrometria IHMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Määritelmä Massaspektrometria on tekniikka-menetelmä, jota käytetään 1) mitattessa orgaanisen molekyylin molekyylimassaa ja 2) määritettäessä
766334A Ydin- ja hiukkasfysiikka
 1 76633A Ydin- ja hiukkasfysiikka Luentomonistetta täydentävää materiaalia: 3 5-3 Kuorimalli Juhani Lounila Oulun yliopisto, Fysiikan laitos, 011 Kuva 7-13 esittää, miten parillis-parillisten ydinten ensimmäisen
1 76633A Ydin- ja hiukkasfysiikka Luentomonistetta täydentävää materiaalia: 3 5-3 Kuorimalli Juhani Lounila Oulun yliopisto, Fysiikan laitos, 011 Kuva 7-13 esittää, miten parillis-parillisten ydinten ensimmäisen
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio:
 Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016 Vastuuopettaja Muut opettajat Yliopistonlehtori Minna Nieminen, Huone B 201d (vastaanottoajat: sovittaessa) puh. 050 343 8187, sähköposti: Minna.Nieminen@aalto.fi
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016 Vastuuopettaja Muut opettajat Yliopistonlehtori Minna Nieminen, Huone B 201d (vastaanottoajat: sovittaessa) puh. 050 343 8187, sähköposti: Minna.Nieminen@aalto.fi
Kiinteiden materiaalien rakenne
 Kiinteiden materiaalien rakenne Ketelaarin diagrammi Fajansin säännöt: (1) Sidoksen polaarisuus pienenee kationin koon pienentyessä tai varauksen kasvaessa () Sidoksen polaarisuus pienenee anionin koon
Kiinteiden materiaalien rakenne Ketelaarin diagrammi Fajansin säännöt: (1) Sidoksen polaarisuus pienenee kationin koon pienentyessä tai varauksen kasvaessa () Sidoksen polaarisuus pienenee anionin koon
S Fysiikka III (EST) Tentti ja välikoeuusinta
 S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
S-437 Fysiikka III (EST) Tentti ja välikoeuusinta 65007 Välikoeuusinnassa vastataan vain kolmeen tehtävään Kokeesta saatu pistemäärä kerrotaan tekijällä 5/3 Merkitse paperiin uusitko jommankumman välikokeen,
Tehtävä 2. Selvitä, ovatko seuraavat kovalenttiset sidokset poolisia vai poolittomia. Jos sidos on poolinen, merkitse osittaisvaraukset näkyviin.
 KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
KERTAUSKOE, KE1, SYKSY 2013, VIE Tehtävä 1. Kirjoita kemiallisia kaavoja ja olomuodon symboleja käyttäen seuraavat olomuodon muutokset a) etanolin CH 3 CH 2 OH höyrystyminen b) salmiakin NH 4 Cl sublimoituminen
6.2 Vetymolekyyli-ioni Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 238
 MOLEKYYLIT 6.1 Johdanto 7 6. Vetymolekyyli-ioni 8 6.3 Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 38 6.4 Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 4 6.5 Moniatomiset molekyylit
MOLEKYYLIT 6.1 Johdanto 7 6. Vetymolekyyli-ioni 8 6.3 Kaksiatomiset molekyylit ja niiden molekyyliorbitaalit 38 6.4 Muutamien kaksiatomisten molekyylien elektronikonfiguraatio 4 6.5 Moniatomiset molekyylit
8. MONIELEKTRONISET ATOMIT
 8. MONIELEKTRONISET ATOMIT 8.1. ELEKTRONIN SPIN Epärelativistinen kvanttimekaniikka selittää vetyatomin rakenteen melko tarkasti, mutta edelleen kokeellisissa atomien energioiden mittauksissa oli selittämättömiä
8. MONIELEKTRONISET ATOMIT 8.1. ELEKTRONIN SPIN Epärelativistinen kvanttimekaniikka selittää vetyatomin rakenteen melko tarkasti, mutta edelleen kokeellisissa atomien energioiden mittauksissa oli selittämättömiä
KE2 Kemian mikromaailma
 KE2 Kemian mikromaailma 1. huhtikuuta 2015/S.. Tässä kokeessa ei ole aprillipiloja. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Tehtävät arvostellaan asteikolla 0 6. Joissakin tehtävissä
KE2 Kemian mikromaailma 1. huhtikuuta 2015/S.. Tässä kokeessa ei ole aprillipiloja. Vastaa viiteen tehtävään. Käytä tarvittaessa apuna taulukkokirjaa. Tehtävät arvostellaan asteikolla 0 6. Joissakin tehtävissä
EPÄORGAANINEN KEMIA HARJOITUKSIA. Jaksollinen järjestelmä
 EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
Avaruus- eli stereoisomeria
 Avaruus- eli stereoisomeria IHMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Kolme alalajia: 1) cis-trans-isomeria, 2) optinen isomeria ja 3) konformaatioisomeria, Puhtaiden stereoisomeerien valmistaminen ja erottaminen
Avaruus- eli stereoisomeria IHMISEN JA ELINYMPÄ- RISTÖN KEMIAA, KE2 Kolme alalajia: 1) cis-trans-isomeria, 2) optinen isomeria ja 3) konformaatioisomeria, Puhtaiden stereoisomeerien valmistaminen ja erottaminen
Yhtälöryhmä matriisimuodossa. MS-A0004/A0006 Matriisilaskenta. Tarkastellaan esimerkkinä lineaarista yhtälöparia. 2x1 x 2 = 1 x 1 + x 2 = 5.
 2. MS-A4/A6 Matriisilaskenta 2. Nuutti Hyvönen, c Riikka Kangaslampi Matematiikan ja systeemianalyysin laitos Aalto-yliopisto 5.9.25 Tarkastellaan esimerkkinä lineaarista yhtälöparia { 2x x 2 = x + x 2
2. MS-A4/A6 Matriisilaskenta 2. Nuutti Hyvönen, c Riikka Kangaslampi Matematiikan ja systeemianalyysin laitos Aalto-yliopisto 5.9.25 Tarkastellaan esimerkkinä lineaarista yhtälöparia { 2x x 2 = x + x 2
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Lukion kemian OPS 2016
 Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
Kemialliset sidokset lukion kemian opetuksessa
 Kemialliset sidokset lukion kemian opetuksessa Linda Gustafsson Pro gradu -tutkielma 4.9.2007 Kemian opettajan suuntautumisvaihtoehto Kemian koulutusohjelma Matemaattis-luonnontieteellinen tiedekunta Helsingin
Kemialliset sidokset lukion kemian opetuksessa Linda Gustafsson Pro gradu -tutkielma 4.9.2007 Kemian opettajan suuntautumisvaihtoehto Kemian koulutusohjelma Matemaattis-luonnontieteellinen tiedekunta Helsingin
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
Hiukkasfysiikan luento 21.3.2012 Pentti Korpi. Lapuan matemaattisluonnontieteellinen seura
 Hiukkasfysiikan luento 21.3.2012 Pentti Korpi Lapuan matemaattisluonnontieteellinen seura Atomi Aine koostuu molekyyleistä Atomissa on ydin ja fotonien ytimeen liittämiä elektroneja Ytimet muodostuvat
Hiukkasfysiikan luento 21.3.2012 Pentti Korpi Lapuan matemaattisluonnontieteellinen seura Atomi Aine koostuu molekyyleistä Atomissa on ydin ja fotonien ytimeen liittämiä elektroneja Ytimet muodostuvat
Shrödingerin yhtälön johto
 Shrödingerin yhtälön johto Tomi Parviainen 4. maaliskuuta 2018 Sisältö 1 Schrödingerin yhtälön johto tasaisessa liikkeessä olevalle elektronille 1 2 Schrödingerin yhtälöstä aaltoyhtälöön kiihtyvässä liikkeessä
Shrödingerin yhtälön johto Tomi Parviainen 4. maaliskuuta 2018 Sisältö 1 Schrödingerin yhtälön johto tasaisessa liikkeessä olevalle elektronille 1 2 Schrödingerin yhtälöstä aaltoyhtälöön kiihtyvässä liikkeessä
Voima ja potentiaalienergia II Energian kvantittuminen
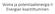 Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
FyKe 7 9 Kemia ja OPS 2016
 Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Hiilen ja vedyn reaktioita (1)
 Hiilen ja vedyn reaktioita (1) Hiilivetyjen tuotanto alkaa joko säteilevällä yhdistymisellä tai protoninvaihtoreaktiolla C + + H 2 CH + 2 + hν C + H + 3 CH+ + H 2 Huom. Reaktio C + + H 2 CH + + H on endoterminen,
Hiilen ja vedyn reaktioita (1) Hiilivetyjen tuotanto alkaa joko säteilevällä yhdistymisellä tai protoninvaihtoreaktiolla C + + H 2 CH + 2 + hν C + H + 3 CH+ + H 2 Huom. Reaktio C + + H 2 CH + + H on endoterminen,
MOLEKYYLIFYSIIKAN OPETUKSESTA SEKÄ KEMIALLISEN SIDOKSEN VAIKUTUKSESTA MOLEKYYLIEN AUGER-ELEKTRONISPEKTREIHIN
 MOLEKYYLIFYSIIKAN OPETUKSESTA SEKÄ KEMIALLISEN SIDOKSEN VAIKUTUKSESTA MOLEKYYLIEN AUGER-ELEKTRONISPEKTREIHIN PRO GRADU -TUTKIELMA SAKARI MIKKONEN OULUN YLIOPISTO FYSIKAALISTEN TIETEIDEN LAITOS 2005 Sisällysluettelo
MOLEKYYLIFYSIIKAN OPETUKSESTA SEKÄ KEMIALLISEN SIDOKSEN VAIKUTUKSESTA MOLEKYYLIEN AUGER-ELEKTRONISPEKTREIHIN PRO GRADU -TUTKIELMA SAKARI MIKKONEN OULUN YLIOPISTO FYSIKAALISTEN TIETEIDEN LAITOS 2005 Sisällysluettelo
Ydin- ja hiukkasfysiikka: Harjoitus 1 Ratkaisut 1
 Ydin- ja hiukkasfysiikka: Harjoitus Ratkaisut Tehtävä i) Isotoopeilla on sama määrä protoneja, eli sama järjestysluku Z, mutta eri massaluku A. Tässä isotooppeja keskenään ovat 9 30 3 0 4Be ja 4 Be, 4Si,
Ydin- ja hiukkasfysiikka: Harjoitus Ratkaisut Tehtävä i) Isotoopeilla on sama määrä protoneja, eli sama järjestysluku Z, mutta eri massaluku A. Tässä isotooppeja keskenään ovat 9 30 3 0 4Be ja 4 Be, 4Si,
PHYS-C0240 Materiaalifysiikka (5op), kevät 2016
 PHYS-C0240 Materiaalifysiikka (5op), kevät 2016 Prof. Martti Puska Emppu Salonen Tomi Ketolainen Ville Vierimaa Luento 7: Hilavärähtelyt tiistai 12.4.2016 Aiheet tänään Hilavärähtelyt: johdanto Harmoninen
PHYS-C0240 Materiaalifysiikka (5op), kevät 2016 Prof. Martti Puska Emppu Salonen Tomi Ketolainen Ville Vierimaa Luento 7: Hilavärähtelyt tiistai 12.4.2016 Aiheet tänään Hilavärähtelyt: johdanto Harmoninen
Reaktiot ja energia. Kurssin yleiset tiedot. (työt to-pe!!! Ehkä ma-ti) Kurssi 3 (syventävä): Reaktiot ja energia, Ke3 Tunnit (45min):
 Reaktiot ja energia Kurssi 3, Ke3 Kurssin yleiset tiedot Kurssi 3 (syventävä): Tunnit (45min): ma 8:00-8:45 ja 14:10 14:55, ti, ke ja pe 8:00 8:45 ja to 14:10 14:55 (työt to-pe!!! Ehkä ma-ti) Kurssikirja:
Reaktiot ja energia Kurssi 3, Ke3 Kurssin yleiset tiedot Kurssi 3 (syventävä): Tunnit (45min): ma 8:00-8:45 ja 14:10 14:55, ti, ke ja pe 8:00 8:45 ja to 14:10 14:55 (työt to-pe!!! Ehkä ma-ti) Kurssikirja:
Sukunimi: Etunimi: Henkilötunnus:
 K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot
 REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot Kertausta: Alun perin hapot luokiteltiin aineiksi, jotka maistuvat happamilta. Toisaalta karvaalta maistuvat
REAKTIOT JA TASAPAINO, KE5 Vahvat&heikot protolyytit (vesiliuoksissa) ja protolyysireaktiot Kertausta: Alun perin hapot luokiteltiin aineiksi, jotka maistuvat happamilta. Toisaalta karvaalta maistuvat
Helsingin yliopiston kemian valintakoe. Keskiviikkona klo Vastausselvitykset: Tehtävät:
 1 elsingin yliopiston kemian valintakoe Keskiviikkona 9.5.2018 klo 10-13. Vastausselvitykset: Tehtävät: 1. Kirjoita seuraavat reaktioyhtälöt olomuotomerkinnöin: a. Sinkkipulveria lisätään kuparisulfaattiliuokseen.
1 elsingin yliopiston kemian valintakoe Keskiviikkona 9.5.2018 klo 10-13. Vastausselvitykset: Tehtävät: 1. Kirjoita seuraavat reaktioyhtälöt olomuotomerkinnöin: a. Sinkkipulveria lisätään kuparisulfaattiliuokseen.
