Influenssa A- ja B-virus sekä käytössä olevat influenssarokotteet ja kehitteillä olevat universaalit influenssarokotteet
|
|
|
- Sakari Härkönen
- 6 vuotta sitten
- Katselukertoja:
Transkriptio
1 Kirjallisuustutkielma Influenssa A- ja B-virus sekä käytössä olevat influenssarokotteet ja kehitteillä olevat universaalit influenssarokotteet Mira Mäkelä Oulun yliopisto Biokemian ja molekyylilääketieteen tiedekunta 2018
2 Käytetyt lyhenteet ADCC APC COBRA CTL DC ER HA IL-2 IFN-γ Vasta-aine riippuvainen soluvälitteinen sytotoksisuus Antigeenin esittelijä solu a computationally optimized broadly reactive antigen Sytotoksinen T-solu Dentriittisolu Endoplasmakalvosto Hemagglutiniini Interleukiini-2 Interferoni-γ M1/2 Matriksi1/2 NA NEP NK-solut NLR NLS Neuraminidaasi nuclear export -proteiini Luonnollinen tappajasolu NLR-inflammasomi Tumalokalisaatiosignaali NOS2 Typpioksidisyntaasi 2 NP Nukleoproteiini NS1 Ei-rakenteelliset proteiinit 1 PA PAMP Polymeerasi happo Patogeeneihin liittyvät molekyylikuviot PB1 Polymeerasi emäs 1 PB2 Polymeraasi emäs 2 PRR pattern recognition -reseptori
3 QIV RdRp RLR RNP Th1/2/17 TIV TLR TNF-α VLP WHO Nelivalenttinen influenssarokote Heterotrimeerisen RNA-riippuvaisen RNApolymeraasi RIG-I-reseptori Ribonukleoproteiini T-auttajasolut1/2/17 Trivalenttinen influenssarokote Toll like -reseptori Tuumorinekroositekijä alfa Viruksen kaltaiset partikkelit Maailman terveysjärjestö
4 Sisällysluettelo Käytetyt lyhenteet Sisällys 1. Johdanto 1 2. Influenssa A- ja B-virusten rakenne Hemagglutiniini Neuraminidaasi M2-ionikanava Genomi 5 3. Influenssaviruksen lisääntyminen 6 4. Influenssaviruksen aiheuttama immuunivaste Synnynnäinen immuniteetti Adaptiivinen immuniteetti 9 5. Kausi-influenssarokotteen tuotantoprosessi Ongelmat influenssarokotteen tuotantoprosessia Käytössä olevat influenssarokotteet Trivalenttinen influenssarokote (TIV) Elävää heikennettyä influenssavirusta sisältävä rokote (LAIV-rokote) Nelivalenttinen influenssarokote (QIV) Pandemiarokotteet Kehitteillä olevat influenssarokotteet HA:n varsidomeeniin pohjautuvat influenssarokotteet HA:n globulaariseen päädomeeniin pohjautuvat influenssarokotteet NA:n pohjautuvat influenssarokotteet M2-ionikanavan ektodomeeniin pohjautuva influenssarokote Sytotoksisia T-lymfosyyttejä aktivoivat influenssarokotteet Lopuksi Lähteet 19
5 1. Johdanto Influenssa A- ja B-virukset ovat ortomyksovirusten heimoon kuuluvia negatiivisäikeisiä RNA-viruksia (Bouvier & Palese 2008). Influenssaviruksen aiheuttaman hengitystieinfektion oireita ovat mm. korkea kuume, väsymys sekä päänsärky. Ihmisillä esiintyy sekä influenssa A- että B-virusta. Lisäksi Influenssa A-virusta on löydetty mm. monilta lämminverisiltä eläimiltä, kuten linnuilta, hevosilta sekä sioilta. (Taubenberger & Morens 2008) Influenssa A- ja B-virukset aiheuttavat kausittaisia epidemioita eteläisellä pallonpuoliskolla maaliskuusta syyskuuhun ja pohjoisella pallonpuoliskolla lokakuusta maaliskuuhun. (Sautto et al. 2018). Nämä kausittaiset influenssaepidemiat aiheutuvat kahdesta kiertävästä influenssa A-viruksen alatyyppistä (H1N1 ja H3N2) sekä kahdesta influenssa B- viruksen haarautuneesta sukulinjasta (Yamagata ja Victoria) (Krammer & Palese 2015, Sautto et al. 2018). Arvion mukaan influenssa A- ja B-viruksien aiheuttamiin kausittaisesti esiintyviin epidemioihin sairastuu vuosittain 2-5 miljoonaa ihmistä, joista ihmistä menehtyy infektion seurauksena. (Krammer & Palese 2015) Lisäksi influenssa A-virus aiheuttaa ajoittain odottamattomia pandemioita, kuten vuonna 1918 espanjantauti, johon menehtyi maailmanlaajuisesti yli 50 miljoonaa ihmistä. (Wong & Webby 2013) Hemagglutiniini (HA) sekä neuraminidaasi (NA) ovat influenssa A- ja B-viruksen lipidivaipassa sijaitsevia kalvoglykoproteiineja, joiden avulla influenssa A-virukset voidaan luokitella alatyyppeihin (Bouvier & Palese 2008). HA:sta on löydetty yhteensä 18 alatyyppiä (H1-H18), jotka voidaan jakaa fylogeneettisesti kahteen erilliseen ryhmään. Ryhmä 1 sisältää 12 HA:n alatyyppiä (H1, H2, H5, H6, H8, H9, H11, H12, H13, H16, H17 ja H18) ja ryhmä 2 sisältää kuusi HA:n alatyyppiä (H3, H4, H7, H10, H14 ja H15). Influenssa A-viruksen NA:sta on puolestaan löydetty yhteensä 11 alatyyppiä (N1-N11), jotka voidaan jakaa kahteen fylogeneettisesti erilliseen ryhmään. (Sautto et al. 2018) Lukuun ottamatta lepakosta eristettyjä N10:tä sekä N11:ta, jotka eivät näytä kuuluvan kumpaankaan NA:n ryhmistä (Wohlbold & Krammer 2014). Ryhmä 1 sisältää neljä NA:n alatyyppiä (N1, N4, N5 ja N8) ja ryhmä 2 sisältää viisi NA:n alatyyppiä (N2, N3, N6, N7 ja N9) (Gamblin & Skehel 2010). Influenssavirusten nimeämistapa on standardoitu WHO:n ohjeiden mukaan. Nimeäminen aloitetaan ilmoittamalla influenssaviruksen tyyppi sekä alkuperäinen isäntä (jos ei ihminen). Seuraavaksi ilmoitetaan eristyksen paikka, numero sekä vuosi. Viimeisenä, jos kyseessä on influenssa A-virus, ilmoitetaan HA:n sekä NA:n alatyypit. Esimerkiksi influenssa - 1 -
6 A-viruksen alatyyppi H1N1, joka on eristetty ihmisestä vuonna 1999 Uudessa-Kaledoniassa eristysnumerolla 20 nimettäisiin seuraavasti: A/New Caledonia/20/1999 (H1N1). (Taubenberger & Morens 2008) Influenssa A- ja B-viruksen aiheuttamaa infektiota vastaan voi suojautua influenssarokotteella. Influenssarokotteen tehokkuus vaihtelee 60-90% välillä. Influenssaviruksia vastaan on käytössä useita erilaisia rokotteita, kuten trivalenttinen influenssarokote (TIV) sekä nelivalenttinen influenssarokote (QIV). Influenssarokotteet voivat sisältää mm. inaktivoituja kokonaisia influenssaviruksia, pilkottuja influenssaviruksia sekä influenssaviruksien pintaproteiineja. Käytössä olevat influenssarokotteet voidaan antaa joko intramuskulaarisesti tai intranasaalisesti. (Soema et al. 2015) Influenssarokotteella on kuitenkin heikompi tehokkuus pieniin lapsiin, ikäihmisiin sekä immuunipuutteisiin yksilöihin. Pienillä lapsilla influenssarokotteen heikompi tehokkuus johtuu heikosta vasteesta rokotteeseen, kun taas ikäihmisillä sekä immuunipuutoksesta kärsivillä henkilöillä rokotteen heikompi tehokkuus johtuu heikentyneestä immuunijärjestelmästä. Influenssarokotteen tehokkuutta näissä ryhmissä voidaan lisätä kasvattamalla rokotteen immunogeenisyyttä sekä laajentamalla rokotteesta aiheutuvaa immuunivastetta. (Soema et al. 2015) Uusia influenssarokotteita kehitetään jatkuvasti, koska tällä hetkellä käytettävät rokotteet mahdollistavat vain hyvin spesifisen ja lyhyen immuniteetin influenssaviruksia vastaan (Sautto et al. 2018). Tällä hetkellä kehitteillä olevat influenssarokotteet pyrkivät antamaan mahdollisimman universaalin sekä pitkän suojan influenssa A- ja B-viruksia vastaan. Nämä rokotteet indusoisivat vasta-ainetuotantoa influenssaviruksissa esiintyviä muuttumattomia alueita kohtaan, kuten HA:n varsidomeeni ja M2-ionikanava. Lisäksi influenssarokotteiden tuotantoprosessia kehitetään tehokkaammaksi mm. uusien tekniikoiden avulla. (Rajão & Pérez 2018) 2. Influenssa A- ja B-virusten rakenne Influenssa A- ja B-virukset voivat olla muodoltaan joko pallomaisia tai filamenttisia. Halkaisijaltaan pallomaiset influenssavirukset ovat noin 100 nanometriä, kun taas filamenttisten influenssavirusten pituus voi ylittää jopa 300 nanometriä. (Bouvier & Palese 2008) - 2 -
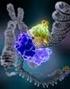
7 Influenssa A- ja B-virusta ympäröi lipidivaippa, joka on peräisin isäntäsolun membraanista. Lipidivaippa sisältää integraalisia kalvoproteiineja, joita ovat HA, NA sekä M2- ionikanavat. (Bouvier & Palese 2008) HA:n määrä influenssaviruksen integraalisista kalvoproteiineista on noin 80%, kun taas NA:n määrä on noin 17%. Integraalisista kalvoproteiineista M2-ionikanavia on vähiten, vain noin 3% integraalisista kalvoproteiineista. (Samji 2009) Selitteet: HA NA M1-proteiini (B)M2-ionikanava NEP-proteiini Kuva 1. Influenssa A- ja B-viruksen rakenne. Influenssaviruksen lipidivaippaan on uppoutuneena HA:a, NA:a sekä M2-ionikanavia. Lipidivaipan sisäpuolella sijaitsee M1-proteiinin muodostama kerros, joka sulkee influenssaviruksen ytimen sisäpuolelleen. Influenssaviruksen ytimessä sijaitsevat nuclear export -proteiini (NEP) sekä ribonukleoproteiini (RNP) kompleksi. RNP kompleksi koostuu viraalisista RNA segmenteistä, jotka ovat päällystetty nukleoproteiinilla (NP). Lisäksi RNP kompleksi sisältää heterotrimeerisen RNA-riippuvaisen RNA-polymeraasin (RdRp), joka rakentuu kolmesta polymeraasi alayksiköstä: polymeraasi emäs 1 (PB1), Polymeraasi emäs 2 (PB2) sekä polymeraasi happo (PA). (Bouvier & Palese 2008) Kuvan lähde: Rajão & Pérez 2018 (muokattu ja suomennettu) 2.1. Hemagglutiniini HA on homotrimeerinen integraalinen kalvoglykoproteiini influenssa A- ja B- viruksen lipidivaipalla, jonka tehtävänä on sitoutua isäntäsolun pinnalla olevaan siaalihappoon sekä aiheuttaa endosomaalisen membraanin ja viraalisen membraanin fuusioituminen. (Bouvier & Palese 2008, Gamblin & Skehel 2010). RdRp Toimiakseen HA monomeerin esiaste (HA0) täytyy katkaista kahdeksi polypeptidiksi (HA1 ja HA2), jotka sitoutuvat toisiinsa kahdella rikkisidoksilla. (Bouvier & Palese 2008) Aktiivinen monomeeri muodostuu globulaarisesta päädomeenista sekä NP vrna - 3 -
8 varsidomeenista. Monomeerin rikkisidoksien muodostavien kysteiinien väliin jäävät aminohapot muodostavat HA:n globulaarisen pään (Krammer & Palese 2015). HA:n varsidomeenin muodostavat HA1-polypeptidin C- Ja N-terminaaliset päät sekä HA2- polypeptidin N-terminaalinen pää. (Krammer & Palese 2013) Siaalihapon sekä antigeenin sitova kohta sijaitsee HA:n globulaarisessa päädomeenissa. Siaalihapon Sitoutumiskohdan muodostavat 190-α-heliksi, 130- ja 220- silmukka sekä vetysidoksilla toisiinsa sitoutuneiden konservoituneiden aminohappojen verkosto. 130-silmukan aminohappotähteet luovat keskeisiä sidoksia HA:n sekä siaalihapon välille. 220-silmukan aminohapoissa tapahtuneet mutaatiot ovat aiheuttaneet lajispesifisyyttä yhdessä 190-α-heliksin kanssa. (Byrd-Leotis et al. 2017) Vetysidoksilla toisiinsa sitoutuneet konservoituneet aminohapot: Tyr-98, Trp-153, His-183, ja Tyr-195 muodostavat siaalihappoa sitovan taskun. (Gamblin & Skehel 2010). Influenssaviruksen RdRp:lla ei ole korjauslukua, jonka vuoksi influenssaviruksen genomissa tapahtuu suhteellisen paljon pistemutaatioita. (Krammer & Palese 2015) Näiden pistemutaatioiden kertyessä HA:n globulaarisen päädomeenin antigeeniä sitovan alueen geeneihin, tapahtuu aminohappojen muuttumista alueella. Tämän vuoksi olemassa olevat vastaaineet eivät enää tunnista influenssavirusta, jonka ansiosta influenssavirus pystyy ns. pakenemaan immuunijärjestelmää. Tätä tapahtumaa kutsutaan antigeeniseksi ajautumiseksi. (Bouvier & Palese 2008) 2.2. Neuraminidaasi NA on sienimäinen homotetrameerinen integraalinen kalvoglykoproteiini, joka toimii siaalihapon tuhoavana entsyyminä (Gamblin & Skehel 2010). NA monomeeri muodostuu varsidomeenista sekä päädomeenista. Influenssaviruksen varsidomeenin pituus vaihtelee alatyyppien välillä. (Gamblin & Skehel 2010) Lisäksi varsidomeenin pituutta voidaan muunnella tarpeen mukaan esim. lyhentämällä. Päädomeeni muodostuu kuudesta antiparalleelista β-levystä, jotka muodostavat propellin kaltaisen asetelman. Päädomeeni sisältää NA:n aktiivisen alueen, joka koostuu varauksellisista konservoituneista aminohapoista: Arg118, Asp151, Arg152, Arg224, Glu276, Arg292, Arg371 ja Tyr406. Lisäksi NA monomeerin päädomeeni sisältää kalsiumia sitovan alueen sekä joissakin kannoissa sekundäärisen siaalihappoa sitovan alueen. (Byrd-Leotis et al. 2017) - 4 -
9 2.3. M2-ionikanava M2-ionikanava on homotetrameerinen tyypin III integraalinen kalvoproteiini, jolla on tärkeä rooli influenssa A- ja B-virusten monistumisessa isäntäsolussa. Influenssa A- viruksen M2-ionikanavan sekä influenssa B-viruksen BM2-ionkanavan monomeeri koostuu N- terminaalisesta ektodomeenista, yksinkertaisesta transmembraanidomeenista sekä C- terminaalisesta sytoplasmisesta hännästä. (Pinto & Lamb 2005) Influenssa A- ja B-virusten M2-ionikanavat eroavat toisistaan aminohappojen lukumäärän sekä järjestyksen suhteen. Influenssa A-viruksen M2-ionikanavan monomeeri koostuu 97 aminohaposta, kun taas influenssa B-viruksen BM2-ionikanavan monomeeri koostuu 109 aminohaposta. (Pielak & Chou 2011) Ainoa homologinen sekvenssi M2- sekä BM2-ionikanavien välillä on transmembraanidomeenissa sijaitseva HXXXW aminohapposekvenssi, joka on olennainen M2-ionikanavan toiminnan kannalta. (Pinto & Lamb 2005) His37 sekä Trp41 aminohapoilla on tärkeä rooli influenssa A-viruksen M2- ionikanavien toiminnan kannalta, kun taas influenssa B-viruksella vastaavat aminohapot ovat His19 sekä Trp41. His37 ja His19 aminohapot ovat tärkeitä influenssaviruksien ionikanavien selektiivisyyden kannalta. M2-ionikanavan porttina toimivat puolestaan Trp41 sekä Trp29. (Pielak & Chou 2011) Influenssa A- ja B-viruksien M2-ionikanavat aukeavat, kun influenssaviruksen ulkopuolinen ph on alle 6,5. M2-ionikanavan portti on puolestaan suljettuna influenssaviruksen ulkopuolisen ph:n ollessa yli 7,5. (Pinto & Lamb 2005) 2.4. Genomi Influenssa A- ja B-viruksen genomit muodostuvat kahdeksaan osaan segmentoituneesta negatiivisäikeisestä viraalisesta RNA:sta. Segmentit ovat numeroitu yhdestä kahdeksaan laskevan pituuden mukaan (Bouvier & Palese 2008). Segmentit 1, 2 ja 3 koodaavat RdRp:n osia: Segmentti 1 koodaa PB2:ta, segmentti 2 PB1:ta ja segmentti 3 PA:a. Lisäksi segmentti 2 koodaa tietyissä influenssa A-viruksen kannoissa PB1-F2-proteiinia. Influenssaviruksen kalvoglykoproteiineja koodaavat segmentit neljä sekä kuusi. Segmentti 4 koodaa HA:a ja segmentti 6 koodaa NA:a. Nukleoproteiinia koodaa segmentti 5. Segmentti 7 koodaa puolestaan sekä M1- että M2-matriksi proteiineja. NS1 proteiinia ja NEP/NS2 proteiinia koodaa segmentti 8. (Bouvier & Palese 2008) Influenssa A-viruksen segmentoitunut genomi mahdollistaa antigeenisen siirtymän. Antigeenisessä siirtymässä influenssa A-viruksen HA:a sekä NA:a koodaavat - 5 -
10 segmentit korvataan eri alatyypin segmenteillä. Siirtymää voi tapahtua, jos saman solun on infektoinut samaan aikaan kaksi eri influenssa A-viruksen alatyyppiä. Juurikin influenssa A- viruksessa tapahtunut antigeeninen siirtymä voi aiheuttaa pandemian, jos ihmisellä ei ole ennestään vastustuskykyä kyseiselle uudelle influenssa A-viruksen alatyypille. (Bouvier & Palese 2008) 3. Influenssaviruksen lisääntyminen HA:n globulaarisen päädomeenin avulla influenssavirus sitoutuu isäntäsolun pinnalla olevaan siaalihappoon, joka on muodostanut sidoksen galaktoosin kanssa. Siaalihapon ja galaktoosin välinen sidos voi olla joko α(2,6)- tai α(2,3)-sidos. Sidostyppi määrittää influenssaviruksen lajispesifisyyden. (Byrd-Leotis et al. 2017). Influenssaviruksen HA tunnistaa ihmisillä pääasiassa α(2,6)-sidoksen (Gagneux et al. 2003). HA:n sitoutuminen solun pinnalla olevaan siaalihappoon aktivoi influenssaviruksen endosytoosin, jonka seurauksesta virus kuljetetaan solun sisälle endosomissa (Samji 2009). Endosomin alhainen ph aiheuttaa konformationaalisia muutoksia HA:ssa sekä aukaisee M2-ionikanavat. Muutokset HA:ssa aiheuttavat endosomaalisen membraanin sekä viruksen lipidivaipan fuusioitumisen. M2-ionikanavien avautuminen aiheuttaa viruksen ytimen ph:n alenemisen, jolloin viraalinen RNP kompleksi voidaan kuljettaa isäntäsolun sytoplasmaan. (Samji 2009) Viraalinen RNP kompleksi kuljetetaan sytoplasmasta isäntäsolun tumaan tumalokalisaatiosignaalien (NLS) avulla. Tumassa tapahtuu influenssaviruksen genomin transkriptio sekä replikaatio. Transkriptiota varten influenssaviruksen negatiivisäikeinen RNA täytyy muuttaa positiivisäikeiseksi RNA:ksi, joka toimii mrna:n tavoin templaattina sekä viraalisessa proteiini synteesissä, että komplementaarisen RNA:n (crna) synteesissä. Uutta negatiivisäikeistä RNA:ta voidaan valmistaa crna:n avulla. (Bouvier & Palese 2008) RdRp aloittaa influenssaviruksen genomin replikaation sisäisesti 5 - sekä 3 - päiden avulla ilman aluketta. Influenssaviruksen 5 - ja 3 - päät voivat muodostaa keskenään korkkiruuvimaisen rakenteen emäsjärjestys vastaavuuden takia. Ennen kuin influenssaviruksen viraalinen RNA voidaan lukea mrna:ksi ja käyttää translaatiossa isäntäsolussa, täytyy siihen lisätä poly-a häntä sekä 5 cap (Bouvier & Palese 2008). Poly-A häntä lisätään viraalisen RNA:n 3 -päähän ns. sulkumekanismin avulla. Jokaisen influenssaviruksen vrna segmentin 5 -pään lähettyviltä löytyy 5-7 emäksen jakso urasiilia, jonka avulla RdRp luo poly-a hännän - 6 -
11 liikkumalla edestakaisin. Influenssavirus on kehittänyt omalaatuisen mekanismin 5 capin lisäämiseen, jossa metyloitu 5 cap varastetaan isäntäsolun mrna:lta. (Samji 2009) Tätä mekanismia kutsutaan cap-snatching -mekanismiksi. Mekanismiin osallistuu PB2 proteiinin cap-binding -domeeni, joka nappaa isäntäsolun metyloidun 5 capin. Tämän jälkeen PA:n endonukleaasidomeeni irrottaa cap-rakenteen isäntäsolulta. (Te Velthuis & Fodor 2016) Isäntäsolun mrna:sta varastetun 5 cap-rakenteen avulla isäntäsolun polymeerasi II aloittaa viraalisen RNA:n transkription. (Samji 2009) Lukuun ottamatta kahta segmenttiä (7 ja 8) jokainen influenssa A-viruksen segmentti koodaa vain yhtä proteiinia. Segmentit 7 sekä 8 pystyvät koodaamaan kahta erilaista proteiinia silmukoinnin avulla. Segmentti 7 koodaa pääsääntöisesti M1-proteiinia, kun taas segmentti 8:n päätuote on NS1. Segmentit pystyvät koodaamaan myös M2-proteiinia sekä NEP-proteiinia, jotka syntyvät silmukoinnin lopputuloksena. (Bouvier & Palese 2008) Influenssaviruksella ei ole omaa silmukointikoneistoa, vaan se käyttää isäntäsolun silmukointikoneistoa. Lisäksi influenssavirus kykenee inhiboimaan isäntäsolua käyttämästä silmukointikoneistoa omiin toimintoihin, pääosin NS1-proteiinien avulla. Inhibointi tapahtuu silmukointi partikkeleiden uudelleen järjestämisen avulla, jonka NS1 aktivoi sitoutumalla mm. snrna:han. (Samji 2009) Integraaliset kalvoproteiinit valmistetaan ribosomeilla, josta ne kuljetetaan ER:lle laskostumista varten. ER:lta proteiinit kuljetetaan golgin laitteelle, jossa ne muokkaantuvat lopullisesti. Lopullisen muokkaamisen jälkeen proteiinit kulkeutuvat lopulta solukalvolle. M1- matriksiproteiinien sekä muiden proteiinien proteiinisynteesistä sekä kuljetuksesta solukalvolle tiedetään vain vähän. (Bouvier & Palese 2008) Ainoastaan negatiivisäikeiset vrnp kompleksit poistetaan tumahuokosten kautta. Kun kaikki influenssaviruksen osat on valmistettu ja kuljetettu solukalvon lähettyville voidaan viraaliset partikkelit koota ja vapauttaa solusta. (Samji 2009) 4. Influenssaviruksen aiheuttama immuunivaste Influenssaviruksen infektiossa synnynnäinen vastustuskyky vastaa nopeasta, mutta epäspesifisestä puolustautumisesta influenssaviruksia vastaan. Synnynnäinen immuniteetti ei kuitenkaan pysty luomaan muistia. Adaptiivinen immuniteetti on puolestaan hitaampi ja spesifisempi kuin synnynnäinen immuniteetti. Lisäksi adaptiivinen immuniteetti pystyy luomaan muistisoluja, kuten T- ja B-muistisolut. (Van de Sandt et al. 2012) - 7 -
12 4.1. Synnynnäinen immuniteetti Synnynnäinen immuniteetti rakentuu fyysisistä esteistä (esim. lima ja lysotsyymi) sekä synnynnäisistä soluvasteista, kuten PRR-reseptoreista, makrofageista, NK-soluista ja dentriittisoluista (Van de Sandt et al. 2012) Influenssaviruksen tunnistavat PRR-reseptorit voidaan jakaa kolmeen reseptorityyppiin. Näihin reseptoreihin kuuluvat TLR-reseptorit, RLR-reseptorit sekä NLRinflammasomit. Influenssaviruksen RNA on immuunipuolustuksen aktivoija eli PAMP, jonka PRR-reseptorit tunnistavat. (Kreijzt et al. 2011) Intrasellulaariset TLR7-reseptorit tunnistavat influenssa viruksen ssrna:n, kun taas intrasellulaariset TLR3-reseptorit sekä sytosolissa sijaitsevat RLR-reseptorit tunnistavat dsrna:n. NLR-inflammasomeista NLRP3 aktivoituu influenssa viruksen dsrna:sta. Näiden kaikkien reseptorien aktivoituminen johtaa lopulta interferonien, proinflammatoristen sytokiinien ja kemokiinien transkriptioon sekä neutrofiilien, makrofagien ja dentriittisolujen aktivointiin (Van de Sandt et al. 2012) Alveolaariset makrofagit aktivoituvat influenssaviruksen infektoidessa keuhkoja. Nämä makrofagit estävät influenssaviruksen aiheuttaman infektion leviämistä fagosytoosin avulla. Lisäksi alveolaariset makrofagit tuottavat NOS2:ta ja TNF-α: a. (Kreijzt et al. 2011) NOS2 sekä TNF-α ovat vastuussa influenssaviruksen aiheuttaman taudin vakavuudesta (Van de Sandt et al. 2012). NK-solut tunnistavat vasta-aineilla merkityn infektoituneen solun, jonka jälkeen NK-solut kykenevät hajottamaan influenssaviruksen infektoiman solun vasta-aineesta riippuvaisen soluvälitteisen sytotoksisuuden (ADCC)-mekanismin avulla (Kreijzt et al. 2011). Dendriittisolut (DC) ovat ns. professionaalisia antigeenin esittelijä soluja (APC) influenssaviruksen aiheuttamassa infektiossa. DC:t aktivoivat adaptiivistä immuunijärjestelmää esittelemällä viraalisia antigeenejä naiiveille T- ja B-soluille sekä muisti T- ja B-soluille. DC:illa on kaksi toisistaan erillistä mekanismia tätä varten. Toinen reitti aktivoituu influenssaviruksen infektoidessa DC:n, jolloin proteasomit hajottavat viraaliset proteiinit pieniksi peptideiksi. Peptidit muodostavat MHC1-molekyylin kanssa kompleksin, joka kuljetetaan solun pinnalle virusspesifisten CD8 + -sytotoksisten T-solujen tunnistettavaksi. Toinen mekanismi aktivoituu, kun DC:t fagosytoivat viruspartikkelin tai apoptoottisen epiteelisolun. Fagosytoosin jälkeen viraaliset proteiinit hajotetaan joko lysosomissa tai endosomeissa peptideiksi, jotka muodostavat kompleksin MHCII-molekyylin kanssa. CD4 + T- avustaja solut tunnistavat MHCII-molekyyliin sitoutuneen peptidin. (Van de Sandt et al. 2012) - 8 -
13 4.2. Adaptiivinen immuniteetti Adaptiivinen immuunijärjestelmä voidaan jakaa humoraaliseen sekä soluvälitteiseen immuniteettiin. Humoraalinen immuniteetti koostuu influenssavirukselle spesifisestä vastaainevasteesta. Influenssa spesifiset vasta-aineet tunnistavat mm. influenssaviruksen integraaliset kalvoproteiinit (HA, NA ja M2-ionikanava) sekä nukleoproteiinit. Influenssaviruksen aiheuttama infektio indusoi IgA, IgM sekä IgG vasta-aineita. (Kreijzt et al. 2011) Naiivien DC:en aktivoimat CD4 + -solut voivat erikoistua joko T-auttaja 1 soluiksi (Th1) tai T-auttaja 2 soluiksi (Th2). Th1-solut tuottavat IFN-γ:a ja IL-2:ta sekä ovat vastuussa CTL-solujen aktivoinnissa. Lisäksi Th1-solut ovat olennaisia muisti CD8 + -solujen indusoinnissa. CD4 + -muistisoluja tuotetaan ensimmäisen influenssaviruksen aiheuttaman infektion jälkeen, jonka vuoksi CD4 + -muistisoluilla on tärkeä rooli toisessa influenssaviruksen aiheuttamassa infektiossa. Naiivit CD8 + -solut erikoistuvat CTL-soluiksi, jotka tunnistavat ja eliminoivat influenssaviruksen infektoimia soluja. CTL tunnistaa pääasiassa influenssaviruksen muuttumattomia sisäisiä proteiineja, kuten M1-proteiineja, NP ja PA. Tämän vuoksi CTL-solut mahdollistavat laajan immuniteetin influenssaviruksen alatyyppejä vastaan. Regulatoriset T-solut tasapainottavat immuunivastetta mm. kontrolloimalla CD4+- sekä CTL-vastetta. Th17 solut puolestaan estävät regulatoristen T-solujen toimintaa täten aktivoiden T-auttaja soluja. (Van de Sandt et al. 2012) 5. Kausi-influenssarokotteiden tuotantoprosessi Kausi-influenssarokotteen tuotantoprosessi muodostuu useista eri vaiheista, jotka suoritetaan 6 kuukauden aikana. Tuotantoprosessiin sisältyy sopivien influenssavirusten kantojen valitseminen, reassortanttivirusten tuotanto, reagenssin valmistus säteittäistä immunodiffuusiota varten, virusten tuotanto, monovalenttisen tuotteen valmistus, TIV sekoitteen valmistus, rokotteen lopullinen valmistus, rokotteen vapautus, kliinisen datan keräys sekä rokotteen jakelu datan hyväksymisen jälkeen. (Soema et al. 2015) Kausi-influenssarokotteen valmistaminen aloitetaan valitsemalla kyseisellä hetkellä kiertävien influenssaviruksien kannat rokotteeseen. Valinnassa hyödynnetään - 9 -
14 kolmenlaista antigeenistä dataa, jotka ovat HA:n inhibitiomääritys fretin infektion jälkeisestä antiseerumista, serologiset analyysit ennen ja jälkeen rokotuksen seerumi näytteistä sekä influenssaviruksen HA:sta sekvensoidusta datasta. Kerätyt datat esitellään kokouksissa, jotka pidetään kahdesti vuodessa. (Wong & Webby 2013) WHO päättää kausi-influenssarokotteiden suositeltavan koostumuksen, mutta kunkin maan kansalliset sääntelyelimet tekevät itse lopullisen päätöksen käytettävistä influenssaviruksien kannoista kunakin vuonna. (Wong & Webby 2013) Käytettävien influenssaviruksen kantojen valitsemisen jälkeen influenssarokotteen jakelun aloittamiseen on noin 6 kuukautta aikaa (Soema et al. 2015). Valinnan jälkeen influenssarokotteiden teollinen tuotantovaihe aloitetaan (Wong & Webby 2013). Villi tyypin Influenssa A-virusten kasvu kananmunissa optimoidaan käyttämällä master-viruksien, kuten A/Puerto Rico/8/1934 (PR8) (Soema et al. 2015). Villityypin influenssa A-virus muodostaa yhdessä master-viruksen kanssa reassortanttiviruksen, joka sisältää ainakin HA sekä NA segmentit villityypin influenssa A- viruksesta ja loput segmentit master-virukselta. Reassortanttivirukset valmistetaan infektoimalla kananmunat sekä master-viruksella että valitulla influenssa A-viruksen kannoilla. Tuotetut reassortanttivirukset kloonataan ja varmistetaan sekvensoimalla. Puolestaan influenssa B-virusten tuottoon influenssarokotteita varten käytetään tyypillisesti ainoastaan villityypin viruksia. (Wong &Webby 2013) Virusten tuotannon jälkeen valmistetaan lopullinen rokote, jonka jakelu aloitetaan pohjoisella pallonpuoliskolla elo-syyskuussa ja eteläisellä pallonpuoliskolla helmimaaliskuussa (Soema et al.2015) Ongelmat influenssarokotteen tuotantoprosessissa Influenssarokotteiden tuotannossa mahdollisia ongelmia aiheuttavat kananmunien saatavuus, virusten kasvamisnopeus sekä sääntelyvaatimukset. Lisäksi tuottajien täytyy myös täyttää bioturvallisuus sekä steriiliys vaatimukset tuotantoprosessin aikana (Wong & Webby 2013). Ongelmia aiheuttaa erityisesti influenssavirusten kasvatus kananmunissa, joka voitaisiin tulevaisuudessa ratkaista mm. käyttämällä soluviljelyä influenssavirusten kasvatukseen. Soluviljelyn käyttö influenssavirusten tuotannossa mahdollistaisi mm. suuremman tuoton sekä riippumattomuuden virusten tuotantoon sopivista kananmunista
15 (Soema et al. 2015) Lisäksi influenssavirusten tuottaminen kananmunissa aiheuttaa potentiaalisen riskin linnun patogeenien aiheuttamalle kontaminaatiolle sekä teoreettisen riskin henkilöille, jotka ovat allergisia kananmunille (Wong & Webby 2013). 6. Käytössä olevat influenssarokotteet Tällä hetkellä influenssarokote on tehokkain tapa suojautua influenssa A- ja B- viruksen aiheuttamaa infektiota vastaan (Soema et al.2015). Kausi-influenssarokotteen ottamista suositellaan yli 65-vuotiaille, pitkäaikaissairaudesta kärsiville henkilöille, terveydenalalla työskenteleville sekä raskaana oleville naisille (Wong & Webby 2013, Osterholm et al. 2012). Käytössä olevat influenssarokotteet antavat hyvin spesifisen suojan tietyille influenssa A- ja B-viruksen kannoille (Margine et al. 2013). Muodostunut immuniteetti kestää kuitenkin vain lyhyen ajan (Krammer & Palese 2015). Tällä hetkellä yleisimmin käytetty kausi-influenssarokote on trivalenttinen influenssa rokote (TIV) (Wong & Webby 2013). Lisäksi käytössä on LAIV-rokote, joka sisältää eläviä heikennettyjä influenssaviruksia. LAIV-rokote voidaan antaa henkilöille jotka ovat 2-49-vuotiaita, eivätkä ole raskaana. LAIV-rokotteen on todettu olevan tehokas erityisesti 2-7 vuotiaille lapsille. (Osterholm et al. 2012) Heikentyneestä immuunipuolustuksesta kärsiville henkilöille tai heidän lähiomaisilleen ei kuitenkaan suositella LAIV-rokotetta (Wong & Webby 2013). Influenssarokotteita valmistetaan erikseen vuotuisia epidemioita sekä ajoittaisia pandemioita varten. (Krammer & Palese 2015) Käytössä olevat influenssarokotteet sisältävät joko inaktivoituja influenssa A- ja B-viruksia tai eläviä heikennettyjä influenssa A- ja B-viruksia. Influenssarokotteen sisältämät inaktivoidut influenssavirukset voivat olla mm. kokonaisia tai pilkottuja influenssaviruksia (split-rokote). Lisäksi käytetään paljon ainoastaan influenssaviruksen pintaproteiineja sisältävää influenssarokotetta (subunit-rokote). (Soema et al. 2015) Käytössä olevat influenssarokotteet indusoivat pääasiassa neutralisoivien vastaaineiden tuotantoa HA:n globulaarista päädomeenia vastaan. Ongelmana on kutenkin jatkuva antigeeninen ajautuminen HA:n globulaarisessa päädomeenissa, jonka vuoksi hankittu immuunijärjestelmä ei kykene havaitsemaan influenssavirusta. (Margine et al. 2013) Näiden influenssarokotteiden tehokkuutta voitaisiin parantaa lisäämällä rokotteen immunogeenin määrää sekä käyttämällä adjuvantteja. Lisäksi QIV-rokotteella on saatu
16 parannettua TIV-rokotteen tehokkuutta lisäämällä yksi influenssa B-virus (Krammer & Palese 2015) Trivalenttinen influenssarokote (TIV) TIV-rokote on intramuskulaarisesti annettava influenssarokote, joka sisältää kaksi influenssa A-viruksen kantaa (H1N1 ja H3N2) sekä yhden influenssa B-viruksen linjoista (Yamagata ja Victoria) (Wong & Webby 2013, Sautto et al. 2018). Käytössä olevat TIV-rokotteet sisältävät pääasiassa joko pilkottuja influenssaviruksia tai ainoastaan influenssaviruksen pintaproteiineja. Kokonainen influenssavirus voidaan pilkkoa käyttämällä joko dietyylieetteriä tai pesuainekäsittelyä. Pilkkomisen jälkeen HA ja NA on mahdollista eristää lipidivaipasta subunit-rokotetta varten. Influenssaviruksen rakenteen pilkkominen influenssarokotetta varten heikentää influenssaviruksen luontaista immunogeenisyyttä. Lisäksi immunogeenisyyttä heikentää pilkkomisen yhteydessä menetettävä negatiivisäikeinen RNA. (Soema et al. 2015). Standardien mukaisessa TIV-rokotteessa on kaiken kaikkiaan 45µg HA:a eli 15µg kustakin rokotteessa käytetystä influenssaviruksesta (Wong & Webby 2013). TIVrokotteen tehokkuutta erityisesti ikäihmisiin sekä lapsiin voidaan parantaa esimerkiksi lisäämällä HA:n määrää rokotteessa tai käyttämällä sopivia adjuvantteja, kuten MF59- adjuvanttia. (Soema et al. 2015, Wong & Webby 2013). Lisäksi TIV-rokotteesta on lisensoitu myös intradermaalisesti eli ihonsisäisesti annettava split-rokote, joka sisältää 9µg HA-glykoproteiinia jokaisesta rokotteessa käytetystä influenssaviruksesta. Intradermaalisessa TIV-rokotteessa voidaan käyttää vähemmän HA:a kuin intramuskulaarisesti annettavassa rokotteessa ihon pinnalla olevien APC-solujen takia. (Soema et al. 2015) 6.2. Elävää heikennettyä influenssavirusta sisältävät rokotteet (LAIV-rokote) TIV-rokotteen lisäksi voidaan käyttää intranasaalisesti annettavaa influenssarokotetta, joka sisältää eläviä, heikennettyjä influenssaviruksia (LAIV-rokote) (Soema et al. 2015) LAIV-rokote sisältää TIV-rokotteen tavoin kaksi influenssa A-viruksen kantaa sekä toisen influenssa B-viruksen linjoista. (Wong & Webby 2013). Intranasaalisesti annettava LAIV-rokote jäljittelee luonnollista influenssaviruksen aiheuttamaa infektioita. (Soema et al. 2015)
17 LAIV-rokotteessa käytetään kylmäkäsiteltyjä influenssaviruksia, jotka elävät ja monistuvat lämpötilan ollessa +25 C:sta ja kuolevat lämpötilan noustessa +35 C.een. Toisin sanoen LAIV-rokotteen influenssavirukset kuolevat siirtyessään nenästä hengitysteihin. (Wong & Webby 2013). LAIV-rokote indusoi kauemmin kestävää vasta-ainevastetta kuin TIV-rokote (Wong & Webby 2013). Rokotteen tehokkuus perustuu vahvan mukosaalisen IgA-vasteen syntyyn sekä soluvälitteisen immuniteetin kehittymiseen influenssaviruksia vastaan (Soema et al. 2015) Nelivalenttinen influenssarokote (QIV) QIV-rokote kehitettiin parantamaan TIV-rokotteen tehokkuutta lisäämällä myös toinen influenssa B-viruksen kiertävistä linjoista rokotteeseen. QIV-rokote sisältääkin yhteensä neljää kiertävää influenssavirusta. Ylimääräisen influenssa B-viruksen linjan lisääminen lisää kausi-influenssarokotteen tehokuutta, koska useampana vuonna TIV-rokotteeseen on valittu väärä influenssa B-viruksen kiertävistä linjoista. (Soema et al. 2015) Moa et al. tekemän tutkimuksen mukaan QIV-rokote antaa yhtä hyvän tehokkuuden, kuin TIV-rokote käytetyille kahdelle influenssa A-viruksen kannoille sekä yhdelle influenssa B-viruksen käytetyistä linjoista. Lisäksi tutkimus osoitti QIV-rokotteen antavan erinomaisen suojan myös toiselle QIV-rokotteeseen lisätylle influenssa B-viruksen linjalle. (Moa et al. 2016) QIV-rokotteesta on kehitetty mm. sekä split-rokotteita että subunit-rokotteita. (Soema et al. 2015). Suomen sosiaali- ja terveysministeriön tiedotteen mukaan QIV-rokote otetaan käyttöön ensimmäistä kertaa Suomessa syksyllä Käyttöön otettava QIV-rokote on Sanofi Oy:ltä hankittu Vaxigrip Tetra -influenssarokote. (Sosiaali- ja terveysministeriö 2018) 6.4. Pandemiarokote Ainoastaan Influenssa A-virus voi aiheuttaa pandemioita, jos se kykenee levittäytymään ihmisestä toiseen tehokkaasti sekä omaa suurimmaksi osaksi uudelleen järjestäytyneen genomin, jossa on segmenttejä sekä ihmiseltä että muilta lajeilta. Pandemian jälkeen kyseinen influenssa A-virus jää kiertämään ja aiheuttaa kausittaisia epidemioita käyden samalla läpi antigeneettistä ajautumista. (Krammer & Palese 2015) Tällä hetkellä potentiaalisin pandemian aiheuttava influenssa A-virus on H5N1, joka on toisinaan aiheuttanut tappavia infektioita laajalla alueella. Ihmiset eivät ole kuitenkaan
18 täysin puolustuskyvyttömiä H5N1 virukselle, koska NA:n alatyyppi N1 on hyvin samankaltainen tällä hetkellä kiertävän H1N1 NA:n kanssa. Lisäksi monet Influenssa A- viruksen alatyypit, kuten H7N9 ja H6N1 ovat aiheuttaneet kuolemia Aasiassa. (Krammer & Palese 2015) Vaikka kokonaisia inaktivoituja influenssaviruksia käytetään harvemmin kausiinfluenssarokotteissa ovat ne yleisiä pandemiarokotteissa. Kokonaisia inaktivoituja influenssaviruksia käytetään pandemiarokotteissa niiden korkean immunogeenisyyden vuoksi. Lisäksi LAIV-rokotteen kaltaista rokotetta ollaan harkittu käytettäväksi influenssa A-viruksen aiheuttamaa pandemiaa vastaan. (Soema et al. 2015) Pandemiarokotteen tehokkuutta voidaan lisätä mm. käyttämällä adjuvantteja. (Soema et al. 2015) Lisäksi yksi strategia parantaa Pandemiarokotteen tehokkuutta on käyttämällä ensisijaisesti LAIV- tai DNA-rokotetta, jonka jälkeen annettaisiin tehosterokotteena inaktivoituja influenssaviruksia sisältävä influenssarokote (Krammer & Palese 2015). 7. Kehitteillä olevat universaalit influenssarokotteet Tänä päivänä käytettävät influenssarokotteet muodostavat immuniteetin ainoastaan rokotteessa käytetyille influenssa A- ja B-viruksen kannoille. Lisäksi influenssarokotteesta syntynyt immuniteetti on hyvin rajoittunut HA:n sekä NA:n antigeenistä variaatiota kohtaan. (Te Velthuis & Fodor 2016, Krammer & Palese 2015) Uudenlaisia influenssarokotteita kehitettäessä pyritään valmistamaan mahdollisimman universaali influenssarokote eli rokotteen antaman immuniteetin tulisi olla mahdollisimman laaja influenssa A- ja B-viruksien kantoja vastaan. Lisäksi influenssarokotteiden kehityksessä tehokkuutta ikäihmisille sekä immuunipuutoksesta kärsiville henkilöille pitäisi parantaa. (Soema et al. 2015) Universaalien influenssarokotteiden kehittämisessä on keskitytty kehittämään rokotteita, jotka luovat immuniteetin influenssa A- ja B-viruksissa esiintyviä muuttumattomia tai samankaltaisia alueita vastaan alatyypistä riippumatta. (Wong & Webby 2013). Tällaisia alueita ovat mm HA:n varsidomeeni sekä M2-ionikananvan N-terminaalinen ektodomeeni. Lisäksi yksi kehitteillä oleva influenssarokote keskittyy aktivoimaan T-soluvastetta. (Soema et al. 2015). Universaalin influenssarokotteen kehittäminen mahdollistaisi influenssarokotteen
19 ympärivuotisen valmistuksen, sillä rokotetta ei tarvitsisi uusia vuosittain. (Wong &Webby 2013). T-soluvaste Kuva 2. Kehitteillä olevien influenssarokotteiden aktivoimat vasta-aineet ja niiden vaikutukset influenssaviruksen monistumiseen sekä immuunijärjestelmään. HA:n pääspesifiset vasta-aineet inhiboivat influenssaviruksen sitoutumista siaalihappoon sekä solumembraanin ja viraalisen membraaninfuusioitumista. HA:n varsispesifiset vasta-aineet estävät endosomin fuusioitumisen. NAspesifiset sekä M2-spesifiset vasta-aineet inhiboivat influenssaviruksien vapautumista solusta. Lisäksi HA:n varsispesifiset vasta-aineet, HA:n pääspesifiset vasta-aineet sekä NA-spesifiset vasta-aineet aktivoivat immuunijärjestelmän eri reittejä mm. NK-solujen ja komplementtijärjestelmän avulla. M2- spesifiset vasta-aineet aktivoivat myös makrofageja. T-soluvastetta aktivoiva rokote aiheuttaa infektoituneiden solujen hajoamisen. (Rãjao & Pérez 2018) Kuvan lähde: Rajão & Pérez 2018 (muokattu ja suomennettu) 7.1. HA:n varsidomeeniin pohjautuvat influenssarokotteet Influenssaviruksen aiheuttama infektio aktivoi neutraloivien vasta-aineiden tuottoa HA:n globulaarista päädomeenia sekä varsidomeenia vastaan. Tällä hetkellä käytössä olevat influenssarokotteet indusoivat pääasiassa kuitenkin vasta-aineiden tuotantoa ainoastaan HA:n globulaarista päädomeenia vastaan. (Sautto et al. 2018)
20 HA:n varsireaktiiviset vasta-aineet voivat estää joko influenssaviruksen siirtymisen solun sisäpuolelle tai influenssaviruksen genomin vapautumisen solun sytosoliin (Soema et al. 2015). Lisäksi varsireaktiiviset vasta-aineet aktivoivat ADCC-mekanismin sekä komplementtijärjestelmän. (Krammer & Palese 2015) Varsi-reaktiiviset vasta-aineet mahdollistavat laajan immuniteetin sekä kausi-influenssaviruksia että pandemia influenssaviruksen kantoja vastaan. Jotta varsi-pohjainen influenssarokote antaisi laajan suojan influenssa A- ja B-viruksia vastaan täytyisi sen sisältää molemmista influenssa A-viruksen fylogeneettisista ryhmistä ainakin yhtä HA:a sekä influenssa B-viruksen HA:a. (Krammer et al. 2014) HA:n varsidomeeniin kohdistuvia influenssarokotteita on kehitteillä useita, koska HA:n varsidomeeni on hyvin konservoitunutta aluetta verrattuna globulaariseen päädomeeniin. (Sautto et al. 2018) Lisäksi mutaatiot HA:n varsidomeenin alueella voisivat mahdollisesti häiritä influenssa viruksen infektoimiskykyä (Krammer & Palese 2013). HA:n varsidomeeniin pohjautuvissa influenssarokotteissa ollaan käytetty mm. kimeeristä HA:a (Sautto et al. 2018). Kimeerinen HA koostuu influenssa A-viruksen H1 tai H3 varsidomeenista tai influenssa B-viruksen varsidomeenista. Lisäksi varsidomeeniin yhdistetään eksoottinen globulaarinen päädomeeni, joka on yleensä peräisin linnun influenssa A-virukselta. HA:n rikkisidokset rajaavat domeenit varsi- ja globulaariseen päädomeeniin. (Krammer & Palese 2015) On kuitenkin havaittu, että kimeeristä HA:a sisältävä influenssarokote antaa yhtä lyhyen suojan influenssaviruksia vastaan kuin tänä päivänä käytettävät influenssarokotteet. Immuniteetin kestoa voitaisiin mahdollisesti parantaa käyttämällä adjuvantteja rokotteessa. Kimeeristä HA:a sisältävä influenssarokote antaisi parhaimman ja monipuolisimman suojan peräkkäisinä annoksina antamalla ensin LAIV-rokote, jonka jälkeen immuniteetin kestävyyttä parannettaisiin vielä TIV-rokotteella. Tällaisen rokotesarjan toiminnan ajatellaan perustuvan eri immuunireittien aktivointiin, koska LAIV-rokote aktivoi ylähengitysteiden immuunijärjestelmää, kun taas intramuskulaarisesti annettava rokote aktivoi jo hankittua immuniteettiä. (Sautto et al. 2018) Useat tutkimustulokset ovat vahvistaneet kimeeristen HA:en muodostavan laajan immuniteetin influenssaviruksia vastaan. Krammer et al. hiirillä tekemän tutkimuksen mukaan peräkkäisinä annetut kimeeristä HA:a sisältävät influenssarokotteet mahdollistavan laajan humoraaliseen vasteen influenssaviruksia vastaan (Krammer et al. 2013). Lisäksi freteille tehty tutkimus on osoittanut kimeeristen HA:en olevan tehokkaita laajan immuniteetin muodostamisessa influenssaviruksia vastaan (Krammer et al. 2014)
21 Muissa HA:n varsidomeeniin pohjautuvissa influenssarokotteissa on käytetty mm. HA:a ilman globulaarista päädomeenia ja hyperglykolysoitua HA:n päädomeenia (ns. glykaanimaski) (Krammer & Palese 2015) HA:n Globulaariseen päädomeeniin pohjautuvat infuenssarokotteet Influenssaviruksen HA:n globulaarisesta päädomeenista löytyy epitooppeja, jotka eivät ole ainoastaan pysyviä influenssavirusten alatyypeillä vaan myös eri alatyyppien välillä. (Sautto et al. 2018) Laajempaa immuniteettiä influenssavirusten HA:n globulaarista päädomeenia kohtaan yritetään kehittää jatkuvasti. Globulaariseen päädomeeniin keskittyvässä influenssarokote kehityksessä keskitytään tunnistamaan ns. keskeisiä sekvenssejä, jotka ovat hyvin vanhoja. Lisäksi tehdään laskennallisia analyyseja (COBRA). COBRA on laskennallisesti optimoitu laajan valikoiman antigeenejä sisältävä synteettisesti valmistettu HA. (Krammer & Palese 2015) COBRA-pohjaiset influenssarokotteen prototyypit aktivoivat immuunivastetta, joka kykenee suojaamaan menneiltä ja nykyisiltä influenssaviruksilta sekä teoreettisesti myös tulevilta influenssaviruksilta. (Sautto et al. 2018) 7.3. NA:n pohjautuvat influenssarokotteet NA:ssa tapahtuu vähemmän antigeenistä ajautumista kuin HA:n globulaarisessa päädomeenissa. Tällä hetkellä käytettävissä influenssarokotteissa ei ole standardoitu NA:n määrää rokotetta kohden. Lisäksi NA:n stabiiliudesta sekä konfirmaatiosta käytettävissä rokotteissa ei ole varmaa tietoa. (Krammer & Palese 2015) NA pohjainen influenssarokote aktivoi NA-spesifisiä vasta-aineita, jotka vaikuttavat influenssaviruksen vapautumiseen solunpinnalta sekä uusien virusten tuotantoon laskevasti (Rajão & Pérez 2018) HA:n globulaarisen pään on huomattu olevan dominoivampi, jonka vuoksi vasta-ainevaste on suurempi HA:n globulaarista päädomeenia vastaan kuin NA:a. Tämän vuoksi NA:n pohjatuvissa influenssarokotteissa voitaisiinkin käyttää sekä NA:a että ns. eksoottisempia HA:n globulaarisia päädomeeneja tai ainoastaan NA:a. Kumpikin tapa aktivoisi enemmän NA-spesifisiä vasta-aineita kuin HA:n pääspesifisiä vasta-aineita. (Krammer & Palese 2015)
22 7.4. M2-ionikanavan ektodomeeniin pohjautuvat influenssarokotteet Tällä hetkellä käytössä olevat kausi-influenssarokotteet eivät juurikaan aktivoi M2- ionikanavalle spesifisiä vasta-aineita (Soema et al. 2015). M2-ionikanavan N-terminaalinen ektodomeeni sisältää hyvin pysyvän sekvenssin, joka on muuttumaton influenssavirusten välillä. Tämä sekvenssin samankaltaisuus influenssavirusten välillä mahdollistaa laajan immuunivasteen syntymisen influenssavirusten eri kantojen välille. (Fiers et al. 2009) Tällä hetkellä käytössä olevat kausi-influenssarokotteet eivät sisällä influenssaviruksen M2-proteiinia eikä se täten myöskään aktivoi vasta-aine tuotantoa M2-ionikanavia vastaan. (Soema et al. 2015) Todennäköisesti M2-spesifiset vasta-aineet eivät neutralisoi influenssavirusta (Wong & Webby 2013). M2-ionikanavan N-terminaaliselle ektodomeenille spesifiset vasta-aineet pystyvät merkitä solun NK-solujen tai makrofagien fagosytoitavaksi ADCC-mekanismin, Opsonisaation tai komplementtijärjestelmän avulla. (Rajão & Pérez 2018) Lisäksi nämä vasta-aineet voivat häiritä influenssaviruksen vapautumista solusta. M2- ionikanavaan pohjautuvat influenssarokotteet eivät kuitenkaan estä influenssaviruksen aiheuttamaa infektioita, mutta vasta-aineet pystyvät inhiboimaan viraalista replikoitumista viruksen kulkeutuessa soluun. (Soema et al. 2015) M2-ionikanavan N-terminaalisen ektodomeenin immunogeenisyys on luonnostaan huono, mutta immunogeenisyyttä on yritetty parantaa mm. lisäämällä rokotteeseen adjuvantteja, M2-ionikanavan multimeerisen rakenteen avulla, immunisoimalla muiden influenssarokotteiden kanssa sekä fuusioimalla kantajaproteiinin kanssa. (Rajão & Perez 2018) Esimerkiksi M2-ionikanavan N-terminaalisen ektodomeenin peptidi muokattiin erittäin immunogeeniseksi fuusioimalla se joko geneettisesti tai kemiallisesti sopivaan kantajaan, kuten viruksen kaltaiseen partikkeliin (VLP). (Fiers et al. 2009) 7.5. Sytotoksisia T-lymfosyyttejä aktivoivat influenssarokotteet Aktivoituvien sytotoksisten T-lymfosyyttien (CTL) määrää influenssarokotteen jälkeen on yritetty kasvattaa, koska CTL:t vaikuttavat erityisesti influenssaviruksen konservoituneisiin proteiineihin luoden laajemman immuniteetin influenssaviruksia vastaan. CTL:t vaikuttavat pääsiassa influenssaviruksen sisäisiin proteiineihin, jonka vuoksi CTL:t eivät estä infektion syntymistä vaan tarjoavat apua infektoituneille soluille sekä estävät infektion leviämistä muihin soluihin
23 Tutkimukset ovat osoittaneet, että influenssaviruksen aiheuttaman infektion olevan lievempi sekä nopeampi, jos henkilöllä on jo ennestään CTL:jä (Soema et al. 2015). Vaikka CTL-immuniteettiä aktivoivat influenssarokotteet eivät todennäköisesti estäisi infektiota tai sairautta ne voisivat vähentää merkittävästi influenssaviruksista johtuvia kuolemia. (Wong & Webby 2013). 8. Lopuksi Tällä hetkellä käytössä olevat influenssarokotteet eivät muodosta riittävän laajaa sekä kauan kestävää vastustuskykyä influenssaviruksia vastaan. Lisäksi käytössä olevien influenssarokotteiden tehokkuutta laskee huomattavasti yhteensopimattomuudet kiertävien influenssavirusten kanssa (Krammer & Palese 2015). Kehitteillä olevien universaalien influenssarokotteiden tulisi aktivoida useita eri immuunireittejä, kuten vasta-ainetuotantoa ja T-soluvastetta influenssaviruksien muuttumattomia sekä alatyyppien ylittäviä epitooppeja kohtaan. (Rajãro & Pérez 2018) Influenssaviruksen monistumisen ymmärtäminen isäntäsolussa mahdollistaisi mm. parempien rokotteiden kehityksen (Samji 2009). Lisäksi influenssaviruksen aktivoiman immuniteetin ymmärtäminen paremmin sekä laajemmin edesauttaisi tehokkaampien influenssarokotteiden kehitystä (Van de Sandt et al. 2012) Universaalien influenssarokotteiden tuotantoprosessin kehittäminen universaalille influenssarokotteelle vähentäisi merkittävästi influenssavirusten aiheuttamien epidemioiden sekä pandemioiden terveydellistä taakkaa (Rajãro & Pérez 2018). 9. Lähteet Bouvier NM & Palese P (2008) THE BIOLOGY OF INFLUENZA VIRUSES. Vaccine [online] 26(4):D49-D53 [viitattu 6 tammikuuta 2018] saatavissa: Byrd-Leotis L, Cummings RD & Steinhauer DA (2017) The Interplay between the Host Receptor and Influenza Virus Hemagglutinin and Neuraminidase. International Journal of Molecular Sciences [online] 18(7): 1541 [viitattu 20 maaliskuuta 2018] saatavissa: -
24 Fiers W, De Filette M, El Bakkouri K, Schepens B, Roose K, Schotsaert M, Birkett A & Saelens X (2009) M2e-based universal influenza A vaccine. Vaccine [online] 23;27(45): [viitattu 25 maaliskuuta 2018] saatavissa: Gagneux P, Cheriyan M, Hurtado-Ziola N, Brinkman van der Linden ECM, Anderson D, McClure H, Varki A and Varki NM (2011) Human-specific Regulation of α2 6-linked Sialic Acids. Journal of biological chemistry [online] 278: [viitattu 20 maaliskuuta 2018] saatavissa: Gamblin SJ & Skehel JJ (2010) Influenza Hemagglutinin and Neuraminidase Membrane Glycoproteins. Journal of biological chemistry [online] 285(37): [viitattu 10 maaliskuuta 2018] saatavissa: Krammer F & Palese P (2013) Influenza virus hemagglutinin stalk-based antibodies and vaccines. Current Opinion in Virology [online] 3(5): [viitattu 10 maaliskuuta 2018] saatavissa: Krammer F & Palese P (2015) Advances in the development of influenza virus vaccines. Nature reviews drug discovery [online] 14(3): [viitattu 1 maaliskuuta 2018] saatavissa: Krammer F, Hai R, Yondola, M, Tan GS, Leyva-Grado VH, Ryder AB, Miller MS, Rose,JK, Palese P, García-Sastre A & Albrecht RA (2014) Assessment of Influenza Virus Hemagglutinin Stalk-Based Immunity in Ferrets. Journal of Virology [online] 88(6): [viitattu 25 maaliskuuta 2018] saatavissa: Krammer F, Pica N, Hai R, Margine I & Palese P (2013). Chimeric Hemagglutinin Influenza Virus Vaccine Constructs Elicit Broadly Protective Stalk-Specific Antibodies. Journal of Virology [online] 87(12): [viitattu 25 maaliskuuta 2018] saatavissa: Kreijtz JH, Fouchier RA & Rimmelzwaan GF (2011) Immune responses to influenza virus infection. Virus research [online] 162:19-30 [viitattu 28 maaliskuuta 2018] saatavissa: Margine I, Krammer F, Hai R, Heaton NS, Tan GS, Andrews SA, Runstadler JA, Wilson PC, Albrecht RA, Garcia-sastre A & Palese P (2013). Hemagglutinin Stalk-Based Universal Vaccine Constructs Protect against Group 2 Influenza A Viruses. Journal of Virology [online]
25 87(19): [viitattu 18 maaliskuuta 2018] saatavissa: Moa AM, Chughtai AA, Muscatello DJ, Turner RM & MacIntyre CR (2016) Immunogenicity and safety of inactivated quadrivalent influenza vaccine in adults: A systematic review and meta-analysis of randomised controlled trials. Vaccine [online] 29;34(35): [viitattu 21 maaliskuuta 2018] saatavissa: Osterholm MT, Kelley NS, Sommer A, & Belongia EA (2012) Efficacy and effectiveness of influenza vaccines: a systematic review and meta-analysis.the lancet infectious diseases [online] 12(1):36-44 [viitattu 20 maaliskuuta 2018] saatavissa: Pielak RM & Chou JJ (2011) Influenza M2 proton channels. Biochimica et Biophysica Acta [online] 1808(2): [viitattu 15 maaliskuuta 2018] saatavissa: Pinto LH & Lamb RA (2005) The M2 Proton Channels of Influenza A and B Viruses. Journal of biological chemistry [online] 281, [viitattu 15 helmikuuta 2018] saatavissa: Rajão, DS & Pérez DR (2018) Universal Vaccines and Vaccine Platforms to Protect against Influenza Viruses in Humans and Agriculture. Frontiers in Microbiology [online] 9:123 [viitattu 15 maaliskuuta 2018] saatavissa: Samji T (2009) Influenza A: Understanding the Viral Life Cycl. Yale journal of biology and medicine [online] 82(4): [viitattu 15 maaliskuuta 2018] saatavissa: Sautto GA, Kirchenbaum GA & Ross TM (2018) Towards a universal influenza vaccine: different approaches for one goal. Virology Journal [online] 15:17 [viitattu 28 helmikuuta 2018] saatavissa: Soema PC, Kompier R, Amorij J-P & Kersten GFA (2015) Current and next generation influenza vaccines: Formulation and production strategies. European Journal of Pharmaceutics and Biopharmaceutics [online] 94: [viitattu 9 tammikuuta 2018] saatavissa: -
KandiakatemiA Kandiklinikka
 Kandiklinikka Kandit vastaavat Immunologia Luonnollinen ja hankittu immuniteetti IMMUNOLOGIA Ihmisen immuniteetti pohjautuu luonnolliseen ja hankittuun immuniteettiin. Immunologiasta vastaa lymfaattiset
Kandiklinikka Kandit vastaavat Immunologia Luonnollinen ja hankittu immuniteetti IMMUNOLOGIA Ihmisen immuniteetti pohjautuu luonnolliseen ja hankittuun immuniteettiin. Immunologiasta vastaa lymfaattiset
Bioteknologian tutkinto-ohjelma Valintakoe Tehtävä 3 Pisteet / 30
 Tampereen yliopisto Bioteknologian tutkinto-ohjelma Valintakoe 21.5.2015 Henkilötunnus - Sukunimi Etunimet Tehtävä 3 Pisteet / 30 3. a) Alla on lyhyt jakso dsdna:ta, joka koodaa muutaman aminohappotähteen
Tampereen yliopisto Bioteknologian tutkinto-ohjelma Valintakoe 21.5.2015 Henkilötunnus - Sukunimi Etunimet Tehtävä 3 Pisteet / 30 3. a) Alla on lyhyt jakso dsdna:ta, joka koodaa muutaman aminohappotähteen
Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö
 Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö 1 ESITYKSEN SISÄLTÖ Miten rokottaminen suojaa yksilöä? Immuunijärjestelmä Taudinaiheuttajilta suojaavan immuniteetin
Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö 1 ESITYKSEN SISÄLTÖ Miten rokottaminen suojaa yksilöä? Immuunijärjestelmä Taudinaiheuttajilta suojaavan immuniteetin
11. Elimistö puolustautuu
 11. Elimistö puolustautuu Taudinaiheuttajat Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin
11. Elimistö puolustautuu Taudinaiheuttajat Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin
Peptidi ---- F ----- K ----- V ----- R ----- H ----- A ---- A. Siirtäjä-RNA:n (trna:n) (3 ) AAG UUC CAC GCA GUG CGU (5 ) antikodonit
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 3 Pisteet / 20 Osa 1: Haluat selvittää -- F -- K -- V -- R -- H -- A peptidiä
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 3 Pisteet / 20 Osa 1: Haluat selvittää -- F -- K -- V -- R -- H -- A peptidiä
Influenssa. Niina Ikonen. Tartuntatautikurssi, Helsinki 8.4.2016
 Influenssa Niina Ikonen Tartuntatautikurssi, Helsinki 8.4.2016 Influenssan tautitaakka vuosittaisia epidemioita ja ajoittain pandemioita vuosittain 5-10% aikuisista ja 20-30% lapsista sairastuu influenssaan
Influenssa Niina Ikonen Tartuntatautikurssi, Helsinki 8.4.2016 Influenssan tautitaakka vuosittaisia epidemioita ja ajoittain pandemioita vuosittain 5-10% aikuisista ja 20-30% lapsista sairastuu influenssaan
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA MITÄ ROKOTUKSIA? Muistatko mitä rokotuksia olet saanut ja minkä viimeiseksi? Miten huolehdit koulun jälkeen rokotuksistasi? Mikrobit uhkaavat elimistöä Mikrobit voivat olla bakteereita,
BI4 IHMISEN BIOLOGIA MITÄ ROKOTUKSIA? Muistatko mitä rokotuksia olet saanut ja minkä viimeiseksi? Miten huolehdit koulun jälkeen rokotuksistasi? Mikrobit uhkaavat elimistöä Mikrobit voivat olla bakteereita,
Mitä opittiin kuluneen influenssakauden infektioista?
 Mitä opittiin kuluneen influenssakauden infektioista? Mika Salminen Professori Infektiotaudit -osasto Helsinki 13.5.2016 4.4.2016 Tartuntatautikurssi 2016/Niina Ikonen 1 Influenssan tautitaakka vuosittain
Mitä opittiin kuluneen influenssakauden infektioista? Mika Salminen Professori Infektiotaudit -osasto Helsinki 13.5.2016 4.4.2016 Tartuntatautikurssi 2016/Niina Ikonen 1 Influenssan tautitaakka vuosittain
Genomin ilmentyminen Liisa Kauppi, Genomibiologian tutkimusohjelma
 Genomin ilmentyminen 17.1.2013 Liisa Kauppi, Genomibiologian tutkimusohjelma liisa.kauppi@helsinki.fi Genomin ilmentyminen transkription aloitus RNA:n synteesi ja muokkaus DNA:n ja RNA:n välisiä eroja
Genomin ilmentyminen 17.1.2013 Liisa Kauppi, Genomibiologian tutkimusohjelma liisa.kauppi@helsinki.fi Genomin ilmentyminen transkription aloitus RNA:n synteesi ja muokkaus DNA:n ja RNA:n välisiä eroja
Elimistö puolustautuu
 Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Mistä taudinaiheuttajat
Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Mistä taudinaiheuttajat
IMMUNOLOGIAN PERUSTEET Haartman-instituutti
 IMMUNOLOGIAN PERUSTEET Petteri.Arstila@helsinki.fi 2012 Haartman-instituutti Immuunijärjestelmän tarkoituksena on torjua vieraita taudinaiheuttajia. Immuunipuolustus on organisoitu siten, että perifeerisissä
IMMUNOLOGIAN PERUSTEET Petteri.Arstila@helsinki.fi 2012 Haartman-instituutti Immuunijärjestelmän tarkoituksena on torjua vieraita taudinaiheuttajia. Immuunipuolustus on organisoitu siten, että perifeerisissä
Elimistö puolustautuu
 Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Miten elimistö
Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Miten elimistö
Sanna Nikunen ELL 4.10.2012
 Sanna Nikunen ELL 4.10.2012 Kuuluu heimoon Orthomyxoviridae, joka jaetaan kahteen sukuun; Influenssa A- ja B- virukset sekä influenssa C-virukset A-virukset eläimillä ja ihmisillä, B- virukset harvinaisempia,
Sanna Nikunen ELL 4.10.2012 Kuuluu heimoon Orthomyxoviridae, joka jaetaan kahteen sukuun; Influenssa A- ja B- virukset sekä influenssa C-virukset A-virukset eläimillä ja ihmisillä, B- virukset harvinaisempia,
6 GEENIT OHJAAVAT SOLUN TOIMINTAA nukleiinihapot DNA ja RNA Geenin rakenne Geneettinen informaatio Proteiinisynteesi
 6 GEENIT OHJAAVAT SOLUN TOIMINTAA nukleiinihapot DNA ja RNA Geenin rakenne Geneettinen informaatio Proteiinisynteesi GENEETTINEN INFORMAATIO Geeneihin pakattu informaatio ohjaa solun toimintaa ja siirtyy
6 GEENIT OHJAAVAT SOLUN TOIMINTAA nukleiinihapot DNA ja RNA Geenin rakenne Geneettinen informaatio Proteiinisynteesi GENEETTINEN INFORMAATIO Geeneihin pakattu informaatio ohjaa solun toimintaa ja siirtyy
100 vuotta Espanjantaudista voiko se toistua?
 100 vuotta Espanjantaudista voiko se toistua? Ilkka Julkunen, LKT, Virusopin professori Turun yliopisto ja TYKS jathl, Helsinki ilkka.julkunen@utu.fi Tarttuvat taudit. (s. 739) Influenssa on kulkutautina
100 vuotta Espanjantaudista voiko se toistua? Ilkka Julkunen, LKT, Virusopin professori Turun yliopisto ja TYKS jathl, Helsinki ilkka.julkunen@utu.fi Tarttuvat taudit. (s. 739) Influenssa on kulkutautina
Immuunijärjestelmän eri komponentit voidaan jakaa luonnolliseen ja adaptiiviseen immuniteettiin:
 1 IMMUUNIVASTEEN KULKU Petteri Arstila (2011) Immuunijärjestelmän tehtävä on torjua ulkoisia taudinaiheuttajia. Immuunipuolustukseen osallistuu iso joukko erilaisia soluja, jotka kuuluvat elimistön valkosoluihin
1 IMMUUNIVASTEEN KULKU Petteri Arstila (2011) Immuunijärjestelmän tehtävä on torjua ulkoisia taudinaiheuttajia. Immuunipuolustukseen osallistuu iso joukko erilaisia soluja, jotka kuuluvat elimistön valkosoluihin
Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20 3: Osa 1 Tumallisten solujen genomin toiminnassa sekä geenien
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20 3: Osa 1 Tumallisten solujen genomin toiminnassa sekä geenien
Molekyylitiedon avulla influenssaa vastaan
 Katsaus Leevi Kääriäinen ja Tero Ahola Molekyylitiedon avulla influenssaa vastaan Käänteisen genetiikan avulla pystytään nykyisin tuottamaan uusia influenssaviruksia, joista patogeenisuustekijät on eliminoitu
Katsaus Leevi Kääriäinen ja Tero Ahola Molekyylitiedon avulla influenssaa vastaan Käänteisen genetiikan avulla pystytään nykyisin tuottamaan uusia influenssaviruksia, joista patogeenisuustekijät on eliminoitu
RESPIRATORY SYNCYTIAL VIRUS (RSV)
 RESPIRATORY SYNCYTIAL VIRUS (RSV) Infektioiden torjuntapäivät 8.11.2018 Espoo, Dipoli 8.11.2018 Respiratory syncytial virus/ Niina Ikonen 1 RS-VIRUS Virus eristettiin 1956 Aiheuttaa vuosittaisia epidemioita
RESPIRATORY SYNCYTIAL VIRUS (RSV) Infektioiden torjuntapäivät 8.11.2018 Espoo, Dipoli 8.11.2018 Respiratory syncytial virus/ Niina Ikonen 1 RS-VIRUS Virus eristettiin 1956 Aiheuttaa vuosittaisia epidemioita
Hevosten rokottaminen. Eläinlääkäri Martti Nevalainen Intervet Oy, osa Schering-Plough konsernia
 Hevosten rokottaminen Eläinlääkäri Martti Nevalainen Intervet Oy, osa Schering-Plough konsernia Miksi rokotuttaa hevosia? Pyritään ennaltaehkäisemään tai lieventämään tartuntatauteja, jotka saattavat aiheuttaa
Hevosten rokottaminen Eläinlääkäri Martti Nevalainen Intervet Oy, osa Schering-Plough konsernia Miksi rokotuttaa hevosia? Pyritään ennaltaehkäisemään tai lieventämään tartuntatauteja, jotka saattavat aiheuttaa
Biologian tehtävien vastaukset ja selitykset
 Biologian tehtävien vastaukset ja selitykset Ilmainen lääkiksen harjoituspääsykoe, kevät 2017 Tehtävä 2. (20 p) A. 1. EPÄTOSI. Ks. s. 4. Menetelmää käytetään geenitekniikassa geenien muokkaamisessa. 2.
Biologian tehtävien vastaukset ja selitykset Ilmainen lääkiksen harjoituspääsykoe, kevät 2017 Tehtävä 2. (20 p) A. 1. EPÄTOSI. Ks. s. 4. Menetelmää käytetään geenitekniikassa geenien muokkaamisessa. 2.
Vastaa lyhyesti selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
Synteettinen biologia Suomessa: Virukset synteettisen biologian työkaluina
 Synteettinen biologia Suomessa: Virukset synteettisen biologian työkaluina Minna Poranen Akatemiatutkija Helsingin yliopisto FinSynBio-ohjelma Suomen Akatemia Virukset synteettisen biologian työkaluina
Synteettinen biologia Suomessa: Virukset synteettisen biologian työkaluina Minna Poranen Akatemiatutkija Helsingin yliopisto FinSynBio-ohjelma Suomen Akatemia Virukset synteettisen biologian työkaluina
Hankittu ja luontainen immuunijärjestelmä
 IMMUUNIJÄRJESTELMÄ Autoimmuunitaudeissa immuunijärjestelmä sekoaa, mutta kuinka immuunijärjestelmä toimii normaalisti. Olen kiinnostunut autoimmuunitautien toimintamekanismeista, mutta monien aihetta käsittelevien
IMMUUNIJÄRJESTELMÄ Autoimmuunitaudeissa immuunijärjestelmä sekoaa, mutta kuinka immuunijärjestelmä toimii normaalisti. Olen kiinnostunut autoimmuunitautien toimintamekanismeista, mutta monien aihetta käsittelevien
IMMUUNIPUUTOKSET. Olli Vainio Turun yliopisto
 IMMUUNIPUUTOKSET Olli Vainio Turun yliopisto 130204 IMMUNOLOGIA Oppi kehon puolustusmekanismeista infektiota vastaan Immuunijärjestelmä = kudokset, solut ja molekyylit, jotka muodostavat vastustuskyvyn
IMMUUNIPUUTOKSET Olli Vainio Turun yliopisto 130204 IMMUNOLOGIA Oppi kehon puolustusmekanismeista infektiota vastaan Immuunijärjestelmä = kudokset, solut ja molekyylit, jotka muodostavat vastustuskyvyn
Mitä opittiin lasten H1N1 (sikainfluenssa) -pandemiarokotteista
 Narkolepsiavanhempien tapaaminen Helsinki, 13.12.2010 Mitä opittiin lasten H1N1 (sikainfluenssa) -pandemiarokotteista Professori Timo Vesikari Rokotetutkimuskeskus Tampereen yliopisto Taustaa I WHO julisti
Narkolepsiavanhempien tapaaminen Helsinki, 13.12.2010 Mitä opittiin lasten H1N1 (sikainfluenssa) -pandemiarokotteista Professori Timo Vesikari Rokotetutkimuskeskus Tampereen yliopisto Taustaa I WHO julisti
Etunimi: Henkilötunnus:
 Kokonaispisteet: Lue oheinen artikkeli ja vastaa kysymyksiin 1-25. Huomaa, että artikkelista ei löydy suoraan vastausta kaikkiin kysymyksiin, vaan sinun tulee myös tuntea ja selittää tarkemmin artikkelissa
Kokonaispisteet: Lue oheinen artikkeli ja vastaa kysymyksiin 1-25. Huomaa, että artikkelista ei löydy suoraan vastausta kaikkiin kysymyksiin, vaan sinun tulee myös tuntea ja selittää tarkemmin artikkelissa
Immuunijärjestelmän toimintamekanismit
 Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Tunnin sisältö. Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS
 Immuunipuolustus Tunnin sisältö Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS Lymfaattinen elinjärjestelmä Muodostuu imukudoksesta imusuonet imusolmukkeet
Immuunipuolustus Tunnin sisältö Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS Lymfaattinen elinjärjestelmä Muodostuu imukudoksesta imusuonet imusolmukkeet
NON-CODING RNA (ncrna)
 NON-CODING RNA (ncrna) 1. Yleistä NcRNA eli non-coding RNA tarkoittaa kaikkia proteiinia koodaamattomia rnamolekyylejä. Näistä yleisimmin tunnetut ovat ribosomaalinen RNA (rrna) sekä siirtäjä-rna (trna),
NON-CODING RNA (ncrna) 1. Yleistä NcRNA eli non-coding RNA tarkoittaa kaikkia proteiinia koodaamattomia rnamolekyylejä. Näistä yleisimmin tunnetut ovat ribosomaalinen RNA (rrna) sekä siirtäjä-rna (trna),
Tutkimus odottaville äideille.
 Tutkimus odottaville äideille. Suojaa itsesi ja lapsesi influenssalta Hyvä odottava äiti! Tiesitkö, että influenssa on vakava tauti sekä odottavalle äidille että imeväisikäiselle lapselle? Se on myös riski
Tutkimus odottaville äideille. Suojaa itsesi ja lapsesi influenssalta Hyvä odottava äiti! Tiesitkö, että influenssa on vakava tauti sekä odottavalle äidille että imeväisikäiselle lapselle? Se on myös riski
Ribosomit 1. Ribosomit 2. Ribosomit 3
 Ribosomit 1 Palade & Siekevitz eristivät jaottelusentrifugaatiolla ns. mikrosomeja radioakt. aminohapot kertyivät mikrosomeihin, jotka peräisin rer:ää sisältävistä soluista proteiinisynteesi soluliman
Ribosomit 1 Palade & Siekevitz eristivät jaottelusentrifugaatiolla ns. mikrosomeja radioakt. aminohapot kertyivät mikrosomeihin, jotka peräisin rer:ää sisältävistä soluista proteiinisynteesi soluliman
Genomi-ilmentyminen Genom expression (uttryckning) Nina Peitsaro, yliopistonlehtori, Medicum, Biokemia ja Kehitysbiologia
 Genomi-ilmentyminen Genom expression (uttryckning) DNA RNA 7.12.2017 Nina Peitsaro, yliopistonlehtori, Medicum, Biokemia ja Kehitysbiologia Osaamistavoitteet Lärandemål Luennon jälkeen ymmärrät pääperiaatteet
Genomi-ilmentyminen Genom expression (uttryckning) DNA RNA 7.12.2017 Nina Peitsaro, yliopistonlehtori, Medicum, Biokemia ja Kehitysbiologia Osaamistavoitteet Lärandemål Luennon jälkeen ymmärrät pääperiaatteet
PROTEIINIEN MUOKKAUS JA KULJETUS
 PROTEIINIEN MUOKKAUS JA KULJETUS 1.1 Endoplasmakalvosto Endoplasmakalvosto on organelli joka sijaitsee tumakalvossa kiinni. Se on topologisesti siis yhtä tumakotelon kanssa. Se koostuu kahdesta osasta:
PROTEIINIEN MUOKKAUS JA KULJETUS 1.1 Endoplasmakalvosto Endoplasmakalvosto on organelli joka sijaitsee tumakalvossa kiinni. Se on topologisesti siis yhtä tumakotelon kanssa. Se koostuu kahdesta osasta:
GEENITEKNIIKAN PERUSASIOITA
 GEENITEKNIIKAN PERUSASIOITA GEENITEKNIIKKKA ON BIOTEKNIIKAN OSA-ALUE! Biotekniikka tutkii ja kehittää elävien solujen, solun osien, biokemiallisten menetelmien sekä molekyylibiologian uusimpien menetelmien
GEENITEKNIIKAN PERUSASIOITA GEENITEKNIIKKKA ON BIOTEKNIIKAN OSA-ALUE! Biotekniikka tutkii ja kehittää elävien solujen, solun osien, biokemiallisten menetelmien sekä molekyylibiologian uusimpien menetelmien
VASTAUS 1: Yhdistä oikein
 KPL3 VASTAUS 1: Yhdistä oikein a) haploidi - V) ihmisen sukusolu b) diploidi - IV) ihmisen somaattinen solu c) polyploidi - VI) 5n d) iturata - III) sukusolujen muodostama solulinja sukupolvesta toiseen
KPL3 VASTAUS 1: Yhdistä oikein a) haploidi - V) ihmisen sukusolu b) diploidi - IV) ihmisen somaattinen solu c) polyploidi - VI) 5n d) iturata - III) sukusolujen muodostama solulinja sukupolvesta toiseen
HEVOSEN INFLUENSSA: ESIINTYMINEN, VIRUSKANNAT, ROKOTUKSET JA VASTUSTUS
 HEVOSEN INFLUENSSA: ESIINTYMINEN, VIRUSKANNAT, ROKOTUKSET JA VASTUSTUS Maria Pyykönen Eläinlääketieteen lisensiaatin tutkielma Helsingin yliopisto Eläinlääketieteellinen tiedekunta Eläinlääketieteellisten
HEVOSEN INFLUENSSA: ESIINTYMINEN, VIRUSKANNAT, ROKOTUKSET JA VASTUSTUS Maria Pyykönen Eläinlääketieteen lisensiaatin tutkielma Helsingin yliopisto Eläinlääketieteellinen tiedekunta Eläinlääketieteellisten
Virustautien immunologia
 Virustautien immunologia Kalle Saksela L3 luento 4.11.2013 Yleistä virusimmunologiasta Virusten ja niiden isäntälajien pitkä yhteiselo evoluutiossa on tehnyt viruksista immuunipuolustuksen mestareita sekä
Virustautien immunologia Kalle Saksela L3 luento 4.11.2013 Yleistä virusimmunologiasta Virusten ja niiden isäntälajien pitkä yhteiselo evoluutiossa on tehnyt viruksista immuunipuolustuksen mestareita sekä
Rutto ja muut zoonoosit ihmiskunnan historiassa
 Rutto ja muut zoonoosit ihmiskunnan historiassa Heikki S. Vuorinen LKT, lääketieteen historian dosentti Tampereen yliopisto ja Helsingin yliopisto heikki.vuorinen@helsinki.fi RUTON LEVINNEISYYS KÄSITYS
Rutto ja muut zoonoosit ihmiskunnan historiassa Heikki S. Vuorinen LKT, lääketieteen historian dosentti Tampereen yliopisto ja Helsingin yliopisto heikki.vuorinen@helsinki.fi RUTON LEVINNEISYYS KÄSITYS
Virukset Materiaalitieteiden Rakennusaineina Suomalainen Tiedeakatemia
 Virukset Materiaalitieteiden Rakennusaineina Suomalainen Tiedeakatemia Mauri Kostiainen Molekyylimateriaalit-ryhmä Teknillisen fysiikan osasto Aalto-yliopisto Virukset materiaaleina Virus on isäntäsolussa
Virukset Materiaalitieteiden Rakennusaineina Suomalainen Tiedeakatemia Mauri Kostiainen Molekyylimateriaalit-ryhmä Teknillisen fysiikan osasto Aalto-yliopisto Virukset materiaaleina Virus on isäntäsolussa
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä
 Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
Usein kysyttyä kausi-influenssarokotuksista
 Lehdistötiedote 4.10.2011 Usein kysyttyä kausi-influenssarokotuksista 1) Suojaako viime talvena otettu sikainfluenssarokote edelleen? Syksyllä 2009 tai talvella 2010 otettu Pandemrix-rokote antaa edelleen
Lehdistötiedote 4.10.2011 Usein kysyttyä kausi-influenssarokotuksista 1) Suojaako viime talvena otettu sikainfluenssarokote edelleen? Syksyllä 2009 tai talvella 2010 otettu Pandemrix-rokote antaa edelleen
DNA:n informaation kulku, koostumus
 DNA:n informaation kulku, koostumus KOOSTUMUS Elävien bio-organismien koostumus. Vety, hiili, happi ja typpi muodostavat yli 99% orgaanisten molekyylien rakenneosista. Biomolekyylit voidaan pääosin jakaa
DNA:n informaation kulku, koostumus KOOSTUMUS Elävien bio-organismien koostumus. Vety, hiili, happi ja typpi muodostavat yli 99% orgaanisten molekyylien rakenneosista. Biomolekyylit voidaan pääosin jakaa
Influenssakausi Suomessa viikot 40/2012 20/2013
 Niina Ikonen Satu Murtopuro Mikko J. Virtanen Outi Lyytikäinen TYÖPAPERI Influenssakausi Suomessa viikot 40/2012 20/2013 28 2013 TYÖPAPERI 28/2013 Niina Ikonen, Satu Murtopuro, Mikko J. Virtanen, Outi
Niina Ikonen Satu Murtopuro Mikko J. Virtanen Outi Lyytikäinen TYÖPAPERI Influenssakausi Suomessa viikot 40/2012 20/2013 28 2013 TYÖPAPERI 28/2013 Niina Ikonen, Satu Murtopuro, Mikko J. Virtanen, Outi
Kenelle mikä influenssarokote ja miksi?
 Kenelle mikä influenssarokote ja miksi? Tartuntatautipäivät 9.11.2015 Tampere Hanna Nohynek 2015-11-09 TTpäivät Influenssa HNohynek 1 2015-11-09 2015-10-06 TTpäivät Influenssa HNohynek 2 2015-11-09 13.11.2015
Kenelle mikä influenssarokote ja miksi? Tartuntatautipäivät 9.11.2015 Tampere Hanna Nohynek 2015-11-09 TTpäivät Influenssa HNohynek 1 2015-11-09 2015-10-06 TTpäivät Influenssa HNohynek 2 2015-11-09 13.11.2015
Syöpä. Ihmisen keho muodostuu miljardeista soluista. Vaikka. EGF-kasvutekijä. reseptori. tuma. dna
 Ihmisen keho muodostuu miljardeista soluista. Vaikka nämä solut ovat tietyssä mielessä meidän omiamme, ne polveutuvat itsenäisistä yksisoluisista elämänmuodoista, jotka ovat säilyttäneet monia itsenäisen
Ihmisen keho muodostuu miljardeista soluista. Vaikka nämä solut ovat tietyssä mielessä meidän omiamme, ne polveutuvat itsenäisistä yksisoluisista elämänmuodoista, jotka ovat säilyttäneet monia itsenäisen
Tutkijat askelta lähempänä MS-taudin aiheuttajaa
 Tutkijat askelta lähempänä MS-taudin aiheuttajaa Tutkijat ovat askelta lähempänä MS-taudin aiheuttajaa. Exeterin ja Albertan yliopistojen kansainvälinen tutkijaryhmä löysi solujen toimintaan liittyvän
Tutkijat askelta lähempänä MS-taudin aiheuttajaa Tutkijat ovat askelta lähempänä MS-taudin aiheuttajaa. Exeterin ja Albertan yliopistojen kansainvälinen tutkijaryhmä löysi solujen toimintaan liittyvän
HLA alueen geenit ja niiden funktiot. Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti
 HLA alueen geenit ja niiden funktiot Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti 29.1.2014 Vieras versus oma Immuunijärjestelmä puolustaa elimistöä haitallisia organismeja vastaan
HLA alueen geenit ja niiden funktiot Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti 29.1.2014 Vieras versus oma Immuunijärjestelmä puolustaa elimistöä haitallisia organismeja vastaan
Genomin ylläpito Tiina Immonen BLL Lääke8eteellinen biokemia ja kehitysbiologia
 Genomin ylläpito 14.1.2014 Tiina Immonen BLL Lääke8eteellinen biokemia ja kehitysbiologia Luennon sisältö DNA:n kahdentuminen eli replikaa8o DNA:n korjausmekanismit Replikaa8ovirheiden korjaus Emäksenpoistokorjaus
Genomin ylläpito 14.1.2014 Tiina Immonen BLL Lääke8eteellinen biokemia ja kehitysbiologia Luennon sisältö DNA:n kahdentuminen eli replikaa8o DNA:n korjausmekanismit Replikaa8ovirheiden korjaus Emäksenpoistokorjaus
vauriotyypit Figure 5-17.mhc.restriktio 9/24/14 Autoimmuniteetti Kudosvaurion mekanismit Petteri Arstila Haartman-instituutti Patogeeniset mekanismit
 vauriotyypit Kudosvaurion mekanismit Autoimmuniteetti Petteri Arstila Haartman-instituutti Antigeenin tunnistus HLA:ssa pitää sisällään autoimmuniteetin riskin: jokaisella on autoreaktiivisia lymfosyyttejä
vauriotyypit Kudosvaurion mekanismit Autoimmuniteetti Petteri Arstila Haartman-instituutti Antigeenin tunnistus HLA:ssa pitää sisällään autoimmuniteetin riskin: jokaisella on autoreaktiivisia lymfosyyttejä
Pienryhmä 3 immuunipuolustus, ratkaisut
 Pienryhmä 3 immuunipuolustus, ratkaisut 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön
Pienryhmä 3 immuunipuolustus, ratkaisut 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön
Vaaralliset uudet lintuinfluenssaja koronavirusinfektiot ihmisillä
 Vaaralliset uudet lintuinfluenssaja koronavirusinfektiot ihmisillä Ilkka Julkunen Virologian yksikkö, THL, Helsinki ja Virusoppi, Turun yliopisto 07.02.2014 Lintuinfluenssa/MERS-infektiot/Julkunen 1 Respiratoriset
Vaaralliset uudet lintuinfluenssaja koronavirusinfektiot ihmisillä Ilkka Julkunen Virologian yksikkö, THL, Helsinki ja Virusoppi, Turun yliopisto 07.02.2014 Lintuinfluenssa/MERS-infektiot/Julkunen 1 Respiratoriset
Influenssavirusinfektioiden seuranta Suomessa
 Influenssavirusinfektioiden seuranta Suomessa Niina Ikonen Tartuntatautikurssi, Helsinki 15.4.2015 14.4.2015 Influenssavirusinfektioiden seuranta/niina Ikonen 1 Influenssa vuosittaisia epidemioita ja ajoittain
Influenssavirusinfektioiden seuranta Suomessa Niina Ikonen Tartuntatautikurssi, Helsinki 15.4.2015 14.4.2015 Influenssavirusinfektioiden seuranta/niina Ikonen 1 Influenssa vuosittaisia epidemioita ja ajoittain
TARTUNTATAUDIT Ellen, Olli, Maria & Elina
 TARTUNTATAUDIT Ellen, Olli, Maria & Elina ELIMISTÖN PUOLUSTUSKYKY Immuniteetti eli vastutuskyky on elimistön kyky suojautua tarttuvilta taudeilta Jos tauteja aiheuttavat mikrobit uhkaavat elimistöä, käynnistyy
TARTUNTATAUDIT Ellen, Olli, Maria & Elina ELIMISTÖN PUOLUSTUSKYKY Immuniteetti eli vastutuskyky on elimistön kyky suojautua tarttuvilta taudeilta Jos tauteja aiheuttavat mikrobit uhkaavat elimistöä, käynnistyy
VALMISTEYHTEENVETO. Injektioneste, suspensio esitäytetyssä ruiskussa. Kirkas, väritön neste.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Epaxal injektioneste, suspensio esitäytetyssä ruiskussa.. Hepatiitti A -rokote (inaktivoitu, virosomi). 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 rokoteannos (0,5
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Epaxal injektioneste, suspensio esitäytetyssä ruiskussa.. Hepatiitti A -rokote (inaktivoitu, virosomi). 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 rokoteannos (0,5
Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe Tehtävä 1 Pisteet / 15
 Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Spesifinen immuniteetti - Lymfosyyttityypit. 3. Puolustuslinja (hankittu ja spesifinen immuniteetti) Kahdenlaisia imusoluja (lymfosyyttejä):
 Eläinfysiologia ja histologia Luento X Kitarisat Nielurisat. Puolustuslinja (hankittu ja spesifinen immuniteetti) Spesifinen immuniteetti - Lymfosyyttityypit Lymfosyytti Kahdenlaisia imusoluja (lymfosyyttejä):
Eläinfysiologia ja histologia Luento X Kitarisat Nielurisat. Puolustuslinja (hankittu ja spesifinen immuniteetti) Spesifinen immuniteetti - Lymfosyyttityypit Lymfosyytti Kahdenlaisia imusoluja (lymfosyyttejä):
Vanilliini (karbonyyliyhdiste) Etikkahappo (karboksyyliyhdiste)
 1 a) Määrittele karbonyyliyhdiste. Piirrä esimerkkirakennekaava ja nimeä se. Samoin määrittele karboksyyliyhdiste, piirrä esimerkkirakennekaava ja nimeä se. Toisen esimerkin tulee olla rakenteeltaan avoketjuinen,
1 a) Määrittele karbonyyliyhdiste. Piirrä esimerkkirakennekaava ja nimeä se. Samoin määrittele karboksyyliyhdiste, piirrä esimerkkirakennekaava ja nimeä se. Toisen esimerkin tulee olla rakenteeltaan avoketjuinen,
Virus-mediated gene delivery for human gene therapy KURT NURMI
 Virus-mediated gene delivery for human gene therapy KURT NURMI 23.10.2017 Sisältö Lyhyesti geeniterapiasta, yleisimmistä virusvektoreista ja niiden ominaispiirteistä Kliininen käyttö ja ongelmat Johdanto
Virus-mediated gene delivery for human gene therapy KURT NURMI 23.10.2017 Sisältö Lyhyesti geeniterapiasta, yleisimmistä virusvektoreista ja niiden ominaispiirteistä Kliininen käyttö ja ongelmat Johdanto
Immuunijärjestelmän toimintamekanismit
 Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Mikrobiologian tenttitärpit Lyhyet kysymykset Toinen osatentti. Sisällys
 Mikrobiologian tenttitärpit Lyhyet kysymykset Toinen osatentti Sisällys Sivu 2 Antigeeni Antigeeniä esittelevä solu Antigenic drift Antigenic shift Aviditeetti Hemagglutiini Hereditäärinen angioödeema
Mikrobiologian tenttitärpit Lyhyet kysymykset Toinen osatentti Sisällys Sivu 2 Antigeeni Antigeeniä esittelevä solu Antigenic drift Antigenic shift Aviditeetti Hemagglutiini Hereditäärinen angioödeema
Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita
 Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita 10. Valkuaisaineiden valmistaminen solussa 1. Avainsanat 2. Perinnöllinen tieto on dna:n emäsjärjestyksessä 3. Proteiinit koostuvat
Perinnöllisyystieteen perusteita III Perinnöllisyystieteen perusteita 10. Valkuaisaineiden valmistaminen solussa 1. Avainsanat 2. Perinnöllinen tieto on dna:n emäsjärjestyksessä 3. Proteiinit koostuvat
Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen - Sic!
 Page 1 of 5 JULKAISTU NUMEROSSA 3-4/2017 EX TEMPORE Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen Enni-Kaisa Mustonen / Kirjoitettu 18.12.2017 / Julkaistu Oligonukleotidit ovat nukleotideista
Page 1 of 5 JULKAISTU NUMEROSSA 3-4/2017 EX TEMPORE Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen Enni-Kaisa Mustonen / Kirjoitettu 18.12.2017 / Julkaistu Oligonukleotidit ovat nukleotideista
VALMISTEYHTEENVETO. Injektioneste, suspensio esitäytetyssä ruiskussa. Kirkas, väritön neste.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Epaxal injektioneste, suspensio esitäytetyssä ruiskussa.. Hepatiitti A -rokote (inaktivoitu, virosomi). 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 rokoteannos (0,5
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Epaxal injektioneste, suspensio esitäytetyssä ruiskussa.. Hepatiitti A -rokote (inaktivoitu, virosomi). 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 rokoteannos (0,5
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
Autoimmuunitaudit: osa 1
 Autoimmuunitaudit: osa 1 Autoimmuunitaute tunnetaan yli 80. Ne ovat kroonisia sairauksia, joiden syntymekanismia eli patogeneesiä ei useimmissa tapauksissa ymmärretä. Tautien esiintyvyys vaihtelee maanosien,
Autoimmuunitaudit: osa 1 Autoimmuunitaute tunnetaan yli 80. Ne ovat kroonisia sairauksia, joiden syntymekanismia eli patogeneesiä ei useimmissa tapauksissa ymmärretä. Tautien esiintyvyys vaihtelee maanosien,
Hongkongilaisen influenssaviruksen jälkipolvet Suomessa 30 vuotta kujanjuoksua ja perässä pysyttelyä. Reijo Pyhälä
 Katsaus Hongkongilaisen influenssaviruksen jälkipolvet Suomessa 30 vuotta kujanjuoksua ja perässä pysyttelyä Reijo Pyhälä Ihmiseen siirtyneiden influenssavirusten evoluutio on armotonta peliä. Tartunnan
Katsaus Hongkongilaisen influenssaviruksen jälkipolvet Suomessa 30 vuotta kujanjuoksua ja perässä pysyttelyä Reijo Pyhälä Ihmiseen siirtyneiden influenssavirusten evoluutio on armotonta peliä. Tartunnan
BORNA VIRUKSEN FOSFOPROTEIININ p23 EPITOOPPIKARTOITUS BIOSIRULLA
 BORNA VIRUKSEN FOSFOPROTEIININ p23 EPITOOPPIKARTOITUS BIOSIRULLA Sari Pitkänen Pro Gradu Biokemian koulutusohjelma Biotieteellinen kemia Kuopion yliopiston biotieteiden laitos Kemian yksikkö Marraskuu
BORNA VIRUKSEN FOSFOPROTEIININ p23 EPITOOPPIKARTOITUS BIOSIRULLA Sari Pitkänen Pro Gradu Biokemian koulutusohjelma Biotieteellinen kemia Kuopion yliopiston biotieteiden laitos Kemian yksikkö Marraskuu
(B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT A 61K 37/02, 39/145, C 12N 15/44. (22) Hakemispäivä - Ansökningsdag 29.08.85
 (B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 85811 C (51) Kv.lk.5 - Int.c1.5 ' 10 C,1; A 61K 37/02, 39/145, C 12N 15/44 (21) Patenttihakemus - Patentansökning 853320 SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus
(B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 85811 C (51) Kv.lk.5 - Int.c1.5 ' 10 C,1; A 61K 37/02, 39/145, C 12N 15/44 (21) Patenttihakemus - Patentansökning 853320 SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus
Suoliston immuunijärjestelmä ja ruoka-allergia
 OULUN YLIOPISTO, GENETIIKAN JA FYSIOLOGIAN YKSIKKÖ Suoliston immuunijärjestelmä ja ruoka-allergia LuK -tutkielma Matilda Riskumäki 9.12.2016 1. Johdanto... 2 2. Immuunipuolustusjärjestelmä... 3 2.1. Luontainen
OULUN YLIOPISTO, GENETIIKAN JA FYSIOLOGIAN YKSIKKÖ Suoliston immuunijärjestelmä ja ruoka-allergia LuK -tutkielma Matilda Riskumäki 9.12.2016 1. Johdanto... 2 2. Immuunipuolustusjärjestelmä... 3 2.1. Luontainen
Biopolymeerit. Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä.
 Biopolymeerit Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä. Tärkeimpiä biopolymeerejä ovat hiilihydraatit, proteiinit ja nukleiinihapot. 1 Hiilihydraatit Hiilihydraatit jaetaan mono
Biopolymeerit Biopolymeerit ovat kasveissa ja eläimissä esiintyviä polymeerejä. Tärkeimpiä biopolymeerejä ovat hiilihydraatit, proteiinit ja nukleiinihapot. 1 Hiilihydraatit Hiilihydraatit jaetaan mono
Rokottaminen - käytännön ohjeita pulmatilanteisiin
 Rokottaminen - käytännön ohjeita pulmatilanteisiin Th Nina Strömberg Rokotusohjelmayksikkö THL 5.4.2016 1 Rokottamisen muistisäännöt Rokottamisessa ja rokotussarjojen aikatauluttamisessa on tietyt lainalaisuudet,
Rokottaminen - käytännön ohjeita pulmatilanteisiin Th Nina Strömberg Rokotusohjelmayksikkö THL 5.4.2016 1 Rokottamisen muistisäännöt Rokottamisessa ja rokotussarjojen aikatauluttamisessa on tietyt lainalaisuudet,
Ribosomit 1. Ribosomit 4. Ribosomit 2. Ribosomit 3. Proteiinisynteesin periaate 1
 Ribosomit 1 Ribosomit 4 Palade & Siekevitz eristivät jaottelusentrifugaatiolla ns. mikrosomeja radioakt. aminohapot kertyivät mikrosomeihin, jotka peräisin rer:ää sisältävistä soluista proteiinisynteesi
Ribosomit 1 Ribosomit 4 Palade & Siekevitz eristivät jaottelusentrifugaatiolla ns. mikrosomeja radioakt. aminohapot kertyivät mikrosomeihin, jotka peräisin rer:ää sisältävistä soluista proteiinisynteesi
Ajankohtaista infektioiden torjunnasta. Pekka Ylipalosaari Infektiolääkäri /OYS Infektioiden torjuntayksikkö 261015
 Ajankohtaista infektioiden torjunnasta Pekka Ylipalosaari Infektiolääkäri /OYS Infektioiden torjuntayksikkö 261015 Mikä on runsaasti kosketeltujen pintojen merkitys influenssan leviämisessä? 49 näytettä
Ajankohtaista infektioiden torjunnasta Pekka Ylipalosaari Infektiolääkäri /OYS Infektioiden torjuntayksikkö 261015 Mikä on runsaasti kosketeltujen pintojen merkitys influenssan leviämisessä? 49 näytettä
Kansallisen narkolepsiatyöryhmän väliraportti narkolepsian ja Pandemrix rokottamisen välisestä yhteydestä Terhi Kilpi
 Kansallisen narkolepsiatyöryhmän väliraportti narkolepsian ja Pandemrix rokottamisen välisestä yhteydestä Terhi Kilpi 1.2.2011 28.1.2011 1 Suomen tilanne 24.1.2011 THL saanut yhteensä 57 ilmoitusta narkolepsian
Kansallisen narkolepsiatyöryhmän väliraportti narkolepsian ja Pandemrix rokottamisen välisestä yhteydestä Terhi Kilpi 1.2.2011 28.1.2011 1 Suomen tilanne 24.1.2011 THL saanut yhteensä 57 ilmoitusta narkolepsian
22. Ihmiselimistön ulkoiset uhat
 Helena Hohtari Pitkäkurssi I 22. Ihmiselimistön ulkoiset uhat Immuunipuolustus Taudinaiheuttajat Erilaisia mikrobeja: - Bakteerit - Virukset - Sienet - Parasiitit Mikro-organismit elimistölle vieraita,
Helena Hohtari Pitkäkurssi I 22. Ihmiselimistön ulkoiset uhat Immuunipuolustus Taudinaiheuttajat Erilaisia mikrobeja: - Bakteerit - Virukset - Sienet - Parasiitit Mikro-organismit elimistölle vieraita,
Case Ebola ja opit viimeisestä pandemiasta. Mika Mäkinen 26.5.2015
 Case Ebola ja opit viimeisestä pandemiasta Mika Mäkinen 26.5.2015 Bank of America and Merill Lynch (2014): A severe pandemic could kill 360mn and hit global GDP by 5% Pandemian määritelmä Uusi taudin aiheuttaja
Case Ebola ja opit viimeisestä pandemiasta Mika Mäkinen 26.5.2015 Bank of America and Merill Lynch (2014): A severe pandemic could kill 360mn and hit global GDP by 5% Pandemian määritelmä Uusi taudin aiheuttaja
KEESHONDIEN MONIMUOTOISUUSKARTOITUS
 KEESHONDIEN MONIMUOTOISUUSKARTOITUS 2 3. 0 1. 2 0 1 1 K A A R I N A Marjut Ritala DNA-diagnostiikkapalveluja kotieläimille ja lemmikeille Polveutumismääritykset Geenitestit Serologiset testit Kissat, koirat,
KEESHONDIEN MONIMUOTOISUUSKARTOITUS 2 3. 0 1. 2 0 1 1 K A A R I N A Marjut Ritala DNA-diagnostiikkapalveluja kotieläimille ja lemmikeille Polveutumismääritykset Geenitestit Serologiset testit Kissat, koirat,
Miksi influenssarokotukset tulisi ottaa vakavasti? Valtakunnalliset tartuntatautipäivät Ritva Syrjänen ja Hanna Nohynek
 Miksi influenssarokotukset tulisi ottaa vakavasti? Valtakunnalliset tartuntatautipäivät 14.11.2016 Ritva Syrjänen ja Hanna Nohynek Torju influenssa, ota rokote https://www.youtube.com/watch?v=cvwjphuspag
Miksi influenssarokotukset tulisi ottaa vakavasti? Valtakunnalliset tartuntatautipäivät 14.11.2016 Ritva Syrjänen ja Hanna Nohynek Torju influenssa, ota rokote https://www.youtube.com/watch?v=cvwjphuspag
Immuunipuutokset. Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008
 Immuunipuutokset Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008 Immuunijärjestelm rjestelmän n toiminta Synnynnäinen immuniteetti (innate) Välitön n vaste (tunneissa)
Immuunipuutokset Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008 Immuunijärjestelm rjestelmän n toiminta Synnynnäinen immuniteetti (innate) Välitön n vaste (tunneissa)
Euroopan lääkeviraston rooli rokotteen turvallisuuden arvioinnissa - tapaus Pandemrix. Sosiaali- ja Terveysministeriö
 Euroopan lääkeviraston rooli rokotteen turvallisuuden arvioinnissa - tapaus Pandemrix Sosiaali- ja Terveysministeriö 13.12. 2010 Pekka Kurki Rokote tarvitsee myyntiluvan Kansalliset myyntiluvat Fimea arvioi
Euroopan lääkeviraston rooli rokotteen turvallisuuden arvioinnissa - tapaus Pandemrix Sosiaali- ja Terveysministeriö 13.12. 2010 Pekka Kurki Rokote tarvitsee myyntiluvan Kansalliset myyntiluvat Fimea arvioi
Solun tuman rakenne ja toiminta. Pertti Panula Biolääketieteen laitos 2012
 Solun tuman rakenne ja toiminta Pertti Panula Biolääketieteen laitos 2012 Hermosolun rakkulamainen tuma Monenlaisia tumia Valkosolujen tumien monimuotoisuutta Lähde: J.F.Kerr, Atlas of Functional Histology
Solun tuman rakenne ja toiminta Pertti Panula Biolääketieteen laitos 2012 Hermosolun rakkulamainen tuma Monenlaisia tumia Valkosolujen tumien monimuotoisuutta Lähde: J.F.Kerr, Atlas of Functional Histology
Ongelma(t): Mitä voimme oppia luonnosta? Miten voimme hyödyntää näitä oppeja?
 Ongelma(t): Mitä voimme oppia luonnosta? Miten voimme hyödyntää näitä oppeja? 2 Evoluutio on muovannut eliöt ja biomolekyylit elinympäristöönsä sopiviksi. Elinympäristön pysyessä suhteellisen muuttumattomana
Ongelma(t): Mitä voimme oppia luonnosta? Miten voimme hyödyntää näitä oppeja? 2 Evoluutio on muovannut eliöt ja biomolekyylit elinympäristöönsä sopiviksi. Elinympäristön pysyessä suhteellisen muuttumattomana
Injektioneste, suspensio. Vaaleanpunertava tai valkoinen neste, joka sisältää valkoista sakkaa. Sakka sekoittuu helposti ravisteltaessa.
 1. ELÄINLÄÄKKEEN NIMI Trilyme injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi annos (1 ml) sisältää: Vaikuttavat aineet: Inaktivoitu Borrelia burgdorferi sensu lato: Borrelia
1. ELÄINLÄÄKKEEN NIMI Trilyme injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi annos (1 ml) sisältää: Vaikuttavat aineet: Inaktivoitu Borrelia burgdorferi sensu lato: Borrelia
DNA, RNA ja proteiinirakenteen ennustaminen
 S-114.500 Solubiosysteemien perusteet Harjoitustyö Syksy 2003 DNA, RNA ja proteiinirakenteen ennustaminen Ilpo Tertsonen, 58152p Jaakko Niemi, 55114s Sisällysluettelo 1. Alkusanat... 3 2. Johdanto... 4
S-114.500 Solubiosysteemien perusteet Harjoitustyö Syksy 2003 DNA, RNA ja proteiinirakenteen ennustaminen Ilpo Tertsonen, 58152p Jaakko Niemi, 55114s Sisällysluettelo 1. Alkusanat... 3 2. Johdanto... 4
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKEVALMISTEEN NIMI RESPIPORC FLUpan H1N1 suspensio injektiota varten sioille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Jokainen 1 ml:n annos sisältää: Vaikuttava(t)
LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKEVALMISTEEN NIMI RESPIPORC FLUpan H1N1 suspensio injektiota varten sioille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Jokainen 1 ml:n annos sisältää: Vaikuttava(t)
Vasta-aineiden merkitys elinsiirroissa
 Vasta-aineiden merkitys elinsiirroissa Jouni Lauronen Elinsiirtojen perusteet kurssi 29.1.14 1 1 1 1 1 Vasta-aineiden merkitys elinsiirroissa Vasta-aineet voivat johtaa elinsiirtotarpeeseen Autoimmuunitaudit
Vasta-aineiden merkitys elinsiirroissa Jouni Lauronen Elinsiirtojen perusteet kurssi 29.1.14 1 1 1 1 1 Vasta-aineiden merkitys elinsiirroissa Vasta-aineet voivat johtaa elinsiirtotarpeeseen Autoimmuunitaudit
DNA RNA proteiinit transkriptio prosessointi translaatio regulaatio
 CELL 411-- replikaatio repair mitoosi meioosi fertilisaatio rekombinaatio repair mendelistinen genetiikka DNA-huusholli Geenien toiminta molekyyligenetiikka DNA RNA proteiinit transkriptio prosessointi
CELL 411-- replikaatio repair mitoosi meioosi fertilisaatio rekombinaatio repair mendelistinen genetiikka DNA-huusholli Geenien toiminta molekyyligenetiikka DNA RNA proteiinit transkriptio prosessointi
HUSLAB Immunologian osasto Labquality-päivät Vasta-aineet
 Ilkk S älä Ilkka Seppälä HUSLAB Immunologian osasto Labquality-päivät 2010 Vasta-aineet Fab Fab Fc IgG, IgD J IgA IgE J IgM IgM:n monomeeriyksikkö ja IgD ovat käytössä B-lymfosyyttien yy antigeenia tunnistavina
Ilkk S älä Ilkka Seppälä HUSLAB Immunologian osasto Labquality-päivät 2010 Vasta-aineet Fab Fab Fc IgG, IgD J IgA IgE J IgM IgM:n monomeeriyksikkö ja IgD ovat käytössä B-lymfosyyttien yy antigeenia tunnistavina
Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä. Septinen shokki. Tulehdusreaktio 1/2
 Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä 1/2 Tulehdusreaktio Septinen shokki Tiettyjen bakteeri-infektioiden aikaansaama suunnaton immuunijärjestelmän tulehdusvaste
Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä 1/2 Tulehdusreaktio Septinen shokki Tiettyjen bakteeri-infektioiden aikaansaama suunnaton immuunijärjestelmän tulehdusvaste
Nivelreuman serologiset testit: mitä ne kertovat? LT, apulaisylilääkäri Anna-Maija Haapala TAYS Laboratoriokeskus
 Nivelreuman serologiset testit: mitä ne kertovat? LT, apulaisylilääkäri Anna-Maija Haapala TAYS Laboratoriokeskus Sisältö 1. Nivelreuma: etiologia, esiintyvyys, diagnostiikka 2. Nivelreuman serologiset
Nivelreuman serologiset testit: mitä ne kertovat? LT, apulaisylilääkäri Anna-Maija Haapala TAYS Laboratoriokeskus Sisältö 1. Nivelreuma: etiologia, esiintyvyys, diagnostiikka 2. Nivelreuman serologiset
Biomolekyylit ja biomeerit
 Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
DNA (deoksiribonukleiinihappo)
 DNA (deoksiribonukleiinihappo) Kaksoiskierre (10 emäsparin välein täysi kierros) Kaksi sokerifosfaattirunkoa. Huomaa suunta: 5 -päässä vapaana fosfaatti (kiinni sokerin 5. hiilessä) 3 -päässä vapaana sokeri
DNA (deoksiribonukleiinihappo) Kaksoiskierre (10 emäsparin välein täysi kierros) Kaksi sokerifosfaattirunkoa. Huomaa suunta: 5 -päässä vapaana fosfaatti (kiinni sokerin 5. hiilessä) 3 -päässä vapaana sokeri
Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress
 Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress Twan Lammers, Fabian Kiessling, Wim E. Hennik, Gert Storm Journal of Controlled Release 161: 175-187, 2012 Sampo Kurvonen 9.11.2017
Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress Twan Lammers, Fabian Kiessling, Wim E. Hennik, Gert Storm Journal of Controlled Release 161: 175-187, 2012 Sampo Kurvonen 9.11.2017
HPV-rokote tulee rokotusohjelmaan mitä, kenelle, miksi?
 HPV-rokote tulee rokotusohjelmaan mitä, kenelle, miksi? Tuija Leino THL Kerron tässä alkavasta rokotusohjelmasta rokotteesta Miksi otettu ohjelmaan? Miltä taudilta suojaudutaan? Miksi otettu ohjelmaan
HPV-rokote tulee rokotusohjelmaan mitä, kenelle, miksi? Tuija Leino THL Kerron tässä alkavasta rokotusohjelmasta rokotteesta Miksi otettu ohjelmaan? Miltä taudilta suojaudutaan? Miksi otettu ohjelmaan
Tulehdus ja karsinogeneesi. Tulehduksen osuus syövän synnyssä. Tulehdus ja karsinogeneesi. Tulehdus ja karsinogeneesi. Tulehdus ja karsinogeneesi
 Tulehduksen osuus syövän synnyssä Ari Ristimäki, professori Patologia Helsingin yliopisto esiasteissa ja useissa eri syöpäkasvaintyypeissä. 1 A Mantovani, et al. NATURE Vol 454 24 July 2008 Figure 15.22d
Tulehduksen osuus syövän synnyssä Ari Ristimäki, professori Patologia Helsingin yliopisto esiasteissa ja useissa eri syöpäkasvaintyypeissä. 1 A Mantovani, et al. NATURE Vol 454 24 July 2008 Figure 15.22d
"Geenin toiminnan säätely" Moniste sivu 13
 "Geenin toiminnan säätely" Moniste sivu 13 Monisteen alussa on erittäin tärkeitä ohjeita turvallisuudesta Lukekaa sivu 5 huolellisesti ja usein Vaarat vaanivat: Palavia nesteitä ja liekkejä on joskus/usein
"Geenin toiminnan säätely" Moniste sivu 13 Monisteen alussa on erittäin tärkeitä ohjeita turvallisuudesta Lukekaa sivu 5 huolellisesti ja usein Vaarat vaanivat: Palavia nesteitä ja liekkejä on joskus/usein
Virusten genomien evoluutio Robert Kesälahti A LuK-tutkielma Kevät 2017
 Virusten genomien evoluutio Robert Kesälahti 750376A LuK-tutkielma Kevät 2017 Avainsanat: mutaationopeus, influenssavirus, ebolavirus, infektiomekanismit 1 Sisällysluettelo 1. Johdanto... 3 2. Virusten
Virusten genomien evoluutio Robert Kesälahti 750376A LuK-tutkielma Kevät 2017 Avainsanat: mutaationopeus, influenssavirus, ebolavirus, infektiomekanismit 1 Sisällysluettelo 1. Johdanto... 3 2. Virusten
VaxigripTetra injektioneste, suspensio, esitäytetty ruisku , versio 4.0
 VaxigripTetra injektioneste, suspensio, esitäytetty ruisku 16.3.2016, versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Influenssa
VaxigripTetra injektioneste, suspensio, esitäytetty ruisku 16.3.2016, versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Influenssa
Genomin ilmentyminen
 Kauppi 17/01/2014 Genomin ilmentyminen LH1, Molekyylibiologia 17.1.2014 Liisa Kauppi, Genomibiologian tutkimusohjelma liisa.kauppi@helsinki.fi Huone C501b, Biomedicum 1 Transkriptiofaktorin mutaatio voi
Kauppi 17/01/2014 Genomin ilmentyminen LH1, Molekyylibiologia 17.1.2014 Liisa Kauppi, Genomibiologian tutkimusohjelma liisa.kauppi@helsinki.fi Huone C501b, Biomedicum 1 Transkriptiofaktorin mutaatio voi
