1-1 Makroskooppinen fysiikka
|
|
|
- Lauri Tamminen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 1 1 Peruskäsitteitä 1-1 Makroskooppinen fysiikka Statistinen fysiikka tutkii makroskooppisia systeemejä. Systeemi on makroskooppinen, jos se muodostuu hyvin suuresta joukosta atomeja tai molekyylejä. Niiden lukumäärän suuruusluokkaa luonnehtii Avogadron luku (Avogadron vakio) N A = Esimerkiksi litra yhden ilmakehän paineessa ja huoneenlämpötilassa olevaa ilmaa muodostaa makroskooppisen systeemin. Makroskooppisen systeemin täydellinen eli mikroskooppinen kuvaus antaisi tiedon systeemin tilasta molekyylitason tarkkuudella. Tämä edellyttäisi, että pystyttäisiin määrittämään esimerkiksi molekyylin paikat ja nopeudet ajan funktiona. Tällaista tehtävää ei voida käytännössä mitenkään toteuttaa. Näin ollen makroskooppisten systeemien täydellinen mikroskooppinen kuvaaminen ei ole mahdollista. Vaikka makroskooppisten systeemien käyttäytyminen on molekyylitasolla tarkasteltuna äärimmäisen monimutkaista, tietyt makroskooppiset suureet (esimerkiksi paine ja lämpötila) noudattavat kuitenkin yksinkertaisia lakeja. Esimerkiksi: jos kuuma ja kylmä kappale asetetaan kosketuksiin toistensa kanssa, niiden lämpötilat tasaantuvat; yhden ilmakehän paineessa oleva vesi kiehuu aina samassa lämpötilassa; harvan kaasun paine voidaan laskea ideaalikaasun tilanyhtälöllä. Nämä makroskooppiset suureet ovat systeemin mikroskooppisten ominaisuuksien yli otettuja keskiarvoja. Tästä seuraa, että makroskooppiset lait ovat luonteeltaan statistisia (tilastollisia). Tällaisten suureiden todelliset arvot vaihtelevat epäsäännöllisesti eli fluktuoivat (engl. fluctuate) keskiarvojensa ympärillä niitä kuvaavien jakaumafunktioiden (engl. distribution function) osoittamilla todennäköisyyksillä. Molekyylien suuren lukumäärän takia jakaumafunktiot ovat kuitenkin normaalisti äärimmäisen kapeita. Tästä syystä fluktuaatiot ovat niin vähäisiä, että niillä ei ole tavallisesti mitään merkitystä. Näin ollen statistiset lait johtavat käytännössä täysin tarkkoihin ennusteisiin makroskooppisten suureiden käyttäytymisestä. Esimerkki Kaasun paine (P ) voidaan määrittää mäntään (pinta-ala A) kohdistuvan voiman (F ) avulla: P = F/A. Mikroskooppisessa tarkastelussa paine johtuu kaasumolekyylien kimmoisista törmäyksistä mäntään. Tästä syystä mäntään kohdistuva voima on nopeasti vaihteleva ajan funktio ja mäntä suorittaa pientä epäsäännöllistä värähdysliikettä tasapainoasemansa ympärillä (ns. Brownin liikettä).
2 Painetta laskettaessa käytetään voiman keskiarvoa yli tarpeeksi pitkän aikavälin, jonka kuluessa tapahtuu monia törmäyksiä. Tällöin keskiarvo voidaan määrittää molekyylien nopeusjakauman avulla laskemalla liikemäärän muutos aikayksikössä. Makroskooppiseen mäntään kohdistuvan voiman fluktuaatiot ovat äärimmäisen pieniä ja tästä syystä voiman todelliset (hetkelliset) arvot poikkeavat keskiarvostaan merkityksettömän vähän. 2 Makroskooppisten systeemien käyttäytymistä on fysiikan historiassa tarkasteltu kahta hyvin erilaista lähestymistapaa käyttäen: 1. Klassinen termodynamiikka kehittäjinä mm. Sadi Carnot ( ), Rudolf Clausius ( ), William Thomson (lordi Kelvin, ), Robert von Mayer ( ) ja James Joule ( ) perustuu pieneen joukkoon perusperiaatteita, termodynamiikan pääsääntöihin (engl. laws of thermodynamics) lait (esimerkiksi ideaalikaasun tilanyhtälö) ovat fenomenologisia (engl. phenomenological), ts. ne on johdettu ja yleistetty makroskooppisia systeemejä koskevista kokeellisista havainnoista, ei mikroskooppisesta kuvauksesta lait kuvaavat systeemien ominaisuuksia ainoastaan makroskooppisten suureiden (paine, tilavuus, lämpötila jne.) avulla 2. Statistinen mekaniikka kehittäjinä mm. James Clerk Maxwell ( ), Ludwig Boltzmann ( ) ja Josiah Willard Gibbs ( ) pyrkii johtamaan makroskooppisten systeemien lainalaisuudet niiden mikroskooppisista ominaisuuksista käsittelee makroskooppisia suureita mikroskooppisten koordinaattien yli otettuina keskiarvoina 1-2 Lämpötila ja lämpötasapaino Lämpötilan (engl. temperature) käsite on peräisin tuntoaistiemme välittämästä kuuman tai kylmän aistimuksesta. Lämpötila on se aineen ominaisuus, joka aistitaan kuumuutena tai kylmyytenä. Mitä kuumemmalta jokin kappale tuntuu, sitä korkeampi sen lämpötila tavallisesti on. Jotta lämpötila voitaisiin määritellä täsmällisesti, sille tarvitaan jokin objektiivinen, aistimuksista riippumaton mitta-asteikko. Tämä voi perustua sellaisiin mitattavissa oleviin aineen ominaisuuksiin, jotka riippuvat lämpötilasta. Tällaisia ominaisuuksia ovat esimerkiksi metallisauvan pituus, lämmityskattilan höyrynpaine, metallilangan sähkönjohtokyky ja hehkuvan kappaleen väri. Kuvat 1(a) ja 1(b) esittävät kahta yksinkertaista systeemiä, joita voidaan käyttää lämpötilan mittaamiseen. Kun lämpötila nousee, värjätty neste (tavallisesti elohopea tai etyylialkoholi) laajenee ja nousee kapillaariputkessa, tai säiliössä olevan kaasun paine kasvaa. Mitattavat ominaisuudet ovat näissä tapauksissa nestepatsaan korkeus L ja kaasun paine P, ja niiden avulla voidaan rakentaa lämpömittari (engl. thermometer).
3 3 Kuva 1. Jotta kuuman kappaleen lämpötila voitaisiin määrittää, se on asetettava vuorovaikutukseen lämpömittarin kanssa (tämä ei kuitenkaan tarkoita sitä, että mittarin olisi kirjaimellisesti kosketettava kappaletta). Tällaisen termisen kontaktin seurauksena lämpömittari kuumenee (ja samalla itse kappale jäähtyy jonkin verran). Lämpötila voidaan lukea sen jälkeen, kun lämpömittarin kuumeneminen on lakannut. Tällöin systeemi on saavuttanut lämpötasapainon eli termisen tasapainon (engl. thermal equilibrium), jossa sen lämpötila ei enää muutu. Jos kaksi systeemiä erotetaan toisistaan eristeellä (engl. insulator) esimerkiksi puulla, vaahtomuovilla tai lasivillalla niiden keskinäinen vuorovaikutus vähenee. Tällöin systeemien keskinäisen lämpötasapainon saavuttamiseen kuluu pitkä aika. Jos eriste olisi täydellinen, tasapainoa ei syntyisi lainkaan. Tarkastellaan kolmea ulkomaailmasta eristettyä systeemiä A, B ja C, jotka eivät aluksi ole keskenään lämpötasapainossa (kuva 2). Ensimmäisessä vaiheessa systeemit A ja B eristetään toisistaan, mutta molemmat asetetaan termiseen kontaktiin systeemin C kanssa käyttäen niiden välissä lämmönjohdetta (engl. thermal conductor), joka sallii systeemien Kuva 2.
4 välisen termisen vuorovaikutuksen. Tällöin sekä systeemi A että systeemi B saavuttavat jonkin ajan kuluttua lämpötasapainon systeemin C kanssa. Ovatko systeemit A ja B samalla saavuttaneet lämpötasapainon myös keskenään? Tämä saadaan selville korvaamalla systeemien A ja B välissä oleva eriste lämmönjohteella ja eristämällä ne systeemistä C (kuva 2(b)). Kokeet osoittavat, että tässä toisessa vaiheessa systeemeille ei tapahdu mitään. Tehdyillä muutoksilla ei ole systeemeihin mitään vaikutusta, eikä niiden tila enää muutu. Tämä merkitsee sitä, että systeemit A ja B olivat saavuttaneet keskinäisen tasapainon jo ensimmäisessä vaiheessa. Näin saatua tulosta voidaan sanoa termodynamiikan nollanneksi pääsäännöksi (engl. zeroth law of thermodynamics): Jos sekä A että B ovat lämpötasapainossa C:n kanssa, A ja B ovat lämpötasapainossa myös keskenään. Tämän tuloksen kutsumista nollanneksi pääsäännöksi voidaan perustella sillä, että sen tärkeys kävi ilmi vasta termodynamiikan ensimmäisen, toisen ja kolmannen pääsäännön muotoilemisen ja nimeämisen jälkeen. Se voidaan kohottaa pääsääntöjen joukkoon, koska sillä on perustavanlaatuinen merkitys kaikille muille pääsäännöille. Jos systeemi C on lämpömittari, sen lukema osoittaa kuvan 2(a) tapauksessa (lämpötasapainon saavuttamisen jälkeen) sekä systeemin A että systeemin B lämpötilan (koska C on kontaktissa sekä A:n että B:n kanssa). Tästä seuraa, että systeemeillä A ja B on tässä vaiheessa sama lämpötila. Kokeet osoittavat, että eristeiden lisääminen tai poistaminen ei tämän jälkeen enää muuta systeemien välistä lämpötasapainoa. Näin ollen lämpömittarin C lukema ei muutu, vaikka se olisi kontaktissa vain A:n tai vain B:n kanssa. Tästä voidaan päätellä, että kaksi systeemiä on lämpötasapainossa keskenään jos ja vain jos niiden lämpötilat ovat samat. Lämpömittarin hyödyllisyys perustuu juuri tähän tulokseen: itse asiassa lämpömittari mittaa vain oman lämpötilansa, mutta sen ollessa lämpötasapainossa toisen kappaleen kanssa saatu lämpötila on sama kuin ko. toisen kappaleen lämpötila. Jos kahden systeemin lämpötilat poikkeavat toisistaan, ne eivät voi olla lämpötasapainossa keskenään. Nämä tulokset saavat yksinkertaisen fysikaalisen selityksen, jos lämpötilan tulkitaan kuvaavan systeemin molekyylien satunnaisliikkeen keskimääräistä energiaa. Lämpötilaerojen spontaani tasaantuminen johtuu energian virtaamisesta kuumasta systeemistä kylmään systeemiin. Tällaista nimenomaan lämpötilaeron takia tapahtuvaa energian siirtymistä sanotaan lämpövirraksi (engl. heat flow tai flow of heat). Energian siirtyminen jatkuu, kunnes molekyylien keskimääräiset liike-energiat ovat kummassakin systeemissä samat. Tässä vaiheessa systeemien lämpötilat ovat samat ja systeemit ovat keskinäisessä lämpötasapainossa, joten lämpövirta lakkaa Lämpömittarit ja lämpötila-asteikot Nestepatsaan korkeuteen ja kaasun paineeseen perustuvien lämpömittarien (kuva 1) lisäksi yleisessä käytössä on lukuisia muitakin mittarityyppejä. Kaksoismetalliliuska (engl. bimetallic strip) muodostuu kahdesta eri metallista valmistetusta liuskasta, jotka on kiinnitetty toisiinsa (kuva 3). Lämpötilan noustessa kaksoismetalliliuska taipuu, koska toinen metalli laajenee enemmän kuin toinen. Liuska on tavallisesti muotoiltu spiraaliksi, jonka ulompi pää on kiinnitetty lämpömittarin runkoon. Sisempään päähän on kiinnitetty osoitin, joka kääntyy lämpötilan muuttuessa.
5 5 Kuva 3. Vastuslämpömittarissa (engl. resistance thermometer) mitataan ohuen sähkölangan muodostaman käämin, hiilisylinterin tai germaniumkiteen resistanssia. Koska resistanssi voidaan mitata hyvin tarkasti, vastuslämpömittarit ovat yleensä tarkempia kuin useimmat muut lämpömittarityypit. Eräät lämpömittarit eivät tarvitse fyysistä kosketusta tutkittavaan systeemiin. Esimerkiksi korvalämpömittari (engl. ear thermometer) mittaa lämpösähköpariketjulla eli termoparistolla (engl. thermopile) korvan tärykalvon lähettämää infrapunasäteilyä. Se ilmaisee tärykalvon lämpötilan, joka kuvaa hyvin ko. henkilön ruumiinlämpöä. Lämpömittarissa käytettävä mitta-asteikko voidaan valita mielivaltaisesti, ja useita erilaisia asteikkoja onkin käytössä. Celsius-asteikko määritellään sopimalla, että veden jäätymis- ja kiehumispisteen lämpötilat ovat yhden ilmakehän paineessa 0 ja 100 astetta celsiusta ( C) ja jakamalla asteikko näiden pisteiden välillä sataan yhtä suureen osaan (yhden normaali-ilmakehän paine (engl. standard atmospheric pressure) on 1 atm = Pa, missä Pa = pascal = N/m 2 ). Yhdysvalloissa käytössä olevassa Fahrenheit-asteikossa vastaavat jäätymis- ja kiehumispisteen lämpötilat ovat 32 ja 212 astetta fahrenheitia ( F). Näin ollen yhden celsiusasteen suuruinen lämpötilan muutos on (212 32)/100 = 180/100 = 9/5 fahrenheitastetta, joten Celsius-asteikon jonkin lämpötilan mittaluku T C voidaan muuttaa Fahrenheit-asteikon saman lämpötilan mittaluvuksi T F kaavalla Tästä saadaan käänteismuunnos T F = T C. (1.1) T C = 5 9 (T F 32). (1.2)
6 Joskus lämpötilan muutos tai lämpötilaväli T = T 2 T 1 pyritään erottamaan itse lämpötilasta T käyttämällä niille muodollisesti hieman toisistaan poikkeavia yksiköitä: T :lle celsiusastetta (C ) ja T :lle astetta celsiusta ( C), esimerkiksi T = 30 C ja T = 120 C. Tavallisesti molemmille kuitenkin käytetään täsmälleen samaa yksikköä (esimerkiksi C). Kelvin-asteikko saadaan Celsius-asteikosta siirtämällä sen nollakohta veden jäätymispisteestä lämpötilaan 273, 15 C. Näin ollen veden jäätymis- ja kiehumispisteen lämpötilat ovat yhden ilmakehän paineessa 273,15 ja 373,15 kelviniä (K) ja Celsius- ja Kelvin-asteikkojen lämpötilojen mittalukujen T C ja T K välinen muunnoskaava on T K = 273, 15 + T C. (1.3) Lämpötilan ja sen muutoksen yksikkö on siis Kelvin-asteikkoa käytettäessä kelvin, ei astetta kelviniä (kuva 4). Lämpötilan muutos on kelvineissä sama kuin celsiusasteissa. Kelvin-asteikon nollakohta 273, 15 C on lämpötila, jossa vakiotilavuudessa olevan klassisen ideaalikaasun (engl. ideal gas tai perfect gas) paine häviää. Ideaalikaasu muodostuu molekyyleistä, joiden väliset vuorovaikutukset ovat merkityksettömiä. Todellisten kaasujen eli reaalikaasujen (engl. real gas) käyttäytyminen lähestyy klassisen ideaalikaasun käyttäytymistä, kun niiden tiheys pienenee ja lämpötila kasvaa. Tällöin myös kuvan 1(b) mukainen kaasulämpömittari (engl. gas thermometer) lähestyy ideaalista lämpömittaria, jonka antama lämpötila on riippumaton mittauksessa käytetyn materiaalin (kaasun) ominaisuuksista. Muiden lämpömittarien antamat tulokset riippuvat aina jossakin määrin käytettyjen materiaalien spesifisistä ominaisuuksista. Vaikka esimerkiksi kuvan 1(a) mukaisen nestelämpömittarin ja vastuslämpömittarin lukemat olisi kiinnitetty lämpötiloissa 0 C ja 100 C samoiksi, niiden lukemat eivät silti ole muissa lämpötiloissa täsmälleen samat. Todellisella kaasulämpömittarilla ei voida suoraan havaita paineen nollakohtaa, koska kaikki klassiset reaalikaasut nesteytyvät matalissa lämpötiloissa. Hypoteettinen nollakohta voidaan kuitenkin määrittää epäsuorasti mittaamalla kaasun paine P lämpötilan T funktiona ja ekstrapoloimalla saatu kuvaaja P (T ) nollapaineeseen. Jos kaasun tiheys on riittävän pieni ja sen lämpötila on riittävän korkea, kuvaaja osoittautuu aina suoraksi, joka leikkaa paineen nollakohdan lämpötilassa 273, 15 C. Tällöin kaasun paine P on siis suoraan verrannollinen Kelvin-asteikon lämpötilaan T : P = α T. (1.4) Verrannollisuuskerroin α riippuu kaasun määrästä ja kaasusäiliön tilavuudesta, mutta se ei riipu kaasun laadusta (esimerkiksi siitä, onko kaasu vetyä vai hiilidioksidia). Kaikki klassisen ideaalikaasun tavoin käyttäytyvät kaasut noudattavat yhtälöä (1.4). 6 Kuva 4.
7 Yhtälön (1.4) avulla voidaan määritellä ideaalinen, käytetyn kaasun ominaisuuksista riippumaton lämpötila-asteikko, ideaalikaasulämpötila-asteikko. Määritelmä on yksikäsitteinen, jos asteikolta kiinnitetään yksi lämpötila (joka määrää verrannollisuuskertoimen α arvon). Jotta asteikon kalibroinnin tarkkuus ja toistettavuus olisi mahdollisimman hyvä, kiinnityspisteeksi on valittu veden kolmoispiste (engl. triple point) T 3. Se on lämpötila, jossa kiinteä vesi (jää), nestemäinen vesi ja vesihöyry ovat keskenään tasapainossa. Tällainen tila esiintyy vain lämpötilassa 0,01 C, jolloin vesihöyryn paine on 610 Pa. Jotta ideaalikaasulämpötila-asteikon määritelmä olisi eksakti, veden kolmoispisteen lämpötilan arvoksi on määritelty täsmälleen T 3 = 273, 16 K. Jos käytetyssä kaasulämpömittarissa olevan kaasun paineeksi on veden kolmoispisteessä mitattu P 3, kerroin α on tässä mittarissa yhtälön (1.4) mukaan 7 α = P 3 T 3. (1.5) Jos kaasun paineeksi on jossakin toisessa lämpötilassa mitattu samalla mittarilla P, ko. lämpötila on Kelvin-asteikolla yhtälöiden (1.4) ja (1.5) mukaan T = P α = P P 3 T 3 = P P 3 273, 16 K. (1.6) Tämä yhtälö on tarkasti voimassa vain ideaalikaasuille. Reaalikaasujen tapauksessa se voidaan esittää raja-arvona ( ) P T = lim T 3, (1.7) P 3 0 P 3 jossa lämpömittarissa olevan kaasun tiheys lähestyy nollaa. Kelvin-asteikkoa kutsutaan absoluuttiseksi lämpötila-asteikoksi ja tämän asteikon lämpötilaa T kutsutaan absoluuttiseksi lämpötilaksi. Asteikon nollakohtaa (T = 0 K = 273, 15 C) kutsutaan absoluuttiseksi nollapisteeksi (engl. absolute zero). Se on alin mahdollinen lämpötila, ja siinä systeemi saavuttaa alimman mahdollisen energiansa. Jos kvantti-ilmiöitä ei esiintyisi, molekyylien liike lakkaisi tässä lämpötilassa kokonaan. Juuri tästä syystä klassisesti käyttäytyvän ideaalikaasun paine häviää absoluuttisessa nollapisteessä. Celsius-, Fahrenheit- ja Kelvin-asteikkoja vertaillaan toisiinsa kuvassa 5. Kuva 5.
8 1-4 Tilanyhtälöt 8 Edellä on todettu, että termisessä tasapainossa olevassa systeemissä ei ole lämpötilaeroja eikä siinä esiinny lämmön virtausta paikasta toiseen. Tällainen systeemi ei kuitenkaan välttämättä ole kaikilta osin tasapainotilassa. Siinä voi olla esimerkiksi paine-eroja ja tiheysvaihteluita. Jos systeemi jätetään itsekseen, se asettuu lopulta tilaan, jossa kaikki tämän kaltaiset epähomogeenisuudet ovat hävinneet. Tämän jälkeen siinä ei enää tapahdu mitään makroskooppisesti havaittavia muutoksia. Näin saavutettu tila on systeemin todellinen tasapainotila. Tasapainon saavuttamiseen tarvittava aika riippuu systeemissä tapahtuvista prosesseista. Yleensä prosesseja on useita (esimerkiksi paineen tasaantuminen, lämmön johtuminen, diffuusio ym.) ja jokaisella on oma karakteristinen relaksaatioaikansa (engl. relaxation time). Tasapaino saavutetaan, kun on kulunut pitkä aika kaikkiin relaksaatioaikoihin verrattuna. Toisaalta monissa tapauksissa tietyn prosessin relaksaatioaika on niin pitkä, että tämä prosessi voidaan tarkasteluaikana jättää huomiotta. Systeemin kuvaaminen on yksinkertaisinta silloin, kun se on saavuttanut tasapainotilansa. Tällaista tilaa voidaan kuvata täydellisesti muutamalla makroskooppisella muuttujalla, jotka määräävät systeemin kaikki muut makroskooppiset ominaisuudet. Ominaisuuksia, jotka riippuvat ainoastaan systeemin tilasta, sanotaan tilamuuttujiksi (engl. state variable tai function of state). Yksinkertaisena esimerkkinä voidaan tarkastella tasapainotilassa olevaa homogeenista ainetta, esimerkiksi kaasua tai nestettä (engl. fluid). Tällaisen aineen tilavuus (V ) määräytyy tavallisesti yksikäsitteisesti sen paineesta (P ), lämpötilasta (T ) ja ainemäärästä, jota voidaan kuvata esimerkiksi massalla (M). Suureet V, P, T ja M ovat ko. aineen tilamuuttujia, jotka kuvaavat sen makroskooppista tilaa täydellisesti. Yhtä tilamuuttujaa ei voida muuttaa aiheuttamatta muutosta yhdessä tai useammassa muussa tilamuuttujassa. Esimerkiksi lämpötilan muutos aiheuttaa väistämättä paineen muutoksen, jos tilavuus ja ainemäärä pysyvät vakioina. Muuttujien V, P, T ja M välillä on tietty relaatio, jota sanotaan ko. aineen tilanyhtälöksi (engl. equation of state). Jos minkä tahansa kolmen tilamuuttujan arvot tunnetaan, neljännen arvo voidaan laskea tilanyhtälöä käyttäen. Esimerkiksi lämpötila voidaan ratkaista P :n, V :n ja M:n avulla: T = f(p, V, M). (1.8) Tilanyhtälö riippuu tarkasteltavasta aineesta. Se on yleensä hyvin monimutkainen relaatio, joka esitetään graafisesti, numeerisena taulukkona tai potenssisarjana. Joissakin harvoissa tapauksissa tilanyhtälö voidaan kuitenkin esittää yksinkertaisen analyyttisen funktion muodossa. Ideaalikaasun tilanyhtälö Kuva 6 esittää hypoteettistä laitteistoa, jolla voidaan tutkia kaasujen käyttäytymistä. Sylinterissä olevan kaasun tilavuutta voidaan muuttaa mäntää siirtämällä, sen lämpötilaa voidaan muuttaa kuumentamalla, ja kaasun määrää voidaan muuttaa pumppaamalla sylinteriin lisää kaasua. Tutkittavan kaasun tilanyhtälö voidaan määrittää kokeellisesti mittaamalla sen paine, tilavuus, lämpötila ja määrä eri tilanteissa.
9 9 Kuva 6. Tavallisesti kaasun määrää on helpompi kuvata moolien lukumäärällä (n) kuin massalla. Yksi mooli (engl. mole) ainetta sisältää N A tämän aineen molekyyliä, missä N A on Avogadron luku (engl. Avogadro s number). Sen tarkin numeerinen arvo on tällä hetkellä N A = 6, (10) kpl/mol. Jos yhden molekyylin massa on m, yhden moolin massa on M m = N A m, (1.9) jota sanotaan ko. aineen moolimassaksi (engl. molar mass). Mooli määritellään siten, että 12 C-atomeista muodostuvan hiilen moolimassa on täsmälleen M m = 12 g/mol. Tämä merkitsee sitä, että 12 g tällaista hiiltä sisältää täsmälleen yhden moolin ainetta. Jos jotakin ainetta on yhteensä n moolia, tämän ainemäärän kokonaismassa on siis M = nm m. (1.10) Jos kuvan 6 mukaisella laitteistolla tutkittavan kaasun tiheys on riittävän pieni ja sen lämpötila on riittävän korkea, kaasu käyttäytyy klassisen ideaalikaasun tavoin. Tällöin saadaan hyvin yksinkertaisia tuloksia: 1. Jos n ja V ovat vakioita, P on yhtälön (1.4) mukaisesti suoraan verrannollinen absoluuttiseen lämpötilaan T. 2. Jos P ja T ovat vakioita, V on suoraan verrannollinen moolien lukumäärään n. 3. Jos T ja n ovat vakioita, V on kääntäen verrannollinen paineeseen P, ts. tulo P V on vakio. Nämä kolme havaintoa osoittavat, että klassisen ideaalikaasun tilanyhtälö on P V = nrt, (1.11) missä R on tilamuuttujista P, V, T ja n riippumaton kerroin. Itse asiassa mittaukset ovat osoittaneet, että R ei riipu myöskään ideaalikaasun laadusta. Se on universaali vakio, jota
10 sanotaan (yleiseksi) kaasuvakioksi (engl. (universal) gas constant). Sen tämänhetkinen paras arvo on R = 8, (15) J/(mol K). Moolien lukumäärä n voidaan esittää osamääränä n = N/N A, missä N on systeemissä olevien molekyylien lukumäärä. Näin ollen ideaalikaasun tilanyhtälö (1.11) voidaan kirjoittaa myös muodossa P V = NkT, (1.12) missä k = R/N A on Boltzmannin vakio. Se on siis kaasuvakio molekyyliä kohti ja sen arvo on k = 1, (24) J/K. Ideaalikaasun tilanyhtälö (1.11) tai (1.12) voidaan tulkita myös absoluuttisen lämpötilaasteikon määritelmäksi. Jos säiliön tilavuus on V ja se sisältää n moolia ideaalikaasua, jonka paine on P, kaasun absoluuttinen lämpötila on yhtälön (1.11) mukaan 10 T = P V nr. (1.13) Yhtälössä (1.4) esiintyvän verrannollisuuskertoimen α lauseke on siis α = nr/v. Tämä yhtälö määrittelee ideaalikaasulämpötilan. Ideaalikaasun massatiheydelle saadaan yhtälöitä (1.10) ja (1.11) käyttämällä lauseke ρ = M V = nm m V = M mp RT. (1.14) Van der Waalsin tilanyhtälö Hollantilainen fyysikko Johannes D. van der Waals kehitti vuonna 1873 yksinkertaisen tilanyhtälön, joka kuvaa reaalikaasujen käyttäytymistä ideaalikaasun tilanyhtälöä tarkemmin. Van der Waalsin tilanyhtälö on ) (P + an2 V 2 (V bn) = nrt, (1.15) missä a ja b ovat kullekin kaasulle ominaisia empiirisiä vakioita. Vakio b pyrkii ottamaan huomioon kaasumolekyylien äärellisen koon. Se kuvaa sitä tilavuutta, jonka yksi mooli kaasumolekyylejä täyttää. Näin ollen kaikkien molekyylien kokonaistilavuus on bn ja molekyylien liikkumiseen käytettävissä oleva vapaa tilavuus on V bn, joka on sijoitettava ideaalikaasun tilanyhtälöön V :n paikalle. Vakio a pyrkii kuvaamaan molekyylien välisiä vetovoimia. Niiden takia kaasun sisällä vaikuttava paine on suurempi kuin kaasusäiliön seinämiin kohdistuva paine P. Voidaan osoittaa, että vetovoimista johtuva lisäpaine on suoraan verrannollinen molekyylien hiukkastiheyden neliöön. Hiukkastiheydellä tai lukumäärätiheydellä (engl. number density) ϱ tarkoitetaan yleisesti tarkasteltavien objektien ( hiukkasten ) lukumäärää tilavuusyksikköä kohti: ϱ = N V. (1.16) Tässä määrittely-yhtälössä esiintyvä N on tilavuudessa V olevien objektien kokonaislukumäärä. Molekyylien lukumäärä on moolien lukumäärän n avulla esitettynä N = nn A, joten kaasun lisäpaineen lauseke voidaan kirjoittaa verrannollisuuskerrointa a käyttäen
11 muodossa a ϱ 2 = a (nn A /V ) 2 = an 2 /V 2, missä a = a NA 2. Tästä syystä ideaalikaasun tilanyhtälöön on P :n tilalle sijoitettava kaasun sisäisen paineen lauseke P + an 2 /V 2. Kun reaalikaasun tiheys pienenee, sen käyttäytyminen lähestyy ideaalikaasun käyttäytymistä. Van der Waalsin tilanyhtälö (1.15) on sopusoinnussa tämän reunaehdon kanssa, sillä rajalla n/v 0 se redusoituu ideaalikaasun tilanyhtälöksi Lämpömäärä Kun kylmä lusikka pannaan kuumaan kahviin, lusikka kuumenee ja kahvi jäähtyy, kunnes ne ovat saavuttaneet keskinäisen lämpötasapainon (jossa niiden lämpötilat ovat samat). Lämpötilojen tasaantuminen johtuu energian siirtymisestä kahvista lusikkaan (lämpövirrasta). Tällä tavoin siirtyvää energiaa sanotaan lämpömääräksi (engl. heat tai quantity of heat). On syytä kiinnittää huomiota siihen, että lämpömäärällä ei siis kuvata jonkin tietyn systeemin sisältämää energiaa, vaan lämpötilaeron takia systeemistä toiseen siirtyvää energiaa. Näin ollen lämpömäärä ei ole tilamuuttuja, koska se ei ole mikään systeemin ominaisuus ei voida puhua systeemin lämpömäärästä. Brittiläinen fyysikko James Joule osoitti vuonna 1843 ensimmäisenä täsmällisin kokein, että lämpövirta voidaan tulkita energian siirtymiseksi. Hän siirsi lämpöeristettyyn veteen mekaanista energiaa sekoittamalla sitä voimakkaasti siipirattaalla (kuva 7(a)). Tällöin hän havaitsi, että veden lämpötila kohosi. Koska sama lämpötilan kohoaminen voidaan aiheuttaa myös lämpövirralla (kuva 7(b)), voidaan päätellä, että siinäkin on kysymyksessä sama ilmiö, ts. energian siirtyminen veteen. Lämpömäärän yksikkö on sama kuin energian yksikkö, ts. joule (J). Joskus yksikkönä käytetään edelleen kaloria (cal) (engl. calorie), joka on 4,186 J. Ravintoarvoa ilmoitettaessa kalorilla tarkoitetaan itse asiassa monessa tapauksessa kilokaloria (kcal), joka on 1000 kaloria, ts J. Yhden kalorin suuruinen lämpömäärä nostaa lämpötilassa 14,5 C olevan yhden gramman vesimäärän lämpötilaa yhdellä asteella (siis lämpötilaan 15,5 C). Kuva 7.
12 Johonkin systeemiin siirtynyttä lämpömäärää merkitään symbolilla Q. Jos Q on negatiivinen, lämpövirran suunta on tarkasteltavasta systeemistä ulospäin tällöin systeemi menettää lämpövirran takia Q :n suuruisen energian. Hyvin pientä ( äärettömän pientä eli infinitesimaalista) lämpömäärää voidaan merkitä symbolilla d Q. Tällä merkintätavalla korostetaan sitä, että kyseessä ei ole minkään tilamuuttujan muutos (jos käytettäisiin symbolia dq, se voitaisiin virheellisesti tulkita jonkin funktion Q differentiaaliksi). Systeemiin siirtyvä infinitesimaalinen lämpömäärä d Q muuttaa sen lämpötilaa dt :n verran. Näiden suureiden suhdetta C = d Q (1.17) dt sanotaan systeemin lämpökapasiteetiksi (engl. heat capacity). On syytä huomata, että osamäärä (1.17) ei ole funktion Q(T ) derivaatta, sillä tällaista funktiota tai sen differentiaalia dq = Q(T + dt ) Q(T ) ei ole lainkaan olemassa: d Q dq. Sen sijaan lämpötila T on tilamuuttuja ja dt on sen muutos, ts. loppulämpötilan T + dt ja alkulämpötilan T erotus: dt = (T + dt ) T. Lämpökapasiteetti kuvaa systeemin kykyä ottaa vastaan ja varastoida lämpöä. Jos lämpökapasiteetti on suuri, systeemi voi ottaa vastaan paljon lämpöä, sillä tällöin tuotu (positiivinen) lämpömäärä nostaa vain vähän systeemin lämpötilaa. Vastaavasti systeemin luovuttaessa lämpöä (Q < 0) sen lämpötila laskee vain vähän (dt < 0). Lämpökapasiteetin yksikkö on lämpömäärän yksikkö (J) jaettuna lämpötilan yksiköllä (K), ts. J/K. Jos systeemi muodostuu homogeenisesta aineesta (esimerkiksi nesteestä), sen lämpökapasiteetti on suoraan verrannollinen tämän aineen määrään, esimerkiksi sen massaan M tai moolien lukumäärään n. Kun lämpökapasiteetti jaetaan ainemäärällä (esimerkiksi massalla tai moolien lukumäärällä), saadaan ko. ainetta luonnehtiva ominaislämpökapasiteetti (engl. specific heat capacity) eli ominaislämpö (engl. specific heat). Lämpökapasiteetti massayksikköä kohti on c = C M = 1 d Q (1.18) M dt ja lämpökapasiteetti moolia kohti, moolinen lämpökapasiteetti (engl. molar heat capacity) on C m = C n = 1 d Q n dt. (1.19) Jälkimmäinen ominaislämpökapasiteetti saadaan edellisestä kertomalla aineen moolimassalla, joka on yhtälön (1.10) mukaan M m = M/n: C m = C n = M n 12 C M = M mc. (1.20) Näiden ominaislämpökapasiteettien yksiköt ovat J/(kg K) (c) ja J/(mol K) (C m ). Eri aineiden ominaislämpökapasiteetit poikkeavat varsin paljon toisistaan, kuten taulukko 1 osoittaa. Esimerkiksi nestemäisellä vedellä ominaislämpökapasiteetti on hyvin suuri, 15 C:n lämpötilassa kalorin määritelmän mukaan c = 1 cal/(g C) = 4186 J/(kg K), kun taas lyijyllä se on hyvin pieni, c 130 J/(kg K). Lisäksi ominaislämpökapasiteetit riippuvat lämpötilasta: c = c(t ). Usein c(t ):n muutos on kuitenkin kapealla lämpötila-alueella niin pieni, että se voidaan merkittävää virhettä tekemättä jättää huomioon ottamatta. Esimerkiksi nestemäisen veden c(t ) vaihtelee 0 C:n ja 100 C:n välillä vähemmän kuin 1 %, kuten kuva 8 osoittaa.
13 13 Taulukko 1. Kuva 8. Yhtälöiden (1.17) - (1.19) mukaan systeemiin lämpötilavälillä (T, T + dt ) siirtyvä infinitesimaalinen lämpömäärä on d Q = C(T ) dt = M c(t ) dt = n C m (T ) dt. (1.21) Äärellisessä lämpötilan muutoksessa välillä (T 1, T 2 ) systeemiin siirtyvä kokonaislämpömäärä Q on infinitesimaalisten lämpömäärien d Q summa, ts. integraali Q = T2 T 1 C(T ) dt = M T2 T 1 c(t ) dt = n T2 T 1 C m (T ) dt. (1.22) Jos lämpökapasiteetti voidaan approksimoida välillä (T 1, T 2 ) vakioksi, lämpömäärän lausekkeet yksinkertaistuvat muotoon missä on käytetty merkintää T 2 T 1 = T. Q = C T = M c T = n C m T, (1.23)
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2
 I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa?
 Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
energian), systeemi on eristetty (engl. isolated). Tällöin sekä systeemiin siirtynyt
 14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2011 Luku 4 SULJETTUJEN SYSTEEMIEN ENERGIA- ANALYYSI Copyright The McGraw-Hill Companies, Inc. Permission
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Tämän päivän ohjelma: ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 7 / 30.10.2017 v. 03 / T. Paloposki Tämän päivän ohjelma: Entropia Termodynamiikan 2. pääsääntö Palautuvat ja palautumattomat prosessit 1 Entropia Otetaan
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
6. Yhteenvetoa kurssista
 Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Statistinen fysiikka, osa A (FYSA241) Vesa Apaja vesa.apaja@jyu.fi Huone: YN212. Ei kiinteitä vastaanottoaikoja. kl 2016 6. Yhteenvetoa kurssista 1 Keskeisiä käsitteitä I Energia TD1, siirtyminen lämpönä
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 1: Lämpötila ja lämpö Maanantai 30.10. ja tiistai 31.10. A theory is the more impressive the greater the simplicity of its
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 1: Lämpötila ja lämpö Maanantai 30.10. ja tiistai 31.10. A theory is the more impressive the greater the simplicity of its
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics)
 2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
7 Termodynaamiset potentiaalit
 82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
82 7 ermodynaamiset potentiaalit 7-1 Clausiuksen epäyhtälö Kappaleessa 4 tarkasteltiin Clausiuksen entropiaperiaatetta, joka määrää eristetyssä systeemissä (E, ja N vakioita) tapahtuvien prosessien suunnan.
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2
 I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde...2 1.2 Mikroskooppiset ja makroskooppiset teoriat...3 1.3 Terminen tasapaino ja lämpötila...5 1.4 Termodynamiikan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ... 2 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde...2 1.2 Mikroskooppiset ja makroskooppiset teoriat...3 1.3 Terminen tasapaino ja lämpötila...5 1.4 Termodynamiikan
Spontaanissa prosessissa Energian jakautuminen eri vapausasteiden kesken lisääntyy Energia ja materia tulevat epäjärjestyneemmäksi
 KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
Termodynamiikka. Fysiikka III 2007. Ilkka Tittonen & Jukka Tulkki
 Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Luku 13 KAASUSEOKSET
 Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2010 Luku 13 KAASUSEOKSET Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
Thermodynamics: An Engineering Approach, 7 th Edition Yunus A. Cengel, Michael A. Boles McGraw-Hill, 2010 Luku 13 KAASUSEOKSET Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Z 1 = Np i. 2. Sähkömagneettisen kentän värähdysliikkeen energia on samaa muotoa kuin molekyylin värähdysliikkeen energia, p 2
 766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 206 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 2: BE- ja FD-jakaumat, kvanttikaasut Pe 5.4.206 AIHEET. Kvanttimekaanisesta vaihtosymmetriasta
Ilman suhteellinen kosteus saadaan, kun ilmassa olevan vesihöyryn osapaine jaetaan samaa lämpötilaa vastaavalla kylläisen vesihöyryn paineella:
 ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
ILMANKOSTEUS Ilmankosteus tarkoittaa ilmassa höyrynä olevaa vettä. Veden määrä voidaan ilmoittaa höyryn tiheyden avulla. Veden osatiheys tarkoittaa ilmassa olevan vesihöyryn massaa tilavuusyksikköä kohti.
Lämmityksen lämpökerroin: Jäähdytin ja lämmitin ovat itse asiassa sama laite, mutta niiden hyötytuote on eri, jäähdytyksessä QL ja lämmityksessä QH
 Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 1: lämpötila, Boltzmannin jakauma Ke 22.2.2017 1 Richard Feynmanin miete If,
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 1: lämpötila, Boltzmannin jakauma Ke 22.2.2017 1 Richard Feynmanin miete If,
Lämpötila ja lämpö. 2.1 Terminen tasapaino
 2 Lämpötila ja lämpö Lämpötila ja lämpö ovat meille arkipäivästä tuttuja käsitteitä jo oman aistimaailmamme kautta. Me tunnemme "lämmön"ja "kylmän"ja lämpömittareiden lukemat säätelevät päivittäistä toimintaamme:
2 Lämpötila ja lämpö Lämpötila ja lämpö ovat meille arkipäivästä tuttuja käsitteitä jo oman aistimaailmamme kautta. Me tunnemme "lämmön"ja "kylmän"ja lämpömittareiden lukemat säätelevät päivittäistä toimintaamme:
Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste.
 TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
TYÖ 36b. ILMANKOSTEUS Tehtävä Työssä määritetään luokkahuoneen huoneilman vesihöyryn osapaine, osatiheys, huoneessa olevan vesihöyryn massa, absoluuttinen kosteus ja kastepiste. Välineet Taustatietoja
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 1: Lämpötila ja lämpö Maanantai 31.10. ja tiistai 1.11. Yleistä kurssista Luennot maanantaisin 14-16 ja tiistaisin 10-12
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 1: Lämpötila ja lämpö Maanantai 31.10. ja tiistai 1.11. Yleistä kurssista Luennot maanantaisin 14-16 ja tiistaisin 10-12
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 4: entropia Pe 3.3.2017 1 Aiheet tänään 1. Klassisen termodynamiikan entropia
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 10: Reaalikaasut Pe 1.4.2016 1 AIHEET 1. Malleja, joissa pyritään huomioimaan
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 10: Reaalikaasut Pe 1.4.2016 1 AIHEET 1. Malleja, joissa pyritään huomioimaan
Muita lämpökoneita. matalammasta lämpötilasta korkeampaan. Jäähdytyksen tehokerroin: Lämmityksen lämpökerroin:
 Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Vauhti = nopeuden itseisarvo. Nopeuden itseisarvon keskiarvo N:lle hiukkaselle määritellään yhtälöllä
 S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
Käyttämällä annettua kokoonpuristuvuuden määritelmää V V. = κv P P = P 0 = P. (b) Lämpölaajenemisesta johtuva säiliön tilavuuden muutos on
 766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
Ohjeellinen pituus: 2 3 sivua. Vastaa joko tehtävään 2 tai 3
 PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
Lämpötila, lämpö energiana
 Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila, lämpö energiana Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila, lämpö energiana Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Elastisuus: Siirtymä
 Elastisuus: Siirtymä x Elastisuus: Siirtymä ja jännitys x σ(x) σ(x) u(x) ℓ0 u(x) x ℓ0 x Elastisuus: Lämpövenymä ja -jännitys Jos päät kiinnitetty eli ε = 0 Jos pää vapaa eli σ = 0 Elastisuus: Venymätyypit
Elastisuus: Siirtymä x Elastisuus: Siirtymä ja jännitys x σ(x) σ(x) u(x) ℓ0 u(x) x ℓ0 x Elastisuus: Lämpövenymä ja -jännitys Jos päät kiinnitetty eli ε = 0 Jos pää vapaa eli σ = 0 Elastisuus: Venymätyypit
Maxwell-Boltzmannin jakauma
 Maxwell-Boltzmannin jakauma Homogeenisessa tasapainotilassa redusoidut yksihiukkastodennäköisyydet f voivat olla vain nopeuden funktioita, f = f(v ), ja H-funktio ei toisaalta voi riippua ajasta, eli dh
Maxwell-Boltzmannin jakauma Homogeenisessa tasapainotilassa redusoidut yksihiukkastodennäköisyydet f voivat olla vain nopeuden funktioita, f = f(v ), ja H-funktio ei toisaalta voi riippua ajasta, eli dh
Entalpia - kuvaa aineen lämpösisältöä - tarvitaan lämpötasetarkasteluissa (usein tärkeämpi kuin sisäenergia)
 Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Luento 4: Entroia orstai 12.11. klo 14-16 47741A - ermodynaamiset tasaainot (Syksy 215) htt://www.oulu.fi/yomet/47741a/ ermodynaamisten tilansuureiden käytöstä Lämökaasiteetti/ominaislämö - kuvaa aineiden
Aineopintojen laboratoriotyöt 1. Veden ominaislämpökapasiteetti
 Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Lämpötila ja lämpöenergia
 Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila ja lämpöenergia Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
Matematiikan, fysiikan ja kemian opettajan kandiohjelma Didaktisen fysiikan kokeellisuus I Lämpötila ja lämpöenergia Tilanmuuttujien perushahmotus Lämpötila, paine, tasapaino Lämpötilalla tarkoitetaan
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Integroimalla ja käyttämällä lopuksi tilanyhtälöä saadaan T ( ) ( ) H 5,0 10 J + 2,0 10 0,50 1,0 10 0,80 Pa m 70 kj
 S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Wien R-J /home/heikki/cele2008_2010/musta_kappale_approksimaatio Wed Mar 13 15:33:
 1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
1.2 T=12000 K 10 2 T=12000 K 1.0 Wien R-J 10 0 Wien R-J B λ (10 15 W/m 3 /sterad) 0.8 0.6 0.4 B λ (10 15 W/m 3 /sterad) 10-2 10-4 10-6 10-8 0.2 10-10 0.0 0 200 400 600 800 1000 nm 10-12 10 0 10 1 10 2
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
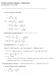 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
Oikeat vastaukset: Tehtävän tarkkuus on kolme numeroa. Sulamiseen tarvittavat lämmöt sekä teräksen suurin mahdollinen luovutettu lämpö:
 A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
A1 Seppä karkaisee teräsesineen upottamalla sen lämpöeristettyyn astiaan, jossa on 118 g jäätä ja 352 g vettä termisessä tasapainossa Teräsesineen massa on 312 g ja sen lämpötila ennen upotusta on 808
V T p pv T pv T. V p V p p V p p. V p p V p
 S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
PHYS-A0120 Termodynamiikka. Emppu Salonen
 PHYS-A0120 Termodynamiikka Emppu Salonen 27. lokakuuta 2017 Termodynamiikka, syksy 2017 1 Thermodynamics is easy I ve learned it many times. Harvey S. Leff 1 Johdanto Tässä luvussa teemme yleiskatsauksen
PHYS-A0120 Termodynamiikka Emppu Salonen 27. lokakuuta 2017 Termodynamiikka, syksy 2017 1 Thermodynamics is easy I ve learned it many times. Harvey S. Leff 1 Johdanto Tässä luvussa teemme yleiskatsauksen
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
Vastaa kaikkiin kysymyksiin. Oheisista kaavoista ja lukuarvoista saattaa olla apua laskutehtäviin vastatessa.
 Valintakoe 2016/FYSIIKKA Vastaa kaikkiin kysymyksiin. Oheisista kaavoista ja lukuarvoista saattaa olla apua laskutehtäviin vastatessa. Boltzmannin vakio 1.3805 x 10-23 J/K Yleinen kaasuvakio 8.315 JK/mol
Valintakoe 2016/FYSIIKKA Vastaa kaikkiin kysymyksiin. Oheisista kaavoista ja lukuarvoista saattaa olla apua laskutehtäviin vastatessa. Boltzmannin vakio 1.3805 x 10-23 J/K Yleinen kaasuvakio 8.315 JK/mol
Lämpöopin pääsäännöt
 Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Differentiaali- ja integraalilaskenta
 Differentiaali- ja integraalilaskenta Opiskelijan nimi: DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona
Differentiaali- ja integraalilaskenta Opiskelijan nimi: DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona
Valomylly. (tunnetaan myös Crookesin radiometrinä) Pieni välipala nykyisin lähinnä leluksi jääneen laitteen historiasta.
 Valomylly (tunnetaan myös Crookesin radiometrinä) Mikko Marsch Pieni välipala nykyisin lähinnä leluksi jääneen laitteen historiasta Valomylly (tunnetaan myös Crookesin radiometrinä) Pieni välipala nykyisin
Valomylly (tunnetaan myös Crookesin radiometrinä) Mikko Marsch Pieni välipala nykyisin lähinnä leluksi jääneen laitteen historiasta Valomylly (tunnetaan myös Crookesin radiometrinä) Pieni välipala nykyisin
VII LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ
 II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
3 Raja-arvo ja jatkuvuus
 3 Raja-arvo ja jatkuvuus 3. Raja-arvon käsite Raja-arvo kuvaa funktion kättätmistä jonkin lähtöarvon läheisdessä. Raja-arvoa tarvitaan toisinaan siksi, että funktion arvoa ei voida laskea kseisellä lähtöarvolla
3 Raja-arvo ja jatkuvuus 3. Raja-arvon käsite Raja-arvo kuvaa funktion kättätmistä jonkin lähtöarvon läheisdessä. Raja-arvoa tarvitaan toisinaan siksi, että funktion arvoa ei voida laskea kseisellä lähtöarvolla
Ekvipartitioteoreema. Entropia MB-jakaumassa. Entropia tilastollisessa mekaniikassa
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ
 I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
Fysiikan maailmankuva 2015 Luento 8. Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa?
 Fysiikan maailmankuva 2015 Luento 8 Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa? Ajan nuoli Aika on mukana fysiikassa niinkuin jokapäiväisessä
Fysiikan maailmankuva 2015 Luento 8 Aika ja ajan nuoli lisää pohdiskelua Termodynamiikka Miten aika ja termodynamiikka liittyvät toisiinsa? Ajan nuoli Aika on mukana fysiikassa niinkuin jokapäiväisessä
Mekaniikan jatkokurssi Fys102
 Mekaniikan jatkokurssi Fys10 Kevät 010 Jukka Maalampi LUENTO 8 Vaimennettu värähtely Elävässä elämässä heilureiden ja muiden värähtelijöiden liike sammuu ennemmin tai myöhemmin. Vastusvoimien takia värähtelijän
Mekaniikan jatkokurssi Fys10 Kevät 010 Jukka Maalampi LUENTO 8 Vaimennettu värähtely Elävässä elämässä heilureiden ja muiden värähtelijöiden liike sammuu ennemmin tai myöhemmin. Vastusvoimien takia värähtelijän
Mikrotila Makrotila Statistinen paino Ω(n) 3 Ω(3) = 4 2 Ω(2) = 6 4 Ω(4) = 1
 76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
FY9 Fysiikan kokonaiskuva
 FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
H 2 O. Kuva 1. Kalorimetri. missä on kalorimetriin tuotu lämpömäärä. Lämpökapasiteetti taas määräytyy yhtälöstä
 KALORIMETRI 1 TEORIAA Kalorimetri on laite, jolla voidaan mitata lämpömääriä. Mittaus voidaan suorittaa tarkastelemalla lämpömuutoksia, faasimuutoksia, kemiallisia reaktioita jne. Kun mittaus perustuu
KALORIMETRI 1 TEORIAA Kalorimetri on laite, jolla voidaan mitata lämpömääriä. Mittaus voidaan suorittaa tarkastelemalla lämpömuutoksia, faasimuutoksia, kemiallisia reaktioita jne. Kun mittaus perustuu
