Neuroimmuniteetti aivojen immuunijärjestelmä
|
|
|
- Marja-Leena Leppänen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 Neuroimmuniteetti aivojen immuunijärjestelmä Lauri Wilhelm Hella LuK-tutkielma Oulun yliopisto Genetiikka ja fysiologia Laajuus: 10 op Avainsanat: neuroimmunologia, neuroimmunology, neuroimmunity, kantasolut, regeneratiivinen lääketiede.
2 Sisällysluettelo 1. Johdatus neuroimmuniteettiin Keskushermoston neuroimmuniteetin anatomia ja fysiologia Anatomia Aivokalvot, veri-aivoesteet ja plexus choiroideus ja aivojen imusuonisto Synnynnäinen neuroimmuniteetti Mikrogliat ja makrofagit Astrosyytit Komplementtijärjestelmä Adaptiivinen neuroimmuniteetti Lymfosyytit, autoreaktiiviset T-solut ja suojaavan autoimmuniteetin teoria Keskushermoston patofysiologia ja neuroimmuniteetti Keskushermoston häiriöt, vauriot, neurodegeneraatio ja vanheneminen Autoimmuunisairaudet, syöpä ja mikrobi-infektiot Tulevaisuuden näkymiä Nanopartikkelit lääkevektoreina Neurokantasolut, niiden ohjelmointi ja kantasoluterapiat Yhteenveto Viitteet
3 1. Johdatus neuroimmuniteettiin Tutkielmani käsittelee kirjallisuuskatsauksen muodossa nisäkkäiden immuunijärjestelmän roolia aivojen ja keskushermoston ylläpitäjänä. Tarkastelen aihetta viimeisten 15 vuoden aikana tehtyjen tutkimusten pohjalta sekä pohdin tutkimuksen tulevaisuuden suuntaa. Aivot ja keskushermosto ovat aiemmin esitetty immuunivapaina alueina, mutta viime vuosien läpimurrot ovat vähitellen aiheuttaneet paradigman muutoksen. Jäsennän nykykäsitystä aiheesta ja esittelen tutkimusten uusia fysiologisia löydöksiä. Näiden perusteella hahmottelen immuunijärjestelmän keskeistä roolia aivojen ja keskushermoston kehityksessä, toiminnassa, tasapainon ylläpidossa sekä patofysiologiassa. Tarkoituksena ei ole käydä kaikkia immuunijärjestelmän soluja tai mekanismeja läpi, vaan käsitellä niitä joille on löydetty rooli keskushermostossa. Käsittelen ensin yleisesti immuunijärjestelmän mekanismeja, soluja ja näiden erittämiä molekyylejä. Tämän jälkeen käyn läpi keskushermoston anatomiaa ja soluja. Tarkastelen vielä immuunijärjestelmän häiriöitä ja epästabiloitumisesta seuraavia kudosvaurioita, patogeenien infektioita sekä lukuisia neurodegeratiivisia sairauksia. Patologioiden lisäksi käsittelen vanhenemisen tuomia immuunijärjestelmän muutoksia, sekä toisaalta toimivan immuunijärjestelmän roolia hermoston kehityksen, oppimisen ja neurogeneesin kannalta. Lopuksi pohdin neuroimmuniteetin tutkimuksen tulevaisuuden suuntia, nanopartikkeleita lääkevektoreina, keskushermoston kantasolujen ja regeneratiivisen lääketieteen tuomia terapeuttisia mahdollisuuksia. Kehon immuunijärjestelmän tärkeimpiä tehtäviä ovat kehon omien ja vieraiden solujen tunnistaminen (self/non-self recognition). Järjestelmän pitää tunnistaa paitsi kehoon tunkeutuvat patogeenit, sen on tunnistettava myös kehon omat vaurioituneet solut ja yleiset häiriötilat. Toiminnallisuudeltaan immuunijärjestelmä voidaan jakaa kahteen pääosaan. Synnynnäinen immuniteetti periytyy sukusoluissa. Se reagoi nopeasti patogeeneihin ja patogeeni- ja kudosvauriotoistokuvioihin (pathogen-associated molecular pattern PAMP, damage-associated molecular pattern DAMP), mutta reaktio on epäspesifistä eikä kehity myöhemmän yksilönkehityksen mukana. Adaptiivinen immuniteetti taas muodostuu elämän aikana vasteena erilaisiin patologisiin haasteisiin. Se on evolutiiviselta alkuperältään synnynnäistä immuniteettia myöhempi. Immuunivasteesta myös 2
4 jää muistijälki järjestelmään, jolloin järjestelmä aktivoituu nopeammin ja voimakkaammin kohdatessaan saman patogeenin seuraavan kerran. Adaptiivinen immuniteetti aktivoituu hitaammin, mutta pystyy kohdistamaan immunologisen vasteen hyvin spesifisesti kohteeseensa. Immuunijärjestelmä voidaan jakaa edelleen soluvälitteiseen ja humoraaliseen osaan. Soluvälitteisessä immuniteetissa valkosolut toimivat järjestelmän efektoreina ja säätelijöinä. Humoraalisessa immuniteetissa veressä ja kudosnesteissä kiertävät vasta-aineet, sytokiinit, kemokiinit ja komplementtiproteiinit tunnistavat ja sitoutuvat antigeeniensä epitooppeihin. Efektorisolujen erittämät sytokiinit, interferonit, interleukiinit ja kemokiinit koordinoivat ja säätelevät paitsi tulehdusreaktiota ja immuunisolujen toimintaa, mutta vaikuttavat myös suoraan hermosolujen toimintaan (Vezzani ym. 2015). Humoraalinen immuniteetti lisäksi yhdessä soluvälitteisen immuniteetin kanssa ja tukee muiden immuunisolujen toimintaa. Immuunijärjestelmä voidaan myös jakaa toiminta-alueeltaan perifeeriseen immuunijärjestelmään ja keskushermoston immuunijärjestelmään (Murphy ym. 2012). Ne eroavat merkittävästi toisistaan, mutta ovat kummatkin kehoa ja kudoksia suojelevia systeemeitä. Neuroimmuniteettijärjestelmässä normaalit perifeerisen immuunijärjestelmän mekanismit ovat usein rajattuja tai jopa käänteisiä. Tämä johtuu keskushermoston pitkälti post-mitoottisesta tilasta, heikosta uusiutumiskyvystä sekä neuroimmuniteetin ensisijaisesti keskushermostoa suojelevasta luonteesta. Kehon immuunijärjestelmä aktivoituu paitsi vasteena kehon ulkoisten patogeenien muodostamaan uhkaan, myös haavan tai vamman seurauksena syntyvien kudosvaurioiden yhteydessä. Immuunisolujen aktivaatiosta seuraa inflammaatio l. tulehdusreaktio, johon kuuluu kuumotusta (calor), turvotusta (tumor), kipua (dolor) ja punoitusta (rubor), sekä kudosvaurioita (functio laesa) luvun alussa biologi Elie Metshnikoff määritteli fysiologisen inflammaation kehon pyrkimyksenä palauttaa tasapainotila häiriön jälkeen, torjua patogeenit, korjata kudosvauriot ja ylläpitää homeostasiaa (Tauber 2003). Korjaava fysiologinen inflammaatio muuttuu krooniseksi, patologiseksi inflammaatioksi, jos sitä ei enää saada säädeltyä tai sammutettua. Keskushermoston immuunijärjestelmää on tutkittu jo yli sata vuotta luvun alussa neurotieteen perustajaksi luonnehdittu Santiago Ramon y Cajal visualisoi hermoston anatomiaa. Hän päätteli, ettei neuroneita enää synny aikuisiällä. Aivoissa ei myöskään havaittu muualla kehossa normaalia elinsiirrännäisten hylkimisreaktiota, eikä aivojen immuniteetti reagoinut sinne siirrettyihin syöpäkasvaimiin. Myöhemmin on selvinnyt, että keskushermostossa tapahtuu neurogeneesiä vielä 3
5 aikuisiällä, mutta se on pienimuotoista, eikä aivovaurioita yleisesti korjaavaa. Normaalissa fysiologisessakin tulehdusreaktiossa kohdekudokseen syntyy aina vaurioita, jotka korjataan tulehdusreaktion loputtua. Tulehdusreaktion katsottiin pitkään olevan luonteeltaan puhtaasti patologista. Aivojen inflammaation katsottiin olevan erittäin vaarallista, koska neuroneita ei enää aikuisiällä uskottu syntyvän. Aivoissa tulehdusreaktion pääteltiin johtavan aina aivovaurioon. Näiden havaintojen pohjalta aivot julistettiin immuunivapaaksi alueeksi, immuunijärjestelmän ulkopuoliseksi veri-aivoesteiden rajaamaksi saarekkeeksi. Viimeisen 30 vuoden aikana on alkanut näyttää yhä selvemmältä, ettei dogma aivoista immuunivapaana alueena pidä paikkaansa (Carson ym. 2006). Michal Schwartz tutkimusryhmineen on viimeisten 15 vuoden aikana perustavanlaatuisilla tutkimuksillaan muodostanut uuden kokonaiskäsityksen aivojen immunologiasta (Schwartz 2015). Kirjassaan Neuroimmunity: A New Science Schwartz käsittelee immuunijärjestelmän roolia aivojen toiminnan säätelijänä ja toisaalta aivojen terveyden kannalta välttämättömän immuunijärjestelmän rajoitettua pääsyä aivokudokseen evolutiivisena vaihtokauppana. Aivojen homeostasian ylläpitämiseksi ja sen tulehduksille erityisen herkän mikroympäristön takia immuunijärjestelmä on keskushermostossa joutunut luopumaan ja rajoittamaan muualla kehossa tärkeitä patogeenien torjumiseen tähtääviä toimintojaan. Immuunisoluilla näyttää olevan aivoissa selkeästi määrätty ja rajattu rooli. Tämän vuoksi aivojen signaloitua paikallisille immuunisoluille, ne eivät pääsääntöisesti suuntaa suoraan aivokudokseen vaan erittävät erilaisia välittäjäaineita ja sytokiineja gliasoluille vaurion korjaamiseksi. Keskushermostossa tulehdusreaktio on erityisen tiukasti säädeltyä ja immuunisolujen toiminta poikkeaa muusta kehosta. Viimeisen 15 vuoden aikana muodostunut kokonaan uusi neuroimmuniteettia tutkiva tutkimussuunta. Se tutkii aivojen monimutkaista vuoropuhelua kehon immuunijärjestelmän kanssa sekä järjestelmän kriittistä roolia aivojen hyvinvoinnin ylläpitämisessä. Se pyrkii selvittämään aivoissa tapahtuvia immuunireaktioita, niiden vuorovaikutuksia muun kehon kanssa, sen mahdollista osuutta hermostosairauksien synnyssä sekä terapeuttista potentiaalia näiden kansanterveydellisesti merkittävien sairauksien hoidossa. Myös muiden aiemmin immuunivapaina pidettyjen alueiden kuten kivesten ja eturauhasen on huomattu olevan aivojen lailla aktiivisia immuunialueita. Samoin kuin aivoissa, myös näissä immuunijärjestelmä toimii periferaalisesta poikkeavalla tavalla ja on erittäin tiukasti säädeltyä. 4
6 2. Keskushermoston neuroimmuniteetin anatomia ja fysiologia 2.1 Anatomia Keskushermosto koostuu aivoista ja spinaalikanavassa kulkevasta selkäytimestä. Näiden lisäksi silmien voidaan katsoa muodostavan aivojen kanssa anatomisesti yhtenevän kokonaisuuden. Kallon ja selkärangan luusto ympäröi ja suojelee keskushermoston muutoin varsin hauraita rakenteita. Lisäksi keskushermostoa ympäröivät erilaiset kalvostot ja näiden lisäksi aivoille lisäsuojaa antaa aivo-selkäydinneste eli likvori, jossa aivot kelluvat. Aivot koostuvat kalvojen ympäröivästä iso-ja pikku- aivoista sekä syvistä aivolisäkkeistä. Isot aivot jakaantuvat kahteen hemisfääriin, joita yhdistää corpus callosum l. aivokurkiainen sekä pienemmät aksonikimpuista koostuvat komissuurat. Isoaivojen uloin pintakerros cortex l. aivokuori koostuu noin 2-7 mm paksusta, voimakkaasti poimuuntuneesta harmaasta aineesta. Aivokuoren alapuolella sijaitsee subkortikaalinen kerros l. valkea aine. Tämä koostuu hermosolujen l. neuronien aksonikimpuista. Harmaassa aineessa sijaitsevat hermosolujen solukeskukset l. soomat. Yhdessä harmaa ja valkea-aine muodostavat aivojen hermokudoksen l. parenkyymin (Soinila ym. 2006). Keskushermoston hermokudoksen muodostavat parenkyymin neuronit sekä näitä fasilitoivat glia-tukisolut. Varsinaisten neuronien kolme päätyyppiä ovat ympäristöä aistivat sensoriset tuovat l. afferentit neuronit, keskushermoston parenkyymin interneuronit sekä keskushermoston vievät l. efferentit motoneuronit. Motoneuronit hermottavat paitsi kehon liikeitä ohjaavia lihaksia, myös sisäelimiä. Eri tyypin neuronit muodostavat yhdessä glia-solujen kanssa hermoverkkoja. Aivoissa tuki- l. gliasoluja on noin kolme kertaa enemmän kuin neuroneita. Gliasolut voidaan jakaa neljään morfologialtaan ja fysiologialtaan eroavaan tyyppiin. Oligodendrosyytit muodostavat aksoneita ympäröivän moninkertaisista solukalvoista koostuvan myeliinitupen, joka nopeuttaa aktiopotentiaalin johtumista aksonissa toimien samalla eristeenä. Myeliinituppien pituus ja paksuus vaihtelee eri osissa keskushermostoa. Osalla neuroneista tuppi saattaa olla jopa 200 solukalvoa paksu. Osalla neuroneista ei ole aksonin ympärillä lainkaan myeliinituppea. Myeliinitupen ansiosta signaali välittyy aksonissa kaikki-tai-ei-mitään aktiopotentiaalina. Mikäli tuppea ei ole signaali kulkee neuronissa elektrotonisesti gradeerattuna heikentyvänä signaalina. Yksi oligodendrosyytti voi eristää jopa 50 interneuronin aksonia. Ependyymisolut muodostavat neuroepiteelikerroksen aivokammioiden pinnalle. Neurokantasolujen mikroympäristö sijaitsee ependyymisolukossa. Astrosyytit ovat morfologialtaan tähtimäisiä aivojen kemiallisesta tasapainosta huolehtivia 5
7 gliasoluja. Kuten myöhemmin käy ilmi, näillä on parenkyymissä myös muita tärkeitä toimintoja. Perivaskulaarisilla ulokkeillaan ne muodostavat veri-aivoesteen keskushermoston hiussuoniston endoteelisolujen kanssa. Ne siirtävät hermosoluille ravinteita sekä poistavat parenkyymistä toksiineja ja metabolista jätettä. Mikrogliat taas ovat pääasiassa keskushermoston kudosmakrofageja, jotka poistavat solujätettä, mutta osallistuvat myös aivojen kehitykseen sekä tulehdusreaktion syntyyn erittämällä signaalimolekyylejä, pääasiassa sytokiineja Aivokalvot, veri-aivoesteet ja plexus choiroideus ja aivojen imusuonisto Aivokalvot ympäröivät aivoja ja selkäydintä. Kalvostot koostuvat kolmesta eri kalvosta sekä näiden väliin jäävistä välitiloista. Näistä uloimpana on kovakalvo l. dura mater, joka rakentuu kahdesta sidekudoslehdestä. Ulompi kalvoista on kiinnittynyt kalotin luihin, sisempi peittää aivot ja työntyy hemisfäärien väliin muodostaen väliseinän aivosirpin l. falx cerebrin. Kovakalvon alla sijaitseva lukinkalvo l. araknoidea koostuu myös kahdesta epiteelikalvosta. Ulompi kalvo myötäilee kovakalvoa, mutta on irti siitä ja näiden väliin muodostuu subduraalitila. Sisempi seittimäinen sidekudoskalvosto kiinnittyy pia materiin. Pia mater on sisin aivojen parenkyymiä ympäröivistä kalvostoista. Lukinkalvon ja pia materin väliin jää aivo-selkäydinnesteen täyttämä subaraknoidiaalitila. Lukinkalvoa ja pia mater muodostavat yhdessä leptomeningeksen. Selkäytimen kalvosto eroaa aivoista siten, että sitä ympäröi luukalvo. Se ei ole sulautunut kovakalvoon vaan näiden väliin jää rasvan täyttämä epiduraalitila (Soinila ym. 2006). Veri-aivoesteet ympäröivät aivoja ja muodostavat fyysisen esteen kehon ja aivojen välille. Se on evolutiiviselta alkuperältään jo selkärangattomille kehittynyt este ja rajapinta, joka varmistaa neuronien optimaalisen toiminnan tiukasti säädellyn kemia- ja ioni-mikroympäristön avulla. Veriaivoesteitä ovat varsinainen veri-aivoeste (BBB, blood brain barrier) sekä plexus chorioideuksessa sijaitseva veri-likvorieste (BCSFB, epithelial blood-cerebrospinal fluid barrier). Lisäksi aivokalvojen välitilan ja aivojen parenkyymin välillä on oma esteensä aivo-aivokalvoeste (BMB, brain meninges barrier). Aivoissa kiertävän verisuoniston seinämä koostuu fenestroimattomista endoteelisoluista, jotka vähentävät seinämän läpäisevyyttä. Tästä poikkeuksena ovat plexus choroideuksen verisuonten endoteelisolut, jotka ovat fenestroituja. Varsinainen veri-aivoeste eristää aivoissa kiertävän hiussuoniston aivojen parenkyymistä. Se koostuu fenestroimattomista verisuonten seinämien 6
8 epiteelisoluista, näitä ympäröivästä tyvikalvosta, perisyyteistä sekä astrosyyttien perivaskulaarisista ulokkeista ja mikroglioista. Neljästä solukalvosta koostuva este on selkeästi polaarinen ja eri puolilla estettä vallitsee erilainen kalvopotentiaali ja ph. Muuhun kehoon verrattuna aivot ovat lievästi hapan ympäristö. Happi, ionit ja tietyt pienet rasvaliukoiset molekyylit voivat ylittää neljästä solukalvosta koostuvan varsinaisen veri-aivoesteen passiivisesti (Ransohoff ym. 2012). Sen sijaan se ei suoraan päästä suuria molekyylejä kuten hormoneja, metaboliitteja tai soluja ulos eikä sisään aivojen sisäosiin. Estettä luonnehtii sen rajoitettu pinosytoosi-ja trans-sytoosipotentiaali ja erilaiset spesifiset kuljettejaproteiinit, kuten glukoosia kuljettava GLUT1. Seerumista aivoihin otettavan glukoosin lisäksi, aminohapoille, vitamiineille, sytokiineille, oligonukleotidi-analogeille ja nukleosideille löytyy jokaiselle oma kuljettajansa kalvon yli. Samoin aivoista seerumiin vieviä effluksikuljettajia löytyy lähes joka aineelle. Kuljettajaproteiinit voivat nopeuttaa glukoosin ja aminohappojen liikettä veri-aivoesteen yli jopa kertaisesti verrattuna ilman kuljetusta tapahtuvaan siirtymiseen (Carson 2006). Toisaalta aivoista poistettaville metaboliiteille, toksiineille ja β-amyloidille on myös omat, tehokkaat kuljettajaproteiininsa. Jopa vasta-aine immuunoglobuliini G (IgG) on oma erilaistunut kuljettajaproteiini keskushermostoon (Banks 2016). Aivoissa on neljä aivokammiota, jotka ovat yhteydessä toisiinsa. Parilliset lateraalikammiot ovat yhteydessä talamuksen välissä olevaan kolmanteen kammioon. Siitä on aivonesteviemärin kautta yhteys pikkuaivojen l. cerebellumin tyvessä sijaitsevaan neljänteen aivokammioon. Jokaisen aivokammion alaosassa, epiteelisoluista muodostuvan ependyymin alla on valtimosta ja verisuonista koostuva pitkulainen sykkyrä, plexus choiroideus. Se on aivokammioiden pohjalla sijaitseva tiheästi verisuonitettu elin, jonka pääasiallinen tehtävä on suodattaa seerumia ja tuottaa aivojen likvori (Soinila ym. 2006). Plexus choiroideus on myös aktiivinen lymfaattinen elin, jossa tapahtuu T-solujen MHC-I ja MHC-II-tunnistuksen indusoimaa aktivaatiota (Schwartz 2015). Plexus choiroideuksesta lymfosyytit pääsevät adheesioreseptorien avulla siirtymään verilikvoriesteen yli subaraknoidiaalitilaan. Veri-likvorieste sijaitsee plexus choiroideusten yhteydessä. Este muodostuu tihein liitoksin suljetuista ja tiheästi pakkautuneista epiteelisoluista. Se erottaa likvorin täyttämät aivokammiot verisuonien seinämien fenestroiduista endoteelisoluista. Aivokammioiden seinämiä peittävää epiteelisolukkoa kutsutaan ependyymiksi. Imujärjestelmä eli lymfaattinen järjestelmä poistaa kehosta kuona-aineita ja kudosnestettä. Aivojen lymfaattinen järjestelmä ja imukanavat löydettiin leptomeningeaalisesta tilasta vuonna Kari Alitalo ja Anders Aspelund (Aspelund ym. 2015) sekä Adrian Louveau (Louveau ym. 2015) 7
9 ryhmineen löysivät tahoillaan toisistaan riippumatta kiistattomia todisteita aivojen lymfaattisesta järjestelmästä. Sitä on sittemmin alettu kutsua glia-soluja mukaillen glymfaattiseksi järjestelmäksi. Plexus chorioideuksessa seerumista pulssimaisesti suodattuva, ja siitä muodostettu aivoselkäydinneste l. likvori eritetään aivokammiohin. Sieltä se pääsee kiertämään neljännen aivokammion kolmen aukon kautta subaraknoidiaalitilaan. Likvorin suodatuksen ja kierron pumppuvoimana toimii aivoverenkierron pulssi. Nesteen liikettä edistää myös neuroepiteeli mikrovilluksilla ja värekarvoillaan. Likvoria tuotetaan aivokammioihin noin 500 ml vuorokaudessa. Neste huuhtelee parenkyymiä ja suodattuu lopulta glymfaattisiin kanaviin. Parenkyymiin likvori pääsee astrosyyttien akvaporiini 4 kautta. Lopulta kanavat laskevat syvällä kaulassa sijaitseviin imusolmukkeiden (DCLN, deep vertical lymph nodes) kautta eteenpäin solislaskimon kautta sydämeen. Imusolmukkeissa neste kulkeutuu naiivien T-solujen ohi ja altistuu immuunivalvonnalle. On mahdollista, että inflammaation aikana imusuonistoa saattaa kasvaa suoraan parenkyymin sisään. Tällöin imusuoniston kasvu ja tehostunut imu voisi vähentää inflammaatiosta johtuvaa turvotusta (Kipnis 2016). Veri-aivoesteet ovat enemmän kuin pelkkiä passiivisia esteitä. Ne ovat myös dynaamisia cross-talkrajapintoja aivojen ja kehon välillä. Niitä voidaan pitää eräänlaisena erilaisten signaalien tulkkina ja suodattimena. Erityisesti plexus choroideuksen rajapinnalla on jatkuvaa signalointia aivojen ja immuunijärjestelmän välillä (Schwerk ym. 2015). Toisaalta signalointia tapahtuu myös suoraan motoneuronien kautta hermotettuihin sisäelimiin ja niissä oleviin immuunisoluihin. Muualta kehosta tulevia signaaleja tulkitaan näillä rajapinnoilla sekä välitetään tarvittaessa eteenpäin aivoihin. Myös aivoista tulevia signaaleja tulkitaan rajapinnoilla ja välitetään moduloituina eteenpäin muualle kehoon. Vereen voidaan erittää erilaisia signaalimolekyylejä, joiden avulla kommunikaatiota tapahtuu keskushermoston ja muun kehon välillä sekä suoraan periferaaliseen immuunijärjestelmään. Tarvittaessa veri-aivoesteiden läpi rekrytoidaan immuunisoluja. Niitä muokataan vielä ennen kuin ne päästetään aivokammioihin. Osa lymfosyyteistä eliminoidaan saman tien aktivoimalla näiden apoptoosin indusoiva Fas-ligandi. Veri-aivoesteiden solujen, muun keskushermoston ja kokonaisimmuunijärjestelmän välistä kommunikaatiota kuvaamaan on esitetty neurovaskulaarisen yksikön käsitettä (Neurovascular unit NVU). NVU-BBB ristikkäistä kommunikointia tutkitaan intensiivisesti. Se myös muuttuu patologioiden yhteydessä (Banks 2016). 8
10 2.2. Synnynnäinen neuroimmuniteetti Mikrogliat ja makrofagit Mikrogliat ovat keskushermoston myeloidista solulinjaa olevia, fagosyyttisesti aktiivisia tukisoluja ja kudosmakrofageja. Muista kehon kudosmakrofageista poiketen mikrogliat syntyvät primitiivisessä hematopoieesissa jo ruskuaispussissa. Sieltä ne lähtevät vaeltamaan kehittyvään hermostoputkeen. Nämä hematopoieettisista kantasoluista kehittyvät mikrogliojen kaltaiset solut vaeltavat hiirellä alkion ruskuaispussista E 7,5 (embryonic day) aikana. Ne syntyvät huomattavan aikaisin verrattuna vasta E 10,5 vaiheessa ilmaantuviin myeloidisen solulinjan kantasoluihin, joista muut kehon makrofagit aikanaan erilaistuvat. Ihmisellä mikrogliojen kaltaiset solut alkavat vaeltaa ruskuaispussista 3. raskausviikolla ja kolonisoivat selkäytimen 9. viikolla. Mikrogliat levittäytyvät ympäröivään keskushermostoon viikkojen aikana. Vasta viikolla 35 voidaan aivoissa havaita erilaistuneita mikrogliapopulaatioita (Prinz & Priller ym. 2014). Mikroglioilla on tärkeä rooli synnynnäisen immuniteetin ensilinjan puolustuksessa infektoivia patogeenejä vastaan. Veriaivoesteiden läpi pääsee jatkuvasti viruksia ja patogeenejä, joita vastaan mikrogliat ja muut synnynnäisen immuunijärjestelmän solut aktiivisesti hyökkäävät. Neutrofiilit ja syöttö- l. mast-solut toimivat myös ensilinjan puolustuksessa ja signaloivat lymfosyyttien kanssa. Patogeeneja vastaan ne erittävät TNF-α ja IL-1β (Ransohoff & Brown 2012). Mikrogliat voivat ilmentää MHC II ja MHC I komplekseja ja voivat näin toimia myös antigeenejä esittelevinä soluina (APC) CD4+ ja CD8+ T-soluille. Mikrogliat voidaan nähdä toiminnallisuudeltaan eräänlaisina glia-solujen ja leukosyyttien hybrideinä, joissa yhdistyy neuronien morfologia ja immuunisolujen toiminnallisuus (Streit ym. 2014). Ne voivat suoraan tunnistaa mikrobeja ja erittävät muiden makrofagien lailla tuumori nekroosifaktoria (TNF), interleukiinia (IL-1) sekä interferoneja (INF). Kemokiineillä ja muilla kemoatraktanteilla ne voivat myös tarvittaessa rekrytoida avukseen muita immuunisoluja. Äkillinen selkäytimen tai optisen hermon vaurio muuttaa koko kehon immunologista profiilia. Tällöin keskushermosto alkaa erittää alarmiineja, kuten IL-33, ATP ja HMGB1, jotka aktivoivat gliasoluja ja rekrytoivat granulosyyttejä sekä monosyyttejä vauriopaikalle. Kehon muihin alueisiin verrattuna keskushermosto ekspressoi hyvin voimakkaasti IL-33, jolla voi olla monosyyttien rekrytoinnin lisäksi muita tärkeitä vielä tuntemattomia toimintoja (Kipnis 2016). Keskushermoston on helpompi korjata osittain vaurioituneita tai murskautuneita hermoyhteyksiä verrattuna kokonaan katkenneisiin hermoihin. 9
11 Osittain vaurioutuneiden hermojen jäljellä olevat rakenteet voivat tällöin toimia hermoston uusiutumista edistävänä scaffold-rakenteina. Nykykäsityksen mukaan aivojen reaktiivinen mikrogliapopulaatio voidaan jakaa kahteen äärifenotyyppiin M1 ja M2, joiden väli on liukuva. Aktivoidut mikrogliat voidaan jakaa edelleen M2a-, M2b-, M2c- sekä M1-fenotyyppeihin. Solut voivat muuttaa fenotyyppiään ja asettuvat jonnekin M1-ja M2-fenotyyppien välimaastoon. Niiden fenotyyppi määräytyy polarisaatiossa, kuten kehon muillakin makrofageilla. Hapen saatavuus vaikuttaa suoraan polarisaatioon. Anaerobisten metabolisten reittien ollessa aktiivisia M1-fenotyypin reaktiiviset mikrogliat ovat yleisempiä. Aerobisten metabolisten reittien aktivoituessa taas mikrogliat aktivoituvat enimmäkseen M2- fenotyyppiin (Franco ym. 2015) ja (Prinz ym. 2014). Parenkyymissä mikrogliat ympäröivät neuroneja ja tiedustelevat ulokkeillaan parenkyymiä aina noin kolmen tunnin välein. Kun ne havaitsevat merkkejä kudosvaurioista, kuten vapaata ATPtä tai solunulkoisia kalsiumpulsseja, ne aktivoituvat M1-tai M2-skaalalla. Terveessä keskushermostossa mikrogliat pidetään hiljennetyssä M0-fenotyypissä neuronien CD200 reseptorin ja mikrogliojen CD200 ligandin avulla (Hanisch ym. 2007). M0-fenotyypin aktivoimattomat mikrogliat toimivat perinteisten kudosmakrofagien tavoin poistaen solujätettä parenkyymistä. Aktivoidut M1-tyyppiset mikrogliat tuhoavat neuroneita demyelinisaation kautta. M2-tyypin mikrogliat korjaavat neuroneita remyelinisaation avulla, ja erittävät TGF- β kasvutekijää (transforming growth factor) (Cherry ym. 2014). Mikroglioilla on tärkeä rooli neuronien ja keskushermoston homeostaasin ylläpidossa. Ne erittävät neurotrofiineja, neurotrofista kasvutekijää (NGF), aivoperäistä hermokasvutekijää (BDNF), neurotrofiini-3 (NT3) ja gliasoluperäistä hermokasvutekijää (GDNF), jotka suojelevat ja säätelevät hermosolujen selviämistä ja uusiutumista (Ousman ym. 2012). Mikroglioilla on myös tärkeä rooli synaptisten verkkojen kehityksessä, synapsien karsinnassa ja myöhemmin niiden ylläpidossa. MHC I reseptorit ovat voimakkaasti ekspressoituneita aktivoitujen mikrogliojen pinnalla. Keskushermoston normaalista tilasta poiketen MHC I geenit ovat myös voimakkaasti aktivoituneet niillä aivojen alueilla, joissa on aktiivista synapsien uudelleenmuokkautumista (Michell-Robinson ym. 2015). MHC I proteiinit kolonialisoivat dendriittejä yhdessä post-synaptisten PSD95- proteiinien kanssa, mutta itse MHC I esittelemä peptidi-antigeeni on vielä toistaiseksi tuntematon (Bilimoria ym. 2015). Aivojen varhaisen kehityksen mikroglia välitteinen synapsien karsinta toimii yhteistyössä komplementin proteiinien kanssa. 10
12 Aivoihin voidaan tarvittaessa rekrytoida myös periferaalisen immuunijärjestelmän monosyyttistä solulinjaa olevia makrofageja. Ne eroavat mikroglioista paitsi alkuperänsä, myös fysiologisen roolinsa ja toimintaympäristönsä myötä. Niiden pääsy aivoihin tapahtuu kontrolloidusti plexus choroideuksen kautta. Mast-soluja l. syöttösoluja on löydetty paitsi aivokalvostosta, myös perivaskulaarisesta tilasta. Ne erittävät serotoniinia hippokampukseen ja edistävät näin aivojen oppimisprosesseja ja neurogeneesiä. Kuten mikrogliojen, myös mast-solujen liiallinen aktivaatio voi olla haitallista aivoille. Keskushermostossa sama kuvio toistuu myös muiden glia- ja immuunisolujen kohdalla Astrosyytit Astrosyytit ovat mesenkymaalista alkuperää olevia keskushermoston immunologisesti aktiivisia gliasoluja. Astrosyytit huolehtivat keskushermoston kalium-ioni ja vesi-tasapainosta, ne käsittelevät ja poistavat potentiaalisesti toksista glutamaattia sekä moduloivat synapsien aktiivisuutta ja verenkiertoa. Mikrogliojen tapaan myös astrosyytit tuottavat neurotrofiineja ja anti-inflammatorisia sytokiinejä, kuten IL-10. Lisäksi TLR ja NLR signaalien aktivoimat astrosyytit tuottavat IL-1β, IL- 6, kemokiineja sekä lukuisia komplementti-järjestelmän komponentteja. Astrosyytit ovat lisäksi jatkuvassa vuorovaikutuksessa mikrogliojen kanssa (Ransohoff & Brown 2012). Astrosyyttejä on morfologialtaan kahdenlaisia. Säikeiset astrosyytit ovat lokalisoituneet aivojen parenkyymin valkeaan aineeseen. Protoplasmisia astrosyyttejä tavataan pääasiallisesti harmaassa aineessa. Reaktiiviset astrosyytit voidaan myös jakaa karkeasti kahteen äärifenotyyppiin A1 ja A2, jotka vastaavat makrofagien M1-ja M2-skaalaa (Aronica 2012). A1-tyypin astrosyytit ovat pääasiallisesti neurotoksisia. A2-tyypin astrosyytit ovat puolestaan neuroprotektiivisia ja pyrkivät voimakkaasti korjaamaan keskushermoston vaurioita. Kuten aiemmin mainituilla mikroglioilla, myös astrosyyteillä on rooli aivojen kehityksen aikana tapahtuvassa synapsien karsinnassa ja fagosytoosissa. Näitä muodostuu nopeasti keskushermoston vaurioitumisen seurauksena sekä monien neurodegeneratiivisten sairauksien yhteydessä (Liddelow ym. 2016). Neurotoksiset reaktiiviset A1-astrosyytit ovat aktivoitujen mikrogliojen indusoimia. A1-tyypin astrosyytit aktivoituvat mikrogliojen erittämien IL-1α, TNF sekä komplementin C1q-proteiinien indusoimina kokeellisesti in vitro sekä in vivo. A1-fenotyypin astrosyytit menettävät kykynsä tukea synapseja ja fagosytoida solujätettä. Sen sijaan ne alkavat aktiivisesti pilkkomaan synapseja. A1- tyypin astrosyytit tuottavat toistaiseksi tuntematonta liukoista toksiinia, joka tuhoaa 11
13 keskushermoston neuroneja ja oligodendrosyyttejä, muttei tapa muita soluja. A1-astrosyyttien on myös todettu indusoivan komplementtiproteiinien komponenttien ilmentymistä. Varsinkin Alzheimerin taudin yhteydessä A1-fenotyypin astrosyyttien on havaittu ekspressoivan voimakkaasti C3-proteiinia. On mahdollista, että keskushermostoa uhkaavan vaurion, bakteeri- tai virus-infektion tai neurodegeneratiivisen sairauden yhteydessä A1-tyypin astrosyytit yrittävät pelastaa neuroverkon aggressiivisella toimimattomien neuronien eliminaatiolla ja komplementin aktivaatiolla (Liddelow ym. 2017) Komplementtijärjestelmä Komplementtijärjestelmä koostuu noin 60 eri tyyppisestä liukoisesta proteiinista. Suurin osa periferaalisen immuunijärjestelmän komplementtiproteiineista tuotetaan maksassa. Keskushermoston komplementtiproteiinien tuotannosta vastaavat neuronien lisäksi mikrogliat ja astrosyytit. Perifeerisessä immuunijärjestelmässä komplemnettiproteiinit muodostavat synnynnäisen puolustuksen humoraalisen etulinjan, mutteivät pääse kulkemaan veri-aivoesteen yli. Aivoissa paikallisilla komplementtijärjestelmän proteiineilla on tärkeä rooli synaptisten verkkojen kehityksessä ja ylimääräisten synapsien merkitsemisessä karsittaviksi. Niitä tarvitaan myös neurogeneesissä, solujen migraatiossa sekä kokonaishomeostasian ylläpitämisessä. Komplementtikaskadi voi aktivoitua kolmella eri tavalla, jotka kaikki johtavat C3- ja C5- komplementtiproteiinien aktivoitumiseen. Signaalikaskadin lopuksi muodostuu kalvohyökkäyskompleksi (membrane attack complex, MAC), joka rakentuu yhteenliittyneistä C9- proteiineista. Kompleksi muodostaa kanavan kohteensa solukalvoon ja aiheuttaa kohdesolun hallitsemattoman lyysautumisen ja nekroosin. Komplementtiproteiinit voivat myös peittää toksiinin tai patogeenin l. opsonoida sen, jolloin sen toksiini inaktivoituu tai patogeeni solusyödään l. fagosytoidaan (Hedman ym. 2011). Keskushermostossa komplementtiproteiinien aktivaatiota ja toimintaa säädellään tiukasti neuroimmuni-säätelijöiden avulla (NIReg). Neuroneja lukuun ottamatta, muut keskushermoston solut ilmentävät edellä mainittuja komplementti-inhibiittoreita kuten CD59 ja komplementtifaktori H (CFH) ja Crry, jotka pääasiassa estävät C3- komplementtiproteiinin toimintaa. Klassisen komplementtikaskadin proteiinit lokalisoituvat aivojen normaalin kehityksen aikana karsittavien heikkojen tai vähemmän aktiivisten synapsien solukalvoille. Ne toimivat merkkeinä 12
14 mikroglioille, joiden pinnalla on komplementtireseptoreita. Neuronaaliselta aktiivisuudeltaan voimakkaammat aksonit lähettävät niitä suojelevaa paikallista signaalia sekä pidemmälle kulkeutuvaa muiden aksonien eliminaatiosignaalia. Synapsien eliminaatio tapahtuu vierekkäisten aksonien kilpailuna post-synaptisesta tilasta. Mikrogliat karsivat komplementtiproteiineilla merkityt synapsit. Erityisesti C1q, C1ql2 ja pre-synaptisesti eritettävät cerebelliini Cbln1 sekä C3b komplementtiproteiinien on todettu toimivan fagosytoosin merkkiaineina. Mikrogliat yleisesti ekspressoivat C1q, C3 ja C5 komplementtireseptoreita, joiden avulla indusoidaan fagosytoosia, sytokiini signalointia sekä kemotaksista. Reaktiiviset astrosyytit ekspressoivat myös voimakkaasti C3 ja muita komplementtikaskadin proteiineja (Stephan ym. 2012). Komplementtijärjestelmä on myös jatkuvassa vuorovaikutuksessa muun neuroimmunijärjestelmän osien kanssa Adaptiivinen neuroimmuniteetti Lymfosyytit, autoreaktiiviset T-solut ja suojaavan autoimmuniteetin teoria Lymfosyytit koostuvat luuytimessä syntyvistä T- ja B-soluista. T-solujen maturaatio tapahtuu kateenkorvassa ja B-solujen luuytimessä. T- ja B-solut erilaistuvat edelleen imusolmukkeissa ja muissa sekundaarisissa imuelimissä, joissa niille esitellään imunesteestä löytyneitä antigeenejä. Perifeerisessä immuunijärjestelmässä T-solut erilaistuvat klonaalisen valinnan kautta, jolloin autoreaktiiviset solut karsitaan pois. Dendriittisolujen järjestämä antigeenien esittely tapahtuu joko MHC I- tai MHC II- kompleksin avulla, johon T-solut tarttuvat t-solureseptorillaan. Tunnistaakseen antigeeninsä T-solu tarvitsee reseptorin lisäksi erilaisia apureseptoreja ja proteiineja. Toimiva T- solureseptori on oktameerinen proteiinikompleksi, jossa on itse reseptorin ja CD3-apuproteiinin lisäksi joko CD4- tai CD8-apureseptori. T-solut maturoituvat myöhemmin joko CD4+ tai CD8+ T- soluiksi, edellisen ligandi on MHC II- ja jälkimmäisen MHC I-kompleksin esittelemä antigeenin epitooppi (Komal ym. 2015) ja (Murphy ym. 2012). Aivoissa lymfoidista solulinjaa olevia immuunisoluja esiintyy lähinnä perifeerisillä pinnoilla ja aivokalvostoissa kiertävässä aivo-selkäydinnesteessä. Parenkyymin ulkopuolella CD4+ T-solut l. auttaja- ja muisti T-solut muodostavat jopa 80% aivojen immuunisoluista (Ousman ym. 2012). Paikallisia CD8+ T-soluja l. sytotoksisia T-soluja on myös löydetty parenkyymistä (Selmi ym. 2016). Näistä ainakin osa on pitkäikäisiä CD8+ muisti-t-soluja. Kehon muista T-soluista poiketen keksuhermoston T-solut ekspressoivat CD103 integriiniä, eivätkä myöskään ole riippuvaisia samoista selviytymissignaaleista kuin kehon muut T-solut (Solomos ym. 2016). 13
15 CD4+ T-solut läpäisevät veri-likvoriesteen (BCSFB) epiteelisolukon adheesiomolekyylien ja reseptorien vuorovaikutuksella. Adheesiomolekyyleinä ovat mm. vaskulaariset soluadheesiomolekyylit (VCAM), ja intrasellulaariset adheesiomolekyylit (ICAM), sekä liitosadheesiomolekyylit (JAM) (Engelhardt & Ransohoff 2012). Aktivoidut lymfosyytit voivat tulehdusreaktiossa siirtyä myös varsinaisen veri-aivoesteen (BBB) läpi selektiinien ja integriinien välisellä vuorovaikutuksella. Migraatiota voi tapahtua samoin kemokiinien (CCL19, CCL21) ja metalloproteinaasien (MMP) sekä kudos-spesifisten inhibiittorien (TIMP) vuorovaikutuksella. Lymfosyyttien funktionalisuuteen liittyvä antigeeni (LFA-1) sitoutuu ICAM-1 ja ICAM-2 adheesiomolekyyleihin ja mahdollistaa lymfosyyttien transendoteelisen migraation veri-aivoesteen läpi. Näin tapahtuvaa lymfosyyttien migraatiota voidaan havaita erityisesti systeemisten immuunireaktioiden aikana (Schwartz ym. 2014). Kroonisen inflammaation aikana myös adenosiinireseptorit ja CD39 sekä CD73 mahdollistavat migraation BBB yli (Selmi ym. 2016). Aktivoidut keskushermoston paikalliset CD4+ T-solut voivat rekrytoida BBB läpi muita, naïveja periferaalisen immuunijärjestelmän T-soluja. Mekanismit, joilla T-solut pääsevät aivoaivokalvoesteen (BMB) yli itse parenkyymiin ovat vielä toistaiseksi tuntemattomia. Autoreaktiiviset T-solut ovat kriittisessä roolissa aivojen terveyden ylläpidossa (Schwartz 2015). Toisin kuin muualla kehossa, likvorissa kiertävät lymfosyytit ovat useimmiten autoreaktiivisia CD4+ tai CD8+ T-soluja. Tämä häkellyttävältä kuulostava seikka saattaa johtua parenkyymin solujen vähäisestä MHC I ekspressiosta ja täten self-tunnistuksen mahdottomuudesta ilman totaalista autoreaktiivisuutta. Toisin sanottuna keskushermoston CD8+ T-lymfosyytit eivät voi tunnistaa keskushermoston omia soluja muutoin kuin tunnistamalla spesifisesti nämä kehon omat rakenteet antigeeneikseen. Muualla kehossa tämän kaltainen autoreaktiivisuus on tiukasti valvottua yli 20 vartiopisteen kautta lymfosyyttien maturaation aikana. Autoreaktiivisuus johtaa perifeerisessä immuunijärjestelmässä väistämättä joko indusoituun solukuolemaan l. apoptoosiin, anergiaan, T-reg supression tai kuolemaan hyljinnän kautta (death by neglect). Perifeerisessessä immuunijärjestelmässä autoreaktiiviset T-solut hyökkäisivät siis kehon omia soluja ja kudoksia kohtaan. Keskushermostossa näin ei tapahdu, ja autoreaktiivisten T-solujen voidaan katsoa tältä osin olevan immunologisesti ignorantteja (Murphy ym. 2012). T-solujen autoreaktiivisuuden säätely on tärkeää immuunokompetenssin ylläpitämisen kannalta. Liiallinen supressio ja säätely heikentää immuunokompetenssia, liian vähäinen kontrolli taas saattaa laukaista autoimmuunisairauden. 14
16 Glymfaattisen suoniston endoteelisolukossa epäillään olevan jokin, vielä tuntematon anergiaa ylläpitävä komponentti (Carson ym. 2006). Keskushermostossa tavattavien lymfosyyttien aktivaatio ja erilaistuminen ovat intensiivisen tutkimuksen kohteena, koska likvorissa esiintyvistä T-soluista suurin osa on autoreaktiivisia CD4+ T-soluja, joilla on MHC II-kompleksin esittelemän antigeenin epitoopin tunnistava T-solureseptori. Osa autoreaktiivisista protektiivisista CD4+ T-soluista toimii myös MHC II riippumattomasti. Keskushermoston tai selkäytimen vaurioituessa esimerkiksi onnettomuuden seurauksena MHC II-riippumattomien autoreaktiivisten CD4+ T-solujen on havaittu estävän erittämällään IL-4 neuronien sekundaarista degeneraatiota. Tällöin itse primaarisessa vauriossa tuhoutuneet neuronit luovat hajotessaan toksisen mikroympäristön, joka aiheuttaa muiden neuronien tuhoutumisen sekundaarisen degeneraation seurauksena (Walsh ym. 2015). T-soluille antigeenejä esitteleviä dendriittisoluja ei ole tavattu parenkyymistä, mutta niitä on runsaasti hiiren ja ihmisten kova- ja lukinkalvoissa, pia materissa, likvorissa sekä plexus chorioideuksessa (Ousman ym. 2012). Antigeenien esittelyn ja T-solujen aktivaation uskotaan tapahtuvan aivokalvostossa. Lisäksi makrofagit ja mikrogliat voivat esitellä antigeenejä T-soluille. Neuronit eivät ekpressoi MHC II molekyylejä, mutta voivat kommunikoida T-solujen kanssa suoraan B7-ligandin avulla. Toiselle tärkeälle lymfosyyttien populaatiolle, B-soluille ei ole löydetty suurta roolia keskushermoston immunijärjestelmässä. Perifeerisessä immuunijärjestelmässä ne tuottavat vastaaineita, ja toimivat muistisoluina adaptiivisen immuunijärjestelmän ensimmäisen kerran kohtaamille patogeeneille. Patogeeni-spesifisillä vasta-aineilla B-solut aktivoivat immuunipuolustuksen nopeasti ja tehokkaasti jos sama patogeeni tavataan kehosta uudestaan. Johtuen autoreaktiivisista T-soluista vasta-aineiden rooli keskushermostossa on kuitenkin rajoitettu ja erilainen periferiaan verrattuna. Veri-aivoesteen läpi kuljetettavalla IgG-vasta-aineella tosin on rooli komplementin aktivaatiossa sekä opsonisaatiossa. Suojaavan autoimmuniteetin teoria pohjautuu immuunisoluverkon (immune cell network) käsitteeseen. Verkko koostuu CNS-antigeeneille spesifisistä efektorisoluista, T-reg säätelijäsoluista, sekä näiden yhteisestä toiminnasta keskushermoston ylläpidossa ja korjaamisessa. Yli kymmenen vuoden tutkimusten tuloksena on selvinnyt, että monosyyttistä alkuperää olevat makrofagit yhdessä ja koordinoidusti autoreaktiivisten T-solujen kanssa tukevat CNS toipumista akuutin steriilin mekaanisen vaurion yhteydessä. Samalla tavoin näiden yhteistyö mahdollistaa poikkeamat 15
17 homeostaasista, kuten voimistuneen aivotoiminnan, plastisuuden tai häiriösignaaleihin vastaamisen. Immuunisoluverkko edesauttaa homeostasian palautumisen tasapainotilaan sytokiinien ja kasvutekijöiden osalta (Schwartz 2005). Kehossa keskushermostolla on ainutlaatuinen mahdollisuus valikoida immuunisolupopulaationsa ja samalla maksimoida immuunijärjestelmän hyödyt sekä minimoida autoimmuunireaktioiden haitat. Suojaava autoimmuniteetti perustuu tarkasti säädeltyyn, suojaavaan ja hyödylliseen autoreaktiivisuuteen. Sen on oltava paitsi temporaalisesti T-reg säädeltyä, mutta myös spatiaalisesti eristettyä omiin kalvostoihin ja tiloihin. Se on myös dynaaminen ja itsenäisesti toimiva integroitujen immuunisolujen verkko. Hiirimalleilla tehtyjen tutkimusten perusteella autoreaktiivisilla T-soluilla on voimakas oppimista ja neurogeneesiä tukeva vaikutus. Ikääntymiseen liittyvät degeneratiiviset aivosairaudet ja aivojen heikentynyt kyky palautua tasapainotilaan akuutista stressistä tai vaurioista voi johtua heikentyneestä autoreaktiivisesta immuunisoluverkosta (Schwartz & Raposo 2014). 3. Keskushermoston patofysiologia ja neuroimmuniteetti 3.1 Keskushermoston häiriöt, vauriot, neurodegeneraatio ja vanheneminen Keskushermoston immuunijärjestelmän tärkeimpiä tehtäviä on vakaan kemiosmoottisen ympäristön ylläpito sekä mikrogliojen ja astrosyyttien tarjoama suojelu ja troofinen tuki varsinaisille hermosoluille. Häiriötilanteissa aivojen homeostasia usein järkkyy ja kroonisen inflammaation myötä veri-aivoesteiden eristävä vaikutus voi heikentyä. BBB moduloivat IL-1β, IL-6 ja TNF α, sekä adenosiini adenosiinieseptorien ja P1 purinergisten reseptorien kautta. BBB toiminta muuttuu myös selkäydinvaurion, tai aivoverenkiertohäiriön seurauksena. Selkäydinvauriossa neuroinflammatoristen sekä neurotrofisten tekijöiden kuten TNF, neuroprotektiivisen peptidin PACAP:in (pituitary adenylate cyclase-activating polypeptide) ja leukemia inhibitorisen tekijän kuljetus voimistuu. Aivoverenkiertohäiröissä taas TNF ja PACAP kuljetus voimistuu (Banks 2016). Keskushermoston vauriot ovat yleensä joko traumaperäisiä, aivojen hapensaannin estymisestä l. hypoksiasta tai neurodegeneratiivisista sairauksista johtuvia. Vaurio johtaa neuronien välittömään tai hitaammin etenevään tuhoutumiseen. Aivokudoksen hypoksia voi johtua joko aivoverenkierronhäiriöstä tai esimerkiksi sydänkohtauksen tai hukkumisen aiheuttamasta kehon systeemisestä happivajeesta. Tällöin neuronien mitokondrioiden kaspaasi-3 entsyymi aktivoituu ja johtaa ohjelmoituun solukuolemaan l. apoptoosiin. Apoptoottisen signaalikaskadin aktivoi myös 16
18 kasvutekijöiden vaje, DNA vauriot, tai muut stressitekijät. Hypoksian myötä aivokudokseen alkaa kerääntyä glutamaattia. Tällöin neuronien glutaminerginen ylistimulaatio aiheuttaa eksitotoksisen stressitilan, joka voi laukaista Bcl-2 ja sytokromi-c välitteisen apoptoottisen signaalikaskadin. Yleisimpiä keskushermoston neurodegeneratiivisia sairauksia ovat Parkinsonin tauti (PD) ja Alzheimerin tauti (AD). Näiden ja monien muiden neurologisten sairauksien taustalta on viime aikoina löydetty neuroimflammatorinen komponentti (Streit ym. 2014). Krooninen imflammaatio myötävaikuttaa osaltaan myös neuronien degeneraatioon aktivoimalla neurotoksisia reaktiivisia mikrogliasoluja. Komplementtijärjestelmän vääränlainen aktivaatio destabiloi hermoverkkoja myös aikuisiällä. Neurodegeneratiivisten tautien, kuten Alzheimerin taudin taustalla vaikuttaa neuronien massiivinen tuhoutuminen, jota edeltää synapsien toiminnan häiriintyminen ja karsinta. Noin puolet kaikista dementiatapauksista on AD aiheuttamia. Tällöinkin neuroverkkojen laaja tuhoutuminen ja patologinen inflammaatio edeltävät usein varsinaisten oireiden ilmaantumista. Oireita alkaa ilmaantua vasta kun neurodegeneraatio on laajamittaista. Myös Parkinsonin taudin oireet ilmaantuvat vasta, kun aivojen substantia nigran motoriikasta vastaavista dopaminergisistä A9- neuroneista suuri osa on tuhoutunut ja aivoihin alkaa kertyä Lewy-plakkeja. Dopaminergiset neuronit altistuvat myös oksidatiiviselle stressille, joka vaurioittaa niiden mitokondrioita ja aiheuttaa häiriöitä neuronin solukalvon normaalille depolarisaatiolle. Alzheimerin tauti on yleensä oireeton noin 20 vuoden ajan, jonka jälkeen oireita alkaa ilmaantua. Vähäisten oireiden vaihe (Mild cognitive impairment MCI) kestää noin 10 vuotta, jonka jälkeen puhkeaa varsinainen dementia. Aivojen surkastuminen kiihtyy ja β-amyloidi plakit suurentuvat MCI-vaiheen aikana (Okano & Yamanaka 2014). Komplementtiproteiinien on havaittu yliekspressoituneen monissa degeneratiivisissa aivosairauksissa ennen varsinaista hermosolujen tuhoutumista. Tämä voi mahdollisesti johtua samantyyppisestä synapsien merkitsemisestä karsittaviksi kuin normaalisti aivojen varhaisen kehityksen aikana. Etenkin Alzheimerin taudissa ja silmän glaukoomassa synapsien merkintä karsittaviksi edeltää oireiden ilmaantumista. Merkittävässä roolissa ovat reaktiiviset gliasolut, jotka erittävät sytokiineja ja aktivoivat komplementtikaskadin. Synaptisen karsinnan seurauksena neuronin aksoni vaurioituu ja johtaa yleensä neuronin kuolemaan. Glioosis, mikrogliaaktivaatio ja koko komplementtikaskadin aktivaatio Alzheimerin taudin mukana näkyy likvorissa jopa 80- kertaisena C1q-proteiinin määränä normaaliin verrattuna. Alzheimerin taudille ovat ominaisia myös 17
19 väärin laskostuneet β-amyloidi plakit. Synapsien karsinta ja komplementtijärjestelmän aktivaatio ovat yksi Huntingtonin taudin, Parkinsonin ja MS- ja ALS-taudin tunnusmerkkejä. Raskaudenaikainen altistuminen tulehduksille saattaa aktivoida sikiön keskushermoston komplementtijärjestelmän tuhoisin seurauksin. Reaktiiviset M2-mikrogliat ja astrosyytit alkavat tällöin karsia syntyviä aksoneita liian tehokkaasti. Samalla aksonien karsiminen tuhoaa neuroneja ja saattaa aiheuttaa neurologisia kehityshäiriöitä kuten autismia (Stephan ym. 2012). Immunologinen skenesenssi vanhenemisen myötä tarkoittaa luuytimen rasvoittumisesta johtuvaa efektori-solujen asteittaista vähenemistä ja tuotannon hiipumista. Terveessä immuunijärjestelmässä efektorisolut ovat tasapainossa säätelysolujen kanssa ja immuunireaktiot ovat tiukasti säädeltyjä, mutta tarvittaessa voimakkaita. Vanhenemisen myötä, sekä synnynnäisen immuniteetin efektorisolujen kuten mikrogliojen, että adaptiivisen immuniteetin T-efektorisolujen määrä vähenee. Samalla sekä synnynnäisen immuniteetin, että adaptiivisen immuniteetin säätelysolujen, kuten T- reg-solujen suhteellinen määrä kasvaa kehossa ja aivoissa. Tämä immuunosuppressiivisten solujen osuuden kasvu keikauttaa immuunisolujen tasapainon immuunosupression suuntaan. Samaan aikaan mikrogliojen neuroneita suojaava vaikutus heikkenee ikääntymisen myötä. Troofisen tuen sekä immuunivalvonnan heikkenemisen lisäksi amyloidiplakkeja ja tau-proteiineja, sekä muuta solujätettä kerääntyy parenkyymiin mikrogliojen fagosytoositoiminnan hiipuessa. Tällä mikrogliojen dystrofialla, on joidenkin tutkijoiden mukaan neuroinflammaatiota suurempi rooli Alzheimerin- ja Parkinsonin taudeissa (Streit ym. 2014). Myös kateenkorva surkastuu iän myötä ja johtaa lopulta immuunijärjestelmän systeemiseen heikkenemiseen T-solujen määrän vähentyessä. Tämä vaikuttaa suoraan aivojen homeostasiaan ja saattaa siten johtaa krooniseen neuroimflammaatioon, tai laukaista piileviä neurodegeneratiivisia sairauksia. Aivojen meningeaalinen lymfaattinen järjestelmä heikkenee iän myötä eikä enää huuhtele parenkyymiä tehokkaasti. Tällöin kudoksiin alkaa kerääntyä metabolista jätettä, toksiineja, solujätettä sekä elävien solujen ravinnon saanti heikkenee. Monosyyttisten makrofagien tiedetään myös poistavan beta-amyloidi plakkeja, väärin laskostuneita proteiineja, myeliini-inhibiittoreita ja säätelevän reaktiivisia mikroglioja. Myös tämä, parenkyymiä puhdistava toiminta näyttää heikkenevän iän myötä (Schwartz & Raposo 2014). 18
20 3.2 Autoimmuunisairaudet, syöpä ja mikrobi-infektiot Aiemmin käsittelin autoimmuunien T-solujen tärkeyttä keskushermoston homeostasian ylläpidossa. Immuunijärjestelmä yrittää korjata aivoja, mutta joissain tapauksissa kuten MS- ja ALS-taudeissa, autoimmuunit solut hyökkäävät tervettä aivokudosta vastaan. MS-tauti, kuten autoimmuunisairaudet yleensä, ovat yleisempiä naisilla kuin miehillä. Tämä johtuu naisten miehiä yleisesti robustimmasta ja voimakkaammasta immuunijärjestelmästä. Tästä johtuen naisille immuunijärjestelmän T-reg kontrollin heikkeneminen on vaarallisempaa kuin miehille. Tämä selittää myös joidenkin naisten raskaudenaikaisen momnesian, pregnancy brainin tai brain fogin - ilmiön. Suojellakseen sikiötä odottavan äidin immuunijärjestelmä supressoi itseään ja tämä johtaa häiriöihin aivojen homeostasiassa. Homeostasian muutos saattaa häiritä aivojen kognitiivisia toimintoja. Synnytyksen jälkeen äitien immuunijärjestelmä ja aivojen homeostasia kuitenkin palautuu nopeasti normaaliksi (Schwartz 2015). MS-taudin alkuvaiheessa mikrogliat ja makrofagit aktivoituvat ja aiheuttavat patologisen tulehdusreaktion, jonka yhteydessä veri-aivoesteet voivat alkaa vuotaa, kudoksessa alkaa liikkua reaktiivisia astrosyyttejä ja parenkyymissä alkaa ilmetä neuroneiden demyelinisaatiota. Lopulta sekä CD4+, että CD8+ T-solut hyökkäävät myeliiniä vastaan ja alkavat tuhota sitä ja niiden ympäröimää aksonia. Synaptisten autoimmuunisairauksien laukaisevia signaaleja ei varmuudella tunneta, mutta viruksilla voi olla osuutta niiden synnyssä. Esimerkkinä jopa 20% herpes simplexvirusta (HSV) kantavista potilaista kärsii HSV enkefaliitista ja kroonisista oireista ilman viruksen aktivoitumista (Selmi ym. 2016). Neurotrooppiset virukset kuten rabies, herpesvirukset ja poliovirukset ovat tunnettuja keskushermoston patogeeneja. Muita keskushermostoa infektoivia viruksia ovat influenssa-, länsiniilin- ja tuhkarokkovirus. Virusten tiedetään siirtyvän muualta kehosta aivoihin transneuronaalisesti sekä verisolujen mukana. Herpes simplex I ja II, sekä rabies-virus tuottavat proteiineja, joiden avulla ne voivat dyneiiniä ja kinesiiniä moottoreinaan käyttäen kulkea aksonien mikrotubuluksia pitkin aivoihin. Keskushermostoon päästyään, ne yrittävät infektoida viereisiä neuroneita virioneillaan. HIV taas piiloutuu infektoimiinsa CD4+ T-soluihin ja kulkee sen mukana parenkyymiin, jossa se aktiivisesti infektoi neuroneita ja astrosyyttejä (Solomos ym. 2016). Virukset pääsevät usein aivoihin myös veri-aivoesteen ja veri-likvoriesteen läpi verisuonista ja plexus choiroideuksen kautta. Länsi-niilin-virus käyttää TLR3, herpes varicella zoster-virus ja vapaana solujen ulkopuolella oleva HIV-1 käyttävät mannoosi-6-fosfaatti reseptoria (M6PR) 19
21 infektoidakseen soluja (Dohgu ym. 2012). Enterovirukset voivat suoraan infektoida epiteelisolukkoa ja levittäytyä enteenpäin keskushermostoon. Infektio havaitaan tällöin Toll likereseptorien (TLR) avulla ja se synnyttää vasteen synnynnäisissä immuunisoluissa. Immuunisoluja rekrytoidaan muualta kehosta adheesiomolekyylien ICAM1 ja ICAM3, sekä sytokiinien ja kemokiinien avulla TNF-α, IL-6, IL-8, IL-1β sekä CCL5 ja CXCLI-3 (Schwerk ym. 2015). Virukset tuhotaan muualla kehossa pääasiassa sytolyyttisesti CD8+ T-solujen, tai luonnollisten tappaja T-solujen toimesta (NKT), mutta inflammaation minimoimiseksi aivoissa on muita, korvaavia mekanismeja. Neuronit itsessään aktivoituvat INF-γ läsnäolosta, mutta antiviraalisten geenien aktivointi on hidastunut. Muista soluista poiketen, neuronit eivät syntetisoi anti-viraalisia proteiineja nopeasti, vaan INF-γ itsessään suojelee niitä interferonien sytotoksisilta, apoptoosia indusoivilta vaikutuksilta jollain, toistaiseksi vielä tuntemattomalla mekanismilla (O donnell ym. 2015). Ihmisen suolistobakteerit vaikuttavat myös keskushermoston homeostasiaan. Bakteerialtistuksella tiedetään olevan rooli BBB-lujittumisessa ja muovautumisessa. Toisaalta joissain tapauksissa suolistobakteerien on myös todettu laukaisevan piilevän autoimmuunisairauden (Wekerle 2016). Myös patogeenisten bakteerien kesken voi olla immuunijärjestelmää moduloivaa vuorovaikutusta. Keskushermosto saattaa olla alttiimpi polymikrobiaalisille sairauksille, joiden infektion laukaisemia T-soluja voi myös kulkeutua aivoihin ja aiheuttaa siellä tulehdusreaktion. Samoin kahden viruksen samanaikainen infektio voi aiheuttaa patologisen inflammaation CD8+ T-solujen hyökätessä ependymaalisolujen kimppuun (Solomos ym. 2016). Keskushermoston rajoitetun immuunivalvonnan takia neurokarsinoomat muodostavat vakavan uhan keskushermostolle. Syöpäsolut pystyvät manipuloimaan immuunivasteita erittämällä immuunosupressiivisia interleukiineita kuten IL-10. Perinteisesti kemoterapia aivokasvaimia vastaan on ollut vaikeaa johtuen lääkkeiden heikosta BBB läpäisykyvystä. Uusien nanopartikkelien avulla lääkkeitä voidaan teoriassa kuljettaa paremmin kohteisiinsa, jopa syvälle aivoihin. 20
KandiakatemiA Kandiklinikka
 Kandiklinikka Kandit vastaavat Immunologia Luonnollinen ja hankittu immuniteetti IMMUNOLOGIA Ihmisen immuniteetti pohjautuu luonnolliseen ja hankittuun immuniteettiin. Immunologiasta vastaa lymfaattiset
Kandiklinikka Kandit vastaavat Immunologia Luonnollinen ja hankittu immuniteetti IMMUNOLOGIA Ihmisen immuniteetti pohjautuu luonnolliseen ja hankittuun immuniteettiin. Immunologiasta vastaa lymfaattiset
11. Elimistö puolustautuu
 11. Elimistö puolustautuu Taudinaiheuttajat Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin
11. Elimistö puolustautuu Taudinaiheuttajat Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA MITÄ ROKOTUKSIA? Muistatko mitä rokotuksia olet saanut ja minkä viimeiseksi? Miten huolehdit koulun jälkeen rokotuksistasi? Mikrobit uhkaavat elimistöä Mikrobit voivat olla bakteereita,
BI4 IHMISEN BIOLOGIA MITÄ ROKOTUKSIA? Muistatko mitä rokotuksia olet saanut ja minkä viimeiseksi? Miten huolehdit koulun jälkeen rokotuksistasi? Mikrobit uhkaavat elimistöä Mikrobit voivat olla bakteereita,
Elimistö puolustautuu
 Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Miten elimistö
Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Miten elimistö
Elimistö puolustautuu
 Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Mistä taudinaiheuttajat
Elimistö puolustautuu Tautimikrobit (= patogeenit): Bakteerit (esim. kolera), virukset (esim. influenssa), alkueliöt (esim. malaria), eräät sienet (esim. silsa) Aiheuttavat infektiotaudin Mistä taudinaiheuttajat
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA IHMINEN ON TOIMIVA KOKONAISUUS Ihmisessä on noin 60 000 miljardia solua Solujen perusrakenne on samanlainen, mutta ne ovat erilaistuneet hoitamaan omia tehtäviään Solujen on oltava
BI4 IHMISEN BIOLOGIA IHMINEN ON TOIMIVA KOKONAISUUS Ihmisessä on noin 60 000 miljardia solua Solujen perusrakenne on samanlainen, mutta ne ovat erilaistuneet hoitamaan omia tehtäviään Solujen on oltava
IMMUNOLOGIAN PERUSTEET Haartman-instituutti
 IMMUNOLOGIAN PERUSTEET Petteri.Arstila@helsinki.fi 2012 Haartman-instituutti Immuunijärjestelmän tarkoituksena on torjua vieraita taudinaiheuttajia. Immuunipuolustus on organisoitu siten, että perifeerisissä
IMMUNOLOGIAN PERUSTEET Petteri.Arstila@helsinki.fi 2012 Haartman-instituutti Immuunijärjestelmän tarkoituksena on torjua vieraita taudinaiheuttajia. Immuunipuolustus on organisoitu siten, että perifeerisissä
Autoimmuunitaudit: osa 1
 Autoimmuunitaudit: osa 1 Autoimmuunitaute tunnetaan yli 80. Ne ovat kroonisia sairauksia, joiden syntymekanismia eli patogeneesiä ei useimmissa tapauksissa ymmärretä. Tautien esiintyvyys vaihtelee maanosien,
Autoimmuunitaudit: osa 1 Autoimmuunitaute tunnetaan yli 80. Ne ovat kroonisia sairauksia, joiden syntymekanismia eli patogeneesiä ei useimmissa tapauksissa ymmärretä. Tautien esiintyvyys vaihtelee maanosien,
Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö
 Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö 1 ESITYKSEN SISÄLTÖ Miten rokottaminen suojaa yksilöä? Immuunijärjestelmä Taudinaiheuttajilta suojaavan immuniteetin
Miten rokottaminen suojaa yksilöä ja rokotuskattavuus väestöä Merit Melin Rokotusohjelmayksikkö 1 ESITYKSEN SISÄLTÖ Miten rokottaminen suojaa yksilöä? Immuunijärjestelmä Taudinaiheuttajilta suojaavan immuniteetin
Anatomia ja fysiologia 1
 Anatomia ja fysiologia 1 Tehtävät Laura Partanen 2 Sisällysluettelo Solu... 3 Aktiopotentiaali... 4 Synapsi... 5 Iho... 6 Elimistön kemiallinen koostumus... 7 Kudokset... 8 Veri... 9 Sydän... 10 EKG...
Anatomia ja fysiologia 1 Tehtävät Laura Partanen 2 Sisällysluettelo Solu... 3 Aktiopotentiaali... 4 Synapsi... 5 Iho... 6 Elimistön kemiallinen koostumus... 7 Kudokset... 8 Veri... 9 Sydän... 10 EKG...
Pienryhmä 3 immuunipuolustus, ratkaisut
 Pienryhmä 3 immuunipuolustus, ratkaisut 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön
Pienryhmä 3 immuunipuolustus, ratkaisut 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön
vauriotyypit Figure 5-17.mhc.restriktio 9/24/14 Autoimmuniteetti Kudosvaurion mekanismit Petteri Arstila Haartman-instituutti Patogeeniset mekanismit
 vauriotyypit Kudosvaurion mekanismit Autoimmuniteetti Petteri Arstila Haartman-instituutti Antigeenin tunnistus HLA:ssa pitää sisällään autoimmuniteetin riskin: jokaisella on autoreaktiivisia lymfosyyttejä
vauriotyypit Kudosvaurion mekanismit Autoimmuniteetti Petteri Arstila Haartman-instituutti Antigeenin tunnistus HLA:ssa pitää sisällään autoimmuniteetin riskin: jokaisella on autoreaktiivisia lymfosyyttejä
IMMUUNIPUUTOKSET. Olli Vainio Turun yliopisto
 IMMUUNIPUUTOKSET Olli Vainio Turun yliopisto 130204 IMMUNOLOGIA Oppi kehon puolustusmekanismeista infektiota vastaan Immuunijärjestelmä = kudokset, solut ja molekyylit, jotka muodostavat vastustuskyvyn
IMMUUNIPUUTOKSET Olli Vainio Turun yliopisto 130204 IMMUNOLOGIA Oppi kehon puolustusmekanismeista infektiota vastaan Immuunijärjestelmä = kudokset, solut ja molekyylit, jotka muodostavat vastustuskyvyn
Hankittu ja luontainen immuunijärjestelmä
 IMMUUNIJÄRJESTELMÄ Autoimmuunitaudeissa immuunijärjestelmä sekoaa, mutta kuinka immuunijärjestelmä toimii normaalisti. Olen kiinnostunut autoimmuunitautien toimintamekanismeista, mutta monien aihetta käsittelevien
IMMUUNIJÄRJESTELMÄ Autoimmuunitaudeissa immuunijärjestelmä sekoaa, mutta kuinka immuunijärjestelmä toimii normaalisti. Olen kiinnostunut autoimmuunitautien toimintamekanismeista, mutta monien aihetta käsittelevien
Tunnin sisältö. Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS
 Immuunipuolustus Tunnin sisältö Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS Lymfaattinen elinjärjestelmä Muodostuu imukudoksesta imusuonet imusolmukkeet
Immuunipuolustus Tunnin sisältö Immuunijärjestelmä Luonnollinen immuniteetti Hankittu immuniteetti Rokotukset Allergiat HIV / AIDS Lymfaattinen elinjärjestelmä Muodostuu imukudoksesta imusuonet imusolmukkeet
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA Verenkierto toimii elimistön kuljetusjärjestelmänä 6 Avainsanat fibriini fibrinogeeni hiussuoni hyytymistekijät imusuonisto iso verenkierto keuhkoverenkierto laskimo lepovaihe eli
BI4 IHMISEN BIOLOGIA Verenkierto toimii elimistön kuljetusjärjestelmänä 6 Avainsanat fibriini fibrinogeeni hiussuoni hyytymistekijät imusuonisto iso verenkierto keuhkoverenkierto laskimo lepovaihe eli
Immuunijärjestelmän toimintamekanismit
 Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA KESKUS- JA ÄÄREISHERMOSTO SÄÄTELEVÄT ELIMISTÖN TOIMINTAA Elimistön säätely tapahtuu pääasiassa hormonien ja hermoston välityksellä Hermostollinen viestintä on nopeaa ja täsmällistä
BI4 IHMISEN BIOLOGIA KESKUS- JA ÄÄREISHERMOSTO SÄÄTELEVÄT ELIMISTÖN TOIMINTAA Elimistön säätely tapahtuu pääasiassa hormonien ja hermoston välityksellä Hermostollinen viestintä on nopeaa ja täsmällistä
MS-taudissa immuunisolut läpäisevät veri-aivoesteen
 MS-taudissa immuunisolut läpäisevät veri-aivoesteen MS-taudissa immuunisolut läpäisevät veri-aivoesteen. Tutkijat ovat tunnistaneet kaksi mekanismia, joiden avulla lymfosyytit eli valkoiset verisolut läpäisevät
MS-taudissa immuunisolut läpäisevät veri-aivoesteen MS-taudissa immuunisolut läpäisevät veri-aivoesteen. Tutkijat ovat tunnistaneet kaksi mekanismia, joiden avulla lymfosyytit eli valkoiset verisolut läpäisevät
tulehduksellisten suolistosairauksien yhteydessä
 ADACOLUMN -HOITO tulehduksellisten suolistosairauksien yhteydessä www.adacolumn.net SISÄLTÖ Maha-suolikanava...4 Haavainen paksusuolitulehdus...6 Crohnin tauti...8 Elimistön puolustusjärjestelmä ja IBD...10
ADACOLUMN -HOITO tulehduksellisten suolistosairauksien yhteydessä www.adacolumn.net SISÄLTÖ Maha-suolikanava...4 Haavainen paksusuolitulehdus...6 Crohnin tauti...8 Elimistön puolustusjärjestelmä ja IBD...10
Suoliston immuunijärjestelmä ja ruoka-allergia
 OULUN YLIOPISTO, GENETIIKAN JA FYSIOLOGIAN YKSIKKÖ Suoliston immuunijärjestelmä ja ruoka-allergia LuK -tutkielma Matilda Riskumäki 9.12.2016 1. Johdanto... 2 2. Immuunipuolustusjärjestelmä... 3 2.1. Luontainen
OULUN YLIOPISTO, GENETIIKAN JA FYSIOLOGIAN YKSIKKÖ Suoliston immuunijärjestelmä ja ruoka-allergia LuK -tutkielma Matilda Riskumäki 9.12.2016 1. Johdanto... 2 2. Immuunipuolustusjärjestelmä... 3 2.1. Luontainen
Immuunijärjestelmän eri komponentit voidaan jakaa luonnolliseen ja adaptiiviseen immuniteettiin:
 1 IMMUUNIVASTEEN KULKU Petteri Arstila (2011) Immuunijärjestelmän tehtävä on torjua ulkoisia taudinaiheuttajia. Immuunipuolustukseen osallistuu iso joukko erilaisia soluja, jotka kuuluvat elimistön valkosoluihin
1 IMMUUNIVASTEEN KULKU Petteri Arstila (2011) Immuunijärjestelmän tehtävä on torjua ulkoisia taudinaiheuttajia. Immuunipuolustukseen osallistuu iso joukko erilaisia soluja, jotka kuuluvat elimistön valkosoluihin
Tutkijat askelta lähempänä MS-taudin aiheuttajaa
 Tutkijat askelta lähempänä MS-taudin aiheuttajaa Tutkijat ovat askelta lähempänä MS-taudin aiheuttajaa. Exeterin ja Albertan yliopistojen kansainvälinen tutkijaryhmä löysi solujen toimintaan liittyvän
Tutkijat askelta lähempänä MS-taudin aiheuttajaa Tutkijat ovat askelta lähempänä MS-taudin aiheuttajaa. Exeterin ja Albertan yliopistojen kansainvälinen tutkijaryhmä löysi solujen toimintaan liittyvän
Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä. Septinen shokki. Tulehdusreaktio 1/2
 Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä 1/2 Tulehdusreaktio Septinen shokki Tiettyjen bakteeri-infektioiden aikaansaama suunnaton immuunijärjestelmän tulehdusvaste
Tulehdusreaktio (yksinkertaistettu malli) The Immune System Immuunijärjestelmä 1/2 Tulehdusreaktio Septinen shokki Tiettyjen bakteeri-infektioiden aikaansaama suunnaton immuunijärjestelmän tulehdusvaste
Immuunijärjestelmän toimintamekanismit
 Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen (synnynnäinen)
TARTUNTATAUDIT Ellen, Olli, Maria & Elina
 TARTUNTATAUDIT Ellen, Olli, Maria & Elina ELIMISTÖN PUOLUSTUSKYKY Immuniteetti eli vastutuskyky on elimistön kyky suojautua tarttuvilta taudeilta Jos tauteja aiheuttavat mikrobit uhkaavat elimistöä, käynnistyy
TARTUNTATAUDIT Ellen, Olli, Maria & Elina ELIMISTÖN PUOLUSTUSKYKY Immuniteetti eli vastutuskyky on elimistön kyky suojautua tarttuvilta taudeilta Jos tauteja aiheuttavat mikrobit uhkaavat elimistöä, käynnistyy
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA 5 HORMONIT OVAT ELIMISTÖN TOIMINTAA SÄÄTELEVIÄ VIESTIAINEITA Avainsanat aivolisäke hormoni hypotalamus kasvuhormoni kortisoli palautesäätely rasvaliukoinen hormoni reseptori stressi
BI4 IHMISEN BIOLOGIA 5 HORMONIT OVAT ELIMISTÖN TOIMINTAA SÄÄTELEVIÄ VIESTIAINEITA Avainsanat aivolisäke hormoni hypotalamus kasvuhormoni kortisoli palautesäätely rasvaliukoinen hormoni reseptori stressi
Syöpä. Ihmisen keho muodostuu miljardeista soluista. Vaikka. EGF-kasvutekijä. reseptori. tuma. dna
 Ihmisen keho muodostuu miljardeista soluista. Vaikka nämä solut ovat tietyssä mielessä meidän omiamme, ne polveutuvat itsenäisistä yksisoluisista elämänmuodoista, jotka ovat säilyttäneet monia itsenäisen
Ihmisen keho muodostuu miljardeista soluista. Vaikka nämä solut ovat tietyssä mielessä meidän omiamme, ne polveutuvat itsenäisistä yksisoluisista elämänmuodoista, jotka ovat säilyttäneet monia itsenäisen
Tärkeimpien solutyyppien tunnistaminen kudosleikkeissä immunohistokemiallisilla värjäyksillä
 Tärkeimpien solutyyppien tunnistaminen kudosleikkeissä immunohistokemiallisilla värjäyksillä Mikael Niku 28.2.2006 Kuvissa on naudan kudoksia, joita on värjätty immunohistokemialla erilaisia vasta aineita
Tärkeimpien solutyyppien tunnistaminen kudosleikkeissä immunohistokemiallisilla värjäyksillä Mikael Niku 28.2.2006 Kuvissa on naudan kudoksia, joita on värjätty immunohistokemialla erilaisia vasta aineita
IMMUUNIJÄRJESTELMÄN KEHITYS Petteri Arstila (2011)
 1 IMMUUNIJÄRJESTELMÄN KEHITYS Petteri Arstila (2011) Immuunipuolustukseen osallistuvien solujen kehitys jakautuu kahteen päälinjaan, myeloidiseen ja lymfoidiseen, jotka molemmat saavat alkunsa hematopoieettisista
1 IMMUUNIJÄRJESTELMÄN KEHITYS Petteri Arstila (2011) Immuunipuolustukseen osallistuvien solujen kehitys jakautuu kahteen päälinjaan, myeloidiseen ja lymfoidiseen, jotka molemmat saavat alkunsa hematopoieettisista
Narkolepsian immunologiaa ja Pandemrixiin liittyvät tutkimkset
 Narkolepsian immunologiaa ja Pandemrixiin liittyvät tutkimkset Outi Vaarala, Immuunivasteyksikön päällikkö, THL Narkolepsian kulku - autoimmuunihypoteesiin perustuva malli Hypokretiinia Tuottavat neuronit
Narkolepsian immunologiaa ja Pandemrixiin liittyvät tutkimkset Outi Vaarala, Immuunivasteyksikön päällikkö, THL Narkolepsian kulku - autoimmuunihypoteesiin perustuva malli Hypokretiinia Tuottavat neuronit
Etunimi: Henkilötunnus:
 Kokonaispisteet: Lue oheinen artikkeli ja vastaa kysymyksiin 1-25. Huomaa, että artikkelista ei löydy suoraan vastausta kaikkiin kysymyksiin, vaan sinun tulee myös tuntea ja selittää tarkemmin artikkelissa
Kokonaispisteet: Lue oheinen artikkeli ja vastaa kysymyksiin 1-25. Huomaa, että artikkelista ei löydy suoraan vastausta kaikkiin kysymyksiin, vaan sinun tulee myös tuntea ja selittää tarkemmin artikkelissa
22. Ihmiselimistön ulkoiset uhat
 Helena Hohtari Pitkäkurssi I 22. Ihmiselimistön ulkoiset uhat Immuunipuolustus Taudinaiheuttajat Erilaisia mikrobeja: - Bakteerit - Virukset - Sienet - Parasiitit Mikro-organismit elimistölle vieraita,
Helena Hohtari Pitkäkurssi I 22. Ihmiselimistön ulkoiset uhat Immuunipuolustus Taudinaiheuttajat Erilaisia mikrobeja: - Bakteerit - Virukset - Sienet - Parasiitit Mikro-organismit elimistölle vieraita,
LOPPUTENTTI
 Mikrobiologian ja immunologian kurssi 2012-2013 LOPPUTENTTI 22.2.2013 Tehtävä 1. Vastaa lyhyesti alla oleviin kysymyksiin. 1. Luettele vasta-aineiden tehtäviä (4kpl) immuunipuolustuksessa. (2p) 2. HLA
Mikrobiologian ja immunologian kurssi 2012-2013 LOPPUTENTTI 22.2.2013 Tehtävä 1. Vastaa lyhyesti alla oleviin kysymyksiin. 1. Luettele vasta-aineiden tehtäviä (4kpl) immuunipuolustuksessa. (2p) 2. HLA
Päästä varpaisiin. Tehtävät. Ratkaisut. Päivitetty 8.4.2013 ISBN 978-951-37-6416-6, 978-951-37-6417-3, 978-951-6418-0. Sisällys (ratkaisut) Johdanto
 OPETTAJAN AINEISTO Käyttöehdot Päästä varpaisiin Ihmisen anatomia ja fysiologia Eliisa Karhumäki Mari Kärkkäinen (os. Lehtonen) Päivitetty 8.4.2013 ISBN 978-951-37-6416-6, 978-951-37-6417-3, 978-951-6418-0
OPETTAJAN AINEISTO Käyttöehdot Päästä varpaisiin Ihmisen anatomia ja fysiologia Eliisa Karhumäki Mari Kärkkäinen (os. Lehtonen) Päivitetty 8.4.2013 ISBN 978-951-37-6416-6, 978-951-37-6417-3, 978-951-6418-0
Essential Cell Biology
 Alberts Bray Hopkin Johnson Lewis Raff Roberts Walter Essential Cell Biology FOURTH EDITION Chapter 16 Cell Signaling Copyright Garland Science 2014 1 GENERAL PRINCIPLES OF CELL SIGNALING Signals Can Act
Alberts Bray Hopkin Johnson Lewis Raff Roberts Walter Essential Cell Biology FOURTH EDITION Chapter 16 Cell Signaling Copyright Garland Science 2014 1 GENERAL PRINCIPLES OF CELL SIGNALING Signals Can Act
Pienryhmä 3 immuunipuolustus
 Pienryhmä 3 immuunipuolustus 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön valikoivasta
Pienryhmä 3 immuunipuolustus 1. Biologian yo 2013 mukailtu. Merkitse onko väittämä oikein vai väärin, Korjaa väärien väittämien virheet ja perustele korjauksesi. a. Syöjäsolut vastaavat elimistön valikoivasta
Hermosolu tiedonkäsittelyn perusyksikkönä. Muonion lukio Noora Lindgrén
 Hermosolu tiedonkäsittelyn perusyksikkönä Muonion lukio 20.8.2018 Noora Lindgrén Hermosolu perusyksikkönä äärimmäisen monimutkaisessa verkostossa Aivoissa on lähes sata miljardia hermosolua Aivojen toiminta
Hermosolu tiedonkäsittelyn perusyksikkönä Muonion lukio 20.8.2018 Noora Lindgrén Hermosolu perusyksikkönä äärimmäisen monimutkaisessa verkostossa Aivoissa on lähes sata miljardia hermosolua Aivojen toiminta
Biologian tehtävien vastaukset ja selitykset
 Biologian tehtävien vastaukset ja selitykset Ilmainen lääkiksen harjoituspääsykoe, kevät 2017 Tehtävä 2. (20 p) A. 1. EPÄTOSI. Ks. s. 4. Menetelmää käytetään geenitekniikassa geenien muokkaamisessa. 2.
Biologian tehtävien vastaukset ja selitykset Ilmainen lääkiksen harjoituspääsykoe, kevät 2017 Tehtävä 2. (20 p) A. 1. EPÄTOSI. Ks. s. 4. Menetelmää käytetään geenitekniikassa geenien muokkaamisessa. 2.
Vastaa lyhyesti selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
1 1) Tunnista molekyylit (1 piste) ja täytä seuraava taulukko (2 pistettä) a) b) c) d) a) Syklinen AMP (camp) (0.25) b) Beta-karoteeni (0.25 p) c) Sakkaroosi (0.25 p) d) -D-Glukopyranoosi (0.25 p) 2 Taulukko.
Spesifinen immuniteetti - Lymfosyyttityypit. 3. Puolustuslinja (hankittu ja spesifinen immuniteetti) Kahdenlaisia imusoluja (lymfosyyttejä):
 Eläinfysiologia ja histologia Luento X Kitarisat Nielurisat. Puolustuslinja (hankittu ja spesifinen immuniteetti) Spesifinen immuniteetti - Lymfosyyttityypit Lymfosyytti Kahdenlaisia imusoluja (lymfosyyttejä):
Eläinfysiologia ja histologia Luento X Kitarisat Nielurisat. Puolustuslinja (hankittu ja spesifinen immuniteetti) Spesifinen immuniteetti - Lymfosyyttityypit Lymfosyytti Kahdenlaisia imusoluja (lymfosyyttejä):
Käsitteitä. Hormones and the Endocrine System Hormonit ja sisäeritejärjestelmä. Sisäeriterauhanen
 Käsitteitä Hormones and the Endocrine System Hormonit ja sisäeritejärjestelmä 1/2 Umpirauhanen vs. sisäeriterauhanen Endokrinologia Parakriininen Autokriininen Neurotransmitteri Reseptori Sisäeriterauhanen
Käsitteitä Hormones and the Endocrine System Hormonit ja sisäeritejärjestelmä 1/2 Umpirauhanen vs. sisäeriterauhanen Endokrinologia Parakriininen Autokriininen Neurotransmitteri Reseptori Sisäeriterauhanen
POTILAAN OPAS MAVENCLAD. Potilaan opas. Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä
 MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
Reseptoripotentiaalista (RP) aktiopotentiaaliin
 Haju- ja makuaisti Reseptoripotentiaalista (RP) aktiopotentiaaliin Reseptoristimulaatio lokaalinen sähköinen ärtyminen (melkein aina depolarisaatio) RP syntymekanismi vaihtelee aistimesta toiseen RP leviää
Haju- ja makuaisti Reseptoripotentiaalista (RP) aktiopotentiaaliin Reseptoristimulaatio lokaalinen sähköinen ärtyminen (melkein aina depolarisaatio) RP syntymekanismi vaihtelee aistimesta toiseen RP leviää
Hermoimpulssi eli aktiopotentiaali
 Hermoimpulssi eli aktiopotentiaali Piirrä opettajan johdolla kuvat hermoimpulssin etenemisestä 1. KAIKKI solut ovat sähköisesti varautuneita o sähköinen varaus solun sisäpuolella on noin 70 millivolttia
Hermoimpulssi eli aktiopotentiaali Piirrä opettajan johdolla kuvat hermoimpulssin etenemisestä 1. KAIKKI solut ovat sähköisesti varautuneita o sähköinen varaus solun sisäpuolella on noin 70 millivolttia
Komplementtitutkimukset
 Komplementtitutkimukset Hanna Jarva HUSLAB ja Haartman-instituutti Bakteriologian ja immunologian osasto Komplementti osa luontaista immuunijärjestelmää koostuu yli 30 proteiinista aktivoituu kaskadimaisesti
Komplementtitutkimukset Hanna Jarva HUSLAB ja Haartman-instituutti Bakteriologian ja immunologian osasto Komplementti osa luontaista immuunijärjestelmää koostuu yli 30 proteiinista aktivoituu kaskadimaisesti
NEUTROFIILISTEN GRANULOSYYTTIEN KÄYTTÖ TERVEYSHAITAN ARVIOINNISSA. Janne Atosuo FT Biokemian laitos Immunokemia Kliininen tutkimusyksikkö TROSSI 2018
 NEUTROFIILISTEN GRANULOSYYTTIEN KÄYTTÖ TERVEYSHAITAN ARVIOINNISSA FT Biokemian laitos Immunokemia Kliininen tutkimusyksikkö TROSSI 218 NEUTROFIILIT Granylosyyttiset neutrofiilit ovat yleisin valkosolutyyppi
NEUTROFIILISTEN GRANULOSYYTTIEN KÄYTTÖ TERVEYSHAITAN ARVIOINNISSA FT Biokemian laitos Immunokemia Kliininen tutkimusyksikkö TROSSI 218 NEUTROFIILIT Granylosyyttiset neutrofiilit ovat yleisin valkosolutyyppi
Tunnetut endokannabinoidireseptorit
 Endokannabinoidit Historia Tunnetut endokannabinoidireseptorit Esiintyvät deuterostomeilla (nilviäisistä nisäkkäisiin) Tunnistettu kaksi pääasiallista tyyppiä: CB 1 (1990) ja CB 2 (1993), ensimmäisestä
Endokannabinoidit Historia Tunnetut endokannabinoidireseptorit Esiintyvät deuterostomeilla (nilviäisistä nisäkkäisiin) Tunnistettu kaksi pääasiallista tyyppiä: CB 1 (1990) ja CB 2 (1993), ensimmäisestä
Mind Master. Matti Vire 11.5.2013
 Stressi = ympäristön yksilöön kohdistava uhka tai vahingollinen vaikutus sympaattinen hermojärjestelmä ja hypotalamus-aivolisäke-lisämunuainen aktivoituvat Akuutissa stressissä sydämen syke nousee, hengitys
Stressi = ympäristön yksilöön kohdistava uhka tai vahingollinen vaikutus sympaattinen hermojärjestelmä ja hypotalamus-aivolisäke-lisämunuainen aktivoituvat Akuutissa stressissä sydämen syke nousee, hengitys
Meeri Apaja-Sarkkinen. Aineiston jatkokäyttöön tulee saada lupa oikeuksien haltijalta.
 Meeri Apaja-Sarkkinen Aineiston jatkokäyttöön tulee saada lupa oikeuksien haltijalta. HODGKININ LYMFOOMA IAP Tampere 4.-5.5.2006 Dosentti Meeri Apaja-Sarkkinen OYS/Patologian osasto Hodgkinin lymfooma/alatyypit
Meeri Apaja-Sarkkinen Aineiston jatkokäyttöön tulee saada lupa oikeuksien haltijalta. HODGKININ LYMFOOMA IAP Tampere 4.-5.5.2006 Dosentti Meeri Apaja-Sarkkinen OYS/Patologian osasto Hodgkinin lymfooma/alatyypit
Mycobacterium tuberculosis
 Mycobacterium tuberculosis Osoitus immuunireaktioiden perusteella Ilkka Seppälä HUSLAB Immunologian osasto M. tuberculosis immuniteetti Tyypillisesti Th1-immuniteettia -CD4-T-solut dominantissa asemassa
Mycobacterium tuberculosis Osoitus immuunireaktioiden perusteella Ilkka Seppälä HUSLAB Immunologian osasto M. tuberculosis immuniteetti Tyypillisesti Th1-immuniteettia -CD4-T-solut dominantissa asemassa
Autofagia silmänpohjan ikärappeumassa. LT Niko Kivinen Silmälääkäriyhdistys Kevätkoulutuspäivät 2018
 Autofagia silmänpohjan ikärappeumassa LT Niko Kivinen Silmälääkäriyhdistys Kevätkoulutuspäivät 2018 Sidonnaisuudet Apurahat Lääketieteen säätiö Silmäsäätiö Evald ja Hilda Nissin säätiö Itä-Suomen yliopisto
Autofagia silmänpohjan ikärappeumassa LT Niko Kivinen Silmälääkäriyhdistys Kevätkoulutuspäivät 2018 Sidonnaisuudet Apurahat Lääketieteen säätiö Silmäsäätiö Evald ja Hilda Nissin säätiö Itä-Suomen yliopisto
KANSAINVÄLINEN KATSAUS AJANKOHTAISEEN YMPÄRISTÖSAIRAUSTUTKIMUKSEEN
 KANSAINVÄLINEN KATSAUS AJANKOHTAISEEN YMPÄRISTÖSAIRAUSTUTKIMUKSEEN Suomen Ympäristösairauskeskus perustettiin viime vuonna ajantasaisen ympäristösairaustiedon asiantuntijakeskukseksi. Tavoitteena on ajantasaisen,
KANSAINVÄLINEN KATSAUS AJANKOHTAISEEN YMPÄRISTÖSAIRAUSTUTKIMUKSEEN Suomen Ympäristösairauskeskus perustettiin viime vuonna ajantasaisen ympäristösairaustiedon asiantuntijakeskukseksi. Tavoitteena on ajantasaisen,
Ma > GENERAL PRINCIPLES OF CELL SIGNALING
 Ma 5.12. -> GENERAL PRINCIPLES OF CELL SIGNALING Cell-Surface Receptors Relay Extracellular Signals via Intracellular Signaling Pathways Some Intracellular Signaling Proteins Act as Molecular Switches
Ma 5.12. -> GENERAL PRINCIPLES OF CELL SIGNALING Cell-Surface Receptors Relay Extracellular Signals via Intracellular Signaling Pathways Some Intracellular Signaling Proteins Act as Molecular Switches
2.1 Solun rakenne - Lisämateriaalit
 2.1 Solun rakenne - Lisämateriaalit Tiivistelmä Esitumaisiset eli alkeistumalliset solut ovat pieniä (n.1-10µm), niissä on vähän soluelimiä, eikä tumaa (esim. arkeonit, bakteerit) Tumalliset eli aitotumalliset
2.1 Solun rakenne - Lisämateriaalit Tiivistelmä Esitumaisiset eli alkeistumalliset solut ovat pieniä (n.1-10µm), niissä on vähän soluelimiä, eikä tumaa (esim. arkeonit, bakteerit) Tumalliset eli aitotumalliset
Likvorin biomarkkerit. diagnostiikassa. Sanna Kaisa Herukka, FM, LL, FT. Kuopion yliopistollinen sairaala
 Likvorin biomarkkerit neurodegeneratiivisten sairauksien diagnostiikassa Sanna Kaisa Herukka, FM, LL, FT Itä Suomen yliopisto ja Kuopion yliopistollinen sairaala Selkäydinneste Tilavuus n. 150ml, muodostuu
Likvorin biomarkkerit neurodegeneratiivisten sairauksien diagnostiikassa Sanna Kaisa Herukka, FM, LL, FT Itä Suomen yliopisto ja Kuopion yliopistollinen sairaala Selkäydinneste Tilavuus n. 150ml, muodostuu
LYMFOSYTOOSIT SANOIN JA KUVIN. Pentti Mäntymaa TAYS, Laboratoriokeskus
 LYMFOSYTOOSIT SANOIN JA KUVIN Pentti Mäntymaa TAYS, Laboratoriokeskus Lymfosytoosin määritelmä veren lymfosyyttien määrä >3.5 x 10 9 /l lymfosyyttien kohonnut %-osuus erittelyjakaumassa voi johtua joko
LYMFOSYTOOSIT SANOIN JA KUVIN Pentti Mäntymaa TAYS, Laboratoriokeskus Lymfosytoosin määritelmä veren lymfosyyttien määrä >3.5 x 10 9 /l lymfosyyttien kohonnut %-osuus erittelyjakaumassa voi johtua joko
Jaksokirja - oppimistavoi/eet
 Jaksokirja - oppimistavoi/eet Osaa epäillä MS-tautia kliinisen oireiston perusteella Tietää MS-taudin pahenemisvaiheen hoitoperiaatteet Tietää MS-potilaan yleishoidon periaatteet Tietää MS-taudin diagnoosin
Jaksokirja - oppimistavoi/eet Osaa epäillä MS-tautia kliinisen oireiston perusteella Tietää MS-taudin pahenemisvaiheen hoitoperiaatteet Tietää MS-potilaan yleishoidon periaatteet Tietää MS-taudin diagnoosin
Immuunipuutokset. Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008
 Immuunipuutokset Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008 Immuunijärjestelm rjestelmän n toiminta Synnynnäinen immuniteetti (innate) Välitön n vaste (tunneissa)
Immuunipuutokset Olli Vainio OY Diagnostiikan laitos OYS Kliinisen mikrobiologian laboratorio 17.10.2008 Immuunijärjestelm rjestelmän n toiminta Synnynnäinen immuniteetti (innate) Välitön n vaste (tunneissa)
HLA alueen geenit ja niiden funktiot. Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti
 HLA alueen geenit ja niiden funktiot Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti 29.1.2014 Vieras versus oma Immuunijärjestelmä puolustaa elimistöä haitallisia organismeja vastaan
HLA alueen geenit ja niiden funktiot Maisa Lokki, dosentti Transplantaatiolaboratorio Haartman Instituutti 29.1.2014 Vieras versus oma Immuunijärjestelmä puolustaa elimistöä haitallisia organismeja vastaan
Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe Tehtävä 1 Pisteet / 15
 Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Flunssavirus voidaan ohjelmoida infektoimaan vain syöpäsoluja
 Flunssavirus voidaan ohjelmoida infektoimaan vain syöpäsoluja Flunssavirus aseeksi syöpäsoluja vastaan? Tutkijoiden mukaan viruksen pintareseptoria voidaan muuttaa niin, että se tunnistaa pahanlaatuiset
Flunssavirus voidaan ohjelmoida infektoimaan vain syöpäsoluja Flunssavirus aseeksi syöpäsoluja vastaan? Tutkijoiden mukaan viruksen pintareseptoria voidaan muuttaa niin, että se tunnistaa pahanlaatuiset
BOS D 2 -ALLERGEENIN IMMUNODOMINANTISTA T-SOLUEPITOOPISTA JOHDETUN HETEROKLIITTISEN MUUNNELLUN PEPTIDIN MAHDOLLISUUDET ALLERGIAN IMMUNOTERAPIAN
 BOS D 2 -ALLERGEENIN IMMUNODOMINANTISTA T-SOLUEPITOOPISTA JOHDETUN HETEROKLIITTISEN MUUNNELLUN PEPTIDIN MAHDOLLISUUDET ALLERGIAN IMMUNOTERAPIAN TEHOSTAMISEEN Kalle Jutila Opinnäytetutkielma Lääketieteen
BOS D 2 -ALLERGEENIN IMMUNODOMINANTISTA T-SOLUEPITOOPISTA JOHDETUN HETEROKLIITTISEN MUUNNELLUN PEPTIDIN MAHDOLLISUUDET ALLERGIAN IMMUNOTERAPIAN TEHOSTAMISEEN Kalle Jutila Opinnäytetutkielma Lääketieteen
kivunhoito.info Kivun kliininen fysiologia
 Kivun kliininen fysiologia Kliininen kivun fysiologia neurobiologia neurofarmakologia Kivunhoito.info: Kivun kliininen fysiologia 4:1 Kipu on epämiellyttävä sensorinen ja emotionaalinen kokemus, joka liittyy
Kivun kliininen fysiologia Kliininen kivun fysiologia neurobiologia neurofarmakologia Kivunhoito.info: Kivun kliininen fysiologia 4:1 Kipu on epämiellyttävä sensorinen ja emotionaalinen kokemus, joka liittyy
Fysiologiset signaalit ylikuormituksen varhaisessa tunnistamisessa. Harri Lindholm erikoislääkäri Työterveyslaitos
 Fysiologiset signaalit ylikuormituksen varhaisessa tunnistamisessa Harri Lindholm erikoislääkäri Työterveyslaitos Stressin merkitys terveydelle Työelämän fysiologiset stressitekijät Aikapaine Työn vaatimukset
Fysiologiset signaalit ylikuormituksen varhaisessa tunnistamisessa Harri Lindholm erikoislääkäri Työterveyslaitos Stressin merkitys terveydelle Työelämän fysiologiset stressitekijät Aikapaine Työn vaatimukset
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Genetiikan perusteiden toisen jakson kaavailua
 Genetiikan perusteiden toisen jakson kaavailua Tiedämme kaiken siitä, miten geenit siirtyvät sukupolvelta seuraavalle solun ja yksilön tasolla Toisen jakson sisältö: Mitä geenit ovat? Miten geenit toimivat?
Genetiikan perusteiden toisen jakson kaavailua Tiedämme kaiken siitä, miten geenit siirtyvät sukupolvelta seuraavalle solun ja yksilön tasolla Toisen jakson sisältö: Mitä geenit ovat? Miten geenit toimivat?
Aleksi Jokinen, Timo Viljanen & Lassi 81: 1 &82: 4 Ti 3.3.
 Biologian kurssi 4: Ihmisen biologia Laadi monisteen tehtäviä apuna käyttäen selkeä suullinen esitelmä ihmisen elimistä, niiden rakenteista, toiminnan säätelystä ja yleisimmistä toimintahäiriöistä. Aihe:
Biologian kurssi 4: Ihmisen biologia Laadi monisteen tehtäviä apuna käyttäen selkeä suullinen esitelmä ihmisen elimistä, niiden rakenteista, toiminnan säätelystä ja yleisimmistä toimintahäiriöistä. Aihe:
OHJEET SYDÄMEN JA VERISUONIEN TERVEYTEEN. Kuopiolaistutkimus: Sydänperäinen äkkikuolema kaataa myös nuoria ja kovakuntoisia
 OHJEET SYDÄMEN JA VERISUONIEN TERVEYTEEN Kuopiolaistutkimus: Sydänperäinen äkkikuolema kaataa myös nuoria ja kovakuntoisia Kymmenvaiheinen ohjelma sepelvaltimoiden terveyden ylläpitoon luontaishoidoilla
OHJEET SYDÄMEN JA VERISUONIEN TERVEYTEEN Kuopiolaistutkimus: Sydänperäinen äkkikuolema kaataa myös nuoria ja kovakuntoisia Kymmenvaiheinen ohjelma sepelvaltimoiden terveyden ylläpitoon luontaishoidoilla
Neuropeptidit, opiaatit ja niihin liittyvät mekanismit. Pertti Panula Biolääketieteen laitos 2013
 Neuropeptidit, opiaatit ja niihin liittyvät mekanismit Pertti Panula Biolääketieteen laitos 2013 Neuroendokriinisen järjestelmän säätely elimistössä Neuropeptidit Peptidirakenteisia hermovälittäjäaineita
Neuropeptidit, opiaatit ja niihin liittyvät mekanismit Pertti Panula Biolääketieteen laitos 2013 Neuroendokriinisen järjestelmän säätely elimistössä Neuropeptidit Peptidirakenteisia hermovälittäjäaineita
Biologia. Pakolliset kurssit. 1. Eliömaailma (BI1)
 Biologia Pakolliset kurssit 1. Eliömaailma (BI1) tuntee elämän tunnusmerkit ja perusedellytykset sekä tietää, miten elämän ilmiöitä tutkitaan ymmärtää, mitä luonnon monimuotoisuus biosysteemien eri tasoilla
Biologia Pakolliset kurssit 1. Eliömaailma (BI1) tuntee elämän tunnusmerkit ja perusedellytykset sekä tietää, miten elämän ilmiöitä tutkitaan ymmärtää, mitä luonnon monimuotoisuus biosysteemien eri tasoilla
BIOLOGIAN KYSYMYKSET
 BIOLOGIAN KYSYMYKSET Biologian osakokeessa on 10 kysymystä. Tarkista, että saamassasi vastausmonisteessa on sivut 1-10 numerojärjestyksessä. Tarkastajien merkintöjä varten 1 2 3 4 5 6 7 8 9 10 max 80p
BIOLOGIAN KYSYMYKSET Biologian osakokeessa on 10 kysymystä. Tarkista, että saamassasi vastausmonisteessa on sivut 1-10 numerojärjestyksessä. Tarkastajien merkintöjä varten 1 2 3 4 5 6 7 8 9 10 max 80p
Plasmasolukasvaimet (hematologin näkökulmasta) Eeva-Riitta Savolainen LKT, dos Os.ylilääkäri
 Plasmasolukasvaimet (hematologin näkökulmasta) Eeva-Riitta Savolainen LKT, dos Os.ylilääkäri Monoklonaaliset gammapatiat (plasmasolutaudit) Plasmasolumyelooma Merkitykseltään epäselvä monoklonaalinen gammapatia
Plasmasolukasvaimet (hematologin näkökulmasta) Eeva-Riitta Savolainen LKT, dos Os.ylilääkäri Monoklonaaliset gammapatiat (plasmasolutaudit) Plasmasolumyelooma Merkitykseltään epäselvä monoklonaalinen gammapatia
Kysymys 1: Mallivastaus:
 Kysymys 1: Selitä solukalvon rakenne havainnollisesti. Mitä tarkoitetaan aktiivisella kuljetuksella solukalvon läpi, mihin se perustuu ja mihin sitä käytetään solussa? Mallivastaus: Solukalvo on puoliläpäisevä
Kysymys 1: Selitä solukalvon rakenne havainnollisesti. Mitä tarkoitetaan aktiivisella kuljetuksella solukalvon läpi, mihin se perustuu ja mihin sitä käytetään solussa? Mallivastaus: Solukalvo on puoliläpäisevä
Miksi aivot hyötyvät liikunnasta?
 Miksi aivot hyötyvät liikunnasta? 15.11.2011 Oulu Liisa Paavola PsL, neuropsykologian erikoispsykologi Neural Oy Aivot ja fyysinen aktiivisuus Aivojen kehitys on geneettisesti ohjelmoitu muovautumaan vallitseviin
Miksi aivot hyötyvät liikunnasta? 15.11.2011 Oulu Liisa Paavola PsL, neuropsykologian erikoispsykologi Neural Oy Aivot ja fyysinen aktiivisuus Aivojen kehitys on geneettisesti ohjelmoitu muovautumaan vallitseviin
ASEA. Maailman ensimmäinen ja ainoa redoxsignalointimolekyyli valmiste. Mitä ovat redoxsignalointimolekyylit?
 ASEA Maailman ensimmäinen ja ainoa redoxsignalointimolekyyli valmiste Mitä ovat redoxsignalointimolekyylit? Kaikissa kehon soluissa on mitokondrioita, jotka ovat solujen voimanlähde. Mitokondriot erittävät
ASEA Maailman ensimmäinen ja ainoa redoxsignalointimolekyyli valmiste Mitä ovat redoxsignalointimolekyylit? Kaikissa kehon soluissa on mitokondrioita, jotka ovat solujen voimanlähde. Mitokondriot erittävät
VERIRYHMÄT JA VERIRYHMÄVASTA-AINEET
 VERIRYHMÄT JA VERIRYHMÄVASTA-AINEET Raskaudenaikaiset veriryhmäimmunisaatiot 2018 Kati Sulin Biokemisti 12.4.2018 Sisältö Veriryhmät ABO Rh-veriryhmäjärjestelmä Sikiön veriryhmämääritykset äidin verinäytteestä
VERIRYHMÄT JA VERIRYHMÄVASTA-AINEET Raskaudenaikaiset veriryhmäimmunisaatiot 2018 Kati Sulin Biokemisti 12.4.2018 Sisältö Veriryhmät ABO Rh-veriryhmäjärjestelmä Sikiön veriryhmämääritykset äidin verinäytteestä
Yhtäläisyydet selkärankaisten aivoissa, osa II. Niko Lankinen
 Yhtäläisyydet selkärankaisten aivoissa, osa II Niko Lankinen Sisältö Neuroneille tyypilliset molekyylit Suoraa jatkoa Niinan esitykseen Alkion aivojen vertailua Neuromeerinen malli Neuromeerisen mallin
Yhtäläisyydet selkärankaisten aivoissa, osa II Niko Lankinen Sisältö Neuroneille tyypilliset molekyylit Suoraa jatkoa Niinan esitykseen Alkion aivojen vertailua Neuromeerinen malli Neuromeerisen mallin
Lääkkeet muistisairauksissa
 Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
RUOANSULATUS JA SUOLISTON KUNTO. Iida Elomaa & Hanna-Kaisa Virtanen
 RUOANSULATUS JA SUOLISTON KUNTO Iida Elomaa & Hanna-Kaisa Virtanen Edellisen leirin Kotitehtävä Tarkkaile sokerin käyttöäsi kolmen päivän ajalta ja merkkaa kaikki sokeria ja piilosokeria sisältävät ruuat
RUOANSULATUS JA SUOLISTON KUNTO Iida Elomaa & Hanna-Kaisa Virtanen Edellisen leirin Kotitehtävä Tarkkaile sokerin käyttöäsi kolmen päivän ajalta ja merkkaa kaikki sokeria ja piilosokeria sisältävät ruuat
Diabetes. Iida, Sofia ja Vilma
 Diabetes Iida, Sofia ja Vilma Diabetes Monia aineenvaihduntasairauksia, joissa veren sokeripitoisuus kohoaa liian korkeaksi Useimmiten syynä on haiman erittämän insuliinihormonin vähäisyys tai sen puuttuminen
Diabetes Iida, Sofia ja Vilma Diabetes Monia aineenvaihduntasairauksia, joissa veren sokeripitoisuus kohoaa liian korkeaksi Useimmiten syynä on haiman erittämän insuliinihormonin vähäisyys tai sen puuttuminen
Kuva 1. Utaretulehdustilanteen kehitys 1975-2001.
 Utareterveyskampanja 2009-2010 Laura Kulkas Utaretulehdusten synty- ja paranemismekanismit Utaretulehdus on tavallisin ja kallein tarttuva tauti lypsykarjoissamme Tavallisimmat utaretulehdusbakteerit ovat
Utareterveyskampanja 2009-2010 Laura Kulkas Utaretulehdusten synty- ja paranemismekanismit Utaretulehdus on tavallisin ja kallein tarttuva tauti lypsykarjoissamme Tavallisimmat utaretulehdusbakteerit ovat
SELKÄYDINNESTEEN PERUSTUTKIMUKSET
 Käyttöönottopäivä: 21.11.2011 1 (5) SELKÄYDINNESTEEN PERUSTUTKIMUKSET Atk-numero ja -lyhenne 1154 Li-BaktVi 1470 Li-Gluk 2186 Li-Laktaat 2514 Li-Prot 2655 Li-Solut 4059 Li-Syto Likvorin irtosolututkimus
Käyttöönottopäivä: 21.11.2011 1 (5) SELKÄYDINNESTEEN PERUSTUTKIMUKSET Atk-numero ja -lyhenne 1154 Li-BaktVi 1470 Li-Gluk 2186 Li-Laktaat 2514 Li-Prot 2655 Li-Solut 4059 Li-Syto Likvorin irtosolututkimus
HUSLAB Immunologian osasto Labquality-päivät Vasta-aineet
 Ilkk S älä Ilkka Seppälä HUSLAB Immunologian osasto Labquality-päivät 2010 Vasta-aineet Fab Fab Fc IgG, IgD J IgA IgE J IgM IgM:n monomeeriyksikkö ja IgD ovat käytössä B-lymfosyyttien yy antigeenia tunnistavina
Ilkk S älä Ilkka Seppälä HUSLAB Immunologian osasto Labquality-päivät 2010 Vasta-aineet Fab Fab Fc IgG, IgD J IgA IgE J IgM IgM:n monomeeriyksikkö ja IgD ovat käytössä B-lymfosyyttien yy antigeenia tunnistavina
NOPEAKASVUISET B SOLUB NON HODGKIN LYMFOOMAT. Tampere 4. 5. 2006 derström
 NOPEAKASVUISET B SOLUB NON HODGKIN LYMFOOMAT Tampere 4. 5. 2006 Karl Ove SöderstrS derström B solujen erilaistuminen Nopeakasvuiset B solub lymfoomat Diffuusi suurisoluinen B solub lymfooma Manttelisolu
NOPEAKASVUISET B SOLUB NON HODGKIN LYMFOOMAT Tampere 4. 5. 2006 Karl Ove SöderstrS derström B solujen erilaistuminen Nopeakasvuiset B solub lymfoomat Diffuusi suurisoluinen B solub lymfooma Manttelisolu
Pfapa Eli Jaksoittainen Kuume, Johon Liittyy Aftainen Nielu- Ja Imusolmuketulehdus
 https://www.printo.it/pediatric-rheumatology/fi/intro Pfapa Eli Jaksoittainen Kuume, Johon Liittyy Aftainen Nielu- Ja Imusolmuketulehdus Versio 2016 1. MIKÄ ON PFAPA? 1.1 Mikä se on? PFAPA on lyhenne englannin
https://www.printo.it/pediatric-rheumatology/fi/intro Pfapa Eli Jaksoittainen Kuume, Johon Liittyy Aftainen Nielu- Ja Imusolmuketulehdus Versio 2016 1. MIKÄ ON PFAPA? 1.1 Mikä se on? PFAPA on lyhenne englannin
Immuunijärjestelmän toimintamekanismit
 Ravinto & Terveys Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen
Ravinto & Terveys Immuunijärjestelmän toimintamekanismit Immuunipuolustus rakentuu kahden toisiaan täydentävän immuunijärjestelmän varaan. Nämä ovat adaptiivinen eli hankittu immuunijärjestelmä ja luontainen
Kotitehtävä. Ruokapäiväkirja kolmelta vuorokaudelta (normi reenipäivä, lepopäivä, kisapäivä) Huomioita, havaintoja?
 Kotitehtävä Ruokapäiväkirja kolmelta vuorokaudelta (normi reenipäivä, lepopäivä, kisapäivä) Huomioita, havaintoja? VÄLIPALA Tehtävä Sinun koulupäiväsi on venähtänyt pitkäksi etkä ehdi ennen illan harjoituksia
Kotitehtävä Ruokapäiväkirja kolmelta vuorokaudelta (normi reenipäivä, lepopäivä, kisapäivä) Huomioita, havaintoja? VÄLIPALA Tehtävä Sinun koulupäiväsi on venähtänyt pitkäksi etkä ehdi ennen illan harjoituksia
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
Teabepäeva korraldamist toetab Euroopa Liit Eesti riikliku mesindusprogrammi 2013 2016 raames
 Teabepäeva korraldamist toetab Euroopa Liit Eesti riikliku mesindusprogrammi 2013 2016 raames Eesti mesinike suvine teabepäev Koht ja aeg: Olustvere Teenindus- ja Maamajanduskooli ruumides, 11.07.2015.a.
Teabepäeva korraldamist toetab Euroopa Liit Eesti riikliku mesindusprogrammi 2013 2016 raames Eesti mesinike suvine teabepäev Koht ja aeg: Olustvere Teenindus- ja Maamajanduskooli ruumides, 11.07.2015.a.
Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress
 Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress Twan Lammers, Fabian Kiessling, Wim E. Hennik, Gert Storm Journal of Controlled Release 161: 175-187, 2012 Sampo Kurvonen 9.11.2017
Drug targeting to tumors: Principles, pitfalls and (pre-) cilinical progress Twan Lammers, Fabian Kiessling, Wim E. Hennik, Gert Storm Journal of Controlled Release 161: 175-187, 2012 Sampo Kurvonen 9.11.2017
Hermoston toiminnallinen jako
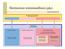 Hermoston toiminnallinen jako Autonominen hermosto ylläpitää homeostasiaa Hypotalamus, aivosilta ja ydinjatke päävastuussa homeostaasin säätelystä Aivojen autonomiset säätelykeskukset Hypotalamus Vesitasapaino,
Hermoston toiminnallinen jako Autonominen hermosto ylläpitää homeostasiaa Hypotalamus, aivosilta ja ydinjatke päävastuussa homeostaasin säätelystä Aivojen autonomiset säätelykeskukset Hypotalamus Vesitasapaino,
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA LAPSUUS ON VOIMAKKAAN KASVUN JA KEHITYKSEN AIKAA Pitkän lapsuusajan uskotaan vähentävän lapsikuolleisuutta. Lapsuus on pitkä ajanjakso ihmisen elämässä. Se on yhteydessä aivojen kehittymiseen
BI4 IHMISEN BIOLOGIA LAPSUUS ON VOIMAKKAAN KASVUN JA KEHITYKSEN AIKAA Pitkän lapsuusajan uskotaan vähentävän lapsikuolleisuutta. Lapsuus on pitkä ajanjakso ihmisen elämässä. Se on yhteydessä aivojen kehittymiseen
Neuronifysiologia 2. Jänniteherkät ionikanavat
 Neuronifysiologia 2 Jänniteherkät ionikanavat Jänniteherkät ionikanavat Tyyppi Na + kanavat K + kanavat Ca 2+ kanavat Merkitys aktiopotentiali aktiopotentiali inhibiitio transmitteri vapautuminen plastisiteetti
Neuronifysiologia 2 Jänniteherkät ionikanavat Jänniteherkät ionikanavat Tyyppi Na + kanavat K + kanavat Ca 2+ kanavat Merkitys aktiopotentiali aktiopotentiali inhibiitio transmitteri vapautuminen plastisiteetti
SSLY Kortisoni. Heikki Saaren-Seppälä, HYKS
 SSLY Kortisoni Heikki Saaren-Seppälä, HYKS 23.3.2017 Mitä se sellainen kortisoni ihan oikeesti on?? Stressireaktion säätelijä Mitä se stressi ihan tarkalleen ottaen sitten on?? Ei vain hetkellinen fyysinen
SSLY Kortisoni Heikki Saaren-Seppälä, HYKS 23.3.2017 Mitä se sellainen kortisoni ihan oikeesti on?? Stressireaktion säätelijä Mitä se stressi ihan tarkalleen ottaen sitten on?? Ei vain hetkellinen fyysinen
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia)
 ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
Laserin käyttö eläinlääkinnässä
 Laserin käyttö eläinlääkinnässä Syyskoulutuspäivät Turussa 6.-7.10.2017 MAOL-Turku ry ELL Jouni Niemi Vetman Oy LASER Light Amplification by Stimulated Emission of Radiation MITEN DIODILASERIN VALO ON
Laserin käyttö eläinlääkinnässä Syyskoulutuspäivät Turussa 6.-7.10.2017 MAOL-Turku ry ELL Jouni Niemi Vetman Oy LASER Light Amplification by Stimulated Emission of Radiation MITEN DIODILASERIN VALO ON
Adacolumn -hoito tulehduksellisten suolistosairauksien yhteydessä
 Adacolumn -hoito tulehduksellisten suolistosairauksien yhteydessä Hellävarainen vallankumous IBD-tautien hoidossa Sisältö Maha-suolikanava...4 Haavainen paksusuolitulehdus...6 Crohnin tauti...8 Elimistön
Adacolumn -hoito tulehduksellisten suolistosairauksien yhteydessä Hellävarainen vallankumous IBD-tautien hoidossa Sisältö Maha-suolikanava...4 Haavainen paksusuolitulehdus...6 Crohnin tauti...8 Elimistön
KEESHONDIEN MONIMUOTOISUUSKARTOITUS
 KEESHONDIEN MONIMUOTOISUUSKARTOITUS 2 3. 0 1. 2 0 1 1 K A A R I N A Marjut Ritala DNA-diagnostiikkapalveluja kotieläimille ja lemmikeille Polveutumismääritykset Geenitestit Serologiset testit Kissat, koirat,
KEESHONDIEN MONIMUOTOISUUSKARTOITUS 2 3. 0 1. 2 0 1 1 K A A R I N A Marjut Ritala DNA-diagnostiikkapalveluja kotieläimille ja lemmikeille Polveutumismääritykset Geenitestit Serologiset testit Kissat, koirat,
