VI TILANYHTÄLÖ
|
|
|
- Noora Hiltunen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 VI TILANYHTÄLÖ Ideaalikaasun tilanyhtälö Van der Waalsin tilanyhtälö Semiempiirinen lähestymistapa Van der Waalsin kaasun ominaisuuksia: Van der Waalsin kaasun kriittiset parametrit Van der Waalsin kaasu ja faasimuutokset Tilanyhtälön viriaalikehitelmä Kaasun ja kiinteän aineen tilavuudenmuutokset Kaasut Kiinteä aine FLT-systeemi FLT-systeemin tilanyhtälö Tilavuuden lämpötilakerroin Jännityksen muutokseen liittyvä työ...167
2 150 VI Tilanyhtälö VI Tilanyhtälö 6.1 Ideaalikaasun tilanyhtälö Makroskooppisen systeemin termodynaaminen tila on yksikäsitteisesti määrätty, jos tunnemme riittävän monen (yleensä muutaman) systeemille ominaisten tilanmuuttujan arvot. Termodynaamisen tilan määrääminen on mahdollista vain sisäisessä termodynaamisessa tasapainossa olevalle systeemille. Kaasulle ja nesteille tilanmuuttujia ovat paine p, tilavuus V ja lämpötila T. Avoimelle systeemille voimme pitää myös systeemin ainemäärää (ν ) tilanmuuttujana. Tilanmuuttujia sitoo toisiinsa tilanyhtälö, jonka voimme esittää muodossa f( p, V, T, N ) = 0. (6.1) Erityistapauksissa tarvitaan näiden suureiden lisäksi systeemin tilan kuvaamiseen muitakin tilanmuuttujia kuten magnetoituma, varaustiheys, kemiallinen koostumus jne. Seuraavassa rajoitumme systeemeihin, joita voidaan kuvata tilanmuuttujien pv,, Tja N avulla. Kaasun tilanyhtälö voidaan esittää siten, että se kuvaa kaasun tilaa ainemäärän yksikköä kohden. Tällöin käytämme kaasun tilavuuden sijaan moolia kohden laskettua tilavuutta V = V / ν. m Olemme käsitelleet ideaalikaasun tilanyhtälöä termodynaamisen lämpötilan määrittelyn yhteydessä. Ideaalikaasun termodynaaminen lämpötila voidaan määritellä myös Boylen lain avulla. Moolitilavuuden avulla lausuttuna voimme kirjoittaa Boylen lain muotoon Kuva 6-1 Ideaalikaasun paine tilavuuden ja lämpötilan funktiona.
3 6. Van der Waalsin tilanyhtälö 151 pv m R T =.. (6.) Korkeissa paineissa kaasujen käyttäytyminen poikkeaa oleellisesti Boylen laista, mutta lämpötilasta ja kaasusta riippumatta lähestytään paineen alentuessa yhtälöä 6.. Yhtälön 6. perusteella voimme ymmärtää paineen tilavuuden ja lämpötilan funktioksi. Paine voidaan esittää pintana muuttujien p ja V määräämässä avaruudessa. Kuvassa 6.1 on esitetty ideaalikaasun paine lämpötilan ja tilavuuden funktiona. Käyriä, jotka kuvaavat paineen muutosta tilavuuden funktiona, kutsutaan isotermeiksi (yhtenäinen viiva). Paineen muutosta tilavuuden ollessa vakio kuvaa suora, jota kutsutaan isokooriksi (katkoviiva) ja lämpötilan muutosta paineen olleessa vakio suora, jota kutsutaan isobaariksi (pistekatkoviiva). Sellaisia kaasun tilanmuutoksia, joissa jokin näistä tilanmuuttujista on vakio, kutsutaan vastaavasti isotermisiksi, isobaarisiksi ja isokoorisiksi prosesseiksi. 6. Van der Waalsin tilanyhtälö 6..1 Semiempiirinen lähestymistapa Kuva 6- Molekyylien välinen vuorovaikutus reaalikaasuissa. Heikko attraktiivinen vuorovaikutus etäisyyksillä r1 > r0 ja voimakas hylkivä voima, kun r1 < r0. Olemme tarkastelleet keskenään vuorovaikuttavien molekyylien muodostaman kaasun tilastollista mekaniikkaa luvussa 3.1. Tilastollisessa mekaniikassa molekyylien välinen vuorovaikutus on tunnettava molekyylien välisen etäisyyden funktiona, jotta voimme laskea potentiaalienergiasta aiheutuvan muutoksen partitiofunktioon ja siitä johdettavaan tilanyhtälöön. Makroskooppisessa termodynamiikassa molekyylien välinen vuorovaikutus otetaan huomioon semiempiirisen tarkastelun kautta. Lähtökohtana on verrata reaalikaasujen ja ideaalikaasun ominaisuuksien eroja ja löytää sellainen tilanyhtälön
4 15 VI Tilanyhtälö yleistys, joka voisi mahdollisimman vähin parametrein kuvata ainakin karkeasti reaalikaasuja. Verrattaessa ideaalikaasun ja reaalikaasun ominaisuuksia huomataan, että kaasun lämpötilan laskiessa ja (tai) tiheyden kasvaessa kaasumolekyylien välisten vuorovaikutusten merkitys kasvaa. Kokeelliset havainnot voidaan tiivistää seuraaviin kahteen tulokseen: 1. Korkeissa lämpötiloissa tiheyden kasvaessa kaasun paine on korkeampi, kuin ideaalikaasun tilanyhtälön antama arvo.. Matalissa lämpötiloissa reaalikaasun paine on vastaavasti alempi kuin ideaalikaasun. Nämä poikkeamat ideaalikaasun käyttäytymisestä voidaan ymmärtää molekyylien välisen vuorovaikutuspotentiaalin perusteella seuraavasti: 1. Paineen nousu korkeissa lämpötiloissa Korkeissa lämpötiloissa heikon attraktiivisen potentiaalin vaikutus on vähäinen. Tämä johtuu siitä, että molekyylien translaatioliikkeen energian kasvaessa heikot van der Waalsin voimat molekyylien välillä eivät vaikuta merkittävästi vaikuttaa molekyylien liiketilaan. Suurillakaan nopeuksilla molekyylit eivät voi kuitenkaan tunkeutua toistensa sisään, sillä tämä edellyttää tiukasti sidottujen kuorielektronien uudelleenjärjestäytymistä, mistä aiheutuu erittäin voimakas hylkivä sähköstaattinen voima. Oletamme siis, että molekyylien välisen etäisyyden tullessa pienemmäksi kuin kaksi kertaa molekyylien säde vuorovaikutuksen potentiaalienergia kasvaa liki äärettömäksi E, kun r < r, p1 1 0 missä r 0 on molekyylien säde. Koska molekyylit eivät voi tunkeutua toistensa sisään, niiden näkemä efektiivinen tilavuus on tosiasiassa pienempi kuin kaasusäiliön tilavuus V. Johdamme nyt arvion efektiivisen tilavuuden pienenemiselle.
5 6. Van der Waalsin tilanyhtälö Jos molekyyli oletetaan pallomaiseksi, sen tilavuus on (4/3) π r 0 ja 3 molekyylien yhteinen tilavuus on N(4/3) π r. Molekyylien vaatima efektiivinen tilavuus on kuitenkin huomattavasti suurempi, sillä yksittäinen molekyyli rajaa massakeskipisteensä ympärille r 0 säteisen pallomaisen tilan, jonka sisällä toisen molekyylien massakeskipiste ei voi sijaita. Näin laskien saisimme molekyylien yhteiseksi efektiiviseksi tilavuudeksi 3 8 N(4/3) π r0. Tästä on kuitenkin puolet liikaa, sillä massakeskipisteen sijainnin estävä säteeltään r 0 suuruisen pallon tilavuus voidaan varata vain joka toiselle molekyylille. Tämän huomaa helposti tutkimalla esimerkiksi kahden molekyylin systeemiä. Molekyylien yhteinen efektiivinen tilavuus on siis Nb, missä b on yhden molekyylin efektiivinen tilavuus ja suuruudeltaan b = 4 π r0. (6.3) 3 Tällöin kaasusäiliön efektiivinen tilavuus on V Nb (6.4) ja ideaalikaasun tilanyhtälöstä saadaan NkT p =. (6.5) V Nb Tilanyhtälö 6.5 ottaa huomioon molekyylien äärellisestä tilavuudesta johtuvan paineen kasvun, muttei molekyylien välistä vetovoimaa suurilla etäisyyksillä, joten ideaalikaasun tilanyhtälöä on vielä muutettava jälkimmäisen ilmiön huomioonottamiseksi.. Paineen lasku matalissa lämpötiloissa Lämpötilan laskiessa ja tiheyden kasvaessa kaasumolekyylien väliset pitkän kantaman van der Waalsin vetovoimat vaikuttavat yhä enemmän molekyylien liikkeeseen. Kvalitatiivisesti voidaan ajatella, että molekyylien tullessa lähelle toisiaan, ne vetovoiman ansiosta viipyvät mielellään toistensa läheisyydessä. Tänä aikana ne eivät voi törmätä astian seinään. Paine siis laskee.
6 154 VI Tilanyhtälö Kokeellisesti on havaittu, että paineen pieneneminen on muotoa N p = a V, (6.6) missä a on molekyylien välisen vetovoiman voimakkuutta kuvaava parametri. Sijoittamalla tämä termi tilanyhtälöön 6.5 voimme esittää tilanyhtälön muodossa NkT N p = a V Nb V. (6.7) Parametrejä a ja b kutsutaan van der Waalsin vakioiksi. Yhtälö 6.7 tunnetaan van der Waalsin tilanyhtälönä. Se kirjoitetaan usein muodossa N p+ a ( V Nb) = knt. (6.8) V Van der Waalsin tilanyhtälö on varsin karkea approksimaatio, mutta sen avulla voidaan kuitenkin ymmärtää useita sellaisia reaalikaasujen ominaisuuksia, joiden olemassaoloa ideaalikaasun tilanyhtälö ei lainkaan pysty ennustamaan. 6.. Van der Waalsin kaasun ominaisuuksia: Kuvassa 6.3 a) on esitetty van der Waalsin tilanyhtälön isotermejä. Kuvassa 6.3 b) on lisäksi verrattu van der Waalsin kaasun ja ideaalikaasun isotermejä kriittisen lämpötilan yläpuolella T > TC. Kuvasta voidaan tehdä seuraavia havaintoja: 1. Korkeissa lämpötiloissa ( T >> TC ) reaalikaasun ja ideaalikaasun isotermit muistuttavat läheisesti toisiaan. Paineen kasvaessa reaalikaasun paineen asymptoottina on suora V=Nb. Ideaalikaasun asymptoottina on vastaavasti suora V = 0. Korkeissa lämpötiloissa reaalikaasun paine on aina korkeampi kuin ideaalikaasun. Tiheyden pienentyessä van der Waalsin kaasun käyttäytyminen lähenee ideaalikaasun käyttäytymistä kaikissa lämpötiloissa.
7 6. Van der Waalsin tilanyhtälö Matalissa lämpötiloissa tilavuuden pienentyessä molekyylien väliset vetovoimat pienentävät aluksi painetta ideaalikaasuun verrattuna. Tilavuuden pienentyessä edelleen reaalikaasun paine tulee kuitenkin suuremmaksi, sillä van der Waalsin kaasulle paine tulee äärettömäksi kun V=Nb. Kuvasta a) havaitaan lisäksi, että kriittisen lämpötilan alapuolella van der Waalsin kaasun käyttäytyminen poikkeaa täysin ideaalikaasun käyttäytymisestä. Tämä alue liittyy nestekaasu-faasimuutokseen Van der Waalsin kaasun kriittiset parametrit Tarkastellaan lähemmin isotermiä T C kuvassa 6-3. Se poikkeaa korkeampiin lämpötiloihin liittyvistä isotermeistä siinä, että kriittisessä pisteessä E ( pc, VC, T C ) p V T = 0 ja p V T = 0 (6.9) ts. paineella on kriittisessä pisteessä sekä lokaali toispuoleinen maksimi että käännepiste. Kriittinen piste on mielenkiintoinen, koska tilavuuden differentiaalinen pieneneminen ei tässä pisteessä enää johda paineen kasvuun. Kuva 6-3 a) Van der Waalsin kaasun isotermejä. Katkoviivalla merkitty alue kuvaa neste-kaasu faasimuutosten esiintymistä kriittisen lämpötilan T C alapuolella. b) Van der Waalsin kaasun ja ideaalikaasun isotermien vertailu (kvalitatiivinen) kriittisen lämpötilan yläpuolella. Derivoidaan van der Waalsin yhtälö tilavuuden suhteen
8 156 VI Tilanyhtälö p NkT N = + a = 0. (6.10) V 3 T ( V Nb ) V Käännepisteelle pätee lisäksi p NkT N = 6a = 0. (6.11) 3 4 V T ( V Nb) V Näistä yhtälöistä saamme yhtälöparin NkT N = a 3 ( V Nb ) V. NkT N = 6a 3 V 4 ( V Nb ) Jakamalla puolittain saadaan kriittinen tilavuus VC = 3Nb. (6.1) Sijoittamalla tämä yhtälöön 6.10 saadaan kriittinen lämpötila T C 8 a =. (6.13) 7 bk Sijoittamalla kriittinen tilavuus ja lämpötila tilanyhtälöön 6.7 saadaan kriittinen paine p C 1 a = (6.14) 7 b C C Huomaa, että kriittinen piste määräytyy yksinomaan parametrien a ja b arvojen perusteella. Vaikka vakiot a ja b voidaan aina valita siten, että kriittisen isotermin lokaali maksimi ja käännepiste vastaavat kokeellisesti havaittuja arvoja V ja T ei tämä vielä takaa, että van der Waalsin tilanyhtälön antama paine olisi sama kuin kokeellisesti havaittu paine. Yleisesti taulukoituja van der Waalsin parametrejä ei ole optimoitu antamaan tarkkaa kuvausta reaalikaasun käyttäytymisestä kriittisen pisteen läheisyydessä vaan alueelle, jossa molekyylien väliset vuorovaikutukset edustavat pientä korjausta ideaalikaasun tilanyhtälöön.
9 6. Van der Waalsin tilanyhtälö 157 Esimerkki 6.1. Määrätään van der Waalsin vakiot kriittisen tilavuuden ja lämpötilan avulla, sijoitetaan näin saadut arvot tilanyhtälöön ja lasketaan paine. Taulukosta 6.1 ja yhtälöistä 6.1 ja 6.13 saadaan hapelle 9 3 b= VC /3NA = m /molek a T Pa m /molek 8 C = bk =. Kun nämä sijoitetaan van der Waalsin tilanyhtälöön, saadaan kriittiseksi paineeksi 5 p C = Pa, 5 mikä poikkeaa huomattavasti taulukon arvosta 50,8 10 Pa. Van der Waalsin tilanyhtälön tarkkuus on siis rajallinen, mutta riittää faasimuutosten kvalitatiiviseen tarkasteluun. Tilanyhtälö on tietenkin huomattavasti tarkempi lähellä normaaliolosuhteita. Tämä johtuu siitä, että kriittinen piste on neste-kaasu-faasimuutoksen raja-alueella, jossa systeemin käyttäytyminen on hyvin herkkä molekyylien välisen vuorovaikutuksen yksityiskohdille. Van der Waalsin tilanyhtälö perustuu malliin, jossa molekyylien välinen vuorovaikutus on vain "pieni korjaus" ideaalikaasun tilanyhtälöön. Kertaa tilastollisen mekaniikan tarkastelu reaalikaasuista luvussa III. Taulukko 6.1 Eräiden kaasujen kokeellisesti määrätyt kriittiset parametrit Kaasu T C [ K] 5 p C 10 Pa V 10 m mol C Helium Vety Happi Vesi Van der Waalsin kaasu ja faasimuutokset Kriittisen lämpötilan alapuolella on kullakin isotermillä sellainen tilavuusakselin väli, jolla paine on vakio tai pienenee tilavuuden pienentyessä. Tämä käyttäytyminen on yhteydessä neste-kaasu faasimuutokseen. Tilanmuutos alkaa tilavuuden pienentyessä ja isotermin leikatessa kuvaan katkoviivalla merkityn alueen (kuva 6.3a). Tarkastellaan lähemmin isotermiä T. Välillä AB kaasun tilavuus pienenee ja paine kasvaa. Välillä BC van der Waalsin tilanyhtälöstä laskettu paine käyttäytyy pisteviivan mukaisesti. Havaitaan, että osalla välistä paine pie-
10 158 VI Tilanyhtälö nenee tilavuuden pienentyessä. Todellisuudessa paine välillä BC on vakio ja tällä välillä tapahtuu faasimuutos - tilavuus pienenee paineen ja lämpötilan ollessa vakioita, kunnes kaasu on kokonaisuudessaan tiivistynyt nesteeksi. Todellista kokeellisesti havaittavaa painetta kuvaa yhtenäinen viiva BC. Tämä viivan sijainti määrätään siten, että sen ja pisteviivan ylä- ja alapuolelle jäävien alueiden pinta-alat ovat yhtä suuret. Palaamme perusteluihin faasimuutoksia koskevassa luvussa. Välillä CD paine kasvaa rajusti, koska nestefaasin kokoonpuristuvuus on erittäin pieni. Kaasun todellinen paine ei tällä osavälillä noudata edes kvalitatiivisesti van der Waalsin tilanyhtälöä Tilanyhtälön viriaalikehitelmä Kaasun tilanyhtälön viriaalikehitelmällä tarkoitetaan kaasun paineen esittämistä tiheyden sarjakehitelmänä (Rudolf Clausius ) knt N N p = 1 + A( T) + B( T) +... V V V (6.15) Kertoimia A, B,.. yhtälössä kutsutaan viriaalikertoimiksi. Huomataan, että ideaalikaasun tilanyhtälölle A= B =... = 0 kaikissa lämpötiloissa. Reaalikaasut muistuttavat ideaalikaasua erityisesti tarkasti siinä lämpötilassa, jossa AT ( ) = 0, sillä sarja on nopeasti suppeneva, jos tiheys (N/V) on pieni. Tätä lämpötilaa kutsutaan Boylen lämpötilaksi ja merkitään T B. Esimerkki 6.. Van der Waalsin kaasun viriaalikehitelmä Yhtälöstä 6.7 saadaan: knt 1 1 bn p a N = V V V (6.16) Binomikehitelmän 1 (1 + x) = 1 x+ x... avulla saadaan 3 3 knt bn b N b N knt an p = V V 3 V V V ktv, (6.17)
11 6.3 Kaasun ja kiinteän aineen tilavuudenmuutokset 159 missä yhtälön jälkimmäistä termiä on järjestelty uudelleen. Ryhmittelemällä termit ja ottamalla yhteiset tekijät saamme knt a N N p = 1 + b + b +... V kt V V. (6.18) Van der Waalsin kaasun ensimmäinen ja toinen viriaalikerroin ovat siis a AT ( ) b ja BT ( ) b kt = = (6.19) Taulukossa 6. on annettu van der Waalsin vakioiden arvot molekyyliä kohden. van der Waalsin tilanyhtälö voidaan kirjoittaa moolimäärien avulla, ts. p ν 1 RT b 1 ν a ν = V V V. (6.0) Yhtälössä esiintyvät pilkutetut van der Waalsin vakiot ovat b = bn. A A a = N a ja Taulukko 6. Van der Waalsin kertoimia ja Boylen lämpötiloja T B. Kaasu 6 a Pa m /molek. b 3 m /molek. He (yksiatominen) Ar " Xe " Hg " T B [ K/molek. ] H (kaksiatominen) O Cl
12 160 VI Tilanyhtälö 6.3 Kaasun ja kiinteän aineen tilavuudenmuutokset Kaasut Kuva 6-4 Kaasun tilavuuden muutos paineen ja lämpötilan differentiaalisessa muutoksessa. Ratkaisemalla kaasun tilanyhtälö tilavuuden suhteen voidaan tilavuus esittää riippumattomien tilanmuuttujien T ja p funktiona. Kuva 6.4 esittää kvalitatiivisesti ideaalikaasun tilavuutta muuttujien p ja T funktiona. Tilavuus voidaan esittää paineen ja lämpötilan funktiona myös reaalikaasuille. Yleisessä tapauksessa ei tilanyhtälön ratkaiseminen tilavuuden suhteen ole analyyttisesti mahdollista, mutta silloinkin voidaan seuraavat tarkastelut tehdä numeerisesti ja kaasua kuvaaville suureille, kuten lämpölaajenemiskerroin ja kokoonpuristuvuus, voidaan laskea numeroarvot. Seuraavassa lienee havainnollisuuden vuoksi helpointa olettaa, että tilavuus voidaan esittää paineen ja lämpötilan analyyttisesti tunnettuna funktiona. Tarkastelemme nyt kaasun tilavuuden muutosta tilanmuutoksessa 1. Tällä välillä lämpötila saa Kuva 6-5 Tilavuuden muutos kuvan 6.4 pienen lisäyksen T = T T1. Jos välillä 1Æ painetta pidetään vakiona ja lämpötilan muutos T 0, huomaamme kuvasta 6.5., että kaasun tilavuuden muutos lähestyy rajatta arvoa
13 6.3 Kaasun ja kiinteän aineen tilavuudenmuutokset 161 missä V V V1 = V = T, (6.1) T V T p on funktion V isobaarille pisteeseen 1 piirretyn tangentin p kulmakerroin. Tangentin suunta lähestyy rajatta pisteitä 1 ja yhdistävän suoran suuntaa, jolloin tangentin kulmakerroin lähestyy arvoa V / T. Tätä kerrointa kutsutaan funktion V osittaisderivaataksi lämpötilan suhteen vakiopaineessa. Jos lämpötilan muutos on differentiaalisen (äärettömän) pieni, on yhtälö 6.1 tapana kirjoittaa muodossa V dv = T p dt (6.) Oletetaan seuraavaksi, että T on vakio ja paine p saa lisäyksen p. Siirrymme pisteestä 1 pisteeseen 4 kuvassa 6.4. Tilavuuden muutos lähestyy tällöin rajalla p 0 arvoa missä V V4 V1 = V = p, (6.3) p V p T on funktion V isotermille pisteeseen 1 piirretyn tangentin T kulmakerroin. Tätä kerrointa kutsutaan vastaavasti funktion V osittaisderivaataksi paineen suhteen vakiolämpötilassa. Jos paineen muutos on äärettömän pieni, voimme kirjoittaa yhtälön 6.3 muodossa V dv = p T dp. (6.4) Yhdistämällä edelliset tulokset voimme laskea kaasun tilavuudenmuutoksen, kun paine ja lämpötila saavat molemmat differentiaalisen lisäykset dp ja dt : V V dv dp dt. (6.5) T = + p T p Yhtälön 6.5 antaman tilavuuden muutoksen on tietenkin oltava riippumaton järjestyksestä, jossa differentiaaliset muutokset tehdään. Tästä seuraa
14 16 VI Tilanyhtälö tietty ehto tilavuuden ristiderivaatoille paineen ja lämpötilan suhteen. Tätä ehtoa on tarkasteltu lähemmin liitteessä C. Yhtälössä 6.5 esiintyvien osittaisderivaattojen avulla määrittelemme kaasulle ominaiset materiaalivakiot, jotka kuvaavat kaasun ominaistilavuuden muutosta lämpötilan ja paineen muuttuessa. Tilavuuden lämpötilakerroin kuvaa kaasun tilavuuden muutosta lämpötilan muuttuessa vakiopaineessa: 1 V γ = V T p. (6.6) Isoterminen kokoonpuristuvuus kuvaa kaasun tilavuuden muutosta paineen kasvaessa vakiolämpötilassa: 1 V κ =. (6.7) V p T Kertoimelle on valittu negatiivinen etumerkki, jotta sen numeroarvo olisi positiivinen. (Tilavuuden osittaisderivaatta paineen suhteen vakiolämpötilassa on aina negatiivinen). Laajenemiskertoimen ja kokoonpuristuvuuden avulla voidaan yhtälö 6.5 esittää muodossa dv = Vγ dt Vκ dp. (6.8) Esimerkki 6.3. Ideaalikaasulle V = ν RT / p, joten derivoimalla ja käyttämällä ideaalikaasun tilanyhtälöä saadaan 1 V 1 γ = = V T p T ja 1 V 1 κ = =. V p p T Esimerkki 6.4. Kaasun tilavuuden muutos äärellisen suuressa paineen ja lämpötilan muutoksessa saadaan integroimalla yhtälöstä 6.5. Yhtälöistä 6.6 ja 6.7 saadaan
15 6.3 Kaasun ja kiinteän aineen tilavuudenmuutokset 163 dv V = γ dt κ dp. (6.9) Tilavuuden muutos äärellisessä siirtymässä pisteestä p 0, T 0, V 0 pisteeseen p,t,v saadaan integroimalla yhtälö 6.9 puolittain V T p dv = γ dt κ dp V V0 T0 p0. (6.30) Integraalin 6.30 laskeminen edellyttää yleisessä tapauksessa suureiden γ ja κ paine- ja lämpötilariippuvuuden tuntemista integrointireittiä pitkin. Ideaalikaasulle saadaan kuitenkin sijoittamalla edellisestä esimerkistä V T p dv dt dp = V T p V0 T0 p0 (6.31) ja integroimalla V T p Tp ln ln ln ln 0 = = V0 T0 p0 T0p. Ottamalla puolittain eksponenttifunktio saadaan (käyttämällä tilanyhtälöä ν R = p0v0/ T0) V Tp0 p0v0 T T0 T T0 = V V0 = = ν R V0 Tp 0 T0 V V0 V V0 Lopputulos saadaan tietenkin myös suoraan ideaalikaasun tilanyhtälöstä Kiinteä aine. Tiiviille aineelle eli kiinteälle aineelle ja nesteille laajenemiskerroin ja kokoonpuristuvuus määritellään samoin kuin kaasuille yhtälöillä 6.6 ja 6.7. Toisin kuin kaasuille laajenemiskerroin ja kokoonpuristuvuus ovat kuitenkin likimain vakioita laajalla paineen ja lämpötilan vaihteluvälillä. Äärellisen suuren paineen ja lämpötilan muutokseen liittyvä tilavuuden muutos voidaan näin ollen integroida yhtälöstä 6.30 V T p T dv = γdt κdp γ dt κ dp V. V T p T p p
16 164 VI Tilanyhtälö Laskemalla integraalit saamme = γ 0 0 V0 ( ) κ( ) ln V T T p p. (6.3) Elastisten muutosten alueella tilavuuden suhteellinen muutos on pieni, joten logaritmifunktio voidaan esittää sarjana [ ln(1 + x) x x << 1] : V V V V V V V V ln = ln + = ln 1+. V0 V0 V0 V0 V0 Sijoittamalla tämä yhtälöön 6.3 saadaan tiiviin aineen approksimatiivinen tilanyhtälö V V 0 ( T T ) κ ( p p ) = 1+ γ 0 0. (6.33) 6.4 FLT-systeemi FLT-systeemin tilanyhtälö Esimerkkinä tiiviin aineen termodynamiikasta ja tilanyhtälöstä tarkastelemme lähemmin kiinteästä aineesta (metalli) valmistetun tangon pituuden L(F,T) riippuvuutta tangossa vallitsevasta tangon suuntaisesta voimasta F ja tangon lämpötilasta T. Tangon pituuden kokonaisdifferentiaali on L L dl dt df. (6.34) F = + T F T Kuva 6-6 Palkin pituuden muutos dl venyttävän voiman kasvaessa määrällä df. Valitsemme voiman positiiviseksi jos sauvaa venytetään - puristava voima on vastaavasti negatiivinen. Määrittelemme isotermisen kimmokertoimen (englanninkielessä kirjal-
17 6.4 FLT-systeemi 165 lisuudessa Young s modulus of elasticity) yhtälöllä L F E = A L, T missä A on tangon poikkipinta-ala. Pituuden lämpötilakerroin määritellään yhtälöllä 1 L α =. L T F Tangon pituuden muutos 6.34 lämpötilan ja voiman differentiaalisessa muutoksessa voidaan siis esittää muodossa L dl = α LdT + df. (6.35) AE Äärellisen suuressa tilanmuutoksessa ( T, F ) ( T, F) 0 0 saadaan tangon pituuden muutos integroimalla yhtälö Pituuden lämpötilakerroin ja kimmokerroin ovat likimain vakioita laajalla lämpötilan ja jännityksen osavälillä, joten pituuden likiarvoksi saadaan L T F dl 1 L 1 L AE L L T F 0 AE = α dt + df ln = α( T T0 ) + ( F F0 ). (6.36) Koska 1 L/ L0 << 1, voidaan logaritmifunktio kehittää sarjaksi, ja tangon pituudeksi saadaan L L L L T T F F AE 0 ( ) ( ) = 0 + α (6.37) Yhtälöä 6.37 voimme kutsua tangon tilanyhtälöksi. Esimerkki 6.5. Hooken laki Yhtälö 6.37 voidaan esittää myös suhteellisen venymän ε = ( ) avulla muodossa L L0 / L0 ε 1 0 AE 0 = α( T T ) + ( F F ). (6.38)
18 166 VI Tilanyhtälö Usein käytetään voiman sijasta myös tangossa vallitsevaa jännitystä σ = F/ A, jolloin yhtälö 6.38 voidaan esittää muodossa 1 0 E 0 = ( T T ) + ( ). (6.39) ε α σ σ Jos lämpötila on vakio, ( T T 0 ) = 0 ja voimme kirjoittaa σ ε =. (6.40) E Tämä tulos tunnetaan nimellä Hooken laki. Taulukko 6.3 Eräiden materiaalien kimmokertoimia 11 Materiaali Kimmokerroin 10 Nm Alumiini 0,70 Kupari 1,5 Rauta,06 Lyijy 0,16 Nikkeli,1 Teräs,0 Esimerkki 6.6. Terästanko lämpenee 50 K. Kuinka suuri jännitys muodostuu tankoon, jos pituuden muutos on rajoitettu 1,0 promilleen? Kyseisen teräksen lämpötilakerroin α = /K ja kimmokerroin 6 10 E = 10 N/m. Suhteelliselle venymälle voidaan kirjoittaa: 1 = ( T T0 ) + = 0.001, E ε α σ missä T 0 on alkulämpötila. Jännitys on alussa σ 0 = 0. Olkoon T ja σ lämpötilan ja jännityksen arvot lopputilassa. Sijoittamalla T T0 = 50 K saadaan σ ε α = E E( T T0 ) = 495 MPa.
19 6.4 FLT-systeemi 167 Tässä negatiivinen arvo tarkoittaa puristusjännitystä Tilavuuden lämpötilakerroin Tarkastellaan tilavuuden muutosta (vakiopaineessa) suorakulmaisessa särmiössä, jossa särmien pituudet ovat a, b ja c. Lämpötilan muutoksesta seuraava tilavuuden differentiaali on (tulon derivointisääntö) dv = d( abc) = ( bcda) + ( acdb) + ( abdc), missä (isotrooppiselle aineelle) da = αdta, db = αdtb ja dc = αdtc. Sijoittamalla saamme dv = ab( cαdt) + bc( aαdt) + ac( bαdt) = 3abcαdT = 3αVdT. Taulukko 6.4 Kiinteän aineen lämpölaajenemiskertoimia (keskiarvoja lämpötilojen 0 0 C ja C välillä). Aine -1 kerroin K Aine -1 kerroin K Alumiini Rauta Kupari 16.8 Lasi Kvartsi Hopea Pronssi Nikkeli Platina Teräs Kulta Sinkki Iridium Tina Tilavuuden lämpötilakerroin määriteltiin dv = γvdt, joten γ = 3α Jännityksen muutokseen liittyvä työ Tarkastelemme lopuksi isotermiseen jännityksen muutokseen liittyvää työtä. Oletetaan, että jännitys metallitangossa kasvaa arvosta σ 1 arvoon σ samalla, kun tangon pituus muuttuu arvosta L 1 arvoon L.
20 168 VI Tilanyhtälö Venymälle isotermisessä tilanmuutoksessa saadaan L L dl = α LdT + df = df. (6.41) AE AE Ulkoisen voiman tekemä työ saadaan integroimalla puolittain lauseke δ W = FdL. Integroimalla saamme ext L F F ( 1 ) FL L L Wext = FdL = df FdF = F F AE AE AE, L F F missä sauvan venymä oletettiin niin pieneksi, että tekijää voidaan pitää vakiona. L AE Sijoittamalla lopuksi F = Aσ ja V = AL saadaan ulkoisen voiman tekemäksi työksi W ext = V ( 1 ) E σ σ. (6.4) Työ on siis nollaa suurempi, jos jännityksen itseisarvo kasvaa venytyksen tai puristamisen aikana.
Termodynamiikka. Fysiikka III 2007. Ilkka Tittonen & Jukka Tulkki
 Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
Termodynamiikka Fysiikka III 2007 Ilkka Tittonen & Jukka Tulkki Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät
VI TILANYHTÄLÖ... 150
 VI TILANYHTÄLÖ... 150 6.1 Ideaalikaasun tilanyhtälö... 150 6. Van der Waalsin tilanyhtälö... 151 6..1 Semiempiirinen lähestymistapa... 151 6.. Van der Waalsin kaasun ominaisuuksia:... 154 6..3 Van der
VI TILANYHTÄLÖ... 150 6.1 Ideaalikaasun tilanyhtälö... 150 6. Van der Waalsin tilanyhtälö... 151 6..1 Semiempiirinen lähestymistapa... 151 6.. Van der Waalsin kaasun ominaisuuksia:... 154 6..3 Van der
ln2, missä ν = 1mol. ja lopuksi kaasun saama lämpömäärä I pääsäännön perusteella.
 S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
S-114.42, Fysiikka III (S 2. välikoe 4.11.2002 1. Yksi mooli yksiatomista ideaalikaasua on alussa lämpötilassa 0. Kaasu laajenee tilavuudesta 0 tilavuuteen 2 0 a isotermisesti, b isobaarisesti ja c adiabaattisesti.
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 10: Reaalikaasut Pe 1.4.2016 1 AIHEET 1. Malleja, joissa pyritään huomioimaan
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 10: Reaalikaasut Pe 1.4.2016 1 AIHEET 1. Malleja, joissa pyritään huomioimaan
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
m h = Q l h 8380 J = J kg 1 0, kg Muodostuneen höyryn osuus alkuperäisestä vesimäärästä on m h m 0,200 kg = 0,
 76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
76638A Termofysiikka Harjoitus no. 9, ratkaisut syyslukukausi 014) 1. Vesimäärä, jonka massa m 00 g on ylikuumentunut mikroaaltouunissa lämpötilaan T 1 110 383,15 K paineessa P 1 atm 10135 Pa. Veden ominaislämpökapasiteetti
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
VII LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ
 II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
II LÄMPÖOPIN ENSIMMÄINEN PÄÄSÄÄNTÖ 7. Lämpö ja työ... 70 7.2 Kaasun tekemä laajenemistyö... 7 7.3 Laajenemistyön erityistapauksia... 73 7.3. Työ isobaarisessa tilanmuutoksessa... 73 7.3.2 Työ isotermisessä
Integroimalla ja käyttämällä lopuksi tilanyhtälöä saadaan T ( ) ( ) H 5,0 10 J + 2,0 10 0,50 1,0 10 0,80 Pa m 70 kj
 S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
S-4.35 Fysiikka (ES) entti 3.8.. ääritä yhden haikaasumoolin (O) (a) sisäenergian, (b) entalian muutos tilanmuutoksessa alkutilasta =, bar, =,8 m3 loutilaan =, bar, =,5 m3. ärähtelyn vaausasteet voidaan
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
Käyttämällä annettua kokoonpuristuvuuden määritelmää V V. = κv P P = P 0 = P. (b) Lämpölaajenemisesta johtuva säiliön tilavuuden muutos on
 766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
766328A ermofysiikka Harjoitus no. 3, ratkaisut (syyslukukausi 201) 1. (a) ilavuus V (, P ) riippuu lämpötilasta ja paineesta P. Sen differentiaali on ( ) ( ) V V dv (, P ) dp + d. P Käyttämällä annettua
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
S , Fysiikka III (Sf) tentti/välikoeuusinta
 S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
S-114.45, Fysiikka III (Sf) tentti/välikoeuusinta.11.4 1. välikokeen alue 1. Osoita, että hyvin alhaisissa lämpötiloissa elektronin FD systeemin energia on U = (3/ 5) ε F. Opastus: oleta, että kaikki tilat
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
V T p pv T pv T. V p V p p V p p. V p p V p
 S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
S-45, Fysiikka III (ES välikoe 004, RAKAISU Laske ideaalikaasun tilavuuden lämötilakerroin ( / ( ja isoterminen kokoonuristuvuus ( / ( Ideaalikaasun tilanyhtälö on = ν R Kysytyt suureet ovat: ilavuuden
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ
 I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
I PERUSKÄSITTEITÄ JA MÄÄRITELMIÄ 1.1 Tilastollisen fysiikan ja termodynamiikan tutkimuskohde... 2 1.2 Mikroskooppiset ja makroskooppiset teoriat... 3 1.3 Terminen tasapaino ja lämpötila... 5 1.4 Termodynamiikan
Vauhti = nopeuden itseisarvo. Nopeuden itseisarvon keskiarvo N:lle hiukkaselle määritellään yhtälöllä
 S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
S-4.35, Fysiikka III (ES) entti 8.3.006. Laske nopeuden itseisarvon keskiarvo v ave ja nopeuden neliöllinen keskiarvo v rms seuraaville 6 molekyylien nopeusjakaumille: a) kaikkien vauhti 0 m/s, b) kolmen
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: b) 0 e x + 1
 Tehtävä : Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: a) a) x b) e x + Integraali voisi ratketa muuttujanvaihdolla. Integroitava on muotoa (a x ) n joten sopiva muuttujanvaihto voisi olla
Tehtävä : Tehtävänanto oli ratkaista seuraavat määrätyt integraalit: a) a) x b) e x + Integraali voisi ratketa muuttujanvaihdolla. Integroitava on muotoa (a x ) n joten sopiva muuttujanvaihto voisi olla
Spontaanissa prosessissa Energian jakautuminen eri vapausasteiden kesken lisääntyy Energia ja materia tulevat epäjärjestyneemmäksi
 KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
KEMA221 2009 TERMODYNAMIIKAN 2. PÄÄSÄÄNTÖ ATKINS LUKU 3 1 1. TERMODYNAMIIKAN TOINEN PÄÄSÄÄNTÖ Lord Kelvin: Lämpöenergian täydellinen muuttaminen työksi ei ole mahdollista 2. pääsääntö kertoo systeemissä
2 Pistejoukko koordinaatistossa
 Pistejoukko koordinaatistossa Ennakkotehtävät 1. a) Esimerkiksi: b) Pisteet sijaitsevat pystysuoralla suoralla, joka leikkaa x-akselin kohdassa x =. c) Yhtälö on x =. d) Sijoitetaan joitain ehdon toteuttavia
Pistejoukko koordinaatistossa Ennakkotehtävät 1. a) Esimerkiksi: b) Pisteet sijaitsevat pystysuoralla suoralla, joka leikkaa x-akselin kohdassa x =. c) Yhtälö on x =. d) Sijoitetaan joitain ehdon toteuttavia
Lämpötila Lämpölaajeneminen Ideaalikaasu. Luku 17
 Lämpötila Lämpölaajeneminen Ideaalikaasu Luku 17 Ch 17-1 3 Termodynaaminen tasapaino Termodynaaminen tasapaino: Tuotaessa kaksi systeemiä lämpökontaktiin niiden termodynaaminen tasapaino on saavutettu,
Lämpötila Lämpölaajeneminen Ideaalikaasu Luku 17 Ch 17-1 3 Termodynaaminen tasapaino Termodynaaminen tasapaino: Tuotaessa kaksi systeemiä lämpökontaktiin niiden termodynaaminen tasapaino on saavutettu,
Luku6 Tilanyhtälö. Ideaalikaasun N V. Yleinen aineen. paine vakio. tilavuus vakio
 Luku6 Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät saadaan leikkaamalla painepinta pv suuntaisilla
Luku6 Tilanyhtälö paine vakio tilavuus vakio Ideaalikaasun N p= kt pinta V Yleinen aineen p= f V T pinta (, ) Isotermit ja isobaarit Vakiolämpötilakäyrät saadaan leikkaamalla painepinta pv suuntaisilla
Ch 12-4&5 Elastisuudesta ja lujuudesta
 Ch 12-4&5 Elastisuudesta ja lujuudesta Jännitys ja venymä Hooken laki F = k l Δl = 1 k F Jousivakio k riippuu langan dimensioista Saadaan malli Δl = l o EA F k = E A l o Lisäksi tarvitaan materiaalia kuvaava
Ch 12-4&5 Elastisuudesta ja lujuudesta Jännitys ja venymä Hooken laki F = k l Δl = 1 k F Jousivakio k riippuu langan dimensioista Saadaan malli Δl = l o EA F k = E A l o Lisäksi tarvitaan materiaalia kuvaava
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy Millä reaaliluvun x arvoilla. 3 4 x 2,
 MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 6. Millä reaaliluvun arvoilla a) 9 =, b) + + + 4, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + 4 + 6 + +, b) 8 + 4 6 + + n n, c) + + +
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 6. Millä reaaliluvun arvoilla a) 9 =, b) + + + 4, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + 4 + 6 + +, b) 8 + 4 6 + + n n, c) + + +
l 1 2l + 1, c) 100 l=0 AB 3AC ja AB AC sekä vektoreiden AB ja
 MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 7. Millä reaaliluvun arvoilla a) 9 =, b) + 5 + +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c) +
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 7. Millä reaaliluvun arvoilla a) 9 =, b) + 5 + +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c) +
KIINTEÄN AINEEN JA NESTEEN TILANYHTÄLÖT
 KIINTEÄN AINEEN JA NESTEEN TILANYHTÄLÖT Lämpölaajeneminen Pituuden lämpölaajeneminen: l = αl o t lo l l = l o + l = l o + αl o t l l = l o (1 + α t) α = pituuden lämpötilakerroin esim. teräs: α = 12 10
KIINTEÄN AINEEN JA NESTEEN TILANYHTÄLÖT Lämpölaajeneminen Pituuden lämpölaajeneminen: l = αl o t lo l l = l o + l = l o + αl o t l l = l o (1 + α t) α = pituuden lämpötilakerroin esim. teräs: α = 12 10
= 1 kg J kg 1 1 kg 8, J mol 1 K 1 373,15 K kg mol 1 1 kg Pa
 766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
766328A Termofysiikka Harjoitus no. 8, ratkaisut syyslukukausi 2014 1. 1 kg nestemäistä vettä muuttuu höyryksi lämpötilassa T 100 373,15 K ja paineessa P 1 atm 101325 Pa. Veden tiheys ρ 958 kg/m 3 ja moolimassa
l 1 2l + 1, c) 100 l=0
 MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
f(x 1, x 2 ) = x x 1 k 1 k 2 k 1, k 2 x 2 1, 0 1 f(1, 1)h 1 = h = h 2 1, 1 12 f(1, 1)h 1 h 2
 HY / Matematiikan ja tilastotieteen laitos Vektorianalyysi I, syksy 7 Harjoitus 6 Ratkaisuehdotukset 6.. Olkoon f : G R, G = {(x, x ) R x > }, f(x, x ) = x x. Etsi differentiaalit d k f(, ), k =,,. Ratkaisu:
HY / Matematiikan ja tilastotieteen laitos Vektorianalyysi I, syksy 7 Harjoitus 6 Ratkaisuehdotukset 6.. Olkoon f : G R, G = {(x, x ) R x > }, f(x, x ) = x x. Etsi differentiaalit d k f(, ), k =,,. Ratkaisu:
Z 1 = Np i. 2. Sähkömagneettisen kentän värähdysliikkeen energia on samaa muotoa kuin molekyylin värähdysliikkeen energia, p 2
 766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
766328A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 24). Klassisen ideaalikaasun partitiofunktio on luentojen mukaan Z N! [Z (T, V )] N, (9.) missä yksihiukkaspartitiofunktio Z (T, V ) r e βɛr.
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
Kaasu 2-atominen. Rotaatio ja translaatiovapausasteet virittyneet (f=5) c. 5 Ideaalikaasun tilanyhtälöstä saadaan kaasun moolimäärä: 3
 S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
S-4.5.vk. 6..000 Tehtävä Ideaalikaasun aine on 00kPa, lämötila 00K ja tilavuus,0 litraa. Kaasu uristetaan adiabaattisesti 5-kertaiseen aineeseen. Kaasumolekyylit ovat -atomisia. Laske uristamiseen tarvittava
IX TOINEN PÄÄSÄÄNTÖ JA ENTROPIA...208
 IX OINEN PÄÄSÄÄNÖ JA ENROPIA...08 9. ermodynaamisen systeemin pyrkimys tasapainoon... 08 9. ermodynamiikan toinen pääsääntö... 0 9.3 Entropia termodynamiikassa... 0 9.3. Entropian määritelmä... 0 9.3.
IX OINEN PÄÄSÄÄNÖ JA ENROPIA...08 9. ermodynaamisen systeemin pyrkimys tasapainoon... 08 9. ermodynamiikan toinen pääsääntö... 0 9.3 Entropia termodynamiikassa... 0 9.3. Entropian määritelmä... 0 9.3.
Laskuharjoitus 2 Ratkaisut
 Vastaukset palautetaan yhtenä PDF-tiedostona MyCourses:iin ke 7.3. klo 14 mennessä. Mahdolliset asia- ja laskuvirheet ja voi ilmoittaa osoitteeseen serge.skorin@aalto.fi. Laskuharjoitus 2 Ratkaisut 1.
Vastaukset palautetaan yhtenä PDF-tiedostona MyCourses:iin ke 7.3. klo 14 mennessä. Mahdolliset asia- ja laskuvirheet ja voi ilmoittaa osoitteeseen serge.skorin@aalto.fi. Laskuharjoitus 2 Ratkaisut 1.
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Ratkaisut 2. KJR-C2001 Kiinteän aineen mekaniikan perusteet, IV/2016. Tehtävä 1 Selitä käsitteet kohdissa a) ja b) sekä laske c) kohdan tehtävä.
 Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
Ratkaisut 3. KJR-C2001 Kiinteän aineen mekaniikan perusteet, IV/2016
 Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
Kotitehtävät palautetaan viimeistään keskiviikkoisin ennen luentojen alkua eli klo 14:00 mennessä. Muistakaa vastaukset eri tehtäviin palautetaan eri lokeroon! Joka kierroksen arvostellut kotitehtäväpaperit
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
η = = = 1, S , Fysiikka III (Sf) 2. välikoe
 S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
S-11445 Fysiikka III (Sf) välikoe 710003 1 Läpövoiakoneen kiertoprosessin vaiheet ovat: a) Isokorinen paineen kasvu arvosta p 1 arvoon p b) adiabaattinen laajeneinen jolloin paine laskee takaisin arvoon
Mikrotila Makrotila Statistinen paino Ω(n) 3 Ω(3) = 4 2 Ω(2) = 6 4 Ω(4) = 1
 76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
76628A Termofysiikka Harjoitus no. 4, ratkaisut (syyslukukausi 204). (a) Systeemi koostuu neljästä identtisestä spin- -hiukkasesta. Merkitään ylöspäin olevien spinien lukumäärää n:llä. Systeemin mahdolliset
LIITE 1 VIRHEEN ARVIOINNISTA
 1 LIITE 1 VIRHEEN ARVIOINNISTA Mihin tarvitset virheen arviointia? Mittaustulokset ovat aina todellisten luonnonvakioiden ja tutkimuskohdetta kuvaavien suureiden likiarvoja, vaikka mittauslaite olisi miten
1 LIITE 1 VIRHEEN ARVIOINNISTA Mihin tarvitset virheen arviointia? Mittaustulokset ovat aina todellisten luonnonvakioiden ja tutkimuskohdetta kuvaavien suureiden likiarvoja, vaikka mittauslaite olisi miten
3Työ. 3.1 Yleinen määritelmä
 3Työ Edellisessä luvussa käsittelimme systeemin sisäenergian muutosta termisen energiansiirron myötä, joka tapahtuu spontaanisti kahden eri lämpötilassa olevan kappaleen välillä. Toisena mekanismina systeemin
3Työ Edellisessä luvussa käsittelimme systeemin sisäenergian muutosta termisen energiansiirron myötä, joka tapahtuu spontaanisti kahden eri lämpötilassa olevan kappaleen välillä. Toisena mekanismina systeemin
Differentiaali- ja integraalilaskenta 1 Ratkaisut 5. viikolle /
 MS-A8 Differentiaali- ja integraalilaskenta, V/7 Differentiaali- ja integraalilaskenta Ratkaisut 5. viikolle / 9..5. Integroimismenetelmät Tehtävä : Laske osittaisintegroinnin avulla a) π x sin(x) dx,
MS-A8 Differentiaali- ja integraalilaskenta, V/7 Differentiaali- ja integraalilaskenta Ratkaisut 5. viikolle / 9..5. Integroimismenetelmät Tehtävä : Laske osittaisintegroinnin avulla a) π x sin(x) dx,
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
BM20A5840 Usean muuttujan funktiot ja sarjat Harjoitus 1, Kevät 2018
 BM20A5840 Usean muuttujan funktiot ja sarjat Harjoitus 1, Kevät 2018 1. (a) Tunnemme vektorit a = [ 5 1 1 ] ja b = [ 2 0 1 ]. Laske (i) kummankin vektorin pituus (eli itseisarvo, eli normi); (ii) vektorien
BM20A5840 Usean muuttujan funktiot ja sarjat Harjoitus 1, Kevät 2018 1. (a) Tunnemme vektorit a = [ 5 1 1 ] ja b = [ 2 0 1 ]. Laske (i) kummankin vektorin pituus (eli itseisarvo, eli normi); (ii) vektorien
Kvanttifysiikan perusteet 2017
 Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Tekijä Pitkä matematiikka
 K1 Tekijä Pitkä matematiikka 5 7..017 a) 1 1 + 1 = 4 + 1 = 3 = 3 4 4 4 4 4 4 b) 1 1 1 = 4 6 3 = 5 = 5 3 4 1 1 1 1 1 K a) Koska 3 = 9 < 10, niin 3 10 < 0. 3 10 = (3 10 ) = 10 3 b) Koska π 3,14, niin π
K1 Tekijä Pitkä matematiikka 5 7..017 a) 1 1 + 1 = 4 + 1 = 3 = 3 4 4 4 4 4 4 b) 1 1 1 = 4 6 3 = 5 = 5 3 4 1 1 1 1 1 K a) Koska 3 = 9 < 10, niin 3 10 < 0. 3 10 = (3 10 ) = 10 3 b) Koska π 3,14, niin π
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
2 Raja-arvo ja jatkuvuus
 Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 5.7.6 Raja-arvo ja jatkuvuus. a) Kun suorakulmion kärki on kohdassa =, on suorakulmion kannan pituus. Suorakulmion korkeus on käyrän y-koordinaatti
Juuri 6 Tehtävien ratkaisut Kustannusosakeyhtiö Otava päivitetty 5.7.6 Raja-arvo ja jatkuvuus. a) Kun suorakulmion kärki on kohdassa =, on suorakulmion kannan pituus. Suorakulmion korkeus on käyrän y-koordinaatti
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
4 (x 1)(y 3) (y 3) (x 1)(y 3)3 5 3
 . Taylorin polynomi; funktion ääriarvot.1. Taylorin polynomi 94. Kehitä funktio f (x,y) = x 2 y Taylorin polynomiksi kehityskeskuksena piste ( 1,2) a) laskemalla osittaisderivaatat, b) kirjoittamalla muuttujat
. Taylorin polynomi; funktion ääriarvot.1. Taylorin polynomi 94. Kehitä funktio f (x,y) = x 2 y Taylorin polynomiksi kehityskeskuksena piste ( 1,2) a) laskemalla osittaisderivaatat, b) kirjoittamalla muuttujat
Differentiaali- ja integraalilaskenta
 Differentiaali- ja integraalilaskenta Opiskelijan nimi: DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona
Differentiaali- ja integraalilaskenta Opiskelijan nimi: DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona
Funktiojonot ja funktiotermiset sarjat Funktiojono ja funktioterminen sarja Pisteittäinen ja tasainen suppeneminen
 4. Funktiojonot ja funktiotermiset sarjat 4.1. Funktiojono ja funktioterminen sarja 60. Tutki, millä muuttujan R arvoilla funktiojono f k suppenee, kun Mikä on rajafunktio? a) f k () = 2k 2k + 1, b) f
4. Funktiojonot ja funktiotermiset sarjat 4.1. Funktiojono ja funktioterminen sarja 60. Tutki, millä muuttujan R arvoilla funktiojono f k suppenee, kun Mikä on rajafunktio? a) f k () = 2k 2k + 1, b) f
4. Käyrän lokaaleja ominaisuuksia
 23 VEKTORIANALYYSI Luento 3 4 Käyrän lokaaleja ominaisuuksia Käyrän tangentti Tarkastellaan parametrisoitua käyrää r( t ) Parametrilla t ei tarvitse olla mitään fysikaalista merkitystä, mutta seuraavassa
23 VEKTORIANALYYSI Luento 3 4 Käyrän lokaaleja ominaisuuksia Käyrän tangentti Tarkastellaan parametrisoitua käyrää r( t ) Parametrilla t ei tarvitse olla mitään fysikaalista merkitystä, mutta seuraavassa
Ekvipartitioteoreema. Entropia MB-jakaumassa. Entropia tilastollisessa mekaniikassa
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema
 Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
Ekvipartitioteoreema lämpötilan ollessa riittävän korkea, kukin molekyylin liikkeen vapausaste tuo energian ½ kt sekä keskimääräiseen liike-energiaan ja kineettiseen energiaan energian lisäys ja riittävän
energian), systeemi on eristetty (engl. isolated). Tällöin sekä systeemiin siirtynyt
 14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
14 2 Ensimmäinen pääsääntö 2-1 Lämpömäärä ja työ Termodynaaminen systeemi on jokin maailmankaikkeuden osa, jota rajoittaa todellinen tai kuviteltu rajapinta (engl. boundary). Systeemi voi olla esimerkiksi
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
LIITE 1 VIRHEEN ARVIOINNISTA
 1 Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi miten uudenaikainen tai kallis tahansa ja mittaaja olisi alansa huippututkija Tästä johtuen mittaustuloksista
1 Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi miten uudenaikainen tai kallis tahansa ja mittaaja olisi alansa huippututkija Tästä johtuen mittaustuloksista
LIITE 1 VIRHEEN ARVIOINNISTA
 Oulun yliopisto Fysiikan opetuslaboratorio Fysiikan laboratoriotyöt 1 1 LIITE 1 VIRHEEN RVIOINNIST Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi
Oulun yliopisto Fysiikan opetuslaboratorio Fysiikan laboratoriotyöt 1 1 LIITE 1 VIRHEEN RVIOINNIST Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
H7 Malliratkaisut - Tehtävä 1
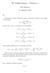 H7 Malliratkaisut - Tehtävä Eelis Mielonen 7. lokakuuta 07 a) Palautellaan muistiin Maclaurin sarjan määritelmä (Taylorin sarja origon ympäristössä): f n (0) f(x) = (x) n Nyt jos f(x) = ln( + x) saadaan
H7 Malliratkaisut - Tehtävä Eelis Mielonen 7. lokakuuta 07 a) Palautellaan muistiin Maclaurin sarjan määritelmä (Taylorin sarja origon ympäristössä): f n (0) f(x) = (x) n Nyt jos f(x) = ln( + x) saadaan
3 = Lisäksi z(4, 9) = = 21, joten kysytty lineaarinen approksimaatio on. L(x,y) =
 BM20A5810 Differentiaalilaskenta ja sovellukset Harjoitus 6, Syksy 2016 1. (a) Olkoon z = z(x,y) = yx 1/2 + y 1/2. Muodosta z:lle lineaarinen approksimaatio L(x,y) siten että approksimaation ja z:n arvot
BM20A5810 Differentiaalilaskenta ja sovellukset Harjoitus 6, Syksy 2016 1. (a) Olkoon z = z(x,y) = yx 1/2 + y 1/2. Muodosta z:lle lineaarinen approksimaatio L(x,y) siten että approksimaation ja z:n arvot
f (28) L(28) = f (27) + f (27)(28 27) = = (28 27) 2 = 1 2 f (x) = x 2
 BMA581 - Differentiaalilaskenta ja sovellukset Harjoitus 4, Syksy 15 1. (a) Olisiko virhe likimain.5, ja arvio antaa siis liian suuren arvon. (b) Esim (1,1.5) tai (,.5). Funktion toinen derivaatta saa
BMA581 - Differentiaalilaskenta ja sovellukset Harjoitus 4, Syksy 15 1. (a) Olisiko virhe likimain.5, ja arvio antaa siis liian suuren arvon. (b) Esim (1,1.5) tai (,.5). Funktion toinen derivaatta saa
Mekaniikan jatkokurssi Fys102
 Mekaniikan jatkokurssi Fys10 Kevät 010 Jukka Maalampi LUENTO 8 Vaimennettu värähtely Elävässä elämässä heilureiden ja muiden värähtelijöiden liike sammuu ennemmin tai myöhemmin. Vastusvoimien takia värähtelijän
Mekaniikan jatkokurssi Fys10 Kevät 010 Jukka Maalampi LUENTO 8 Vaimennettu värähtely Elävässä elämässä heilureiden ja muiden värähtelijöiden liike sammuu ennemmin tai myöhemmin. Vastusvoimien takia värähtelijän
Vastaus: 10. Kertausharjoituksia. 1. Lukujonot lim = lim n + = = n n. Vastaus: suppenee raja-arvona Vastaus:
 . Koska F( ) on jokin funktion f ( ) integraalifunktio, niin a+ a f() t dt F( a+ t) F( a) ( a+ ) b( a b) Vastaus: Kertausharjoituksia. Lukujonot 87. + n + lim lim n n n n Vastaus: suppenee raja-arvona
. Koska F( ) on jokin funktion f ( ) integraalifunktio, niin a+ a f() t dt F( a+ t) F( a) ( a+ ) b( a b) Vastaus: Kertausharjoituksia. Lukujonot 87. + n + lim lim n n n n Vastaus: suppenee raja-arvona
766328A Termofysiikka Harjoitus no. 10, ratkaisut (syyslukukausi 2014)
 7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
7668A Termofysiikka Harjoitus no., ratkaisut (syyslukukausi 4). Johdetaan yksiatomisen klassisen ideaalikaasun kemiallisen potentiaalin µ(t,, N) lauseke. (a) Luentojen yhtälön mukaan kemiallinen potentiaali
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Clausiuksen epäyhtälö
 1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
1 Kuva 1: Clausiuksen epäyhtälön johtaminen. Clausiuksen epäyhtälö otesimme Carnot n koneelle, että syklissä lämpötiloissa H ja L vastaanotetuille lämmöille Q H ja Q L pätee Q H H oisin ilmaistuna, Carnot
x 4 e 2x dx Γ(r) = x r 1 e x dx (1)
 HY / Matematiikan ja tilastotieteen laitos Todennäköisyyslaskenta IIA, syksy 217 217 Harjoitus 6 Ratkaisuehdotuksia Tehtäväsarja I 1. Laske numeeriset arvot seuraaville integraaleille: x 4 e 2x dx ja 1
HY / Matematiikan ja tilastotieteen laitos Todennäköisyyslaskenta IIA, syksy 217 217 Harjoitus 6 Ratkaisuehdotuksia Tehtäväsarja I 1. Laske numeeriset arvot seuraaville integraaleille: x 4 e 2x dx ja 1
läheisyydessä. Piirrä funktio f ja nämä approksimaatiot samaan kuvaan. Näyttääkö järkeenkäyvältä?
 BM20A5840 - Usean muuttujan funktiot ja sarjat Harjoitus 1, Kevät 2017 1. Tunnemme vektorit a = [ 1 2 3 ] ja b = [ 2 1 2 ]. Laske (i) kummankin vektorin pituus (eli itseisarvo, eli normi); (ii) vektorien
BM20A5840 - Usean muuttujan funktiot ja sarjat Harjoitus 1, Kevät 2017 1. Tunnemme vektorit a = [ 1 2 3 ] ja b = [ 2 1 2 ]. Laske (i) kummankin vektorin pituus (eli itseisarvo, eli normi); (ii) vektorien
LIITTEET Liite A Stirlingin kaavan tarkkuudesta...2. Liite B Lagrangen kertoimet...3
 LIITTEET... 2 Liite A Stirligi kaava tarkkuudesta...2 Liite B Lagrage kertoimet... 2 Liitteet Liitteet Liite A Stirligi kaava tarkkuudesta Luoollista logaritmia suureesta! approksimoidaa usei Stirligi
LIITTEET... 2 Liite A Stirligi kaava tarkkuudesta...2 Liite B Lagrage kertoimet... 2 Liitteet Liitteet Liite A Stirligi kaava tarkkuudesta Luoollista logaritmia suureesta! approksimoidaa usei Stirligi
a) on lokaali käänteisfunktio, b) ei ole. Piirrä näiden pisteiden ympäristöön asetetun neliöruudukon kuva. VASTAUS:
 6. Käänteiskuvaukset ja implisiittifunktiot 6.1. Käänteisfunktion olemassaolo 165. Määritä jokin piste, jonka ympäristössä funktiolla f : R 2 R 2, f (x,y) = (ysinx, x + y + 1) a) on lokaali käänteisfunktio,
6. Käänteiskuvaukset ja implisiittifunktiot 6.1. Käänteisfunktion olemassaolo 165. Määritä jokin piste, jonka ympäristössä funktiolla f : R 2 R 2, f (x,y) = (ysinx, x + y + 1) a) on lokaali käänteisfunktio,
0, niin vektorit eivät ole kohtisuorassa toisiaan vastaan.
 Tekijä Pitkä matematiikka 4 9.1.016 168 a) Lasketaan vektorien a ja b pistetulo. a b = (3i + 5 j) (7i 3 j) = 3 7 + 5 ( 3) = 1 15 = 6 Koska pistetulo a b 0, niin vektorit eivät ole kohtisuorassa toisiaan
Tekijä Pitkä matematiikka 4 9.1.016 168 a) Lasketaan vektorien a ja b pistetulo. a b = (3i + 5 j) (7i 3 j) = 3 7 + 5 ( 3) = 1 15 = 6 Koska pistetulo a b 0, niin vektorit eivät ole kohtisuorassa toisiaan
KJR-C2002 Kontinuumimekaniikan perusteet, tentti
 KJR-C2002 Kontinuumimekaniikan perusteet, tentti 13.12.2017 1. Jos r θ on paikkavektori, niin mitä ovat r θ, esitksiä r θ ja r θ? Kätä Karteesisen koordinaatiston T θ θ r < j < j zθ θ k k z ja / θ < j
KJR-C2002 Kontinuumimekaniikan perusteet, tentti 13.12.2017 1. Jos r θ on paikkavektori, niin mitä ovat r θ, esitksiä r θ ja r θ? Kätä Karteesisen koordinaatiston T θ θ r < j < j zθ θ k k z ja / θ < j
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
KJR-C1001 Statiikka ja dynamiikka. Luento Susanna Hurme
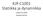 KJR-C1001 Statiikka ja dynamiikka Luento 9.3.2016 Susanna Hurme Päivän aihe: Palkin leikkausvoima- ja taivutusmomenttijakaumat ja kuviot (Kirjan luvut 7.2 ja 7.3) Osaamistavoitteet: Ymmärtää, miten leikkausvoima
KJR-C1001 Statiikka ja dynamiikka Luento 9.3.2016 Susanna Hurme Päivän aihe: Palkin leikkausvoima- ja taivutusmomenttijakaumat ja kuviot (Kirjan luvut 7.2 ja 7.3) Osaamistavoitteet: Ymmärtää, miten leikkausvoima
IV. TASAINEN SUPPENEMINEN. f(x) = lim. jokaista ε > 0 ja x A kohti n ε,x N s.e. n n
 IV. TASAINEN SUPPENEMINEN IV.. Funktiojonon tasainen suppeneminen Olkoon A R joukko ja f n : A R funktio, n =, 2, 3,..., jolloin jokaisella x A muodostuu lukujono f x, f 2 x,.... Jos tämä jono suppenee
IV. TASAINEN SUPPENEMINEN IV.. Funktiojonon tasainen suppeneminen Olkoon A R joukko ja f n : A R funktio, n =, 2, 3,..., jolloin jokaisella x A muodostuu lukujono f x, f 2 x,.... Jos tämä jono suppenee
Matematiikan tukikurssi
 Matematiikan tukikurssi Kurssikerta 8 1 Funktion kuperuussuunnat Derivoituva funktio f (x) on pisteessä x aidosti konveksi, jos sen toinen derivaatta on positiivinen f (x) > 0. Vastaavasti f (x) on aidosti
Matematiikan tukikurssi Kurssikerta 8 1 Funktion kuperuussuunnat Derivoituva funktio f (x) on pisteessä x aidosti konveksi, jos sen toinen derivaatta on positiivinen f (x) > 0. Vastaavasti f (x) on aidosti
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
Differentiaalilaskennan tehtäviä
 Differentiaalilaskennan tehtäviä DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona 2. Derivoimiskaavat 2.1
Differentiaalilaskennan tehtäviä DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona 2. Derivoimiskaavat 2.1
Matematiikan tukikurssi
 Matematiikan tukikurssi Kurssikerta 10 1 Funktion monotonisuus Derivoituva funktio f on aidosti kasvava, jos sen derivaatta on positiivinen eli jos f (x) > 0. Funktio on aidosti vähenevä jos sen derivaatta
Matematiikan tukikurssi Kurssikerta 10 1 Funktion monotonisuus Derivoituva funktio f on aidosti kasvava, jos sen derivaatta on positiivinen eli jos f (x) > 0. Funktio on aidosti vähenevä jos sen derivaatta
