CHEM-C2200 Kemiallinen termodynamiikka. Työ 2: Kaliumkloridin liukenemisentalpian määrittäminen. Työohje
|
|
|
- Jutta Lahtinen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 CHEM-C2200 Kemiallinen termodynamiikka Työ 2: Kaliumkloridin liukenemisentalpian määrittäminen Työohje
2 1 Johdanto Kalorimetriassa tutkitaan lämpötilan ja lämpöenergian muutoksia eristetyssä järjestelmässä. Kalorimetri on vertailuastia, joka on suojattu ulkoista lämmönvaihtoa vastaan mahdollisimman hyvin. Kalorimetrin avulla kemialliseen reaktioon, faasimuutokseen, liukenemiseen ja laimenemiseen liittyviä energian muutoksia voidaan mitata. Tässä työssä tutkitaan kalorimetrissä liukenemisreaktiota KCl(s) KCl(aq) (1) ja määritetään reaktion moolinen entalpia äärettömässä laimennuksessa DH m,liuk,. 2 Teoreettinen tarkastelu 2.1. Adiabaattiset kalorimetriset mittaukset Ennen reaktiota kalorimetri (K) ja lähtöaineet (A) ovat lämpötilassa T i, reaktion jälkeen kalorimetri ja tuotteet (B) ovat lämpötilassa T f. Kokonaisprosessia kuvaa yhtälö K(T i) + A(T i) Æ K(T f) + B(T f) DH (2) jossa DH on entalpiamuutos koko systeemissä. Jos kalorimetri on vakiopaineessa DH = 0, koska prosessi tapahtuu adiabaattisesti. Voidaan ajatella että kokonaisprosessi (2) tapahtuu kahdessa vaiheessa A(Ti) Æ B(Ti) K(T i) + B(T i) Æ K(T f) + B(T f) D H T (3) i D HT i Æ T f (4) Koska reaktio (2) on vaiheiden (3) ja (4) summa 1
3 DH = DH T + DH T i i ÆT f = 0 (5) Vaiheen (4) entalpia voidaan laskea yhtälöstä DH Ti ÆTf = Tf Ú Ti C P dt = C P ( T -T ) = C DT f i P (6) jossa C P on systeemin (kalorimetriastia + sisältö) vakioksi oletettu lämpökapasiteetti ja T on reaktion aiheuttama lämpötilan muutos, joka voidaan mitata. C P voidaan määrittää kalibroimalla kalorimetri reaktiolla, jonka entalpia tunnetaan. Vaiheeseen (3) liittyvä entalpia lämpötilassa T i voidaan siten laskea DH = - DH Æ = -C DT (7) Ti Ti Tf P Moolinen reaktioentalpia saadaan jakamalla D H Ti reagoivan aineen ainemäärällä n DHT CP DT i D Hm, T = = - (8) i n n Yleensä kalorimetrin lämpöeristys ei ole niin hyvä, että kalorimetri olisi täysin adiabaattinen. Tämän vuoksi on kalorimetrin ja ympäristön välinen lämmönvaihto otettava huomioon. Mittauksissa kalorimetrin lämpötilaa seurataan ajan funktiona ennen koetta (esijakso), kokeen aikana (pääjakso) ja kokeen jälkeen (jälkijakso). Sen jälkeen piirretään aika-lämpötila-käyrä ja ekstrapoloidaan lineaarisesti esijaksoa eteenpäin ja jälkijaksoa taaksepäin jonkin matkaa. Lämpötilanmuutos T c määritetään kuvan 1 mukaisesti esi- ja jälkijakson lämpötilojen erotuksena kohdasta T(0,63), jossa lämpötilanmuutoksesta on tapahtunut 63 %. 2
4 Kuva 1. Kalorimetrin lämpötilamuutoksen eri vaiheet eksotermisessä reaktiossa. Huom: Tc = Tf -Ti 2.2. KCl:n liukenemisreaktion entalpia Tässä työssä tutkitaan KCl(s):n liukenemisreaktiota. Vaiheena (3) on reaktio KCl(s) KCl(aq,x) D H m,liuk, x (9) jossa x on muodostuneen liuoksen väkevyys. Tämän reaktion moolinen entalpia DH m,liuk,x saadaan laskettua yhtälön (8) avulla, kun ensin C p ja T määritetään kokeellisesti kalorimetrisillä mittauksilla. Aineen liukenemisreaktion entalpia riippuu syntyvästä loppukonsentraatiosta. Kun liuottimen määrä kasvaa, liukenemisentalpia lähestyy raja-arvoa, joka on liukenemisreaktion moolinen entalpia äärettömässä laimennuksessa. KCl(s) KCl(aq, ) DH (10) m, liuk, Reaktio (10) voidaan jakaa kahteen vaiheeseen, joista ensimmäisessä (a) suola liukenee väkevyyteen x ja toisessa (b) liuos laimenee siten, että muodostuva liuos on äärettömän laimea, eli 3
5 KCl(s) KCl(aq,x) H m,liuk,x (10a) KCl(aq,x) KCl(aq, ) H m,laim (10b) Koska reaktio (10) on osareaktioiden (10a) ja (10b) summa, saadaan H m,liuk, = H m,liuk,x + H m,laim (11) Laimennusentalpia DH m,laim voidaan laskea muodostusmisentalpioiden avulla H m,laim = fh o (KCl, ) fh o (KCl,x) (12) jossa fh o (KCl,x) ja fh o (KCl, ) ovat vesiliuosten KCl(aq,x) ja KCl(aq, ) muodostumisentalpiat, jotka saadaan kirjallisuudesta [1]. Yhtälöiden (11) ja (12) avulla voidaan laskea H m,liuk,. 3 Työn suoritus Työ suoritetaan kahdessa vaiheessa. Ensin kalorimetri (kuva 2) kalibroidaan reaktiolla, jonka entalpia tunnetaan. Kalibroinnin avulla lasketaan kalorimetriastian lämpökapasiteetti Cp(astia). Toisessa vaiheessa määritetään liukenemisreaktioon (9) liittyvä entalpia D H m,liuk, x saadaan laskettua Hm,liuk, äärettömässä laimennuksessa., josta kaavojen (11) ja (12) ja kirjallisuusarvojen avulla eli KCl:n liukenemisreaktion moolinen entalpia 4
6 Kuva 2. Kalorimetrinen mittauslaitteisto. 3.1 Kalorimetrin kalibrointi Kalibrointi suoritetaan tutkimalla kiinteän TRIS:n (trishydroksimetyyli-aminometaani) liukenemista 0,10 M vetykloridihappoon HCl(aq). Tämän liukenemisreaktion entalpia tunnetaan. Käynnistetään kalorimetri ja tietokone. Punnitaan Dewar-astiaan huoneenlämpötilassa 100 g 0,10 M HCl:a (kirjaa ylös tarkka massalukema) ja sovitetaan astia laitteeseen. Punnitaan laitteen puhtaaseen ja kuivaan muoviastiaan 0,5 g TRIS:a (kirjaa ylös tarkka massalukema) ja kiinnitetään astia sylinteriin. Työnnetään akseli Dewar-astian kannen läpi ja kiinnitetään sylinteri akseliin assistentin ohjeiden mukaan. Asetetaan kansi Dewar-astiaan ja sekoitushihna paikoilleen. Käynnistetään mittausohjelma. Ensin kalorimetrin lämpötilan annetaan tasaantua (esijakso kuvassa 1). Tämän jälkeen työnnetään varovasti muoviputkella muoviastia irti sylinteristä niin, että TRIS tulee kerralla kontaktiin liuoksen kanssa, ja seurataan lämpötilan muuttumista (pääjakso kuvassa 1). Mittausta jatketaan kunnes lämpötila tasoittuu jälleen (mittaa riittävän pitkä jälkijakso, kuva 1). Lopuksi tarkistetaan, että kaikki mittausdata on siirtynyt tietokoneelle (painamalla F5), kopioidaan data Exceliin ja tallennetaan saatu Excel tiedosto muistitikulle työselostusta varten. 5
7 3.2 KCl:n liukenemisentalpian määrittäminen Itse mittaus toteutetaan samoin kuin kalibrointi. Ensin puhdistetaan ja kuivataan kalibroinnissa käytetty Dewar-astia sekä muoviastia. 100 g tislattua vettä punnitaan (kirjaa ylös tarkka massalukema) kuivaan Dewar-astiaan ja astia asetetaan laitteeseen. Tämän jälkeen 0,5 g KCl(s) suolaa punnitaan (kirjaa ylös tarkka massalukema) muoviastiaan ja kootaan mittaussysteemi samoin kuin kalibrointivaiheessa. Käynnistetään mittausohjelma, ja seurataan ohjelman ohjeita. Mittauksen jälkeen tallennetaan saatu Excel tiedosto muistitikulle työselostusta varten. Lopuksi kaikki astiat tyhjennetään ja pestään. 4 Tulosten käsittely 4.1 Kalorimetriastian lämpökapasiteetin, C P(astia), laskeminen Ensin piirretään kalibrointitulosten perusteella aika-lämpötilakuvaaja eli termogrammi. Määrätään T(0,63) kal ja DT c,kal. TRIS:n liukenemisreaktion entalpia lämpötilassa T(0,63) kal saadaan yhtälöstä DH J TRIS m = - g TRIS È Ê T(0,63) Í245,76 + 1,435 Á25 - o Î Ë C kal ˆ (13) jossa T(0,63) kal on termogrammin lämpötila kohdassa, jolloin lämpötilan noususta on tapahtunut 63 % (kuva 1). Systeemin lämpökapasiteetti C P voidaan laskea kaavasta (7). C P DH DT TRIS = - (14) c,kal Systeemin lämpökapasiteetti on 6
8 C P= C P(astia) + C P(HCl(aq)) (15) Liuoksen lämpökapasiteetti on C P(HCl(aq)) ª C P(vesi) = m HCl(aq) c P(vesi) (16) jossa m HCl(aq) on HCl-liuoksen massa ja c P(vesi) = 4,181 J K -1 g -1 on veden ominaislämpökapasiteetti 25 ºC lämpötilassa. Kaavojen (14)-(16) avulla saadaan laskettua kalorimetriastian lämpökapasiteetti C P(astia). 4.2 Reaktion KCl(s) KCl(aq,x) entalpian DHm,liuk,x laskeminen Piirretään mittauksen perusteella termogrammi. Määrätään T(0,63) mittaus ja DT c,mittaus. Kaavan (8) perusteella moolinen reaktioentalpia saadaan laskettua yhtälöstä C D T P c,mittaus D Hm,liuk,x = - (17) nkcl jossa n KCl on KCl:n ainemäärä. Systeemin lämpökapasiteetti C P on C P= C P(astia) + C P(vesi) = C P(astia) + m vesi c P(vesi) (18) jossa m vesi on veden massa. C P(astia) ja c P(vesi) tunnetaan (kts. vaihe 4.1), joten C p voidaan laskea yhtälön (18) avulla. 4.3 Reaktion KCl(s) KCl(aq, ) entalpian DH m,liuk, laskeminen Liukenemisreaktion moolinen entalpia äärettömässä laimennuksessa, H m,liuk,, lasketaan yhtälöiden (11) ja (12) avulla. 7
9 Kirjallisuudessa [1] on esitetty eri väkevyisten KCl(aq)-liuosten muodostumisentalpia-arvoja. Väkevyys on taulukoissa määritetty suhteena n n vesi x = (19) KCl jossa n vesi on KCl:ään kosketuksessa olevan veden ainemäärä ja n KCl on KCl:n ainemäärä. Jos laskettu x:n arvo ei osu taulukkoarvojen kohdalle, taulukosta otetaan ylös laskettua arvoa lähimmät muodostumisentalpian arvot ja käytetään niiden sopivasti painotettua keskiarvoa. 5 Virhetarkastelu Mietitään, mistä tekijöistä virhe mittauksessa koostuu. Arvioidaan mittauksen aikana virheet ainakin kaikille punnituille massoille, termogrammeista saaduille lämpötilamuutoksille sekä T(0,63) lämpötilalle. Lasketaan numeerinen virhearvio H m,liuk, -arvolle. H m,liuk,x -termin virhe saadaan laskettua osittaisderivoimalla tarvittavat yhtälöt virhelähteiden suhteen. Esitetään kaikki virhelaskujen kaavat esimerkkisijoituksineen. Vaikka H m,laim -termissä on myös epätarkkuutta, koska kirjallisuudesta [1] saatava muodostumisentalpian fh o (KCl,x) arvo ei todennäköisesti osu tarkalleen oikean väkevyyden kohdalle, on H m,laim -termin virhe kuitenkin numeerisesti niin pieni, että se voidaan jättää huomioimatta. 6 Tulosten tarkastelu ja johtopäätökset KCl:n liukenemisreaktion moolinen entalpia äärettömässä laimennuksessa, D H m, liuk,, esitetään virhearvioineen ja verrataan saatua arvoa kirjallisuudessa [2] esitettyyn arvoon. Pohditaan työn mahdollisia virhelähteitä. 8
10 7 Lähdeluettelo 1. Wagman, D.D. & al (Eds.), The NBS tables of chemical thermodynamic properties: Selected values for inorganic and C 1 and C 2 organic substances in SI units, National Bureau of Standards, American Chemical Society, USA 1982 (Journal of Physical and Chemical Reference Data, Volume 11, 1982, supplement No. 2) 2. Weast, C.R. & al (Eds.), CRC, Handbook of Chemistry and Physics, USA. (Huom! Lähteessä ilmoitetun H m,liuk, -arvon oikea yksikkö on kcal/mol. Joissain painoksissa lukee virheellisesti cal/mol) 9
Aineopintojen laboratoriotyöt 1. Veden ominaislämpökapasiteetti
 Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
HSC-ohje laskuharjoituksen 1 tehtävälle 2
 HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
Koesuunnitelma Alumiinin lämpölaajenemiskertoimen määrittäminen
 KON-C3004 Kone- ja rakennustekniikan laboratoriotyöt Koesuunnitelma Alumiinin lämpölaajenemiskertoimen määrittäminen Ryhmä 3 Henri Palosuo Kaarle Patomäki Heidi Strengell Sheng Tian 1. Johdanto Materiaalin
KON-C3004 Kone- ja rakennustekniikan laboratoriotyöt Koesuunnitelma Alumiinin lämpölaajenemiskertoimen määrittäminen Ryhmä 3 Henri Palosuo Kaarle Patomäki Heidi Strengell Sheng Tian 1. Johdanto Materiaalin
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
H 2 O. Kuva 1. Kalorimetri. missä on kalorimetriin tuotu lämpömäärä. Lämpökapasiteetti taas määräytyy yhtälöstä
 KALORIMETRI 1 TEORIAA Kalorimetri on laite, jolla voidaan mitata lämpömääriä. Mittaus voidaan suorittaa tarkastelemalla lämpömuutoksia, faasimuutoksia, kemiallisia reaktioita jne. Kun mittaus perustuu
KALORIMETRI 1 TEORIAA Kalorimetri on laite, jolla voidaan mitata lämpömääriä. Mittaus voidaan suorittaa tarkastelemalla lämpömuutoksia, faasimuutoksia, kemiallisia reaktioita jne. Kun mittaus perustuu
Eksimeerin muodostuminen
 Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Tarvittavat välineet: Kalorimetri, lämpömittari, jännitelähde, kaksi yleismittaria, sekuntikello
 1 LÄMPÖOPPI 1. Johdanto Työssä on neljä eri osiota, joiden avulla tutustutaan lämpöopin lakeihin ja ilmiöihin. Työn suoritettuaan opiskelijan on tarkoitus ymmärtää lämpöopin keskeiset käsitteet, kuten
1 LÄMPÖOPPI 1. Johdanto Työssä on neljä eri osiota, joiden avulla tutustutaan lämpöopin lakeihin ja ilmiöihin. Työn suoritettuaan opiskelijan on tarkoitus ymmärtää lämpöopin keskeiset käsitteet, kuten
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Työ 3: Veden höyrystymislämmön määritys
 Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
SISÄLLYSLUETTELO SYMBOLILUETTELO 4
 1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
1 SISÄLLYSLUETTELO SYMBOLILUETTELO 4 1 KEMIALLISESTI REAGOIVA TERMODYNAAMINEN SYSTEEMI 6 11 Yleistä 6 12 Standarditila ja referenssitila 7 13 Entalpia- ja entropia-asteikko 11 2 ENTALPIA JA OMINAISLÄMPÖ
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
Luento 2: Lämpökemiaa, osa 1 Torstai klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 orstai 11.10. klo 14-16 477401A - ermodynaamiset tasapainot (Syksy 2012) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen Faasi
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
CHEM-C2230 Pintakemia. Työ 2: Etikkahapon adsorptio aktiivihiileen. Työohje
 CHEM-C2230 Pintakemia Tö 2: Etikkahapon orptio aktiivihiileen Töohje 1 Johdanto Kaasun ja kiinteän aineen rajapinnalla tapahtuu leensä kaasun orptiota. Mös liuoksissa tapahtuu usein liuenneen aineen orptiota
CHEM-C2230 Pintakemia Tö 2: Etikkahapon orptio aktiivihiileen Töohje 1 Johdanto Kaasun ja kiinteän aineen rajapinnalla tapahtuu leensä kaasun orptiota. Mös liuoksissa tapahtuu usein liuenneen aineen orptiota
ROMUMETALLIA OSTAMASSA (OSA 1)
 ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
Kuva 1. Nykyaikainen pommikalorimetri.
 DEPARTMENT OF CHEMISTRY NESTEIDEN JA KIINTEIDEN AINEIDEN LÄMPÖARVOJEN MÄÄRITYS Matti Kuokkanen 1, Reetta Kolppanen 2 ja Toivo Kuokkanen 3 1 Oulun yliopisto, kemian laitos, PL 3000, FI-90014, Oulu, matti.kuokkanen@oulu.fi
DEPARTMENT OF CHEMISTRY NESTEIDEN JA KIINTEIDEN AINEIDEN LÄMPÖARVOJEN MÄÄRITYS Matti Kuokkanen 1, Reetta Kolppanen 2 ja Toivo Kuokkanen 3 1 Oulun yliopisto, kemian laitos, PL 3000, FI-90014, Oulu, matti.kuokkanen@oulu.fi
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
. Veden entropiamuutos lasketaan isobaariselle prosessille yhtälöstä
 LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
LH- Kilo vettä, jonka lämpötila on 0 0 asetetaan kosketukseen suuren 00 0 asteisen kappaleen kanssa Kun veden lämpötila on noussut 00 0, mitkä ovat veden, kappaleen ja universumin entropian muutokset?
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
CHEM-A1110 Virtaukset ja reaktorit. Laskuharjoitus 9/2016. Energiataseet
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti
 CHEM-C2200 Kemiallinen termodynamiikka Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti Työohje 1 Johdanto Happo-emäsindikaattorina käytetty bromitymolisininen muuttaa
CHEM-C2200 Kemiallinen termodynamiikka Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti Työohje 1 Johdanto Happo-emäsindikaattorina käytetty bromitymolisininen muuttaa
(l) B. A(l) + B(l) (s) B. B(s)
 FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 LIUKOISUUDEN IIPPUVUUS LÄMPÖTILASTA 6. 11. 1998 (HJ) A(l) + B(l) µ (l) B == B(s) µ (s) B FYSIKAALISEN KEMIAN LAUDATUTYÖ N:o 3 1. TEOIAA Kyllästetty liuos LIUKOISUUDEN
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
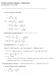 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Molaariset ominaislämpökapasiteetit
 Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Molaariset ominaislämpökapasiteetit Yleensä, kun systeemiin tuodaan lämpöä, sen lämpötila nousee. (Ei kuitenkaan aina, kannattaa muistaa, että työllä voi olla osuutta asiaan.) Lämmön ja lämpötilan muutoksen
Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen
 KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
Mittaustulosten tilastollinen käsittely
 Mittaustulosten tilastollinen käsittely n kertaa toistetun mittauksen tulos lasketaan aritmeettisena keskiarvona n 1 x = x i n i= 1 Mittaustuloksen hajonnasta aiheutuvaa epävarmuutta kuvaa keskiarvon keskivirhe
Mittaustulosten tilastollinen käsittely n kertaa toistetun mittauksen tulos lasketaan aritmeettisena keskiarvona n 1 x = x i n i= 1 Mittaustuloksen hajonnasta aiheutuvaa epävarmuutta kuvaa keskiarvon keskivirhe
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
761121P-01 FYSIIKAN LABORATORIOTYÖT 1. Oulun yliopisto Fysiikan tutkinto-ohjelma Kevät 2016
 1 76111P-01 FYSIIKAN LABORATORIOTYÖT 1 Oulun yliopisto Fysiikan tutkinto-ohjelma Kevät 016 JOHDANTO Fysiikassa pyritään löytämään luonnosta lainalaisuuksia, joita voidaan mitata kokeellisesti ja kuvata
1 76111P-01 FYSIIKAN LABORATORIOTYÖT 1 Oulun yliopisto Fysiikan tutkinto-ohjelma Kevät 016 JOHDANTO Fysiikassa pyritään löytämään luonnosta lainalaisuuksia, joita voidaan mitata kokeellisesti ja kuvata
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
Reaktiolämpö KINEETTINEN ENERGIA POTENTIAALI- ENERGIA
 POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
Termodynamiikan mukaan ideaalikaasujen molaaristen lämpökapasiteettien erotus on yleinen kaasuvakio R
 ADIABAATTIVAKIO 1 Johdanto Aineen ominaislämpökapasiteetti c kertoo kuinka paljon lämpöä vaaditaan aineen lämpötilan kasvattamiseen massayksikköä kohden. Kiinteillä ja nestemäisillä aineilla ominaislämpö
ADIABAATTIVAKIO 1 Johdanto Aineen ominaislämpökapasiteetti c kertoo kuinka paljon lämpöä vaaditaan aineen lämpötilan kasvattamiseen massayksikköä kohden. Kiinteillä ja nestemäisillä aineilla ominaislämpö
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
Limsan sokeripitoisuus
 KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Standarditilat. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 2 - Luento 2. Tutustua standarditiloihin
 Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
PERMITTIIVISYYS. 1 Johdanto. 1.1 Tyhjiön permittiivisyyden mittaaminen tasokondensaattorilla . (1) , (2) (3) . (4) Permittiivisyys
 PERMITTIIVISYYS 1 Johdanto Tarkastellaan tasokondensaattoria, joka koostuu kahdesta yhdensuuntaisesta metallilevystä Siirretään varausta levystä toiseen, jolloin levyissä on varaukset ja ja levyjen välillä
PERMITTIIVISYYS 1 Johdanto Tarkastellaan tasokondensaattoria, joka koostuu kahdesta yhdensuuntaisesta metallilevystä Siirretään varausta levystä toiseen, jolloin levyissä on varaukset ja ja levyjen välillä
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti
 CHEM-C2200 Kemiallinen termodynamiikka Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti Työohje 1 Johdanto Happo-emäsindikaattorina käytetty bromitymolisininen muuttaa
CHEM-C2200 Kemiallinen termodynamiikka Työ 1: ph-indikaattorin tasapainovakion arvon määrittäminen spektrofotometrisesti Työohje 1 Johdanto Happo-emäsindikaattorina käytetty bromitymolisininen muuttaa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Työselostusohjeen käyttäjälle
 CHEM-C2200 Kemiallinen termodynamiikka TYÖN NIMI Selostuksen tekijä Kaisa Kemisti, 43210A Työpari Teemu Teekkari, 121212 Assistentti Aapo Assistentti Työ suoritettu Selostus jätetty Palautettu korjattuna
CHEM-C2200 Kemiallinen termodynamiikka TYÖN NIMI Selostuksen tekijä Kaisa Kemisti, 43210A Työpari Teemu Teekkari, 121212 Assistentti Aapo Assistentti Työ suoritettu Selostus jätetty Palautettu korjattuna
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka. Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU
 MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
MIKKELIN AMMATTIKORKEAKOULU Tekniikka ja liikenne / Sähkövoimatekniikka T8415SJ Energiatekniikka Hannu Sarvelainen HÖYRYKATTILAN SUUNNITTELU HARJOITUSTYÖOHJE SISÄLLYS SYMBOLILUETTELO 3 1 JOHDANTO 4 2 TYÖOHJE
LIITE 1 VIRHEEN ARVIOINNISTA
 1 Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi miten uudenaikainen tai kallis tahansa ja mittaaja olisi alansa huippututkija Tästä johtuen mittaustuloksista
1 Mihin tarvitset virheen arviointia? Mittaustuloksiin sisältyy aina virhettä, vaikka mittauslaite olisi miten uudenaikainen tai kallis tahansa ja mittaaja olisi alansa huippututkija Tästä johtuen mittaustuloksista
Ainemäärien suhteista laskujen kautta aineiden määriin
 REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
1. Laske ideaalikaasun tilavuuden lämpötilakerroin (1/V)(dV/dT) p ja isoterminen kokoonpuristuvuus (1/V)(dV/dp) T.
 S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
S-35, Fysiikka III (ES) välikoe Laske ideaalikaasun tilavuuden lämpötilakerroin (/V)(dV/d) p ja isoterminen kokoonpuristuvuus (/V)(dV/dp) ehtävän pisteyttäneen assarin kommentit: Ensimmäisen pisteen sai
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Perusopintojen Laboratoriotöiden Työselostus 1
 Perusopintojen Laboratoriotöiden Työselostus 1 Kalle Hyvönen Työ tehty 1. joulukuuta 008, Palautettu 30. tammikuuta 009 1 Assistentti: Mika Torkkeli Tiivistelmä Laboratoriossa tehdyssä ensimmäisessä kokeessa
Perusopintojen Laboratoriotöiden Työselostus 1 Kalle Hyvönen Työ tehty 1. joulukuuta 008, Palautettu 30. tammikuuta 009 1 Assistentti: Mika Torkkeli Tiivistelmä Laboratoriossa tehdyssä ensimmäisessä kokeessa
Muita lämpökoneita. matalammasta lämpötilasta korkeampaan. Jäähdytyksen tehokerroin: Lämmityksen lämpökerroin:
 Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
Muita lämpökoneita Nämäkin vaativat ovat työtälämpövoimakoneiden toimiakseen sillä termodynamiikan pääsääntö Lämpökoneita lisäksi laitteet,toinen jotka tekevät on Clausiuksen mukaan: laiteilmalämpöpumppu
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1)
 MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Differentiaalilaskennan tehtäviä
 Differentiaalilaskennan tehtäviä DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona 2. Derivoimiskaavat 2.1
Differentiaalilaskennan tehtäviä DIFFERENTIAALILASKENTA 1. Raja-arvon käsite, derivaatta raja-arvona 1.1 Raja-arvo pisteessä 1.2 Derivaatan määritelmä 1.3 Derivaatta raja-arvona 2. Derivoimiskaavat 2.1
Korkealämpötilakemia
 1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
1.11.217 Korkealämpötilakemia Standarditilat Ti 1.11.217 klo 8-1 SÄ11 Tavoite Tutustua standarditiloihin liuosten termodynaamisessa mallinnuksessa Miksi? Millaisia? Miten huomioidaan tasapainotarkasteluissa?
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
Oppikirjan tehtävien ratkaisut
 Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Lämmityksen lämpökerroin: Jäähdytin ja lämmitin ovat itse asiassa sama laite, mutta niiden hyötytuote on eri, jäähdytyksessä QL ja lämmityksessä QH
 Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
Muita lämpökoneita Nämäkin vaativat työtä toimiakseen sillä termodynamiikan toinen pääsääntö Lämpökoneita ovat lämpövoimakoneiden lisäksi laitteet, jotka tekevät on Clausiuksen mukaan: Mikään laite ei
1.1 Tyhjiön permittiivisyyden mittaaminen tasokondensaattorilla
 PERMITTIIVISYYS Johdanto Tarkastellaan tasokondensaattoria, joka koostuu kahdesta yhdensuuntaisesta metallilevystä. Siirretään varausta levystä toiseen, jolloin levyissä on varaukset +Q ja Q ja levyjen
PERMITTIIVISYYS Johdanto Tarkastellaan tasokondensaattoria, joka koostuu kahdesta yhdensuuntaisesta metallilevystä. Siirretään varausta levystä toiseen, jolloin levyissä on varaukset +Q ja Q ja levyjen
Spektrofotometria ja spektroskopia
 11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
Ohjeellinen pituus: 2 3 sivua. Vastaa joko tehtävään 2 tai 3
 PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
PHYS-A0120 Termodynamiikka, syksy 2017 Kotitentti Vastaa tehtäviin 1, 2/3, 4/5, 6/7, 8 (yhteensä viisi vastausta). Tehtävissä 1 ja 7 on annettu ohjeellinen pituus, joka viittaa 12 pisteen fontilla sekä
Torsioheiluri IIT13S1. Selostuksen laatija: Eerik Kuoppala. Ryhmä B3: Eerik Kuoppala G9024 Petteri Viitanen G8473
 Torsioheiluri IIT3S Selostuksen laatija: Eerik Kuoppala Ryhmä B3: Eerik Kuoppala G904 Petteri Viitanen G8473 Mittauspäivämäärä:..4 Selostuksen jättöpäivä: 4.3.4 Torsioheilurin mitatuilla neljän jakson
Torsioheiluri IIT3S Selostuksen laatija: Eerik Kuoppala Ryhmä B3: Eerik Kuoppala G904 Petteri Viitanen G8473 Mittauspäivämäärä:..4 Selostuksen jättöpäivä: 4.3.4 Torsioheilurin mitatuilla neljän jakson
LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä
 LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä. Diffuusio yksiulotteisessa epäjärjestäytyneessä hilassa E J ii, J ii, + 0 E b, i E i i i i+ x Kuva.:
LASKENNALLISEN TIETEEN OHJELMATYÖ: Diffuusion Monte Carlo -simulointi yksiulotteisessa systeemissä. Diffuusio yksiulotteisessa epäjärjestäytyneessä hilassa E J ii, J ii, + 0 E b, i E i i i i+ x Kuva.:
Nimi: Muiden ryhmäläisten nimet:
 Nimi: Muiden ryhmäläisten nimet: PALKKIANTURI Työssä tutustutaan palkkianturin toimintaan ja havainnollistetaan sen avulla pienten ainepitoisuuksien havainnointia. Työn mittaukset on jaettu kolmeen osaan,
Nimi: Muiden ryhmäläisten nimet: PALKKIANTURI Työssä tutustutaan palkkianturin toimintaan ja havainnollistetaan sen avulla pienten ainepitoisuuksien havainnointia. Työn mittaukset on jaettu kolmeen osaan,
1. Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta
 766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
766328A Termofysiikka Harjoitus no. 5, ratkaisut syyslukukausi 204). Yksiulotteisen harmonisen oskillaattorin energiatilat saadaan lausekkeesta E n n + ) ω, n 0,, 2,... 2 a) Oskillaattorin partitiofunktio
PROSESSISUUNNITTELUN SEMINAARI. Luento 5.3.2012 3. vaihe
 PROSESSISUUNNITTELUN SEMINAARI Luento 5.3.2012 3. vaihe 1 3. Vaihe Sanallinen prosessikuvaus Taselaskenta Lopullinen virtauskaavio 2 Sanallinen prosessikuvaus Prosessikuvaus on kirjallinen kuvaus prosessin
PROSESSISUUNNITTELUN SEMINAARI Luento 5.3.2012 3. vaihe 1 3. Vaihe Sanallinen prosessikuvaus Taselaskenta Lopullinen virtauskaavio 2 Sanallinen prosessikuvaus Prosessikuvaus on kirjallinen kuvaus prosessin
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kohti entalpiamuutoksiin liittyviä laskuja
 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Kohti entalpiamuutoksiin liittyviä laskuja Ilona Linnavuori Kemian opettajankoulutusyksikkö, Helsingin yliopisto ilona.linnavuori@helsinki.fi Tiivistelmä
KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Kohti entalpiamuutoksiin liittyviä laskuja Ilona Linnavuori Kemian opettajankoulutusyksikkö, Helsingin yliopisto ilona.linnavuori@helsinki.fi Tiivistelmä
Tuulen nopeuden mittaaminen
 KON C3004 Kone ja rakennustekniikan laboratoriotyöt Koesuunnitelma / ryhmä K Tuulen nopeuden mittaaminen Matias Kidron 429542 Toni Kokkonen 429678 Sakke Juvonen 429270 Kansikuva: http://www.stevennoble.com/main.php?g2_view=core.downloaditem&g2_itemid=12317&g2_serialnumber=2
KON C3004 Kone ja rakennustekniikan laboratoriotyöt Koesuunnitelma / ryhmä K Tuulen nopeuden mittaaminen Matias Kidron 429542 Toni Kokkonen 429678 Sakke Juvonen 429270 Kansikuva: http://www.stevennoble.com/main.php?g2_view=core.downloaditem&g2_itemid=12317&g2_serialnumber=2
Käyttöohje HI98127 / HI98128. Pietiko Oy Tykistökatu 4 B 310(ElektroCity) 20520 Turku, puh (02) 2514402, fax (02) 2510015 www.pietiko.
 HI98127 / Tekniset tiedot Mittausalue HI98127-2,0...16,0 ph -2,00...16,00 ph Lämpötila -5...+60 C Resoluutio HI98127 0,1 ph 0,01 ph Lämpötila 0,1 C Tarkkuus HI98127 ± 0,1 ph ± 0,001 ph Lämpötila ± 0,5
HI98127 / Tekniset tiedot Mittausalue HI98127-2,0...16,0 ph -2,00...16,00 ph Lämpötila -5...+60 C Resoluutio HI98127 0,1 ph 0,01 ph Lämpötila 0,1 C Tarkkuus HI98127 ± 0,1 ph ± 0,001 ph Lämpötila ± 0,5
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
RAKEISUUSMÄÄRITYS, HYDROMETRIKOE
 Kiviainekset, yleisominaisuudet PANK-2103 PANK RAKEISUUSMÄÄRITYS, HYDROMETRIKOE PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: 17.4.2002 Korvaa menetelmän: 20.3.1995 1. MENETELMÄN TARKOITUS 2. MENETELMÄN SOVELTAMISALUE
Kiviainekset, yleisominaisuudet PANK-2103 PANK RAKEISUUSMÄÄRITYS, HYDROMETRIKOE PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: 17.4.2002 Korvaa menetelmän: 20.3.1995 1. MENETELMÄN TARKOITUS 2. MENETELMÄN SOVELTAMISALUE
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 7.11. ja tiistai 8.11. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
KÄYTTÖOHJE LÄMPÖTILA-ANEMOMETRI DT-619
 KÄYTTÖOHJE LÄMPÖTILA-ANEMOMETRI DT-619 2007 S&A MATINTUPA 1. ILMAVIRTAUKSEN MITTAUS Suora, 1:n pisteen mittaus a) Kytke mittalaitteeseen virta. b) Paina UNITS - näppäintä ja valitse haluttu mittayksikkö
KÄYTTÖOHJE LÄMPÖTILA-ANEMOMETRI DT-619 2007 S&A MATINTUPA 1. ILMAVIRTAUKSEN MITTAUS Suora, 1:n pisteen mittaus a) Kytke mittalaitteeseen virta. b) Paina UNITS - näppäintä ja valitse haluttu mittayksikkö
33 SOLENOIDIN JA TOROIDIN MAGNEETTIKENTTÄ
 TYÖOHJE 14.7.2010 JMK, TSU 33 SOLENOIDIN JA TOROIDIN MAGNEETTIKENTTÄ Laitteisto: Kuva 1. Kytkentä solenoidin ja toroidin magneettikenttien mittausta varten. Käytä samaa digitaalista jännitemittaria molempien
TYÖOHJE 14.7.2010 JMK, TSU 33 SOLENOIDIN JA TOROIDIN MAGNEETTIKENTTÄ Laitteisto: Kuva 1. Kytkentä solenoidin ja toroidin magneettikenttien mittausta varten. Käytä samaa digitaalista jännitemittaria molempien
ja piirrä sitä vastaavat kaksi käyrää ja tarkista ratkaisusi kuvastasi.
 Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt
 KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
Oletetaan, että virhetermit eivät korreloi toistensa eikä faktorin f kanssa. Toisin sanoen
 Yhden faktorin malli: n kpl sijoituskohteita, joiden tuotot ovat r i, i =, 2,..., n. Olkoon f satunnaismuuttuja ja oletetaan, että tuotot voidaan selittää yhtälön r i = a i + b i f + e i avulla, missä
Yhden faktorin malli: n kpl sijoituskohteita, joiden tuotot ovat r i, i =, 2,..., n. Olkoon f satunnaismuuttuja ja oletetaan, että tuotot voidaan selittää yhtälön r i = a i + b i f + e i avulla, missä
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics)
 2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
2 Termodynamiikan ensimmäinen pääsääntö (First Law of Thermodynamics) 1 Tässä luvussa päästää käsittelemään lämmön ja mekaanisen työn välistä suhdetta. 2 Näistä molemmat ovat energiaa eri muodoissa, ja
Havaitsevan tähtitieteen peruskurssi I
 Havaintokohteita 9. Polarimetria Lauri Jetsu Fysiikan laitos Helsingin yliopisto Havaintokohteita Polarimetria Havaintokohteita (kuvat: @phys.org/news, @annesastronomynews.com) Yleiskuvaus: Polarisaatio
Havaintokohteita 9. Polarimetria Lauri Jetsu Fysiikan laitos Helsingin yliopisto Havaintokohteita Polarimetria Havaintokohteita (kuvat: @phys.org/news, @annesastronomynews.com) Yleiskuvaus: Polarisaatio
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Perjantai VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN
 Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
AKK-MOTORSPORT ry Katsastuksen käsikirja ISKUTILAVUUDEN MITTAAMINEN. 1. Tarkastuksen käyttö
 ISKUTILAVUUDEN MITTAAMINEN 1. Tarkastuksen käyttö 2. Määritelmät 3. Välineet 4. Olosuhteet Kyseisen ohjeen tarkoituksena on ohjeistaa moottorin iskutilavuuden mittaaminen ja laskeminen. Kyseinen on mahdollista
ISKUTILAVUUDEN MITTAAMINEN 1. Tarkastuksen käyttö 2. Määritelmät 3. Välineet 4. Olosuhteet Kyseisen ohjeen tarkoituksena on ohjeistaa moottorin iskutilavuuden mittaaminen ja laskeminen. Kyseinen on mahdollista
DEE Sähkömagneettisten järjestelmien lämmönsiirto Ehdotukset harjoituksen 2 ratkaisuiksi
 DEE-4000 Sähkömagneettisten järjestelmien lämmönsiirto Ehdotukset harjoituksen ratkaisuiksi Yleistä asiaa lämmönjohtumisen yleiseen osittaisdifferentiaaliyhtälöön liittyen Lämmönjohtumisen yleinen osittaisdifferentiaaliyhtälön
DEE-4000 Sähkömagneettisten järjestelmien lämmönsiirto Ehdotukset harjoituksen ratkaisuiksi Yleistä asiaa lämmönjohtumisen yleiseen osittaisdifferentiaaliyhtälöön liittyen Lämmönjohtumisen yleinen osittaisdifferentiaaliyhtälön
T H V 2. Kuva 1: Stirling kiertoprosessi. Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista (kts. kuva 1):
 1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
1 c 3 p 2 T H d b T L 4 1 a V Kuva 1: Stirling kiertoprosessi. Stirlingin kone Ideaalisen Stirlingin koneen sykli koostuu neljästä osaprosessista kts. kuva 1: 1. Työaineen ideaalikaasu isoterminen puristus
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PANK-4113 PANK PÄÄLLYSTEEN TIHEYS, DOR -MENETELMÄ. Asfalttipäällysteet ja massat, perusmenetelmät
 Asfalttipäällysteet ja massat, perusmenetelmät PANK-4113 PANK PÄÄLLYSTEEN TIHEYS, DOR -MENETELMÄ PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: Korvaa menetelmän: 13.05.2011 17.04.2002 1. MENETELMÄN TARKOITUS
Asfalttipäällysteet ja massat, perusmenetelmät PANK-4113 PANK PÄÄLLYSTEEN TIHEYS, DOR -MENETELMÄ PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: Korvaa menetelmän: 13.05.2011 17.04.2002 1. MENETELMÄN TARKOITUS
