Kohti entalpiamuutoksiin liittyviä laskuja
|
|
|
- Mauno Laine
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Kohti entalpiamuutoksiin liittyviä laskuja Ilona Linnavuori Kemian opettajankoulutusyksikkö, Helsingin yliopisto Tiivistelmä Lukion kemian KE3-kurssin (Reaktiot ja energia) keskeisiin sisältöihin kuuluu energian muutokset kemiallisissa reaktioissa (Opetushallitus, 2003). Tässä yhteydessä tavallisesti suoritetaan kalorimetrisia mittauksia ja lasketaan mittauksiin perustuvia entalpiamuutoslaskuja. Ennen siirtymistä mittauksista laskuihin on opetuksessa hyvä huomioida muutamia asioita, joita tämä artikkeli esittelee. Molekyylitason potentiaalienergian ja hiukkasten liike-energian oppimisen tueksi olen luonut kaksi lyhyttä animaatiota, joita voidaan hyödyntää opetuksessa aiheen yhteydessä. 1 Johdanto Tutkimusten mukaan kemian laskemista vaativien ongelmatehtävien onnistuneessa ratkaisussa laskuihin liittyvien käsitteiden ymmärtäminen on keskeisessä osassa (esim. Bodner & Herron, 2002; BouJaoude & Barakat, 2000). Vaikka kalorimetriseen mittaukseen perustuvat entalpiamuutoslaskut ovat suhteellisen suoraviivaisia, on opiskelijoilla niissä vaikeuksia jopa yliopistotasolla (Greenbowe & Meltzer, 2003). Kemiallisten reaktioiden energiamuutoksiin liittyvään käsitteelliseen ymmärrykseen tulee siis opetuksessa selkeästi panostaa. Tämän artikkelin luku 2 käsittelee lyhyesti kemiallisten reaktioiden energiamuutoksiin ja kalorimetrisiin mittauksiin liittyvää kemiaa jossakin määrin hieman yli yleisimpien lukion oppikirjojen tason. Tutkimusten mukaan energia on opiskelijoille hyvin vaikea aihealue (esim. Lundell & Aksela, 2004). Luvussa 3 esitelläänkin liikkuvia animaatioita molekyylitason energiakäsitteiden oppimisen tukena. Luku 4 puolestaan keskittyy tarkemmin kalorimetrisiin mittauksiin perustuvien laskutehtävien kannalta oleellisiin asioihin ja käsitteisiin. Jos ei näihin tietoisesti kiinnitetä huomiota, jäävät ne opetuksessa helposti taka-alalle. 2 Energian muutokset kemiallisissa reaktioissa Kun puhutaan kemiallisten reaktioiden energian muutoksista, jaetaan universumi kahteen osaan: kemialliseen systeemiin ja ympäristöön. Systeemillä tarkoitetaan tässä tapauksessa reaktion lähtöaineita ja tuotteita. Ympäristö puolestaan sisältää kaiken muun ympärillä olevan: reaktioastian, huoneen ja niin edelleen. (Zumdahl & Zumdahl, 2007) Mikäli systeemi luovuttaa lämpöenergiaa ympäristöönsä, kutsutaan reaktiota eksotermiseksi. Mikäli systeemi taas sitoo lämpöenergiaa ympäristöstään, on reaktio endoterminen. Molekyylitasolla reaktiossa vapautuvan tai sitoutuvan energian taustalla on 195
2 TUOMISTO ET AL. ero reaktion lähtöaineiden ja tuotteiden potentiaalienergioissa. (Tro, 2008; Zumdahl & Zumdahl, 2007) Pohjimmiltaan potentiaalienergia on ns. varastoitunutta energiaa, joka aiheutuu jonkin objektin kokemista vetovoimista ja repulsioista suhteessa muihin objekteihin (Brown, LeMay, Bursten, Murphy & Woodward, 2012). Molekyylitason kemiallinen potentiaalienergia aiheutuu varautuneiden hiukkasten välisistä sähköstaattisista vuorovaikutuksista tarkemmin sanoen vuorovaikutuksista systeemin atomien ja molekyylien sisältämien protonien ja elektronien välillä (Brown, LeMay, Bursten, Murphy & Woodward, 2012; Tro, 2008). Kemiallisissa reaktioissa sidoksia katkeaa ja uusia muodostuu. Eksotermisissa reaktioissa protonit ja elektronit uudelleenjärjestäytyvät korkeamman potentiaalienergian tasolta matalammalle potentiaalienergian tasolle, mikä havaitaan lämpöenergian vapautumisena. Endotermisissa reaktioissa puolestaan protonit ja elektronit järjestäytyvät matalamman potentiaalienergian tasolta korkeammalle potentiaalienergian tasolle, jolloin lämpöenergiaa sitoutuu. (Tro, 2008) 2.1 Reaktion entalpiamuutoksen määrittäminen kalorimetrissä Kun kemiallinen reaktio tapahtuu vakiopaineessa, on reaktion entalpiamuutos ΔH yhtä suuri kuin reaktiossa vapautuvan tai sitoutuvan lämpöenergian määrä. Vesiliuoksessa tapahtuvan kemiallisen reaktion entalpiamuutos voidaan siis määrittää kokeellisesti ympäristön kautta käyttämällä vakiopaine-kalorimetriä. Tähän tarkoitukseen käy esimerkiksi yksinkertainen, kahdesta styroksisesta kertakäyttömukista rakennettu kahvikuppi-kalorimetri. (Tro, 2008; Zumdahl & Zumdahl, 2007) Vesiliuoksessa tapahtuvan eksotermisen reaktion vapauttama lämpöenergia kasvattaa liuotinpartikkeleiden satunnaista liikettä, mikä havaitaan reaktioseoksen lämpötilan kohoamisena (Zumdahl & Zumdahl, 2007). Termodynamiikan ensimmäisen pääsäännön mukaan universumin energia on vakio. Kun siis oletetaan kalorimetrin eristyksen olevan täydellinen, voidaan reaktion entalpiamuutos määrittää ympäristön kautta lämpötilan kasvun, liuoksen massan ja liuoksen ominaislämpökapasiteetin perusteella. Tällöin entalpiamuutos ΔH on itseisarvoltaan yhtä suuri kuin vesiliuoksen sitoma lämpömäärä Q = c m T. Tavallisesti laskuissa liuos ajatellaan puhtaana vetenä, jolloin kaavan suureet c ja m viittaavat veden ominaislämpökapasiteettiin ja massaan. (Tro, 2008; Zumdahl & Zumdahl, 2007) Endotermisen reaktion tapauksessa reaktion entalpiamuutos voidaan määrittää vastaavasti vesiliuoksen vapauttaman lämpömäärän perusteella. 2.2 Entalpiamuutoksen etumerkki Määritelmän mukaan kemiallisen reaktion entalpiamuutos saadaan yhtälöstä: H reaktio = H tuotteet H lähtöaineet. Eksotermisen reaktion tapauksessa lämpöenergiaa vapautuu ympäristöön, jolloin reaktiotuotteiden entalpia on pienempi kuin lähtöaineiden. Reaktion entalpiamuutos ΔH on siis negatiivinen. Endotermisen reaktion tapauksessa systeemi 196
3 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: puolestaan sitoo lämpöenergiaa, jolloin reaktiotuotteiden entalpia on suurempi kuin lähtöaineiden. Entalpiamuutos ΔH on positiivinen. (Zumdahl & Zumdahl, 2007) 3 Syvyyttä molekyylitason energiakäsitteiden oppimiseen Energiaan ja energian muutoksiin liittyvien käsitteiden ja aiheiden on todettu olevan vaikeita lukio-opiskelijoille (esim. Chang, 2009; Cooper & Klymkowsky, 2013). Etenkin energian ymmärtäminen ja potentiaalienergian käsite molekyylitason ilmiöinä tuottavat opiskelijoille hankaluuksia (Cooper & Klymkowsky, 2013). Syitä vaikeuksiin on monia. Esimerkkeinä mainittakoon: 1) fysiikasta tuttu makroskooppinen lähestymistapa energiakäsitteisiin, 2) oppimista hankaloittavat vaihtoehtoiset käsitykset, 3) energiamuutoksiin liittyvien määritelmien perustuminen oletuksiin, joihin ei kiinnitetä riittävästi huomiota opetuksessa ja 4) kemian kurssien epäonnistuminen molekyylitason energiailmiöiden linkittämisessä makroskooppiselle tasolle (Chang, 2009; Cooper & Klymkowsky, 2013). Energia-aiheen oppimisen tueksi tarvitaankin uusia lähestymistapoja. Yhden hyvän välineen energian havainnollistamiseen kemian opetuksessa antaa molekyylimallinnus. (Lundell & Aksela, 2004) 3.1 Liikkuvat visualisoinnit oppimisen tukena Tutkimusten mukaan liikkuvat visualisoinnit voivat tehokkaammin kehittää opiskelijoiden ymmärrystä abstrakteista käsitteistä staattisiin kuviin verrattuna (Ryoo & Linn, 2012). Reaktioiden energiamuutoksiin ja entalpiaan liittyviä käsitteitä voidaankin selventää esimerkiksi tietokoneanimaatioiden kautta. Molekyylitason potentiaalienergian ja liikeenergian käsitteiden ymmärrystä tukemaan olen luonut Spartan Student - molekyylimallinnusohjelman avulla kaksi animaatiota, joita voidaan hyödyntää oppitunneilla ennen entalpiamuutoslaskuihin siirtymistä. Oppitunneilla käytettävät animaatiot toimivat parhaiten sanallisen selityksen kanssa: opiskelijat saavat samanaikaisesti sekä visuaalista että sanallista informaatiota (esim. Mayer & Anderson, 1991). Kuvan 1 animaatio havainnollistaa etaanimolekyylin potentiaalienergian muuttumista hiili-hiilisidoksen kiertyessä. Animaation tarkastelun aikana opettajan kannattaa selostaa, mistä kemiallinen potentiaalienergia aiheutuu ja miksi etaanimolekyylin potentiaalienergia animaatiossa vaihtelee. Jos tietokoneanimaatioita käytetään oppitunneilla yhdessä kokeellisten demonstraatioiden rinnalla, opiskelijat pystyvät paremmin linkittämään kemian submikroskooppisen, makroskooppisen ja symbolisen tason toisiinsa (Russell, Kozma, Jones, Wykoff, Marx & Davis, 1997, viitattu teoksessa Burke, Greenbowe & Windschitl, 1998). Siksi potentiaalienergia-animaation yhteydessä oppitunneilla on hyödyllistä tarkastella myös jotakin konkreettista eksotermista tai endotermista reaktiota. Samalla voidaan opiskelijoiden kanssa keskustella, mistä kyseisessä 197
4 TUOMISTO ET AL. Kuva 1 Kemiallinen potentiaalienergia aiheutuu sähköisesti varautuneiden protonien ja elektronien välisistä vuorovaikutuksista. Etaanimolekyylin potentiaalienergia muuttuu hiili-hiilisidoksen kiertyessä, kun molekyylin sisältämien protonien ja elektronien asemat toisiinsa nähden muuttuvat. Animaatio on käyttökelpoinen myös KE2-kurssilla (Kemian mikromaailma) konformaatioisomerian yhteydessä. reaktiossa vapautuva tai sitoutuva energia on peräisin. Animaation, opettajan selostuksen ja demonstraation kautta opiskelijan on todennäköisesti helpompi linkittää makrotasolla havaittava lämpötilanmuutos sub-mikrotason ilmiöihin ja edelleen helpompi ymmärtää reaktion energiamuutoksen taustalla olevan ero reaktion lähtöaineiden ja reaktiotuotteiden potentiaalienergioissa. Entalpiaan liittyy myös laajempi sisäenergian käsite: systeemin sisäenergia on sen kaikkien partikkelien kineettisten ja potentiaalienergioiden summa (Tro, 2008). Tämän ymmärtämistä tukee potentiaalienergia-animaation rinnalla tarkasteltava animaatio hiukkasten liike-energian ilmentymisestä (Kuva 2). Animaatiota voidaan hyödyntää myös muissa yhteyksissä, kun puhutaan atomien ja molekyylien liikkeistä. Kuva 2 Hiukkasten liike-energia ilmenee aineen rakenneosien lämpöliikkeenä, hiukkasten pyörimisenä sekä sidosten taipumisena ja venymisenä. 4 Tarkkana eksotermisten ja endotermisten reaktioiden kanssa! Opiskelijan näkökulmasta ekso- ja endotermisten reaktioiden määritelmät voivat olla hämmentäviä ja herättää kysymyksiä: Jos reaktio on endoterminen ja se sitoo lämpöenergiaa, miten reaktioseoksen lämpötila voi laskea? ; Toisaalta, jos reaktio on eksoterminen ja se vapauttaa lämpöenergiaa ympäristöön, miten reaktioseos voi kuumentua? (Chang, 2009) Mahdollinen syy hämmennykseen on siinä, että ekso- ja endotermisten reaktioiden määritelmät perustuvat oletuksiin, joiden tarkempi käsittely opetuksessa jää helposti taka- 198
5 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: alalle. Jotta opiskelijat voisivat ymmärtää ja käyttää näitä käsitteitä oikein, on heidän ymmärrettävä reaktioiden energian muutokset kemiallisen systeemin ja ympäristön kautta. (Chang, 2009) Vaikka kemistille on ilmeistä, että reaktion lähtöaineet ja tuotteet muodostavat systeemin ja reaktioastia, vesiliuos, käsi tai lämpömittari ympäristön, ei tämä ole selvää aloittelijalle (Chang, 2009; Greenbowe & Meltzer, 2003). Kemiallisen systeemin ja ympäristön väliset erot on siis syytä ottaa erillisen tarkastelun kohteeksi, jotta mahdolliselta sekaannukselta vältyttäisiin. Tämä onnistuu esimerkkireaktioiden avulla. Niissä opiskelijat itse määrittävät kemiallisen systeemin ja ympäristön (Kuva 3). Kuva 3 Kemiallisen systeemin ja ympäristön eroja voidaan pohtia esimerkiksi yksinkertaisen ja turvallisen, ruokasoodan ja etikan välisen endotermisen reaktion avulla. Vaikka kalorimetriseen mittaukseen perustuva entalpiamuutoksen määrittäminen onkin melko suoraviivaista, tekevät opiskelijat virheitä kalorimetrilaskuissa jopa yliopistotasolla. Juuri laskujen näennäisen yksinkertaisuuden vuoksi sekä opettajat että 199
6 TUOMISTO ET AL. opiskelijat helposti unohtavat kiinnittää tarkempaa huomiota laskujen kannalta oleellisiin asioihin. (Greenbowe & Meltzer, 2003) Tutkimusten mukaan yleinen opiskelijoiden tekemä virhe vesiliuoksessa tapahtuvan reaktion entalpiamuutosta määritettäessä on se, että veden massan sijaan kaavassa Q = c m T käytetään kokonaismassana m reagenssien massoja (Greenbowe & Meltzer, 2003). Tämä todennäköisesti viittaa juuri ymmärryksen puutteeseen kemiallisen systeemin ja ympäristön käsitteissä (Chang, 2009). Kemiallisen systeemin ja ympäristön välisen eron sekä ekso- ja endotermisten reaktioiden käsitteiden ymmärtäminen on siis oleellista myös kalorimetrilaskujen kannalta. Vasta käsitteellisen ymmärryksen pohjalta reaktion entalpiamuutoksen määrittäminen ja laskeminen ympäristön kautta selkiytyvät. Opiskelijoita on autettava ymmärtämään, että kaavassa Q = c m T lämpötilanmuutos T viittaa koko kalorimetrin sisältöön, jolloin myös massan m, ominaislämpökapasiteetin c ja vesiliuoksen sitoman tai vapauttaman lämpömäärän Q on viitattava koko kalorimetrin sisältöön (Greenbowe & Meltzer, 2003). Toisaalta opiskelijat eivät kiinnitä tarpeeksi huomiota reaktion entalpiamuutoksen H etumerkkiin. Siksi merkkisääntöjen johdonmukainen huomioiminen on tärkeää. Opiskelijoita voidaan esimerkiksi ohjeistaa pohtimaan määritettävän suureen etumerkki heti kalorimetrilaskujen ensimmäisenä vaiheena. (Greenbowe & Meltzer, 2003) Lähteet Bodner, G. M. & Herron, J. D. (2002). Problem-solving in Chemistry. Teoksessa J. K. Gilbert, O. Jong, R. Justi, D. F. Treagust & J. H. Driel (Toim.), Chemical Education: Towards Researchbased Practice (luku 11, s ). Alankomaat: Kluwer Academic Publishers. BouJaoude, S. & Barakat, H. (2000). Secondary school students difficulties with stoichiometry. School Science Review, 81(296), Brown, T. L., LeMay, H. E., Bursten, B. E., Murphy, C. J. & Woodward, P.M. (2012). Chemistry, The Central Science (12. painos). Lontoo: Pearson Prentice Hall. Burke, K. A., Greenbowe, T. J. & Windschitl, M. A. (1998). Developing and Using Conceptual Computer Animations for Chemistry Instruction. Journal of Chemical Education, 75(12), Chang, K. (2009). Learning thermochemistry: Understanding the challenges and promoting its success. Väitöskirja. University of California, Berkeley. Cooper, M. M. & Klymkowsky, M. W. (2013). The Trouble with Chemical Energy: Why Understanding Bond Energies Requires an Interdisciplinary Systems Approach. CBE Life Sciences Education, 12, Greenbowe, T. J. & Meltzer, D. E. (2003). Student learning of thermochemical concepts in the context of solution calorimetry. International Journal of Science Education, 25, Lundell, J. & Aksela, M. (2004). Molekyylimallinnus kemian opetuksessa, osa 2: Molekyylimallinnus ja energia. Dimensio, 1, Mayer, R. E. & Anderson, R. B. (1991). Animations Need Narrations: An Experimental Test of a Dual- Coding Hypothesis. Journal of Educational Psychology, 83(4), Opetushallitus. (2003). Lukion opetussuunnitelman perusteet. Helsinki: Opetushallitus. 200
7 KEMIAN KÄSITTEIDEN JA ILMIÖIDEN OPETUS SEKÄ OPPIMINEN: Ryoo, K. & Linn, M. C. (2012). Can Dynamic Visualizations Improve Middle School Students Understanding of Energy in Photosynthesis? Journal of Research in Science Teaching, 49, Tro, N. J. (2008). Chemistry, A Molecular Approach. Lontoo: Pearson Prentice Hall. Zumdahl, S. S. & Zumdahl, S. A. (2007). Chemistry (7. painos). New York, NY: Houghton Miffin Company. 201
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Reaktiolämpö KINEETTINEN ENERGIA POTENTIAALI- ENERGIA
 POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
Termodynamiikan suureita ja vähän muutakin mikko rahikka
 Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Termodynamiikan suureita ja vähän muutakin mikko rahikka 2006 m@hyl.fi 1 Lämpötila Suure lämpötila kuvaa kappaleen/systeemin lämpimyyttä (huono ilmaisu). Ihmisen aisteilla on hankala tuntea lämpötilaa,
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Työ 3: Veden höyrystymislämmön määritys
 Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
Työ 3: Veden höyrystymislämmön määritys Työryhmä: Tehty (pvm): Hyväksytty (pvm): Hyväksyjä: 1. Tavoitteet Työssä vettä höyrystetään uppokuumentimella ja mitataan jäljellä olevan veden painoa sekä höyrystymiseen
FY9 Fysiikan kokonaiskuva
 FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
FY9 Sivu 1 FY9 Fysiikan kokonaiskuva 6. tammikuuta 2014 14:34 Kurssin tavoitteet Kerrata lukion fysiikan oppimäärä Yhdistellä kurssien asioita toisiinsa muodostaen kokonaiskuvan Valmistaa ylioppilaskirjoituksiin
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
Tieto- ja viestintätekniikka kemian opetuksessa FL Johannes Pernaa Kemian opettajankoulutusyksikkö Kemian laitos
 Tieto- ja viestintätekniikka kemian opetuksessa FL Johannes Pernaa Kemian opettajankoulutusyksikkö Kemian laitos 1 Sisältö Määritelmä ja rajaaminen Lisensiaattitutkielmani tuloksia Tapaus: Molekyylimallinnusta
Tieto- ja viestintätekniikka kemian opetuksessa FL Johannes Pernaa Kemian opettajankoulutusyksikkö Kemian laitos 1 Sisältö Määritelmä ja rajaaminen Lisensiaattitutkielmani tuloksia Tapaus: Molekyylimallinnusta
KE1 Ihmisen ja elinympäristön kemia
 KE1 Ihmisen ja elinympäristön kemia Arvostelu: koe 60 %, tuntitestit (n. 3 kpl) 20 %, kokeelliset työt ja palautettavat tehtävät 20 %. Kurssikokeesta saatava kuitenkin vähintään 5. Uusintakokeessa testit,
KE1 Ihmisen ja elinympäristön kemia Arvostelu: koe 60 %, tuntitestit (n. 3 kpl) 20 %, kokeelliset työt ja palautettavat tehtävät 20 %. Kurssikokeesta saatava kuitenkin vähintään 5. Uusintakokeessa testit,
CHEM-C2200 Kemiallinen termodynamiikka. Työ 2: Kaliumkloridin liukenemisentalpian määrittäminen. Työohje
 CHEM-C2200 Kemiallinen termodynamiikka Työ 2: Kaliumkloridin liukenemisentalpian määrittäminen Työohje 1 Johdanto Kalorimetriassa tutkitaan lämpötilan ja lämpöenergian muutoksia eristetyssä järjestelmässä.
CHEM-C2200 Kemiallinen termodynamiikka Työ 2: Kaliumkloridin liukenemisentalpian määrittäminen Työohje 1 Johdanto Kalorimetriassa tutkitaan lämpötilan ja lämpöenergian muutoksia eristetyssä järjestelmässä.
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
Kertausta 1.kurssista. KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä. Hiilen isotoopit
 KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
KEMIAN MIKROMAAILMA, KE2 Atomin rakenne ja jaksollinen järjestelmä Kertausta 1.kurssista Hiilen isotoopit 1 Isotoopeilla oli ytimessä sama määrä protoneja, mutta eri määrä neutroneja. Ne käyttäytyvät kemiallisissa
Asetyylisalisyylihapon energiaprofiili. - Konformaatioisomeria
 Asetyylisalisyylihapon energiaprofiili - Konformaatioisomeria Kemian mallit ja visualisointi Tom Olsson Simo Tolvanen 25.4.2008 Suoritus Kohderyhmänä on lukion kemian 2- kurssi. Aiheena on Asetyylisalisyylihapon
Asetyylisalisyylihapon energiaprofiili - Konformaatioisomeria Kemian mallit ja visualisointi Tom Olsson Simo Tolvanen 25.4.2008 Suoritus Kohderyhmänä on lukion kemian 2- kurssi. Aiheena on Asetyylisalisyylihapon
Tutkimustietoa oppimisen arvioinnista
 Tutkimustietoa oppimisen arvioinnista Miten arviointi suuntaa oppimista? Viivi Virtanen 28.2.2011 1/10 Millä keinoin opiskelijan saisi oppimaan sen mitä opetan? 2/10 Miten arviointi vaikuttaa siihen, miten
Tutkimustietoa oppimisen arvioinnista Miten arviointi suuntaa oppimista? Viivi Virtanen 28.2.2011 1/10 Millä keinoin opiskelijan saisi oppimaan sen mitä opetan? 2/10 Miten arviointi vaikuttaa siihen, miten
Reaktioyhtälö. Sähköisen oppimisen edelläkävijä www.e-oppi.fi. Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava
 Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 2: Työ ja termodynamiikan 1. pääsääntö Maanantai 6.11. ja tiistai 7.11. Pohdintaa Mitä tai mikä ominaisuus lämpömittarilla
Ideaalikaasulaki. Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua
 Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Ideaalikaasulaki Ideaalikaasulaki on esimerkki tilanyhtälöstä, systeemi on nyt tietty määrä (kuvitteellista) kaasua ja tilanmuuttujat (yhä) paine, tilavuus ja lämpötila Isobaari, kun paine on vakio Kaksi
Kemia. Kemia Tutkii luontoa, sen rakenteita. Tutkii ainetta, sen koostumusta. sekä reaktioita. Eli kuinka aine muuttuu toiseksi aineeksi.
 Tutkii luontoa, sen rakenteita ja ilmiöitä. Tutkii ainetta, sen koostumusta ja ominaisuuksia sekä reaktioita. Eli kuinka aine muuttuu toiseksi aineeksi. 1. oppiaineena ja tieteen alana 2. n opetuksen tavoitteet,
Tutkii luontoa, sen rakenteita ja ilmiöitä. Tutkii ainetta, sen koostumusta ja ominaisuuksia sekä reaktioita. Eli kuinka aine muuttuu toiseksi aineeksi. 1. oppiaineena ja tieteen alana 2. n opetuksen tavoitteet,
782630S Pintakemia I, 3 op
 782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
TUTKIMUKSELLISUUS. LUKION KEMIASSA PÄIVI TOMPERI paivi.tomperi@helsinki.fi KEMIAN OPETUKSEN KESKUS KEMMA HELSINGIN YLIOPISTO
 TUTKIMUKSELLISUUS Kemian opetuksen päivät Oulussa 13.4.2012 LUKION KEMIASSA PÄIVI TOMPERI paivi.tomperi@helsinki.fi KEMIAN OPETUKSEN KESKUS KEMMA HELSINGIN YLIOPISTO MITÄ TUTKIMUKSELLINEN (= INQUIRY) TARKOITTAA?.
TUTKIMUKSELLISUUS Kemian opetuksen päivät Oulussa 13.4.2012 LUKION KEMIASSA PÄIVI TOMPERI paivi.tomperi@helsinki.fi KEMIAN OPETUKSEN KESKUS KEMMA HELSINGIN YLIOPISTO MITÄ TUTKIMUKSELLINEN (= INQUIRY) TARKOITTAA?.
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 28.11. ja tiistai 29.11. Kotitentti Julkaistaan to 8.12., palautus viim. to 22.12.
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 5: Termodynaamiset potentiaalit Ke 9.3.2016 1 AIHEET 1. Muut työn laadut sisäenergiassa
Visualisoinnin ja animaatioiden merkitys kemian opetuksessa.
 Liite 7 - Animaatioryhmä: Suolan liukeneminen Tausta Koulun oppikirjoissa käsitellään suolat ionien yhteydessä. Otavan Avain kurssikirjassa kappaleen 3 nimi on 'ionisidos' ja siinä mainitaan suoloja. Kuvassa
Liite 7 - Animaatioryhmä: Suolan liukeneminen Tausta Koulun oppikirjoissa käsitellään suolat ionien yhteydessä. Otavan Avain kurssikirjassa kappaleen 3 nimi on 'ionisidos' ja siinä mainitaan suoloja. Kuvassa
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
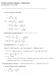 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
sivu 1/7 OPETTAJALLE Työn motivaatio
 sivu 1/7 PETTAJALLE Työn motivaatio Työssä saadaan kemiallinen reaktio näkyväksi käyttämällä katalyyttiä. Työssä katalyyttinä toimii veren hemoglobiinin rauta tai yhtä hyvin liuos joka sisältää esimerkiksi
sivu 1/7 PETTAJALLE Työn motivaatio Työssä saadaan kemiallinen reaktio näkyväksi käyttämällä katalyyttiä. Työssä katalyyttinä toimii veren hemoglobiinin rauta tai yhtä hyvin liuos joka sisältää esimerkiksi
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 /
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 8 / 7.11.2016 v. 02 / T. Paloposki Tämän päivän ohjelma: Sisäenergia (kertaus) termodynamiikan 1. pääsääntö Entropia termodynamiikan 2. pääsääntö 1 Termodynamiikan
13 KALORIMETRI. 13.1 Johdanto. 13.2 Kalorimetrin lämmönvaihto
 13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
13 KALORIMETRI 13.1 Johdanto Kalorimetri on ympäristöstään mahdollisimman täydellisesti lämpöeristetty astia. Lämpöeristyksestä huolimatta kalorimetrin ja ympäristön välinen lämpötilaero aiheuttaa lämmönvaihtoa
PHYS-A0120 Termodynamiikka syksy 2017
 PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
PHYS-A0120 Termodynamiikka syksy 2017 Emppu Salonen Prof. Peter Liljeroth Viikko 5: Termodynaamiset potentiaalit Maanantai 27.11. ja tiistai 28.11. Kotitentti Julkaistaan ti 5.12., palautus viim. ke 20.12.
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka
 Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
Lämpöistä oppia ja energiaa Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2014 Alkudemonstraatio: Käsi lämpömittarina Laitetaan kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä.
kuonasula metallisula Avoin Suljettu Eristetty S / Korkealämpötilakemia Termodynamiikan peruskäsitteitä
 Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
Termodynamiikan peruskäsitteitä The Laws of thermodynamics: (1) You can t win (2) You can t break even (3) You can t get out of the game. - Ginsberg s theorem - Masamune Shirow: Ghost in the shell Systeemillä
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
Termodynamiikka. Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt. ...jotka ovat kaikki abstraktioita
 Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
Termodynamiikka Termodynamiikka on outo teoria. Siihen kuuluvat keskeisinä: Systeemit Tilanmuuttujat Tilanyhtälöt...jotka ovat kaikki abstraktioita Miksi kukaan siis haluaisi oppia termodynamiikkaa? Koska
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2016 Emppu Salonen Lasse Laurson Toni Mäkelä Arttu Lehtinen Luento 6: Vapaaenergia Pe 11.3.2016 1 AIHEET 1. Kemiallinen potentiaali 2. Maxwellin
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Voima ja potentiaalienergia II Energian kvantittuminen
 Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
Voima ja potentiaalienergia II Energian kvantittuminen Mene osoitteeseen presemo.helsinki.fi/kontro ja vastaa kysymyksiin Tavoitteena tällä luennolla Miten määritetään voima kun potentiaalienergia U(x,y,z)
FyKe 7 9 Kemia ja OPS 2016
 Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
1 Eksergia ja termodynaamiset potentiaalit
 1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1 PHYS-C0220 Termodynamiikka ja statistinen fysiikka, kevät 2017 Emppu Salonen 1 Eksergia ja termodynaamiset potentiaalit 1.1 Suurin mahdollinen hyödyllinen työ Tähän mennessä olemme tarkastelleet sisäenergian
1. (*) Luku 90 voidaan kirjoittaa peräkkäisen luonnollisen luvun avulla esimerkiksi
 Matematiikan pulmasivu Koonnut Martti Heinonen martti.heinonen@luukku.com Vaikeustaso on merkitty tähdillä: yhden tähden (*) tehtävä on helpoin ja kolmen (***) haastavin. 1. (*) Luku 90 voidaan kirjoittaa
Matematiikan pulmasivu Koonnut Martti Heinonen martti.heinonen@luukku.com Vaikeustaso on merkitty tähdillä: yhden tähden (*) tehtävä on helpoin ja kolmen (***) haastavin. 1. (*) Luku 90 voidaan kirjoittaa
Törmäysteoria. Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa
 Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Perusvuorovaikutukset. Tapio Hansson
 Perusvuorovaikutukset Tapio Hansson Perusvuorovaikutukset Vuorovaikutukset on perinteisesti jaettu neljään: Gravitaatio Sähkömagneettinen vuorovaikutus Heikko vuorovaikutus Vahva vuorovaikutus Sähköheikkoteoria
Perusvuorovaikutukset Tapio Hansson Perusvuorovaikutukset Vuorovaikutukset on perinteisesti jaettu neljään: Gravitaatio Sähkömagneettinen vuorovaikutus Heikko vuorovaikutus Vahva vuorovaikutus Sähköheikkoteoria
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
FYSA242 Statistinen fysiikka, Harjoitustentti
 FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
FYSA242 Statistinen fysiikka, Harjoitustentti Tehtävä 1 Selitä lyhyesti: a Mikä on Einsteinin ja Debyen kidevärähtelymallien olennainen ero? b Mikä ero vuorovaikutuksessa ympäristön kanssa on kanonisella
LÄHI- JA VERKKO- OPETUKSEEN OSALLISTUNEIDEN KOKEMUKSIA OPETUKSESTA
 LÄHI- JA VERKKO- OPETUKSEEN OSALLISTUNEIDEN KOKEMUKSIA OPETUKSESTA Tarja Tuononen, KM, tohtorikoulutettava Yliopistopedagogiikan keskus Jenni Krapu, Yliopisto-opettaja, Avoin yliopisto Risto Uro, Yliopistonlehtori,
LÄHI- JA VERKKO- OPETUKSEEN OSALLISTUNEIDEN KOKEMUKSIA OPETUKSESTA Tarja Tuononen, KM, tohtorikoulutettava Yliopistopedagogiikan keskus Jenni Krapu, Yliopisto-opettaja, Avoin yliopisto Risto Uro, Yliopistonlehtori,
Alkuaineita luokitellaan atomimassojen perusteella
 IHMISEN JA ELINYMPÄRISTÖN KEMIAA, KE2 Alkuaineen suhteellinen atomimassa Kertausta: Isotoopin määritelmä: Saman alkuaineen eri atomien ytimissä on sama määrä protoneja (eli sama alkuaine), mutta neutronien
IHMISEN JA ELINYMPÄRISTÖN KEMIAA, KE2 Alkuaineen suhteellinen atomimassa Kertausta: Isotoopin määritelmä: Saman alkuaineen eri atomien ytimissä on sama määrä protoneja (eli sama alkuaine), mutta neutronien
Ajattelu ja oppimaan oppiminen (L1)
 Ajattelu ja oppimaan oppiminen (L1) Mitä on oppimaan oppiminen? Kirjoita 3-5 sanaa, jotka sinulle tulevat mieleen käsitteestä. Vertailkaa sanoja ryhmässä. Montako samaa sanaa esiintyy? 1 Oppimaan oppiminen
Ajattelu ja oppimaan oppiminen (L1) Mitä on oppimaan oppiminen? Kirjoita 3-5 sanaa, jotka sinulle tulevat mieleen käsitteestä. Vertailkaa sanoja ryhmässä. Montako samaa sanaa esiintyy? 1 Oppimaan oppiminen
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Luento 4. Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit
 Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2. pääsääntö Termodynaamiset potentiaalit Luento 4 Termodynamiikka Termodynaamiset prosessit ja 1. pääsääntö Entropia ja 2.
Mekaaninen energia. Energian säilymislaki Työ, teho, hyötysuhde Mekaaninen energia Sisäenergia Lämpö = siirtyvää energiaa. Suppea energian määritelmä:
 Mekaaninen energia Energian säilymislaki Työ, teho, hyötysuhde Mekaaninen energia Sisäenergia Lämpö = siirtyvää energiaa Suppea energian määritelmä: Energia on kyky tehdä työtä => mekaaninen energia Ei
Mekaaninen energia Energian säilymislaki Työ, teho, hyötysuhde Mekaaninen energia Sisäenergia Lämpö = siirtyvää energiaa Suppea energian määritelmä: Energia on kyky tehdä työtä => mekaaninen energia Ei
Ohjeita fysiikan ylioppilaskirjoituksiin
 Ohjeita fysiikan ylioppilaskirjoituksiin Kari Eloranta 2016 Jyväskylän Lyseon lukio 11. tammikuuta 2016 Kokeen rakenne Fysiikan kokeessa on 13 tehtävää, joista vastataan kahdeksaan. Tehtävät 12 ja 13 ovat
Ohjeita fysiikan ylioppilaskirjoituksiin Kari Eloranta 2016 Jyväskylän Lyseon lukio 11. tammikuuta 2016 Kokeen rakenne Fysiikan kokeessa on 13 tehtävää, joista vastataan kahdeksaan. Tehtävät 12 ja 13 ovat
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
ENERGIAA! ASTE/KURSSI AIKA 1/5
 1/5 ASTE/KURSSI Yläasteelle ja lukioon elintarvikkeiden kemian yhteydessä. Sopii myös alaasteryhmille opettajan avustaessa poltossa, sekä laskuissa. AIKA n. ½ tuntia ENERGIAA! Vertaa vaahtokarkin ja cashewpähkinän
1/5 ASTE/KURSSI Yläasteelle ja lukioon elintarvikkeiden kemian yhteydessä. Sopii myös alaasteryhmille opettajan avustaessa poltossa, sekä laskuissa. AIKA n. ½ tuntia ENERGIAA! Vertaa vaahtokarkin ja cashewpähkinän
Kuva 1. Nykyaikainen pommikalorimetri.
 DEPARTMENT OF CHEMISTRY NESTEIDEN JA KIINTEIDEN AINEIDEN LÄMPÖARVOJEN MÄÄRITYS Matti Kuokkanen 1, Reetta Kolppanen 2 ja Toivo Kuokkanen 3 1 Oulun yliopisto, kemian laitos, PL 3000, FI-90014, Oulu, matti.kuokkanen@oulu.fi
DEPARTMENT OF CHEMISTRY NESTEIDEN JA KIINTEIDEN AINEIDEN LÄMPÖARVOJEN MÄÄRITYS Matti Kuokkanen 1, Reetta Kolppanen 2 ja Toivo Kuokkanen 3 1 Oulun yliopisto, kemian laitos, PL 3000, FI-90014, Oulu, matti.kuokkanen@oulu.fi
Näiden aihekokonaisuuksien opetussuunnitelmat ovat luvussa 8.
 9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 4: Entropia Maanantai 21.11. ja tiistai 22.11. Ideaalikaasun isoterminen laajeneminen Kaasuun tuodaan määrä Q lämpöä......
Aineopintojen laboratoriotyöt 1. Veden ominaislämpökapasiteetti
 Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
Aineopintojen laboratoriotyöt 1 Veden ominaislämpökapasiteetti Aki Kutvonen Op.nmr 013185860 assistentti: Marko Peura työ tehty 19.9.008 palautettu 6.10.008 Sisällysluettelo Tiivistelmä...3 Johdanto...3
3.4 Liike-energiasta ja potentiaalienergiasta
 Työperiaatteeksi (the work-energy theorem) kutsutaan sitä että suljetun systeemin liike-energian muutos Δ on voiman systeemille tekemä työ W Tämä on yksi konservatiivisen voiman erityistapaus Työperiaate
Työperiaatteeksi (the work-energy theorem) kutsutaan sitä että suljetun systeemin liike-energian muutos Δ on voiman systeemille tekemä työ W Tämä on yksi konservatiivisen voiman erityistapaus Työperiaate
YLEINEN KEMIA. Alkuaineiden esiintyminen maailmassa. Alkuaineet. Alkuaineet koostuvat atomeista. Atomin rakenne. Copyright Isto Jokinen
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan?
 2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
Tämän päivän ohjelma: ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 28.9.2015 / T. Paloposki / v. 01 Tämän päivän ohjelma: Tilanyhtälöt (kertaus) Termodynamiikan 1. pääsääntö (energian häviämättömyyden laki)
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 28.9.2015 / T. Paloposki / v. 01 Tämän päivän ohjelma: Tilanyhtälöt (kertaus) Termodynamiikan 1. pääsääntö (energian häviämättömyyden laki)
Opetuksen suunnittelun lähtökohdat. Keväällä 2018 Johanna Kainulainen
 Opetuksen suunnittelun lähtökohdat Keväällä 2018 Johanna Kainulainen Shulmanin (esim. 1987) mukaan opettajan opetuksessaan tarvitsema tieto jakaantuu seitsemään kategoriaan: 1. sisältötietoon 2. yleiseen
Opetuksen suunnittelun lähtökohdat Keväällä 2018 Johanna Kainulainen Shulmanin (esim. 1987) mukaan opettajan opetuksessaan tarvitsema tieto jakaantuu seitsemään kategoriaan: 1. sisältötietoon 2. yleiseen
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin?
 Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka
 Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Alkudemonstraatio Käsi lämpömittarina Laittakaa kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä. 1) Pitäkää
Lämpöistä oppia Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Alkudemonstraatio Käsi lämpömittarina Laittakaa kolmeen eri altaaseen kylmää, haaleaa ja lämmintä vettä. 1) Pitäkää
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
vetyteknologia Polttokennon termodynamiikkaa 1 DEE Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
DEE-5400 olttokennot ja vetyteknologia olttokennon termodynamiikkaa 1 DEE-5400 Risto Mikkonen ermodynamiikan ensimmäinen pääsääntö aseraja Ympäristö asetila Q W Suljettuun systeemiin tuotu lämpö + systeemiin
Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet
 Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet Kari Sormunen Syksy 2014 Kemiallinen reaktio Kemiallinen reaktio on prosessi, jossa aineet muuttuvat toisiksi aineiksi: atomien
Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet Kari Sormunen Syksy 2014 Kemiallinen reaktio Kemiallinen reaktio on prosessi, jossa aineet muuttuvat toisiksi aineiksi: atomien
dl = F k dl. dw = F dl = F cos. Kun voima vaikuttaa kaarevalla polulla P 1 P 2, polku voidaan jakaa infinitesimaalisen pieniin siirtymiin dl
 Kun voima vaikuttaa kaarevalla polulla P 2, polku voidaan jakaa infinitesimaalisen pieniin siirtymiin dl Kukin siirtymä dl voidaan approksimoida suoraviivaiseksi, jolloin vastaava työn elementti voidaan
Kun voima vaikuttaa kaarevalla polulla P 2, polku voidaan jakaa infinitesimaalisen pieniin siirtymiin dl Kukin siirtymä dl voidaan approksimoida suoraviivaiseksi, jolloin vastaava työn elementti voidaan
Students Experiences of Workplace Learning Marja Samppala, Med, doctoral student
 Students Experiences of Workplace Learning Marja Samppala, Med, doctoral student Research is focused on Students Experiences of Workplace learning (WPL) 09/2014 2 Content Background of the research Theoretical
Students Experiences of Workplace Learning Marja Samppala, Med, doctoral student Research is focused on Students Experiences of Workplace learning (WPL) 09/2014 2 Content Background of the research Theoretical
Teddy 1. välikoe kevät 2008
 Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 1. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Trialoginen oppiminen: Miten edistää kohteellista, yhteisöllistä työskentelyä oppimisessa?
 Trialoginen oppiminen: Miten edistää kohteellista, yhteisöllistä työskentelyä oppimisessa? Tekijä: Sami Paavola, Helsingin yliopisto 1 Muuttaako uusi teknologia oppimista? Miten oppimisen tulisi muuttua?
Trialoginen oppiminen: Miten edistää kohteellista, yhteisöllistä työskentelyä oppimisessa? Tekijä: Sami Paavola, Helsingin yliopisto 1 Muuttaako uusi teknologia oppimista? Miten oppimisen tulisi muuttua?
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta Insinöörivalinnan kemian koe MALLIRATKAISUT
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Perjantai VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN
 Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
KOTITEKOINEN PALOSAMMUTIN (OSA II)
 Johdanto KOTITEKOINEN PALOSAMMUTIN (OSA II) Monet palosammuttimet, kuten kuvassa esitetty käsisammutin, käyttävät hiilidioksidia. Jotta hiilidioksidisammutin olisi tehokas, sen täytyy vapauttaa hiilidioksidia
Johdanto KOTITEKOINEN PALOSAMMUTIN (OSA II) Monet palosammuttimet, kuten kuvassa esitetty käsisammutin, käyttävät hiilidioksidia. Jotta hiilidioksidisammutin olisi tehokas, sen täytyy vapauttaa hiilidioksidia
Tehostettu kisällioppiminen tietojenkäsittelytieteen ja matematiikan opetuksessa yliopistossa Thomas Vikberg
 Tehostettu kisällioppiminen tietojenkäsittelytieteen ja matematiikan opetuksessa yliopistossa Thomas Vikberg Matematiikan ja tilastotieteen laitos Tietojenkäsittelytieteen laitos Kisällioppiminen = oppipoikamestari
Tehostettu kisällioppiminen tietojenkäsittelytieteen ja matematiikan opetuksessa yliopistossa Thomas Vikberg Matematiikan ja tilastotieteen laitos Tietojenkäsittelytieteen laitos Kisällioppiminen = oppipoikamestari
Tämän päivän ohjelma: ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 3 / Kommentti kotilaskuun 2 Termodynamiikan 1. pääsääntö 9/26/2016
 ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 3 / 26.9.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Kommentti kotilaskuun 2 Termodynamiikan 1. pääsääntö 1 Kotilasku 2 Kotilasku 2 2 Termodynamiikan
ENY-C2001 Termodynamiikka ja lämmönsiirto Luento 3 / 26.9.2016 v. 03 / T. Paloposki Tämän päivän ohjelma: Kommentti kotilaskuun 2 Termodynamiikan 1. pääsääntö 1 Kotilasku 2 Kotilasku 2 2 Termodynamiikan
Lukion kemia 3, Reaktiot ja energia. Leena Piiroinen Luento 2 2015
 Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
EPIONEN Kemia 2015. EPIONEN Kemia 2015
 EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
TUTKIMUSLÄHTÖINEN FYSIIKAN OPISKELU. MAOL:n syyskoulutuspäivät
 TUTKIMUSLÄHTÖINEN FYSIIKAN OPISKELU MAOL:n syyskoulutuspäivät 7.10.2017 TUTKIMUSLÄHTÖINEN OPPIMINEN IBE - Inquiry Based Education Opetusjärjestely, jossa oppilas laitetaan tutkijan asemaan keräämään ja
TUTKIMUSLÄHTÖINEN FYSIIKAN OPISKELU MAOL:n syyskoulutuspäivät 7.10.2017 TUTKIMUSLÄHTÖINEN OPPIMINEN IBE - Inquiry Based Education Opetusjärjestely, jossa oppilas laitetaan tutkijan asemaan keräämään ja
Lukion kemian OPS 2016
 Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
Reflektiivinen ammattikäytäntö. Merja Sylgren 07.05.2007
 Reflektiivinen ammattikäytäntö Arjen työn vaatimukset Työyhteisöt ja yksittäiset työntekijät vastaavat arjen työssään työelämän asettamiin vaatimuksiin. Tästä nousee tarkasteltavaksi: yhteisöjen ja yksilöiden
Reflektiivinen ammattikäytäntö Arjen työn vaatimukset Työyhteisöt ja yksittäiset työntekijät vastaavat arjen työssään työelämän asettamiin vaatimuksiin. Tästä nousee tarkasteltavaksi: yhteisöjen ja yksilöiden
Flipped Classroom Pedagogiikka Kemian opetuksessa Case Kemiallisen tasapainon kurssi
 Flipped Classroom Pedagogiikka Kemian opetuksessa Case Kemiallisen tasapainon kurssi Ari Myllyviita MSc (Chem.Ed.), BSc (Chem.), BEd (soc.pedag.) Lecturer (Chemistry and Mathematics), Project Coordinator
Flipped Classroom Pedagogiikka Kemian opetuksessa Case Kemiallisen tasapainon kurssi Ari Myllyviita MSc (Chem.Ed.), BSc (Chem.), BEd (soc.pedag.) Lecturer (Chemistry and Mathematics), Project Coordinator
Integrointialgoritmit molekyylidynamiikassa
 Integrointialgoritmit molekyylidynamiikassa Markus Ovaska 28.11.2008 Esitelmän kulku MD-simulaatiot yleisesti Integrointialgoritmit: mitä integroidaan ja miten? Esimerkkejä eri algoritmeista Hyvän algoritmin
Integrointialgoritmit molekyylidynamiikassa Markus Ovaska 28.11.2008 Esitelmän kulku MD-simulaatiot yleisesti Integrointialgoritmit: mitä integroidaan ja miten? Esimerkkejä eri algoritmeista Hyvän algoritmin
RATKAISUT: 12. Lämpöenergia ja lämpöopin pääsäännöt
 Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
Physica 9 1. painos 1(7) : 12.1 a) Lämpö on siirtyvää energiaa, joka siirtyy kappaleesta (systeemistä) toiseen lämpötilaeron vuoksi. b) Lämpöenergia on kappaleeseen (systeemiin) sitoutunutta energiaa.
1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa?
 Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Kysymys 1. Kumpi painaa enemmän normaalipaineessa: 1m2 80 C ilmaa vai 1m2 0 C ilmaa? 2. EXTRA-PÄHKINÄ (menee yli aiheen): Heität vettä kiukaalle. Miksi vesihöyry nousee voimakkaasti kiukaasta ylöspäin?
Vesimolekyylien kiehtova maailma
 Vesimolekyylien kiehtova maailma Luokka-aste Oppitunti molekyylimallinnuksesta oli suunniteltu 8. luokan oppilaille. Tavoitteet Tavoitteena on tarkastella kemiallista mallia ja syventää kemiallisen mallin
Vesimolekyylien kiehtova maailma Luokka-aste Oppitunti molekyylimallinnuksesta oli suunniteltu 8. luokan oppilaille. Tavoitteet Tavoitteena on tarkastella kemiallista mallia ja syventää kemiallisen mallin
FYSIIKAN JA MATEMATIIKAN LAITOS, JOENSUU 1. vuosikurssi 2. vuosikurssi 3. vuosikurssi
 FYSIIKAN JA MATEMATIIKAN LAITOS, JOENSUU FYSIIKKA 1. tai op koodi. tai Ruotsia fysiikan, kemian ja matematiikan 3 80130 metsätieteiden matematiikan 801338 Science, MATEMATIIKKA 1. tai op koodi. tai Ruotsia
FYSIIKAN JA MATEMATIIKAN LAITOS, JOENSUU FYSIIKKA 1. tai op koodi. tai Ruotsia fysiikan, kemian ja matematiikan 3 80130 metsätieteiden matematiikan 801338 Science, MATEMATIIKKA 1. tai op koodi. tai Ruotsia
Atomimallit. Tapio Hansson
 Atomimallit Tapio Hansson Atomin käsite Atomin käsite on peräisin antiikin Kreikasta. Filosofi Demokritos päätteli (n. 400 eaa.), että äärellisen maailman tulee koostua äärellisistä, jakamattomista hiukkasista
Atomimallit Tapio Hansson Atomin käsite Atomin käsite on peräisin antiikin Kreikasta. Filosofi Demokritos päätteli (n. 400 eaa.), että äärellisen maailman tulee koostua äärellisistä, jakamattomista hiukkasista
Lämpöopin pääsäännöt
 Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Lämpöopin pääsäännöt 0. Eristetyssä systeemissä lämpötilaerot tasoittuvat. Systeemin sisäenergia U kasvaa systeemin tuodun lämmön ja systeemiin tehdyn työn W verran: ΔU = + W 2. Eristetyn systeemin entropia
Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
Diplomi-insinööri- ja arkkitehtikoulutuksen yhteisvalinta 2017 DI-kemian valintakoe 31.5. Malliratkaisut Lasku- ja huolimattomuusvirheet - ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim.
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
