Ioniselektiivinen elektrodi
|
|
|
- Irma Hänninen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento n. 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely 3,5 h Opettaja: yliopistonlehtori Minna Nieminen (minna.nieminen@aalto.fi, p ) Laboratoriotöitä ohjaa kurssiapulaiset: Hanna Kuha / Lotta Knuutila / Henrik Nikkilä Tavoite Työn suoritettuaan, opiskelija osaa kuvata ioniselektiivisten elektrodien tyypit ja toiminnan sekä määritysmenetelmän periaatteen. valmistaa standardiliuoksia ja käyttää oikein ioniselektiivisiä elektrodeja. laatia standardisuoran mittaustuloksista ja laskea sen perusteella näytteen pitoisuuden. Minna Nieminen 1
2 Laboratoriotyö: vesijohtoveden ja kivennäisveden kloridipitoisuuden määritys Työhön valmistautuminen ennen työkertaa: kertaa työn teoria (mittauksen suoritus, elektrodityypit) lue työohje mieti, miten standardiliuokset valmistetaan mieti, miten standardisuora piirretään ja miten tulos lasketaan etsi, mikä on Espoon vesijohtoveden kloridipitoisuus Työkerralla : kerrataan teoria valmistetaan näytteet ja standardit, tehdään mittaukset lasketaan tulokset, verrataan tiedettyihin pitoisuuksiin täytetään tuloslomake Kokoontumispaikka ja laboratorio Ota mukaan muistiinpanovälineet! Laboratoriossa lainataan jokaiselle laboratoriotakki ja suojalasit, mutta voit käyttää myös omia. Työ tehdään tässä laboratoriossa Kemian talo, Kemistintie 1 Oppilaslaboratorion ala-aula 1. kerros Minna Nieminen 2
3 Arviointi: opettaja arvioi työn suorituksen arvosanalla 1 5 Heikko Hyvä Kiitettävä Työhön valmistautuminen (Työohjeisiin tutustuminen ennen työtä, ohjeiden ymmärtäminen, alustavan työsuunnitelman teko) Työskentelyn suunnittelu (Työsuunnitelman tekoon osallistuminen, työnjaon suunnittelu, ryhmän jäsenten huomioiminen) Laboratoriotyöskentely (Turvalliset ja huolelliset työtavat, aktiivisuus ryhmässä, ryhmän jäsenten huomioiminen) Tulosten käsittely (Pohdintojen teko, osallistuminen tulosten laskemiseen, osallistuminen tuloslomakkeen täyttöön) Minna Nieminen 3
4 Taustaa työlle ELIMISTÖN NESTETASAPAINO kaikki elollinen tapahtuu vedessä vesi on solunsisäisen ympäristön pääkomponentti solut kelluvat laimeaa merivettä muistuttavassa solunulkoisessa nesteessä solut kommunikoivat ympäristönsä kanssa veden välityksellä tavoitteena on säilyttää soluja ympäröivän nesteen määrä ja koostumus sellaisena, että se sallii vakaan solunsisäisen ympäristön, joka mahdollistaa häiriöttömät elintoiminnat toiminnallisesti elimistön nesteet jaetaan: - solunulkoiseen nesteeseen - solunsisäiseen nesteeseen ELIMISTÖN NESTETILAT (MIES 70 kg) Lapsilla suurempi, naisilla ja vanhuksilla hieman pienempi Veden kokonaismäärä 60 % (42 l) Solukalvon ympäristöstä eristämä neste, jossa tapahtuu suurin osa elämän perusreaktioista Solunsisäinen neste 40 % (28 l) Solunulkoinen neste 20 % (14 l) Verisolujen soluvälineste, jossa verisolut sijaitsevat, - siirtää happea, hiilidioksidia, ravinteita ja aineenvaihduntatuotteita elimiltä toisille Soluvälineste 15 % (11 l) Plasma 5 % (3,5 l) Kudosten soluja ympäröivä neste - välittää happea, hiilidioksidia, ravinteita ja aineenvaihduntatuotteita plasman ja solun sisäisen nesteen välillä Minna Nieminen 4
5 Plasman, soluvälinesteen ja solunsisäisen nesteen elektrolyyttikoostumukset [mmol/l] Elektrolyytti Plasma Soluvälineste Solunsisäinen neste Natrium Kalium 4,2 4,0 140 Kalsium 1,3 1,2 < 0,001 Magnesium 0,8 0,7 20 Kloridi Bikarbonaatti Sulfaatti 0,5 0,5 1 Fosfaatti Proteiini 1,2 0,2 4 Lähde: Guyton, A.C, Hall, J.E., Textbook of Medical Physiology, Veden ja elektrolyyttien aineenvaihdunnan kannalta keskeistä: Diffuusio eli elektrolyyttien siirtyminen solujen ja veren välillä Osmoosi eli veden siirtyminen puoliläpäisevän kalvon läpi laimeammasta liuoksesta väkevämpään Na ja sen mukana tulevat anionit Cl - ja HCO 3- ovat osmoottisesti aktiivisimmat liuenneet aineet solunulkoisessa nesteessä Minna Nieminen 5
6 NESTETASAPAINO tavoitteena on säilyttää solujen tilavuus eli vesitasapaino ja elektrolyyttikoostumus eli osmoottinen tasapaino vakaana ja turvata riittävä verenkierron tilavuus hapen tarjonnan ylläpitämiseksi häiriöt ovat tavallisia eri kuivumistiloihin tai ylimääräiseen nesteenpoistoon liittyen (hypertoninen plasma, dehydraatio), tai erilaisissaturvotustiloissa ja liiallisen juomisen seurauksena (hypotoninen plasma, hyperhydraatio). häiriöiden tutkimisessa tarvitaan sekä plasman (seerumin) että virtsan osmolaliteetti- ja elektrolyyttimäärityksiä ja happo-emästasapainon tietoja Kloridi elimistön tärkein anioni, liittyneenä Na, K, H n. 88 % solunulkoisessa nesteessä kloridin aineenvaihdunta on merkittävältä osalta sidottu Na :n ja HCO 3- :n aineenvaihduntaan ja happo-emästasapainon säätelyyn korkeiden kloridiarvojen syyt: kuivuminen, pitkäaikainen ripuli, liiallinen NaClsaanti, akuutit munuaisvauriot matalien kloridiarvojen syyt: oksentelu tai nenä-mahaletkun aiheuttama, sydämen vajaatoiminta, bromidimyrkytys, nesteenpoistolääkitys, munuaisvauriot, synnynnäinen kloridiripuli, palovammat korjataan fysiologisella keittosuolalla ( KCl tarvittaessa) Minna Nieminen 6
7 Elektrolyyttikoostumuksen tutkiminen Elektrolyytti Kloridi Tutkimusmenetelmä Ioniselektiivinen elektrodi (virtsa, plasma) Kulometrinen titraus (virtsa) Natrium Ioniselektiivinen elektrodi (plasma) Liekkifotometria (virtsa) Kalium Ioniselektiivinen elektrodi (plasma, punasolut) Liekkifotometria (virtsa) Kalsium Ioniselektiivinen elektrodi (ionisoitunut, plasmasta) Fotometria (plasma, virtsa) Spektrofotometria (plasma) Lähde: GALVAANISIA KENNOJA KÄYTETÄÄN Hapettumispelkistymisreaktioiden energiaa muuntuu suoraan sähköenergiaksi Kennon lähdejännite on riippuvainen aineiden pitoisuuksista TASAVIRRAN LÄHTEINÄ primaariparistot akut polttokennot ANALYYTTISINA TYÖKALUINA potentiometriset ph-mittarit muut ioniselektiiviset elektrodit Minna Nieminen 7
8 POTENTIOMETRINEN MITTAUS Sähkökemiallinen kenno: vertailuelektrodi suolasilta tutkittava liuos indikaattorielektrodi Vertailuelektrodi: potentiaali tunnetaan (vakio), ei riipu tutkittavan liuoksen ionipitoisuudesta Indikaattorielektrodi: potentiaali riippuu tutkittavasta liuoksen ionipitoisuudesta Nernstin lain mukaisesti, tietylle ionille selektiivinen Suolasilta: erottaa vertailuelektrodin tutkittavasta liuoksesta estää liuosten sekoittumisen nesteliitokset nestepotentiaali, E j Kennon sähkömotorinen voima E = E ind. E ref E j Mitataan vertailuelektrodin ja indikaattorielektrodin välinen lähdejännite. Nernstin laki: E = E o kenno RT z F i lna i jossa a i = mitattavan ionin aktiivisuus z i = mitattavan ionin varausluku E o kenno = kennon standardipotentiaali Mitataan vertailuelektrodin ja indikaattorielektrodin välinen lähdejännite : DE = E(indikaattorielektrodi) - E(vertailuelektrodi) Kalibrointi standardiliuosten avulla. Minna Nieminen 8
9 Vertailuelektrodi Metalli kosketuksissa niukkaliukoisen suolansa ja sen kyllästetyn liuoksen kanssa. esim. Ag / AgCl -elektrodi Elektrodireaktiot: Ag (aq) e Ag(s) AgCl(s) Ag (aq) Cl (aq) AgCl(s) e Ag(s) Cl (aq) Metalli-ionin konsentraatio liuoksessa on liukoisuustulon määräämä ja pysyy lähes vakiona pienillä sähkövirroilla Elektrodin potentiaali on vakio.! Ioniselektiiviset membraanielektrodit a) lasielektrodi b) kiinteäaineinen c) nestemäinen membraanielektrodi membraanielektrodi Elektrodin potentiaali riippuu tutkittavasta liuoksesta. Minna Nieminen 9
10 Lasielektrodi potentiaaliero membraanin yli Lasimembraani (Corning 015): n. 200 μm paksu, 72 % SiO 2, 6 % CaO, 22 % Na 2 O vetyioniherkkä ph - alueella 2 12 jos CaO, Na 2 O korvataan BaO, Li 2 O ph 14 asti Kosketus liuoksen kanssa: -SiO-Na H (aq) fi -SiO-H Na (aq) IONIVAIHTOREAKTIO! Selektiivinen H -ioneille pinnan rakenne riippuu a(h ) = g[h ]» [H ] membraanin potentiaalin muutos liuoksen suhteen Elektrodin potentiaalin riippuu liuoksen ph:sta Minna Nieminen 10
11 vertailu- H (tuntem.) lasimembraani H (tunnettu) sisäinen elektrodi vert.elektrodi Ag/AgCl E lasi = E o RT a( H ) - ln zf a( H ) tunnettu tuntem. E lasi = E o 0,059 V a( H ) - log z a( H ) tunnettu tuntem. E lasi = E o - 0,059 ( log a( H ) -log a( H ) ) tunnettu tuntem. E lasi = E o - 0,059 log a(h ) tunnettu 0,059 log a(h ) tuntem. E lasi = vakio 0,059 log a(h ) tuntem. ph = log a(h ) E kenno = vakio - 0,059 V ph ph-mittaus Kaksi liuosta, joiden ph eri suuruinen, erotettu toisistaan ohuella erikoislasimembraanilla potentiaaliero voidaan mitata asettamalla sopiva elektrodi kalvon kummallekin puolelle E = E o 0,059 V ph Mittauksen virhe tyypillisesti 0,02 ph ph-mittari kalibroitava aina ennen käyttöä, mihin käytetään puskuriliuoksia, esim. ph 4, ph 7 ja ph 10 Kuva: Tekniikan kemia Minna Nieminen 11
12 Lasielektrodit muille kationeille Lasilaatua kehittämällä saadaan lasimembraaneja, jotka ovat selektiivisiä muille kationeille kuin vetyioneille. Lasin koostumus Elektrodin herkkyys Na 2 O 22 %, CaO 6 %, SiO 2 72 % H (suuri alkaalivirhe) Li 2 O 28 %, Cs 2 O 2 %, BaO 4 %, La 2 O 3 3 %, SiO 2 63 % H (pieni alkaalivirhe) Li 2 O 15 %, Al 2 O 3 25 %, SiO 2 60 % Na 2 O 11 %, Al 2 O 3 18 %, SiO 2 71 % Na 2 O 27 %, Al 2 O 3 5 %, SiO 2 68 % Li Na K Kiinteäaineiset membraanielektrodit lasimembraanin tilalla yksittäiskide tai kiteisestä aineesta puristettu tabletti. sähkönkuljetus perustuu hilavirheisiin: hilan pienin ja varaukselta alhaisin ioni siirtyy hilavirheen aiheuttamasta kolosta toiseen kolot sopivia vain tietylle ionille ioniselektiivinen membraanimateriaali on hyvin niukkaliukoista Minna Nieminen 12
13 Fluoridielektrodi Lantaanifluoridikide, LaF 3, joka on seostettu Eu 2 :lla hilavirheiden lisäämiseksi sähkönjohtavuus paranee LaF 3 (kide) La 3 (kide) 3 F (aq) kiteen pintarakenne muuttuu sen mukaan, mikä on liuoksen a(f ) = g[f ] standardit ja näyte puskuroidaan samaan ph-arvoon, esim. 5,5, jolloin fluoridin aktiivisuuskerroin g on sama kaikissa liuoksissa RT - E = vakio ln[f ] nf - = vakio- 0,059 log[f ] Taulukko 1. Kiinteäaineisten membraanielektrodien ominaisuuksia. Ioni Konsentraatioalue (mol/l) Membraani ph-alue Häiritsevät ionit F LaF OH (0,1 M) Cl Ag 2 S/AgCl 2 11 CN, S 2, l S 2 O 3 2, Br Br Ag 2 S/AgBr 2 12 CN, S 2, l l Ag 2 S/AgI 3 12 S 2 SCN Ag 2 S/AgSCN 2 12 S 2, l, CN, Br, S 2 O 3 2 CN Ag 2 S/AgCN S 2, l S Ag 2 S Kloridielektrodin vertailuelektrodina käytetään kaksoisnesteliitoksella varustettua vertailuelektrodia, jossa uloin kammio täytetään KNO 3 -liuoksella, joka ei häiritse kloridin määritystä. Minna Nieminen 13
14 Nestemäiset membraanielektrodit Lasimembraanin tilalla huokoinen polymeerimembraani (usein PVC), joka on kyllästetty ioninvaihtonesteellä. uloin putki muodostaa säiliön, jossa ioninvaihtoneste kostuttaa membraania membraanin rakenne muuttuu sen mukaan, mikä on mitattavan ionin aktiivisuus (konsentraatio) liuoksessa potentiaaliero membraanin yli Tyypilliset mitattavat ionit: NH 4, Ca 2, K, NO 3 Ioninvaihtoneste: suuria, veteen liukenemattomia orgaanisia yhdisteitä liuotettuna orgaaniseen liuottimeen Esim. di-(n-dekyyli) fosfaatti Ioninvaihtaja on selektiivinen tietylle ionille. Minna Nieminen 14
15 Taulukko 1. Esimerkkejä nestemäisistä membraanielektrodeista. Ioni Konsentraatioalue (mol/l) Ca di-(n-dekyyli) fosfaatti/ dioktyylifenyylifosfonaatti Ioninvaihtaja/liuotin ph-alue Häiritsevät ionit 6 10 Zn 2, Pb 2, Fe 2, Cu 2 K Valinomysiini/ dioktyylisebasaatti NO Tri(dodekyyli)heksa(dekyyli) ammonium/ oktyyli-2-nitrofenyylieetteri ClO ,10-fenantroliinin rautakompleksi/ p-nitrokymeeni BF ,10-fenantroliinin nikkelikompleksi/ p-nitrokymeeni 4 9 Rb, Cs, NH 4, 3 8 ClO 4,l, ClO 3, CN, Br, CN 4 10 l, Br, NO NO 3 Kalibrointi ja näytteen pitoisuuden laskeminen, esimerkki Veden Ca 2 -ionikonsentraatio määritettiin ioniselektiivisellä elektrodilla. Näytteen ja standardien ionivahvuus säädettiin vakioksi lisäämällä jokaiseen liuokseen 0,5 M KNO 3 -liuosta. Taulukossa 1 on esitetty standardiliuosten mittaustulokset. Taulukko 1. Standardiliuosten konsentraatiot ja mitatut potentiaalit. [Ca 2 ] (mol/l) E kenno (V) 1, ,125 5, ,103 1, ,093 5, ,072 1, ,065 5, ,043 1, ,033 Mikä on vesinäytteen Ca 2 -ionikonsentraatio, kun liuoksen potentiaali oli -0,084 V? Minna Nieminen 15
16 Ratkaisu: Standardisuoran yhtälö: E kenno = 0,027 0,0303 log [Ca 2 ] Sijoitetaan yhtälöön E(näyte) = -0,084 V jolloin saadaan [Ca 2 ] = 2, mol/l Ioniselektiivisten elektrodien edut lineaarinen vaste laajalla konsentraatioalueella ei kontaminoi näytettä ei tuhoa näytettä mittaus jopa sekunneissa tai minuuteissa soveltuu esim. prosessivirtausten analysointiin liuosten väri tai sameus ei vaikuta mittaukseen Minna Nieminen 16
17 Ioniselektiivisten elektrodien haitat/ häiriöt toistotarkkuus 1 % tai huonompi mikään ioniselektiivinen elektrodi ei ole täysin spesifinen, vaan muut ionit voivat vaikuttaa jokaisen elektrodin toimintaan: - häiritsevä ioni tunkeutuu yhdessä mitattavan ionin kanssa membraaniin - häiritsevä ioni reagoi membraanimateriaalin kanssa muodostaen niukkaliukoisen yhdisteen sen pinnalle (kiinteäaineinen membraanielektrodi) ioniselektiivisten elektrodien käyttöikä on rajoitettu. Elektrodin vanheneminen näkyy vasteen pienenemisenä ja lukeman ryömimisenä. potentiaalin mittauksen epätarkkuus aiheuttaa virhettä Ioniselektiiviset elektrodit käyttö nykyään membraanielektrodeja noin 30 ionille Lisäksi elektrodeja myös kaasumolekyylien ja orgaanisten molekyylien pitoisuuksien määrittämiseen. ph:n määritys, yleisin mittaus kliiniset määritykset vesianalytiikka esimerkiksi vesijohtoveden kloridipitoisuus biokemia ja bioteknologia Minna Nieminen 17
18 Kirjallisuutta: Lehtonen, P.O., Potentiometrinen analyysi, ph- ja ISE-mittaukset, Edita, Helsinki Harris, D.C., Quantitative Chemical Analysis, W.H. Freeman and Company, New York Minna Nieminen 18
Ioniselektiivinen elektrodi
 ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
CHEM-A1400 Tulevaisuuden materiaalit (5 op) LABORATORIOTYÖN RAPORTTI
 CHEM-A1400 Tulevaisuuden materiaalit (5 op) LABORATORIOTYÖN RAPORTTI TYÖ Litiumioniakku Ryhmä Ryhmän johtaja työ tehty palautus pvm Vastaa raportissa alla esitettyihin kysymyksiin. Tee raportista kuitenkin
CHEM-A1400 Tulevaisuuden materiaalit (5 op) LABORATORIOTYÖN RAPORTTI TYÖ Litiumioniakku Ryhmä Ryhmän johtaja työ tehty palautus pvm Vastaa raportissa alla esitettyihin kysymyksiin. Tee raportista kuitenkin
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
Käsitteitä. Hapetusluku = kuvitteellinen varaus, jonka atomi saa elektronin siirtyessä
 Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Oppikirjan tehtävien ratkaisut
 Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Sähkökemia. Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali
 Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
AKKU- JA PARISTOTEKNIIKAT
 AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
125,0 ml 0,040 M 75,0+125,0 ml Muodostetaan ionitulon lauseke ja sijoitetaan hetkelliset konsentraatiot
 4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
Normaalipotentiaalit
 Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
17VV VV 01021
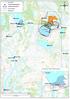 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
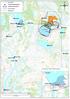 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
Limsan sokeripitoisuus
 KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
Seokset ja liuokset. 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen
 Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Elektrolyysi Anodilla tapahtuu aina hapettuminen ja katodilla pelkistyminen!
 Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
TUTKIMUSTODISTUS. Jyväskylän Ympäristölaboratorio. Sivu: 1(1) Päivä: 09.10.14. Tilaaja:
 Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Jaksollinen järjestelmä ja sidokset
 Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
Liukoisuus
 Liukoisuus REAKTIOT JA TASAPAINO, KE5 Kertausta: Eri suolojen liukeneminen veteen on tärkeä arkipäivän ilmiö. Yleensä suolan liukoisuus veteen kasvaa, kun lämpötila nousee. Tosin esimerkiksi kalsiumkarbonaatti,
Liukoisuus REAKTIOT JA TASAPAINO, KE5 Kertausta: Eri suolojen liukeneminen veteen on tärkeä arkipäivän ilmiö. Yleensä suolan liukoisuus veteen kasvaa, kun lämpötila nousee. Tosin esimerkiksi kalsiumkarbonaatti,
Vesi. Pintajännityksen Veden suuremman tiheyden nesteenä kuin kiinteänä aineena Korkean kiehumispisteen
 Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo. Luento 8 CHEM-A1250
 Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Verikaasuanalyysi. Esitys (anestesia)hoitajille. Vesa Lappeteläinen 3.10.2013
 Verikaasuanalyysi Esitys (anestesia)hoitajille Vesa Lappeteläinen 3.10.2013 Yleistä Yleensä valtimoverestä otettava verinäyte, joka analysoidaan vieritestianalysaattorilla Nopein tapa saada keskeistä tietoa
Verikaasuanalyysi Esitys (anestesia)hoitajille Vesa Lappeteläinen 3.10.2013 Yleistä Yleensä valtimoverestä otettava verinäyte, joka analysoidaan vieritestianalysaattorilla Nopein tapa saada keskeistä tietoa
ROMUMETALLIA OSTAMASSA (OSA 1)
 ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/natrii chloridum B. Braun 1,5 mg/ml
Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/natrii chloridum B. Braun 1,5 mg/ml
Í%SC{ÂÂ!5eCÎ. Korvaa* Kevitsan vesistötarkkailu, PERUS, marraskuu 2018
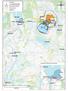 Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-008423-02 Tutkimusnro EUAA56-00006080 Asiakasnro RZ0000092 Näytteenottaja Timo Putkonen
Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-008423-02 Tutkimusnro EUAA56-00006080 Asiakasnro RZ0000092 Näytteenottaja Timo Putkonen
Kevitsan vesistötarkkailu, perus, syyskuu 2018
 Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-002382-01 12.10.2018 Tutkimusnro EUAA56-00002241 Asiakasnro RZ0000092 Näytteenottaja
Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-002382-01 12.10.2018 Tutkimusnro EUAA56-00002241 Asiakasnro RZ0000092 Näytteenottaja
Kemia s10 Ratkaisut. b) Kloorin hapetusluvun muutos: +VII I, Hapen hapetusluvun muutos: II 0. c) n(liclo 4 ) = =
 1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
Workshop: Tekniikan kemia OAMK:ssa
 1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hemosol B0 käsittää kaksitilaisen PVC (polyvinyyli) pussin, joka sisältää
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hemosol B0 käsittää kaksitilaisen PVC (polyvinyyli) pussin, joka sisältää
vi) Oheinen käyrä kuvaa reaktiosysteemin energian muutosta reaktion (1) etenemisen funktiona.
 3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016
 CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016 Kontaktiopetus 70 h Luennot 44 h Laboratoriotyöt 24 h + 2 h = 26 h Oma työ 65 h Laskutuvat ja kotitehtävät 24 h Laboratoriotöiden loppuraportti
CHEM-A1200 Kemiallinen rakenne ja sitoutuminen, syksy 2016 Kontaktiopetus 70 h Luennot 44 h Laboratoriotyöt 24 h + 2 h = 26 h Oma työ 65 h Laskutuvat ja kotitehtävät 24 h Laboratoriotöiden loppuraportti
Luku 3. Protolyysireaktiot ja vesiliuoksen ph
 Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Lääketiede Valintakoeanalyysi 2015 Fysiikka. FM Pirjo Haikonen
 Lääketiede Valintakoeanalyysi 5 Fysiikka FM Pirjo Haikonen Fysiikan tehtävät Väittämä osa C (p) 6 kpl monivalintoja, joissa yksi (tai useampi oikea kohta.) Täysin oikein vastattu p, yksikin virhe/tyhjä
Lääketiede Valintakoeanalyysi 5 Fysiikka FM Pirjo Haikonen Fysiikan tehtävät Väittämä osa C (p) 6 kpl monivalintoja, joissa yksi (tai useampi oikea kohta.) Täysin oikein vastattu p, yksikin virhe/tyhjä
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
Jaksollinen järjestelmä
 Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
Alikuoret eli orbitaalit
 Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen
 KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
KEMA221 2009 YKSINKERTAISET SEOKSET ATKINS LUKU 5 1 YKSINKERTAISET SEOKSET Gibbsin energia ja kemiallinen potentiaali määräävät seosten käyttäytymisen Seoksia voidaan tarkastella osittaisten moolisuureitten
Kemia s2011 ratkaisuja. Kemian koe s 2011 lyhennettyjä ratkaisuja
 Kemian koe s 2011 lyhennettyjä ratkaisuja 1. a) Veden autoprotolyysin 2H 2 O(l) H 3 O + (aq) + OH (aq) seurauksena vedessä on pieni määrä OH ja H 3 O + ioneja, jotka toimivat varauksen kuljettajina. Jos
Kemian koe s 2011 lyhennettyjä ratkaisuja 1. a) Veden autoprotolyysin 2H 2 O(l) H 3 O + (aq) + OH (aq) seurauksena vedessä on pieni määrä OH ja H 3 O + ioneja, jotka toimivat varauksen kuljettajina. Jos
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
joka voidaan määrittää esim. värinmuutosta seuraamalla tai lukemalla
 REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA
 ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
Vinkkejä opettajille ja odotetut tulokset SIVU 1
 Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Eksimeerin muodostuminen
 Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Käytännön esimerkkejä on lukuisia.
 PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
Veden kovuus. KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi.
 KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi. KESTO: n. 60 min. Työn kesto riippuu käsittelylaajuudesta ja ryhmän koosta. MOTIVAATIO: Huomaat,
KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi. KESTO: n. 60 min. Työn kesto riippuu käsittelylaajuudesta ja ryhmän koosta. MOTIVAATIO: Huomaat,
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
3. Protolyysireaktiot ja vesiliuoksen ph
 3. Protolyysireaktiot ja vesiliuoksen ph Happo Happo on protonin (H+) luovuttaja Esim. suolahappo (tässä vesi on emäs) Happo luovuttaa vetyionin ja syntyy oksoniumioni H₃O+ Maistuu happamalta, esim. karboksyylihapot
3. Protolyysireaktiot ja vesiliuoksen ph Happo Happo on protonin (H+) luovuttaja Esim. suolahappo (tässä vesi on emäs) Happo luovuttaa vetyionin ja syntyy oksoniumioni H₃O+ Maistuu happamalta, esim. karboksyylihapot
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Mannitol Braun 150 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mannitol Braun 150 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1000 ml infuusionestettä sisältää 150 g mannitolia. Ominaisuudet: Teoreettinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mannitol Braun 150 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1000 ml infuusionestettä sisältää 150 g mannitolia. Ominaisuudet: Teoreettinen
CHEM-A1250 KEMIAN PERUSTEET kevät 2016
 CHEM-A1250 KEMIAN PERUSTEET kevät 2016 Luennoitsijat Tuula Leskelä (huone B 201c, p. 0503439120) sähköposti: tuula.leskela@aalto.fi Gunilla Fabricius (huone C219, p. 0504095801) sähköposti: gunilla.fabricius@aalto.fi
CHEM-A1250 KEMIAN PERUSTEET kevät 2016 Luennoitsijat Tuula Leskelä (huone B 201c, p. 0503439120) sähköposti: tuula.leskela@aalto.fi Gunilla Fabricius (huone C219, p. 0504095801) sähköposti: gunilla.fabricius@aalto.fi
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt
 KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Neutraloituminen = suolan muodostus
 REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Metallien ympäristölaatunormit ja biosaatavuus. Matti Leppänen SYKE,
 Metallien ympäristölaatunormit ja biosaatavuus Matti Leppänen SYKE, 20.11.2018 Uudet ympäristölaatunormit direktiivissä ja asetuksessa Muutos Ni ja Pb AA-EQS Biosaatavuus Miksi mukana? Vedenlaatu vaihtelee
Metallien ympäristölaatunormit ja biosaatavuus Matti Leppänen SYKE, 20.11.2018 Uudet ympäristölaatunormit direktiivissä ja asetuksessa Muutos Ni ja Pb AA-EQS Biosaatavuus Miksi mukana? Vedenlaatu vaihtelee
Prosessimittaukset. Miksi prosessikierroista tehdään mittauksia
 Prosessimittaukset Miksi prosessikierroista tehdään mittauksia Saadaan informaatiota prosessiolosuhteista Tiedetään, että prosessissa tapahtuu oikeita asioita Osataan ohjata prosessia Virtausmittaukset
Prosessimittaukset Miksi prosessikierroista tehdään mittauksia Saadaan informaatiota prosessiolosuhteista Tiedetään, että prosessissa tapahtuu oikeita asioita Osataan ohjata prosessia Virtausmittaukset
dekantterilaseja eri kokoja, esim. 100 ml, 300 ml tiivis, kannellinen lasipurkki
 Vastuuhenkilö Tiina Ritvanen Sivu/sivut 1 / 5 1 Soveltamisala Tämä menetelmä on tarkoitettu lihan ph:n mittaamiseen lihantarkastuksen yhteydessä. Menetelmää ei ole validoitu käyttöön Evirassa. 2 Periaate
Vastuuhenkilö Tiina Ritvanen Sivu/sivut 1 / 5 1 Soveltamisala Tämä menetelmä on tarkoitettu lihan ph:n mittaamiseen lihantarkastuksen yhteydessä. Menetelmää ei ole validoitu käyttöön Evirassa. 2 Periaate
TESTAUSSELOSTE Vesilaitosvesi
 LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 3.8.2017 17-2767 #1 1 (6) Vihdin kunta / Vihdin Vesi Saarikko Santeri vesilaitoksen johtaja PL 13 03101 NUMMELA Tilausnro
LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 3.8.2017 17-2767 #1 1 (6) Vihdin kunta / Vihdin Vesi Saarikko Santeri vesilaitoksen johtaja PL 13 03101 NUMMELA Tilausnro
VEREN ph TAUSTAA. Veressä toimii 4 erilaista puskuria. Bikarbonaattipuskuri Fosfaattipuskuri Hemoglobiini Plasmaproteiinit
 VEREN ph TAUSTAA Kehossamme kiertävä veri on nestemäinen kudos, joka voidaan kemiallisesta näkökulmasta ajateltuna määritellä seokseksi, joka sisältää useita eri komponentteja. Veren protoni konsentraation,
VEREN ph TAUSTAA Kehossamme kiertävä veri on nestemäinen kudos, joka voidaan kemiallisesta näkökulmasta ajateltuna määritellä seokseksi, joka sisältää useita eri komponentteja. Veren protoni konsentraation,
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
Liitetaulukko 1/11. Tutkittujen materiaalien kokonaispitoisuudet KOTIMAINEN MB-JÄTE <1MM SAKSAN MB- JÄTE <1MM POHJAKUONA <10MM
 Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä
 Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
MITÄ PIILEE TALOUSVEDESSÄ?
 MITÄ PIILEE TALOUSVEDESSÄ? Lahtiset olivatkin yllättäen mökillään, kun Virtaset palasivat ensimmäiseltä muuton jälkeiseltä ulkomaanmatkaltaan. He olivat tulleet mökille, koska kaupungissa oli vesijohtolaitoksen
MITÄ PIILEE TALOUSVEDESSÄ? Lahtiset olivatkin yllättäen mökillään, kun Virtaset palasivat ensimmäiseltä muuton jälkeiseltä ulkomaanmatkaltaan. He olivat tulleet mökille, koska kaupungissa oli vesijohtolaitoksen
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
Lkm keski- maksimi Lkm keski- maksimi. Lkm keski- maksimi Lkm keski- maksimi
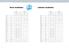 Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
Spektrofotometria ja spektroskopia
 11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta Insinöörivalinnan kemian koe MALLIRATKAISUT
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
HERMOSTON FYSIOLOGIA I
 Hermoston fysiologia I 1 HERMOSTON FYSIOLOGIA I Biosähköiset ilmiöt Kalvopotentiaali Hermosolun lepopotentiaali Hermosolun aktiopotentiaali Ionikanavat Intrasellulaarinen/ekstrasellulaarinen mittaus Neuronin
Hermoston fysiologia I 1 HERMOSTON FYSIOLOGIA I Biosähköiset ilmiöt Kalvopotentiaali Hermosolun lepopotentiaali Hermosolun aktiopotentiaali Ionikanavat Intrasellulaarinen/ekstrasellulaarinen mittaus Neuronin
VESI JA VESILIUOKSET
 VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
VESI JA VESILIUOKSET KEMIAA KAIKKIALLA, KE1 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä
AKKREDITOITU TESTAUSLABORATORIO ACCREDITED TESTING LABORATORY LUONNONVARAKESKUS VANTAA, ROVANIEMI
 T203/M13/2014 Liite 1 / Appendix 1 Sivu / Page 1(5) AKKREDITOITU TESTAUSLABORATORIO ACCREDITED TESTING LABORATORY LUONNONVARAKESKUS VANTAA, ROVANIEMI NATURAL RESOURCES INSTITUTE FINLAND VANTAA, ROVANIEMI
T203/M13/2014 Liite 1 / Appendix 1 Sivu / Page 1(5) AKKREDITOITU TESTAUSLABORATORIO ACCREDITED TESTING LABORATORY LUONNONVARAKESKUS VANTAA, ROVANIEMI NATURAL RESOURCES INSTITUTE FINLAND VANTAA, ROVANIEMI
Näytenumero Näytetunnus Tunnus Ottopvm. Näytteenottaja Saapunut pvm. Tutkimus alkoi Tutkimus valmis
 Tutkimustodistus '1.RA03' Kierros: elo 26.09.2018 Ranuan Infra Oy Keskustie 11 97700 Ranua Tulokset hyväksynyt Hanna Kemppe Laboratoriokemisti 040 704 0528 22569 (26.09.2018), 22570 (21.09.2018), 22571
Tutkimustodistus '1.RA03' Kierros: elo 26.09.2018 Ranuan Infra Oy Keskustie 11 97700 Ranua Tulokset hyväksynyt Hanna Kemppe Laboratoriokemisti 040 704 0528 22569 (26.09.2018), 22570 (21.09.2018), 22571
KE5 Kurssikoe Kastellin lukio 2012 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko.
 KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
TESTAUSSELOSTE *Talousvesi 30.6.2015
 1 (6) Kankaanpään kaupunki Tekninen virasto Vaajasaari Marja PL 36 38701 KANKAANPÄÄ Tilausnro 231959 (0KANKA/Kankaanp), saapunut 17.6.2015, näytteet otettu 17.6.2015 (9:40) Näytteenottaja: Terv. tark.
1 (6) Kankaanpään kaupunki Tekninen virasto Vaajasaari Marja PL 36 38701 KANKAANPÄÄ Tilausnro 231959 (0KANKA/Kankaanp), saapunut 17.6.2015, näytteet otettu 17.6.2015 (9:40) Näytteenottaja: Terv. tark.
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Etunimet Tehtävä 5 Pisteet / 20
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 5 Pisteet / 20 Glukoosidehydrogenaasientsyymi katalysoi glukoosin oksidaatiota
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24.5.2006 Etunimet Tehtävä 5 Pisteet / 20 Glukoosidehydrogenaasientsyymi katalysoi glukoosin oksidaatiota
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA Työskentelet metallinkierrätyslaitoksella. Asiakas tuo kierrätyslaitokselle 1200 kilogramman erän kellertävää metallimateriaalia, joka on löytynyt purettavasta
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA Työskentelet metallinkierrätyslaitoksella. Asiakas tuo kierrätyslaitokselle 1200 kilogramman erän kellertävää metallimateriaalia, joka on löytynyt purettavasta
Reaktiot ja tasapaino
 Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä/ohjattu tenttiminen*): Tunnit (ohjausajat ja labrat 1,5h): labrat: ke 12:15 14:00, ohjausajat: ti 14-15 ja pe 10-11 sopiiko? Kurssikirja: Reaktio
Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä/ohjattu tenttiminen*): Tunnit (ohjausajat ja labrat 1,5h): labrat: ke 12:15 14:00, ohjausajat: ti 14-15 ja pe 10-11 sopiiko? Kurssikirja: Reaktio
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
VÄRIKÄSTÄ KEMIAA. MOTIVAATIO: Mitä tapahtuu teelle kun lisäät siihen sitruunaa? Entä mitä havaitset kun peset mustikan värjäämiä sormia saippualla?
 VÄRIKÄSTÄ KEMIAA KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. Parhaiten työ soveltuu alakouluun kurssille aineet ympärillämme tai yläkouluun kurssille
VÄRIKÄSTÄ KEMIAA KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. Parhaiten työ soveltuu alakouluun kurssille aineet ympärillämme tai yläkouluun kurssille
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
Firan vesilaitos. Laitosanalyysit. Lkm keski- maksimi Lkm keski- maksimi
 Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
Standarditilat. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 2 - Luento 2. Tutustua standarditiloihin
 Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Standarditilat Ilmiömallinnus prosessimetallurgiassa Syksy 216 Teema 2 - Luento 2 Tavoite Tutustua standarditiloihin Miksi käytössä? Millaisia käytössä? Miten huomioitava tasapainotarkasteluissa? 1 Miten
Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo
 Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo 15.3.2017 Kationinvaihtokapasiteetti Ca 2+ K + Mg 2+ Kationi = Positiivisesti varautunut ioni Kationinvaihtokapasiteetti
Mikä on kationinvaihtokapasiteetti? Iina Haikarainen ProAgria Etelä-Savo Ravinnepiian Kevätinfo 15.3.2017 Kationinvaihtokapasiteetti Ca 2+ K + Mg 2+ Kationi = Positiivisesti varautunut ioni Kationinvaihtokapasiteetti
Suolaliuoksen ph
 Suoaiuoksen ph REAKTIOT JA TASAPAINO, KE5 Liuoksen ph-arvoon vaikuttaa oksonium- ja hydroksidi-ionien ainemäärien isäksi neutraoitumisessa muodostuvan suoan protoyysi sen mukaan mistä suoasta on kyse.
Suoaiuoksen ph REAKTIOT JA TASAPAINO, KE5 Liuoksen ph-arvoon vaikuttaa oksonium- ja hydroksidi-ionien ainemäärien isäksi neutraoitumisessa muodostuvan suoan protoyysi sen mukaan mistä suoasta on kyse.
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
1-12 R1-R3. 21, 22 T4 Tutkielman palautus kurssin lopussa (Työ 2 ja Työ 3), (R4-R6) Sopii myös itsenäiseen opiskeluun Työ 4 R7 - R8
 I Aineet ympärillämme 1 Kemia on 1x75 min tai 1-12 R1-R3 Kemia 1 kurssiin tutustumisen voi aloittaa Pohditehtävällä, jonka jälkeen opiskelijat tekevät ryhmissä yhden tehtävistä R1-R3 (tietokoneet). Oheismateriaali:
I Aineet ympärillämme 1 Kemia on 1x75 min tai 1-12 R1-R3 Kemia 1 kurssiin tutustumisen voi aloittaa Pohditehtävällä, jonka jälkeen opiskelijat tekevät ryhmissä yhden tehtävistä R1-R3 (tietokoneet). Oheismateriaali:
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Määritelmät. Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin
 Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
VALMISTEYHTEENVETO. Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos ja
 1. LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT
1. LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT
Ylioppilastutkintolautakunta S tudentexamensnämnden
 Ylioppilastutkintolautakunta S tudentexamensnämnden KEMIAN KOE 22.3.2013 HYVÄN VASTAUKSEN PIIRTEITÄ Alla oleva vastausten piirteiden ja sisältöjen luonnehdinta ei sido ylioppilastutkintolautakunnan arvostelua.
Ylioppilastutkintolautakunta S tudentexamensnämnden KEMIAN KOE 22.3.2013 HYVÄN VASTAUKSEN PIIRTEITÄ Alla oleva vastausten piirteiden ja sisältöjen luonnehdinta ei sido ylioppilastutkintolautakunnan arvostelua.
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
(Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen)
 KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
