Espoossa ) Perjeta-liitännäishoidon hoidollinen arvo
|
|
|
- Raimo Melasniemi
- 6 vuotta sitten
- Katselukertoja:
Transkriptio
1 Espoossa Roche Oy:n kommentteja Fimean julkaisemaan arviointiraporttiin pertutsumabin hoidollisesta ja taloudellisesta arvosta HER2-positiivisen varhaisvaiheen rintasyövän liitännäishoidossa Roche kiittää Fimeaa Perjetan (pertutsumabi) toukokuussa 2018 EU:ssa hyväksytyn HER2-positiivisen rintasyövän varhaisvaiheen liitännäishoitokäyttöaiheen arvioinnista. Alla esitämme kommentteja ja korjauksia Fimean arviointiraporttiin. 1) Perjeta-liitännäishoidon hoidollinen arvo Olemme samaa mieltä Fimean kanssa siitä, että uusiutumisriskin pienentämisellä on suuri merkitys hoidettaessa sairauksia, joissa leviämisen seuraukset ovat vakavia. Arvioinnissa tarkasteltu HER2-positiivinen rintasyöpä on aggressiivinen rintasyövän muoto. Siihen sairastutaan keskimäärin viisi vuotta nuorempina kuin rintasyöpään yleensä, noin 55 -vuotiaana (Perjetan liitännäishoidon EPAR s. 113; Kwan ym. 2009; Neven ym. 2008). Jos rintasyöpä muuttuu levinneeksi, ei tautia ole enää mahdollista parantaa. Levinneessä rintasyövässä HER2-spesifisillä ensimmäisen ja toisen linjan lääkehoidoilla voidaan pidentää merkittävästi elinaikaa. Kuitenkin esimerkiksi yli 50 % potilaista, jotka saavat Perjeta-Herceptin-taksaani yhdistelmähoitoa ensimmäisen linjan HER2-positiivisen levinneen taudin hoidossa, kuolevat viidessä vuodessa. Eliniän menetyksen mediaani on noin 20 vuotta. (Perjetan liitännäishoidon EPAR s. 113; Swain ym ) Varhaisen vaiheen rintasyöpä voidaan parantaa. Hoidossa tavoitteena onkin kuraatio eli estää taudin paikallinen uusiminen sekä levinneen rintasyövän kehittyminen. Uudelleen sairastuminen sekä paikalliseen rintasyöpään että sairastuminen levinneeseen rintasyöpään aiheuttaa suurta kärsimystä potilaalle ja hänen läheisilleen sekä merkittäviä kustannuksia yhteiskunnalle. Rintasyöpä tulisi pyrkiä parantamaan silloin, kuin se vielä on mahdollista. Ennen Perjetan HER2-positiivisen rintasyövän liitännäishoidon käyttöaiheen myyntiluvan hyväksymistä on standardihoitona käytetty vuoden Herceptin-liitännäishoitoa yhdistettynä kuuden syklin solunsalpaajahoitoon (Herceptin valmisteyhteenveto; Suomen Rintasyöpäryhmä Ry:n hoitosuositus 2018). Huolimatta nykyisestä Herceptin liitännäishoidosta yli 25 % HER2-positiivisista rintasyöpäpotilaista sairastuu uudelleen pitkäaikaisseurannassa. Erityisesti imusolmukepositiivisilla potilailla on suuri riski uudelleensairastumiselle pitkäaikaiseurantatutkimusten mukaan (BCIRG-006-tutkimus 10 vuoden seuranta: Slamon ym. 2015; HERA-tutkimus 11 vuoden seuranta: Cameron ym. 2017). Uusille lääkehoidoille HER2-positiivisten potilaiden varhaisvaiheen rintasyövän hoidossa on täten kuratiivisessa tilanteessa selkeä lääketieteellinen tarve (Perjetan liitännäishoidon EPAR s. 114). Laajassa (4805 tutkimuspotilasta) vaiheen III APHINITY-rekisteröintitutkimuksessa varhaisen vaiheen HER2- positiiviset rintasyöpäpotilaat satunnaistettiin saamaan liitännäishoitona Perjetaa tai lumelääkettä yhdistelmänä Herceptinin ja solunsalpaajan kanssa. Perjetan lisääminen Herceptin solusalpaajahoitoon korkean riskin potilasryhmissä (imusolmukkeisiin levinnyt ja/tai hormonireseptorinegatiivinen tauti) oli sekä kliinisesti että tilastollisesti merkittävää (esim. Perjetan liitännäishoidon EPAR s ). Tutkimuksen 1
2 ensisijainen päätetapahtuma oli elossaoloaika ilman invasiivista tautia (IDFS). Riskinalenema sairastua uudestaan paikalliseen rintasyöpään, sairastua levinneeseen rintasyöpään tai kuolemaan oli imusolmukepositiivisessa potilasryhmässä 23 % (IDFS HR 0,77; 95 % LV 0,62-0,96) ja hormonireseptorinegatiivisilla potilailla 24 % (IDFS HR 0,76; 95 % LV 0,56-1,04), kun varhaisen vaiheen HER2-positiivisen rintasyövän hoitoon lisättiin 18 sykliä Perjetaa. Rintasyövän liitännäislääkehoito on kehittynyt valtavasti vuosien varrella. APHINITY-tutkimuksessa havaittiin, että suhteellinen riski sairastua uudelleen pieneni samassa määrin kuin aiemmin on havaittu solunsalpaajaja hormoniliitännäislääkehoitojen kehittyessä (Perjetan liitännäishoidon EPAR s. 117). Perjetan liitännäishoidon käyttöaihe sai EU:ssa Significant Clinical Benefit -statuksen (merkittävä kliininen etu verrattuna aiemmin hyväksyttyihin lääkehoitoihin; Perjetan liitännäishoidon EPAR), ja sen perustella Perjetan markkinointisuoja-aikaa pidennettiin vuodella. Rekisteröintitutkimuksen päätetapahtumat APHINITY-tutkimuksen ensisijainen päätetapahtuma IDFS on yhdistelmämuuttuja, joka valittiin yhteisymmärryksessä kliinisten asiantuntijoiden ja myyntilupaviranomaisten kanssa sopivimmaksi ja herkimmäksi päätetapahtumaksi varhaisvaiheen rintasyövän liitännäishoito-tutkimukseen (esim. Perjetan liitännäishoidon EPAR s. 64). Fimean näkemyksen mukaan lopulta kiinnostuksen kohteena on syöpäpotilaiden elinajan piteneminen (arvion s. 19). Fimea esittää (arvion sivut 9, 15, 19, 24), että APHINITYn päätetapahtumista erityisesti DRFI (etäpesäkkeiden uusiutumisvapaa aika) voisi olla olennaisempi päätetapahtuma kuin IDFS. DRFI mittaa aikaa mahdollisen etäpesäkkeen ilmaantumiseen. DRFI ei sisällä kuolemaa tai aikaa kuolemaan, ja sitä ei Rochen näkemyksen mukaan tule käyttää korvikemuuttujana esimerkiksi kokonaiselinajalle. Lisäksi tulisi huomioida, että DRFI jättää huomiotta paikallisesti uusiutuvan taudin, jonka estäminen on erityisesti potilaan kannalta yksi tärkeistä kuratiiviseen Perjeta-hoidon tavoitteista. Fimean raportissa (s. 19) vertaillaan DRFI- ja IDFS-päätetapahtumia: DRFI- ja IDFS- päätetapahtumat eroavat siinä, että jälkimmäiseen sisällytetään tapahtumiksi syövän paikallinen uusiutuminen, mutta DRFI:aan tätä ei lasketa. DRFI-päätetapahtumassa otetaan huomioon vain aika etäpesäkkeiden uusiutumiseen. IDFSpäätetapahtuman arvioinnissa puolestaan otetaan huomioon invasiivisen rintasyövän paikallinen ja alueellinen uusiutuminen samassa rinnassa, invasiivinen syöpä toisessa rinnassa, etäpesäkkeet ja kuolema mistä tahansa syystä. Täten Fimean arviointiraportin DRFI:n ja IDFS:n vertailu on virheellinen. EMA on luokitellut EPAR:n analyysiosuuksissa DRFI:n kokeelliseksi päätetapahtumaksi (Perjetan liitännäishoidon EPAR s. 65, 114, 116). Hierarkkisessa testauksessa käytettiin toissijaisia päätetapatumia (IDFS-SPNBC, DFS ja OS), jotka EMA näki oleelliseksi kuratiivisessa asetelmassa. DRFI-tuloksia ei myöskään esitetä EMAn hyväksymässä Perjetan valmisteyhteenvedon tulosyhteenvedossa (Perjetan valmisteyhteenveto Taulukko 5). Arviointiraportin sivulla 15 on esitetty Fimean laskennallinen arvio paikallisesti uusiutuneen taudin osuudelle. Jos kontralateraalista uusiutumista ei luokitella paikallisesti uusiutuneeksi taudiksi, on laskentatapa virheellinen. Varhaisen vaiheen taudin tavoite on potilaan parantuminen, ja myös mikäli potilas saa paikallisen taudin uusiutumisen, ei hän ole parantunut ja hänen hoitonsa alkaa uudelleen. Taulukon 3 (s. 21) määritelmissä IDFS:n kohdalla on virhe. IDFS on elossaoloaika ilman invasiivista tautia, ei elossaoloaika ennen invasiivista tautia. Varhaisvaiheen rintasyövän hoidon päätavoite on kuraatio. 2
3 Tutkimussuunnitelman muutos Fimean arvion sivu 19: APHINITY-tutkimusta suunniteltaessa ennakoitiin tutkimukseen rekrytoitavan enemmän huonon ennusteen potilaita ja tämän valossa pertutsumabin hoitovaikutuksen arvioitiin olevan ennakoitua suurempi. Tästä syystä tutkimuksen rekrytointikriteerejä muutettiin ja otoskokoa suurennettiin tilastollisen vaikutuksen havaitsemiseksi. Myös nämä muutokset voivat Tutkimussuunnitelmaa muutettiin, jotta aikaisempia tutkimuksia vastaava (BCIRG006) imusolmukepositiivisten ja imusolmukenegatiivisten potilasmäärien suhde (65% vs. 35%) pysyisi oletettuna (esim. Perjetan liitännäishoidon EPAR s. 36). Tutkimuksen alkuvaiheessa oli rekrytoitu tutkimussuunnitelmassa ennalta määriteltyä enemmän sellaisia potilaita, joilla tauti ei ollut levinnyt imusolmukkeisiin. Hoitovaikutuksen suuruutta ei rekrytoinnin aikana tiedetty (tutkimus oli kaksoissokkoutettu: potilaat, tutkijat, henkilöstö, Roche), ja näin ollen otoskokoa ei olisi voitu suurentaa tilastollisen vaikutuksen havaitsemiseksi. Hoitovaikutuksen suhteellisen suuruuden HR-estimaatti ei muuttunut, tilastollisia hypoteeseja ei vaihdettu ja tutkimuksen kaksoissokkoutusasetelma säilyi protokollamuutoksesta huolimatta. Tähän perustuen Fimean arvion s. 19 kohta on virheellinen. Pyydämme korjaaman virheellisen kohdan koskien rekrytointikriteerien muutosta sekä siihen liittyvät virheelliset pohdinnat. Valmisteyhteenvedon mukaista lyhyemmät HER2-spesifiset hoidot Kuten Fimean arvioinnin johtopäätöksissä todetaan, standardihoidon kestoa voisi lyhentää vain, jos tiedetään, ettei hoitotulos heikkene. Sivulla 12 mainittu PERSEPHONE-tutkimus oli ns. non-inferioritytutkimus. Non-inferiority tutkimuksessa pyritään osoittamaan, että toinen hoito ei ole huonompi kuin toinen hoito tietyin ehdoin. PERSEPHONE-tutkimuksessa osoitettiin 6 kk trastutsumabihoidon ei-huonommuus verrattuna 12 kk standardihoitoon. Johtopäätöksen ehtona oli kuitenkin, että neljän vuoden kuluessa hoidon aloituksesta lyhyemmän hoidon saaneiden potilaiden joukossa sallittiin 3 % suurempi osuus kuolemia tai uudelleen sairastumisia (DFS). Tämän johdosta tutkimuksen non-inferiority-raja oli 1,31 eli sallittiin 31 % suurempi riski taudin uusiutumiseen tai kuolemaan lyhyemmällä liitännäishoidolla. Tutkimuksessa havaittu hasardisuhde (HR) oli 1,07 ja 90 % luottamusväli 0,93-1,24. Lyhyemmän hoidon saaneilla potilailla oli siis jopa 24 % suurempi riski uudelleen sairastumiseen tai kuolemaan, vaikka tutkimustulos osoittikin lyhyemmän hoidon ei-huonommuuden. Muissa aikaisemmissa liitännäishoidon kestoa arvioivissa non-inferiority tutkimuksissa ei ole pystytty osoittamaan lyhyen hoidon ei-huonommuutta (mm. PHARE: Pivot ym. 2013; SOLD: Joensuu ym. 2017; ShortHER: Conte ym. 2017). Myös tehotutkimusten meta-analyysit sekä Suomen rintasyöpäryhmä tukevat vuoden kestävää liitännäishoitoa (Gyawali ja Niraula 2017; Suomen rintasyöpäryhmän Ry:n hoitosuositus 2018). HER2-spesifisiä trastutsumabihoitoja ja myös Perjeta-hoitoja tulee olemassa olevan tutkimusnäytön valossa antaa valmisteyhteenvetojen mukaisesti potilaille vuoden ajan varhaisen vaiheen rintasyövän liitännäishoidoissa, jotta potilaille annetaan paras mahdollisuus parantua. 2) Perjeta-liitännäishoidon taloudellinen arvo Fimean laskelmien mukaan kertaluonteisen Perjeta-liitännäislääkehoidon aiheuttamat kokonaislisäkustannukset ovat keskimäärin euroa potilasta kohti. Suomessa osa korkean uusiutumisriskin HER2- positiivista varhaisvaiheen rintasyöpää sairastavista potilaista saa Perjeta-Herceptin yhdistelmähoitoa jo ennen leikkausta (neoadjuvanttihoito) (Perjetan käyttöaiheen laajennus ; Suomen Rintasyöpäryhmä Ry:n hoitosuositus 2018). Valmisteyhteenvedon mukaan Perjeta-neoadjuvanttihoitoa annetaan 3
4 3-6 hoitosykliä. Uusi Perjetan 18 syklin käyttöaihe näille potilaille tarkoittaa Perjeta-lisäsykliä leikkauksen jälkeen ja täten arvioraportissa esitettyä selvästi pienempää lisäkustannusta. Kuten Fimea mainitsee, poikkeaa heidän arvionsa (200 potilasta) vuosittaisesta Perjeta-hoitoa saavista potilaista merkittävästi myyntiluvan haltijan edustajan arviosta (alle 100 potilasta), ja potilasmääräarvioon liittyy suurta epävarmuutta. Fimea käyttää arviossaan korkean uusiutumisriskin potilaiden osuudessa APHINITY-tutkimukseen rekrytoitua populaatiota (s. 22). APHINITYn potilasryhmäosuudet säädettiin vastaamaan historiallisia tutkimuksia esimerkiksi imusolmukepositiivisten/ imusolmukenegatiivisten potilaiden osalta (Perjetan liitännäishoidon EPAR s. 30). Täten tämä arvio ei myyntiluvan haltijan näkemyksen mukaan täysin vastaa kuvaa Suomen potilaista. Potilaskohtainen välitön lääkekustannus ja budjettivaikutus eivät anna todellista kuvaa kuratiivisen valmisteen arvosta, mikäli näitä ei tarkastella yksilölle, hänen läheisilleen, terveydenhuollolle ja yhteiskunnalle lääkehoidolla pitkässä aikahorisontissa saavutettavien hyötyjen kanssa. Perjetan kertaluonteisen vuoden liitännäishoidon tarkoituksena on estää paikallisen rintasyövän uusiminen sekä rintasyövän muuttuminen levinneeksi taudiksi, joka johtaa kuolemaan. Varhaiseen vaiheen HER2-positiivisesta rintasyövästä parantuneella naisella voi olla Suomessa vielä 25 vuotta elinaikaa, josta hän voi olla yli 10 vuotta työelämässä ja sen jälkeenkin olla yhteiskunnalle merkittävä voimavara. Levinneen taudin aiheuttamasta työkyvyttömyydestä ja kuolemasta johtuva resurssimenetys yhteiskunnalle on merkittävä. Kuratiivisessa hoidossa on erityisen tärkeää ottaa huomioon ihmishengen arvo sekä inhimilliset tekijät, kuten levinneeseen tautiin sairastuneiden potilaiden ja heidän omaistensa kärsimyksen välttäminen. Levinneen HER2-positiivisen taudin pitkäaikaisesta sairaanhoidosta yhteiskunnalle tulevat kustannukset ovat korkeat. Varhaisen vaiheen rintasyövän Perjeta-Herceptin -yhdistelmähoidon oletettu vaikutus levinneen taudin epidemiologiaan (levinneen rintasyövän insidenssi mahdollisesti laskee vähitellen) säästänee sekä terveydenhuollon että koko yhteiskunnan kustannuksia. Lääkekustannuksia arvioitaessa tulisi miettiä rintasyöpähoidon kokonaisuutta ja huomioida erityisesti parantumismahdollisuus sekä pitkäaikaisvaikutus, jolloin myös uusiutumisriskin vähäiselläkin pienentämisellä voi olla suuri vaikutus. Lääkekustannusten osalta Roche Oy:llä on valmius neuvotella sairaaloiden kanssa hallitun käyttöönoton sopimuksista, hintamalleista ym. keinoista, joilla parhaat syöpähoidot saadaan potilaan käyttöön taloudellisesti kestävällä tavalla. Roche Oy:n puolesta, Nina Isonen-Sjölund Market Access Director Roche Oy Klovinpellontie 3, Espoo 4
5 Lähteet Cameron D, Piccart-Gebhart MJ, Gelber RD ym. 11 years' follow-up of trastuzumab after adjuvant chemotherapy in HER2-positive early breast cancer: final analysis of the HERceptin Adjuvant (HERA) trial. Lancet 2017;389(10075): Conte PF, Bisagni G, Frassoldati A ym. 9 weeks vs 1 year adjuvant trastuzumab in combination with chemotherapy: results of the Phase III multicentric Italian ShortHER study. Annual Meeting of the American Society of Clinical Oncology (ASCO) 2017; Abstract 501. Gyawali B ja Niraula S. Duration of adjuvant trastuzumab in HER2 positive breast cancer: Overall and disease free survival results from meta-analyses of randomized controlled trials. Cancer Treatment Reviews, 2017, 60: Herceptin valmisteyhteenveto (Luettu ) Joensuu H ym. A randomized phase III study of adjuvant trastuzumab for a duration of 9 weeks versus 1 year, combined with adjuvant taxane-anthracycline chemotherapy, for early HER2-positive breast cancer (the SOLD study). SABCS 2017, GS3-04. Kwan ML, Kushi LH, Weltzien E ym. Epidemiology of breast cancer subtypes in two prospective cohort studies of breast cancer survivors. Breast Cancer Res 2009;11(3):R31 Neven P, Van Calster B, Van den Bempt I ym. Age interacts with the expression of steroid and HER-2 receptors in operable invasive breast cancer. Breast Cancer Res Treat 2008;110(1): Perjetan liitännäishoidon EPAR epar-assessment-report-variation_en.pdf (Luettu ) Perjeta valmisteyhteenveto (Luettu ) Pivot X, Romieu G, Debled M ym. 6 months versus 12 months of adjuvant trastuzumab for patients with HER2-positive early breast cancer (PHARE): a randomised phase 3 trial. Lancet Oncol 2013; 14: Slamon DJ ym. Ten year follow-up of the BCIRG-006 trial comparing doxorubicin plus cyclophosphamide followed by docetaxel (AC T) with doxorubicin plus cyclophosphamide followed by docetaxel and trastuzumab (AC TH) with docetaxel, carboplatin and trastuzumab (TCH) in HER2+ early breast cancer patients. SABCS 2015, S5-04 Suomen Rintasyöpäryhmä Ry:n hoitosuositus 2018: +ja+hoitosuositus pdf Swain SM, Baselga J, Kim SB, Ro J ym. Pertuzumab, trastuzumab, and docetaxel in HER2-positive metastatic breast cancer. N Engl J Med 2015;372(8): DOI: /NEJMoa
PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA
 Hyväksytty Palkon kokouksessa 5.2.2019 Palveluvalikoimaneuvoston perustelumuistio PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA Sisällys 1. Taustaa, perusteet suosituksen
Hyväksytty Palkon kokouksessa 5.2.2019 Palveluvalikoimaneuvoston perustelumuistio PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA Sisällys 1. Taustaa, perusteet suosituksen
PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA
 versio 18.12.2018 Palveluvalikoimaneuvoston perustelumuistio PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA versio 18.12.2018 Sisällys 1. Taustaa, perusteet suosituksen laatimiseen...
versio 18.12.2018 Palveluvalikoimaneuvoston perustelumuistio PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA versio 18.12.2018 Sisällys 1. Taustaa, perusteet suosituksen laatimiseen...
JULKAISUSARJA 13/2018 PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA. Uusien sairaalalääkkeiden arviointi
 JULKAISUSARJA 13/2018 PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA Uusien sairaalalääkkeiden arviointi PERTUTSUMABI VARHAISVAIHEEN HER2-POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA
JULKAISUSARJA 13/2018 PERTUTSUMABI VARHAISVAIHEEN HER2- POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA Uusien sairaalalääkkeiden arviointi PERTUTSUMABI VARHAISVAIHEEN HER2-POSITIIVISEN RINTASYÖVÄN LIITÄNNÄISHOIDOSSA
Uutta lääkkeistä: Palbosiklibi
 Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Kenelle täsmähoitoja ja millä hinnalla?
 Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen
 Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku
 1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
Arviointien hyödyntäminen käytännön työssä Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue
 Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Liite III Valmisteyhteenvetoon ja pakkausselosteeseen tehtävät muutokset
 Liite III Valmisteyhteenvetoon ja pakkausselosteeseen Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen jäsenvaltioiden
Liite III Valmisteyhteenvetoon ja pakkausselosteeseen Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen jäsenvaltioiden
Suomen Syöpärekisteri Syöpätautien tilastollinen ja epidemiologinen tutkimuslaitos. Syöpäpotilaiden eloonjäämisluvut alueittain
 Syöpäpotilaiden eloonjäämisluvut alueittain Sivuilla 2 15 esitetään ikävakioidut suhteelliset elossaololuvut yliopistollisten sairaaloiden vastuualueilla vuosina 2007 2014 todetuilla ja 2012 2014 seuratuilla
Syöpäpotilaiden eloonjäämisluvut alueittain Sivuilla 2 15 esitetään ikävakioidut suhteelliset elossaololuvut yliopistollisten sairaaloiden vastuualueilla vuosina 2007 2014 todetuilla ja 2012 2014 seuratuilla
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP
 Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
Rintasyövän liitännäislääkehoidot
 Riikka Huovinen, Päivi Auvinen, Johanna Mattson ja Heikki Joensuu KATSAUS Rintasyövän liitännäislääkehoidot Suurin osa rintasyövistä on hormonireseptoripositiivisia ja kasvutavaltaan hitaita. Biologisten
Riikka Huovinen, Päivi Auvinen, Johanna Mattson ja Heikki Joensuu KATSAUS Rintasyövän liitännäislääkehoidot Suurin osa rintasyövistä on hormonireseptoripositiivisia ja kasvutavaltaan hitaita. Biologisten
Rintasyövän uudet täsmälääkehoidot
 Petri Bono ja Heikki Joensuu RINTASYÖPÄ Ajatus rintasyövän hoidosta täsmälääkkeillä ei ole uusi. Täsmälääkkeenä voidaan jo pitää kohteeseensa (estrogeenireseptoriin) spesifisesti sitoutuvaa, tehokasta
Petri Bono ja Heikki Joensuu RINTASYÖPÄ Ajatus rintasyövän hoidosta täsmälääkkeillä ei ole uusi. Täsmälääkkeenä voidaan jo pitää kohteeseensa (estrogeenireseptoriin) spesifisesti sitoutuvaa, tehokasta
Miten uudet (syöpä)lääkkeet tulevat kliiniseen käyttöön?
 Lääkehoitojen priorisointi Miten uudet (syöpä)lääkkeet tulevat kliiniseen käyttöön? Vesa Kataja, erikoislääkäri kliinisen onkologian dosentti johtajaylilääkäri Keski-Suomen sairaanhoitopiiri Terveysfoorumi
Lääkehoitojen priorisointi Miten uudet (syöpä)lääkkeet tulevat kliiniseen käyttöön? Vesa Kataja, erikoislääkäri kliinisen onkologian dosentti johtajaylilääkäri Keski-Suomen sairaanhoitopiiri Terveysfoorumi
Kliiniset lääketutkimukset yliopistosairaalan näkökulma. Lasse Viinikka 18.3.2014 Etiikan päivä 2014
 Kliiniset lääketutkimukset yliopistosairaalan näkökulma Lasse Viinikka 18.3.2014 Etiikan päivä 2014 Tutkimustyön merkitys potilashoidon kannalta parantaa asiantuntijuutta korkeatasoinen tutkija on alansa
Kliiniset lääketutkimukset yliopistosairaalan näkökulma Lasse Viinikka 18.3.2014 Etiikan päivä 2014 Tutkimustyön merkitys potilashoidon kannalta parantaa asiantuntijuutta korkeatasoinen tutkija on alansa
Noin neljäsosa EU:ssa uuden myyntiluvan saavista. Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN
 OLLI TENHUNEN LT, syöpätautien erikoislääkäri Ylilääkäri, Fimea Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN Jotta uusi syöpälääke pääsee markkinoille, edellytyksenä
OLLI TENHUNEN LT, syöpätautien erikoislääkäri Ylilääkäri, Fimea Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN Jotta uusi syöpälääke pääsee markkinoille, edellytyksenä
Opas terveydenhuollon ammattilaisille. Kadcyla (trastutsumabiemtansiini)
 Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Mitä uutta rintasyövästä
 Mitä uutta rintasyövästä Onkologiapäivät 2013 31.8.2013 Käsiteltäviä aiheita Neoadjuvanttihoidot NOAH-studyn pitkäaikaistulokset Adjuvanttihoidot Tamoksifeeni 5v. vs. 10 v. HERA-tutkimuksen päivityksiä
Mitä uutta rintasyövästä Onkologiapäivät 2013 31.8.2013 Käsiteltäviä aiheita Neoadjuvanttihoidot NOAH-studyn pitkäaikaistulokset Adjuvanttihoidot Tamoksifeeni 5v. vs. 10 v. HERA-tutkimuksen päivityksiä
Mitä uutta rintasyövästä. Onkologiapäivät
 Mitä uutta rintasyövästä Onkologiapäivät 2013 31.8.2013 Käsiteltäviä aiheita Neoadjuvanttihoidot NOAH-studyn pitkäaikaistulokset Adjuvanttihoidot Tamoksifeeni 5v. vs. 10 v. HERA-tutkimuksen päivityksiä
Mitä uutta rintasyövästä Onkologiapäivät 2013 31.8.2013 Käsiteltäviä aiheita Neoadjuvanttihoidot NOAH-studyn pitkäaikaistulokset Adjuvanttihoidot Tamoksifeeni 5v. vs. 10 v. HERA-tutkimuksen päivityksiä
JULKAISUSARJA 3/2015 TRASTUTSUMABIEMTANSIINI HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA
 JULKAISUSARJA 3/2015 TRASTUTSUMABIEMTANSIINI HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA TRASTUTSUMABIEMTANSIINI HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 3/2015
JULKAISUSARJA 3/2015 TRASTUTSUMABIEMTANSIINI HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA TRASTUTSUMABIEMTANSIINI HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 3/2015
RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA
 RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA Johanna Mattson dosentti ylilääkäri, vs. toimialajohtaja HYKS Syöpäkeskus 28.11.2016 1 RINTASYÖPÄ SUOMESSA 5008 uutta tapausta vuonna 2014 Paikallinen rintasyöpä
RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA Johanna Mattson dosentti ylilääkäri, vs. toimialajohtaja HYKS Syöpäkeskus 28.11.2016 1 RINTASYÖPÄ SUOMESSA 5008 uutta tapausta vuonna 2014 Paikallinen rintasyöpä
Kysely syöpäpotilaiden hoidosta Tulokset FIN-P-CARF /18
 Kysely syöpäpotilaiden hoidosta Tulokset FIN-P-CARF-0918-0844-9/18 OTOS Näissä tuloksissa on mukana tulokset, jotka on kerätty ajalla 4.5 18..18. Tässä esityksessä tuloksia tarkastellaan seuraavien kohderyhmien
Kysely syöpäpotilaiden hoidosta Tulokset FIN-P-CARF-0918-0844-9/18 OTOS Näissä tuloksissa on mukana tulokset, jotka on kerätty ajalla 4.5 18..18. Tässä esityksessä tuloksia tarkastellaan seuraavien kohderyhmien
Lataa Pirstaloitumisesta kohti naisena eheytymistä - Kaija Leino. Lataa
 Lataa Pirstaloitumisesta kohti naisena eheytymistä - Kaija Leino Lataa Kirjailija: Kaija Leino ISBN: 9789514485541 Sivumäärä: 268 Formaatti: PDF Tiedoston koko: 23.51 Mb Rintasyöpä on naisten yleisin syöpä
Lataa Pirstaloitumisesta kohti naisena eheytymistä - Kaija Leino Lataa Kirjailija: Kaija Leino ISBN: 9789514485541 Sivumäärä: 268 Formaatti: PDF Tiedoston koko: 23.51 Mb Rintasyöpä on naisten yleisin syöpä
Lääkkeiden taloudellinen arviointi Olli Pekka Ryynänen Itä Suomen yliopisto, Fimea
 Lääkkeiden taloudellinen arviointi Olli Pekka Ryynänen Itä Suomen yliopisto, Fimea Lääkevalmisteiden arviointi Onko lääke tehokas ja turvallinen; täyttääkö se laatuvaatimukset? Lääkehoitojen arviointi
Lääkkeiden taloudellinen arviointi Olli Pekka Ryynänen Itä Suomen yliopisto, Fimea Lääkevalmisteiden arviointi Onko lääke tehokas ja turvallinen; täyttääkö se laatuvaatimukset? Lääkehoitojen arviointi
Kehittyneet terapiat ja kalliit lääkehoidot. Vesa Kiviniemi Arviointipäällikkö Fimea
 Kehittyneet terapiat ja kalliit lääkehoidot Vesa Kiviniemi Arviointipäällikkö Fimea Seminaarissa suurennuslasin alla Mitä lääkekehityksen horisontissa näkyy? Kehittyneet terapiat ja kalliit lääkehoidot
Kehittyneet terapiat ja kalliit lääkehoidot Vesa Kiviniemi Arviointipäällikkö Fimea Seminaarissa suurennuslasin alla Mitä lääkekehityksen horisontissa näkyy? Kehittyneet terapiat ja kalliit lääkehoidot
rakko ja virtsatiet (C65 68, D09.0 1, D30.1 9, D41.1)
 Syöpäpotilaiden eloonjäämisluvut alueittain Sivuilla 2 14 esitetään suhteelliset elossaololuvut yliopistollisten sairaaloiden vastuualueilla vuosina 2005 2012 todetuilla ja 2010 2012 seuratuilla potilailla
Syöpäpotilaiden eloonjäämisluvut alueittain Sivuilla 2 14 esitetään suhteelliset elossaololuvut yliopistollisten sairaaloiden vastuualueilla vuosina 2005 2012 todetuilla ja 2010 2012 seuratuilla potilailla
Fimean suositus lääkkeiden hoidollisen ja taloudellisen arvon arvioinnista. Hannes Enlund Tutkimuspäällikkö Fimea
 Fimean suositus lääkkeiden hoidollisen ja taloudellisen arvon arvioinnista Hannes Enlund Tutkimuspäällikkö Fimea hannes.enlund@fimea.fi Kysymyksiä joihin etsitään vastauksia? Onko uusi lääke A tehokkaampi
Fimean suositus lääkkeiden hoidollisen ja taloudellisen arvon arvioinnista Hannes Enlund Tutkimuspäällikkö Fimea hannes.enlund@fimea.fi Kysymyksiä joihin etsitään vastauksia? Onko uusi lääke A tehokkaampi
Clostridium difficile diagnostiikan nykyvaihe ja pulmat. Janne Aittoniemi, LT, dos, oyl Fimlab Laboratoriot Oy
 Clostridium difficile diagnostiikan nykyvaihe ja pulmat Janne Aittoniemi, LT, dos, oyl Fimlab Laboratoriot Oy 1.10.2013 Cd-laboratoriodiagnostiikan pulmat - Kuinka Cd-infektio pitäisi diagnostisoida laboratoriossa?
Clostridium difficile diagnostiikan nykyvaihe ja pulmat Janne Aittoniemi, LT, dos, oyl Fimlab Laboratoriot Oy 1.10.2013 Cd-laboratoriodiagnostiikan pulmat - Kuinka Cd-infektio pitäisi diagnostisoida laboratoriossa?
Adaptiiviset lääkekokeet. Lääketieteellisen tutkimusetiikan seminaari Olli Tenhunen FIMEA, OYS/syöpätaudit ja hematologia
 Adaptiiviset lääkekokeet Lääketieteellisen tutkimusetiikan seminaari 1.12.2017 Olli Tenhunen FIMEA, OYS/syöpätaudit ja hematologia 2 Sisältöä Määritelmät Adaptiivisten tutkimusten keskeiset adaptaatiot
Adaptiiviset lääkekokeet Lääketieteellisen tutkimusetiikan seminaari 1.12.2017 Olli Tenhunen FIMEA, OYS/syöpätaudit ja hematologia 2 Sisältöä Määritelmät Adaptiivisten tutkimusten keskeiset adaptaatiot
Tutkimusasetelmat. - Oikea asetelma oikeaan paikkaan - Vaikeakin tutkimusongelma voi olla ratkaistavissa oikealla tutkimusasetelmalla
 Tutkimusasetelmat - Oikea asetelma oikeaan paikkaan - Vaikeakin tutkimusongelma voi olla ratkaistavissa oikealla tutkimusasetelmalla Jotta kokonaisuus ei unohdu Tulisi osata Tutkimusasetelmat Otoskoko,
Tutkimusasetelmat - Oikea asetelma oikeaan paikkaan - Vaikeakin tutkimusongelma voi olla ratkaistavissa oikealla tutkimusasetelmalla Jotta kokonaisuus ei unohdu Tulisi osata Tutkimusasetelmat Otoskoko,
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
KEUHKOSYÖVÄN SEULONTA. Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema
 KEUHKOSYÖVÄN SEULONTA Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema Seulonta on tiettyyn väestöryhmään kohdistuva tutkimus, jolla pyritään
KEUHKOSYÖVÄN SEULONTA Tiina Palva Dosentti, Syöpätautien ja sädehoidon erikoislääkäri, Väestövastuulääkäri, Kuhmoisten terveysasema Seulonta on tiettyyn väestöryhmään kohdistuva tutkimus, jolla pyritään
Hoidollisen ja taloudellisen arvon arviointi tukee lääkehoitoja koskevaa päätöksenteko...
 Page 1 of 4 JULKAISTU NUMEROSSA 1/2016 TEEMAT Hoidollisen ja taloudellisen arvon arviointi tukee lääkehoitoja koskevaa päätöksentekoa Piia Rannanheimo, Ulla Härkönen, Vesa Kiviniemi / Kirjoitettu 21.2.2016
Page 1 of 4 JULKAISTU NUMEROSSA 1/2016 TEEMAT Hoidollisen ja taloudellisen arvon arviointi tukee lääkehoitoja koskevaa päätöksentekoa Piia Rannanheimo, Ulla Härkönen, Vesa Kiviniemi / Kirjoitettu 21.2.2016
Mikä on HER2-positiivinen rintasyöpä?
 Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Uutta lääkkeistä: Vemurafenibi
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
PYLL-seminaari 30.3.2011
 PYLL-seminaari 30.3.2011 Sairaalajohtaja Jari Välimäki syöpätautien osuus ennenaikaisten elinvuosien menetysten aiheuttajina etenkin ESshp:n naisten keskuudessa kiinnittää huomiota ne ovat PYLL-tilastossa
PYLL-seminaari 30.3.2011 Sairaalajohtaja Jari Välimäki syöpätautien osuus ennenaikaisten elinvuosien menetysten aiheuttajina etenkin ESshp:n naisten keskuudessa kiinnittää huomiota ne ovat PYLL-tilastossa
Uusien sairaalalääkkeiden arviointi Fimeassa. Vesa Kiviniemi Fimea
 Uusien sairaalalääkkeiden arviointi Fimeassa Vesa Kiviniemi Fimea 29.9.2016 Arvioinnin ja arviointiprosessin taustaa Sairaalalääkkeille ei Suomessa toistaiseksi ole ollut keskitettyä tai yhtenäistä arviointiprosessia
Uusien sairaalalääkkeiden arviointi Fimeassa Vesa Kiviniemi Fimea 29.9.2016 Arvioinnin ja arviointiprosessin taustaa Sairaalalääkkeille ei Suomessa toistaiseksi ole ollut keskitettyä tai yhtenäistä arviointiprosessia
LAPATINIBI, PERTUTSUMABI JA TRASTUTSUMABIEMTANSIINI METASTASOITUNEEN HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA. JÄRJESTELMÄLLINEN KIRJALLISUUSKATSAUS
 LAPATINIBI, PERTUTSUMABI JA TRASTUTSUMABIEMTANSIINI METASTASOITUNEEN HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA. JÄRJESTELMÄLLINEN KIRJALLISUUSKATSAUS Nina Järvinen Pro gradu -tutkielma Helsingin yliopisto
LAPATINIBI, PERTUTSUMABI JA TRASTUTSUMABIEMTANSIINI METASTASOITUNEEN HER2-POSITIIVISEN RINTASYÖVÄN HOIDOSSA. JÄRJESTELMÄLLINEN KIRJALLISUUSKATSAUS Nina Järvinen Pro gradu -tutkielma Helsingin yliopisto
Noona osana potilaan syövän hoitoa
 Noona osana potilaan syövän hoitoa Noona lyhyesti Noona on mobiilipalvelu osaksi potilaan syövän hoitoa Noonan avulla Potilas osallistuu aktiivisesti hoitoonsa raportoimalla hoidon aikaisia haittoja. Hän
Noona osana potilaan syövän hoitoa Noona lyhyesti Noona on mobiilipalvelu osaksi potilaan syövän hoitoa Noonan avulla Potilas osallistuu aktiivisesti hoitoonsa raportoimalla hoidon aikaisia haittoja. Hän
Eturauhassyövän uudet lääkehoidot
 Eturauhassyövän uudet lääkehoidot 24.04.2015 Petteri Hervonen, LT, Syöpätautien erikoislääkäri Docrates Syöpäsairaala, TAYS Yleistä Eturauhassyöpä on miesten yleisin syöpätyyppi Lähes 5000 uutta diagnoosia/vuosi
Eturauhassyövän uudet lääkehoidot 24.04.2015 Petteri Hervonen, LT, Syöpätautien erikoislääkäri Docrates Syöpäsairaala, TAYS Yleistä Eturauhassyöpä on miesten yleisin syöpätyyppi Lähes 5000 uutta diagnoosia/vuosi
Sanofin kommentit Fimean arviointiraporttiin Semiplimabi
 21.10.2019 Sanofin kommentit Fimean arviointiraporttiin Semiplimabi Semiplimabi on ainoa lääke, jolla on Europan lääkeviraston hyväksymä käyttöaihe edenneen ihon okasolusyövän hoidossa. Valmisteelle on
21.10.2019 Sanofin kommentit Fimean arviointiraporttiin Semiplimabi Semiplimabi on ainoa lääke, jolla on Europan lääkeviraston hyväksymä käyttöaihe edenneen ihon okasolusyövän hoidossa. Valmisteelle on
Mitä kuuluu MALLIMAAHAN?
 Thomas Babington Macaulay: "Tosiasioiden tunnustaminen on kaiken viisauden alku." Mitä kuuluu MALLIMAAHAN? Professori Jukka Westermarck, LT Biotekniikan keskus Biolääketieteen laitos Turun Yliopisto https://tiedeedella.blogspot.fi
Thomas Babington Macaulay: "Tosiasioiden tunnustaminen on kaiken viisauden alku." Mitä kuuluu MALLIMAAHAN? Professori Jukka Westermarck, LT Biotekniikan keskus Biolääketieteen laitos Turun Yliopisto https://tiedeedella.blogspot.fi
Femar 2,5 mg tabletti, kalvopäällysteinen , versio 5.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Femar 2,5 mg tabletti, kalvopäällysteinen 18.7.2016, versio 5.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Rintasyöpä on maailmanlaajuisesti
Femar 2,5 mg tabletti, kalvopäällysteinen 18.7.2016, versio 5.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Rintasyöpä on maailmanlaajuisesti
Durvalumabi ei-pienisoluisen keuhkosyövän hoidossa kemosädehoidon jälkeen
 versio 13.3.2019 Palveluvalikoimaneuvoston suositus Durvalumabi ei-pienisoluisen keuhkosyövän hoidossa kemosädehoidon jälkeen Durvalumabi kuuluu kansalliseen palveluvalikoimaan paikallisesti edenneen,
versio 13.3.2019 Palveluvalikoimaneuvoston suositus Durvalumabi ei-pienisoluisen keuhkosyövän hoidossa kemosädehoidon jälkeen Durvalumabi kuuluu kansalliseen palveluvalikoimaan paikallisesti edenneen,
NEWS. N o 2/15. Pääkirjoitus: SOLDista BOLDiin! 10 kysymystä rintakirurgian koulutuksesta Suomessa
 NEWS S U O M E N R I N TA S Y Ö P Ä RY H M Ä RY N o 2/15 F I N N I S H B R E A S T C A N C E R G RO U P Pääkirjoitus: SOLDista BOLDiin! s.3 HEiKKi joensuu 10 kysymystä rintakirurgian koulutuksesta Suomessa
NEWS S U O M E N R I N TA S Y Ö P Ä RY H M Ä RY N o 2/15 F I N N I S H B R E A S T C A N C E R G RO U P Pääkirjoitus: SOLDista BOLDiin! s.3 HEiKKi joensuu 10 kysymystä rintakirurgian koulutuksesta Suomessa
Rintasyövän nykyaikainen hoito ja seuranta
 Rintasyövän nykyaikainen hoito ja seuranta One fits all vai Räätälöity hoito Rintasyöpä Suomessa Rintasyöpään sairastui 2007 4142 suomalaista naista ja 16 miestä Hoitotulokset ovat kansainvälisestikin
Rintasyövän nykyaikainen hoito ja seuranta One fits all vai Räätälöity hoito Rintasyöpä Suomessa Rintasyöpään sairastui 2007 4142 suomalaista naista ja 16 miestä Hoitotulokset ovat kansainvälisestikin
Fimean ja PALKOn yhteistyö lääkkeiden arvioinnissa
 Fimean ja PALKOn yhteistyö lääkkeiden arvioinnissa Vesa Kiviniemi Fimea 22.11.2016 Fimean ja PALKOn yhteistyöalueet Uusien sairaalalääkkeiden hoidollisen ja taloudellisen arvon arviointi sekä tähän liittyvä
Fimean ja PALKOn yhteistyö lääkkeiden arvioinnissa Vesa Kiviniemi Fimea 22.11.2016 Fimean ja PALKOn yhteistyöalueet Uusien sairaalalääkkeiden hoidollisen ja taloudellisen arvon arviointi sekä tähän liittyvä
Palliatiivinen hoito ja saattohoito - hoitosuunnitelma
 25.11.2016 Palliatiivinen hoito ja saattohoito - hoitosuunnitelma Tiina Saarto, yl, Palliatiivisen lääketieteen professori, Helsingin Yliopisto, HYKS Palliatiivinen keskus WHO - Palliatiivinen hoito Palliatiivisella
25.11.2016 Palliatiivinen hoito ja saattohoito - hoitosuunnitelma Tiina Saarto, yl, Palliatiivisen lääketieteen professori, Helsingin Yliopisto, HYKS Palliatiivinen keskus WHO - Palliatiivinen hoito Palliatiivisella
Lataa Seksuaalisuuden muutokset syöpään sairastuessa - Katja Hautamäki-Lamminen. Lataa
 Lataa Seksuaalisuuden muutokset syöpään sairastuessa - Katja Hautamäki-Lamminen Lataa Kirjailija: Katja Hautamäki-Lamminen ISBN: 9789514487590 Sivumäärä: 156 Formaatti: PDF Tiedoston koko: 28.41 Mb Suomalaisista
Lataa Seksuaalisuuden muutokset syöpään sairastuessa - Katja Hautamäki-Lamminen Lataa Kirjailija: Katja Hautamäki-Lamminen ISBN: 9789514487590 Sivumäärä: 156 Formaatti: PDF Tiedoston koko: 28.41 Mb Suomalaisista
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi)
 Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Levinneen rintasyövän hoito
 Johanna Mattson ja Riikka Huovinen KATSAUS Levinneen rintasyövän hoito Levinnyt rintasyöpä on edelleen parantumaton sairaus, vaikka sen hoitoon on viime vuosina tullut useita uusia tehokkaita lääkkeitä.
Johanna Mattson ja Riikka Huovinen KATSAUS Levinneen rintasyövän hoito Levinnyt rintasyöpä on edelleen parantumaton sairaus, vaikka sen hoitoon on viime vuosina tullut useita uusia tehokkaita lääkkeitä.
Propecia (finasteridi 0,2 ja 1 mg) tabletti , versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Bayer Suomessa Bayer HealthCare Bayer MaterialScience Bayer CropScience
 Bayer Suomessa Bayer HealthCare Bayer MaterialScience Bayer CropScience Suomessa toimivat liiketoimintaryhmät Bayer HealthCare keskittyy terveydenhuoltoon Bayer MaterialScience palvelee teollisuuden raaka-ainetarpeita
Bayer Suomessa Bayer HealthCare Bayer MaterialScience Bayer CropScience Suomessa toimivat liiketoimintaryhmät Bayer HealthCare keskittyy terveydenhuoltoon Bayer MaterialScience palvelee teollisuuden raaka-ainetarpeita
Miten geenitestin tulos muuttaa syövän hoitoa?
 ChemBio Helsingin Messukeskus 27.-29.05.2009 Miten geenitestin tulos muuttaa syövän hoitoa? Kristiina Aittomäki, dos. ylilääkäri HYKS Perinnöllisyyslääketieteen yksikkö Genomin tutkiminen FISH Sekvensointi
ChemBio Helsingin Messukeskus 27.-29.05.2009 Miten geenitestin tulos muuttaa syövän hoitoa? Kristiina Aittomäki, dos. ylilääkäri HYKS Perinnöllisyyslääketieteen yksikkö Genomin tutkiminen FISH Sekvensointi
Rintasyöpäpotilaan seuranta terveyskeskuksessa
 Katsaus Liisa Sailas syöpätautien ja sädehoidon erikoislääkäri KYS, Syöpäkeskus liisa.sailas@kuh.fi Pirjo Leinonen Terveyskeskuslääkäri Nurmeksen terveysasema Rintasyöpäpotilaan seuranta terveyskeskuksessa
Katsaus Liisa Sailas syöpätautien ja sädehoidon erikoislääkäri KYS, Syöpäkeskus liisa.sailas@kuh.fi Pirjo Leinonen Terveyskeskuslääkäri Nurmeksen terveysasema Rintasyöpäpotilaan seuranta terveyskeskuksessa
Mitä uutta kolorektaalisyövästä?
 Mitä uutta kolorektaalisyövästä? Tapio Salminen, TAYS Valtakunnalliset onkologiapäivät 2013 Metastasoineen taudin hoidon valinnan periaatteet kolorektaalisyövässä Ryhmä 0 R0 resekoitavissa oleva maksa
Mitä uutta kolorektaalisyövästä? Tapio Salminen, TAYS Valtakunnalliset onkologiapäivät 2013 Metastasoineen taudin hoidon valinnan periaatteet kolorektaalisyövässä Ryhmä 0 R0 resekoitavissa oleva maksa
Sakari Hietanen TYKS/Gynekologinen syövänhoito
 Sakari Hietanen TYKS/Gynekologinen syövänhoito Ei sidonnaisuuksia 900 Kohdun runko- osan syövän insidenssi 800 700 600 500 400 300 200 100 0 1957-1961 1962-1966 1967-1971 1972-1976 1977-1981 1982-1986
Sakari Hietanen TYKS/Gynekologinen syövänhoito Ei sidonnaisuuksia 900 Kohdun runko- osan syövän insidenssi 800 700 600 500 400 300 200 100 0 1957-1961 1962-1966 1967-1971 1972-1976 1977-1981 1982-1986
Lääkealan turvallisuus- ja kehittämiskeskus Fimea ja arviointiylilääkäreiden verkosto
 1 (7) 5.2.2015 Dnro 1896/60.02.01/2014 UUSIEN SAIRAALALÄÄKKEIDEN NOPEA ARVIOINTI Lääkealan turvallisuus- ja kehittämiskeskus Fimea ja arviointiylilääkäreiden verkosto Fimea ja arviointiylilääkärien verkosto
1 (7) 5.2.2015 Dnro 1896/60.02.01/2014 UUSIEN SAIRAALALÄÄKKEIDEN NOPEA ARVIOINTI Lääkealan turvallisuus- ja kehittämiskeskus Fimea ja arviointiylilääkäreiden verkosto Fimea ja arviointiylilääkärien verkosto
PET-tutkimusten vaikuttavuus ja kustannukset. Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala
 PET-tutkimusten vaikuttavuus ja kustannukset Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala ISI Web of Science: hakusana PET/CT N = 4974, 27.4.2010 Mihin diagnostisia menetelmiä tarvitaan?
PET-tutkimusten vaikuttavuus ja kustannukset Esko Vanninen palvelualuejohtaja Kuopion yliopistollinen sairaala ISI Web of Science: hakusana PET/CT N = 4974, 27.4.2010 Mihin diagnostisia menetelmiä tarvitaan?
Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
RINTASYÖVÄN VAIKUTUKSET NAISEN SEKSUAALISUUTEEN. Milla Talman & Niina Äyhö
 RINTASYÖVÄN VAIKUTUKSET NAISEN SEKSUAALISUUTEEN Milla Talman & Niina Äyhö SEKSUAALISUUS Ihmiset ymmärtävät seksuaalisuuden eri tavoilla. Seksuaalisuus koetaan myös erilailla eri-ikäisinä ja eri aikakausina
RINTASYÖVÄN VAIKUTUKSET NAISEN SEKSUAALISUUTEEN Milla Talman & Niina Äyhö SEKSUAALISUUS Ihmiset ymmärtävät seksuaalisuuden eri tavoilla. Seksuaalisuus koetaan myös erilailla eri-ikäisinä ja eri aikakausina
Eturauhassyövän seulonta. Patrik Finne
 Eturauhassyövän seulonta Patrik Finne Ulf-Håkan Stenman-juhlasymposiumi, 21.4.2009 Seulonnan tavoite löytää syöpä aikaisemmin, ennen kuin se on levinnyt mahdollistaa radikaalinen hoito Vähentää kuolleisuutta
Eturauhassyövän seulonta Patrik Finne Ulf-Håkan Stenman-juhlasymposiumi, 21.4.2009 Seulonnan tavoite löytää syöpä aikaisemmin, ennen kuin se on levinnyt mahdollistaa radikaalinen hoito Vähentää kuolleisuutta
Lääkehoitojen arviointi
 Lääkehoitojen arviointi Vesa Kiviniemi Arviointipäällikkö Fimea 23.2.2018 Sisältö Sairaalalääkkeiden arviointi Tausta ja tavoitteet Arvioinnin prosessi ja PALKOn suositukset Tulevaisuuden suunnitelmia
Lääkehoitojen arviointi Vesa Kiviniemi Arviointipäällikkö Fimea 23.2.2018 Sisältö Sairaalalääkkeiden arviointi Tausta ja tavoitteet Arvioinnin prosessi ja PALKOn suositukset Tulevaisuuden suunnitelmia
Syöpätautien hoidoista vaikuttavia tuloksia, lisää elinvuosia, odotuksia ja pettymyksiä
 Syöpätautien hoidoista vaikuttavia tuloksia, lisää elinvuosia, odotuksia ja pettymyksiä Pirkko-Liisa Kellokumpu-Lehtinen Säde- ja kasvainhoidon professori/ylilääkäri, Tay/Tays 20.11.2012 Sairaalapäivät,
Syöpätautien hoidoista vaikuttavia tuloksia, lisää elinvuosia, odotuksia ja pettymyksiä Pirkko-Liisa Kellokumpu-Lehtinen Säde- ja kasvainhoidon professori/ylilääkäri, Tay/Tays 20.11.2012 Sairaalapäivät,
Miten ehkäistä suolisyöpää? Jukka- Pekka Mecklin Yleiskirurgian professori K- SKS ja Itä- Suomen yliopisto
 Miten ehkäistä suolisyöpää? Jukka- Pekka Mecklin Yleiskirurgian professori K- SKS ja Itä- Suomen yliopisto Suolisyövän ehkäisy 1. Suolisyövän yleisyys väestössä 2. Suolisyövän riskiryhmät 3. Suolisyövän
Miten ehkäistä suolisyöpää? Jukka- Pekka Mecklin Yleiskirurgian professori K- SKS ja Itä- Suomen yliopisto Suolisyövän ehkäisy 1. Suolisyövän yleisyys väestössä 2. Suolisyövän riskiryhmät 3. Suolisyövän
Guideline on Similar biological medicinal products containing biotechnology-derived proteins as active substance: non-clinical and clinical issues
 Guideline on Similar biological medicinal products containing biotechnology-derived proteins as active substance: non-clinical and clinical issues EMA Workshop on Biosimilars, 31 October 2014 Pekka Kurki
Guideline on Similar biological medicinal products containing biotechnology-derived proteins as active substance: non-clinical and clinical issues EMA Workshop on Biosimilars, 31 October 2014 Pekka Kurki
Seminoman hoito ja seuranta. S. Jyrkkiö
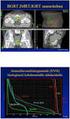 Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Ajankohtaista lääkealalla toukokuussa
 Page 1 of 5 JULKAISTU NUMEROSSA 2/2018 AJANKOHTAISTA LÄÄKEALALLA Ajankohtaista lääkealalla toukokuussa Päivi Ruokoniemi / Kirjoitettu 13.6.2028 / Julkaistu 18.6.2018 Toukokuun ajankohtaisissa lääkealan
Page 1 of 5 JULKAISTU NUMEROSSA 2/2018 AJANKOHTAISTA LÄÄKEALALLA Ajankohtaista lääkealalla toukokuussa Päivi Ruokoniemi / Kirjoitettu 13.6.2028 / Julkaistu 18.6.2018 Toukokuun ajankohtaisissa lääkealan
Syöpäpotilaan luunhoito
 Syöpäpotilaan luunhoito Petteri Hervonen Syöpätautien el, LT Oyl, HYKS Syöpäkeskus 18.4.2018 ja 26.4.2018 Syöpäpotilaan luunhoito Eturauhassyöpäpotilaan luunhoito Hormonaalinen liitännäishoito Levinneen
Syöpäpotilaan luunhoito Petteri Hervonen Syöpätautien el, LT Oyl, HYKS Syöpäkeskus 18.4.2018 ja 26.4.2018 Syöpäpotilaan luunhoito Eturauhassyöpäpotilaan luunhoito Hormonaalinen liitännäishoito Levinneen
Kivessyövän hoidossa tapahtuu
 Kivessyövän hoidossa tapahtuu S. Jyrkkiö, Tyks Onkologiapäivät 30.8.2014 Kivessyöpä yleistyy Nordcan database/ylönen O. 1 ST I kivessyöpä: seuranta tai adj hoito? 2 Seminoma ST I SWENOTECA tulokset V 2007-2010
Kivessyövän hoidossa tapahtuu S. Jyrkkiö, Tyks Onkologiapäivät 30.8.2014 Kivessyöpä yleistyy Nordcan database/ylönen O. 1 ST I kivessyöpä: seuranta tai adj hoito? 2 Seminoma ST I SWENOTECA tulokset V 2007-2010
Ilona Autti-Rämö Pääsihteeri Palveluvalikoimaneuvosto STM/OHJA
 Ilona Autti-Rämö Pääsihteeri Palveluvalikoimaneuvosto STM/OHJA 1 Mitä on palveluvalikoima? Palveluvalikoima eli Suomen julkisin varoin rahoitettujen terveydenhuollon palveluiden kokonaisuus ohjaa terveydenhuollon
Ilona Autti-Rämö Pääsihteeri Palveluvalikoimaneuvosto STM/OHJA 1 Mitä on palveluvalikoima? Palveluvalikoima eli Suomen julkisin varoin rahoitettujen terveydenhuollon palveluiden kokonaisuus ohjaa terveydenhuollon
Tervekudosten huomiointi rinnan sädehoidossa
 Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
Hoidetun rintasyöpäpotilaan seuranta
 Hoidetun rintasyöpäpotilaan seuranta Tavoitteet Seurannassa pyritään rintasyövän mahdollisen paikallisen uusiutumisen ja vastakkaisen rinnan uuden syövän varhaiseen toteamiseen. Oireettomalle potilaalle
Hoidetun rintasyöpäpotilaan seuranta Tavoitteet Seurannassa pyritään rintasyövän mahdollisen paikallisen uusiutumisen ja vastakkaisen rinnan uuden syövän varhaiseen toteamiseen. Oireettomalle potilaalle
GLP myyntilupa-arvioijan näkökulmasta
 GLP myyntilupa-arvioijan näkökulmasta Fimean GLP-keskustelupäivä 2.9. 2015 Kuopio Pauliina Lehtolainen-Dalkilic FIMEA GLPn periaatteiden tarkoitus on edistää korkealaatuisia testaustuloksia Periaatteita,
GLP myyntilupa-arvioijan näkökulmasta Fimean GLP-keskustelupäivä 2.9. 2015 Kuopio Pauliina Lehtolainen-Dalkilic FIMEA GLPn periaatteiden tarkoitus on edistää korkealaatuisia testaustuloksia Periaatteita,
Syöpähoitojen kehitys haja- Pirkko Kellokumpu-Lehtinen Säde- ja kasvainhoidon professori, ylilääkäri, TaY/TAYS 19.02.2008
 Syöpähoitojen kehitys haja- ammunnasta täsmäosumiin Pirkko Kellokumpu-Lehtinen Säde- ja kasvainhoidon professori, ylilääkäri, TaY/TAYS 19.02.2008 Haasteet Syöpämäärien lisäys/väestön vanheminen Ennaltaehkäisy/seulonnat
Syöpähoitojen kehitys haja- ammunnasta täsmäosumiin Pirkko Kellokumpu-Lehtinen Säde- ja kasvainhoidon professori, ylilääkäri, TaY/TAYS 19.02.2008 Haasteet Syöpämäärien lisäys/väestön vanheminen Ennaltaehkäisy/seulonnat
Levinneen suolistosyövän hoito
 Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Läpimurto ms-taudin hoidossa?
 Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Pioglitazone Actavis
 Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
Rintasyöpä Suomessa. Mammografiapäivät Tampere 26.6.2009. Risto Sankila. Ylilääkäri, Suomen Syöpärekisteri, Helsinki
 Rintasyöpä Suomessa Mammografiapäivät Tampere 26.6.2009 Risto Sankila Ylilääkäri, Suomen Syöpärekisteri, Helsinki Suomen Syöpärekisteri Syöpätautien tilastollinen ja epidemiologinen tutkimuslaitos... syöpärekisteri
Rintasyöpä Suomessa Mammografiapäivät Tampere 26.6.2009 Risto Sankila Ylilääkäri, Suomen Syöpärekisteri, Helsinki Suomen Syöpärekisteri Syöpätautien tilastollinen ja epidemiologinen tutkimuslaitos... syöpärekisteri
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
Lääkkeiden hoidollisen ja taloudellisen arvon arviointi. Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi
 Lääkkeiden hoidollisen ja taloudellisen arvon arviointi Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi Arviointien tavoite Tuottaa tietoa lääkkeiden käyttöönottoon ja korvattavuuteen
Lääkkeiden hoidollisen ja taloudellisen arvon arviointi Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi Arviointien tavoite Tuottaa tietoa lääkkeiden käyttöönottoon ja korvattavuuteen
Oppimistavoitteet. Syöpien esiintyvyys, ennuste, hoito ja tutkimus. Syöpien esiintyvyys. Suomen syöpärekisteri. Lisäksi
 Oppimistavoitteet Syöpien esiintyvyys, ennuste, hoito ja tutkimus Sirpa Leppä, professori Syöpätautien klinikka Hankkia yleiskäsitys syövän yleisyydestä, yleisimpien syöpien sairastavuudesta ja kuolleisuudesta
Oppimistavoitteet Syöpien esiintyvyys, ennuste, hoito ja tutkimus Sirpa Leppä, professori Syöpätautien klinikka Hankkia yleiskäsitys syövän yleisyydestä, yleisimpien syöpien sairastavuudesta ja kuolleisuudesta
Annikka Kalliokoski, Vesa Mustalammi / Kirjoitettu / Julkaistu
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2016 Reslitsumabi Annikka Kalliokoski, Vesa Mustalammi / Kirjoitettu 28.9.2016 / Julkaistu 7.11.2016 Cinqaero 10 mg/ml infuusiokonsentraatti, liuosta varten, Teva Pharmaceuticals
Page 1 of 5 JULKAISTU NUMEROSSA 3/2016 Reslitsumabi Annikka Kalliokoski, Vesa Mustalammi / Kirjoitettu 28.9.2016 / Julkaistu 7.11.2016 Cinqaero 10 mg/ml infuusiokonsentraatti, liuosta varten, Teva Pharmaceuticals
Matemaatikot ja tilastotieteilijät
 Matemaatikot ja tilastotieteilijät Matematiikka/tilastotiede ammattina Tilastotiede on matematiikan osa-alue, lähinnä todennäköisyyslaskentaa, mutta se on myös itsenäinen tieteenala. Tilastotieteen tutkijat
Matemaatikot ja tilastotieteilijät Matematiikka/tilastotiede ammattina Tilastotiede on matematiikan osa-alue, lähinnä todennäköisyyslaskentaa, mutta se on myös itsenäinen tieteenala. Tilastotieteen tutkijat
TEHOKKAAN PAHOINVOINNIN ESTOLÄÄKITYKSEN YHTEYS PAHOINVOINNIN VÄHENEMISEEN RINTASYÖPÄPOTILAILLA
 TEHOKKAAN PAHOINVOINNIN ESTOLÄÄKITYKSEN YHTEYS PAHOINVOINNIN VÄHENEMISEEN RINTASYÖPÄPOTILAILLA Laura Takala Syventävien opintojen kirjallinen työ Tampereen yliopisto Lääketieteen yksikkö Helmikuu 2017
TEHOKKAAN PAHOINVOINNIN ESTOLÄÄKITYKSEN YHTEYS PAHOINVOINNIN VÄHENEMISEEN RINTASYÖPÄPOTILAILLA Laura Takala Syventävien opintojen kirjallinen työ Tampereen yliopisto Lääketieteen yksikkö Helmikuu 2017
Pertutsumabi on nisäkkään (kiinanhamsterin munasarja) soluissa rekombinantti DNA teknologialla tuotettu humanisoitu monoklonaalinen IgG1-vasta-aine.
 1. LÄÄKEVALMISTEEN NIMI Perjeta 420 mg infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 14 ml:n injektiopullo sisältää 420 mg pertutsumabia (pitoisuus 30 mg/ml). Laimentamisen
1. LÄÄKEVALMISTEEN NIMI Perjeta 420 mg infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 14 ml:n injektiopullo sisältää 420 mg pertutsumabia (pitoisuus 30 mg/ml). Laimentamisen
Neuroendokriinisten syöpien lääkehoito
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Pertutsumabi on nisäkkään (kiinanhamsterin munasarja) soluissa rekombinantti DNA teknologialla tuotettu humanisoitu monoklonaalinen IgG1-vasta-aine.
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista.
Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista.
Rintasyövän hoitosuositus
 KÄYPÄ HOITO Diagnostiikka Rintasyövän epidemiologiaa, seulontaa ja diagnostiikkaa koskeva suositus julkaistaan erikseen. Luokitus Rintasyövän hoitoratkaisut pohjautuvat pitkälti leikkauksen jälkeiseen
KÄYPÄ HOITO Diagnostiikka Rintasyövän epidemiologiaa, seulontaa ja diagnostiikkaa koskeva suositus julkaistaan erikseen. Luokitus Rintasyövän hoitoratkaisut pohjautuvat pitkälti leikkauksen jälkeiseen
Syöpä ja eriarvoisuus
 Syöpä ja eriarvoisuus Väestöryhmien väliset erot syöpien ilmaantuvuudessa ja kuolleisuudessa Nea Malila, Suomen Syöpärekisteri 1 Syöpäpotilaiden ennuste (5-vuotiselossaolo) koulutustasoittain korkeakoulu
Syöpä ja eriarvoisuus Väestöryhmien väliset erot syöpien ilmaantuvuudessa ja kuolleisuudessa Nea Malila, Suomen Syöpärekisteri 1 Syöpäpotilaiden ennuste (5-vuotiselossaolo) koulutustasoittain korkeakoulu
bukkaalinen fentanyylitabletti Effentora_ohjeet annostitrausta varten opas 6.indd :04:58
 10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
Kohti rintasyövän säästävämpää leikkaus- ja sädehoitoa
 RINTASYÖPÄ Marjut Leidenius ja Leila Vaalavirta Kohti rintasyövän säästävämpää leikkaus- ja sädehoitoa 1198 Rintasyövän leikkaus- ja sädehoidon tavoitteena on minimoida taudin uusiutumisen riski rinnassa,
RINTASYÖPÄ Marjut Leidenius ja Leila Vaalavirta Kohti rintasyövän säästävämpää leikkaus- ja sädehoitoa 1198 Rintasyövän leikkaus- ja sädehoidon tavoitteena on minimoida taudin uusiutumisen riski rinnassa,
POTILAAN OSALLISTAMINEN
 POTILAAN OSALLISTAMINEN TUTKIMUKSEN EDISTÄMISTÄ JA HOIDON JATKUVAA LAADUN PARANTAMISTA, CASE HYKS SYÖPÄKESKUS Tuula Helander Kehittämispäällikkö, Hyks Syöpäkeskus, HUS Asiamies, Suomen Syöpäinstituutti
POTILAAN OSALLISTAMINEN TUTKIMUKSEN EDISTÄMISTÄ JA HOIDON JATKUVAA LAADUN PARANTAMISTA, CASE HYKS SYÖPÄKESKUS Tuula Helander Kehittämispäällikkö, Hyks Syöpäkeskus, HUS Asiamies, Suomen Syöpäinstituutti
Pertutsumabi on nisäkkään (kiinanhamsterin munasarja) soluissa rekombinantti DNA teknologialla tuotettu humanisoitu monoklonaalinen IgG1-vasta-aine.
 1. LÄÄKEVALMISTEEN NIMI Perjeta 420 mg infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 14 ml:n injektiopullo sisältää 420 mg pertutsumabia (pitoisuus 30 mg/ml). Laimentamisen
1. LÄÄKEVALMISTEEN NIMI Perjeta 420 mg infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 14 ml:n injektiopullo sisältää 420 mg pertutsumabia (pitoisuus 30 mg/ml). Laimentamisen
Käsitys rintasyövän patogeneesistä ja hoidosta
 Katsaus Marjut Leidenius Säästävä kirurgia on vakiinnuttanut asemansa rintasyövän hoitomuotona maassamme. Suurimpana ongelmana on syövän taipumus uusiutua leikatussa rinnassa. Säästävän leikkauksen jälkeiset
Katsaus Marjut Leidenius Säästävä kirurgia on vakiinnuttanut asemansa rintasyövän hoitomuotona maassamme. Suurimpana ongelmana on syövän taipumus uusiutua leikatussa rinnassa. Säästävän leikkauksen jälkeiset
Opas laboratoriohenkilökunnalle
 Opas laboratoriohenkilökunnalle HEMLIBRA (emisitsumabi) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Opas laboratoriohenkilökunnalle HEMLIBRA (emisitsumabi) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Pienisoluisen keuhkosyövän (SCLC) hoito. Jussi Koivunen, el, dos Syöpätau<en ja sädehoidon klinikka OYS/OY
 Pienisoluisen keuhkosyövän (SCLC) hoito Jussi Koivunen, el, dos Syöpätau
Pienisoluisen keuhkosyövän (SCLC) hoito Jussi Koivunen, el, dos Syöpätau
Iäkkään elektiivinen kirurgia - miten arvioidaan kuka hyötyy? Petri Virolainen TYKS-TULES
 Iäkkään elektiivinen kirurgia - miten arvioidaan kuka hyötyy? Petri Virolainen TYKS- Milloin potilas tulisi leikata? Potilas tulisi leikata silloin kun hänelle on leikkauksesta enemmän hyötyä kuin haittaa
Iäkkään elektiivinen kirurgia - miten arvioidaan kuka hyötyy? Petri Virolainen TYKS- Milloin potilas tulisi leikata? Potilas tulisi leikata silloin kun hänelle on leikkauksesta enemmän hyötyä kuin haittaa
Teknologian hankintapäätökset sairaaloissa. Risto Roine Professori Itä-Suomen yliopisto
 Teknologian hankintapäätökset sairaaloissa Risto Roine Professori Itä-Suomen yliopisto Uusien menetelmien arviointi sairaanhoitopiireissä Uusien menetelmien käyttöönotolle ei yleensä virallista, organisaatiotason
Teknologian hankintapäätökset sairaaloissa Risto Roine Professori Itä-Suomen yliopisto Uusien menetelmien arviointi sairaanhoitopiireissä Uusien menetelmien käyttöönotolle ei yleensä virallista, organisaatiotason
