KATSAUS. In vitro -menetelmät ja kemikaalien turvallisuuden testaus. Kimmo Louekari, Lotta Salminen ja Hanna Tähti
|
|
|
- Aino Lehtinen
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 KATSAUS In vitro -menetelmät ja kemikaalien turvallisuuden testaus Kimmo Louekari, Lotta Salminen ja Hanna Tähti Uusien kemikaalien turvallisuus pyritään nykyään varmistamaan, ennen kuin ne lasketaan markkinoille. Torjunta-aineiden, lääkkeiden ja kosmeettisten aineiden turvallisuustestaus on jo pitkään ollut käytössä lainsäädännön perusteella. Testauksessa käytetään OECD:n hyväksymiä ohjeita. Useimmat testit tehdään koe-eläimillä, tavallisesti jyrsijöillä, mutta jonkin verran kokeita tehdään myös koirilla, kissoilla ja kädellisillä. Viime vuosina koe-eläinten käyttöä on haluttu vähentää monista syistä. Tutkijat ottavat yhä enemmän huomioon muuttuneet eettiset käsitykset. Myös taloudelliset ja tieteelliset syyt puoltavat usein in vitro -menetelmien käyttöä. Ne ovat nopeampia ja halvempia kuin eläinkokeet, ja joissakin tapauksissa niillä voidaan saada täsmällisempää tietoa aineen vaikutusmekanismeista. Ennen kuin in vitro -testejä voidaan hyväksyä OECD:n virallisiin ohjeistoihin, ne validoidaan eli niiden käyttökelpoisuus arvioidaan monessa eri vaiheessa. Parhaillaan OECD:ssä valmistellaan in vitro -testejä mm. valoärsytyksen (fotoirritaation) ja ihonläpäisykyvyn tutkimiseksi. Kemikaalien toksikologisista vaikutuksista saadaan tietoja mm. eläinkokeissa ja in vitro -tutkimuksissa sekä työlääketieteellisissä selvityksissä. In vitro -tutkimuksilla tarkoitetaan menetelmiä, joissa käytetään viljeltyjä tai eristettyjä soluja, kudoksia tai elimiä koe-eläinten asemesta. Saatavilla on myös ihmisen soluja, esimerkiksi eri kudosten kasvaimista lähtöisin olevia solulinjoja. Toksikologinen kokeellinen tutkimus perustuu kuitenkin suuhavainnot Ihmisrimmaksi osaksi eläinkokeisiin. Viime aikoina on in vitro -menetelmien käyttö lisääntynyt, samalla kun koe-eläinten käyttöön liittyviin eettisiin kysymyksiin on kiinnitetty erityistä huomiota (kuva 1). Eläinkokeisiin liittyviä keskeisiä eettisiä tavoitteita ovat olleet testien kehittäminen ja In vivo -tutkimukset Toksikologian tietokannat In vitro -tutkimukset Kuva 1. Kemiallisen turvallisuuden arvioinnin menetelmät. Duodecim 114: ,
2 Yhdisteen kemialliset ja fysikaaliset ominaisuudet Solutestit Eläinkokeet Arviointivaihe ihmisen myrkytystiedostot Annos/vaste-arviointi Mekanismien arviointi solutesteillä solu- ja eläintulokset Seulontavaihe Toksisuusluokitus Ympäristöpitoisuudet Terveysriskien arviointi Kuva 2. Kaavio in vitro -testien käytöstä osana kokeellista toksikologista riskin arviointia. Aluksi käytetään in vitro -testiä (tai useampia testejä) erottelemaan haitalliset molekyylit. Testausta jatketaan in vivo -kokein molekyyleillä, jotka seulonnassa eivät aiheuttaneet haittaa. In vitro -testejä voidaan käyttää myöhemmässä vaiheessa mm. toksisen mekanismin tarkempaan selvittämiseen. parantaminen, eläinten käytön vähentäminen ja eläinkokeiden korvaaminen in vitro -kokeilla. Russel ja Burch esittivät tämän»kolmen R:n periaatteen» jo vuonna Myöhempi koeeläinten käyttöön liittyvä eettinen keskustelu perustuu paljolti tähän periaatteeseen. Kiinnostus vaihtoehtoisten toksisuuskokeiden kehittämiseen ja validointiin eli tieteellisesti päteväksi osoittamiseen ei ole kasvanut ainoastaan eettisistä syistä vaan myös siksi, että in vitro -menetelmät ovat seulontatesteiksi sopivia, taloudellisesti edullisia ja joissakin tapauksissa paras tapa selvittää toksisuuden mekanismeja. Rohkaistakseen vaihtoehtoisten testimenetelmien kehittämistä EU:n jäsenmaat ovat päättäneet pyrkiä vähentämään koe-eläintutkimuksia 50 %:lla vuoteen 2000 mennessä. Asiaa koskeva komiteanmietintö (86/609/EEC) esitettiin Sen artiklassa 7.2 todetaan:»koetta ei pidä tehdä, jos on käytettävissä tieteellisesti riittävä, tarkoitukseen sopiva menetelmä, jossa ei käytetä koe-eläintä.» Lisäksi EU:n kosmetiikkatuotteita koskeva direktiivi (93/35/EEC) kieltää eläinkokeiden käytön vuodesta 2000 lähtien, jos vaihtoehdoksi löytyy validoitu testimenetelmä (Rasmussen 1995). EU:n komission tekemän selvityksen mukaan suurissa jäsenmaissa kuten Saksassa, Ranskassa ja Isossa-Britanniassa käytetään vuosittain noin miljoonaa koe-eläintä. Yli puolet koe-eläimistä käytetään lääkeaineiden turvallisuuden ja tehon tutkimukseen sekä perustutkimukseen. Muiden kuin lääkeaineiden testaamiseen käytetään noin % koe-eläimistä (EU Commission 1994). In vitro -tutkimukset soveltuvat nykyään parhaiten toksikologiseen seulontaan ja mekanismien tutkimiseen (kuva 2). Kuluu useita vuosia, ennen kuin in vitro -menetelmät yleistyvät kemikaalien lakisääteisessä testauksessa. Seulontatyyppisiä soluviljelmätestejä käytetään sen sijaan teollisuuden laboratorioissa runsaasti, vaikka suurinta osaa niistä ei ole vielä hyväksytty OECD:n testimenetelmiksi. Tällaisia ovat mm. ihon ja silmän ärsytystä ja korroosiota selvittävät soluviljelmäkokeet. Tulevaisuudessa useampaa kuin yhtä solutyyppiä sisältävien soluviljelmien käyttö ja 852 K. Louekari ym.
3 useiden solutason biomerkkiaineiden ja biokemiallisten vasteiden tutkiminen saattavat korvata monimutkaisia eläinkokeita. Viljelmään voidaan lisätä mekanismeja, jotka vaikuttavat oleellisesti kemikaalin toksisuuteen in vivo. On mahdollista käyttää esimerkiksi maksasoluista eristettyjä mikrosomeja, jolloin testissä saadaan selville toksisten metaboliittien mahdolliset vaikutukset. Hermosoluviljelmään voidaan yhdistää veri-aivoesteviljelmä. Sen mallina on käytetty mm. endoteelisolujen viljelmää ja munuaistubuluksen epiteelisolujen viljelmiä, joissa solujen väliset tiiviit liitokset vastaavat veri-aivoesteen rakennetta. Tutkittava yhdiste joutuu läpäisemään tämän lisäviljelmän, ennen kuin se pääsee vaikuttamaan varsinaiseen neuroniviljelmään (Tähti ym. 1995). Eri kudoksille tyypillisten biomerkkiaineiden käyttö ja relevanttia toksisuutta osoittavien reaktioiden määritys on tutkimuksissa oleellisen tärkeää. Uusien in vitro -menetelmien löytäminen on mahdollista solubiologian ja molekyylibiologian tietämyksen lisääntyessä. Vaikutusmekanismien entistä täsmällisempi tuntemus auttaa vähentämään koe-eläinten määrää toksisuustutkimuksissa. OECD:n ohjeistot ja vaihtoehtoisten testien kehittäminen Kemikaalien rekisteröintiä varten tarvittavissa tutkimuksissa käytetään laajalti OECD:n hyväksymiä ohjeita. Jäsenmaiden viranomaiset ovat sitoutuneet hyväksymään myös muissa jäsenmaissa tehdyt tutkimukset, jos niissä on noudatettu OECD:n ohjeita. Tämä säästää huomattavasti aikaa ja varoja sekä johtaa laboratorioiden rajallisen kapasiteetin tehokkaaseen käyttöön. Samaan aikaan kun vaihtoehtoisia menetelmiä on kehitetty ja EU on ollut poliittisista ja eettisistä syistä asiassa aloitteellinen, OECD (1990) on mm. julkaissut monografian in vitro -menetelmien validoinnin tieteellisistä kriteereistä. OECD on myös pyytänyt jäsenmaita täydentämään kansallisten asiantuntijoiden ryhmiä siten, että myös in vitro -menetelmien asiantuntemus olisi riittävää. Edelleen se on käynnistänyt eräiden in vitro -testien valmistelun; näitä ovat: perkutaanisen absorption testi, vaihtoehtoinen in vitro -testi osana fotoirritaatiokoetta sekä solutransformaatiotesti niiden kemikaalien toteamiseksi, joilla saattaa olla ei-mutageeninen karsinogeeninen vaikutus. Myös muiden vaihtoehtoisten ja in vitro -testien kehitys on ollut viime vuosina nopeaa. LD 50 -testi Isossa-Britanniassa julkaistujen tietojen mukaan välittömän myrkyllisyyden tutkimuksiin käytetään 29 % kaikista koe-eläimistä (APC 1994). OECD on viime vuosina hyväksynyt joitakin LD 50 -testiä korvaavia tutkimuksia, jotka tehdään pienemmällä eläinmäärällä. Nämä testit ovat myös»korvaavia», koska ne vähentävät oleellisesti koe-eläinten käyttöä. Niillä ei kuitenkaan saada tarkkaa LD 50 -arvoa. Tulosten perusteella aineet voidaan kuitenkin luokitella välittömän myrkyllisyyden suhteen, ja tuloksia voidaan käyttää myös pitkäaikaistestien annosten valinnassa. Esimerkiksi»up and down» -menetelmässä käytetään aluksi vain yhtä annostasoa ja koe-eläinryhmää. Tuloksen mukaan annosta suurennetaan tai pienennetään, kunnes löydetään pienin välittömästi myrkyllinen annos. Koska uusia menetelmiä pidetään riittävinä, OECD:n kokouksissa on jo keskusteltu LD 50 -testiohjeen poistamisesta tarpeettomana (OECD 1997). Ihmissoluviljelmillä tehdyt toksisuustutkimukset saattavat tulevaisuudessa korvata osan eläinkokeista. Ihoabsorptiotesti Ihoabsorption tutkiminen in vitro on perusteltua, koska tärkein imeytymistä rajoittava kudos on kuollutta solukkoa (marraskesi). In vitro -testissä mitataan kemikaalin passiivista diffuusiota iholeikkeen läpi kammioon, josta kemikaalin pitoisuus voidaan mitata. Tässäkin menetelmässä on tyypillisiä in vitro -kokeen rajoituksia: kuolleessa ihossa ei ole normaalia aineenvaihduntakapasiteettia eikä kykyä parantua. Monet tekijät, kuten ihonäytteen kunto, lämpötila ja kantajaaineet, vaikuttavat imeytymiseen (Frankild 1997). Siksi kokeet tehdään kontrolloiduissa oloissa, jotka määritetään tarkasti OECD:n ohjeluonnoksessa. In vitro -menetelmät ja kemikaalien turvallisuuden testaus 853
4 Genotoksisuus ja karsinogeenisuustestit OECD on hyväksynyt useita in vitro -testiohjeita genotoksisuuden tutkimiseen. Tunnetuin näistä kokeista on Amesin (1973) testi, jossa osoitetaan aineen genotoksisuus salmonellaviljelmän avulla. Näiden testien kustannukset ovat hyvin alhaiset verrattuna koe-eläimillä tehtäviin, noin kaksi vuotta ja satoja eläimiä vaativiin kokeisiin. Genotoksisuustestistä saatavaa positiivista tulosta pidetään yleensä käyttökelpoisena seulontatietona mm. harkittaessa eläinkokeen tarpeellisuutta. Näyttää siltä, että in vitro -genotoksisuustestien alhainen hinta ja verrattain hyväksi todettu korrelaatio in vivo -vasteisiin ovat johtaneet niiden laajaan hyväksymiseen ja käyttöön. In vitro -genotoksisuustesteissä ei kuitenkaan voida havaita ei-mutageenisia karsinogeenisia vaikutuksia eikä epäsuorasti karsinogeenisia vaikutuksia (esim. solujen väliseen kommunikaatioon tai solunsisäisiin signaalijärjestelmiin ja geenien säätelyyn liittyviä). Pitkäkestoisia karsinogeenisuuskokeita on vaikea korvata lyhyellä in vitro -testillä. Vuonna 1996 käynnistyneessä pohjoismaisessa projektissa arvioidaan ei-mutageenisen karsinogeenisuuden mekanismeja ja menetelmien nykytilaa. Ei-mutageenisten karsinogeenien merkitys kasvaa, sillä mutageenit seuloutuvat nykyään jo tuotekehityksen varhaisessa vaiheessa pois. Kaikki karsinogeenit eivät kuitenkaan ole mutageeneja. Ei-mutageeniset karsinogeeniset aineet voivat esimerkiksi kiihdyttää solunjakautumista, ehkäistä solujen välistä kommunikaatiota tai vaikuttaa geenien säätelyyn (Wärngård ja Pelin 1995). Näitä aineita on kutsuttu myös promoottoreiksi tai epigeneettisiksi karsinogeeneiksi. In vitro -testien kehittäminen näiden aineiden havaitsemiseksi on suotavaa, koska nykyisin ei-mutageeniset karsinogeenit voidaan havaita vain eläinkokeilla, jotka ovat erittäin kalliita, kestävät kauan ja laajasti käytettyinä ruuhkauttaisivat täysin maailman testilaboratoriot. On arvioitu, että koe-eläinten käytössä saataisiin aikaan suurin vähennys, jos karsinogeenisuustestaus voitaisiin tehdä vain yhdellä eläinlajilla (Purchase 1997). Toistaiseksi ei-mutageenisten karsinogeenien testausmenetelmiä ei ole hyväksytty OECD:ssä, joskin solutransformaatiota koskevasta menetelmästä on valmistettu testiohjeluonnos. Solujen välisen kommunikaation (gap junctional intercellular communication) estyminen on ilmeisesti se mekanismi, jonka vuoksi esimerkiksi geneettisesti muuttuneiden solujen jakautuminen voi kiihtyä ilman, että ympäröivien solujen viestit tavoittaisivat ne. Menetelmät, joita käytetään solutransformaation ja solujen välisen kommunikaation tutkimiseen, ovat verrattain laajalti käytössä, ja niitä pyritään parhaillaan validoimaan. Muita ei-mutageenisia mekanismeja ovat mm. proteiinifosfataasien estoa seuraavat muutokset solun tukirangassa, solunsisäisen signaalijärjestelmän muutokset, solunjakautumisen nopeutuminen sekä oksidatiivisen stressin vaikutukset geenien ilmentymiseen. On todennäköistä, että lähivuosina virallisiin ohjeistoihin ei vielä hyväksytä menetelmiä, joilla näitä vaikutuksia voidaan havaita. Ihoärsytys, ihokorroosio ja silmäärsytystestit OECD:n asiantuntijakokouksessa on laadittu ehdotukset ihoärsytystä ja -korroosiota sekä silmä-ärsytystä koskeviksi testausstrategioiksi. Näille strategioille on yhteistä se, että rakenneaktiivisuusanalyysit (SAR) ja rakenneominaisuusanalyysit (SPR) sekä ph ovat testauksen pohjana. Jos nämä tiedot riittävät osoittamaan, että aine on ärsyttävä tai syövyttävä, lisätestausta ei tarvita. Seuraavaksi kyseisiä ominaisuuksia tutkitaan validoiduilla in vitro -testeillä. Tässä on huomattava, ettei sellaisia vielä ole silmä-ärsytyksen testaamiseksi. Validaatiotutkimukset, joissa vertailukohtana on käytetty Draizen testiä (Draize ym. 1944), eivät ole tuottaneet hyväksyttäviä tuloksia arvioitaessa in vitro -silmä-ärsytystestien pätevyyttä (Balls ym. 1995b, Brantom ym. 1997). Tavoitteena on, että tulevaisuudessa silmä- ja ihoärsytyksen koe-eläintestit aloitetaan vasta in vitro -testien jälkeen ja aluksi vain yhdellä eläimellä. Jos tulos on positiivinen, in vivo -testausta ei jatketa, ja jos se on negatiivinen, käytetään vielä 1 2 eläintä tuloksen varmistamiseen (kuva 2). OECD:n testiohjeet (404 ja 405) ihoärsytyksen ja -korroosion tutkimiseksi antavat jo nykyi- 854 K. Louekari ym.
5 sin mahdollisuuden käyttää vaihtoehtoisia testejä, joita ei vielä ole muodollisesti validoitu. Testiohje 404:ssä todetaan:»saattaa olla tarpeetonta testata eläinkokeissa sellaisia aineita, joiden kudosta syövyttävät ominaisuudet voidaan ennakoida in vitro -testien perusteella.» Varsinkin kosmetiikkateollisuuden käyttöön on etsitty testejä ja testisarjoja, joilla eläinkokeita voitaisiin korvata (Ohno ym. 1995). Uudet silmätoksisuutta arvioivat testit Koska validoinnissa ei ole löytynyt silmä-ärsytystä mittaavaa hyvää vaihtoehtoista menetelmää, on kehitettävä parempia in vitro -testejä tai muutettava validointimenetelmiä. Validoinnista vastaavat tahot (ECVAM) ovatkin korostaneet, että arviointeihin tulee saada mukaan enemmän kliinistä asiantuntemusta. Toisaalta validoinnissa»huonon tuloksen» saavuttaneet Draizen silmäärsytystestin vaihtoehdot, esimerkiksi HET-CAM (menetelmä, jossa käytetään kanan alkion allantoiskalvoa) ja EYTEX (kaupallinen koeputkitesti), eivät todennäköisesti mittaa kemikaalien silmä-ärsytyksen herkimpiä merkkiaineita (Brantom ym. 1997). Silmätestauksen tarve ei rajoitu ärsytyskokeeseen. Varsinkin lääkehoidon yhteydessä silmän sisäosan kudoksissa voi ilmetä haittavaikutuksia (Grant 1986), joita on vaikea ennakoida eläinkokeiden perusteella. Verkkokalvon eri soluilla suoritetut in vitro -testaukset ovat sopiva seula toksisuuden ennakoimiseksi ja myös paras tapa selvittää toksisuuden mekanismeja. Silmätoksisuustestien tarve kasvaa silmälääkityksen kehittyessä»täsmähoidoksi», jossa lääkkeet, esimerkiksi mikrobilääkkeet ja solunsalpaajat, annetaan suoraan silmän sisään lasiaisinjektioina tai silmänsisäisten lääkeannostelijoiden avulla. Uudet antotavat on kuitenkin otettu käyttöön riittämättömien eläinkokeiden jälkeen, ja potilaille on aiheutettu lukuisia vakavia haittavaikutuksia, kun turvallisina pidettyjä lääkkeitä on annettu lasiaiseen. Campochiaro ja Conway (1991) raportoivat 93 verkkokalvon keskiosan infarktitapausta, jotka oli todettu sen jälkeen, kun potilaiden lasiaiseen oli ruiskutettu gentamisiinia tai muita aminoglykosideja yleisesti turvallisina pidettyinä annoksina. Lisäksi useita lääkkeitä saatetaan käyttää samanaikaisesti, jolloin in vitro -tutkimukset ovat taloudellisesti edullisin vaihtoehto eri lääkeyhdistelmien testaamiseksi. Myös muiden elinten esimerkiksi aivojen»täsmähoidon» kehittyessä tullaan tarvitsemaan lukuisten erityyppisten bioteknisesti tuotettujen lääkeaine-ehdokkaiden testausta. Tämä toteutuu parhaiten käytettäessä asianomaisen kudoksen tai solukon viljelmiä. Testejä kehittävät kansainväliset yhteisöt OECD:n lisäksi myös eräät muut kansainväliset yhteisöt ovat vahvasti mukana vaihtoehtoisten testimenetelmien kehittämisessä, mm. Vaihtoehtoisten menetelmien validoinnin eurooppalainen keskus (European Centre for the Validation of Alternative Methods, ECVAM), joka koordinoi testimenetelmien validointia EU:ssa. ECVAM määrittää myös testiprotokollat, joita validoinnissa käytetään, ja järjestää laboratorioiden välisiä validointitutkimuksia (Balls ym. 1995a, Bruner ym. 1996). ECVAM on äskettäin saanut valmiiksi in vitro -fototoksisuustestin validoinnin (Spielman ym. 1998). Tärkeä taho on myös koe-eläintestien vaihtoehtojen keskus John Hopkins -yliopistossa Yhdysvalloissa. Sen tehtävänä on etsiä tieteellisesti hyväksyttäviä vaihtoehtoja eläinkokeille. Pohjoismainen MEIC-projekti (Multicenter Evaluation of In Vitro Cytotoxicity) on tehnyt uraauurtavaa työtä in vitro -menetelmien käyttökelpoisuuden ja luotettavuuden selvittämiseksi. MEIC-projektissa 30 laboratoriota on tutkinut 50 referenssikemikaalin toksisuutta eri in vitro -menetelmillä. Siinä verrattiin myrkytyskeskusten tietoja sekä 30 laboratorion solutoksisuustuloksia tietyistä aineista (Bondesson ym. 1989). Kuolemaan johtaneissa myrkytystapauksissa verestä mitattuja aineen pitoisuuksia verrattiin vastaaviin in vitro -tutkimuksissa saatuihin solutoksisiin pitoisuuksiin. Vertailu osoitti, että tämä korrelaatio on parempi kuin eläinkokeiden ja ihmiselle tappavien pitoisuuksien välinen korrelaatio. Poikkeuksena ovat aineet, jotka läpäisevät helposti veri-aivoesteen. Nämä aineet ovat paljon myrkyllisempiä kuin ei-neuraalisten solutestien perusteella voidaan päätellä, sillä keskushermosto on In vitro -menetelmät ja kemikaalien turvallisuuden testaus 855
6 herkempi toksisille vaikutuksille kuin muut kudokset (Ekwall ym. 1997). Projektin johtajan Björn Ekwallin päätelmänä on, että solututkimukset ennustavat jonkin aineen ihmiselle vaarallisia pitoisuuksia paremmin kuin eläinkokeet ja että välitöntä toksisuutta mittaavat eläinkokeet voitaisiin korvata soluviljelyillä. Validointi ja testausstrategiat OECD järjesti vuonna 1996 työryhmäkokouksen vaihtoehtoisten toksisuustestien validoinnista ja hyväksyttävyyden kriteereistä. Siinä saavutettiin laaja kansainvälinen yhteisymmärrys niistä periaatteista, joita noudattaen in vitro -testien validointi eli tieteellisesti luotettavaksi osoittaminen tulisi suorittaa. Kokouksessa pohdittiin myös, mitä vaiheita testin validointiin tulisi kuulua ja miten in vitro -testit tulisi liittää eläinkokeisiin ja testausstrategiaan (Draft Group Reports of the OECD Workshop 1996). Viralliseksi testiohjeeksi hyväksyminen edellyttää, että testin tulokset soveltuvat riskin arvioinnin välineeksi terveys- ja ympäristöhaittojen ehkäisemisessä. OECD:n asettamat kriteerit toksisuustestien hyväksynnälle (pätevät luonnollisesti myös in vitro -testeihin) ovat:»ehdotetun testin/tutkimusmenetelmän tulee läpäistä kriittinen arviointi, joka koskee testin tieteellistä perustaa/oikeutusta, herkkyyttä ja toistettavuutta, ja sisältää mahdollisuuksien mukaan vertailevaa tutkimusta, joka tukee testimenetelmän validiteettiä.» Kaavio OECD:n testiohjeen kehittämisen vaiheista on esitetty kuvassa 3. In vitro -kokeiden validoinnille asetetaan yleisesti varsin suuret vaatimukset. Vaatimukset lienevät suuremmat kuin in vivo -kokeilta on aikanaan edellytetty. In vivo -kokeiden validoinnissa ongelmana on luotettavan vertailukohdan ja -aineiston löytäminen. Esimerkiksi jyrsijäkokeiden tuloksia ei useimmiten voi verrata ihmisellä tehtyjen kokeiden tuloksiin, koska jälkimmäisiä ei läheskään aina ole käytettävissä. Siksi in vivo -kokeita ei ole voitu aina validoida muodollisesti. Pohdittaessa in vitro -testien validointia on muistettava, että myös in vivo -testi, johon tuloksia verrataan, saattaa olla epäluotettava. Esimerkiksi Draizen silmä-ärsytys- ja korroosiotesti Aloitteet kansallisilta koordinaattoreilta, tiedeyhteisöiltä tai OECD:n sihteeristöltä Kansallisten koordinaattorien kokous Tieteellinen katsaus testimenetelmiin Testiohjeluonnos OECD:n sihteeristöltä Kommenttikierros ja asiantuntijakokoukset Kansallisten koordinaattorien ja OECD:n ympäristökomitean hyväksyntä Kuva 3. OECD:n testiohjeen kehittäminen kemikaalien turvallisuuden tutkimista varten (Koëter 1995). eivät ole täysin luotettavia, koska löydösten arviointi ja pisteitys on subjektiivista. On siis mahdollista, että joissakin tapauksissa in vitro -testin validointi epäonnistuu vertailukohtana käytettävän in vivo -testin epätarkkuuden takia. Validoinnin kriteerit OECD:n piirissä on päätetty, että kemikaalien turvallisuustestaukseen tarkoitetun metodin tulee täyttää mm. seuraavat kriteerit: 1) Menetelmän tulee olla tieteellisesti ja hallinnollisesti perusteltu. 2) On osoitettava, että in vitro -testissä mitataan samoja biologisia ja toksisia vaikutuksia kuin in vivo -testissä. 3) Validointi tulee dokumentoida yksityiskohtaisesti, jotta se voidaan tarvittaesssa toistaa. 4) Menetelmällä saatujen tulosten pitää olla toistettavissa samassa laboratoriossa ja muissa laboratorioissa. 5) Menetelmän käyttökelpoisuus on osoitettava referenssikemikaaleilla. 6) Menetelmän herkkyys ja vaikutuksille herkät lajit tulee arvioida. Hallinnollisen hyväksymisen kriteerit Hallinnollinen hyväksyminen riippuu tieteellisen validoinnin tuloksesta. Hyväksyntää nopeut- 856 K. Louekari ym.
7 Testin vaihe Kehittelyvaihe Prevalidointi Validointivaihe 1 Validointivaihe 2 Asiantuntijaryhmän käsittely Ohjeistoihin hyväksyminen Aika vuosina menetelmän julkaisemisesta Kuva 4. OECD:n ohjeistoihin tarkoitetun toksisuustestin kehittämisen ja validoinnin aikataulu (Purchase 1997). taa, jos hallinnollinen taho otetaan mukaan validointiprosessiin jo varhaisvaiheessa. Seuraavat kriteerit ovat tärkeitä harkittaessa testimenetelmän hyväksymistä kansainvälisiin, esimerkiksi OECD:n ohjeistoihin: 1) Menetelmän tulisi ennustaa vaikutuksia paremmin kuin aiemmin hyväksytyt menetelmät. 2) Menetelmän tulee tuottaa riskin arviointiin entistä parempaa aineistoa. 3) Ennen hyväksymistä riittävä määrä kemikaaleja pitää testata kyseisellä menetelmällä. 4) Testin tulee olla tehokas ja eri laboratorioihin soveltuva. Tarvittavien erityislaitteistojen ja tekniikoiden pitää olla käytössä useissa laboratorioissa. 5) Tulee esittää tieteellinen, eettinen ja taloudellinen perustelu testin valinnalle aikaisempien menetelmien sijasta. On noudatettava»kolmen R:n periaatetta» (reduce, refine, replace). Testausstrategioiden periaatteet Testausstrategia tarkoittaa useiden testien muodostamaa kokonaisuutta, jossa tietystä tuloksesta päätellään mm., mitä muita kokeita on tarpeen tehdä. Testausstrategioilla pyritään mm. siihen, että selvästi toksiset kemikaalit voidaan seulontatesteillä havaita mahdollisimman aikaisin, jolloin voidaan vähentää koe-eläinten käyttöä. Testausstrategioiden periaatteita ovat mm. seuraavat: 1) Olemassa olevia tietoja fysikaalis-kemiallisista ominaisuuksista, rakenneaktiivisuusanalyyseista ja eri alojen toksikologisista tietokannoista tulee käyttää ennen testauksen aloittamista. 2) On painotettava vähemmän kipua aiheuttavia testejä ja koe-eläinten käytön vähentämistä. 3) Strategian tulosten tulee täyttää riskin arvioinnin tarpeita ja muita hallinnollisia tarpeita. 4) Strategian tulisi sisältää testejä, jotka perustuvat tunnettuihin ja tärkeisiin vaikutusmekanismeihin. 5) Testausstrategiassa tulee suosia ihmissoluviljelmien käyttöä tai muita ihmisillä tehtäviä mittauksia, sikäli kuin se on eettisesti hyväksyttävää. 6) Testausstrategian tuloksista pitäisi pystyä ennakoimaan haitalliset vaikutukset ja annos-vastesuhteet. Tulevaisuuden näkymät Vaihtoehtoisen menetelmän kehittäminen on pitkä prosessi, johon kuuluvat testin kehittäminen, prevalidointi ja validointi, asiantuntijaryhmien lausuntovaihe sekä testin hyväksyminen ohjeistoihin (kuva 4). Testien validointivaihe on hidas. Validoinnissa arvioidaan testin tarkoituksenmukaisuus, luotettavuus ja toistettavuus. Vaiheiden toteuttamiseen kuluu keskimäärin kymmenen vuotta. On arvioitu, että parhaillaan kehitettäviä tai validoitavana olevia vaihtoehtoisia menetelmiä tulisi ohjeistoihin seuraavassa järjestyksessä: ihoabsorptiotesti, akuutti ihokorroosiotesti ja valotoksisuustesti vuosien aikana, akuutti ihoärsytystesti vuosina , akuutti silmä-ärsytystesti , vaihto- In vitro -menetelmät ja kemikaalien turvallisuuden testaus 857
8 ehtoinen testi korvaamaan akuuttia toksisuustestiä (oraalinen LD 50 ) (Purchase 1997). Nopeus, jolla korvaavia testejä voidaan odottaa ohjeistoihin, on ennen muuta riippuvainen in vitro -toksikologian ja validointitutkimuksen edistymisestä. Vastuu kemikaalien ja lääkkeiden turvallisuudesta on tärkein huomioonotettava eettinen tekijä. Jos vaihtoehtoiset menetelmät yhdessä tavanomaisten eläintestien kanssa käytettyinä takaavat turvallisuuden, ne tulisi hyväksyä osaksi toksikologista turvallisuustutkimusta. Kirjallisuutta Ames B N, Durston W E, Yamasaki E, Lee F D. Carcinogens are mutagens: a simple test system combining liver homogenates for activation of bacteria for detection. Proc Natl Acad Sci USA 1973; 70: APC, Animal Procedures Committee Report to the Home Secretary on Regulatory Toxicity. London, Home Office Publications, Balls M, Blauboer B J, Fentem J H, ym. Practical aspects of the validation of toxicity test procedures. ATLA 1995a; 23: Balls M, Botham P A, Bruner L H, Spielmann H. The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol in Vitro 1995b; 9: Bondesson I, Ekwall B, Hellberg S, ym. MEIC a new international multicenter project to evaluate the relevance to human toxicity of in vitro cytotoxicity tests. Cell Biol Toxicol 1989; 5: Brantom P G, Bruner L H, Chamberlain M, ym. A summary report of the COLIPA international validation study on alternatives to Draize rabbit eye irritation test. Toxicol in Vitro 1997; 11: Bruner L H, Carr G J, Chamberlain M, Curren R D. Validation of alternative methods for toxicity testing. Toxicol in Vitro 1996; 10: Campochiaro P A, Conway B P. Aminoglycoside toxicity A survey of retinal specialists. Implications for ocular use. Arch Ophthalmol 1991; 109: Draize J H, Woodard G K, Calvery H O. Methods for the study of irritation and toxicity of substances applied topically to the skin and mucous membranes. J Pharmacol Exp Ther 1944; 82: Ekwall B, Clemedson C, Crafoord B, ym. Correlation between in vivo and in vitro acute toxicity tests: results of the MEIC project. Kirjassa: Louekari K, Tiberg Ebba, toim. Development of ecotoxicity and toxicity tests. TemaNord, Environment 1997: 524. Copenhagen: Nordic Council of Ministers, EU Commission. The Commissions first report to the Council and the European Parliament on statistics concerning the number of animals used for experiments and other scientific purposes. Com(94) 195. Brussels, 1994 Frankild S. In vitro percutaneous absorption test. Kirjassa: Louekari K, Tiberg Ebba, toim. Development of ecotoxicity and toxicity tests. TemaNord Environment 1997: 524. Copenhagen: Nordic Council of Ministers, Grant W M. Toxicology of the eye. Illinois USA: Charles Thomas, Koëter H. International harmonisation of test methods for hazard characterisation and risk assessment. Kirjassa: Louekari K, Tiberg E, toim. Development of (eco)toxicity tests. TemaNord, Environment 1995: 623. Copenhagen: Nordic Council of Ministers, 1995, s OECD Scientific Criteria for Validation of in Vitro Toxicity Tests. Paris: OECD Environment Monograph, No OECD Guidance Document for the Development of OECD Guidelines for the Testing of Chemicals. Paris: OECD, Environment Monograph, No. 76, OECD The role of OECD Test Guideline Programme in the international harmonisation of Validation Criteria for Alternative Test Methods. Paris: ENV/MC/CHEM/TG(94)6, OECD Draft Group Reports of the OECD Workshop on Harmonization of Validation and Acceptance Criteria for Alternative Toxicological Test Methods in Solna, Sweden, January OECD Test Guideline Programme. Progress report for the period september 1996 march Environment Directorate, Chemicals Group and Management Committee, Paris: ENV/ MC/CHEM/TG(97)2, Ohno Y, Kaneko T, Kobayashi T, ym. First Phase Inter-Laboratory Validation of the In Vitro Eye Irritation Tests for Cosmetic Ingredients: (1) Overview, organization and results of the validation study. Aatex 1995; 3: Purchase I F H. Prospects for reduction and replacement alternatives in regulatory toxicology. Toxicol in Vitro 1997; 11: Rasmussen E S. Prospects for Use of in Vitro Methods for Assessment of Human Safety. National Food Agency of Denmark, February Russel W M S, Burch R L. The Principles of Humane Experimental Technique. London: Methuen, Spielman H, Balls M, Dupuis J, ym. The international EU/ COLIPA in vitro phototoxicity validation study: results of Phase II (blind trial); part 1: the 3T3 NRU test for phototoxic pontential. Toxicol in Vitro, 1998 (painossa). Tähti H, Vaalavirta L, Toimela T. In vitro methods as a tool in neurotoxicity studies. 1995; ATLA 23: Wärngård L, Pelin K. Conclusions of the non-genotoxic and related mechanisms -session. Kirjassa: Louekari K, Tiberg E. Development of (eco)toxicity tests. TemaNord, Environment 1995: 623. Copenhagen: Nordic Council of Ministers, KIMMO LOUEKARI, FT, erikoistutkija Työterveyslaitos, työhygienian ja toksikologian osasto Topeliuksenkatu 41a A, Helsinki Jätetty toimitukselle Hyväksytty julkaistavaksi LOTTA SALMINEN, professori, tulosyksikön johtaja TAYS:n silmätautien klinikka PL 2000, Tampere HANNA TÄHTI, dosentti, tutkimusjohtaja Tampereen yliopisto, lääketieteen laitos PL 607, Tampere 858
In vitro -tietojen käyttö REACHtietovaatimusten
 In vitro -tietojen käyttö REACHtietovaatimusten täyttämiseen Webinaari tietovaatimuksista 30. marraskuuta 2009 Yleiskatsaus REACH ja in vitro -testaus Perusteet in vitro -menetelmien käyttöön REACHmenettelyssä
In vitro -tietojen käyttö REACHtietovaatimusten täyttämiseen Webinaari tietovaatimuksista 30. marraskuuta 2009 Yleiskatsaus REACH ja in vitro -testaus Perusteet in vitro -menetelmien käyttöön REACHmenettelyssä
(ETA:n kannalta merkityksellinen teksti)
 1.6.2016 L 144/27 KOMISSION ASETUS (EU) 2016/863, annettu 31 päivänä toukokuuta 2016, kemikaalien rekisteröinnistä, arvioinnista, lupamenettelyistä ja rajoituksista annetun Euroopan parlamentin ja neuvoston
1.6.2016 L 144/27 KOMISSION ASETUS (EU) 2016/863, annettu 31 päivänä toukokuuta 2016, kemikaalien rekisteröinnistä, arvioinnista, lupamenettelyistä ja rajoituksista annetun Euroopan parlamentin ja neuvoston
KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE
 EUROOPAN KOMISSIO Bryssel 13.9.2011 KOM(2011) 558 lopullinen KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE Kertomus eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista
EUROOPAN KOMISSIO Bryssel 13.9.2011 KOM(2011) 558 lopullinen KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE Kertomus eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista
Kokonaisvaltainen toksisuusarviointi: Elintarvikkeet ja elintarvikekontaktimateriaalit
 BioSafe Simple Solutions for Complex Matters Kokonaisvaltainen toksisuusarviointi: Elintarvikkeet ja elintarvikekontaktimateriaalit Ulla Honkalampi Toimitus- ja laboratorionjohtaja Elintarviketoksisuus:
BioSafe Simple Solutions for Complex Matters Kokonaisvaltainen toksisuusarviointi: Elintarvikkeet ja elintarvikekontaktimateriaalit Ulla Honkalampi Toimitus- ja laboratorionjohtaja Elintarviketoksisuus:
Miten EU säätelee hormonihäiriköitä
 Miten EU säätelee hormonihäiriköitä Eduskunnan ympäristövaliokunnan avoin kokous 15.3.2017 Jukka Malm Varapääjohtaja Euroopan kemikaalivirasto Johdanto Euroopan kemikaalivirasto Perustettu 1.6.2007 580
Miten EU säätelee hormonihäiriköitä Eduskunnan ympäristövaliokunnan avoin kokous 15.3.2017 Jukka Malm Varapääjohtaja Euroopan kemikaalivirasto Johdanto Euroopan kemikaalivirasto Perustettu 1.6.2007 580
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä
 Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
KOMISSION LAUSUMA VAIHTOEHTOISISTA TESTIMENETELMISTÄ
 EUROOPAN UNIONIN NEUVOSTO Bryssel, 11. joulukuuta 2006 (12.12) (OR. fr) Toimielinten välinen asia: 2003/0256 (COD) 16295/06 ADD 1 CODEC 1481 COMPET 380 ENV 679 CHIMIE 40 LISÄYS I/A-KOHTAA KOSKEVAAN ILMOITUKSEEN
EUROOPAN UNIONIN NEUVOSTO Bryssel, 11. joulukuuta 2006 (12.12) (OR. fr) Toimielinten välinen asia: 2003/0256 (COD) 16295/06 ADD 1 CODEC 1481 COMPET 380 ENV 679 CHIMIE 40 LISÄYS I/A-KOHTAA KOSKEVAAN ILMOITUKSEEN
ITÄVALLAN JA TŠEKIN TASAVALLAN YHTEINEN LAUSUMA
 Euroopan unionin neuvosto Bryssel, 2. kesäkuuta 2017 (OR. en) Toimielinten välinen asia: 2017/0010 (NLE) 9425/2/17 REV 2 ADD 1 ENV 523 COMPET 424 ILMOITUS: A-KOHTA Lähettäjä: Vastaanottaja: Asia: Neuvoston
Euroopan unionin neuvosto Bryssel, 2. kesäkuuta 2017 (OR. en) Toimielinten välinen asia: 2017/0010 (NLE) 9425/2/17 REV 2 ADD 1 ENV 523 COMPET 424 ILMOITUS: A-KOHTA Lähettäjä: Vastaanottaja: Asia: Neuvoston
KOE-ELÄINTEN ASIALLA
 KOE-ELÄINTEN ASIALLA Eläinkokeet ovat arkipäivää Maailmassa käytetään vuosittain eläinkokeisiin yli sata miljoonaa eläintä, joista EU:n osuus on runsaat 10 miljoonaa koe-eläintä. Suomessa käytettyjen koe-eläinten
KOE-ELÄINTEN ASIALLA Eläinkokeet ovat arkipäivää Maailmassa käytetään vuosittain eläinkokeisiin yli sata miljoonaa eläintä, joista EU:n osuus on runsaat 10 miljoonaa koe-eläintä. Suomessa käytettyjen koe-eläinten
REACH-asetukseen perustuva eläinkokeita korvaavien menetelmien käyttö
 Viite: ECHA-11-FS-06-FI ISBN-13: 978-92-9217-602-0 REACH-asetukseen perustuva eläinkokeita korvaavien menetelmien käyttö Eräs tärkeimmistä REACH-asetuksen laatimisen ja hyväksymisen syistä oli se, että
Viite: ECHA-11-FS-06-FI ISBN-13: 978-92-9217-602-0 REACH-asetukseen perustuva eläinkokeita korvaavien menetelmien käyttö Eräs tärkeimmistä REACH-asetuksen laatimisen ja hyväksymisen syistä oli se, että
Ehdotus EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI
 EUROOPAN KOMISSIO Bryssel 5.3.2012 COM(2012) 90 final 2012/0040 (COD) Ehdotus EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI neuvoston direktiivin 92/65/ETY muuttamisesta koirien, kissojen ja frettien kauppaan
EUROOPAN KOMISSIO Bryssel 5.3.2012 COM(2012) 90 final 2012/0040 (COD) Ehdotus EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI neuvoston direktiivin 92/65/ETY muuttamisesta koirien, kissojen ja frettien kauppaan
NaturaPura Ibérica Elokuu 10, 2009 Rua das Australias, No. 1 4705-322 Braga Portugali
 NaturaPura Ibérica Elokuu 10, 2009 Rua das Australias, No. 1 4705-322 Braga Portugali VIITATEN: IN VITRO IHOÄRSYTTÄVYYSTESTAUSRAPORTTI Oheisena NaturaPuran toimittaman 100% puuvillakangasmateriaalin in
NaturaPura Ibérica Elokuu 10, 2009 Rua das Australias, No. 1 4705-322 Braga Portugali VIITATEN: IN VITRO IHOÄRSYTTÄVYYSTESTAUSRAPORTTI Oheisena NaturaPuran toimittaman 100% puuvillakangasmateriaalin in
Hyötyosuus. ANNOS ja sen merkitys lääkehoidossa? Farmakokinetiikan perusteita. Solukalvon läpäisy. Alkureitin metabolia
 Neurofarmakologia Farmakologian perusteiden kertausta Pekka Rauhala Syksy 2012 Koulu, Mervaala & Tuomisto, 8. painos, 2012 Kappaleet 11-30 (pois kappale 18) tai vastaavat asiat muista oppikirjoista n.
Neurofarmakologia Farmakologian perusteiden kertausta Pekka Rauhala Syksy 2012 Koulu, Mervaala & Tuomisto, 8. painos, 2012 Kappaleet 11-30 (pois kappale 18) tai vastaavat asiat muista oppikirjoista n.
Mitä on GLP? Pirkko Puranen, ylitarkastaja, FT Fimea, Luvat ja tarkastukset
 Mitä on GLP? Pirkko Puranen, ylitarkastaja, FT Fimea, Luvat ja tarkastukset Miksi GLP (Good Laboratory Practice)? Kemikaalien ja lääkkeiden turvallisuuden testaamiseksi myyntilupaa tai rekisteröintiä varten
Mitä on GLP? Pirkko Puranen, ylitarkastaja, FT Fimea, Luvat ja tarkastukset Miksi GLP (Good Laboratory Practice)? Kemikaalien ja lääkkeiden turvallisuuden testaamiseksi myyntilupaa tai rekisteröintiä varten
Eläinkokeet kemiallisten aineiden turvallisen käytön varmistamisessa
 REACH Factsheet ECHA-12-FS-08-EN Eläinkokeet kemiallisten aineiden turvallisen käytön varmistamisessa REACH-asetuksen tavoitteena on varmistaa ihmisten terveyden ja ympäristön korkeatasoinen suojelu kemikaalien
REACH Factsheet ECHA-12-FS-08-EN Eläinkokeet kemiallisten aineiden turvallisen käytön varmistamisessa REACH-asetuksen tavoitteena on varmistaa ihmisten terveyden ja ympäristön korkeatasoinen suojelu kemikaalien
Kemikaalien EU-riskinarviointi ja vähennys
 Kemikaalien EU-riskinarviointi ja vähennys 4 -tert-butyyli-2,6 -dimetyyli-3,5 -dinitroasetofenoni Päivitetty 16.9.2009 CAS nro 81-14-1 Synonyymejä Myskiketoni Musk ketone 3,5-dinitro-2,6-dimetyyli-4-tert-butyyliasetofenoni
Kemikaalien EU-riskinarviointi ja vähennys 4 -tert-butyyli-2,6 -dimetyyli-3,5 -dinitroasetofenoni Päivitetty 16.9.2009 CAS nro 81-14-1 Synonyymejä Myskiketoni Musk ketone 3,5-dinitro-2,6-dimetyyli-4-tert-butyyliasetofenoni
Valtuuskunnille toimitetaan oheisena asiakirja D048947/06 LIITE 1.
 Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11470/17 ADD 1 AGRILEG 145 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Neuvoston pääsihteeristö Kom:n
Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11470/17 ADD 1 AGRILEG 145 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Neuvoston pääsihteeristö Kom:n
Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en)
 Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en) 11882/17 ADD 1 SAATE Lähettäjä: Saapunut: 4. syyskuuta 2017 Vastaanottaja: ENV 727 MI 607 AGRI 443 CHIMIE 78 SAN 319 CONSOM 293 DELACT 149
Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en) 11882/17 ADD 1 SAATE Lähettäjä: Saapunut: 4. syyskuuta 2017 Vastaanottaja: ENV 727 MI 607 AGRI 443 CHIMIE 78 SAN 319 CONSOM 293 DELACT 149
Valtuuskunnille toimitetaan oheisena asiakirja D048947/06.
 Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11470/17 AGRILEG 145 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Kom:n asiak. nro: D048947/06 Asia: Neuvoston
Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11470/17 AGRILEG 145 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Kom:n asiak. nro: D048947/06 Asia: Neuvoston
Ihmissolupohjaisten eläinkokeettomien testimenetelmien kehittäminen ja niistä tiedottaminen
 1 KOLMIVUOTINEN OHJELMA FICAMILLE VUOSILLE 2014 2016: EU-DIREKTIIVIIN TIETEELLISIIN TARKOITUKSIIN KÄYTETTÄVIEN ELÄINTEN SUOJELUSTA (2010/63/EU) LIITTYVÄ MAA-JA METSÄTALOUSMINISTERIÖN OHJELMA Ihmissolupohjaisten
1 KOLMIVUOTINEN OHJELMA FICAMILLE VUOSILLE 2014 2016: EU-DIREKTIIVIIN TIETEELLISIIN TARKOITUKSIIN KÄYTETTÄVIEN ELÄINTEN SUOJELUSTA (2010/63/EU) LIITTYVÄ MAA-JA METSÄTALOUSMINISTERIÖN OHJELMA Ihmissolupohjaisten
GLP myyntilupa-arvioijan näkökulmasta
 GLP myyntilupa-arvioijan näkökulmasta Fimean GLP-keskustelupäivä 2.9. 2015 Kuopio Pauliina Lehtolainen-Dalkilic FIMEA GLPn periaatteiden tarkoitus on edistää korkealaatuisia testaustuloksia Periaatteita,
GLP myyntilupa-arvioijan näkökulmasta Fimean GLP-keskustelupäivä 2.9. 2015 Kuopio Pauliina Lehtolainen-Dalkilic FIMEA GLPn periaatteiden tarkoitus on edistää korkealaatuisia testaustuloksia Periaatteita,
Toksikologian perusteita ja toksisuuden arviointi
 Toksikologia Toksikologian perusteita ja toksisuuden arviointi Pekka Rauhala 2012 Oppi vieraiden aineiden haitallisista vaikutuksista eläviin organismeihin Paracelsus (1493-1541): Ei ole myrkytöntä ainetta,
Toksikologia Toksikologian perusteita ja toksisuuden arviointi Pekka Rauhala 2012 Oppi vieraiden aineiden haitallisista vaikutuksista eläviin organismeihin Paracelsus (1493-1541): Ei ole myrkytöntä ainetta,
EU:n lääketutkimusasetus ja eettiset toimikunnat Suomessa Mika Scheinin
 EU:n lääketutkimusasetus ja eettiset toimikunnat Suomessa 20.5.2016 Mika Scheinin Asetus vs. direktiivi EU-asetus no. 536/2014 korvaa aiemman direktiivin Directive 2001/20/EC on the approximation of the
EU:n lääketutkimusasetus ja eettiset toimikunnat Suomessa 20.5.2016 Mika Scheinin Asetus vs. direktiivi EU-asetus no. 536/2014 korvaa aiemman direktiivin Directive 2001/20/EC on the approximation of the
Ajankohtaiset lainsäädäntöasiat maa- ja metsätalousministeriöstä
 Ajankohtaiset lainsäädäntöasiat maa- ja metsätalousministeriöstä Ajankohtaista laboratoriorintamalla Nina Kaario, eläinlääkintöylitarkastaja Maa- ja metsätalousministeriö Ajankohtaista lainsäädännöstä
Ajankohtaiset lainsäädäntöasiat maa- ja metsätalousministeriöstä Ajankohtaista laboratoriorintamalla Nina Kaario, eläinlääkintöylitarkastaja Maa- ja metsätalousministeriö Ajankohtaista lainsäädännöstä
Hormonihäiriköiden yhteisvaikutusten tutkimus ja hormonihäiriköiden määrittelyn vaikeus sääntelyssä
 Hormonihäiriköiden yhteisvaikutusten tutkimus ja hormonihäiriköiden määrittelyn vaikeus sääntelyssä MITEN HORMONIHÄIRIKÖT KURIIN? Eduskunnan ympäristövaliokunnan avoin kokous 15.3.2017 Hannu Kiviranta
Hormonihäiriköiden yhteisvaikutusten tutkimus ja hormonihäiriköiden määrittelyn vaikeus sääntelyssä MITEN HORMONIHÄIRIKÖT KURIIN? Eduskunnan ympäristövaliokunnan avoin kokous 15.3.2017 Hannu Kiviranta
Valtuuskunnille toimitetaan oheisena asiakirja D043528/02.
 Euroopan unionin neuvosto Bryssel, 8. maaliskuuta 2016 (OR. en) 6937/16 TRANS 72 SAATE Lähettäjä: Euroopan komissio Saapunut: 7. maaliskuuta 2016 Vastaanottaja: Kom:n asiak. nro: D043528/02 Asia: Neuvoston
Euroopan unionin neuvosto Bryssel, 8. maaliskuuta 2016 (OR. en) 6937/16 TRANS 72 SAATE Lähettäjä: Euroopan komissio Saapunut: 7. maaliskuuta 2016 Vastaanottaja: Kom:n asiak. nro: D043528/02 Asia: Neuvoston
(ETA:n kannalta merkityksellinen teksti)
 L 53/166 FI KOMISSION TÄYTÄNTÖÖNPANOASETUS (EU) 2018/250, annettu 15 päivänä helmikuuta 2018, metyyli-2-furoaatin, bis-(2-metyyli-3-furyyli)disulfidin, furfuraalin, furfuryylialkoholin, 2-furaanimetaanitiolin,
L 53/166 FI KOMISSION TÄYTÄNTÖÖNPANOASETUS (EU) 2018/250, annettu 15 päivänä helmikuuta 2018, metyyli-2-furoaatin, bis-(2-metyyli-3-furyyli)disulfidin, furfuraalin, furfuryylialkoholin, 2-furaanimetaanitiolin,
ASIANTUNTIJALAUSUNTO 1638/210/2007 17.4.2007. Elintarviketurvallisuusvirasto Evira
 Elintarviketurvallisuusvirasto Evira Elintarvikkeiden ja eläinlääkinnän valvontaosasto Tuoteturvallisuuden ja tuotemarkkinoinnin yksikkö ALTISTUMINEN KUMARIINILLE Kysely elintarviketeollisuudelle Kartottaakseen
Elintarviketurvallisuusvirasto Evira Elintarvikkeiden ja eläinlääkinnän valvontaosasto Tuoteturvallisuuden ja tuotemarkkinoinnin yksikkö ALTISTUMINEN KUMARIINILLE Kysely elintarviketeollisuudelle Kartottaakseen
REACH ja ECHA - tilannekatsaus
 REACH ja ECHA - tilannekatsaus Tukes-talvitapaaminen 2013 Jukka Malm Johtaja Euroopan kemikaalivirasto (ECHA) 13. helmikuuta 2013 1 Esityksen pääkohdat 1. REACH mitä saavutettu 5 vuodessa 2. Mitä ECHA:lla
REACH ja ECHA - tilannekatsaus Tukes-talvitapaaminen 2013 Jukka Malm Johtaja Euroopan kemikaalivirasto (ECHA) 13. helmikuuta 2013 1 Esityksen pääkohdat 1. REACH mitä saavutettu 5 vuodessa 2. Mitä ECHA:lla
Euroopan unionin neuvosto Bryssel, 13. heinäkuuta 2015 (OR. en)
 Euroopan unionin neuvosto Bryssel, 13. heinäkuuta 2015 (OR. en) 10869/15 SAATE Lähettäjä: Euroopan komissio Saapunut: 10. heinäkuuta 2015 Vastaanottaja: Kom:n asiak. nro: D039794/02 Asia: Neuvoston pääsihteeristö
Euroopan unionin neuvosto Bryssel, 13. heinäkuuta 2015 (OR. en) 10869/15 SAATE Lähettäjä: Euroopan komissio Saapunut: 10. heinäkuuta 2015 Vastaanottaja: Kom:n asiak. nro: D039794/02 Asia: Neuvoston pääsihteeristö
Rakennustuotteiden vaarallisten aineiden arviointi CEN/TC 351. Uudet yhteiset standardit ympäristöanalytiikkaan SFS 13.5.2014 Pekka Vuorinen
 Rakennustuotteiden vaarallisten aineiden arviointi CEN/TC 351 Uudet yhteiset standardit ympäristöanalytiikkaan SFS 13.5.2014 Pekka Vuorinen CEN/TC 351 Construction products - Assessment of release of dangerous
Rakennustuotteiden vaarallisten aineiden arviointi CEN/TC 351 Uudet yhteiset standardit ympäristöanalytiikkaan SFS 13.5.2014 Pekka Vuorinen CEN/TC 351 Construction products - Assessment of release of dangerous
2006R1907 FI 01.01.2015 020.001 194
 2006R1907 FI 01.01.2015 020.001 194 LIITE X VAKIOTIETOVAATIMUKSET AINEISTA, JOITA VALMISTETAAN TAI TUODAAN MAAHAN VÄHINTÄÄN 1 000 TONNIN MÄÄRINÄ ( 1 ) Rekisteröijän on ehdotettava, miten ja millaisella
2006R1907 FI 01.01.2015 020.001 194 LIITE X VAKIOTIETOVAATIMUKSET AINEISTA, JOITA VALMISTETAAN TAI TUODAAN MAAHAN VÄHINTÄÄN 1 000 TONNIN MÄÄRINÄ ( 1 ) Rekisteröijän on ehdotettava, miten ja millaisella
(Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET
 17.11.2017 L 301/1 II (Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET KOMISSION DELEGOITU ASETUS (EU) 2017/2100, annettu 4 päivänä syyskuuta 2017, hormonitoimintaa häiritsevien
17.11.2017 L 301/1 II (Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET KOMISSION DELEGOITU ASETUS (EU) 2017/2100, annettu 4 päivänä syyskuuta 2017, hormonitoimintaa häiritsevien
FI Moninaisuudessaan yhtenäinen FI A8-0305/4. Tarkistus. Mireille D'Ornano ENF-ryhmän puolesta
 21.10.2015 A8-0305/4 4 Johdanto-osan 7 kappale 7) Syyt, joiden perusteella direktiivillä (EU) 2015/412 muutettiin direktiiviä 2001/18/EY viljelyyn tarkoitettujen muuntogeenisten organismien osalta, pätevät
21.10.2015 A8-0305/4 4 Johdanto-osan 7 kappale 7) Syyt, joiden perusteella direktiivillä (EU) 2015/412 muutettiin direktiiviä 2001/18/EY viljelyyn tarkoitettujen muuntogeenisten organismien osalta, pätevät
KOMISSION DELEGOITU ASETUS (EU) /, annettu ,
 EUROOPAN KOMISSIO Bryssel 4.9.2017 C(2017) 5467 final KOMISSION DELEGOITU ASETUS (EU) /, annettu 4.9.2017, hormonitoimintaa häiritsevien ominaisuuksien määrittämistä koskevien tieteellisten kriteerien
EUROOPAN KOMISSIO Bryssel 4.9.2017 C(2017) 5467 final KOMISSION DELEGOITU ASETUS (EU) /, annettu 4.9.2017, hormonitoimintaa häiritsevien ominaisuuksien määrittämistä koskevien tieteellisten kriteerien
Opiskelijoiden nimet, s-postit ja palautus pvm. Kemikaalin tai aineen nimi. CAS N:o. Kemikaalin ja aineen olomuoto Valitse: Kiinteä / nestemäinen
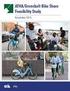 Harjoitus 2: Vastauspohja. Valitun kemikaalin tiedonhaut ja alustava riskinarviointi. Ohje 09.03.2016. Laat. Petri Peltonen. Harjoitus tehdään k2016 kurssilla parityönä. Opiskelijoiden nimet, s-postit
Harjoitus 2: Vastauspohja. Valitun kemikaalin tiedonhaut ja alustava riskinarviointi. Ohje 09.03.2016. Laat. Petri Peltonen. Harjoitus tehdään k2016 kurssilla parityönä. Opiskelijoiden nimet, s-postit
Euroopan unionin neuvosto Bryssel, 17. lokakuuta 2016 (OR. en)
 Euroopan unionin neuvosto Bryssel, 17. lokakuuta 2016 (OR. en) 13322/16 AGRILEG 151 VETER 98 SAATE Lähettäjä: Euroopan komissio Saapunut: 13. lokakuuta 2016 Vastaanottaja: Kom:n asiak. nro: D047122/02
Euroopan unionin neuvosto Bryssel, 17. lokakuuta 2016 (OR. en) 13322/16 AGRILEG 151 VETER 98 SAATE Lähettäjä: Euroopan komissio Saapunut: 13. lokakuuta 2016 Vastaanottaja: Kom:n asiak. nro: D047122/02
Biopankkeja koskeva lainsäädäntö
 1 Biopankkeja koskeva lainsäädäntö Biomedicum 20.9.2004 Mervi Kattelus mervi.kattelus@stm.fi 2 Mikä on biopankki? Ei ole määritelty Suomen lainsäädännössä Suppea määritelmä: kudosnäytekokoelma Laaja määritelmä:
1 Biopankkeja koskeva lainsäädäntö Biomedicum 20.9.2004 Mervi Kattelus mervi.kattelus@stm.fi 2 Mikä on biopankki? Ei ole määritelty Suomen lainsäädännössä Suppea määritelmä: kudosnäytekokoelma Laaja määritelmä:
TYÖTURVALLISUUSSÄÄNNÖKSIÄ VALMISTELEVA NEUVOTTELUKUNTA Luonnos 2/HTP2012
 TYÖTURVALLISUUSSÄÄNNÖKSIÄ VALMISTELEVA NEUVOTTELUKUNTA Luonnos 2/HTP2012 5.5.2011 1 (6) Propyleeni HTP-ARVON PERUSTELUMUISTIO Yksilöinti ja ominaisuudet CAS No: 115-07-1 EINECS No: 204-062-1 EEC No: 601-011-00-9
TYÖTURVALLISUUSSÄÄNNÖKSIÄ VALMISTELEVA NEUVOTTELUKUNTA Luonnos 2/HTP2012 5.5.2011 1 (6) Propyleeni HTP-ARVON PERUSTELUMUISTIO Yksilöinti ja ominaisuudet CAS No: 115-07-1 EINECS No: 204-062-1 EEC No: 601-011-00-9
Euroopan unionin neuvosto Bryssel, 25. marraskuuta 2016 (OR. en)
 Euroopan unionin neuvosto Bryssel, 25. marraskuuta 2016 (OR. en) 14899/16 SAATE Lähettäjä: Euroopan komissio Saapunut: 24. marraskuuta 2016 Vastaanottaja: Kom:n asiak. nro: D047976/02 Asia: Neuvoston pääsihteeristö
Euroopan unionin neuvosto Bryssel, 25. marraskuuta 2016 (OR. en) 14899/16 SAATE Lähettäjä: Euroopan komissio Saapunut: 24. marraskuuta 2016 Vastaanottaja: Kom:n asiak. nro: D047976/02 Asia: Neuvoston pääsihteeristö
KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE
 EUROOPAN KOMISSIO Bryssel 19.9.2016 COM(2016) 599 final KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista ja oikeudellisesta
EUROOPAN KOMISSIO Bryssel 19.9.2016 COM(2016) 599 final KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista ja oikeudellisesta
Euroopan unionin neuvosto Bryssel, 24. huhtikuuta 2017 (OR. en)
 Euroopan unionin neuvosto Bryssel, 24. huhtikuuta 2017 (OR. en) 8318/17 AGRILEG 82 SAATE Lähettäjä: Euroopan komissio Saapunut: 19. huhtikuuta 2017 Vastaanottaja: Kom:n asiak. nro: D046260/03 Asia: Neuvoston
Euroopan unionin neuvosto Bryssel, 24. huhtikuuta 2017 (OR. en) 8318/17 AGRILEG 82 SAATE Lähettäjä: Euroopan komissio Saapunut: 19. huhtikuuta 2017 Vastaanottaja: Kom:n asiak. nro: D046260/03 Asia: Neuvoston
Samankaltaisuuksien vertailu ja luokat REACH-lainsäädännössä. Webinaari tietovaatimuksista
 Samankaltaisuuksien vertailu ja luokat REACH-lainsäädännössä Webinaari tietovaatimuksista 10.12.2009 Puitteet Luokkien rajauksen ja samankaltaisuuksien vertailun perusperiaatteet Vaiheittainen lähestymistapa
Samankaltaisuuksien vertailu ja luokat REACH-lainsäädännössä Webinaari tietovaatimuksista 10.12.2009 Puitteet Luokkien rajauksen ja samankaltaisuuksien vertailun perusperiaatteet Vaiheittainen lähestymistapa
Nanoteknologian mahdollisuudet lääkesovelluksissa
 Nanoteknologian mahdollisuudet lääkesovelluksissa Marjo Yliperttula 1,3 ja Arto Urtti 1,2 1 Farmaseuttisten biotieteiden osasto, Lääketutkimuksen keskus, Farmasian tiedekunta, Helsingin Yliopisto, Helsinki;
Nanoteknologian mahdollisuudet lääkesovelluksissa Marjo Yliperttula 1,3 ja Arto Urtti 1,2 1 Farmaseuttisten biotieteiden osasto, Lääketutkimuksen keskus, Farmasian tiedekunta, Helsingin Yliopisto, Helsinki;
Lääkkeiden hoidollisen ja taloudellisen arvon arviointi. Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi
 Lääkkeiden hoidollisen ja taloudellisen arvon arviointi Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi Arviointien tavoite Tuottaa tietoa lääkkeiden käyttöönottoon ja korvattavuuteen
Lääkkeiden hoidollisen ja taloudellisen arvon arviointi Terveysfoorumi 2011 Piia Peura Lääketaloustieteilijä Piia.Peura@fimea.fi Arviointien tavoite Tuottaa tietoa lääkkeiden käyttöönottoon ja korvattavuuteen
Mitä hyötyä kliinisestä tutkimuksesta on yritykselle - Case Medix Biochemica
 Mitä hyötyä kliinisestä tutkimuksesta on yritykselle - Case Medix Biochemica FiHTA SEMINAARI: Kliininen arviointi ja kliininen tieto - mikä riittää? 6.6.2012, Sinikka Tiisala Liiketoiminnan kehitysjohtaja
Mitä hyötyä kliinisestä tutkimuksesta on yritykselle - Case Medix Biochemica FiHTA SEMINAARI: Kliininen arviointi ja kliininen tieto - mikä riittää? 6.6.2012, Sinikka Tiisala Liiketoiminnan kehitysjohtaja
KOMISSION DELEGOITU DIREKTIIVI / /EU, annettu 18.10.2013,
 EUROOPAN KOMISSIO Bryssel 18.10.2013 C(2013) 6835 final KOMISSION DELEGOITU DIREKTIIVI / /EU, annettu 18.10.2013, Euroopan parlamentin ja neuvoston direktiivin 2011/65/EU liitteen IV muuttamisesta sen
EUROOPAN KOMISSIO Bryssel 18.10.2013 C(2013) 6835 final KOMISSION DELEGOITU DIREKTIIVI / /EU, annettu 18.10.2013, Euroopan parlamentin ja neuvoston direktiivin 2011/65/EU liitteen IV muuttamisesta sen
Mittaamisen maailmasta muutamia asioita. Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori
 Mittaamisen maailmasta muutamia asioita Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori SISÄLTÖ 1. Mittari vs. indikaattori vs. menetelmä - mittaaminen 2. Luotettavat mittarit 3. Arvioinnin
Mittaamisen maailmasta muutamia asioita Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori SISÄLTÖ 1. Mittari vs. indikaattori vs. menetelmä - mittaaminen 2. Luotettavat mittarit 3. Arvioinnin
Lääkealan turvallisuus- ja kehittämiskeskuksen määräys
 Määräys pp.kk.vvvv Dnro 002646/00.01.00/2014 /2014 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys PITKÄLLE KEHITETYSSÄ TERAPIASSA KÄY- TETTÄVIEN LÄÄKKEIDEN (ATMP) VALMISTA- MINEN YKSITTÄISEN POTILAAN
Määräys pp.kk.vvvv Dnro 002646/00.01.00/2014 /2014 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys PITKÄLLE KEHITETYSSÄ TERAPIASSA KÄY- TETTÄVIEN LÄÄKKEIDEN (ATMP) VALMISTA- MINEN YKSITTÄISEN POTILAAN
REACH = Registaration Evaluation and Authorisation of Chemicals. ja VTT:n palvelut
 REACH = Registaration Evaluation and Authorisation of Chemicals ja VTT:n palvelut REACH:in kattavuus REACH Kemikaalit ennen v. 1981 = n. 100106 tuotetta joita REACH koskee, jos niitä tuotetaan tai tuodaan
REACH = Registaration Evaluation and Authorisation of Chemicals ja VTT:n palvelut REACH:in kattavuus REACH Kemikaalit ennen v. 1981 = n. 100106 tuotetta joita REACH koskee, jos niitä tuotetaan tai tuodaan
Avainsanat: BI5 III Biotekniikan sovelluksia 9. Perimä ja terveys.
 Avainsanat: mutaatio Monitekijäinen sairaus Kromosomisairaus Sukupuu Suomalainen tautiperintö Geeniterapia Suora geeninsiirto Epäsuora geeninsiirto Kantasolut Totipotentti Pluripotentti Multipotentti Kudospankki
Avainsanat: mutaatio Monitekijäinen sairaus Kromosomisairaus Sukupuu Suomalainen tautiperintö Geeniterapia Suora geeninsiirto Epäsuora geeninsiirto Kantasolut Totipotentti Pluripotentti Multipotentti Kudospankki
Vaikutusperustaiset menetelmät haitallisten aineiden seurannassa. Matti Leppänen Suomen ympäristökeskus Haitallisten aineiden päivä, YM, 12.3.
 Vaikutusperustaiset menetelmät haitallisten aineiden seurannassa Matti Leppänen Suomen ympäristökeskus Haitallisten aineiden päivä, YM, 12.3.2019 Vaikutusperustaiset menetelmät Effect-based methods (EBMs)
Vaikutusperustaiset menetelmät haitallisten aineiden seurannassa Matti Leppänen Suomen ympäristökeskus Haitallisten aineiden päivä, YM, 12.3.2019 Vaikutusperustaiset menetelmät Effect-based methods (EBMs)
Turvallisuus prosessien suunnittelussa ja käyttöönotossa
 Turvallisuus prosessien suunnittelussa ja käyttöönotossa Moduuli 1 Turvallisuus prosessin valinnassa ja skaalauksessa 1. Luennon aiheesta yleistä 2. Käsiteltävät kemikaalit 3. Tuotantomäärät 4. Olemassa
Turvallisuus prosessien suunnittelussa ja käyttöönotossa Moduuli 1 Turvallisuus prosessin valinnassa ja skaalauksessa 1. Luennon aiheesta yleistä 2. Käsiteltävät kemikaalit 3. Tuotantomäärät 4. Olemassa
Ehdotus NEUVOSTON DIREKTIIVI
 EUROOPAN KOMISSIO Bryssel 5.2.2013 COM(2013) 46 final 2013/0026 (NLE) Ehdotus NEUVOSTON DIREKTIIVI Euroopan parlamentin ja neuvoston direktiivin 98/8/EY muuttamisesta jauhetun maissintähkän lisäämiseksi
EUROOPAN KOMISSIO Bryssel 5.2.2013 COM(2013) 46 final 2013/0026 (NLE) Ehdotus NEUVOSTON DIREKTIIVI Euroopan parlamentin ja neuvoston direktiivin 98/8/EY muuttamisesta jauhetun maissintähkän lisäämiseksi
EUROOPAN YHTEISÖJEN KOMISSIO. Ehdotus: EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI
 EUROOPAN YHTEISÖJEN KOMISSIO Bryssel 05.08.2002 KOM(2002) 451 lopullinen 2002/0201 (COD) Ehdotus: EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI direktiivin 95/2/EY muuttamisesta elintarvikelisäaineen E
EUROOPAN YHTEISÖJEN KOMISSIO Bryssel 05.08.2002 KOM(2002) 451 lopullinen 2002/0201 (COD) Ehdotus: EUROOPAN PARLAMENTIN JA NEUVOSTON DIREKTIIVI direktiivin 95/2/EY muuttamisesta elintarvikelisäaineen E
Ehdotus NEUVOSTON DIREKTIIVI
 EUROOPAN KOMISSIO Bryssel 23.6.2011 KOM(2011) 377 lopullinen 2011/0164 (NLE) Ehdotus NEUVOSTON DIREKTIIVI kosmeettisia valmisteita koskevan direktiivin 76/768/ETY muuttamisesta sen liitteen III mukauttamiseksi
EUROOPAN KOMISSIO Bryssel 23.6.2011 KOM(2011) 377 lopullinen 2011/0164 (NLE) Ehdotus NEUVOSTON DIREKTIIVI kosmeettisia valmisteita koskevan direktiivin 76/768/ETY muuttamisesta sen liitteen III mukauttamiseksi
REACH-asetus Kemikaalien arviointi ja GLP-vaatimukset
 REACH-asetus Kemikaalien arviointi ja GLP-vaatimukset GLP-seminaari, FIMEA 10.2.2010 Kirsi Sihvonen Euroopan kemikaalivirasto - ECHA Sisältö REACH-asetus Prosessit Rekisteröinnin aikataulu Rekisteröintiasiakirja
REACH-asetus Kemikaalien arviointi ja GLP-vaatimukset GLP-seminaari, FIMEA 10.2.2010 Kirsi Sihvonen Euroopan kemikaalivirasto - ECHA Sisältö REACH-asetus Prosessit Rekisteröinnin aikataulu Rekisteröintiasiakirja
TOKSISUUSTESTI SISÄILMALLE?
 TOKSISUUSTESTI SISÄILMALLE? TOXTEST-TUTKIMUKSEN TULOKSIA Kati Huttunen Toksisuustestin tarve Kosteusvauriokohteita on enemmän kuin varoja niiden korjaamiseen Korjauskohteiden priorisointi pitäisi tehdä
TOKSISUUSTESTI SISÄILMALLE? TOXTEST-TUTKIMUKSEN TULOKSIA Kati Huttunen Toksisuustestin tarve Kosteusvauriokohteita on enemmän kuin varoja niiden korjaamiseen Korjauskohteiden priorisointi pitäisi tehdä
Kliinisten laboratoriomittausten jäljitettävyys ja IVD-direktiivi
 Kliinisten laboratoriomittausten jäljitettävyys ja IVD-direktiivi Dos Jaakko-Juhani Himberg HUSLAB /laatupäällikkö JJH November 2004 1 IVD-direktiivi ja siirtymäaika In vitro -diagnostiikkaan tarkoitettuja
Kliinisten laboratoriomittausten jäljitettävyys ja IVD-direktiivi Dos Jaakko-Juhani Himberg HUSLAB /laatupäällikkö JJH November 2004 1 IVD-direktiivi ja siirtymäaika In vitro -diagnostiikkaan tarkoitettuja
NÄYTTEENLUOVUTTAJIEN TIEDOTTAMINEN JA KÄYTTÖTARKOITUKSEN MUUTOKSET 20.9.2004 ARPO AROMAA
 NÄYTTEENLUOVUTTAJIEN TIEDOTTAMINEN JA KÄYTTÖTARKOITUKSEN MUUTOKSET TILANTEEN KUVAUS Vuosi 0 Tutkimus tavoitteineen Suostumus Näytteet Muut tiedot Vuosi 10-30 Tutkimus: uusi vai entinen käyttötarkoitus
NÄYTTEENLUOVUTTAJIEN TIEDOTTAMINEN JA KÄYTTÖTARKOITUKSEN MUUTOKSET TILANTEEN KUVAUS Vuosi 0 Tutkimus tavoitteineen Suostumus Näytteet Muut tiedot Vuosi 10-30 Tutkimus: uusi vai entinen käyttötarkoitus
Miten raportoin in vitro -tiedot Käytännön opas 1. Versio 1.1 syyskuu 2012
 Miten raportoin in vitro -tiedot Käytännön opas 1 Versio 1.1 syyskuu 2012 2 Käytännön opas 1 Versio 1.1 syyskuu 2012 OIKEUDELLINEN HUOMAUTUS Tässä asiakirjassa selostetaan REACH-lainsäädännön mukaiset
Miten raportoin in vitro -tiedot Käytännön opas 1 Versio 1.1 syyskuu 2012 2 Käytännön opas 1 Versio 1.1 syyskuu 2012 OIKEUDELLINEN HUOMAUTUS Tässä asiakirjassa selostetaan REACH-lainsäädännön mukaiset
Kemiallisten menetelmien validointi ja mittausepävarmuus Leena Saari Kemian ja toksikologian tutkimusyksikkö
 Kemiallisten menetelmien validointi ja mittausepävarmuus Leena Saari Kemian ja toksikologian tutkimusyksikkö Validointi Validoinnilla varmistetaan että menetelmä sopii käyttötarkoitukseen ja täyttää sille
Kemiallisten menetelmien validointi ja mittausepävarmuus Leena Saari Kemian ja toksikologian tutkimusyksikkö Validointi Validoinnilla varmistetaan että menetelmä sopii käyttötarkoitukseen ja täyttää sille
Helvi Käsnänen SILMÄHOITAJAPÄIVÄT
 Helvi Käsnänen SILMÄHOITAJAPÄIVÄT 19-20.09.2008 Sisätauti-kirurginen sairaanhoitaja 24 vuotta silmätautien klinikassa: osasto, pkl, ls Tutkimushoitajana 03/03 alkaen Selvittää erilaisten solutason tapahtumien,kuten
Helvi Käsnänen SILMÄHOITAJAPÄIVÄT 19-20.09.2008 Sisätauti-kirurginen sairaanhoitaja 24 vuotta silmätautien klinikassa: osasto, pkl, ls Tutkimushoitajana 03/03 alkaen Selvittää erilaisten solutason tapahtumien,kuten
EUROOPAN UNIONIN NEUVOSTO. Bryssel, 30. heinäkuuta 2012 (30.07) (OR. en) 12991/12 ENV 654 ENT 191 SAATE
 EUROOPAN UNIONIN NEUVOSTO Bryssel, 30. heinäkuuta 2012 (30.07) (OR. en) 12991/12 ENV 654 ENT 191 SAATE Lähettäjä: Euroopan komissio Saapunut: 25. heinäkuuta 2012 Vastaanottaja: Euroopan unionin neuvoston
EUROOPAN UNIONIN NEUVOSTO Bryssel, 30. heinäkuuta 2012 (30.07) (OR. en) 12991/12 ENV 654 ENT 191 SAATE Lähettäjä: Euroopan komissio Saapunut: 25. heinäkuuta 2012 Vastaanottaja: Euroopan unionin neuvoston
KOMISSION YKSIKÖIDEN VALMISTELUASIAKIRJA
 EUROOPAN KOMISSIO Bryssel 11.3.2013 SWD(2013) 67 final KOMISSION YKSIKÖIDEN VALMISTELUASIAKIRJA TIIVISTELMÄ KOSMEETTISISTA VALMISTEISTA ANNETTUUN ASETUKSEEN (EY) N:O 1223/2009 SISÄLTYVIEN ELÄINKOKEITA
EUROOPAN KOMISSIO Bryssel 11.3.2013 SWD(2013) 67 final KOMISSION YKSIKÖIDEN VALMISTELUASIAKIRJA TIIVISTELMÄ KOSMEETTISISTA VALMISTEISTA ANNETTUUN ASETUKSEEN (EY) N:O 1223/2009 SISÄLTYVIEN ELÄINKOKEITA
Tämä esitys käsittelee siivouksen arviointia peruskouluissa Yhdysvalloissa tehdyn tutkimuksen valossa
 Tämä esitys käsittelee siivouksen arviointia peruskouluissa Yhdysvalloissa tehdyn tutkimuksen valossa 1 Sisältö - Sisäympäristön laatu kouluissa - Tutkimuksen taustaa - Siivouksen arviointiin liittyvien
Tämä esitys käsittelee siivouksen arviointia peruskouluissa Yhdysvalloissa tehdyn tutkimuksen valossa 1 Sisältö - Sisäympäristön laatu kouluissa - Tutkimuksen taustaa - Siivouksen arviointiin liittyvien
Turvallisuus prosessien suunnittelussa ja käyttöönotossa. Moduuli 1 Turvallisuus prosessin valinnassa ja skaalauksessa
 Turvallisuus prosessien suunnittelussa ja käyttöönotossa Moduuli 1 Turvallisuus prosessin valinnassa ja skaalauksessa Moduuli 1: Turvallisuus prosessin valinnassa ja skaalauksessa Turvallisuus mahdollisten
Turvallisuus prosessien suunnittelussa ja käyttöönotossa Moduuli 1 Turvallisuus prosessin valinnassa ja skaalauksessa Moduuli 1: Turvallisuus prosessin valinnassa ja skaalauksessa Turvallisuus mahdollisten
Kaivannaisjätedirektiivi ja pysyvän jätteen määritelmä. Margareta Wahlström, Tommi Kaartinen & Jutta Laine-Ylijoki VTT
 Kaivannaisjätedirektiivi ja pysyvän jätteen määritelmä Margareta Wahlström, Tommi Kaartinen & Jutta Laine-Ylijoki VTT Sisällys Tausta Komission päätös pysyvän jätteen määritelmästä Kansallisia täsmennyksiä
Kaivannaisjätedirektiivi ja pysyvän jätteen määritelmä Margareta Wahlström, Tommi Kaartinen & Jutta Laine-Ylijoki VTT Sisällys Tausta Komission päätös pysyvän jätteen määritelmästä Kansallisia täsmennyksiä
KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE
 EUROOPAN KOMISSIO Bryssel 10.7.2018 COM(2018) 531 final KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista ja oikeudellisesta
EUROOPAN KOMISSIO Bryssel 10.7.2018 COM(2018) 531 final KOMISSION KERTOMUS EUROOPAN PARLAMENTILLE JA NEUVOSTOLLE eläinkokeille vaihtoehtoisten koemenetelmien kehittämisestä, validoinnista ja oikeudellisesta
Kahden laboratorion mittaustulosten vertailu
 TUTKIMUSSELOSTUS NRO RTE9 (8) LIITE Kahden laboratorion mittaustulosten vertailu Sisältö Sisältö... Johdanto... Tulokset.... Lämpökynttilät..... Tuote A..... Tuote B..... Päätelmiä.... Ulkotulet.... Hautalyhdyt,
TUTKIMUSSELOSTUS NRO RTE9 (8) LIITE Kahden laboratorion mittaustulosten vertailu Sisältö Sisältö... Johdanto... Tulokset.... Lämpökynttilät..... Tuote A..... Tuote B..... Päätelmiä.... Ulkotulet.... Hautalyhdyt,
Mittaamisen hyödyt. Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori
 Mittaamisen hyödyt Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori TOIMIA-verkosto ja TOIMIA-tietokanta Kansallinen TOImintakyvyn MIttaamisen ja Arvioinnin asiantuntijaverkoston tavoitteet
Mittaamisen hyödyt Heli Valkeinen, erikoistutkija, TtT TOIMIA-verkoston koordinaattori TOIMIA-verkosto ja TOIMIA-tietokanta Kansallinen TOImintakyvyn MIttaamisen ja Arvioinnin asiantuntijaverkoston tavoitteet
TALOUSVEDEN LAATUVAATIMUKSET JA LAATUSUOSITUKSET
 TALOUSVEDEN LAATUVAATIMUKSET JA LAATUSUOSITUKSET ERKKI VUORI PROFESSORI, EMERITUS 27.11.2012 HJELT INSTITUUTTI OIKEUSLÄÄKETIETEEN OSASTO MEISSÄ ON PALJON VETTÄ! Ihmisen vesipitoisuus on keskimäärin yli
TALOUSVEDEN LAATUVAATIMUKSET JA LAATUSUOSITUKSET ERKKI VUORI PROFESSORI, EMERITUS 27.11.2012 HJELT INSTITUUTTI OIKEUSLÄÄKETIETEEN OSASTO MEISSÄ ON PALJON VETTÄ! Ihmisen vesipitoisuus on keskimäärin yli
Ehdotus NEUVOSTON PÄÄTÖS
 EUROOPAN KOMISSIO Bryssel 1.7.2016 COM(2016) 437 final 2016/0200 (NLE) Ehdotus NEUVOSTON PÄÄTÖS luonnonvaraisen eläimistön ja kasviston uhanalaisten lajien kansainvälistä kauppaa koskevan yleissopimuksen
EUROOPAN KOMISSIO Bryssel 1.7.2016 COM(2016) 437 final 2016/0200 (NLE) Ehdotus NEUVOSTON PÄÄTÖS luonnonvaraisen eläimistön ja kasviston uhanalaisten lajien kansainvälistä kauppaa koskevan yleissopimuksen
KOMISSION TÄYTÄNTÖÖNPANOPÄÄTÖS (EU) /, annettu ,
 EUROOPAN KOMISSIO Bryssel 11.7.2017 C(2017) 4675 final KOMISSION TÄYTÄNTÖÖNPANOPÄÄTÖS (EU) /, annettu 11.7.2017, organisaatioiden hyväksymiseen Eures-jäseniksi ja Eures-yhteistyökumppaneiksi käytettävien
EUROOPAN KOMISSIO Bryssel 11.7.2017 C(2017) 4675 final KOMISSION TÄYTÄNTÖÖNPANOPÄÄTÖS (EU) /, annettu 11.7.2017, organisaatioiden hyväksymiseen Eures-jäseniksi ja Eures-yhteistyökumppaneiksi käytettävien
Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen - Sic!
 Page 1 of 5 JULKAISTU NUMEROSSA 3-4/2017 EX TEMPORE Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen Enni-Kaisa Mustonen / Kirjoitettu 18.12.2017 / Julkaistu Oligonukleotidit ovat nukleotideista
Page 1 of 5 JULKAISTU NUMEROSSA 3-4/2017 EX TEMPORE Oligonukleotidi-lääkevalmisteet ja niiden turvallisuuden tutkiminen Enni-Kaisa Mustonen / Kirjoitettu 18.12.2017 / Julkaistu Oligonukleotidit ovat nukleotideista
KOMISSION ASETUS (EU) N:o /, annettu XXX,
 EUROOPAN KOMISSIO Bryssel XXX SANCO/10387/2013 Rev. 1 (POOL/E3/2013/10387/10387R1- FI.doc) D030733/02 [ ](2013) XXX draft KOMISSION ASETUS (EU) N:o /, annettu XXX, poikkeuksen myöntämisestä asetuksen (EY)
EUROOPAN KOMISSIO Bryssel XXX SANCO/10387/2013 Rev. 1 (POOL/E3/2013/10387/10387R1- FI.doc) D030733/02 [ ](2013) XXX draft KOMISSION ASETUS (EU) N:o /, annettu XXX, poikkeuksen myöntämisestä asetuksen (EY)
Noin neljäsosa EU:ssa uuden myyntiluvan saavista. Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN
 OLLI TENHUNEN LT, syöpätautien erikoislääkäri Ylilääkäri, Fimea Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN Jotta uusi syöpälääke pääsee markkinoille, edellytyksenä
OLLI TENHUNEN LT, syöpätautien erikoislääkäri Ylilääkäri, Fimea Uusien syöpälääkkeiden vilkas kehitys haastaa myös MYYNTILUPA-ARVIOINNIN KEHITTYMÄÄN Jotta uusi syöpälääke pääsee markkinoille, edellytyksenä
Farmasian tutkimuksen tulevaisuuden näkymiä. Arto Urtti Lääketutkimuksen keskus Farmasian tiedekunta Helsingin yliopisto
 Farmasian tutkimuksen tulevaisuuden näkymiä Arto Urtti Lääketutkimuksen keskus Farmasian tiedekunta Helsingin yliopisto Auttaako lääkehoito? 10 potilasta 3 saa avun 3 ottaa lääkkeen miten sattuu - ei se
Farmasian tutkimuksen tulevaisuuden näkymiä Arto Urtti Lääketutkimuksen keskus Farmasian tiedekunta Helsingin yliopisto Auttaako lääkehoito? 10 potilasta 3 saa avun 3 ottaa lääkkeen miten sattuu - ei se
LIITE I NIMI, LÄÄKEMUOTO, LÄÄKEVALMISTEIDEN VAHVUUDET, ELÄINLAJI, ANTOREITIT JA MYYNTILUVAN HALTIJA. EMEA/CVMP/166766/2006-FI Toukokuu /7
 LIITE I NIMI, LÄÄKEMUOTO, LÄÄKEVALMISTEIDEN VAHVUUDET, ELÄINLAJI, ANTOREITIT JA MYYNTILUVAN HALTIJA EMEA/CVMP/166766/2006-FI Toukokuu 2006 1/7 Jäsenvaltio Myyntiluvan haltija Hakija Valmisteen kauppanimi
LIITE I NIMI, LÄÄKEMUOTO, LÄÄKEVALMISTEIDEN VAHVUUDET, ELÄINLAJI, ANTOREITIT JA MYYNTILUVAN HALTIJA EMEA/CVMP/166766/2006-FI Toukokuu 2006 1/7 Jäsenvaltio Myyntiluvan haltija Hakija Valmisteen kauppanimi
Kemikaalien EU-riskinarviointi ja -vähennys
 Kemikaalien EU-riskinarviointi ja -vähennys Päivitetty: 9.7.2007 3,4-Dikloorianiliini CAS nro 95-76-1 Synonyymejä 3,4-Dichlorophenylaniline 3,4-dichlorophenylamine 3,4-dichlorobenzeneamine 3,4-DCA Tuoterekisteritiedot
Kemikaalien EU-riskinarviointi ja -vähennys Päivitetty: 9.7.2007 3,4-Dikloorianiliini CAS nro 95-76-1 Synonyymejä 3,4-Dichlorophenylaniline 3,4-dichlorophenylamine 3,4-dichlorobenzeneamine 3,4-DCA Tuoterekisteritiedot
Mitä eri tutkimusmetodeilla tuotetusta tiedosta voidaan päätellä? Juha Pekkanen, prof Hjelt Instituutti, HY Terveyden ja Hyvinvoinnin laitos
 Mitä eri tutkimusmetodeilla tuotetusta tiedosta voidaan päätellä? Juha Pekkanen, prof Hjelt Instituutti, HY Terveyden ja Hyvinvoinnin laitos Päätöksentekoa tukevien tutkimusten tavoitteita kullakin oma
Mitä eri tutkimusmetodeilla tuotetusta tiedosta voidaan päätellä? Juha Pekkanen, prof Hjelt Instituutti, HY Terveyden ja Hyvinvoinnin laitos Päätöksentekoa tukevien tutkimusten tavoitteita kullakin oma
Uudet tutkimusmenetelmät sisäilmaongelmien ratkomisessa tapaus toksisuustesti. Kati Huttunen Itä-Suomen Yliopisto
 Uudet tutkimusmenetelmät sisäilmaongelmien ratkomisessa tapaus toksisuustesti Kati Huttunen Itä-Suomen Yliopisto Sisäilmaongelmien tutkimusmenetelmät Lähtötilanne Käyttäjien haastattelu Tiedot rakennuksesta
Uudet tutkimusmenetelmät sisäilmaongelmien ratkomisessa tapaus toksisuustesti Kati Huttunen Itä-Suomen Yliopisto Sisäilmaongelmien tutkimusmenetelmät Lähtötilanne Käyttäjien haastattelu Tiedot rakennuksesta
EUROOPAN PARLAMENTTI
 EUROOPAN PARLAMENTTI 1999 2004 Ympäristöasioiden, kansanterveyden ja kuluttajapolitiikan valiokunta 30. huhtikuuta 2002 PE 232.377/1-11 TARKISTUKSET 1-11 Luonnos suositukseksi toiseen käsittelyyn (PE 232.377)
EUROOPAN PARLAMENTTI 1999 2004 Ympäristöasioiden, kansanterveyden ja kuluttajapolitiikan valiokunta 30. huhtikuuta 2002 PE 232.377/1-11 TARKISTUKSET 1-11 Luonnos suositukseksi toiseen käsittelyyn (PE 232.377)
Tähtäimessä vaikuttavuus turvallisesti. - HTA terveydenhuollon laitteiden näkökulmasta. Tom Ståhlberg Johtaja, Viranomaisasiat
 Tähtäimessä vaikuttavuus turvallisesti - HTA terveydenhuollon laitteiden näkökulmasta Tom Ståhlberg Johtaja, Viranomaisasiat 29.9.2016 FiHTA Tähtäimessä vaikuttavuus turvallisesti - HTA terveydenhuollon
Tähtäimessä vaikuttavuus turvallisesti - HTA terveydenhuollon laitteiden näkökulmasta Tom Ståhlberg Johtaja, Viranomaisasiat 29.9.2016 FiHTA Tähtäimessä vaikuttavuus turvallisesti - HTA terveydenhuollon
TIETOISKU LÄÄKETUTKIMUSTEN OHJEISTOISTA JA SUOSITUKSISTA
 1 TIETOISKU LÄÄKETUTKIMUSTEN OHJEISTOISTA JA SUOSITUKSISTA Outi Konttinen, ylitarkastaja STM/ETENE/TUKIJA Kirkkokatu 14, Helsinki PL 33, 00023 Valtioneuvosto puhelin 09-160 01 (vaihde), telekopio 09-160
1 TIETOISKU LÄÄKETUTKIMUSTEN OHJEISTOISTA JA SUOSITUKSISTA Outi Konttinen, ylitarkastaja STM/ETENE/TUKIJA Kirkkokatu 14, Helsinki PL 33, 00023 Valtioneuvosto puhelin 09-160 01 (vaihde), telekopio 09-160
Kliiniset lääketutkimukset yliopistosairaalan näkökulma. Lasse Viinikka 18.3.2014 Etiikan päivä 2014
 Kliiniset lääketutkimukset yliopistosairaalan näkökulma Lasse Viinikka 18.3.2014 Etiikan päivä 2014 Tutkimustyön merkitys potilashoidon kannalta parantaa asiantuntijuutta korkeatasoinen tutkija on alansa
Kliiniset lääketutkimukset yliopistosairaalan näkökulma Lasse Viinikka 18.3.2014 Etiikan päivä 2014 Tutkimustyön merkitys potilashoidon kannalta parantaa asiantuntijuutta korkeatasoinen tutkija on alansa
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Nobivac L4 injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttavat aineet: Inaktivoidut Leptospira
LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Nobivac L4 injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttavat aineet: Inaktivoidut Leptospira
(Q)SAR:ien sääntelykäyttö REACHlainsäädännössä
 (Q)SAR:ien sääntelykäyttö REACHlainsäädännössä Webinaari tietovaatimuksista 10.12.2009 http://echa.europa.eu 1 (Q)SAR-mallien käyttö Soveltaminen REACH-lainsäädännössä tietovaatimusten täyttämiseksi Ennusteiden
(Q)SAR:ien sääntelykäyttö REACHlainsäädännössä Webinaari tietovaatimuksista 10.12.2009 http://echa.europa.eu 1 (Q)SAR-mallien käyttö Soveltaminen REACH-lainsäädännössä tietovaatimusten täyttämiseksi Ennusteiden
Valtuuskunnille toimitetaan oheisena asiakirja D050358/04.
 Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11471/17 AGRILEG 146 DENLEG 61 VETER 68 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Kom:n asiak. nro:
Euroopan unionin neuvosto Bryssel, 24. heinäkuuta 2017 (OR. en) 11471/17 AGRILEG 146 DENLEG 61 VETER 68 SAATE Lähettäjä: Euroopan komissio Saapunut: 20. heinäkuuta 2017 Vastaanottaja: Kom:n asiak. nro:
LAUSUNTOLUONNOS. FI Moninaisuudessaan yhtenäinen FI. Euroopan parlamentti 2015/0068(CNS) 1.9.2015. oikeudellisten asioiden valiokunnalta
 Euroopan parlamentti 2014-2019 Oikeudellisten asioiden valiokunta 2015/0068(CNS) 1.9.2015 LAUSUNTOLUONNOS oikeudellisten asioiden valiokunnalta talous- ja raha-asioiden valiokunnalle ehdotuksesta neuvoston
Euroopan parlamentti 2014-2019 Oikeudellisten asioiden valiokunta 2015/0068(CNS) 1.9.2015 LAUSUNTOLUONNOS oikeudellisten asioiden valiokunnalta talous- ja raha-asioiden valiokunnalle ehdotuksesta neuvoston
Säteilyvaikutuksen synty. Erikoistuvien lääkärien päivät 25 26.1.2013 Kuopio
 Säteilyvaikutuksen synty Erikoistuvien lääkärien päivät 25 26.1.2013 Kuopio Säteilyn ja biologisen materian vuorovaikutus Koska ihmisestä 70% on vettä, todennäköisin (ja tärkein) säteilyn ja biologisen
Säteilyvaikutuksen synty Erikoistuvien lääkärien päivät 25 26.1.2013 Kuopio Säteilyn ja biologisen materian vuorovaikutus Koska ihmisestä 70% on vettä, todennäköisin (ja tärkein) säteilyn ja biologisen
Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en) Jeppe TRANHOLM-MIKKELSEN, Euroopan unionin neuvoston pääsihteeri
 Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en) 11882/17 SAATE Lähettäjä: Saapunut: 4. syyskuuta 2017 Vastaanottaja: Kom:n asiak. nro: ENV 727 MI 607 AGRI 443 CHIMIE 78 SAN 319 CONSOM 293
Euroopan unionin neuvosto Bryssel, 5. syyskuuta 2017 (OR. en) 11882/17 SAATE Lähettäjä: Saapunut: 4. syyskuuta 2017 Vastaanottaja: Kom:n asiak. nro: ENV 727 MI 607 AGRI 443 CHIMIE 78 SAN 319 CONSOM 293
KOMISSION TIEDONANTO. eurooppalaisesta kansalaisaloitteesta "Stop Vivisection"
 EUROOPAN KOMISSIO Bryssel 3.6.2015 C(2015) 3773 final KOMISSION TIEDONANTO eurooppalaisesta kansalaisaloitteesta "Stop Vivisection" FI FI 1. JOHDANTO Eurooppalainen kansalaisaloite Stop Vivisection ( Ei
EUROOPAN KOMISSIO Bryssel 3.6.2015 C(2015) 3773 final KOMISSION TIEDONANTO eurooppalaisesta kansalaisaloitteesta "Stop Vivisection" FI FI 1. JOHDANTO Eurooppalainen kansalaisaloite Stop Vivisection ( Ei
UUDET TEKNIIKAT SISÄYMPÄRISTÖN MIKROBIEN TOTEAMISESSA
 UUDET TEKNIIKAT SISÄYMPÄRISTÖN MIKROBIEN TOTEAMISESSA LIITU-päivä 4.5.2006 FT Helena Rintala Kansanterveyslaitos, Ympäristöterveyden osasto Mihin sisäympäristön mikrobien mittauksia tarvitaan? Rakennusten
UUDET TEKNIIKAT SISÄYMPÄRISTÖN MIKROBIEN TOTEAMISESSA LIITU-päivä 4.5.2006 FT Helena Rintala Kansanterveyslaitos, Ympäristöterveyden osasto Mihin sisäympäristön mikrobien mittauksia tarvitaan? Rakennusten
Miten EU vaikuttaa Suomen itsehoitolääkevalikoimaan? Farmasian Päivät / Lehdistöinfo
 Miten EU vaikuttaa Suomen itsehoitolääkevalikoimaan? Farmasian Päivät 20.11.2009 / Lehdistöinfo Yksikön päällikkö Marjo-Riitta Helle Fimea Itsehoitolääkkeiden tilanne Suomessa 2009 Lähtökohtaisesti lääkkeiksi
Miten EU vaikuttaa Suomen itsehoitolääkevalikoimaan? Farmasian Päivät 20.11.2009 / Lehdistöinfo Yksikön päällikkö Marjo-Riitta Helle Fimea Itsehoitolääkkeiden tilanne Suomessa 2009 Lähtökohtaisesti lääkkeiksi
KOMISSION ASETUS (EU) /, annettu ,
 EUROOPAN KOMISSIO Bryssel 23.5.2017 C(2017) 279 final KOMISSION ASETUS (EU) /, annettu 23.5.2017, säännöistä farmakologisesti vaikuttavalle aineelle tietyn elintarvikkeen osalta vahvistetun jäämän enimmäismäärän
EUROOPAN KOMISSIO Bryssel 23.5.2017 C(2017) 279 final KOMISSION ASETUS (EU) /, annettu 23.5.2017, säännöistä farmakologisesti vaikuttavalle aineelle tietyn elintarvikkeen osalta vahvistetun jäämän enimmäismäärän
Yhteiskunta- ja humanistiset tieteet (SSH) 7. puiteohjelman syksyn 2011 haku Vuoden 2012 työohjelma
 Yhteiskunta- ja humanistiset tieteet (SSH) 7. puiteohjelman syksyn 2011 haku Vuoden 2012 työohjelma Yleisiä huomioita 2012 SSH-työohjelmasta Kohdennettu erityisten yhteiskunnallisten haasteiden ratkaisemiseksi.
Yhteiskunta- ja humanistiset tieteet (SSH) 7. puiteohjelman syksyn 2011 haku Vuoden 2012 työohjelma Yleisiä huomioita 2012 SSH-työohjelmasta Kohdennettu erityisten yhteiskunnallisten haasteiden ratkaisemiseksi.
Benchmarking Controlled Trial - a novel concept covering all observational effectiveness studies
 Benchmarking Controlled Trial - a novel concept covering all observational effectiveness studies Antti Malmivaara, MD, PhD, Chief Physician Centre for Health and Social Economics National Institute for
Benchmarking Controlled Trial - a novel concept covering all observational effectiveness studies Antti Malmivaara, MD, PhD, Chief Physician Centre for Health and Social Economics National Institute for
Hoitovirheistä ja läheltä piti tilanteista oppiminen!
 1 Hoitovirheistä ja läheltä piti tilanteista oppiminen! Erna Snellman, lääkintöneuvos, dosentti, STM 2 Primum est non nocere - Do not harm Hippocrates Hoito ei saa olla vaarallisempaa kuin sen antamatta
1 Hoitovirheistä ja läheltä piti tilanteista oppiminen! Erna Snellman, lääkintöneuvos, dosentti, STM 2 Primum est non nocere - Do not harm Hippocrates Hoito ei saa olla vaarallisempaa kuin sen antamatta
Biosidiasetus - mitä uutta?
 Biosidiasetus - mitä uutta? Eeva Nurmi 10.4.2013 Sisältö Yleistä Käsitellyt esineet Rinnakkaisvalmisteiden kauppa ECHAn rooli Maksut Neuvontapalvelu Biosidiasetus (BPR) Euroopan parlamentin ja neuvoston
Biosidiasetus - mitä uutta? Eeva Nurmi 10.4.2013 Sisältö Yleistä Käsitellyt esineet Rinnakkaisvalmisteiden kauppa ECHAn rooli Maksut Neuvontapalvelu Biosidiasetus (BPR) Euroopan parlamentin ja neuvoston
