Mitotaani lisämunuaissyövän hoidossa
|
|
|
- Petteri Korhonen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
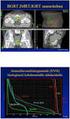
1 KATSAUS Timo Sane Lisämunuaiskuoren levinneen syövän hoidossa on käytetty peruslääkkeenä mitotaania 50 vuoden ajan. Mitotaani on hyönteismyrkkynä käytetyn DDT:n johdos. Se vähentää tämän harvinaisen taudin paikallista uusiutumista ja etäpesäkkeiden ilmaantumista myös kasvaimen täydelliseltä vaikuttaneen kirurgisen poiston jälkeen. Mitotaanin käyttöä ovat hankaloittaneet runsaat haittavaikutukset, jotka liittyvät aineen poikkeavaan farmakokinetiikkaan. Käyttö edellyttää valmisteen ominaisuuksien ja biologisten vaikutusten tuntemista. Hoidon toteuttamisen apuna on plasman mitotaanipitoisuuden määritys, jota kannattaa hyödyntää. Pitoisuutta seuraten voidaan optimoida annos ja välttää lääkkeen haittavaikutuksia Lisämunuaisen kasvaimet ovat varsin tavallisia, mutta lisämunuaiskuoren syöpä on hyvin harvinainen tauti. Sen ilmaantuvuus on vain 1 2 uutta tapausta miljoonaa henkilöä kohti vuodessa ja sen osuus kaikista syöpätapauksista on noin 0,2 % (Fassnacht ja Allolio 2009). Suomessa tauti todetaan vuosittain noin kymmenellä potilaalla. Mitotaani on syövän hoidon ensimmäisiä täsmälääkkeitä. Sitä käytettiin lisämunuaisen kuorikerrossoluja selektiivisesti tuhoavana lääkkeenä lisämunuaiskuoren syövän hoidossa ensimmäisen kerran jo 50 vuotta sitten (Bergenstal ym. 1959). Mitotaani on edelleen ainoa FDA:n ja EMEA:n yksinomaan lisämunuaiskuoren syövän hoitoon hyväksymä lääke (Fassnacht ja Allolio 2009). Sen käyttö on ollut hankalaa runsaiden haittavaikutusten ja niiden edellyttämien liitännäishoitojen vuoksi. Viime vuosina on Suomessakin ollut mahdollista määrittää plasman mitotaanipitoisuus annosten optimoimiseksi. Lisämunuaiskuoren syövän kliininen kuva ja levinneisyyden arviointi Lisämunuaiskuoren syöpä todetaan useimmiten naisilla vuoden ja miehillä vuoden iässä, mutta sairautta esiintyy myös lapsilla ja nuorilla aikuisilla (Fassnacht ja Allolio 2009, Sane 2009). Lisämunuaiskuoren syöpä on toteamisen aikaan kookas kasvain, jonka läpimitta on keskimäärin 11 cm, lähes aina yli 4 cm (Fassnacht ja Allolio 2009). Suuren kokonsa vuoksi kasvain voi aiheuttaa ylävatsa-, kylki- tai selkäkipua, mutta noin %:lla potilaista diagnoosiin päädytään lyhyessä ajassa ilmenneiden, kasvaimen hormonituotantoon liittyvien oireiden pohjalta. Useimmiten lisämunuaiskuoren syöpäkasvain erittää verenkiertoon kortisolia, toisinaan androgeeneja, harvoin estrogeeneja ja hyvin harvoin mineralokortikoideja (Sane 2009). Tietokonetomografiassa lisämunuaiskuoren syövän tiheys on ilman varjoainetta tehdyssä kuvauksessa aina yli 10 Hounsfieldin yksikköä, useimmiten HU. Kasvaimen muoto vaihtelee, se tehostuu varjoaineella epätasaisesti ja siinä saattaa näkyä kalkkeja (kuva 1). Histologisesti lisämunuaiskuoren syövän diagnoosi perustuu Weissin kriteereihin, joista vähintään neljän on täytyttävä (Sane 2009). Lisämunuaiskuoren syöpä kasvaa melko usein invasiivisesti ympäröiviin kudoksiin sekä tappimaisesti lisämunuaislaskimoon ja edelleen munuais- ja alaonttolaskimoon. Etä- Duodecim 2010;126:2040 6
2 pesäkkeitä todetaan paikallisissa imusolmukkeissa tai kauempana yleisyysjärjestyksessä keuhkoissa, maksassa ja luustossa. Levinneisyysaste luokiteltiin aiemmin McFarlanen esittämällä tavalla (Sane 2009), mutta hiljattain on esitetty käytettäväksi TNM-luokitusta (Fassnacht ym. 2009). Saksalaisessa lähes 500 potilaan aineistossa 47 % potilaista oli elossa viiden vuoden kuluttua diagnoosista ja 41 % kymmenen vuoden kuluttua (Fassnacht ja Allolio 2009). Ennusteen ratkaisee taudin levinneisyys toteamisen aikaan (taulukko 1). Ennustetta huonontavia tekijöitä ovat kasvaimen suuri koko, kirurgisen poiston epätäydellisyys, kasvainsolujen suuri mitoosiaktiivisuus tai Ki67-proliferaatioindeksi ja joidenkin tutkimusten mukaan myös kasvaimen kortisolineritys (Abiven ym. 2006, Assie ym. 2007, Fassnacht ja Allolio 2009). * Kuva 1. Kookas vasemman lisämunuaiskuoren syöpä (*), jonka läpimitta on 10 cm ja tiheys 40 Hounsfieldin yksikköä. Kasvaimen rakenne on epätasainen. Lisämunuaiskuoren syövän hoitoperiaatteet Lisämunuaiskuoren syövän ainoa varmasti parantava hoito on kasvaimen täydellinen kirurginen poisto (Fassnacht ja Allolio 2009). Jos lisämunuaiskuoren syöpä tuottaa kortisolia, on muistettava peri- ja postoperatiivinen hydrokortisonikorvaushoito. Jos kasvain on toteamisen aikaan laajalle levinnyt, ei primaarikasvaimen poistosta ole osoitettu olevan hyötyä paitsi hormonaalisesti aktiivisen kasvaimen kortisolintuotantoa hillitsevänä toimenpiteenä. Primaarikasvaimen poiston jälkeen myöhemmin ilmaantuvia yksittäisiä kookkaitakin etäpesäkkeitä kannattaa poistaa kirurgisesti, kuten jo vuosikymmeniä sitten julkaistussa kotimaisessa tapausselostuksessa kuvattiin (Tikkanen ym. 1980). Paikallisen sädehoidon käyttö leikkauksen jälkeen ei ole Suomessa vakiintunut. Se voi vähentää lisämunuaiskuoren syövän paikallista uusiutumista, mutta etäpesäkkeiden ilmaantuvuuteen tai taudin ennusteeseen hoidolla ei ole vaikutusta (Fassnacht ym. 2006, Fassnacht ja Allolio 2009). Paikallista sädehoitoa on suositeltu, mikäli kasvaimen levinneisyysaste on T1-2, N1 tai T3-4, N0-1 tai niissä rajoittuneissa kasvaimissa (T1-2, N0), joissa nähdään mikroskooppisesti verisuoni-invaasiota tai kasvaimen proliferaatioindeksi (Ki67) on yli 10 %. Sädehoito suositellaan annettavaksi kolmen kuukauden kuluessa leikkauksesta 1,8 2,0 Gy:n kerta-annoksina viitenä päivänä viikossa pyrkien vähintään 40 Gy:n kokonaisannokseen (Polat ym. 2009). Mitotaanihoitoa käytetään levinneen lisämunuaiskuoren syövän ainoana lääkkeenä tai muun solunsalpaajahoidon rinnalla. Primaarikasvaimen radikaalilta vaikuttaneen poiston jälkeen tauti uusiutuu paikallisesti tai etäpesäkkeinä %:lla potilaista. Hiljattain julkaistussa laajassa takautuvassa tutkimuk- Taulukko 1. Lisämunuaissyövän TNM-luokitus ja sen vaikutus taudin ennusteeseen. Kasvaimen luokka Koko tai levinneisyys T1 5 cm 84 T2 > 5 cm 63 T3 kasvaa paikallisesti 51 ympäröiviin kudoksiin tai laskimoihin T4 etäpesäkkeitä, kasvaa viereisiin kudoksiin 15 Viiden vuoden ennuste (%) 2041
3 KATSAUS 2042 sessa mitotaani hidasti taudin uusiutumista leik kaushoidon jälkeen (Schteingart 2007, Terzolo ym. 2007). Tutkimusta on kuitenkin kritisoitu sen takautuvuuden ja käytettyjen tilastollisten analyysien vuoksi (Huang ja Fojo 2008). Lopullinen vastaus mitotaanin merkityksestä leikkausta täydentävänä hoitona saadaan, kun pienen tai kohtalaisen uusiutumisriskin potilailla tehtävä etenevä satunnaistettu tutkimus (ADIUVO) valmistuu (Terzolo ym. 2009). Fassnachtin ja Allolion (2009) tuoreessa katsauksessa on suositeltu mitotaanihoidon aloittamista leikkauksen jälkeen, jos poistettu kasvain on ollut suuri (läpimitta yli 8 cm), tai sen proliferaatioindeksi on yli 10 % tai jos siinä todetaan mikroskooppisesti verisuoniinvaasiota. Tähän näkemykseen on helppo yhtyä. Mitotaanihoitoa jatketaan yhtäjaksoisesti ainakin 2 3 vuotta. Ellei viitteitä taudista tänä aikana ole ilmaantunut, hoito voidaan lopettaa. Jos tauti on toteamisen aikaan aggressiivinen (Ki67-proliferaatioindeksi yli 20 %) tai etenee hoidon aikana, mitotaaniin liitetään heti streptotsotosiini tai usean solunsalpaajan yhdistelmä (Kirschner 2006, Fassnacht ja Allolio 2009). Mitotaanin farmakologiset ominaisuudet ja vaikutusmekanismi Mitotaani löydettiin sattumalta, kun hyönteismyrkkynä tunnetun DDT:n (diklooridifenyylitrikloorietaani, C 14 H 9 5 ) johdoksen DDD:n (diklooridifenyylidikloorietaani, C 14 H 10 4 ) todettiin aiheuttavan koirille selektiivisesti lisämunuaisten kuorikerrossolujen nekroosin. Syynä oli DDD:n isomeeri o,p DDD eli mitotaani (kuva 2), joka identifioitiin vuonna 1949 (Nelson ja Woodard). Hyvin lipofiilisena mitotaani läpäisee solukalvon ja erittyy siksi myös äidinmaitoon. Kuorikerrossolujen mitokondrioissa se hydroksyloituu P450-entsyymijärjestelmän katalysoimassa reaktiossa (Schteingart 2007). Hydroksylaation jälkeen mitotaanista muodostuu asyylikloridijohdos, joka kiinnittyy mitokondrioiden seinämiin ja vaurioittaa niitä, tai siitä muodostuu asetaattijohdos (o,p -DDA), joka erittyy virtsaan. Kasvainsolujen kyky metaboloida mitotaania C C H H Kuva 2. Mitotaanin eli triviaalinimeltään o,p DDD:n (C 14 H 10 4 ) 1,1-dikloro-2-(o-klorofenyyli)-2-(p-klorofenyyli)-etaanin) molekyylirakenne. on ratkaisevaa lääkkeen vaikutukselle, ja tämä selittää vaihtelevan hoitovasteen (Schteingart 2007, Fassnacht ja Allolio 2009). Spironolaktonin on esitetty estävän mitotaanin vaikutusta, mutta ilmiön mekanismi on avoin. Mitotaani on sytotoksinen erityisesti lisämunuaiskuoren kortisolia muodostaville zona fasciculatan ja zona reticulariksen soluille. Vaikutus uloimman zona glomerulosan soluihin on vähäisempi. Hoito heikentää siten usein jäljelle jääneen lisämunuaiskuoren kortisolineritystä mutta harvemmin aldosteronintuotantoa. Kortisolineritys voi hiipua hyvin nopeasti tai vasta myöhemmin hoidon aikana. Mitotaani aktivoi maksan mikrosomaalista entsyymijärjestelmää, mikä ilmenee plasman glutamyylitransferaasin pitoisuuden suurentumisena ja nopeuttaa mm. varfariinin, fenytoiinin, steroidien (kortisoli, ehkäisypillerit, fludrokortisoni) ja kilpirauhashormonien metaboliaa (Fassnacht ja Allolio 2009). Mitotaani lisää maksassa sukupuolihormonien ja kortisolin kuljettajavalkuaisten synteesiä, ja yksittäisillä potilailla näiden pitoisuudet voivat moninkertaistua (Nader ym. 2006, Fassnacht ja Allolio 2009). Tämän vuoksi seerumin kokonaistestosteroni- ja kortisolipitoisuudet voivat olla mitotaania käyttävillä näennäisesti normaaleja, vaikka tosiasiassa potilaalla on kyseisten hormonien puute. Mitotaani pienentää seerumin vapaan tyroksiinin (T 4 V) ja vapaan trijodityroniinin (T 3 V) pitoisuuksia, mutta seerumin tyreotropiinipitoisuus säilyy normaalina tai jopa voi pienentyä. Mitotaani lisää T 4 V:n ja T 3 V:n sitoutumista kantajaval- T. Sane
4 kuaiseen, jonka pitoisuutta se myös suurentaa. Mitotaanihoito suurentaa osalla potilaista LDL-kolesterolipitoisuuden jopa kaksinkertaiseksi, mutta se normaalistuu melko pienellä statiiniannoksella (Fassnacht ja Allolio 2009). Mitotaanin annostelu ja potilaan seuranta Mitotaania otetaan suun kautta 500 mg:n tabletteina (Lysodren, HRA Pharma). Ruoka parantaa imeytymistä, ja lääke suositellaan otettavaksi aterian yhteydessä. Mitotaani varastoituu rasvakudokseen, ja siksi sen pitoisuus plasmassa suurenee hyvin hitaasti. Toisaalta käytön lopettamisen jälkeen voi kestää jopa 11 kuukautta, ennen kuin lääke on hävinnyt kokonaan elimistöstä (Baudin ym. 2001). Tutkimusten mukaan plasman optimaalinen mitotaanipitoisuus on mg/l (Haak ym. 1995, Baudin ym. 2001, Fassnacht ja Allolio 2009). Yksittäisissä tapauksissa sytotoksinen hoitovaste on saavutettu ilman, että mitotaanipitoisuus on ollut tavoitetasolla (Seki ym. 1999) tai haittavaikutuksia on ilmaantunut jo tavoitetta paljon pienemmillä pitoisuuksilla (Fassnacht ja Allolio 2009). Mitotaanihoito on yleensä aloitettu noin 2 3 g:n ylläpitoannoksella, mutta näin toimittaessa lääkkeen tavoitepitoisuuden saavuttamiseen kuluu keskimäärin puoli vuotta (Terzolo ym. 2000). Mitotaanipitoisuuden ja kumulatiivisen lääkeannoksen välillä on hyvä korrelaatio, ja lääkkeen tavoitepitoisuus saavutetaan vasta kumulatiivisen annoksen ollessa noin 350 g (Terzolo ym. 2000, Baudin ym. 2001). Kuvassa 3 on esitetty kumulatiivisen mitotaaniannoksen ja plasman mitotaanipitoisuuden suhde neljällä HYKS:n endokrinologian klinikassa pitkään mitotaania käyttäneellä potilaalla. Toksista mitotaanipitoisuutta ei g:n kokonaisannoksella saavuteta, ja tavoitepitoisuus ylittyy vasta noin 700 g:n kumulatiivisella annoksella (Baudin ym. 2001). Viime aikoina on suositeltu mitotaaniannoksen nopeata suurentamista, jotta tavoiteltu pitoisuus ja siten toivottu hoitovaste saavutetaan 1 2 kuukaudessa (Faggiano ym. 2006, Fassnacht ja Allolio 2009). Taulukossa 2 on esitetty mitotaanihoidon käytännön toteutus ja taulukossa 3 potilaan seurannassa käytettävät laboratoriokokeet. Lääkeannosta vähennetään jo mitotaanipitoisuuden lähestyessä tavoitealueen alarajaa (14 mg/l, kumulatiivinen annos noin 350 g), koska annoksen muutos vaikuttaa lääkkeen pitoisuuteen viiveellä. Ylläpitoannokseksi riittää 2 3 g vuorokaudessa, joskus tätä pienempikin määrä. Jos potilaalle Plasman mitotaanipitoisuus (mg/l) Kumulatiivinen mitotaaniannos (g) Kuva 3. Kumulatiivisen mitotaaniannoksen ja plas man mitotaanipitoisuuden välinen korrelaatio (r = 0,80) neljällä HYKS:n endokrinologian klinikassa lisämunuaiskuoren syövän vuoksi hoidetulla potilaalla. 2043
5 KATSAUS 2044 Taulukko 2. Mitotaanihoidon nopea aloitus ja ylläpitohoito. Aloita annoksin 0,5 g x 3 aterian yhteydessä Suurenna annosta viikon välein määriin 1 g x 3 ja 1,5 g x 3 ja 2 g x 3, ellei haittavaikutuksia ilmaannu Jos haittavaikutuksia ilmenee, yritä annoksen suurentamista myöhemmin uudestaan Mittaa plasman mitotaanipitoisuus ensimmäisen kerran neljän viikon kuluttua hoidon aloituksesta, jos kumulatiivinen annos on yli 150 g, ja sen jälkeen neljän viikon välein Siirry ylläpitoannokseen (2 3 g/vrk), kun kumulatiivinen annos ylittää määrän 350 g tai plasman mitotaanipitoisuus on yli 10 mg/l Seuraa plasman mitotaanipitoisuutta 4 8 viikon välein Mikäli haittavaikutuksia ilmaantuu (taulukko 4), keskeytä hoito 1 2 viikoksi ja jatka pienemmällä annoksella Taulukko 3. Mitotaanihoidon seurantakokeet. Tutkimusten väli Laboratoriokoe 4 8 viikon välein Mitotaanipitoisuus Elektrolyytit Kreatiniini Maksakokeet (ASAT, ALAT,bilirubiini, GT Kortisoli ja ACTH 3 kuukauden välein Verenkuva Rasva-arvot Kilpirauhasen toimintakokeet Reniinin aktiivisuus kehittyy haittaoireita tai mitotaanipitoisuus ylittää arvon 20 mg/l, lääkkeen käyttö keskeytetään 1 2 viikoksi ja tämän jälkeen jatketaan aikaisempaa selvästi pienemmällä annoksella lääkepitoisuutta ja haittaoireita seuraten. Plasman mitotaanipitoisuuden määritys Mitotaania valmistava HRA-Pharma on järjestänyt Euroopassa plasman mitotaanipitoisuuden ilmaisen määrityksen hoidon seurantaa varten ( Plasman mitotaanimäärityksellä on ainakin HUSLABis sa oma tutkimusnumeronsa. Verinäyte otetaan muiden laboratoriokokeiden yhteydessä ja lähetetään kuriiripostissa Ranskaan. Lähetetietoihin kirjataan potilaan nimikirjaimien lisäksi paino ja näytettä otettaessa käytetty mitotaaniannos. Tulos ilmoitetaan yleensä viikon kuluessa suoraan hoitavalle lääkärille, ja vastaus näkyy myös kumulatiivisessa laboratoriotuloskertymässä. Haittavaikutukset Mitotaanin haittavaikutukset ovat hyvin moninaiset, ja niitä ilmenee jossain muodossa 80 %:lla potilaista (Fassnacht ja Allolio 2009). Osa niistä on hyvin tavallisia, osa puolestaan hyvin harvinaisia (taulukko 4). Erilaisia neurologisia haittavaikutuksia todetaan 40 %:lla potilaista. Niiden ilmenemiseen kannattaa kiinnittää huomiota, koska ne tulevat esille Taulukko 4. Mitotaanin haittavaikutukset yleisyyden mukaan. Hyvin tavallisia Ruokahaluttomuus Pahoinvointi, oksentelu Ripuli Maksa-arvojen suureneminen (erityisesti GT) Hyperkolesterolemia Kilpirauhasarvojen poikkeavuus Kortisolin puute Tavallisia Muistin heikentyminen Puheen häiriöt Sekavuus, depressio Huimaus, ataksia Ihoreaktiot Gynekomastia Miehen hypogonadismi Leukopenia Pidentynyt vuotoaika Aldosteronin puute Harvinaisia Anemia Trombosytopenia Hepatiitti Maksan vajaatoiminta Hyvin harvinaisia Retinopatia Makulaturvotus Kaksoiskuvat Kaihi Hemorraginen kystiitti Proteinuria T. Sane
6 usein vain kysyttäessä. Haittavaikutukset häviävät yleensä mitotaanihoidon keskeyttämisen jälkeen. Oireiden hävittyä hoitoa voidaan useimmiten jatkaa uudestaan aiempaa pienemmällä vuorokausiannoksella. Liitännäishoidot Vähäinenkin kortisolin puute voimistaa mitotaanin aiheuttamia gastrointestinaalisia haittaoireita (taulukko 4). Liian pieni glukokortikoidin määrä voi aiheuttaa Addisonin kriisin kaltaisen tilan. Tämän olen nähnyt myös omilla potilaillamme. Mitotaanin annosta nopeasti suurennettaessa on suositeltu glukokortikoidihoidon varhaista aloittamista (Faggiano ym. 2006). Hydrokortisonihoito aloitetaan annoksella mg aamulla ja 5 10 mg iltapäivän lopussa. Vuorokausiannosta suurennetaan voinnin, seerumin suola-arvojen ja plasman ACTH-pitoisuuden perusteella. Addisonin tautiin verrattuna hydrokortisonin tai synteettisten glukokortikoidien tarve on kaksin kolminkertainen (usein 50 mg hydrokortisonia vuorokaudessa tai enemmän), koska mitotaani nopeuttaa hydrokortisonin metaboliaa ja suurentaa sen kantajavalkuaisen määrää (Fassnacht ja Allolio 2009). Glukokortikoidin määrä on sopiva, kun potilaan vointi on hyvä, paino vakaa ja plasman ACTH-pitoisuus viitealueen ylärajoilla (Fassnacht ja Allolio 2009). Myös fludrokortisonin tarve on tavanomaista suurempi, ja annosta muutetaan suola-arvojen ja verenpaineen mukaan ja pitämällä plasman reniinin aktiivisuus viitealueen ylärajoilla. Laboratoriokokeista ei ole hyötyä kilpirauhashormonin puutteen arvioinnissa, joten tyroksiinihoito aloitetaan ensisijaisesti oireiden perusteella. Lopuksi YDINASIAT 88Hoitoa aloitettaessa mitotaanin pitoisuus plasmassa suurenee hyvin hitaasti. 88Mitotaani aiheuttaa usein hyvin monenlaisia haittavaikutuksia, joiden ilmaantuvuus on sidoksissa plasman lääkepitoisuuteen. 88Mitotaani voi aiheuttaa nopeasti kortisolivajeen, minkä vuoksi mitotaanin rinnalle on ajoissa aloitettava glukokortikoidihoito. 88Mitotaanilääkitys edellyttää endokrinologin ja onkologin saumatonta yhteistyötä. Mitotaani on vanha mutta edelleen käyttökelpoinen lääke lisämunuaiskuoren syövän hoidossa. Sen käyttö edellyttää kuitenkin lääkkeen poikkeuksellisen farmakokinetiikan tuntemista ja valppautta, etteivät toksiset haittavaikutukset tai lääkkeen aiheuttama kortisolin puute pääse yllättämään. Lisämunuaiskuoren syövän hoidossa tarvitaan siten onkologin ja endokrinologin hyvää yhteistyötä, kun kirurgi on ensin tehnyt parhaansa. TIMO SANE, dosentti, osastonylilääkäri HYKS:n endokrinologian klinikka PL 340, HUS Summary Mitotane in the treatment of adrenal carcinoma Mitotane has been used for 50 years as the first-line drug in the treatment of disseminated adrenocortical carcinoma. It reduces local recurrence of the disease and development of metastases even after a seemingly total surgical removal of the tumor. The use of mitotane has been hampered by its copious adverse effects. Its use requires knowledge of the properties and biological effects of the product. Determination of plasma levels of mitotane will help in carrying out the treatment. The dosage can be optimized and the drug s adverse effects avoided by monitoring the plasma level. 2045
7 KATSAUS KIRJALLISUUTTA Abiven G, Coste J, Groussin L, ym. inical and biological features in the prognosis of adrenocortical cancer: poor outcome of cortisol-secreting tumors in a series of 202 consecutive patients. J in Endocrinol Metab 2006;91: Assie G, Antoni G, Tissier F, ym. Prognostic parameters of metastatic adrenocortical cancer. J in Endocrinol Metab 2007;92: Baudin E, Pellegriti G, Bonnay M, ym. Impact of monitoring 1,1-dichlorodiphenildichloroethane (o,p DDD) levels on the treatment of patients with adrenocortical carcinoma. Cancer 2001;92: Bergenstal D, Lipsett M, Moy R, Hertz R. Regression of adrenal cancer and suppression of adrenal function in men by o,p-ddd. Trans Am Physicians 1959;72:341. Faggiano A, Leboulleux S, Young J, Schlumberger M, Baudin E. Rapidly progressing high 0,p DDD doses shorten the time required to reach the therapeutic threshold with an acceptable tolerance: preliminary results. in Endocrinol 2006;64: Fassnacht M, Hahner S, Polat B, ym. Efficacy of adjuvant radiotherapy of the tumor bed on local recurrence of adrenocortical carcinoma. J in Endocrinol Metab 2006;91: Fassnacht M, Allolio B. inical review: clinical management of adrenocortical carcinoma. Best Pract Res in Endocrinol Metab 2009;23: Fassnacht M, Johanssen S, Quinkler M, ym. Limited prognostic value of the 2004 International Union Against Cancer staging classification for adrenocortical carcinoma: proposal for a revised TNM classification. Cancer 2009;115: Haak IR, Hermans J, van de Velde CJ, ym. Optimal treatment of adrenocortical carcinoma with mitotane: results in a consecutive series of 96 patients. Br J Cancer 1995;69: Huang H, Fojo F. Commentary: adjuvant mitotane for adrenocortical cancer a recurring controversy. J in Endocrinol Metab 2008;93: Kirschner LS. Review: emerging treatment strategies for adrenocortical carcinoma: a new hope. J in Endocrinol Metab 2006;91: Nader N, Raverot G, Emptoz-Bonneton A, ym. Mitotane has an estrogenic effect on sex hormone-binding globulin and cortico-binding globulin in humans. J in Endocrinol Metab 2006;91: Nelson AA, Woodard G. Severe adrenal cortical atrophy (cytotoxic) and hepatic damage produced in dogs by feeding 2,2- bis- (parachlorophenyl)-1,1-dichloroethane (DDD). Arch Pathol 1949;48:387. Polat B, Fassnacht M, Pfeundner L, ym. Radiation therapy of adrenocortical carcinoma. Cancer 2009;115: Sane T. Lisämunuaisen kasvaimet ja paraganglioomat. Kirjassa: Välimäki M, Sane T, Dunkel L, toim. Endokrinologia. Helsinki: Kustannus Oy Duodecim 2009, s Schteingart DE. Adjuvant mitotane therapy of adrenal cancer use and controversy. N Engl J Med 2007;356: Seki M, Nomura K, Hirohara D, ym. Changes in neoplastic cell features and sensitivity to mitotane during mitotaneinduced remission in a patient with recurrent, metastatic adrenocortical carcinoma. Endocr Relat Cancer 1999;6: Terzolo M, Pia A, Berruti A, ym. Lowdose monitored mitotane treatment achieves the therapeutic range with manageable side effects in patients with adrenocortical carcinoma. J in Endocrinol Metab 2000;85: Terzolo M, Angeli A, Fassnacht M, ym. Adjuvant mitotane treatment in patients with adrenocortical carcinoma. N Engl J Med 2007;356: Terzolo M, Fassnacht M, Ciccone, Allolio B, Berruti A. Adjuvant mitotane for adrenocortical cancer working through uncertainty. J in Endocrinol Metab 2009;95: Tikkanen M, Sivula A, Kahri A, Pelkonen R. Recurrent adrenal cortical carcinoma with Cushing s syndrome: twenty-five-year follow-up of a patient. J Endocrinol Invest 1980;4: Sidonnaisuudet 2046 Kirjoittajalle ei ole sidonnaisuuksia mitotaania markkinoivaan ja valmistavaan yritykseen. Kirjoittaja on 2 viime vuoden aikana osallistunut Novo Nordisk Farma Oy:n ja Novartis Finland Oy:n kustantamille kongressimatkoille ja saanut yksittäisiä luentopalkkioita Suomen MSD Oy:ltä, Sanofi Aventis Oy:ltä.
Kliinikko ja S-korsol/dU-korsol. 4.2.2009 Anna-Mari Koski Keski-Suomen keskussairaala
 Kliinikko ja S-korsol/dU-korsol 4.2.2009 Anna-Mari Koski Keski-Suomen keskussairaala Lisämunuaisen toiminnan tutkimiseen käytettävät t hormonitutkimukset Tutkimusaihe Perustutkimus Rasituskokeet Hyperkortisolismi
Kliinikko ja S-korsol/dU-korsol 4.2.2009 Anna-Mari Koski Keski-Suomen keskussairaala Lisämunuaisen toiminnan tutkimiseen käytettävät t hormonitutkimukset Tutkimusaihe Perustutkimus Rasituskokeet Hyperkortisolismi
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0
 PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
Potilaan päiväkirja. Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi
 Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
kalvopäällysteiset tabletit Titrausopas Uptravi-hoidon aloitus Lue oheinen pakkausseloste ennen hoidon aloittamista.
 1 kalvopäällysteiset tabletit Titrausopas Uptravi-hoidon aloitus Lue oheinen pakkausseloste ennen hoidon aloittamista. 2 3 Sisältö Miten Uptravi otetaan?............................................ 4 Miten
1 kalvopäällysteiset tabletit Titrausopas Uptravi-hoidon aloitus Lue oheinen pakkausseloste ennen hoidon aloittamista. 2 3 Sisältö Miten Uptravi otetaan?............................................ 4 Miten
Levinneen suolistosyövän hoito
 Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Lisämunuaiset. Taneli Raivio
 Lisämunuaiset Taneli Raivio 5.2.2018 Historiaa Steroidogeneesi Säätely Glukokortikoidit Farmakologinen glukokortikoidihoito Lisämunuaisen sairauksia Tietovisa http://www.adrenaltumors.org/history#sthash.jdtjv5pr.dpuf
Lisämunuaiset Taneli Raivio 5.2.2018 Historiaa Steroidogeneesi Säätely Glukokortikoidit Farmakologinen glukokortikoidihoito Lisämunuaisen sairauksia Tietovisa http://www.adrenaltumors.org/history#sthash.jdtjv5pr.dpuf
Pia Jaatinen, TaY, Lääketieteen laitos ja TAYS, sisätautien i vastuualue
 Pia Jaatinen, TaY, Lääketieteen laitos ja TAYS, sisätautien i vastuualue Endopäivät 2008 yleisyys yy etiologia ja patogeneesi kliininen kuva diagnostiikka ja luokittelu hoito ennuste tulevaisuuden näkymiä
Pia Jaatinen, TaY, Lääketieteen laitos ja TAYS, sisätautien i vastuualue Endopäivät 2008 yleisyys yy etiologia ja patogeneesi kliininen kuva diagnostiikka ja luokittelu hoito ennuste tulevaisuuden näkymiä
Erityisturvallisuustiedote
 Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Firmagon eturauhassyövän hoidossa
 Firmagon eturauhassyövän hoidossa Käytännön tietoa ja ohjeita potilaalle Eturauhassyöpään sairastuminen ja sen hoito aiheuttavat uuden elämäntilanteen. Mielessä voi pyöriä monia kysymyksiä. Ajatusten kanssa
Firmagon eturauhassyövän hoidossa Käytännön tietoa ja ohjeita potilaalle Eturauhassyöpään sairastuminen ja sen hoito aiheuttavat uuden elämäntilanteen. Mielessä voi pyöriä monia kysymyksiä. Ajatusten kanssa
Seminoman hoito ja seuranta. S. Jyrkkiö
 Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Seminoman hoito ja seuranta S. Jyrkkiö 17.4.2015 Kivessyöpä yleistyy Pohjoismaissa Seminoman ja non-seminoomien yleisyys Pohjoismaissa Kuolleisuus kivessyöpään Pohjoismaissa Kivessyöpä 5 v OSS Kivestuumoreiden
Hyötyosuus. ANNOS ja sen merkitys lääkehoidossa? Farmakokinetiikan perusteita. Solukalvon läpäisy. Alkureitin metabolia
 Neurofarmakologia Farmakologian perusteiden kertausta Pekka Rauhala Syksy 2012 Koulu, Mervaala & Tuomisto, 8. painos, 2012 Kappaleet 11-30 (pois kappale 18) tai vastaavat asiat muista oppikirjoista n.
Neurofarmakologia Farmakologian perusteiden kertausta Pekka Rauhala Syksy 2012 Koulu, Mervaala & Tuomisto, 8. painos, 2012 Kappaleet 11-30 (pois kappale 18) tai vastaavat asiat muista oppikirjoista n.
Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi
 Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
(pembrolitsumabi) Tietoa potilaille
 Tietoa KEYTRUDA - valmisteesta (pembrolitsumabi) Tietoa potilaille Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Tietoa KEYTRUDA - valmisteesta (pembrolitsumabi) Tietoa potilaille Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka
 Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka Pehmytkudos- ja luusarkoomissa eri hoito-ohjelmat pehmytkudossarkoomissa yleensä kirurgia ensin Onkologinen
Sarkoomien onkologiset hoidot onko sarkoomatyypillä väliä? Paula Lindholm TYKS, syöpätautien klinikka Pehmytkudos- ja luusarkoomissa eri hoito-ohjelmat pehmytkudossarkoomissa yleensä kirurgia ensin Onkologinen
Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista
 Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista Valmisteyhteenveto on luettava huolellisesti ennen Bupropion Sandoz -valmisteen
Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista Valmisteyhteenveto on luettava huolellisesti ennen Bupropion Sandoz -valmisteen
Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten tenofoviiridisoproksiilifumaraattihoidon aikana
 Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten fumaraattihoidon aikana HIV-positiivisilla potilailla on suurentunut heikentyneen munuaistoiminnan
Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten fumaraattihoidon aikana HIV-positiivisilla potilailla on suurentunut heikentyneen munuaistoiminnan
Neuroendokriinisten syöpien lääkehoito
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Mikä on HER2-positiivinen rintasyöpä?
 Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Uutta lääkkeistä: Vemurafenibi
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Lääkkeet muistisairauksissa
 Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
Läpimurto ms-taudin hoidossa?
 Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Läpimurto ms-taudin hoidossa? Läpimurto ms-taudin hoidossa? Kansainvälisen tutkijaryhmän kliiniset kokeet uudella lääkkeellä antoivat lupaavia tuloksia sekä aaltoilevan- että ensisijaisesti etenevän ms-taudin
Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa. Tietoa terveydenhuollon ammattilaisille
 Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa Tietoa terveydenhuollon ammattilaisille Suositukset seuraavissa tilanteissa: - maksan toiminnan seuraaminen - yhteisvaikutukset
Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa Tietoa terveydenhuollon ammattilaisille Suositukset seuraavissa tilanteissa: - maksan toiminnan seuraaminen - yhteisvaikutukset
2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Forthyron vet 200 mikrog tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää 200 mikrogrammaa levotyroksiininatriumia, joka vastaa 194 mikrogrammaa
1. ELÄINLÄÄKKEEN NIMI Forthyron vet 200 mikrog tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää 200 mikrogrammaa levotyroksiininatriumia, joka vastaa 194 mikrogrammaa
Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
Uutta lääkkeistä: Ulipristaali
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
Mitä onkologi toivoo patologilta?
 Mitä onkologi toivoo patologilta? Mikä PAD-lausunnossa vaikuttaa kilpirauhassyövän hoitoon Hanna Mäenpää, dos HUS, Syöpätautien klinikka Onkologian trendejä Entiteetit pirstoutuvat pienemmiksi: lisää tietoa
Mitä onkologi toivoo patologilta? Mikä PAD-lausunnossa vaikuttaa kilpirauhassyövän hoitoon Hanna Mäenpää, dos HUS, Syöpätautien klinikka Onkologian trendejä Entiteetit pirstoutuvat pienemmiksi: lisää tietoa
ALL2000_Amendment_2014
 ALL2000_Amendment_2014 Hoito-ohjelmaa voidaan käyttää yli 15-vuotiaiden T- tai B-ALL-potilaiden hoidossa. ALL2000_amendement_2014 koostuu induktiohoidosta, viidestä konsolidaatiohoidosta ja ylläpitohoidosta.
ALL2000_Amendment_2014 Hoito-ohjelmaa voidaan käyttää yli 15-vuotiaiden T- tai B-ALL-potilaiden hoidossa. ALL2000_amendement_2014 koostuu induktiohoidosta, viidestä konsolidaatiohoidosta ja ylläpitohoidosta.
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Valmistetta ei tule käyttää tiineillä ja imettävillä nartuilla eikä koirilla, joilla on maksan vajaatoiminta.
 1. ELÄINLÄÄKKEEN NIMI Barbivet vet. 30 mg tabletti Barbivet vet. 60 mg tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine Yksi 30 mg tabletti sisältää fenobarbitaalia 30 mg. Yksi 60 mg tabletti
1. ELÄINLÄÄKKEEN NIMI Barbivet vet. 30 mg tabletti Barbivet vet. 60 mg tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine Yksi 30 mg tabletti sisältää fenobarbitaalia 30 mg. Yksi 60 mg tabletti
Miten Truvadaa otetaan
 Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
1. ELÄINLÄÄKKEEN NIMI. Thyroxanil vet 200 mikrogrammaa tabletit koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. 1 tabletti sisältää:
 1. ELÄINLÄÄKKEEN NIMI vet 200 mikrogrammaa tabletit koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 tabletti sisältää: Vaikuttava aine: Levotyroksiininatrium (vastaa levotyroksiinia 200
1. ELÄINLÄÄKKEEN NIMI vet 200 mikrogrammaa tabletit koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 tabletti sisältää: Vaikuttava aine: Levotyroksiininatrium (vastaa levotyroksiinia 200
Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku
 1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
Rintasyöpä ja sen ehkäisy. Jaana Kolin
 Rintasyöpä ja sen ehkäisy Jaana Kolin Syöpä sairautena Uusia syöpiä todetaan maassamme vuosittain noin 29.000 Miehillä ja naisilla syöpiä todetaan suurin piirtein yhtä paljon Vuoteen 2020 mennessä uusien
Rintasyöpä ja sen ehkäisy Jaana Kolin Syöpä sairautena Uusia syöpiä todetaan maassamme vuosittain noin 29.000 Miehillä ja naisilla syöpiä todetaan suurin piirtein yhtä paljon Vuoteen 2020 mennessä uusien
(pembrolitsumabi) Tietoa potilaille
 Tietoa KEYTRUDA - valmisteesta (pembrolitsumabi) Tietoa potilaille Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon
Tietoa KEYTRUDA - valmisteesta (pembrolitsumabi) Tietoa potilaille Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon
Suositukset maksan haittavaikutusten välttämiseksi. Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan.
 Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Uutta lääkkeistä: Palbosiklibi
 Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Potilasopas TREVICTA
 Potilasopas TREVICTA Miten pitkävaikutteinen psykoosilääke toimii? Pitkävaikutteisella psykoosilääkkeellä saadaan vakaa veren lääkepitoisuus. Lääke vapautuu tasaisesti ja saavuttaa pitkäkestoisen vaikutuksen
Potilasopas TREVICTA Miten pitkävaikutteinen psykoosilääke toimii? Pitkävaikutteisella psykoosilääkkeellä saadaan vakaa veren lääkepitoisuus. Lääke vapautuu tasaisesti ja saavuttaa pitkäkestoisen vaikutuksen
Eläimiä koskevat erityiset varotoimet Jos haittavaikutuksia ilmenee, tulee hoito keskeyttää ja ottaa yhteys eläinlääkäriin.
 1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
Liite III. Muutokset tuotetietojen olennaisiin kohtiin
 Liite III Muutokset tuotetietojen olennaisiin kohtiin Huomautus: Nämä valmistetiedot ovat tulos referraaliprosessista, johon tämä komission päätös liittyy. Jäsenvaltioiden toimivaltaiset viranomaiset voivat
Liite III Muutokset tuotetietojen olennaisiin kohtiin Huomautus: Nämä valmistetiedot ovat tulos referraaliprosessista, johon tämä komission päätös liittyy. Jäsenvaltioiden toimivaltaiset viranomaiset voivat
VALMISTEYHTEENVETO. 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni. 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine:
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
TIETOA ETURAUHASSYÖPÄPOTILAAN SOLUNSALPAAJAHOIDOSTA
 TIETOA ETURAUHASSYÖPÄPOTILAAN SOLUNSALPAAJAHOIDOSTA TOSIASIOITA USKOMUSTEN TAKANA HARVINAISET SAIRAUDET I MS-TAUTI I ONKOLOGIA I IMMUNOLOGIA 1 LUKIJALLE Eturauhassyöpä on Suomessa miesten yleisin syöpä.
TIETOA ETURAUHASSYÖPÄPOTILAAN SOLUNSALPAAJAHOIDOSTA TOSIASIOITA USKOMUSTEN TAKANA HARVINAISET SAIRAUDET I MS-TAUTI I ONKOLOGIA I IMMUNOLOGIA 1 LUKIJALLE Eturauhassyöpä on Suomessa miesten yleisin syöpä.
2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Forthyron Smak vet 200 mikrog tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: 200 mikrogrammaa levotyroksiininatriumia, joka vastaa 194 mikrogrammaa
1. ELÄINLÄÄKKEEN NIMI Forthyron Smak vet 200 mikrog tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: 200 mikrogrammaa levotyroksiininatriumia, joka vastaa 194 mikrogrammaa
Caprelsa. Vandetanibi CAPRELSA (VANDETANIBI) POTILAAN JA POTILAAN HUOLTAJAN (PEDIATRINEN KÄYTTÖ) OPAS ANNOSTELUSTA JA SEURANNASTA
 Caprelsa Vandetanibi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Caprelsa Vandetanibi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Tervekudosten huomiointi rinnan sädehoidossa
 Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
Tervekudosten huomiointi rinnan sädehoidossa Onkologiapäivät 30.8.2013 Sairaalafyysikko Sami Suilamo Tyks, Syöpäklinikka Esityksen sisältöä Tervekudoshaittojen todennäköisyyksiä Tervekudosten annostoleransseja
Tasigna (nilotinibi) Tärkeää tietoa lääkehoidostasi
 Tasigna (nilotinibi) Tärkeää tietoa lääkehoidostasi Tärkeää tietoa TASIGNA-hoidosta Mitä TASIGNA ON? TASIGNA on reseptilääke, jota käytetään Philadelphia-kromosomipositiivisen kroonisen myelooisen leukemian
Tasigna (nilotinibi) Tärkeää tietoa lääkehoidostasi Tärkeää tietoa TASIGNA-hoidosta Mitä TASIGNA ON? TASIGNA on reseptilääke, jota käytetään Philadelphia-kromosomipositiivisen kroonisen myelooisen leukemian
Kilpirauhasvasta-aineet: milloin määritys on tarpeen? Dosentti, oyl Anna-Maija Haapala 7.2.2014
 Kilpirauhasvasta-aineet: milloin määritys on tarpeen? Dosentti, oyl Anna-Maija Haapala 7.2.2014 Kilpirauhasvasta-aineet - Tyreoideaperoksidaasi (TPO), vasta-aineet - Tyreoglobuliini (Tygl), vasta-aineet
Kilpirauhasvasta-aineet: milloin määritys on tarpeen? Dosentti, oyl Anna-Maija Haapala 7.2.2014 Kilpirauhasvasta-aineet - Tyreoideaperoksidaasi (TPO), vasta-aineet - Tyreoglobuliini (Tygl), vasta-aineet
Liite I. Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle
 Liite I Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle Tieteelliset johtopäätökset Kun otetaan huomioon lääketurvallisuuden riskinarviointikomitean (PRACin) arviointiraportti
Liite I Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle Tieteelliset johtopäätökset Kun otetaan huomioon lääketurvallisuuden riskinarviointikomitean (PRACin) arviointiraportti
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
Miten tehostan sepelvaltimotaudin lääkehoitoa?
 Miten tehostan sepelvaltimotaudin lääkehoitoa? Dosentti, kardiologi Erkki Ilveskoski Yleislääkäripäivät 27.11.2015 1 Sidonnaisuudet Luennoitsija ja/tai muut asiantuntijatehtävät St. Jude Medical, Novartis,
Miten tehostan sepelvaltimotaudin lääkehoitoa? Dosentti, kardiologi Erkki Ilveskoski Yleislääkäripäivät 27.11.2015 1 Sidonnaisuudet Luennoitsija ja/tai muut asiantuntijatehtävät St. Jude Medical, Novartis,
bukkaalinen fentanyylitabletti Effentora_ohjeet annostitrausta varten opas 6.indd :04:58
 10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
10 10 9 8 7 6 5 4 3 2 1 0 Yksilöllisesti sopiva annos jokaiselle syövän läpilyöntikivuista kärsivälle potilaalle: Viisi Effentora - vahvuutta mahdollistavat yksilöllisen läpilyöntikipujen hoidon Ohjeet
LIITE III. Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin
 HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
Hyponatremian uudet lääkehoidot
 Helsingin ja Uudenmaan sairaanhoitopiiri Na + H 2 O Hyponatremian uudet lääkehoidot Timo Sane HYKS, Endokrinologian klinikka Sisätautilääkäripäivät 23.11.2012 Sidonnaisuudet 2010-2012: luentopalkkiot (Novo
Helsingin ja Uudenmaan sairaanhoitopiiri Na + H 2 O Hyponatremian uudet lääkehoidot Timo Sane HYKS, Endokrinologian klinikka Sisätautilääkäripäivät 23.11.2012 Sidonnaisuudet 2010-2012: luentopalkkiot (Novo
Opas Tietoja potilaille
 Opas Tietoja potilaille Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti
Opas Tietoja potilaille Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Kissa: Leikkauksen jälkeisen kivun lievitys kohdun ja munasarjojen poistoleikkauksen sekä pienten pehmytkudoskirurgisten toimenpiteiden jälkeen.
 1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
Perinnöllinen välimerenkuume
 www.printo.it/pediatric-rheumatology/fi/intro Perinnöllinen välimerenkuume 2. DIAGNOOSI JA HOITO 2.1 Miten tauti todetaan? Yleensä taudin määrittelyssä edetään seuraavasti: Kliininen epäily: Perinnöllistä
www.printo.it/pediatric-rheumatology/fi/intro Perinnöllinen välimerenkuume 2. DIAGNOOSI JA HOITO 2.1 Miten tauti todetaan? Yleensä taudin määrittelyssä edetään seuraavasti: Kliininen epäily: Perinnöllistä
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
Clomicalmin tehoa ja turvallisuutta ei ole varmistettu alle 1,25 kg painavilla eikä alle kuuden kuukauden ikäisillä koirilla.
 1. ELÄINLÄÄKKEEN NIMI Clomicalm 5 mg tabletti koiralle Clomicalm 20 mg tabletti koiralle Clomicalm 80 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Jokainen Clomicalm-tabletti sisältää:
1. ELÄINLÄÄKKEEN NIMI Clomicalm 5 mg tabletti koiralle Clomicalm 20 mg tabletti koiralle Clomicalm 80 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Jokainen Clomicalm-tabletti sisältää:
Opas sädehoitoon tulevalle
 Opas sädehoitoon tulevalle Satakunnan keskussairaala Syöpätautien yksikkö / sädehoito 2014 Teksti ja kuvitus: Riitta Kaartinen Pekka Kilpinen Taru Koskinen Syöpätautien yksikkö / sädehoito Satakunnan keskussairaala
Opas sädehoitoon tulevalle Satakunnan keskussairaala Syöpätautien yksikkö / sädehoito 2014 Teksti ja kuvitus: Riitta Kaartinen Pekka Kilpinen Taru Koskinen Syöpätautien yksikkö / sädehoito Satakunnan keskussairaala
Diabetes (sokeritauti)
 Diabetes (sokeritauti) Lääkärikirja Duodecim Pertti Mustajoki, sisätautien erikoislääkäri Diabeteksessa eli sokeritaudissa veren sokerimäärä on liian korkea. Lääkäri tai hoitaja mittaa verensokerin verinäytteestä
Diabetes (sokeritauti) Lääkärikirja Duodecim Pertti Mustajoki, sisätautien erikoislääkäri Diabeteksessa eli sokeritaudissa veren sokerimäärä on liian korkea. Lääkäri tai hoitaja mittaa verensokerin verinäytteestä
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun
 HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun HIV-positivisilla potilailla on suurentunut munuaisten vajaatoiminnan riski, joka edellyttää
HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun HIV-positivisilla potilailla on suurentunut munuaisten vajaatoiminnan riski, joka edellyttää
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Vatsan turvottelun ja lihavuuden endokrinologiset syyt. Juha Alanko, dosentti Sisätautien ja endokrinologian el
 Vatsan turvottelun ja lihavuuden endokrinologiset syyt Juha Alanko, dosentti Sisätautien ja endokrinologian el 30.11.2018 Lihavuus 1) Hypotyreoosi? 2) Hypogonadismi - matala testosteroni? 3) Cushingin
Vatsan turvottelun ja lihavuuden endokrinologiset syyt Juha Alanko, dosentti Sisätautien ja endokrinologian el 30.11.2018 Lihavuus 1) Hypotyreoosi? 2) Hypogonadismi - matala testosteroni? 3) Cushingin
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
XELJANZ-HOITOA SAAVILLE HENKILÖILLE
 FINNISH XELJANZ Tämä esite on tarkoitettu henkilöille, joille lääkäri on määrännyt XELJANZ-valmistetta. Lisätietoja on lääkkeen mukana tulevassa pakkausselosteessa. XELJANZ-HOITOA SAAVILLE HENKILÖILLE
FINNISH XELJANZ Tämä esite on tarkoitettu henkilöille, joille lääkäri on määrännyt XELJANZ-valmistetta. Lisätietoja on lääkkeen mukana tulevassa pakkausselosteessa. XELJANZ-HOITOA SAAVILLE HENKILÖILLE
301111 Mitä tavallinen psykiatri ymmärtää kehitysvammaisen mielenterveysongelmista? Yl juha kemppinen
 301111 Mitä tavallinen psykiatri ymmärtää kehitysvammaisen mielenterveysongelmista? Yl juha kemppinen Vastaus: hyvin vähän Tietoakin on ollut vaikea hankkia, nyt on juuri uusi kirja julkaistu Tavallisimmin
301111 Mitä tavallinen psykiatri ymmärtää kehitysvammaisen mielenterveysongelmista? Yl juha kemppinen Vastaus: hyvin vähän Tietoakin on ollut vaikea hankkia, nyt on juuri uusi kirja julkaistu Tavallisimmin
K&V kasvattajaseminaari 16.10.2005 Marjukka Sarkanen
 An update on the diagnosis of proteinuria in dogs Oct 1, 2003 By: Johanna Frank, DVM, Dipl. ACVIM PLN: Vioittuneet munuaiskeräset (glomerulus) laskevat veren proteiinin (albumiini) virtsaan. Syitä: glomerulonefriitti
An update on the diagnosis of proteinuria in dogs Oct 1, 2003 By: Johanna Frank, DVM, Dipl. ACVIM PLN: Vioittuneet munuaiskeräset (glomerulus) laskevat veren proteiinin (albumiini) virtsaan. Syitä: glomerulonefriitti
Ongelmana sattumalta todettu lisämunuaiskasvain
 Camilla Schalin-Jäntti KATSAUS Ongelmana sattumalta todettu lisämunuaiskasvain Lisämunuaisen insidentaloomalla tarkoitetaan yleensä yli 1 cm:n läpimittaista lisämunuaiskasvainta, joka todetaan sattumalta
Camilla Schalin-Jäntti KATSAUS Ongelmana sattumalta todettu lisämunuaiskasvain Lisämunuaisen insidentaloomalla tarkoitetaan yleensä yli 1 cm:n läpimittaista lisämunuaiskasvainta, joka todetaan sattumalta
Noona osana potilaan syövän hoitoa
 Noona osana potilaan syövän hoitoa Noona lyhyesti Noona on mobiilipalvelu osaksi potilaan syövän hoitoa Noonan avulla Potilas osallistuu aktiivisesti hoitoonsa raportoimalla hoidon aikaisia haittoja. Hän
Noona osana potilaan syövän hoitoa Noona lyhyesti Noona on mobiilipalvelu osaksi potilaan syövän hoitoa Noonan avulla Potilas osallistuu aktiivisesti hoitoonsa raportoimalla hoidon aikaisia haittoja. Hän
Kenelle täsmähoitoja ja millä hinnalla?
 Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Mitä uudet intensiivihoitotutkimukset kertovat meille hyperglykemian hoidosta
 Mitä uudet intensiivihoitotutkimukset kertovat meille hyperglykemian hoidosta Leena Moilanen, dosentti Sisätautien ja endokrinologian erikoislääkäri Sisätautien klinikka KYS Valtakunnallinen diabetespäivä
Mitä uudet intensiivihoitotutkimukset kertovat meille hyperglykemian hoidosta Leena Moilanen, dosentti Sisätautien ja endokrinologian erikoislääkäri Sisätautien klinikka KYS Valtakunnallinen diabetespäivä
Ihotuumorin biopsia vai leikkaushoito
 Ihotuumorin biopsia vai leikkaushoito Tiina Jahkola HYKS Plastiikkakirurgian klinikka Malignit ihokasvaimet - tavalliset insidenssi Suomessa v. 2004 Levyepiteelikarsinooma = okasolusyöpä = ca spinocellulare
Ihotuumorin biopsia vai leikkaushoito Tiina Jahkola HYKS Plastiikkakirurgian klinikka Malignit ihokasvaimet - tavalliset insidenssi Suomessa v. 2004 Levyepiteelikarsinooma = okasolusyöpä = ca spinocellulare
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
VALMISTEYHTEENVETO. Yli 33 kg painavat lapset (noin 11-vuotiaat), alle 50 kg painavat nuoret ja aikuiset:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Farmakoterapeuttinen ryhmä: steroideihin kuulumaton anti-inflammatorinen lääkeaine, ATCvet-koodi QM01AE90
 VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Quadrisol 100 mg/ml oraaligeeli hevosille 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Quadrisol oraaligeeliä sisältää Vaikuttava(t) aine(et) Vedaprofeeni 100
VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Quadrisol 100 mg/ml oraaligeeli hevosille 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Quadrisol oraaligeeliä sisältää Vaikuttava(t) aine(et) Vedaprofeeni 100
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun
 HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun Tärkeitä seikkoja huomioitavaksi: Tarkasta kaikkien potilaiden kreatiniinipuhdistuma ennen
HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun Tärkeitä seikkoja huomioitavaksi: Tarkasta kaikkien potilaiden kreatiniinipuhdistuma ennen
CORTIMENT -LÄÄKITYKSESI
 CORTIMENT -LÄÄKITYKSESI MITÄ CORTIMENT ON?1 Cortiment-tabletit sisältävät lääkeainetta nimeltä budesonidi. Budesonidi kuuluu kortikosteroidien lääkeryhmään. Näitä lääkkeitä käytetään tulehduksen hoitoon.
CORTIMENT -LÄÄKITYKSESI MITÄ CORTIMENT ON?1 Cortiment-tabletit sisältävät lääkeainetta nimeltä budesonidi. Budesonidi kuuluu kortikosteroidien lääkeryhmään. Näitä lääkkeitä käytetään tulehduksen hoitoon.
Kapseli, kova. Kermanvalkoinen/musta liivatekapseli, kapselin vahvuus painettu kuoreen.
 1. ELÄINLÄÄKKEEN NIMI Vetoryl 10 Mg Kapseli, Kova, Koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 kapseli sisältää: Vaikuttava aine: 10 mg Trilostaani Apuaineet: keltainen rautaoksidi (E172) 0.942
1. ELÄINLÄÄKKEEN NIMI Vetoryl 10 Mg Kapseli, Kova, Koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 kapseli sisältää: Vaikuttava aine: 10 mg Trilostaani Apuaineet: keltainen rautaoksidi (E172) 0.942
VALMISTEYHTEENVETO. Aikuiset (myös iäkkäät): Suositeltu annos on 800 mg eli 2 kapselia vuorokaudessa kerta-annoksena kolmen kuukauden ajan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
Syöpäpotilaan luunhoito
 Syöpäpotilaan luunhoito Petteri Hervonen Syöpätautien el, LT Oyl, HYKS Syöpäkeskus 18.4.2018 ja 26.4.2018 Syöpäpotilaan luunhoito Eturauhassyöpäpotilaan luunhoito Hormonaalinen liitännäishoito Levinneen
Syöpäpotilaan luunhoito Petteri Hervonen Syöpätautien el, LT Oyl, HYKS Syöpäkeskus 18.4.2018 ja 26.4.2018 Syöpäpotilaan luunhoito Eturauhassyöpäpotilaan luunhoito Hormonaalinen liitännäishoito Levinneen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Metronidatsoli 0,75 paino-%, 7,5 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
Pioglitazone Actavis
 Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
Kalvopäällysteinen tabletti Vaaleanoranssi, pyöreä, kalvopäällysteinen tabletti, toisella puolella merkintä 50 tai 150 ja toisella valmistajan logo
 1. ELÄINLÄÄKKEEN NIMI MASIVET 50 mg kalvopäällysteinen tabletti koiralle MASIVET 150 mg kalvopäällysteinen tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi kalvopäällysteinen
1. ELÄINLÄÄKKEEN NIMI MASIVET 50 mg kalvopäällysteinen tabletti koiralle MASIVET 150 mg kalvopäällysteinen tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi kalvopäällysteinen
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Zycortal 25 mg/ml injektioneste, depotsuspensio, koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Desoksikortonipivalaatti 25 mg/ml Apuaineet:
LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Zycortal 25 mg/ml injektioneste, depotsuspensio, koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Desoksikortonipivalaatti 25 mg/ml Apuaineet:
Eturauhassyöpä Suomessa
 Eturauhassyöpä Suomessa Insidenssi 4596 uutta tapausta v. 2009 (Suomen yleisin syöpä ja miesten yleisin syöpä) -14774 uutta syöpätapausta vuonna 2009 Kuolleisuus 784 hlöä v. 2009 (miesten toiseksi yleisin
Eturauhassyöpä Suomessa Insidenssi 4596 uutta tapausta v. 2009 (Suomen yleisin syöpä ja miesten yleisin syöpä) -14774 uutta syöpätapausta vuonna 2009 Kuolleisuus 784 hlöä v. 2009 (miesten toiseksi yleisin
Tärkeää tietoa GILENYA -hoidosta
 Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
VALMISTEYHTEENVETO. Valkoinen, pyöreä, kummaltakin puolelta litteä viistoreunainen tabletti, jossa jakouurre toisella puolella.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO. Tabletti. Beige tai vaaleanruskea, soikea tabletti, jossa molemmilla puolilla jakouurre, 11 x 5,5 mm. Tabletti voidaan puolittaa.
 1. ELÄINLÄÄKKEEN NIMI Fortekor vet. 5 mg, tabletti kissoille ja koirille VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: benatsepriilihydrokloridi 5 mg Täydellinen apuaineluettelo,
1. ELÄINLÄÄKKEEN NIMI Fortekor vet. 5 mg, tabletti kissoille ja koirille VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: benatsepriilihydrokloridi 5 mg Täydellinen apuaineluettelo,
IAP Kuopio 27.9.2007. Mesenkymaalisia. kasvaimia iholla, ja vähän v n muuallakin Jyrki Parkkinen ja Tom BöhlingB
 IAP Kuopio 27.9.2007 Mesenkymaalisia kasvaimia iholla, ja vähän v n muuallakin Jyrki Parkkinen ja Tom BöhlingB Pehmytkudoskasvainten patologiaa Valtaosa pehmytkudoskasvaimista benignejä, malignit harvinaisia,
IAP Kuopio 27.9.2007 Mesenkymaalisia kasvaimia iholla, ja vähän v n muuallakin Jyrki Parkkinen ja Tom BöhlingB Pehmytkudoskasvainten patologiaa Valtaosa pehmytkudoskasvaimista benignejä, malignit harvinaisia,
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
