Oligonukleotidisynteesi isossa mittakaavassa
|
|
|
- Laura Saarinen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 ligonukleotidisynteesi isossa mittakaavassa Johanna Äijälä Pro gradu -tutkielma Helsingin yliopisto Kemian laboratorio
2 HELSIGI YLIPIS HELSIGFRS UIVERSIE UIVERSIY F HELSIKI iedekunta/sasto Fakultet/Sektion Faculty/Section Laitos Institution Department Matemaattis-luonnontieteellinen tiedekunta Kemian laitos ekijä Författare Author Johanna Äijälä yön nimi Arbetets titel itle ligonukleotidisynteesi isossa mittakaavassa ppiaine Läroämne Subject Kemia yön laji Arbetets art Level Aika Datum Month and year Sivumäärä Sidoantal umber of pages Pro gradu -tutkielma Elokuu iivistelmä Referat Abstract Lyhyehköjä oligonukleotideja tarvitaan isossa mittakaavassa moneen eri tarkoitukseen kemiallisesta perustutkimuksesta mahdollisten antisense-lääkkeiden tutkimiseen ja valmistukseen. ligonukleotidien voidaan valmistaa monella eri menetelmällä. ämän työn kirjallisuusosio käsittelee oligonukleotidien synteesiä isossa mittakaavassa. Käsittelyn alla on eri kytkentäreaktioita, joilla synteesi voidaan tehdä, synteesin skaalattavuuten vaikuttavia tekijöitä, sekä oligonukleotidisynteesin automatisointia ja puhdistusta. yön kokeellisessa osiossa kuvaillaan lyhyiden oligonukleotidien ison mittakaavan synteesin kehittämistä. ykyään oligonukleotidisynteesi tehdään yleensä kiintokantajan pinnalla automatisoidulla syntetisaattorilla. Markkinoilla on olemassa paljon erilaisia syntetisaattoreita sekä laboratorio- että teollisuustarpeisiin. Syntetisaattoreilla tehtävän synteesin mittakaava on kuitenkin rajallinen. Esimerkiksi oligonukleotidien kemialliseen perustutkimukseen tarvitaan paljon suurempia määriä oligonukleotidia, kuin mitä laboratoriomittakaavan syntetisaattorilla voidaan valmistaan. Lisäksi teollisuusmittakaavan syntetisaattorit eivät voi kasvaa rajattomasti vastaamaan teollisuuden kasvavaa tarvetta. Vaihtoehtoisia mentelmiä oligonukleotidien syntetisoimiseen liuoksessa tai liukoisella kantajalla kehitetään jatkuvasti. Liuoksessa tehtävää synteesiä pyritään helpottamaan muuttamalla synteesiä niin, että reaktioiden välinen puhdistus voidaan tehdä menetelmällä, joka soveltuu paremmin ison mittakaavan synteesiin kuin perinteinen silikakromatografia. oinen lähestymistapa on tehdä synteesi liukoisen kantajan pinnalla, jolloin reaktioiden välinen puhdistus voidaan tehdä saostamalla. ässä on koottu yhteen tähän asti kehitetyt vaihtoehtoiset menetelmät. Uskotaan, että jokin näistä vaihtoehtoisista menetelmistä tulee korvaamaan kiintokantajamenetelmän tulevaisuudessa ison mittakaavan oligonuklotidisynteesissä. Kokeellisessa osiossa kehitettiin menetelmä lyhyiden oligonukleotidien synteesiin isossa mittakaavassa. Kehitetty synteesi hyödyntää H-fosfonaattimenetelmää ja synteesi tehdään liukoisen polyetyleeniglykolikantajan pinnalla. Polyetyleeniglykoli on liukoinen reaktio-olosuhteissa, mutta tuote saadaan helposti saostettua eetterillä reaktioiden välissä. Menetelmää käytettiin -oligonukleotiditrimeerin valmistamiseen. Menetelmä vaikuttaa pienellä jatkokehityksellä hyvin lupaavalta laboratoriossa tehtävään ison mittakaavan oligonukleotidisynteesiin. Avainsanat yckelord Keywords ligonukleotidisynteesi, fosforamidiittimenetelmä, H-fosfonaattimenetelmä, liukoinen kantaja Säilytyspaikka Förvaringställe Where deposited Gradun säilytyspaikka on Helsingin yliopiston digitaaliset aineistot HELDA/ehesis Muita tietoja Övriga uppgifter Additional information I
3 Sisällysluettelo iivistelmä Sisällysluettelo Lyhenneluettelo I II III 1 Kirjallisuusosio Johdanto Kytkentäreaktiot Fosforamidiittimenetelmä H -fosfonaattimenetelmä Fosfotriesterimenetelmä ligonukleotidisynteesin skaalattavuuteen vaikuttavat tekijät ligonukleotidisynteesi kiintokantajan pinnalla ligonukleotidisynteesi liuoksessa ligonukleotidisynteesi liukoiseen kantajaan sidottuna ligonukleotidisynteesin automatisointi Puhdistus ja eristäminen Yhteenveto Kokeellinen osa ulokset ja tulosten tarkastelu Menetelmät Lähteet 56 II
4 Lyhenneluettelo ABI AC ASS β-cd BP-Cl Bz CPG DCA DCE DCI DCM DDD DMPx DMr DA E FH-tauti GE HPLC ibu LCAA-CPG MMr MS MS-spektroskopia MBE BS D S PADS PAGE PEG PEG-PS PivCl PCS PS RA Applied Bosystems, Inc Asetonitriili Alkyl-chain solube support β-syklodekstriini bis-(2-okso-3-oksatsolidinyyli)fosfiinikloridi Bentsoyyliryhmä Controlled Pore Glass Dikloorietikkahappo Dikloorietaani 4,5-disyanoimidatsoli dikloorimetaani Dietyyliditiokarbonaattisulfidi 5 --2,7-dimetyylipiksyyli 4,4 -dimetoksitrityyli Deoksiribonukleiinihappo 5-etyylitio-1H -tetratsoli Familiaarinen hyperkoleserolemia General electric Suuren erotuskyvyn nestekromatografia Isobutyyliryhmä Long-chain alkylamide CPG 4-monometoksitrityyli 1-(mesityylisuofonyyli)-3-nitro-1H -1,2,4-triatsolilla Massaspektroskopia Mmetyyli-tert-butyylieetteri -bromisukkinimidi ptinen tiheys anosuodatus orgaanisesta liuoksesta, rganic Solvent anofiltration fenyyliasetyylidisulfidi Polyakryyliamidigeelielektroforeesi Polyetyleeniglykoli Polyetyleeniglykolin ja polystyreenin kopolymeeri pivaoyylikloridi Product centrifugal oligonucleotide syntthesize polystyreeni Ribonukleiinihappo III
5 RP-HPLC BA CA EA EAA FA HF Mr r UPLC käänteisfaasikromatografia ributyyliamiini rikloorietikkahappo rietyyliamiini rietyyliammoniumasetaatti rifluorietikkahappo etrahydrofuraani 4,4,4 -trimetoksitrityyli rityyli Erittäin suuren erotuskyvyn nestekromatografia, Ultra performance liquid chromatography IV
6 1 Kirjallisuusosio 1.1 Johdanto Lyhyehköjä oligonukleotideja ja niiden muunnoksia tarvitaan moneen eri tarkoitukseen kemiallisesta perustutkimuksesta mahdollisten antisense-lääkkeiden 1,2 tutkimiseen ja valmistamiseen. äihin ja muihin tarkoituksiin oligonukleotideja tarvitaan suhteellisen isossa mittakaavassa sekä laboratorion että teollisuuden tarpeisiin. Antisense-lääkkeet perustuvat teoriaan, jossa sairauksia aiheuttavat geenit tai virukset deaktivoidaan estämällä niiden lähetti-ra:n toimintaa sitomalla siihen vastin-da tai -RA. 3 ällöin tieto ei pääse kulkemaan DA:n ja proteiinien välillä ja geenin toiminta estyy. Valitettavasti käytäntö ei ole yhtä yksinkertaista kuin teoria. Ensinnäkin modifioimattomat DA- ja RA-ketjut eivät ole stabiileja kehossa, vaan ne hajoavat nukleaasientsyymien vaikutuksesta. Ratkaisu tähän on käyttää tiofosfaatteja tai muita modifioituja oligonukleotideja tavallisten oligonukleotidien sijaan. iofosfaattien käyttö on toimiva ratkaisu monessa tilanteessa niiden liukoisuuden ja antisense-aktiivisuuden ansiosta. Kaikki tähän mennessä markkinoille päätyneet antisense-lääkkeet ovat tiofosfaatteja ja myös suuri osa kehitteillä olevista antisense-lääkkeistä ovat tiofosfaatteja. iofosfaattien huonona puolena ovat niiden sivuvaikutukset etenkin hepariinia sitovia kasvutekijöitä kohtaan. oinen vaikeus on saada antisense-lääke selektiivisesti soluun ja sitoutumaan inhibitoitavaan RA:n. Mekanismi, jolla lääke pääsee soluun, ei ole kunnolla tunnettu, ja yleensä tarpeeksi suuri määrä oligonukleotidia ei pääse sisään soluun itsestään. ligonukleotidin kuljettamiseen solun sisälle on kehitetty vektoreita. Ensimmäiset kehitetyt vektorit olivat liposomeja, joiden pinnalle tai sisäpuolelle oligonukleotidit voidaan sitoa. eutraalit tai positiivisesti varatut liposomit pääsevät paljon helpommin solukalvon läpi kuin negatiivisesti varatut oligonukleotidit. Kun vektori on päässyt soluun, liposomiiin lisätyt auttajamolekyylit auttavat oligonukleotidien vapautumista soluun. Kationisia polymeerejä on myös käytetty vektoreina liposomien lisäksi. Mikä tahansa vastinoligonukleotidi ei pysty sitoutumaan lähetti-ra:n. ämä saattaa johtua lähetti-ra:n ympäristöstä ja 3D-rakenteesta, joka estää antisens-lääkkeen pääsemistä tarpeeksi lähelle. ämä vaikeuttaa huomattavasti sopivien antisense-lääkkeiden löytämistä. 3 Kaikista vaikeuksista huolimatta tähän mennessä on kehitetty kaksi markkinoilla olevaa antisense-lääkettä. Vitravene on ensimmäinen markkinoille tullut antisense-lääke. Se hoitaa CMV retinitis nimistä verkkokalvon virustulehdusta. CMV retinitis on AIDS potilailla esiintyvä tauti, joka hoitamattomana johtaa sokeuteen. 4 oinen julkaistu lääke on Kynamoro, joka hoitaa FH-tautia eli familiaarista hyperkolesterolemiaa. FH-tauti on perinöllinen sairaus, joka aiheuttaa korkeaa kolesterolia, joka vuorostaan johtaa sydänsairauksiin. 5 Antsiense-lääkkeet G3139 ja Isis 3521 ovat esimerkkejä 1
7 lupaavista uusista kehitteillä olevista lääkkeistä. G3139:ä tutkitaan mahdolliseksi lääkkeeksi melanooman hoitoon ja Isis 3521:ä tutkitaan keuhkosyövän hoidoksi. 3 ykyään suurin osa oligonukleotideista valmistetaan fosforamidiittimenetelmällä kiintokantajalla käyttäen apuna automatisoituja syntetisaattoreita. 6 Menetelmä ei kuitenkaan ole ideaalinen skaalattavuuden kannalta ja esimerkiksi laboratoriokäyttöön tarkoitetulla syntetisaattorilla parin sadan milligramman oligonukleotidin valmistamiseen tarvitaan kymmeniä toistoja. 7 ämän takia useat tutkimusryhmät ovat kehittämässä vaihtoehtoisia menetelmiä lyhyiden oligonukleotidien valmistamiseen. ässä on käsitelty oligonukleotidien valmistusta isossa mittakaavassa eri menetelmien avulla. 1.2 Kytkentäreaktiot ligonukletidien valmistamiseen käytetään yleisesti kolmea erilaista kytkentäreaktiota. ämä ovat fosforamidiittimenetelmä, H -fosfonaattimenetelmä ja fosfotriesterimenetelmä. Kaikilla menetelmillä on hyvät ja huonot puolensa ja ne sopivat eri tilanteisiin Fosforamidiittimenetelmä Fosforamidiittimenetelmässä käytetään monomeerinä P(III)-hapetusasteella olevaa fosforamidiittia (1) (Kaavio 1). 8 Yleisimmin käytetyssä fosforamidiitissa aminoryhmä on, -diisopropyyliamiini ja fosfiitti on suojattu syanoetyyli- tai metyyliryhmällä (R 1, Kaavio 1). Fosforamidiittimonomeerin 5 -hydroksyyliryhmä suojataan usein trityyliryhmällä (R 2, Kaavio 1). rityylisuojaryhmistä yleisimmin käytetty on 4,4 - dimetoksitrityyli (DMr). 8 R 2 B P R 1 (ipr) 2 1 R 1 = -Me, -CH 2 CH 2 C R 2 = R' C R''' R'' r: R' = R' '= R''' = H MMr: R' = R'' = H; R'' '= Me DMr: R' = H; R'' = R''' = Me Mr: R' = R'' = R''' = Me Kaavio 1: Yleisesti käytetty fosforamidiittimonomeeri 2
8 ligonukleotidisynteesi tehdään toistamalla nelivaiheista reaktiosykliä. Joka sykli pidentää kasvavaa oligonukleotidiaketjua yhdellä nukleotidillä. Synteesisyklin vaiheet ovat 5 -hydroksyyliryhmän:n suojaryhmän irrotus, kytkentäreaktio, asetylointi ja fosfiitin hapetus fosfaatiksi (Kaavio 2). Synteesi voidaan tehdä liuoksessa tai niin, että ensimmäinen monomeeri on sidottu kiintokantajaan kuten CPG:hen (Controlled Pore Glass) eli huokoiseen lasiin. 8,9 DMr B n oistetaan sykli DMr R B n-1 1. Suojaryhmän irrotus 3 % DCA/DCM P C B n-1 H B n-1 R Fosforamidiittimenetelmä R R 4. Hapetus I 2 / H 2 / HF B n-1 3. Asetylointi Ac 2, lutidiini, metyyliimidatsoli, AC DMr B n DMr 2. Kytkentäreaktio P B n H etratsoli AC C P C B n-1 R Kaavio 2: Fosforamidiittimenetelmän synteesisykli Vaihe 1: Suojaryhmän poisto. rityylisuojaryhmä poistetaan kasvavan ketjun 5 -hydroksyyliryhmästä hapon avulla. Depurinaatio, eli adeniinin ja guaniinin irtoaminen sokeriosasta, on myös happokatalysoitu reaktio, mikä täytyy ottaa huomioon suojaryhmäkemiaa suunniteltaessa. Jos synteesissä usein toistuva 5 - hydroksyyliryhmän suojauksen poisto johtaa depurinaatioon, saattaa depurinoidun tuotteen määrä olla huomattava synteesin päätteeksi. Siksi yleisimmin käytetään mahdollisimman happolabiilia trityylisuojausta. Yleisesti käytettyjä happoreagensseja ovat 2 % trikloorietikkahappo (CA) ja 3 % dikloorietikkahappo (DCA) dikloorimetaanissa. 8 Dikloorimetaanin voi myös korvata tolueenilla, jos halutaan välttää kalliiden ja ympäristölle haitallisten kloorattujen liuottimien käyttöä. 10 rityylisuojauksen poistamiseen on myös kehitetty tarkasti optimoitu menetelmä, jossa trityyliryhmä 3
9 irrotetaan etikkahappopuskurin avulla depurinaation minimoimiseksi. 11 Vaihtoehtoisesti 5 -hydroksyylisuojaryhmiksi, erityisesti ison mittakaavan synteesiin, on esitetty helpommin irrotettavaa suojaryhmää kuten 5 --2,7-dimetyylipiksyyli (DMPx), 12 jolloin tarvittu happokäsittely on miedompi. Miedompi happokäsittely vähentää depurinaatiota ja helpottaa happolabiilien modifikaatioiden lisäämistä oligonukleotidiin. 6 Detritylointi on reversiibeli reaktio, joka ei aina mene loppuun asti. 13 ämä ei ole ongelma kiintokantajalla tehtävässä synteesissä, sillä irronnut trityyliryhmä huuhdellaan pois reaktion aikana. Liuoksessa tehtävässä synteesissä tämä saattaa kuitenkin olla ongelma, ja detritylaatio saattaa olla vaikea saattaa loppuun. Poistajan (scavenger) eli yhdisteen, joka deaktivoi vapautuvan trityylikationin, käyttö voi ratkaista tämän ongelman. Poistajana on käytetty esimerkiksi pyrrolia, trietyylisilaania, metanolia ja etanolia. Vaihe 2: Kytkentäreaktio. Synteesisyklin seuraavassa vaiheessa seuraava nukleotidi liitetään kasvavan ketjun 5 -päähän aktivaattorin avulla (Kaavio 3). 6,13 15 Aktivaattorina on perinteisesti käytetty 1H -tetratsolia (2), jolla saadaan aikaan kytkentäreaktio hyvällä saannolla. 1H -tetratsoli on kuitenkin räjähtävä ja se liukenee huonosti asetonitriiliin ja pyridiiniin, joten se on huono valinta ison mittakaavan synteesiin sekä turvallisuuden, että kustannustehokkuuden kannalta. ykyään ison mittakaavan DA-synteesissä 1H -tetratsoli on usein korvattu 4,5-disyanoimidatsolilla (DCI) (3) ja RA-synteesissä 5-etyylitio-1H -tetratsolilla (E) (4). ämä molemmat ovat sekä turvallisempia kuin 1H -tetratsoli että liukenevat paremmin asetonitriiliin. H H C C H S H-tetratsoli 4,5-disyanoimidatsoli (DCI) 5-etyylitio-1H-tetratsoli (E) Kaavio 3: Yleisesti käytössä olevia fosforamidiittimenetelmän aktivaattoreita Vaihe 3: Asetylointi. Kytkentäreaktion jälkeen reagoimattomat 5 - hydroksyyliryhmät deaktivoidaan asetyloimalla. ämä tehdään, koska puhdistuksessa on vaikeaa erottaa oligonukleotideja, joiden pituus eroaa vain muutamalla nukleotidilla. Asetylointi tehdään etikkahapoanhydridillä, -metyyliimidatsolilla ja 2,6-lutidiinilla asetonitriilissä. 6 Vaihe 4: Hapetus. Synteesisyklin viimeisessä vaiheessa epästabiili, hapetusasteella P(III) oleva, fosfiitti hapetetaan stabiilimmaksi P(V)-fosfaatiksi. ämä tehdään yleensä jodilla vesi-pyridiini tai vesi-hf -liuoksessa. 9 4
10 Yllä olevaa synteesisykliä toistetaan, kunnes oligonukleotidiketju on halutun mittainen. Synteesin jälkeen oligonukleotidi eristetään ja puhdistetaan. ligonukleotidi irrotetaan mahdollisesta kantajasta, ja suojaryhmät poistetaan väkevän ammoniakin avulla. Lopuksi tuote puhdistetaan. Fosforotioaati on hyvin tärkeä oligonukleotidimodifikaatio jota käytetään mm. antisense-lääkkeissä. Siinä fosfaatti on korvattu entsymaattisesti stabiilimmalla tiofosfaatilla. äitä oligonukleotideja voidaan valmistaa helposti fosforamidiittimenetelmällä tekemällä hapetus ennen asetylointivaihetta. Rikkihapettimena voidaan käyttää esimerkiksi fenyyliasetyylidisulfidia (PADS) (5) 3-metyylipyridiinin ja AC:n seoksessa (Kaavio 4). 16 DMr B n S S DMr B n P C B n-1 5 1:1 3-metyylipyridiini:AC S P C B n-1 R R Kaavio 4: Sulfonyloidun oligonukleotidin hapetusvaihe Fosforamidiittimenetelmä on paljon käytetty menetelmä oligonukleotidisynteesissä. Menetelmää käytetään erityisen automatisoidussa oligosynteesissä kiintokantajalla, jolloin synteesisyklin saannoksi saadaan monella syntetisaattorilla yli 99 %. Fosforamidiitti on hyvin herkkä vedelle ja se hydrolysoituu helposti. ämän takia fosforamidiittimenetelmä on hyvin hankala tehdä käsin ja saanto on yleensä paljon huonompi kuin automatisoidussa reaktiossa H -fosfonaattimenetelmä H -fosfonaattimenetelmässä monomeerinä käytetään hapetusasteella P(III) olevaa H -fosfonaattia (Kaavio 5), jonka pysyvin tautomeeri (6) on tetraedrinen. 9,17,18 etraedrisen tautomeerin fosforiatomi on elektrofiilinen eikä sillä ole vapaita elektronipareja. ämän ansiosta H -fosfonaatti on paljon stabiilimpi hapetusta ja hydrolysointia kohtaan kuin fosforamidiitti. H -fosfonaatti on kuitenkin varsin reaktiivinen, kun käytetään sopivaa aktivaattoria. 5
11 DMr B DMr B H P - 6 P H Kaavio 5: Yleisesti käytetty H -fosfonaatti H -fosfonaatin stabiilimman rakenteen ansiosta synteesisyklin hapetusvaihetta ei tarvitse toistaa joka synteesisyklin päätteeksi kuten fosforamidiittimenetelmällä, vaan riittää, että hapetus tehdään koko synteesin lopuksi ennen tuotteen eristystä ja puhdistusta. ämä helpottaa ja nopeuttaa synteesiä, sillä synteesisyklissä on vain kolmen vaihetta; 5 -hydroksyyliryhmän suojauksen irrotus, kytkentäreaktio ja asetylointi (Kaavio 6). DMr B n-1 oistetaan sykli R 1. Suojaryhmän irrotus 3 % DCA/DCM B n-1 H-fosfonaattimenetelmä H R B n-1 R 3. Asetylointi Ac 2, lutidiini, metyyliimidatsoli, AC DMr B n DMr 2. Kytkentäreaktio H P PivCl 1:3 pyridiini:ac - B n H P B n-1 R Kaavio 6: H -fosfonaattimenetelmän synteesisykli 6
12 Suojaryhmän poisto. 5 -hydroksyyliryhmän trityylisuojaus irrotetaan kasvavasta ketjusta samalla tavalla kuin yllä on selitetty fosforamidiittimenetelmälle. Cl Cl P Cl Ph P Ph Cl P Cl Br Kaavio 7: avallisia H-fosfonaattimenetelmän aktivaattoreita Kytkentäreaktio. Kytkentäreaktiossa uusi nukleotidi liitetään kasvavaan oligonukleotidiin kytkentäreagenssin avulla. Kondensaatioreaktio tehdään yleensä happokloridilla tai kloorifosfaatilla AC:n ja pyridiinin seoksessa (Kaavio 7). Pivaoyylikloridi (7) on kaikkein eniten käytetty kytkentäreagenssi, mutta myös adamantaanikarboksyylihappokloridia (8), bis-(2-okso-3-oksatsolidinyyli)fosfiinikloridi (BP-Cl) (9), difenyylifosfokloridia (10), 2-kloori-5,5-dimetyyli-1,3,2-dioksafosforinaani-2- oksidia (11) ja -bromisukkinimidi (BS) (12) käytetään. 9,19 21 Asetylointi. Asetylointi tehdään H -fosfonaattimenetelmällä samalla tavalla kuin yllä on selitetty fosforamidiittimenetelmälle. Kun oligonukleotidi on halutun mittainen se hapetetaan ennen, kun tuote puhdistetaan ja eristetään. Hapetus tehdään yleisesti jodilla vesi-pyridiini -liuoksessa. H -fosfonaattimenetelmällä voidaan valmistaa fosfaattimodifoituja oligonukleotideja suorittamalla hapetusvaihe vedettömissä olosuhteissa. Esimerkiksi tiofosfaattioligonukleotidi voidaan valmistaa hapettamalla rikillä pyridiinin ja rikkihiilen seoksessa. 9,22 H -fosfonaattimenetelmä on yleisesti käytetty menetelmä oligonukleotidijen syntetisointiin fosforamidiittimenetelmän rinnalla. H -fosfonaattimenetelmä ei ole yhtä herkkä vedelle kuin fosforamidiittimenetelmä, joten se soveltuu paljon paremmin laboratoriossa käsin tehtävälle oligonukleotidisynteesille. H -fosfonaattimenetelmällä osa ylimäärämonomeeristä on mahdollista saada takaisin. Lisäksi se soveltuu erityisen hyvin RA-synteesiin. 9 H -fosfonaattimenetelmä kytkentäreaktion saanto on yleisesti pienempi kuin automatisoidulla fosforamidiittimenetelmällä 13 7
13 1.2.3 Fosfotriesterimenetelmä Fosfotriesterimenetelmä on ensimmäinen oligonukleotidisynteesissä käytetty menetelmä. 23,24 ykyään sitä käytetään hyvin vähän, sillä H -fosfonaattimenetelmä ja fosforamidiittimenetelmä ovat syrjäyttäneet sen lähes täysin. Joissakin erikoistapauksissa sitä voidaan kuitenkin edelleen käyttää. 7 DMr B P R 2 R 1 R 1 = R 13 C R Cl 14 R 2 = S R CH 3 17 Kaavio 8: Fosfotriesterimenetelmän monomeeri Fosfotriesterimenelmässä monomeereinä käytetään valmiiksi hapetusasteella P(V) olevia nukleotidejä (Kaavio 8). 7,25 ällöin hapetusvaihetta ei tarvita lainkaan. Fosfaatti on suojattava samalla tavalla kuin fosforamidiittimenetelmässä. 2-kloorifenyyli (14) ja syanoetyyli (13) ovat tähän tarkoitukseen käytettyjä suojaryhmiä. Lisäksi fosfaatti aktivoidaan sopivalla ryhmällä kuten 1-hydroksibentsotriatsolilla (15) tai 1- (mesityylisuofonyyli)-3-nitro-1h -1,2,4-triatsolilla (MS) (16). Kytkentäreagenssinä käytetään yleensä 1-metyylimidatsolia (17). Synteesissä toistetaan synteesisykliä vastaavalla tavalla kuin muissakin synteesimenetelmissä. Ensin 5 -hydroksyyliryhmä:n suojaryhmä poistetaan niin kuin aiemmin on kuvattu. Seuraavaksi tehdään kytkentäreaktio liittämällä juuri aktivoitu fosfotriesteri katalyytin avulla kasvavaan ketjuun. Lopuksi tehdään tarvittaessa asetylointi reagoimattomien H-ryhmien deaktivoimiseksi. Kun oligonukleotidi on halutun mittainen, suojaryhmät poistetaan tuotteesta, ja tuote puhdistetaan ja eristetään. Fosfotriesterimenetelmän hyvänä puolena on, että hapetusvaihetta ei tarvitse tehdä lainkaan, sillä reaktio tehdään jo valmiiksi hapetusasteella P(V) olevalla fosforilla. Etenkin manuaalisesti tehtävälle synteesille tämä on hyödyllinen piirre sillä työmäärä vähenee. 7 Lisäksi menetelmä ei ole niin herkkä kosteudelle, ja fosfotriesterit ovat muutenkin suhteellisen stabiileja yhdisteitä. 25 Fosfotriesterimenetelmän kytkentäreaktio on kuitenkin paljon hitaampi kuin muilla menetelmillä ja sen saanto on huomattavasti pienempi. 8
14 1.3 ligonukleotidisynteesin skaalattavuuteen vaikuttavat tekijät Kuten aikaisemmin tekstissä on mainittu, oligonukleotideja voidaan valmistaa kolmella eri tavalla. Synteesin voidaan tehdä joko kiintokantajan pinnalla, liuoksessa tai näiden välimuodolla liukoisella kantajalla. äille menetelmille on olemassa useita eri variaatioita ligonukleotidisynteesi kiintokantajan pinnalla Kiintokantajasynteesi kehitettiin lähes yhtä aikaa sekä polypeptideille että oligonukleotideille. Robert Merrifield kehitti polypeptidisynteesin kiintokantajalla vuonna ja automatisoi sen vuonna Hän sai obelin palkinnon vuonna 1984 näiden keksintöjen ansiosta. ligonukleotidisynteesi kiintokantajalla kehitettiin vuonna 1965, 28 ja nykyään kiintokantajamenetelmä on eniten käytetty menetelmä oligonukleotidisynteesissä. Kiintokantajamenetelmällä synteesi tehdään heterogeenisessä systeemissä, jossa ensimmäinen nukleosidi on kiinnitetty linkkerillä liukenemattomaan kantajaan. Yleisimmin oligonukleotidisynteesissä käytetyt kiintokantajat ovat huokoinen lasi (CPG) tai ristisilloitettu polystyreeni (PS). 29 CPG on mekaanisesti jäykkää ja kestävää materiaalia, jonka huokosissa oligonukleotidisynteesi tapahtuu. Lyhyiden, noin 40 emäksen mittaisten oligonukleotidien valmistukseen käytetään yleensä CPG:tä, jonka huokoskoko on 500 Å. ässä materiaalissa voi olla kiinnitettynä jopa mikromoolia grammassa CPG:tä, mutta µmol/g on tavallisempi määrä. Yleensä suurempi määrä nukleotidia kantajassa vähentää kytkentäreaktion tehokkuutta. Pidempiä oligonukleotidejä varten tarvitaan materiaalia, jossa on isompi huokoskoko. Samalla kuitenkin myös materiaaliin sidotun nukleotidin määrä vähenee huomattavasti. 29,30 Syntetisoitava oligonukleotidi kiinnitetään kiintokantajaan kovalenttisella sidoksella sidostavan atomiryhmittymän välityksellä. Irrotettavaa osuutta sidostavassa ryhmässä kutsutaan linkkeriksi, mutta sen lisäksi voidaan käyttää lisää välimatkaa oligonukleotidin ja kantajan väliin tuovaa ryhmää (engl.: spacer). Ryhmittymä on yleensä alkyylitai alkoksiketju, joka ei suosi laskostunutta konformaatiota. Linkkerillä ja spacerilla on suuri vaikutus kytkentäreaktion tehokkuuteen. CPG kantajalla on suotavaa, että kiintokantajan pinnan ja ensimmäisen nukleotidin välillä on ainakin 25 atomia. 31,32 ligonukleotidisynteesissä useimmiten käytetty linkkeri on dikarboksyylihappo kuten meripihkahappo, 31 mutta on myös olemassa lukuisia muita vaihtoehtoja. 33 Long-chain alkylamide CPG (LCAA-CPG)(Kaavio 9) on esimerkki yleisiesti käytetystä CPGkantajasta. 31 9
15 DMr B H R H Si sukkinyyli linkkeri LCAA-spaceri CPG kantaja Kaavio 9: Yleisesti käytetty LCAA-CPG kantaja Ristisilloitettu polystyreeni on toinen yleisesti käytetty kiintokantaja. 31,34 Sen hyviä ominaisuuksia ovat hydrofobinen pinta, joka auttaa pitämään kosteuden poissa reaktiosta ja sen suurempi pinta-ala, joka mahdollistaa suuremman nukleotidilatauksen. 35 Polystyreenin ristisilloitusaste on tärkeä polystyreenin ominaisuuksiin vaikuttava tekiä. Vain vähän ristisilloitettu polystyreeni ei paisu kunnolla reaktiossa yleisesti käytetyssä asetonitriilissä. Paisuminen on tärkeä tekijä, sillä suurin osa reaktiossa tapahtuu materiaalin sisäisissä huokosissa pinnan sijaan. Jos materiaali ei paisu reagenssit eivät pääse huokosiin ja reaktiota ei tapahdu. ämän takia oligonukleotidisynteesissä suositaan korkean ristisilloitusasteen omaavaa polystyreeniä, jolla on suhteellisen jäykkä rakenne ja isot huokoskoot. Ison huokoskoon ansiosta korkeasti ristisilloitetun polystyreenin ei kuulu paisua, sillä huokoset ovat jo tarpeeksi isoja aivan niin kuin CPG:llä. Kyseisen materiaalin nukleotidilataus ei ole yleensä yhtä hyvä kuin vähemmän ristisilloitetun polystyreenin ja CPG:n lataus. 31 Joitakin korkeasti ladattuja ristisilloitettuja polystyreenikantaja on kuitenkin olemassa. Esimerkiksi GE:llä (General electric) on ison mittakaavan automatisoituun oligonukleotidisynteesiin tarkoitettua divinyylibentsyylillä ristisilloitettua polystyreenikantajaa, jonka nykleotidilataus on 350 µmol/g. 36 Vaihtoehtoisesti polystyreeniin voi lisätä funktionaalisia ryhmiä, jotka vaikuttavat polystyreenin paisumisominaisuuksiin. Esimerkkinä tästä on polyetyleeniglykolin ja polystyreenin kopolymeeri (PEG-PS), jossa polystyreeninä käytetään vain vähän ristisilloitettua polymeeriä. ämä paisuvat hyvin myös asetonitriilissä ja toimivat täten hyvin oligonukleotidisynteesissä, mutta samalla hydrofobisuus vähennee. 31,34 entageeli on tällainen polymeeri, jonka nukleotidilataus voi olla esimerkiksi 190 µmol/g eli paljon suurempi kuin esimerkiksi CPG:llä. 35,37 ligonukleotidisynteesi kiintokantajalla voidaan tehdä sekä käsin että automatisoidusti. Käsin kiintokantajasyntesiä voidaan tehdä vain mikromoolien mittakaavassa. ällöin kantaja, johon on kiinnitetty ensimmäinen nukleosidi, punnitaan pieneen kolonniin, jonka päihin liitetään ruiskut liuotinvirtauksen aikaansaamiseksi. Menetelmä tarvitsee hyvin suuria reagenssiylimääriä hyvän kytkentäreaktion varmistamiseksi. Reaktioiden välinen puhdistus saadaan helposti aikaan huuhtelemalla kantajaa ase- 10
16 tonitriilillä. Menetelmällä on suhteellisen helppo tehdä referenssioligonukleotidi, tai muuten hyvin pieniä määriä oligonukleotidia. Automatisoitu kiintokantajamenetelmä on nykyään eniten käytetty menetelmä. Sillä on helppo valmistaa korkealaatuisia monomeerejä hyvällä saannolla. Automatisoituja oligonukleotidisyntetisaattoreita on sekä pieniä laboratoriomittakaavan koneita, että suuria teollisuusmittakaavan koneita. GE:n ligoprocess on yksi suurin markkinoilla oleva oligonukleotidisyntetisaattori, jolla voidaan valmistaa jopa 5 moolia oligonukleotidia kerralla. 38 Kiintokantajamenetelmän paras ominaisuus on, että reaktioiden välinen puhdistus helpottuu huomattavasti. Riittää, että ylimääräreagenssit huuhdellaan pois reaktiokolonnista esimerkiksi asetonitriilillä reaktioiden välillä, eikä muuta puhdistusta kuten kromatografiaa tarvita. 31 Lisäksi kiintokantajamenetelmä on mahdollista automatisoida, jonka ansiosta synteesin työmäärä ja inhimilliset virheet saadaan minimoitua. Kiintokantajamenetelmän vaatimuksena on, että kytkentäreaktioiden saannot ovat yli 98 %. Jos kytkentäreaktion saanto on liian pieni, kokonaissaanto pienenee hyvin nopeasti reaktion edetessä, kuten oheisessa kuvaajassa on osoitettu (Kuva 1). 31 ämä on erittäin tärkeää kiintokantajalla tehtävässä synteesissä, sillä reagoimattomia oligonukleotideja ei voida poistaa reaktion aikana, joten jos synteesisyklin saanto on hyvin pieni, synteesin loppupäässä systeemissä on vain hyvin pieni osuus reagoivaa oligonukleotidia. Reagensseja on kuitenkin käytettävä saman verran kuin synteesin alkupäässä, joten synteesin kustannustehokkuus kärsii. nneksi nykyään automatisoidulla oligonukleotidisynteesillä pystytään saamaan aikaan jopa yli 99 % saanto synteesisykliä kohden. 6 Kiintokantajamenetelmän huonoja puolia ovat kiintokantajan korkea hinta, kiintokantajan kertakäyttöisyys ja kiintokantajamenetelmässä usein tarvittavat suuret reagenssiylimäärät. 31 sa näistä ongelmista on saatu ratkaistua. Esimerkiksi ison mittakaavan oligonukleotidisyntetisaattoreilla yli 99 % kytkentäreaktiosaanto voidaan saada käyttämällä vain 1.5 ekv:n nukleotidiylimäärää. 6 Lisäksi on kehitetty monikäyttöisiä kiintokantajia
17 Kuva 1: Kytkentäreaktion saannon vaikutus kokonaissaantoon 31 Kiintokantajamenetelmän käytettävyydellä ison mittakaavan oligonukleotidisynteesissä on rajansa. oisaalta koneet eivät voi kasvaa rajattomasti ja toisaalta laboratoriomittakaavan koneet tarvitsevat kymmeniä toistoja, jotta saadaan parisataa grammaa oligonukleotidia. 7 Jos esimerkiksi antisense-lääkeaineet yleistyvät, oligonukleotidejä tullaan tarvitsemaan useamman kilon mittakaavassa. ätä varten olisi hyvä olla jokin muu paremmin sekä laboratoriossa, että teollisuudessa skaalattavissa oleva menetelmä, jolla oligonukleotideja valmistetaan ligonukleotidisynteesi liuoksessa ligonukleotidisynteesin liuoksessa on alkuperäinen tapa tehdä oligonukleotidisynteesiä. Liuossynteesissä ensimmäisen monomeerin 3 -hydroksyyliryhmä suojataan sopivalla suojaryhmällä, kuten levulinyylillä, ja reaktio tehdään täysin liuoksessa. Menetelmän suurin heikkous on työläät reaktioiden väliset puhdistukset. Perinteisellä liuoksessa tapahtuvassa oligonukleotidisynteesissä välituote puhdistetaan reaktioiden välillä kromatograafisesti, joka on hyvin työläs ja hidas puhdistusmenetelmä. Kromatografiapuhdistus ei sovellu suuren mittakaavan synteesiin, jonka lisäksi tuotehävikki ja oligonukleotidin mahdollinen hajoaminen puhdistuksen aikana ovat ongelmia. Menetelmä soveltuu vain lyhyiden oligonukleotidien valmistukseen. Liuossynteesin vahvuus on liuoksessa tehtävän reaktion helppo skaalattavuus
18 Liuossynteesiä on pyritty helpottamaan suojaamalla oligonukleotidi rasvaliukoisilla suojaryhmillä, jolloin kromatografiapuhdistus voidaan korvata uutoilla (Kaavio 10). 41,42 Menetelmässä 3 -hydroksyyliryhmä suojattiin adamanttaaniasetyyliryhmällä, adeniini ja sytosiini suojattiin bentsoyyliryhmällä (Bz), guaniini suojattiin isobutyyliryhmällä (ibu), tymidiinin 3 suojattiin pivaloyylioksimetyylillä ja synteesi tehtiin fosforamidiittimenetelmällä. Synteesi koostui kahdesta vaiheesta. Ensimmäinen vaihe koostuu kytkentäreaktiosta DCI:lla, ylimääräisen fosforamidiitin hydrolysoinnista lisäämällä vettä, muodostuneen H -fosfonaattimonomeerin ja oligonukleotidin hapetuksesta jodilla HF/pyridiini -liuoksessa, ja ensimmäisestä uuttokäsittelystä. HF/pyridiini-liuos laimennettiin EtAC:lla, minkä jälkeen se uutettiin 1 M a 2 S 2 3 :lla jodin poistamiseksi, 10 % KHS 4 :lla pyridiinin ja diisopropyyliamiinin poistamiseksi ja 10 % ahc 3 :lla DCI:n poistamiseksi. 41 oisessa vaiheessa DMr-suojaryhmä poistettiin käyttäen 0.1 M HCl:a 6:1 MeH/AC-liuoksessa, jonka jälkeen happo neutraloitiin käyttäen ekvimolaarista määrää trietyyliammoniumasetaattin vesiliuosta (EAA). DMrMe poistettiin uuttamalla 2:1 heptaani/dietyylieetteri-liuoksella, jonka jälkeen seokseen lisättiin EtAc:a ja vettä. Syntynyt orgaaninen faasi pestiin vedellä ja uutettiin 10 % ahc 3 :lla ylimääräisen H -fosfonaattimonomeerin poistamiseksi. 41 Menetelmää käytettiin heksameerin valmistukseen. Suojatun heksameerin saanto oli 78 %, joka vastaa noin 92.4 % saantoa synteesisykliä kohden. Suojaamattoman ja puhdistetun oligonukleotidin saanto oli 31 %. 41 Ilmoitettu saanto on todella hyvä liuossynteesille. Lisäksi synteesi ei vaikuta kovin työläältä ja vaikuttaa sopivan hyvin laboratorion isoon mittakaavaan. eollisuusmittakaavassa uuttaminen ei ole paras mahdollinen puhdistustapa, mutta se on huomattavasti helpompi ja nopeampi menetelmä kuin silikakromatografia
19 B H P - B n 1. Kytkentäreaktio 2. Hydrolyysi 3. Hapetus 4. Puhdistus uuttamalla DMr P B n C B Kytkentäreagenssi ja sivutuoteet DMr P - B n+1 DMr B n P H 5. Detritylointi 6. Puhdistus uuttamalla C B H P - B n+1 H B n P H C DMrMe Kaavio 10: Uuttoa hyödyntävä oligonukleotidisynteesi liuoksessa 41 Yllä kuvattua menetelmää on myös käytetty tiofosfaattioligonukleotidien valmistukseen. 42 ällöin hapetusvaiheessa käytetään rikkihapetinta ja ensimmäisen uuton a 2 S 2 3 on vaihdettu vedeksi hapetusvaiheessa syntyneiden vesiliukoisten happojen poistamiseksi. Rikkihapettimena käytettiin yhdistettä (18) H -fosfonaatin hapettamiseen ja PADS:a (5) forsforamidiitin hapettamiseen (Kaavio 11). ällä menetelmällä valmistettiin suojattu heksameeri 78 % saannolla ja puhdistettu tiofosfaattiheksameeri 39 % saannolla. iofosfaattioligonukleotidit ovat lääketieteellisesti tärkeitä, joten on hyvä, että menetelmää voidaan myös käyttää näiden valmistukseen S S S S 5 Kaavio 11: Uuttopuhdistusta hyödyntävän liuossynteesin rikkiä sisältävät hapettimet 42 14
20 Reaktioiden välistä puhdistus voidaan yksinkertaistaa käyttäen nanosuodatusta orgaanisesta liuottimesta (S). 43 Menetelmässä käytetään kalvoa, jonka huokoskoko on nanometriluokkaa. Menetelmä perustuu siihen, että ylimääräreagenssit ja sivutuotteet ovat paljon pienempiä kuin oligonukleotidi, joten ne suodattuvat kalvon läpi kun taas välituote pysyy liuoksessa. arkoitukseen sopiva kalvo voidaan valmistaa poly(bentsimidatsolista) ja ristisilloitetusta para-dibromiksyleenistä (Kuva 2). 43 Kytkentäreakrio ja hapetus Suodatusvaihe Paine Kasvava nukleotidi Kasvava nukleotidi Fosforamidiittimonomeeri Fosforamidiittimonomeeri Aktivaattori sitten hapetin Suodatusvaihe Synteesisykli S kalvo Aktivaattori Hapetin Suojaryhmän irrotus Paine Kasvava nukleotidi S kalvo Happo Suojaamaton Fosforamidiittimonomeeri Kasvava nukleotidi Suojaamaton Fosforamidiittimonomeeri Happo Irronnut suojaryhmä Kuva 2: S-puhdistusta hyödyntävä synteesisykli 43 anosuodatusta käyttävässä menetelmässä kolme aloitusmonomeeria kiinnitettiin kantajaa muistuttavaan symmetriseen homostar-polymeeriin (19) (Kaavio 12). Monisakaraista kantajaa käytettiin, jotta kasvava oligonukleotidi olisi jo yhden kytkentäreaktion jälkeen paljon isompi kuin muut liuoksessa olevat komponentit ja täten nanosuodatus orgaanisesta liuottimesta toimisi paremmin. Menetelmällä valmistettiin 9 nukleotidin mittainen RA-tiofosfaatti fosforiamidiittikemialla käyttäen aktivaattorina E:tä (4), hapettimena PADS:a (5) ja DMr-suojaus irrotukseen DCA:a ja pyrrolipoistajalla. anosuodatus orgaanisesta liuottimesta tehtiin hapetusvaiheen ja detritylointivaiheen jälkeen. Synteesisyklin saanto ei ollut kovin hyvä synteesin alkuvaiheessa, sillä suojatun kantajaan kiinnitetyn tetrameerinukleotidin saanto oli vain 52 %. ämä arvioitiin johtuvan tuotehävikistä nanosuodatuksen aikana synteesin alkuvaiheessa. 43 Synteesisyklin saanto kuitenkin parani oligonukleotidin pidentyessä, jonka ansiosta kantajaan kiinnitetyn 9-merin saanto monomeeristä oli 15
21 39 %. 43 Saantojen perusteella näyttää siltä, että menetelmä soveltuisi parhaiten suhteellisen pitkien oligonukleotidien valmistamiseen, mutta siitä huolimatta saanto ei ole sellaisenaan tarpeeksi hyvä taloudelliseen ison mittakaavan synteesiin. Menetelmän kehittäjät kuitenkin arvioivat, että saantoa voidaan parantaa huomattavasti kehittämällä suodatusmenetelmää. 43 Menetelmä vaikuttaa lupaavalta teollisuusmittakaavan oligonukleotidisynteesiin tulevaisuudessa, jos saantoon vaikuttavat ongelmat saadaan ratkaistua. H 8 H 8 H DMr B 3 Kaavio 12: S -menetelmässä käytetty homostar-yhdiste (20) ja siitä valmistettu aloitusmonomeeri (21) oinen lähestymistapa liuoksessa tehtävän oligonukleotidisynteesin helpottamiseksi on reagenssien, kuten aktivaattorin, kiinnittäminen kantajaan, jolloin aktivaattorista päästään eroon suodattamalla ja kasvava oligonukleotidi voidaan eristää suodoksesta. Lähestymistapaa on kokeiltu H -fosfonaattimenetelmällä käyttäen aktivaattorina polymeeriin kiinnitettyä yhdistettä 22 (Kaavio 13). Menetelmällä valmistettiin eristetty dimeerejä % saannolla. 44 Synteesin saanto vaikuttaa melko pieneltä ja se ei ratkaise reagoimattoman H -fosfonaattimonomeerin poistamista reaktioseoksesta muulla kuin silikan läpi suodattamalla, jonka takia menetelmä ei vaikuta kovin lupaavalta pitkien oligonukleotidien valmistamiseen. Menetelmä saattaisi kuitenkin soveltua lyhyiden oligonukleotidien valmistukseen laboratoriossa isossa mittakaavassa. DMr H H P - B 1 B 2 H 22 Cl P DMr H P B 1 B 2 Kaavio 13: Kantajaan kiinnitetyn aktivaattorin käyttö oligonukleotidisynteesissä 16
22 Liuoksessa tehtävä oligonukleotidisynteesi on mahdollista tehdä myös käyttäen blokkikytkentää yksittäisten monomeerien liittämisen sijaan, jolloin oligonukleotidiketjua kasvatetaan useamman nukleotidin palalla kerrallaan. 4 Menetelmän hyvänä puolena on esimerkiksi, että ei synny oligonukleotideja, joiden pituus on n-1 halutusta oligonukleotidistä, jolloin puhdistus helpottuu. Lisäksi menetelmä vähentää tarvittavien kytkentäreaktioiden määrää etenkin jos samaa blokkia voidaan käyttää useammassa kohtaa synteesiä. ätä menetelmää on ehdotettu esimerkiksi olemassa olevan antisense-lääkkeen Vitravene syntetisointiin ligonukleotidisynteesi liukoiseen kantajaan sidottuna ligonukleotidisynteesi liukoisella kantajalla on yllä käsiteltyjen kiintokantajamenetelmän ja liuosmenetelmän välimuoto. ällöin ensimmäinen monomeeri on sidottu kantajaan, joka on liukoinen reaktio-olosuhteissa, mutta helposti saostettavissa jollakin muulla liuottimella. 13,40 Synteesi liukoisella kantajalla yhdistää sekä kiintokantajamenetelmän, että liuoksessa tehtävän synteesin hyviä puolia. Synteesi liukoisella kantajalla on paljon helpommin muutettavissa isoon mittakaavaan kuin kiintokantajalla tehty synteesi ja reaktioiden välinen puhdistus on helpompi ja nopeampi kuin liuoksessa suoritettu synteesi. Synteesi liukoisella kantajalla on hyvin lupaava menetelmä etenkin laboratoriossa suoritettavaan ison mittakaavan oligonukleotidisynteesiin. 13,40 Polyetyleeniglykoli (PEG) on yksi eniten tutkituista liukoisista kantajista, jota on käytetty fosfotriesterimenetelmässä, fosforamidiittimenetelmässä ja H - fosfonaattimenetelmässä sekä DA:n että DA-tiofosfaattien valmistukseen. 19,45 51 Se on hyvin liukoinen asetonitriiliin ja dikloorimetaaniin, jotka ovat oligonukleotidisynteesissä yleisesti käytettyjä liuottimia, mutta se saostuu helposti eetteristä. ligonukleotidisynteesissä käytetään DA:n PEG:a, johon ensimmäinen nukleotidi kiinnitetään sukkinyylilinkkerin avulla (Kaavio 14). PEG:iin voidaan kiinnittää jopa 200 µmol oligonukleotidia grammaa kantajaa kohden, mutta määrä riippuu hyvin paljon käytetyn PEG:n moolimassasta. Käytetyn PEG:n moolimassa tulee valita syntetisoitavan oligonukleotidin pituuden mukaan. Pienemmälle PEG:lle voidaan kiinniittää enemmän nukleotidia grammaa kohden, mutta pidempi oligonukleotidi tarvitsee suuremman PEG:n, jotta se saostuu kunnolla. Esimerkiksi eräässä tutkimuksessa 5000 DA:n PEG:a käytettiin kahdeksan nukleosidin mittaisen fosfotioaattioligonukleotidin valmistukseen ja DA:n PEG 15 nukleosidin mittaisen fosfotioaattioligonukleotidin valmistukseen. 48 Synteesi tehtiin fosforamidiittimenetelmällä käyttäen aktivaattorina tetratsolia ja rikkiä sisältävänä hapettimena dietyyliditiokarbonaattidisulfidia (DDD). Kahdeksan nukleotidin mittaisen fosforotioaattioligonukleotidin saanto oli 90 %, joka vastaa 96.5 % synteesisykliä kohden ja 15 17
23 nukleotidin mittaisen fosfotioaattioligonukleotidin saanto oli 58 %, joka vastaa 92.5 % synteesisykliä kohden. utkijat selittävät pidemmän oligonukleotidin pienempää saantoa esimerkiksi pitkän oligonukleotidiketjun heikommalla reaktiivisuuudella 48. Ilmoitettu saanto on erittäin hyvä liuoksessa tehtävälle synteesille. DMr B 2 MPEG = MPEG H 3 C H n Kaavio 14: PEG:n kiinnitetty aloitusmonomeeri sukkinyylilinkkerillä ligonukleotidien ja fosforotioaattien valmistamiseen fosforamidiittimenetelmällä PEG-kantajalla on olemassa melko standardoitu menetelmä 50 (Kaavio 15). Synteesi voidaan tehdä joko lisäämällä yksi nukleotidi kerrallaan tai käyttämällä blokkikytkentää. Blokkikytkentämenetelmällä synteesin saanto on hiukan suurempi, sillä synteesisykejä on huomattavasti vähemmän ja tällöin myös eniten hävikkiä aiheuttavia saostuksia on huomattavasti vähemmän. Synteesisykli aloitetaan detrityloinnilla käyttäen 6 % CA:ta dikloorietaanissa (DCE), jonka jälkeen tuote saostetaan metyyli-tert-butyylieetterillä (MBE). Detritylaatio toistetaan täydellisen detrityloinnin varmistamiseksi. Seuraavaksi tehdään kytkentäreaktio käyttäen aktivaattorina tetratsolia ja liuottimena asetonitriiliä. Kytkentäreaktiossa käytetään suurehkoa 3 ekv fosforamidiittiylimäärää hyvän saannon varmistamiseksi. Kytkentäreaktion jälkeen tuote saostetaan. Seuraavaksi hapetus tehdään käyttäen reagenssina DDD:tä asetonitriilissä. ämän vaiheen jälkeen saostus tehdään kaksi kertaa puhtaamman tuotteen varmistamiseksi. Lopuksi tuote asetyloidaan
24 DMr P B n DMr 1. Kytkentäreaktio C 1H-etratsoli, AC, 5-10 min B n DMr 2. Sulfonylointi 0.5 M DDD, AC, 15 min P C B n-1 B n P C B n-1 toista sykli n = n+1 S C P DA MPEG 3' 5' S C P DA MPEG 3' 5' suojausten irrotus H B n 4. Detritylaatio 6 % CA, DCE 30 min 0 o C 3. Asetylointi Ac 2 / 2,6 -lutidiini/mi MeC, 3 min P C B n-1 Ac B n-1 S C P DA MPEG 3' 5' S C P DA MPEG 3' 5' Kaavio 15: ligonukleotidisynteesi käyttäen PEG:a liukoisena kantajana PEG:a on käytetty myös hapettavalla H -fosfonaattimenetelmällä 10 nukleotidin mittaisen oligonukleotidin valmistamiseen. Synteesi tehtiin hyvin samalla tavalla kuin yllä kuvattu synteesi fosforamidittimenetelmälle, paitsi että hapetus tehtiin koko synteesin lopuksi. BS 1:5 AC:EA-liuoksessa todettiin olevan parhaiten toimiva yhdistelmä kytkentäreaktiolle. Kytkentäreaktiossa käytettiin 2,5 ekv H -fosfonaattimonomeeriä. uotteen saanto oli 75 %, joka vastaa noin 96.8 % saantoa synteesisiykliä kohden. 19 Saanto on erinomainen liuoksessa tehtävälle H -fosfonaattisynteesille. H -fosfonaattimenetelmän etuna on lyhyempi synteesisykli, minkä ansiosta tarvitaan vähemmän saostuksia, jotka vievät aikaa ja joissa tulee tuotehävikkiä. Yllä kuvatut menetelmät oligonukleotidisynteesiin liukoisella PEG-kantajalla vaikuttavat hyvin lupaavilta ison mittakaavan synteesiin. Synteesin pitäisi olla helppo tehdä suuressa mittakaavassa, koska reaktio tapahtuu liuoksessa ja sillä on hyvä saanto. Haittapuolena on esimerkiksi tarvittavien saostusten määrä, saostuksessa tarvittavat suuret liuotintilavuudet ja pidempien oligonukleotidien reaktiivisuuden väheneminen. 50 Liuottimet pitäisi olla mahdollista kierrättää, mikä vuorostaan tekee reaktiosta kustannustehokkaamman. 50 Mahdollinen parannus synteesille olisi vaihtaa DMr-suojaus johonkin muuhun suojaryhmään, joka voidaan irrottaa kvantitatiiviseesti yhdellä käsittelyllä. ämä poistaisi yhden vaiheen synteesisyklistä ja täten 19
25 vähentäisi työmäärää ja parantaisi saantoa. oinen mahdollinen kantajatyyppi on ASS (alkyl-chain solube support) (Kaavio 16). 52 ässä menetelmässä käytetään liukoisena kantajana 3,4,5- tris(oktadekyylioksi)bentsoyyliä (23) sisältävää yhdistettä (24), joka liukenee mm. asetonitriiliin ja dikloorimetaaniin mutta ei metanoliin, josta se voidaan saostaa hyvällä saannolla sen suuren hydrofobisuuden ansiosta. Menetelmällä valmistettiin 21 nuklotidin mittainen RA käyttäen fosforamidiittikemiaa. Synteesin raakatuotteen saanto oli 78 %, joka vastaa 98 % saantoa synteesisykliä kohden ja eristetyn tuotteen saanto oli 26 %. Saanto on hyvä pitkien oligonukleotidien valmistukseen. 52 C 18 H 37 C 18 H 37 C 18 H B DMr DMr C 18 H 37 C 18 H 37 C 18 H ASS Z-ACSS B Kaavio 16: Alkyyliketju -liukoinen kantaja menetelmässä käytetyt kantajat ASS 52 ja sen variaatio Z-ACSS. 53 ASS-tyyppistä kantajaa on myös esitetty blokkikytkentää varten tarvittavien lyhyiden suojattujen DA- ja RA-oligonukleotidien valmistukseen. ASS-kantajan muunnos Z-ACSS (25) soveltuu tähän hyvin, sillä valmis oligonukleotidi voidaan irrottaa kantajasta selektiivisesti palladiumkatalysoidulla vedytyksellä ilman, että suojaryhmät irtoavat. 53 Blokkikytkentä on hyvä tapa vähentämään pitkien oligonukleotidien synteesin työmäärää ja parantamaan synteesin saantoa. Esitetyllä menetelmällä on suhteellisen helppo valmistaa isossa mittakaavassa blokkikytkentään tarvittavat rakennuspalat. Yllä esitelty menetelmä vaikuttaa saannon ja työmäärän perusteella hyvältä kilpailijalta PEG:n pinnalla tapahtuvaan DA- ja RA-synteesiin. Halvan β-syklodekstriinin (β-cd) käyttöä liukoisena kantajana on myös tutkittu. 13,54 β-cd:n ajateltiin soveltuvan hyvin oligonukleotidisynteesiin ja mahdollistavan puhdistuksen nanosuodatuksella. β-cd osoittautui kuitenkin hyvin hankalakäyttöiseksi. Kaikki ylimääräiset H-ryhmät on pidettävä suojattuna koko synteesin ajan, ja vain yhden oligonukleotidin liittäminen kantajaan osoittautui hankalaksi. Kantajalla valmistettiin trimeeri fosforamidiittimenetelmällä 85 % saannolla, mikä vastaa 92 % saantoa synteesisyklissä. Synteesissä oli ongelmana mm. se, että DMr-suojauksen irrottaminen osoittautui hankalaksi. Lisäksi detritylointi oli hyvin vaikea saada mene- 20
26 mään loppuun asti. ästä johtuen DMr-suojaus vaihdettiin 1-metoksi-isopropyyliksi (Kaavio 17), joka irrotettaessa laimealla HCl:lla MeH:n ja dioksaanin seoksessa hajoaa asetoniksi ja asetonin dimetyyliasetaaliksi. Suojaryhmän toimivuutta kokeiltiin valmistamalla trimeeri β-cd:llä samalla tavalla kuin aiemmin. rimeerin saanto oli uudella suojaryhmällä 87 % eli hiukan parempi kuin DMr:ä hyödyntävän reaktion saanto. β-cd:n käyttö ei tuottanut toivottavaa tulosta. Synteesi tarvitsi toimiakseen silikakromatografiapuhdistuksen, joka on turhan työläs oligonukleotidisynteesiin. 13,54 Koska yllä käsitelty β-cd ei tuottanut toivottua tulosta, kantaja vaihdettiin tetrapodaaliseksi tetraakis--(4-atsidometyylifenyyli)-pentaerytritoliksi (26), jonka toivottiin toimivan sekä nanosuodatuspuhdistuksella että saostuksella. Kantajaan voidaan kiinnittää 4 oligonukleotidimonomeeriä 27 (Kaavio 17), ja se saostuu metanolista. Kantajalla valmistettiin DA-trimeeri ja -pentameeri käyttäen fosforamidiittimenetelmää. rimeerin saanto oli %, mikä vastaa noin % saantoa synteesisykliä kohden, ja pentameerin saanto oli 43 %, joka vastaa 81 % saantoa synteesisykliä kohden. 13,55 Pidemmän oligonukleotidiketjun huonompi saanto viittaa siihen, että saostus ei ehkä toimi oligonukleotiden kasvaessa. Metanolisaostuksen on havaittu myös muissa tutkimuksissa toimivan epäluotettavasti. oisaalta näissä tapauksissa tuote on pystytty saostamaan etterillä, mutta tällöin ei saavuteta kaikkia metanolisaostuksen etuja tuotteen puhdistuksen kannalta, sillä myös osa reagensseistä saostuu eetterillä B Kaavio 17: etraakis--(4-atsidometyylifenyyli)-pentaeritritoli (26) ja siitä valmistettu aloitusmonomeeri (27). 57 Kantajaa käytettiin myös vastaavan RA-pentameerin valmistukseen fosforamidiittimenetelmällä. ässä 5 -hydroksyyliryhmän suojauksena käytettiin 1-metoksiisopropyyliä, mutta muuten synteesi tehtiin hyvin samalla tavalla kuin yllä oleva synteesi. RA-pentameerin saanto oli 54 %, joka vastaa 86 % saantoa synteesisykliä kohden. ulos osoittaa että DMr:n korvaaminen helpommin irrotettavalla suojaryhmällä parantaa saantoa. 13,57,58 Kantajaa on näiden lisäksi myös käytetty fosfotriesterin kanssa. 7 21
27 Yllä kuvattujen synteesien saannot eivät ole yhtä hyviä kuin esimerkiksi PEGja ASS-kantajaa hyödyntävät synteesi. Lisäksi vaikuttaa siltä, että saostuspuhdistus ei toimi yhtä hyvin pitkille oligonukleotideille kuin yllä mainittu menetelmä. oisaalta samaa kantajaa tutkitaan käytettävän S-puhdistuksen yhteydessä. ästä tutkimuksesta ei kuitenkaan vielä löydy kovinkaan paljon tietoa. Kuten aiemmin todettiin, S toimii paremmin pidemmille oligonukleotideille. ätä kantajaa voisi ehkä olla mahdollista käyttää niin, että muutama ensimmäinen synteesisykli tehdään käyttämällä saostuspuhdistusta ja loput käyttämällä S-puhdistusta. ämä voisi ratkaista S-puhdistuksen huonoa toimivuutta lyhyille oligonukleotideille. Kantajan hyvä puoli on sen korkea oligonukleotidikapasiteetti muihin kantajiin verrattuna, sillä yhteen kantajamolekyyliin voidaan kiinnittää useampi oligonukleotidi toisin kuin esimerkiksi PEG:iin. Kiinnostavaa synteesissä on DMr:n korvaaminen 1-metoksiisopropyylillä. Suojaryhmän käyttö voisi ratkaista muissakin liuoksessa tapahtuvien oligonukleotidisynteesien ongelmat 5 -hydroksyyliryhmän suojaryhmän irrotuksessa. Kyseisellä suojaryhmällä varustettua fosforamidiittia ei kuitenkaan ole vielä saatavilla, joten se on valmistettava itse, mikä lisää toistaiseksi synteesin työmäärää. -metyyliimidatsolista ja 2-bromietanolista valmistettua ioniliuotinta on myös käytetty liukoisena kantajana 59 (Kaavio 18). Kantaja voidaan saostaa 1:9 EtAc:Et 2 -liuoksesta. Sen hyvä puoli on, että se on hyvin pieni (214 g/mol) verrattuna esimerkiksi eniten tutkittuun PEG:iin, minkä ansiosta yhteen grammaan ioniliuotinkantajaa voidaan kiinnittää huomattavasti suurempi määrä oligonukleotidia PEG:iin verrattuna. Menetelmää käytettiin neljän nukleotidin mittaisen oligonukleotidin valmistukseen käyttäen fosforamifiittikemiaa. tetrameerin saanto oli vain noin 54 %, mikä on huomattavasti pienempi kuin aikaisemmin käsiteltyjen menetelmien saanto. Menetelmä tarvitsisi huomattavasti suuremman saannot, jotta sillä voitaisiin valmistaa pitkiä oligonukleotidieja taloudellisesti. Menetelmää on kuitenkin tutkittu hyvin vähän tähän mennessä, joten on hyvin mahdollista, että saantoa saadaan parannettua. Lisäksi ei ole vielä tutkittu, toimiiko saostus myös pitkille oligonukleotideille. H B BF 4 Kaavio 18: Ioniliuotinkantajamenetelmän aloitusmonomeeri. 22
28 1.4 ligonukleotidisynteesin automatisointi Kiintokantajamenetelmän suurin vahvuus on sen helppo automatisointi. Automatisointi vähentää tarvittavan työn määrää, pienentää inhimillisen virheen riskiä, helpottaa reaktion suojaamista vedeltä ja helpottaa optimointia. Markkinoilla on olemmassa paljon erikokoisia ja -merkisiä syntetisaattoreita, jotka käyttävät hyvin erilaisia ratkaisuja tehokkaan synteesin aikaansaamiseksi. Eroa on esimerkiksi reaktioastiassa ja pumppujärjestelmässä. Syntetisaattorin koon kasvattaminen ei ole täysin suoraviivaista eivätkä ratkaisut, jotka toimivat pienessä mittakaavassa, välttämättä toimi suuressa mittakaavassa. Ensimmäinen automatisoitu oligonukleotidisynteesi tehtiin vuona 1977 käyttäen muunneltua peptidisynteesiin tarkoitettua syntetisaattoria. 60 ligonukleotidisynteesiä varten valmistetut synteesisaattorit käyttivät reaktorina HPLC-kolonnia muistuttavaa pakattua kolonnia ja reagenssit pumpattiin kolonnin läpi HPLC-pumpulla (Kuva 3). Vega oli ensimmäinen, joka julkaisi erikseen oligonukleotidisynteesiin tarkoitetun oligonukleotidisyntetisaattorin vuonna 1980, mutta sen myynti lopetettiin jo vuonna 1984, koska se ei pystynyt kilpailemaan muiden markkinoilla olevien syntetisaattoreiden kanssa. Muita varhaisia oligonukleotidisyntetisaattoreiden valmistajia olivat Bio Logical, KabiGen AB ja Biosearch. 61,62 Varhaiset oligonukleotidisyntetisaattorit eivät olleet kovin luotettavia, sillä ne käyttivät enimmäkseen jo olemassa olevia HPLC-laitteisiin tarkoitettuja osia, jotka eivät soveltuneet oligonukleotidisynteesissä käytettävien reagenssien kanssa. Lisäksi ylimääräinen kuollut tila ja korkea paine haittasivat reaktioita ja lisäsivät reagenssikulutusta
29 Kuva 3: Kaaviokuva oligonukleotidisyntetisaattorista 1980-luvun alkupuolelta 61 Applied Biosystems, Inc. (ABI) oli ensimmäinen, joka toi markkinoille luotettavan ja menestyksekkään oligonukleotidisyntetisaattorin vuonna 1983 (ABI 380A). Laite käytti pneumaattisia kalvoventtiilejä, joissa ei ole kuollutta tilavuutta ja reagenssit liikutettiin positiivisella argonpaineella pumppujen sijaan. äiden ansiosta saatiin aikaan tarkka ja luotettava menetelmä reagenssien ja liuottimien liikuttamiseen ja systeemi voitiin huuhdella argonkaasulla reaktiovaiheiden välillä. Argon on tässä parempi kaasu kuin esimerkiksi typpi sen suuremman tiheyden ja puhtauden ansiosta. Lisäksi kuolleen tilavuuden minimointi vähensi reagenssikulutusta huomattavasti. Laite hyödynsi fosforamidiittikemiaa ja käytti reaktorina pyrexistä valmistettua sylinteriä, jonka päät oli suljettu huokoisella teflonkalvolla. Laite pystyi valmistamaan kolme eri DA-ketjua samanaikaisesti 0.2, 1 tai 10 µmol mittakaavassa, ja synteesisykli suoritettiin 10 minuutissa noin 96 % saannolla. 61,63 65 Muita aikaisia ABI DA-symtesisaattoreita olivat ABI 380B, ABI 381A (1985), ABI 392, ABI 394 (1991). ABI 380B käytti fosforamidiittikemiaa ja se hoiti myös automaattisen tuotteen irrottamisen kantajasta ja suojaryhmien poiston. Se pystyi edeltäjänsä tavoin valmistamaan 3 oligonukleotidia rinnakkain. Uusi malli paransi synteesisyklin saantoa %:n ja pystyi valmistamaan jopa nukleotidin mittaisia oligonukleotideja. ABI 380B käytti samanlaista teknologiaa liuottimien välityksessä ja venttiileissä kuin ABI 380A. Laitteen ohjaus toimi valikkopohjaisella ohjelmalla, jota ohjattiin kosketusnäytöllä. hjelmisto mahdollistaa hyvin tarkan kontrollin venttii- 24
30 lien liikuttamiseen, joten syntetisaattoria on mahdollista käyttää muuhun kuin vain tavalliseen fosforamidiittimenetelmällä tehtävään oligonukleotidisynteesiin. ABI 381A oli pienempi ja halvempi versio ABI 380B:stä. Se pystyi valmistamaan vain yhden oligonukleotidin kerrallaan ja se ei mahdollistanut automaattista irrotusta kantajasta. Edullisempi malli mahdollisti oligonukleotidisyntetisaattorien leviämisen useampaan laboratorioon. 64,66,67 ABI 392 ja 394 (Kuva 4) olivat seuraavat syntetisaattorimerkit. Siinä uutena ominaisuutena oli reaktion automaattinen seuranta trityylimittauksella. ABI 292 oli 2 synteesikolonnia ja ABI 294 oli 4. Laitetta pystyi ohjaamaan joko laitteiston omalla valikkopohjaisella ohjelmistolla tai se oli mahdollista kytkeä tietokoneeseen, jonka kautta laitetta ohjattiin. 68,69 Kuva 4: Vuonna 1991 julkaistu ABI 394 DA/RA-syntetisaattori 64 Suuren kysynnän ansiosta on valmistettu useita syntetisaattoreita, jotka pystyvät valmistamaan suuren määrän oligonukleotideja rinnakkain. Jos syntetisaattorissa käytetään suljettua systeemiä reagenssien viemiseen, kaikkiin kolonneihin tarvitaan hyvin monimutkaista venttiili- ja letkusysteemiä, jolloin kuolleen tilavuuden määrä lisääntyy ja myös tarvittavien reagenssien ja pesuliuosten määrä lisääntyy. ämän takia on kehitetty useampia avoimia liikkuvia mekanismeja reagenssien viemiseen reaktiokolonniin. Yksi lähestymistapa on systeemi, jossa reagenssit tiputetaan reaktiokolonneihin argonilla suojatussa kammiossa. Kolonnit liikkuvat vuorollaan kunkin reagenssisuuttimen alle. ämä vuonna 1995 kehitetty mekanismi on käytössä muun muassa Biolyticin Dr ligo syntetisaattorissa, joka pystyy valmistamaan 96 oligonukleotidia rinnakkain(kuva 5). 70,71 25
31 Kuva 5: Kaavio alkuperäisestä avoimesta reagenssinlisäysmekanismista 71 ja sitä hyödyntävästä Dr. ligo syntetisaattorista. 70 oinen menestykäs lähestymistapa on ABI 3900-syntetisaattorissa käytetty konfiguraatio, jossa reagenssikolonnit asetetaan ympyrämuotoiseen pyörivään telineeseen. ässä kolonnit pyörivät vuorollaan oikean reagenssisuuttimen alle. 61,72 ätä ja vastaavaa konfiguraatiota on käytetty esimerkiksi useammassa ABI-syntetisaattorisa. Reagenssien pipetointi kantajan päälle ja niin sanottu teepussimenetelmä, jossa huokoisessa pussissa oleva kantaja kastetaan reagenssilla täytettyihin astioihin, on myös käytetty joissakin syntetisaattoreissa. ämä menetelmät eivät kuitenkaan ole riittävän tehokkaita eivätkä ne toimi suuressa mittakaavassa. Yllämainittujen menetelmien lisäksi on käytetty lukuisia muita menetelmiä, jotka soveltuvat etenkin pienen mittakaavan oligonukleotidisyntessiin. 61 Kuva 6: Kaaviokuva vuonna 2000 julkastusta ABI 3900-syntetisaattorista
32 Edellä käsitellyt oligonukleotidisyntetisaattorit valmistavat oligonukleotideja vain pienessä mittakaavassa. Mittakaavaa kasvatettaessa etenkin reaktioastian kasvattamien ja reagenssien saanti tasaisesti koko reaktioastiaan on hankalaa. Reaktioastiaksi on esitetty kaasulla tai mekaanisesti sekoitettua leijupartikkelireaktori, vyöhykesentrifugaalireaktoria, isompaa pakattua kolonnia tai jotakin näiden yhdistelmää. 73 Ensimmäinen suosittu ison mittakaavan oligonukleotidisyntetisaattori, Biosearch (Millipore) 8800, käytti reaktorina leijupartikkelireaktoria, jossa kantajaa sekoitettiin argonkaasulla. Laite pystyi valmistamaan mmol oligonukleotidia kerrallaan käyttäen 1-10 g kantajaa. ABI toi vuonna 1992 markkinoille oman ison mittakaavan syntetisaattorinsa. ABI 390Z. Se pystyi valmistamaan mmol:a oligonukleotidia kerrallaan ja partikkeleiden tasainen sekoittuminen saatiin aikaan vortex-sekoittimella avulla. Syntetisaattorin mittakaavaa oli mahdollista kasvattaa 1 mmol:n käyttämällä kiintokantajalla entageliä, jonka nukleotidilataus oli paljon suurempi. Syntetisaattori hyödynsi vastaavaa tekniikkaa kuin aikaisemmat ABI-syntetisaattorit ja sitä ohjattiin Machintosh tietokoneelle asennettavalla ohjelmalla. 61,63,74 Large scale biology corporation kehitti PCS-nimisen ison mittakaavan oligonukleotidisyntetisaattorin, joka käytti vyöhyke-sentrifugaalireaktoria (zonal centrifuge rotor reactor) (Kuva 7). Reaktioastian suuri hyöty on, että eri mittakaavan reaktiot voidaan tehdä samalla optimoidulla ohjelmalla ja kaikki reaktioajat pysyvät vakiona. ämä ei esimerkiksi toteudu pakatuilla kolonneilla. Reaktori oli kuitenkin liian monimutkainen käytettäväksi kilogrammojen mittakaavan synteeseissä, joten lähestymistavan tutkiminen lopetettin. 61,73 27
33 Kuva 7: Kaaviokuva PCS-syntetisaattorin reaktorista. 73 Pakatun kolonnin mittakaavan kasvattaminen ei ole kaikkein suoraviivaisinta, mutta siitä huolimatta se on osoittautunut tehokkaimmaksi reaktoriksi teollisuusmittakaavan synteesiin. n toivottavaa, että reagenssit virtaavat kolonnin läpi mahdollisimman tasaisena ja konsentroituneena rintamana ja että reaktio-olosuhteet ovat samat sekä kolonnin alku- että loppupäässä. Jos reagenssirintama on epätasainen, jossakin kohtaa kolonnia todellinen reaktioaika voi olla liian lyhyt, jolloin reaktio ei mene loppuun asti ja taas toisaalla kolonnissa reaktioaika on liian pitkä, jolloin sivureaktiot ovat mahdollisia. asainen liuotinvirtaus on helpompi saada aikaiseksi pienessä kolonnissa kuin suuressa. Kun kolonnin pituutta kasvatetaan, liuotinrintama levenee kolonnin loppupäässä, ja kun kolonnin läpimittaa kasvatetaan liuotinrintama voi helposti vääristyä, jos kiintokantaja ei ole tasakokoista. 73 Käytetyt kolonnit yritetään pitää mahdollisimman lyhyinä ja modernit kantajat valmistetaan mahdollisimman tasakokoisista partikkeleista. 75 Pakatun kolonnin hyviä puolia ovat pienempi reagenssikulutus ja lyhyempi synteesisykli muihin reaktoreihin verrattuna. GE:n ison mittakaavan ligopilot400 ja teollisuusmittakaavan ligoprosess käyttävät pakattua kolonnia reaktorina. ligopilot400 pystyy valmistamaan 4-60 mmol ja ligoprosess pystty valmistamaan mmol:a oligonukleotidia kerrallaan. ligopilot400-syntetisaattorissa käytettään 3-10 cm mittaisia kolonneja, joiden sisähalkaisija on mm ja ligoprocess syntetisaattorissa kolonnin sisähalkaisia voi olla jopa yli 1200 mm (Kuva 8). 75 ligoprosess on luultavasti tunnetuin teollisuusmittakaavan oligonukleotidisyntetisaattori, mutta myös muilla yhtiöillä kuten AsahiKaseilla 76 ja CXH:lla 77 on omat teollisuusmittakaavan syntetisaattorinsa. 28
34 Kuva 8: eollisuusmittakaavan ligoprosess-syntetisaattori ja siinä käytety ison mittakaavan synteesikolonni Puhdistus ja eristäminen Kun syntetisoitava oligonukleotidi on halutun mittainen, seuraa synteesin toinen vaihe eli tuotteen irrottaminen mahdollisesta kantajasta, suojaryhmien irrottaminen ja puhdistus. ligonukleotidin irrotus kantajasta ja suojaryhmien poistaminen voidaan yleensä tehdä yhdessä vaiheessa, koska sekä linkkeri että suojaryhmät ovat emäslabiileja. ligonukleotidi voidaan puhdistaa mm. saostamalla, kokoekskluusiokromatografialla, käänteisfaasipatruunalla, denaturoivalla polyakryyliamidielektroforeesimenetelmällä tai HPLC:llä riippuen mm. puhdistettavan oligonukleotidin pituudesta, tarvittavasta puhtausasteesta, oligonukleotidin käyttötarkoituksesta ja määrästä. 78 ptinen tiheys (D) on tavallinen yksikkö, jolla puhtaan oligonukleotidituotteen saantoa mitataan. D:llä tarkoitetaan 1 ml:aan vettä liuotetun oligonukleotidin absorbanssia 260 nm aallonpituudella 1 cm paksuisen kyvetin läpi mitattuna. D ei ole lineaarinen asteikko ja sen arvo riippuu oligonukleotidin pituudesta, sekvenssistä ja oligonukleotidimäärästä. Hyvä arvio oligonukleotidin D:n ja moolimäärän suhteesta voidaan saada yhtälöstä 1. Yhtälön perusteella 1 D 20 nukleotidin mittaista oligonukleotidiä vastaa noin 5 nmol:a oligonukleotidia. 79 n [ nmol ] = 100 [ D ] 1.54 A G C (1) 29
35 avallisimmin suojaryhmien irrottamiseen ja suojaryhmien poistamiseen käytetään väkevää ammoniakkia. ligonukleotidin irrottamiseen CPG-kantajasta ammoniakilla tarvitaan noin tunnin reaktioaika ja irrottamiseen PS-kantajasta hiukan pidempi reaktioaika. Liian pitkä emäskäsittely saattaa liuottaa CPG:tä. ligonukleotidin irrottaminen kantajasta on automatisoitu useimmissa oligonukleotidisyntetisaattoreissa. Yleisimmin käytetyt emässuojaryhmät (A Bz, G ibu, C Bz, ) ja fosforisuojaryhmänä käytetty syanoetyyli irrotetaan myös ammoniakkikäsittelyllä. Suojaryhmien täydellisen irottamisen varmistamikseksi tarvitaan noin kahdeksan tunnin ammoniakkikäsittely 55 o C:ssa tai noin neljän tunnin ammoniakkikäsittelyä 65 o C:ssa. Puhdistuksen kannalta on hyvin tärkeää, että kaikki suojaryhmät irtoavat tuotteesta. 80 Saostus on tehokas menetelmä pienten molekyylien, kuten suojaryhmien, irrotuksessa muodostuneiden suolojen poistamiseen oligonukleotidituotteesta, mutta se ei sovellu lyhyiden oligonukleotidien poistamiseen tuotteesta. Saostus on halpa ja tehokas menetelmä, joka soveltuu myös isojen oligonukleotidimäärien puhdistukseen. Se soveltuu sekvensointiin, kloonaamiseen tai PCR:ään tarkoitettujen oligonukleotidien puhdistukseen tai käytettyäväksi muiden puhdistusmenetelmien kanssa. ligonukleotidien saostus voidaan mm. tehdä liuottamalla oligonukleotidi pieneen määrään vettä, jonka jälkeen seokseen lisätään pieni määrä natriumasetaattia. ligonukleotidi saostetaan lisäämällä etanolia ja jäähdyttämällä seosta. Etanoli voidaan korvata isopropanolilla, kun saostetaan lyhyitä, alle 15 nukleotidin mittaisia oligonukleotidejä, paremman saostuksen aikaansaamiseksi. Jäähdyttämisen jälkeen seos sentrifugoidaan ja liuos pipetoidaan varovasti tuotteen päältä. uotteeseen lisätään vielä kerran etanolia ja sentrifugoidaan tehokkaamman puhdistuksen varmistamiseksi. 78,80 Denaturoiva polyakryyliamidigeelielektroforeesi (PAGE) soveltuu etenkin pitkien oligonukleotidien puhdistukseen ja analysointiin. Menetelmällä voidaan poistaa tuotteesta oligonukleotideja, jotka ovat lyhyempiä kuin haluttu oligonukleotidi, mutta se ei sovellu hyvin modifioitujen oligonukleotidien puhdistukseen. Esimerkiksi tioloidut oligonukleotidit voivat reagoida geelimatriisin kanssa Michaelin additiolla. 78 PAGE perustuu varattujen molekyylien liikkeeseen geelimatriisissa sähkökentän vaikutuksesta. opeus, jolla molekyyli liikkuu geelimatriisissa, riippuu pääosin sen varauksesta ja massasta. ligonukleotideilla varaus/massa-suhde pysyy suhteellisen vakiona yli 10 nukleotidin mittaisilla oligonukleotideilla, jonka ansiosta oligonukleotidit uuttuvat tasaisin välein lyhyin oligonukleotidi ensin. Lyhyet 2-10 nukleotidin mittaiset oligonukleotidit ovat poikkeus tähän ja dimeeri eluoituu näistä kaikkein hitaimmin. ämä saattaa aiheuttaa lyhyiden oligoukleotidien eluoitumisen tuotteen kanssa. ligonukleotidin pituuden lisäksi myös oligonukleotidin sekvenssi vaikuttaa oligonukleotidin liikkumiseen geelissä, joten samanmittaiset oligonukleotidit saattavat eluoitua eri kohtaan. Pitkille, yli 50 nukleotidin mittaisille oligonukleotideille kannattaa tehdä suolanpoisto esimerkiksi saostamalla ennen PAGE:a. 30
36 PAGE-puhdistus koostuu neljästä vaiheesta: elektroforeesista, tuotteen paikantamisesta UV-valolla, tuotealueen leikkaamisesta irti geelistä ja tuotteen eristämisestä geelistä. Elektroforeesi ajetaan sähkökentän avulla kunnes hitaimmin eluoituva tuote on liikkunut ainakin 2/3 geelistä. Lyhyiden oligonukleotidien eluoituminen geelin yli ei haittaa, koska ne eivät ole haluttuja tuotteita. Pidempi matka parantaa oligonukleotidien erottumista. Ajon jälkeen tuotteen eluoitumiskohta tarkistetaan UV:llä, jonka jälkeen tuote leikataan varovasti irti geelistä partaveitsellä. uote eristetään geelistä joko liuottamalla geeliä 8-24 h veden ja neutraalin puskurin seoksessa tai elektrouutolla. Elektrouutto tarkoittaa varattujen molekyylien uuttamista sähkökentän avulla haluttuun liuottimeen. Lopuksi suolat poistetaan saostamalla, kokoekskluusiosuodatuksella tai sopivalla patruunalla (affinity catridge). 81 PAGE ei sovellu kovin suurien oligonukleotidimäärien puhdistukseen. Integrated DA echnologies (ID) tarjoaa 10 µmol:n mittakaavan puhdistuksen nukleotidien mittaisille oligonukleotideille. Saannoksi on ilmoitettu 100 D, joka on noin puolet HPLC-puhdistuksella saatavasta saannosta. PAGE-puhdistuksella saadaan yli 90 %:sti puhdasta oligonukleotidiä ja se hyvä valinta yli 60 nukleotidin mittaisille oligonukleotideille. 82 HPLC on toinen menetelmä, jolla erimittaiset oligonukleotidit voidaan erotella toisistaan. Se soveltuu alle 50 nukleotidin mittaisten oligonukleotidien puhdistukseen hyvällä saannolla. oin 20 nukleotidin mittaisten oligonukleotidien pudistuksen saanto on % raakatuotteen saannosta. HPLC on nopea menetelmä, joka on suurimmaksi osin automatisoitu ja jonka mittakaavaa on suoraviivaista kasvattaa kasvattamalla laitteistoa ja kolonnia. HPLC-laitteisto on huomattavasti kalliimpi kuin PAGElaitteisto. HPLC-kolonnit ovat yleisimmin joko ioninvaihto- tai käänteisfaasikolonneja, mutta myös muita kolonneja käytetään. 80,83,84 Ioninvaihtokromatografia on hyvä menetelmä, jolla voidaan analysoida ja puhdistaa sekä oligonukleotideja, joissa DMr on vielä kiinni, että täysin suojaamattomia oligonukleotideja. Ioninvaihtokromatografiassa kiinteänä faasina on käytetty mm tertiäärisillä ja kvaternäärisillä ammoniumioniryhminillä derivatisoitua silikageeliä tai polymeeriä. Q-Sepharose, Sucrose-Q GE:tä ja SK-gel Super-Q 5 PW osoh Bioscienceiltä ovat esimerkkejä ison mittakaavan puhdistuksessa käytetyistä kiinteistä faaseista. Yhdisteen eluoitumisnopeus riippuu varausten määrästä: mitä enemmän varauksia, sitä hitaammin yhdiste eluoituu. ligonukleotidien negatiivinen varaus kasvaa oligonukleotidien koon kasvaessa, joten tuote, joka on yleensä raakatuotteen pisin oligonukleotidi, eluoituu viimeiseksi. sa nukleotidiemäksistä ovat varautuneita, joten myös nukleotidin emäskoostumus vaikuttaa nukleotidien retentioaikaan. Ionivaihtokromatografia ei toimi kunnolla, jos oligonukleotidi on kiertyneenä niin, että osa varauksista on suojattuna oligonukleotidikierteen sisällä. ästä johtuen oligonukleotidi pitää yleensä denaturoida lisäämällä orgaanista liuotinta, kuten formamidia, asetonitriiliä tai etanolia, tai käyttämällä korkean ph:n puskuria. Systeemi lämmittäminen o C:een auttaa 31
37 myös denaturoitumista. Ionivaihtokolonnien vahvuus on, että 5 -pään DMr-suojausta ei ole pakko säilyttää puhdistuksen ajaksi, joten puhdistettu oligonukleotidi voidaan heti ottaa käyttöön. Lisäksi tuotteen eluoituminen on helpommin ennakoitavissa kuin muilla HPLC-menetelmillä ja raakatuote voidaan laittaa sellaisenaan kolonniin. Ionivaihtokromatografian eluenttina käytetään ah:n vesiliuoksen ja acl:n gradienttiä DA-oligonukleotideille ja a 3 P 4 :n ja acl:n gradienttä sisältäen 10 % AC:a RA-oligonukleotideille. DMr-ryhmä voidaan poistaa oligonukleotidistä ionivaihtokromatografian aikana eluoimalla kolonnia esimerkiksi 5-10 % DCA-liuoksella kolonnin latausvaiheen ja tuotteen eluoinnin välillä. Kromatografian jälkeen oligonukleotidi on liuoksessa, jossa on suuri määrä suoloja ja mahdollisesti korkea ph. Suola ja vesi on poistettava kromatografian jälkeen, jotta tuote säilyisi kunnolla ja olisi valmis jatkokäyttöön. Suola poistetaan yleensä suodatuksella tai RP-patruunalla ja vesi poistetaan kylmäkuivauksella. 83,84 Käänteisfaasikromatografia (RP-HPLC) soveltuu erityisesti suurten oligonukleotidimäärien puhdistukseen. Kantajana käytetään yleensä silikaa, johon on kiinnitetty hiilivetyketjuja (esim C18) tai divinyylibentseenillä derivatisoitua polystyreeniä. uotteiden erottuminen perustuu yhdisteiden hydrofobisuuteen. Mitä hydrofobisempi aine, sitä pidempi retentioaika tuotteella on. Käänteisfaasikromatografiaa voi tehdä sekä oligonukleotidille, jossa DMr on kiinni, että suojaamattomalle oligonukleotidille. DMr:llä suojattu oligonukleotidi soveltuu hyvin käänteisfaasikromatografiaan. eoriassa vain tuotteella on DMr-ryhmä, sillä DMr ryhmä poistetaan aina synteesisyklin alussa. DMr on iso ja hydrofobinen, joten sitä sisältävän oligonukleotidin retentioaika on huomattavasti pidempi kuin muilla oligonukleotideillä. DMr-suojauksen säilyttäminen kvantitatiivisesti voi olla hyvin hankalaa, sillä se saattaa irrota jo hyvin lievästi happamissa olosuhteissa. Etenkin polymeereihin perustuvilla käänteisfaasikolonneilla on hyvin suuri kapasiteetti sitoa trityloitua tuotetta. äillä kolonneilla on myös yleisesti ottaen pidempi elinikä kuin silikaan perustuvilla kolonneilla. Yleisesti eluenttina käytetään asetonitriilin gradienttia laimeassa trietyyliammoniumasetaattiliuoksessa (EAA). HPLC:n jälkeen DMr:ä sisältävä tuote saostetaan etanolilla ja DMr irrotetaan natriumasetaatilla (ph 3). Kun kaikki DMr on irronnut, seokseen lisätään natriumasetaattia (ph 7.2), ja tuote saostetaan etanolilla. Lopuksi tuote kerätään talteen sentrifugoimalla ja kylmäkuivataan. 83,84 Ionipari-RP-HPLC on RP-HPLC:n variaatio, joka on melko uusi menetelmä oligonukleotidien puhdistamiseen. Siinä käytetään samaa kolonnia kuin tavallisessa RP- HPLC:ssä, mutta eluenttina käytetään esimerkiksi metanolin gradienttia heksafluoriisopropanolin, trietyyliamiinin ja veden seoksessa. Eri eluentin käyttö saa kiinteän faasin toimimaan hiukan niin kuin ioninvaihtokromatografian kiinteä faasi. ämä parantaa kromatografian resoluutiota ja mahdollistaa tuotteen erottamisen -1 oligonukleotideistä ja mahdollisista depurinoiduista sivutuotteista. Eluentit ovat kuitenkin kalliita 32
38 ja myrkyllisiä, mistä johtuen menetelmää ei käytetä ison mittakaavan puhdistukseen. UPLC on HPLC modifikaatio, jossa käytetään hyvin pientä partikkelikokoa (<2 µm) verrattuna HPLC:n normaaliin partikkelikoon (5-10 µm). Pienempi partikkelikoko ja pumppujen korkeampi paine mahdollistaa nopeamman liuosvirtauksen menettämättä resoluutiota, jolloin analyysi nopeutuu ja eluenttikulutus vähenee. UPLC-menetelmää on hyödyllinen kun on monta näytettä analysoitavana. 84 Edellä mainituista menetelmistä ioninvaihtokromatografia ja RP-HPLC ovat kaikkein tärkeimpiä, kun halutaan puhdistaa oligonukleotideja isossa mittakaavassa. rityloidun oligonukleotidin puhdistaminen RP-HPLC:llä on helppo tehdä isommassa mittakaavassa, sillä sen mittakaavaa voidaan muuttaa lineaarisesti kasvattamalla kolonnia ja laitteistoa. Ioninvaihtokromatografiaa on kasvatettu puhdistamaan 300 mmol:a 20 nukleotidin mittaista oligonukleotidia, joka vastaa 2000 g raakatuotetta ja 1000 g puhdistettua tuotetta käyttäen 50 L kolonnia. Isossa teollisuusmittakaavassa ioninvahtokromatografia voi olla suositeltava menetelmä, sillä se ei tarvitse ylimääräisiä vaiheita puhdistuksen jälkeen trityylin poistamiseen. ällä hetkellä ioninvaihtokromatografia on antisens-oligonukleotidien puhdistuksessa käytetty. 84,85 Esimerkiksi AsahiKasehi ja GE valmistavat teollisuusmittakaavaan sopivia kromatografialaitteistoja (Kuva 9). 75,86 Kuva 9: eollisuusmittakaavasa käytetty kromatografiakolonni. 86 ligonukleotidijen puhdistaminen erilaisten patruunojen (Kuva 10)(cartidge) avulla on kromatografiaa muistuttava menetelmä. Patruunoiden käyttö eroaa HPLC:n käytöstä siten, että gradientin käytön sijaan tuote ensin viedään patruunaan liuottimella, joka ei liikuta tuotetta, jonka jälkeen epäpuhtaudet pestään pois tuotteesta ja 33
39 tuote eluoidaan pois patruunasta. Patruunoita on nopea käyttää ja halpa, mutta niillä ei ole samaa kapasiteettia ja saantoa kuin HPLC:llä. Erillaisia patruunoita voidaan käyttää eri tarkoituksiin. RP-kiintokantajaa sisältävää patruunaa voidaan käyttää trityloitujen oligonukleotidien puhdistamiseen. Eri valmistajien patruunojen käyttö eroavat joissakin määrin toisistaan. Applied Biosystemsin patruunalla oligonukleotidituote voidaan ladata patruunaan suoraan suojaryhmien irrotusreaktiosta (liuotettuna laimeaan ammoniakkiin). uotetta sisältävä liuos painetaan kaksi kertaa patruunan läpi, jonka jälkeen patruuna pestään ammoniumhydroksidin vesiliuoksella, vedellä, FA:lla DMr:n irrottamiseksi ja uudestaan vedellä. Lopuksi tuote eluoidaan asetonitriilin vesiliuoksella. Affiniteettipatruunaa voidaan käyttää suolanpoistoon, mutta ei lyhyiden oligonukleotidien poistoon. Menetelmä soveltuu erityisesti PAGE:n ja ioninvaihtokromatografian jälkeiseen suolanpoistoon. Menetelmässä eluenttina käytetään EAA:n vesiliuosta ja asetonitriiliä. Kokoekskluusiosuodatus tai kokoeksluusiokromatografia perustuu molekyylien kokoeroihin eikä vuorovaikutuksiin kiinteän aineen kanssa. Isommat molekyylit kulkevat lyhyemmän matkan kuin pienet molekyylit, sillä isot molekyylit eivät mahdu kaikkiin kiinteän aineen huokosiin, jolloin isot molekyylit eluoituvat aikaisemmin. Menetelmä sopii esimerkiksi suolanpoistoon muun puhdistuksen jälkeen. Patruunamenetelmät ovat hyviä, jos jatkomenetelmien puhtausvaatimus ei ole kovin korkea ja muiden puhdistusmenetelmien yhteydessä. 84,87,88 Kuva 10: Glen Research Glen Gel-Pack patruuna on esimerkki oligonukleotidien puhdistuksessa käytettävästä kokoekskllusiopatruunasta
HELSINGIN YLIOPISTO. Vetyfosfonaattimenetelmä oligonukleotidisynteesissä
 ELSIGI YLIIST Vetyfosfonaattimenetelmä oligonukleotidisynteesissä etra Gargano ro gradu -tutkielma elsingin yliopisto Kemian laitos 24.4.2017 i Sisällysluettelo 1 Kirjallinen osa... 6 1.1 Johdanto...
ELSIGI YLIIST Vetyfosfonaattimenetelmä oligonukleotidisynteesissä etra Gargano ro gradu -tutkielma elsingin yliopisto Kemian laitos 24.4.2017 i Sisällysluettelo 1 Kirjallinen osa... 6 1.1 Johdanto...
arvostelija OSDA ja UDDI palveluhakemistoina.
 Hyväksymispäivä Arvosana arvostelija OSDA ja UDDI palveluhakemistoina. HELSINGIN YLIOPISTO HELSINGFORS UNIVERSITET UNIVERSITY OF HELSINKI Tiedekunta/Osasto Fakultet/Sektion Faculty/Section Laitos Institution
Hyväksymispäivä Arvosana arvostelija OSDA ja UDDI palveluhakemistoina. HELSINGIN YLIOPISTO HELSINGFORS UNIVERSITET UNIVERSITY OF HELSINKI Tiedekunta/Osasto Fakultet/Sektion Faculty/Section Laitos Institution
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä. FT Satu Ikonen, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola
 Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Pro gradu -tutkielma Meteorologia SUOMESSA ESIINTYVIEN LÄMPÖTILAN ÄÄRIARVOJEN MALLINTAMINEN YKSIDIMENSIOISILLA ILMAKEHÄMALLEILLA. Karoliina Ljungberg
 Pro gradu -tutkielma Meteorologia SUOMESSA ESIINTYVIEN LÄMPÖTILAN ÄÄRIARVOJEN MALLINTAMINEN YKSIDIMENSIOISILLA ILMAKEHÄMALLEILLA Karoliina Ljungberg 16.04.2009 Ohjaajat: Ari Venäläinen, Jouni Räisänen
Pro gradu -tutkielma Meteorologia SUOMESSA ESIINTYVIEN LÄMPÖTILAN ÄÄRIARVOJEN MALLINTAMINEN YKSIDIMENSIOISILLA ILMAKEHÄMALLEILLA Karoliina Ljungberg 16.04.2009 Ohjaajat: Ari Venäläinen, Jouni Räisänen
BIOMUOVIA TÄRKKELYKSESTÄ
 BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
Peptidisynteesi. SPPS:n Periaate
 Tapio Nevalainen Lääkeainesynteesit II 2011 eptidisynteesi i eptidisynteesi Suoritetaan yleensä kiinteän faasin pinnalla; solid phase peptide synthesis (SS) Suuret peptidiainemäärät valmistetaan liuosfaasissa.
Tapio Nevalainen Lääkeainesynteesit II 2011 eptidisynteesi i eptidisynteesi Suoritetaan yleensä kiinteän faasin pinnalla; solid phase peptide synthesis (SS) Suuret peptidiainemäärät valmistetaan liuosfaasissa.
vi) Oheinen käyrä kuvaa reaktiosysteemin energian muutosta reaktion (1) etenemisen funktiona.
 3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
Luonnontieteiden popularisointi ja sen ideologia
 Luonnontieteiden popularisointi ja sen ideologia Tapauksina Reino Tuokko ja Helsingin Sanomat 1960-luvulla Ahto Apajalahti Helsingin yliopisto Humanistinen tiedekunta Suomen ja Pohjoismaiden historia Pro
Luonnontieteiden popularisointi ja sen ideologia Tapauksina Reino Tuokko ja Helsingin Sanomat 1960-luvulla Ahto Apajalahti Helsingin yliopisto Humanistinen tiedekunta Suomen ja Pohjoismaiden historia Pro
Aika/Datum Month and year Kesäkuu 2012
 Tiedekunta/Osasto Fakultet/Sektion Faculty Laitos/Institution Department Filosofian, historian, kulttuurin ja taiteiden tutkimuksen laitos Humanistinen tiedekunta Tekijä/Författare Author Veera Lahtinen
Tiedekunta/Osasto Fakultet/Sektion Faculty Laitos/Institution Department Filosofian, historian, kulttuurin ja taiteiden tutkimuksen laitos Humanistinen tiedekunta Tekijä/Författare Author Veera Lahtinen
Entsyymit ja niiden tuotanto. Niklas von Weymarn, VTT Erikoistutkija ja tiiminvetäjä
 Entsyymit ja niiden tuotanto Niklas von Weymarn, VTT Erikoistutkija ja tiiminvetäjä Mitä ovat entsyymit? Entsyymit ovat proteiineja (eli valkuaisaineita), jotka vauhdittavat (katalysoivat) kemiallisia
Entsyymit ja niiden tuotanto Niklas von Weymarn, VTT Erikoistutkija ja tiiminvetäjä Mitä ovat entsyymit? Entsyymit ovat proteiineja (eli valkuaisaineita), jotka vauhdittavat (katalysoivat) kemiallisia
Työn laji Arbetets art Level Aika Datum Month and year Sivumäärä Sidoantal Number of pages
 Tiedekunta/Osasto Fakultet/Sektion Faculty Laitos Institution Department Tekijä Författare Author Työn nimi Arbetets titel Title Oppiaine Läroämne Subject Työn laji Arbetets art Level Aika Datum Month
Tiedekunta/Osasto Fakultet/Sektion Faculty Laitos Institution Department Tekijä Författare Author Työn nimi Arbetets titel Title Oppiaine Läroämne Subject Työn laji Arbetets art Level Aika Datum Month
12. Amiinit. Ammoniakki 1 amiini 2 amiini 3 amiini kvarternäärinen ammoniumioni
 12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
Selainpelien pelimoottorit
 Selainpelien pelimoottorit Teemu Salminen Helsinki 28.10.2017 Seminaaritutkielma Helsingin yliopisto Tietojenkäsittelytiede ! 1 HELSINGIN YLIOPISTO HELSINGFORS UNIVERSITET UNIVERSITY OF HELSINKI Tiedekunta
Selainpelien pelimoottorit Teemu Salminen Helsinki 28.10.2017 Seminaaritutkielma Helsingin yliopisto Tietojenkäsittelytiede ! 1 HELSINGIN YLIOPISTO HELSINGFORS UNIVERSITET UNIVERSITY OF HELSINKI Tiedekunta
Koht dialogia? Organisaation toimintaympäristön teemojen hallinta dynaamisessa julkisuudessa tarkastelussa toiminta sosiaalisessa mediassa
 Kohtdialogia? Organisaationtoimintaympäristönteemojenhallinta dynaamisessajulkisuudessatarkastelussatoiminta sosiaalisessamediassa SatuMariaPusa Helsinginyliopisto Valtiotieteellinentiedekunta Sosiaalitieteidenlaitos
Kohtdialogia? Organisaationtoimintaympäristönteemojenhallinta dynaamisessajulkisuudessatarkastelussatoiminta sosiaalisessamediassa SatuMariaPusa Helsinginyliopisto Valtiotieteellinentiedekunta Sosiaalitieteidenlaitos
! #! %! & #!!!!! ()) +
 ! #! %! & #!!!!! ()) + Tiedekunta/Osasto Fakultet/Sektion Faculty Humanistinen tiedekunta Laitos Institution Department Taiteiden tutkimuksen laitos Tekijä Författare Author Matti Pesonen Työn nimi Arbetets
! #! %! & #!!!!! ()) + Tiedekunta/Osasto Fakultet/Sektion Faculty Humanistinen tiedekunta Laitos Institution Department Taiteiden tutkimuksen laitos Tekijä Författare Author Matti Pesonen Työn nimi Arbetets
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
ALKOHOLIT SEKAISIN KOHDERYHMÄ:
 ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
d) Klooria valmistetaan hapettamalla vetykloridia kaliumpermanganaatilla. (Syntyy Mn 2+ -ioneja)
 Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
Katsaus korruption vaikutuksesta Venäjän alueelliseen talouskasvuun ja suoriin ulkomaisiin investointeihin
 INSTITUUTIOTTALOUSKASVUNEDELLYTYKSENÄ KatsauskorruptionvaikutuksestaVenäjänalueelliseentalouskasvuunjasuoriin ulkomaisiininvestointeihin2000 2010 AshekMohamedTarikHossain HelsinginYliopisto Valtiotieteellinentiedekunta
INSTITUUTIOTTALOUSKASVUNEDELLYTYKSENÄ KatsauskorruptionvaikutuksestaVenäjänalueelliseentalouskasvuunjasuoriin ulkomaisiininvestointeihin2000 2010 AshekMohamedTarikHossain HelsinginYliopisto Valtiotieteellinentiedekunta
Biomolekyylit ja biomeerit
 Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Maailman muutosta tallentamassa Marko Vuokolan The Seventh Wave -valokuvasarja avauksena taidevalokuvan aikaan
 Maailman muutosta tallentamassa Marko Vuokolan The Seventh Wave -valokuvasarja avauksena taidevalokuvan aikaan Pro gradu -tutkielma 31.1.2012 Helsingin yliopisto Humanistinen tiedekunta Filosofian, historian,
Maailman muutosta tallentamassa Marko Vuokolan The Seventh Wave -valokuvasarja avauksena taidevalokuvan aikaan Pro gradu -tutkielma 31.1.2012 Helsingin yliopisto Humanistinen tiedekunta Filosofian, historian,
2. Täydennä seuraavat reaktioyhtälöt ja nimeä reaktiotuotteet
 /Tapio evalainen Loppukuulustelun..00 mallivastaukset. imi: vsk:. Piirrä karboksyylihapporyhmän ja aminoryhmän rakenteet ja piirrä näkyviin myös vapaat elektroniparit. soita mikä hybridisaatio karboksyyli-
/Tapio evalainen Loppukuulustelun..00 mallivastaukset. imi: vsk:. Piirrä karboksyylihapporyhmän ja aminoryhmän rakenteet ja piirrä näkyviin myös vapaat elektroniparit. soita mikä hybridisaatio karboksyyli-
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
8. Alkoholit, fenolit ja eetterit
 8. Alkoholit, fenolit ja eetterit SM -08 Alkoholit ovat orgaanisia yhdisteitä, joissa on yksi tai useampia -ryhmiä. Fenoleissa -ryhmä on kiinnittynyt aromaattiseen renkaaseen. Alkoholit voivat olla primäärisiä,
8. Alkoholit, fenolit ja eetterit SM -08 Alkoholit ovat orgaanisia yhdisteitä, joissa on yksi tai useampia -ryhmiä. Fenoleissa -ryhmä on kiinnittynyt aromaattiseen renkaaseen. Alkoholit voivat olla primäärisiä,
Biodiesel Tuotantomenetelmien kemiaa
 Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Esimerkiksi ammoniakin valmistus typestä ja vedystä on tyypillinen teollinen tasapainoreaktio.
 REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA
 MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
MITÄ SIDOKSILLE TAPAHTUU KEMIALLISESSA REAKTIOSSA REAKTIOT JA ENERGIA, KE3 Kaikissa kemiallisissa reaktioissa atomit törmäilevät toisiinsa siten, että sekä atomit että sidoselektronit järjestyvät uudelleen.
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio:
 Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
(ETA:n kannalta merkityksellinen teksti)
 25.11.2014 FI L 337/53 KMISSIN ASETUS (EU) N:o 1257/2014, annettu 24 päivänä marraskuuta 2014, lannoitteista annetun Euroopan parlamentin ja neuvoston asetuksen (EY) N:o 2003/2003 muuttamisesta sen liitteiden
25.11.2014 FI L 337/53 KMISSIN ASETUS (EU) N:o 1257/2014, annettu 24 päivänä marraskuuta 2014, lannoitteista annetun Euroopan parlamentin ja neuvoston asetuksen (EY) N:o 2003/2003 muuttamisesta sen liitteiden
Joensuun yliopisto Kemian valintakoe/3.6.2009
 Joesuu yliopisto Kemia valitakoe/.6.009 Mallivastaukset 1. Selitä lyhyesti (korkeitaa kolme riviä), a) elektroegatiivisuus b) elektroiaffiiteetti c) amfolyytti d) diffuusio e) Le Chatelieri periaate. a)
Joesuu yliopisto Kemia valitakoe/.6.009 Mallivastaukset 1. Selitä lyhyesti (korkeitaa kolme riviä), a) elektroegatiivisuus b) elektroiaffiiteetti c) amfolyytti d) diffuusio e) Le Chatelieri periaate. a)
KOHDERYHMÄ KESTO: MOTIVAATIO: TAVOITE: AVAINSANAT: - TAUSTAA
 ANTIBIOOTTISYNTEESI KOHDERYHMÄ: Työ soveltuu ensisijaisesti lukiolaisille. Lukiossa työn voi toteuttaa kurssilla KE3 tai työkurssilla. KESTO: Työ kestää 90 min (refluksointi 60min) (120 min tislauksen
ANTIBIOOTTISYNTEESI KOHDERYHMÄ: Työ soveltuu ensisijaisesti lukiolaisille. Lukiossa työn voi toteuttaa kurssilla KE3 tai työkurssilla. KESTO: Työ kestää 90 min (refluksointi 60min) (120 min tislauksen
LIGNIINI yleisesti käytettyjä termejä
 Luennon 9 oppimistavoitteet Ligniinin biosynteesi, rakenne ja ominaisuudet Puu-19210 Puun rakenne ja kemia Ymmärrät, että ligniini on amorfinen makromolekyyli, joka muodostuu monomeeriyksiköistä Tiedät
Luennon 9 oppimistavoitteet Ligniinin biosynteesi, rakenne ja ominaisuudet Puu-19210 Puun rakenne ja kemia Ymmärrät, että ligniini on amorfinen makromolekyyli, joka muodostuu monomeeriyksiköistä Tiedät
Kemian perusteet farmasiassa osa II: orgaaniset yhdisteet/tapio Nevalainen Loppukuulustelu b) ketoni
 /Tapio evalainen Loppukuulustelu 16.1.05 imi: vsk: 1. Laadi rakennekaava ja anna nimi seuraavien yhdisteryhmien moolimassaltaan pienimmälle yhdisteelle: a) esteri, b) ketoni, c) amiini, d) tyydyttymätön
/Tapio evalainen Loppukuulustelu 16.1.05 imi: vsk: 1. Laadi rakennekaava ja anna nimi seuraavien yhdisteryhmien moolimassaltaan pienimmälle yhdisteelle: a) esteri, b) ketoni, c) amiini, d) tyydyttymätön
ALKOHOLIT SEKAISIN TAUSTAA
 ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
Hallintomallit Suomen valtionhallinnon tietohallintostrategioissa
 Hallintomallit Suomen valtionhallinnon tietohallintostrategioissa Lauri Eloranta Helsingin yliopisto Valtiotieteellinen tiedekunta Viestintä Pro gradu -tutkielma, 2014 Hallintomallit)Suomen)valtionhallinnon)tietohallintostrategioissa
Hallintomallit Suomen valtionhallinnon tietohallintostrategioissa Lauri Eloranta Helsingin yliopisto Valtiotieteellinen tiedekunta Viestintä Pro gradu -tutkielma, 2014 Hallintomallit)Suomen)valtionhallinnon)tietohallintostrategioissa
Väittämä Oikein Väärin. 1 Pelkistin ottaa vastaan elektroneja. x. 2 Tyydyttynyt yhdiste sisältää kaksoissidoksen. x
 KUPI YLIPIST FARMASEUTTISE TIEDEKUA KEMIA VALITAKE 27.05.2008 Tehtävä 1: Tehtävässä on esitetty 20 väittämää. Vastaa väittämiin merkitsemällä sarakkeisiin rasti sen mukaan, onko väittämä mielestäsi oikein
KUPI YLIPIST FARMASEUTTISE TIEDEKUA KEMIA VALITAKE 27.05.2008 Tehtävä 1: Tehtävässä on esitetty 20 väittämää. Vastaa väittämiin merkitsemällä sarakkeisiin rasti sen mukaan, onko väittämä mielestäsi oikein
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA
 ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
Ainemäärien suhteista laskujen kautta aineiden määriin
 REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
Metallipitoisten vesien puhdistaminen luonnonmateriaaleilla
 Metallipitoisten vesien puhdistaminen luonnonmateriaaleilla Tiina Leiviskä Kemiallinen prosessitekniikka, Miksi luonnonmateriaaleja vedenpuhdistukseen? Hyvin saatavilla, edullisia/ilmaisia, biomateriaalit
Metallipitoisten vesien puhdistaminen luonnonmateriaaleilla Tiina Leiviskä Kemiallinen prosessitekniikka, Miksi luonnonmateriaaleja vedenpuhdistukseen? Hyvin saatavilla, edullisia/ilmaisia, biomateriaalit
Henkilötunnus - Biokemian/bioteknologian valintakoe. Sukunimi Etunimet Tehtävä 1 Pisteet / 20
 elsingin yliopisto/tampereen yliopisto enkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24. 5. 2004 Etunimet Tehtävä 1 Pisteet / 20 Solujen kalvorakenteet rajaavat solut niiden ulkoisesta ympäristöstä
elsingin yliopisto/tampereen yliopisto enkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 24. 5. 2004 Etunimet Tehtävä 1 Pisteet / 20 Solujen kalvorakenteet rajaavat solut niiden ulkoisesta ympäristöstä
Biologiset lääkkeet ja biosimilaarit
 Biologiset lääkkeet ja biosimilaarit v1.2 Mitä biologiset lääkkeet ja biosimilaarit ovat? Tuotetaan elävissä soluissa useimmiten geenitekniikan avulla Suurempia ja rakenteeltaan huomattavasti monimutkaisempia
Biologiset lääkkeet ja biosimilaarit v1.2 Mitä biologiset lääkkeet ja biosimilaarit ovat? Tuotetaan elävissä soluissa useimmiten geenitekniikan avulla Suurempia ja rakenteeltaan huomattavasti monimutkaisempia
Kondensaatio ja hydrolyysi
 Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
B sivu 1(6) AMMATTIKORKEAKOULUJEN TEKNIIKAN JA LIIKENTEEN VALINTAKOE
 B sivu 1(6) TEHTÄVÄOSA 7.6.2004 AMMATTIKORKEAKOULUJEN TEKNIIKAN JA LIIKENTEEN VALINTAKOE YLEISOHJEITA Tehtävien suoritusaika on 2 h 45 min. Osa 1 (Tekstin ymmärtäminen) Osassa on 12 valintatehtävää. Tämän
B sivu 1(6) TEHTÄVÄOSA 7.6.2004 AMMATTIKORKEAKOULUJEN TEKNIIKAN JA LIIKENTEEN VALINTAKOE YLEISOHJEITA Tehtävien suoritusaika on 2 h 45 min. Osa 1 (Tekstin ymmärtäminen) Osassa on 12 valintatehtävää. Tämän
Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20
 Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20 3: Osa 1 Tumallisten solujen genomin toiminnassa sekä geenien
Helsingin yliopisto/tampereen yliopisto Henkilötunnus - Biokemian/bioteknologian valintakoe Sukunimi 26. 05. 2005 Etunimet Tehtävä 3 Pisteet / 20 3: Osa 1 Tumallisten solujen genomin toiminnassa sekä geenien
Jos kahdella aineella on eri sidosrakenne, mutta sama molekyylikaava, kutsutaan niitä isomeereiksi.
 4.1 Isomeria Jos kahdella aineella on eri sidosrakenne, mutta sama molekyylikaava, kutsutaan niitä isomeereiksi. Eri isomeereillä on siis aina sama moolimassa, mutta usein erilaiset kemialliset ominaisuudet.
4.1 Isomeria Jos kahdella aineella on eri sidosrakenne, mutta sama molekyylikaava, kutsutaan niitä isomeereiksi. Eri isomeereillä on siis aina sama moolimassa, mutta usein erilaiset kemialliset ominaisuudet.
HEXIS EUROOPAN JOHTAVA TEIPPIVALMISTAJA JO 25 VUODEN AJAN TUOTETIEDOT. Hexis on tuonut markkinoille uuden sukupolven ajoneuvojen suojakalvon.
 HEXIS EUROOPAN JOHTAVA TEIPPIVALMISTAJA JO 25 VUODEN AJAN Hexis on tuonut markkinoille uuden sukupolven ajoneuvojen suojakalvon. Huippuluokan teknologiaan perustuva Bodyfence-kalvo suojaa ajoneuvoasi ulkoiselta
HEXIS EUROOPAN JOHTAVA TEIPPIVALMISTAJA JO 25 VUODEN AJAN Hexis on tuonut markkinoille uuden sukupolven ajoneuvojen suojakalvon. Huippuluokan teknologiaan perustuva Bodyfence-kalvo suojaa ajoneuvoasi ulkoiselta
sulfatiatsoli meripihkahappoanhydridi eli dihydro-2,5- furaanidioni etanoli (EtaxA, 99 %)
 ANTIBIOOTTISYNTEESI TAUSTAA Olet kesätöissä lääketehtaalla. Lääkefirman kemistit ovat kehittäneet antibiootin, sulfiatsolin, joka estää bakteerien foolihapon synteesiä. Foolihappoa tarvitaan esimerkiksi
ANTIBIOOTTISYNTEESI TAUSTAA Olet kesätöissä lääketehtaalla. Lääkefirman kemistit ovat kehittäneet antibiootin, sulfiatsolin, joka estää bakteerien foolihapon synteesiä. Foolihappoa tarvitaan esimerkiksi
Kemia ja ympäristö opintojakso
 1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
Tiedelimsa. KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä.
 KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Sukunimi: Etunimi: Henkilötunnus:
 K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
Ympäristöntutkimus 67301
 Ympäristöntutkimus 67301 Ympäristöntutkimussalkku 67301 Erinomainen uusi opetusmateriaali ympäristön tutkimiseen! Pohjautuu tutkivaan ja ongelmakeskeiseen lähestymistapaan, jossa lähtökohtana ovat lähiympäristöön
Ympäristöntutkimus 67301 Ympäristöntutkimussalkku 67301 Erinomainen uusi opetusmateriaali ympäristön tutkimiseen! Pohjautuu tutkivaan ja ongelmakeskeiseen lähestymistapaan, jossa lähtökohtana ovat lähiympäristöön
!"#$%&'$("#)*+,!!,"*--.$*#,&--#"*/".,,%0 1&'23456789::94752;&27455<:4;2;&,9:=>23?277<&8=@74;9&ABBCDABBE
 !"#$%&'$("#)*+,!!,"*--.$*#,&--#"*/".,,%0 1&'23456789::94752;&2745523?27747544H9;&IG@&JG9?=&15=5H42>:9 '28
!"#$%&'$("#)*+,!!,"*--.$*#,&--#"*/".,,%0 1&'23456789::94752;&2745523?27747544H9;&IG@&JG9?=&15=5H42>:9 '28
Press Brake Productivity -pikaopas
 Kuinka aloitat Press Brake Productivity -pikaopas Kiitos, että olet ostanut Wilan valmistaman laatutuotteen Wila on valmistanut jo yli 80 vuotta työkalunpitimiä, työkaluja ja varusteita särmäyspuristimien
Kuinka aloitat Press Brake Productivity -pikaopas Kiitos, että olet ostanut Wilan valmistaman laatutuotteen Wila on valmistanut jo yli 80 vuotta työkalunpitimiä, työkaluja ja varusteita särmäyspuristimien
TÄS ON PROTSKUU! Missä yhteyksissä olet törmännyt sanaan proteiini tai valkuaisaine?
 TÄS ON PROTSKUU! KOHDERYHMÄ: Työ soveltuu parhaiten yläkouluun kurssille elollinen luonto ja yhteiskunta, sekä lukioon kurssille KE1. KESTO: Työ koostuu kahdesta osasta: n. 30 min/osa. MOTIVAATIO: Mitä
TÄS ON PROTSKUU! KOHDERYHMÄ: Työ soveltuu parhaiten yläkouluun kurssille elollinen luonto ja yhteiskunta, sekä lukioon kurssille KE1. KESTO: Työ koostuu kahdesta osasta: n. 30 min/osa. MOTIVAATIO: Mitä
Lukion kemiakilpailu
 MAL ry Lukion kemiakilpailu/avoinsarja Nimi: Lukion kemiakilpailu 11.11.010 Avoin sarja Kaikkiin tehtäviin vastataan. Aikaa on 100 minuuttia. Sallitut apuvälineet ovat laskin ja taulukot. Tehtävät suoritetaan
MAL ry Lukion kemiakilpailu/avoinsarja Nimi: Lukion kemiakilpailu 11.11.010 Avoin sarja Kaikkiin tehtäviin vastataan. Aikaa on 100 minuuttia. Sallitut apuvälineet ovat laskin ja taulukot. Tehtävät suoritetaan
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Liukeneminen 31.8.2016
 Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
(Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET
 1.10.2018 L 245/1 II (Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET KOMISSION ASETUS (EU) 2018/1461, annettu 28 päivänä syyskuuta 2018, Euroopan parlamentin ja neuvoston asetuksen
1.10.2018 L 245/1 II (Muut kuin lainsäätämisjärjestyksessä hyväksyttävät säädökset) ASETUKSET KOMISSION ASETUS (EU) 2018/1461, annettu 28 päivänä syyskuuta 2018, Euroopan parlamentin ja neuvoston asetuksen
Lupahakemuksen täydennys
 Lupahakemuksen täydennys 26.4.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-04-26 2 / 6 Lupahakemuksen täydennys Täydennyskehotuksessa (11.4.2012) täsmennettäväksi pyydetyt
Lupahakemuksen täydennys 26.4.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-04-26 2 / 6 Lupahakemuksen täydennys Täydennyskehotuksessa (11.4.2012) täsmennettäväksi pyydetyt
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
YMPÄRISTÖTOHTORIKOULU JA VIHREÄ KEMIA
 YMPÄRISTÖTOHTORIKOULU JA Suomen Teollisen Ekologian Forumin Seminaari 1.- Jouni Pursiainen POHJOISUUS JA YMPÄRISTÖ PAINOALA OULUN YLIOPISTO THULE-INSTITUUTTI Thule-Instituutti (http://thule.oulu.fi/) Kaikki
YMPÄRISTÖTOHTORIKOULU JA Suomen Teollisen Ekologian Forumin Seminaari 1.- Jouni Pursiainen POHJOISUUS JA YMPÄRISTÖ PAINOALA OULUN YLIOPISTO THULE-INSTITUUTTI Thule-Instituutti (http://thule.oulu.fi/) Kaikki
ÄKTA OLIGOPILOT PLUS DNA- SYNTETISAATTORIN KVALIFIOINTI
 Opinnäytetyö (AMK) Bio- ja elintarviketekniikan ko. Laboratoriotekniikka 2016 Susanna Haavisto ÄKTA OLIGOPILOT PLUS DNA- SYNTETISAATTORIN KVALIFIOINTI OPINNÄYTETYÖ (AMK) TIIVISTELMÄ TURUN AMMATTIKORKEAKOULU
Opinnäytetyö (AMK) Bio- ja elintarviketekniikan ko. Laboratoriotekniikka 2016 Susanna Haavisto ÄKTA OLIGOPILOT PLUS DNA- SYNTETISAATTORIN KVALIFIOINTI OPINNÄYTETYÖ (AMK) TIIVISTELMÄ TURUN AMMATTIKORKEAKOULU
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt
 KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Kuva 1: Yhdisteet A-F viivakaavoin, tehtävän kannalta on relevanttia lisätä näkyviin vedyt ja hiilet. Piiroteknisistä syistä tätä ei ole tehty
 1. Valitse luettelosta kaksi yhdistettä, joille pätee (a) yhdisteiden molekyylikaava on C 6 10 - A, E (b) yhdisteissä on viisi C 2 -yksikköä - D, F (c) yhdisteet ovat tyydyttyneitä ja syklisiä - D, F (d)
1. Valitse luettelosta kaksi yhdistettä, joille pätee (a) yhdisteiden molekyylikaava on C 6 10 - A, E (b) yhdisteissä on viisi C 2 -yksikköä - D, F (c) yhdisteet ovat tyydyttyneitä ja syklisiä - D, F (d)
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
EPIONEN Kemia 2015. EPIONEN Kemia 2015
 EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
EPIONEN Kemia 2015 1 Epione Valmennus 2014. Ensimmäinen painos www.epione.fi ISBN 978-952-5723-40-3 Painopaikka: Kopijyvä Oy, Kuopio Tämän teoksen painamiseen käytetty paperi on saanut Pohjoismaisen ympäristömerkin.
Teollisuusveden ja kaupungin huleveden käsittely bio- ja mineraalisorbenteilla laboratoriomittakaavan tutkimus
 Teollisuusveden ja kaupungin huleveden käsittely bio- ja mineraalisorbenteilla laboratoriomittakaavan tutkimus Tiina Leiviskä HuJa-projektin loppuseminaari, Oulun yliopisto Miksi luonnonmateriaaleja vedenpuhdistukseen?
Teollisuusveden ja kaupungin huleveden käsittely bio- ja mineraalisorbenteilla laboratoriomittakaavan tutkimus Tiina Leiviskä HuJa-projektin loppuseminaari, Oulun yliopisto Miksi luonnonmateriaaleja vedenpuhdistukseen?
Ympäristölupahakemuksen täydennys
 Ympäristölupahakemuksen täydennys Täydennyspyyntö 28.9.2012 19.10.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-10-19 2 / 6 Ympäristölupahakemuksen täydennys Pohjois-Suomen
Ympäristölupahakemuksen täydennys Täydennyspyyntö 28.9.2012 19.10.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-10-19 2 / 6 Ympäristölupahakemuksen täydennys Pohjois-Suomen
Lukion kemia 3, Reaktiot ja energia. Leena Piiroinen Luento 2 2015
 Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Tutkittua tietoa. Tutkittua tietoa 1
 Tutkittua tietoa T. Dybå, T. Dingsøyr: Empirical Studies of Agile Software Development : A Systematic Review. Information and Software Technology 50, 2008, 833-859. J.E. Hannay, T. Dybå, E. Arisholm, D.I.K.
Tutkittua tietoa T. Dybå, T. Dingsøyr: Empirical Studies of Agile Software Development : A Systematic Review. Information and Software Technology 50, 2008, 833-859. J.E. Hannay, T. Dybå, E. Arisholm, D.I.K.
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
Eksimeerin muodostuminen
 Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Vanadiinin maaperäkemiaan liittyvä riskinarviointi
 Vanadiinin maaperäkemiaan liittyvä riskinarviointi 29.3.212 MUTKU-PÄIVÄT Noora Manninen ja Mirva Kauppinen (ohjaus Inka Reijonen, MMM) Maaperä- ja ympäristötiede Elintarvike- ja ympäristotieteiden laitos,
Vanadiinin maaperäkemiaan liittyvä riskinarviointi 29.3.212 MUTKU-PÄIVÄT Noora Manninen ja Mirva Kauppinen (ohjaus Inka Reijonen, MMM) Maaperä- ja ympäristötiede Elintarvike- ja ympäristotieteiden laitos,
Tiedekunta/Osasto Fakultet/Sektion Faculty Valtiotieteellinen tiedekunta
 Tiedekunta/Osasto Fakultet/Sektion Faculty Valtiotieteellinen tiedekunta Laitos Institution Department Politiikan ja talouden tutkimuksen laitos Tekijä Författare Author Virta, Mikko Antero Työn nimi Arbetets
Tiedekunta/Osasto Fakultet/Sektion Faculty Valtiotieteellinen tiedekunta Laitos Institution Department Politiikan ja talouden tutkimuksen laitos Tekijä Författare Author Virta, Mikko Antero Työn nimi Arbetets
Projektisuunnitelma. (välipalautukseen muokattu versio) Vesiprosessin sekvenssiohjelmointi ja simulointiavusteinen testaus
 Projektisuunnitelma (välipalautukseen muokattu versio) Vesiprosessin sekvenssiohjelmointi ja simulointiavusteinen testaus Ville Toiviainen Tomi Tuovinen Lauri af Heurlin Tavoite Projektin tarkoituksena
Projektisuunnitelma (välipalautukseen muokattu versio) Vesiprosessin sekvenssiohjelmointi ja simulointiavusteinen testaus Ville Toiviainen Tomi Tuovinen Lauri af Heurlin Tavoite Projektin tarkoituksena
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä
 Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
Arvokkaiden yhdisteiden tuottaminen kasveissa ja kasvisoluviljelmissä Siirtogeenisiä organismeja käytetään jo nyt monien yleisten biologisten lääkeaineiden valmistuksessa. Esimerkiksi sellaisia yksinkertaisia
Elintarviketeollisuuden hapan vaahtopesuneste
 P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
TKK, TTY, LTY, OY, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 31.5.2006
 TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
ORGAANINEN KEMIA. = kemian osa-alue, joka tutkii hiilen yhdisteitä KPL 1. HIILI JA RAAKAÖLJY
 ORGAANINEN KEMIA = kemian osa-alue, joka tutkii hiilen yhdisteitä KPL 1. HIILI JA RAAKAÖLJY Yleistä hiilestä: - Kaikissa elollisen luonnon yhdisteissä on hiiltä - Hiilen määrä voidaan osoittaa väkevällä
ORGAANINEN KEMIA = kemian osa-alue, joka tutkii hiilen yhdisteitä KPL 1. HIILI JA RAAKAÖLJY Yleistä hiilestä: - Kaikissa elollisen luonnon yhdisteissä on hiiltä - Hiilen määrä voidaan osoittaa väkevällä
Bensiiniä voidaan pitää hiilivetynä C8H18, jonka tiheys (NTP) on 0,703 g/ml ja palamislämpö H = kj/mol
 Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
NUKLEOTIDITRIMEERISYNTEESIN OPTIMOINTI
 NUKLEOTIDITRIMEERISYNTEESIN OPTIMOINTI 5 -HYDROKSYYLISUOJARYHMÄT OLIGONUKLEOTIDISYNTETIIKASSA Pro gradu -tutkielma Ellinoora Koskinen Helsingin yliopisto Orgaanisen kemian laboratorio Toukokuu 2017 HELSINGIN
NUKLEOTIDITRIMEERISYNTEESIN OPTIMOINTI 5 -HYDROKSYYLISUOJARYHMÄT OLIGONUKLEOTIDISYNTETIIKASSA Pro gradu -tutkielma Ellinoora Koskinen Helsingin yliopisto Orgaanisen kemian laboratorio Toukokuu 2017 HELSINGIN
13. Biomolekyylit. 1. Hiilihydraatit
 13. Biomolekyylit. 1. iilihydraatit 13.1. iilihydraattien rakenne ja konfigiraatiot iilihydraateilla tarkoitetaan polyhydroksiketoneja ja aldehydejä, joita nimitetään yleisesti sokereiksi. iilihydraatit
13. Biomolekyylit. 1. iilihydraatit 13.1. iilihydraattien rakenne ja konfigiraatiot iilihydraateilla tarkoitetaan polyhydroksiketoneja ja aldehydejä, joita nimitetään yleisesti sokereiksi. iilihydraatit
Reaktiosarjat
 Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
782630S Pintakemia I, 3 op
 782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
7. Valukappaleiden suunnittelu keernojen käytön kannalta
 7. Valukappaleiden suunnittelu keernojen käytön kannalta Pekka Niemi Tampereen ammattiopisto Keernoja käytetään valukappaleen muotojen aikaansaamiseksi sekä massakeskittymien poistoon. Kuva 23 A D. Ainekeskittymän
7. Valukappaleiden suunnittelu keernojen käytön kannalta Pekka Niemi Tampereen ammattiopisto Keernoja käytetään valukappaleen muotojen aikaansaamiseksi sekä massakeskittymien poistoon. Kuva 23 A D. Ainekeskittymän
Uutta liiketoimintaa jätteestä tuhkien modifiointi ja geopolymerisointi
 Uutta liiketoimintaa jätteestä tuhkien modifiointi ja geopolymerisointi Tuhkasta timantteja Liiketoimintaa teollisista sivutuotteista ja puhtaasta energiasta Peittoon kierrätyspuisto -hanke Yyterin kylpylähotelli,
Uutta liiketoimintaa jätteestä tuhkien modifiointi ja geopolymerisointi Tuhkasta timantteja Liiketoimintaa teollisista sivutuotteista ja puhtaasta energiasta Peittoon kierrätyspuisto -hanke Yyterin kylpylähotelli,
Kaivosten Ympäristöhaitat Vesistöille and Niiden Teknologiset Ratkaisut. Professori Simo O. Pehkonen Ympäristötieteiden Laitos UEF (Kuopio)
 Kaivosten Ympäristöhaitat Vesistöille and Niiden Teknologiset Ratkaisut Professori Simo O. Pehkonen Ympäristötieteiden Laitos UEF (Kuopio) Taustaa Taustaa Elohopea Riski Talvivaaran pohjavesituloksia,
Kaivosten Ympäristöhaitat Vesistöille and Niiden Teknologiset Ratkaisut Professori Simo O. Pehkonen Ympäristötieteiden Laitos UEF (Kuopio) Taustaa Taustaa Elohopea Riski Talvivaaran pohjavesituloksia,
Kestävä sanitaatio Juomavesi
 Kestävä sanitaatio Juomavesi 11.2.2015 Kepa, Helsinki Vesa Arvonen Suomen ympäristöopisto SYKLI vesa.arvonen@sykli.fi Esityksen sisältö Hyvä talousvesi Veden hankinta Veden käsittely 1 Hyvä talousvesi
Kestävä sanitaatio Juomavesi 11.2.2015 Kepa, Helsinki Vesa Arvonen Suomen ympäristöopisto SYKLI vesa.arvonen@sykli.fi Esityksen sisältö Hyvä talousvesi Veden hankinta Veden käsittely 1 Hyvä talousvesi
Lääketiede Valintakoeanalyysi 2015 Fysiikka. FM Pirjo Haikonen
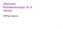 Lääketiede Valintakoeanalyysi 5 Fysiikka FM Pirjo Haikonen Fysiikan tehtävät Väittämä osa C (p) 6 kpl monivalintoja, joissa yksi (tai useampi oikea kohta.) Täysin oikein vastattu p, yksikin virhe/tyhjä
Lääketiede Valintakoeanalyysi 5 Fysiikka FM Pirjo Haikonen Fysiikan tehtävät Väittämä osa C (p) 6 kpl monivalintoja, joissa yksi (tai useampi oikea kohta.) Täysin oikein vastattu p, yksikin virhe/tyhjä
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
TEKNISET TIEDOT. ISO 6432 minisylinterit Ø 8-40 mm
 ISO 6432 minisylinterit Ø 8-40 mm Univerin minisylinterien kehitystyöhön on hyödynnetty vuosien tutkimustyö ja tuotekehityksen saavutukset. Tuloksena on luotettava tuote, joka soveltuu kaikkein vaativimmankin
ISO 6432 minisylinterit Ø 8-40 mm Univerin minisylinterien kehitystyöhön on hyödynnetty vuosien tutkimustyö ja tuotekehityksen saavutukset. Tuloksena on luotettava tuote, joka soveltuu kaikkein vaativimmankin
