Samuli Korhonen FOSFORIN POISTAMINEN VEDESTÄ
|
|
|
- Lasse Pakarinen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 Samuli Korhonen FOSFORIN POISTAMINEN VEDESTÄ Kemiantekniikan koulutusohjelma 2015
2 FOSFORIN POISTAMINEN VEDESTÄ Korhonen Samuli Satakunnan ammattikorkeakoulu Kemiantekniikan koulutusohjelma Toukokuu 2015 Ohjaaja: Hannelius Timo, lehtori, SAMK Sivumäärä: 18 Liitteitä: 3 Asiasanat: fosfori, kalkki, saostus TIIVISTELMÄ Opinäytetyön tavoitteena oli tutkia kalkin (CaO) soveltuvuutta fosforin (P) kemialliseen saostamiseen vesinäytteistä. Kokeita varten tuli valita helppo ja luotettava menetelmä fosforipitoisuuden määrittämiseksi. Menetelmäksi valittiin SFS 3025 Veden fosfaatin määritys. SFS-standardin luotettavuutta testattiin tekemällä liuoksia, joiden fosforipitoisuus oli tiedossa ja määrittämällä standardin mukaan niiden pitoisuus. Mitattiin ja laskettiin pitoisuudet ja todettiin tulosten olevan luotettavia. Testattiin myös oliko analysointiviiveellä huoneenlämmössä tai jäähdytyksessä (5ºC) merkitystä tuloksiin. Tulosten perusteella analysointi tuli suorittaa ohjeiden mukaisen reagointiajan jälkeen. Saostus kokeessa lisättiin fosforiliuokseen kalkkia tarvittava määrä ja annettiin liuoksen reagoinnin jälkeen sedimentoitua yön yli. Reagoinnin ja sedimentoinnin jälkeen saatiin valkoinen sakka liuoksen pohjalle ja tuloksista voitiin todeta, että kalkki saosti vesiliuoksen fosfaatista jopa 88 prosenttia, kun käytettiin 15 minuutin viiveaikaa. Todettiin, että saostusreaktiolle on varattava riittävästi aikaa.
3 REMOVING PHOSPHORUS FROM WATER Korhonen Samuli Satakunta University of Applied Sciences Degree Programme in Chemical Engineering May 2015 Supervisor: Hannelius Timo, senior lecturer, SAMK Number of pages: 18 Appendices: 3 Keywords: phosphorus, lime, precipitation ABSTRACT The purpose of this thesis was to study suitability of lime (CaO) as a chemical precipitator for phosphorus (P) in water. Determination method of phosphorus concentration in water sample has to be reliable and easy to do. Selected method was SFS 3025 Determination of phosphate in water. Reliability of SFS-standard was studied by preparing different phosphorus solutions and analyzing the solutions with this method. Concentration was measured and calculated and the results were found reliable. Also analysis lag time was checked at room temperature and at lowered temperature (5ºC). It was noticed that the samples should be analyzed within the time determined in analysis instructions. Precipitation of phosphate with burnt lime (CaO) as insoluble calcium phosphate was studied. Results indicated that sufficient reaction and sedimentation time for deposit is about 1 day. White solid phase is clearly separated on the bottom leaving visually clear water layer above it. Lime lowered phosphorus concentration in water even by 88 percent.
4 SISÄLLYS 1 JOHDANTO FOSFORIN ESIINTYMINEN Fosforin esiintyminen yleisesti Fosforin merkitys vesistöissä Fosforin poistaminen FOSFORIN MÄÄRITYSMENETELMÄ Käytetty menetelmä Menetelmän testaukset Fosforipitoisuuden testaaminen Analysointiviiveen testaaminen Analysointiviiveen testaaminen jäähdytyksellä FOSFORIN POISTAMINEN SAOSTAMALLA Saostaminen ja saostamiseen käytetty kemikaali Saostamiskokeet Kalkki saostajana sovellettuna haja-asutusalueelle YHTEENVETO JA VIRHEARVIOINTI LÄHTEET LIITTEET LIITE 1A ja 1B FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 2A ja 2B FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 3A ja 3B FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ
5 5 1 JOHDANTO Fosforin poistaminen vedestä on tärkeää, koska jos fosforia tai muita ravinteita (kuten typpeä) joutuu vesistöihin liikaa, aiheuttaa se rehevöitymistä. Haja-asutuksen jätevesiä tulee puhdistaa huolellisesti rehevöinnin estämiseksi. Fosforia voidaan poistaa jätevedestä erimerkiksi kemiallisella saostamisella ja tämä valittiin opinnäytetyön aiheeksi. Saostuskemikaaliksi valittiin kalkki, sillä se on edullista ja se myös mahdollisen saostamisen lisäksi neutraloisi jätevettä samalla. Fosforin määritysmenetelmäksi tuli valita luotettava menetelmä, joka olisi helppo toteuttaa. Yleisesti ollaan käytetty menetelmiä, joissa molybdaattireagenssi saa fosforiliuoksen sinertymään sitä enemmän mitä enemmän fosforia liuoksessa on. Sinertyneestä näytteestä mitataan absorbanssi, joka korreloi fosfaattipitoisuuden kanssa. Näitä menetelmiä on monia, kuten SFS3025 Veden fosfaatin määritys tai SFS3026 Kokonaisfosforin määritys. Näillä kahdella menetelmällä ei ole kovin suuria eroavaisuuksia. Kokonaisfosforin määrityksessä näytteet asetetaan autoklaaviin, mutta veden fosfaatin määrityksessä tätä ei tarvitse tehdä. Päätettiin valita fosforin määritysmenetelmäksi SFS3025 Veden fosfaatin määritys, sillä fosfori yleensä esiintyy liuoksissa fosfaattina. Valitun menetelmän luotettavuutta tuli testata ennen kuin siirryttiin itse kalkkisaostuskokeisiin.
6 6 2 FOSFORIN ESIINTYMINEN 2.1 Fosforin esiintyminen yleisesti Fosforia tarvitsevat niin kasvit kuin ihmisetkin ja maanviljelyksessä ei tunneta ainetta, joka pystyisi korvaamaan sen. Näin ollen fosforin saanti ja olemassa olo on tärkeää kaikelle elolliselle. Fosforin käyttö maataloudessa on hyvin tärkeää, sillä se edistää kasvien kasvua ja lisää siten ruoantuotantoa. Fosforin käyttö maanviljelyssä on oltava oikeassa mittakaavassa, sillä liian pieni käyttö jättää sadon liian pieneksi ja liian suuri käyttö aiheuttaa päästöjä vesistöihin ja lisää rehevöitymistä. Fosforia esiintyy luonnossa paljon, mutta se ei yleensä esiinny sellaisessa muodossa että sitä voitaisiin käyttää suoraan. Kallioperästä valmistettu fosfori on ollut fosforin päälähteenä jo 1950-luvusta lähtien. Ennen sitä käytettiin fosforin raaka-aineena luujauhoa ja ulosteita. Noin 35 maata valmistaa kallioperästä fosforia, suurin tuottaja on Marokko. Yleisin luonnossa esiintyvä fosforimineraali on apatiitti (Ca 10 (PO 4 ) 6 (OH,F,Cl) 2 ). Apatiittia louhitaan Suomessa Siilinjärvellä ja Yara Suomi Oy:llä on siellä fosforihappotehdas. /1/ 2.2 Fosforin merkitys vesistöissä Jos valuma-alueelta tulee liikaa fosforia verrattuna järvien normaaliin fosforimäärään, aiheuttaa se järvissä rehevöitymistä. Fosfori on usein järvissä minimiravinteena ja sen lisääntyessä levien ja kasvien kasvu nopeutuu ja lisääntyy. Rehevöityvässä järvessä kasvien tarvittavien ravinteiden määrä kasvaa, jolloin rantaja vesikasvillisuus sekä kasviplankton runsastuvat. Bakteerit kuluttavat enemmän happea runsaamman ravinnon takia ja tämä voi johtaa talvella happikatoon järvessä. /2/ Fosfori on siis merkittävä kasviravinne. Jos tätä ei olisi, kiertäisi fosfori ekosysteemissä tuottajista kuluttajiin ja lopulta fosfori sedimentoituu vesistöjen pohjalle. Jos fosfori pysyy hapellisissa oloissa, on se sitoutuneena pohjasedimenttiin. Rehevässä järvessä levämassat vajoavat järven pohjaan kuluttaen hajotessaan happea pohjan läheisyydestä.
7 7 Kun happipitoisuus pienenee pohjassa, alkaa fosforia vapautua sedimentistä veteen ja näin ollen järvi kuormittaa itseään. Kaivostoiminta, maanviljely ja jätevedet hajaasutusalueilla lisäävät fosforin määrää vesistöissä. /3/ 2.3 Fosforin poistaminen Fosforia voidaan poistaa vedestä saostamalla se niukkaliukoisena suolana. Esimerkiksi ferro (Fe 2+ )-, ferri (Fe 3+ ) ja kalsium (Ca 2+ ) reagoivat fosfaatin (PO 3-4 ) kanssa muodostaen hyvin niukkaliukoista rauta- ja kalsiumfosfaattia reaktioyhtälöiden (1), (2) ja (3) mukaisesti. 3 Fe 2+ (aq) + 2 H 2 O(l) + 2 PO 4 3- (aq) Fe 3 (PO 4 ) 2 2 H 2 O(s) (1) Fe 3+ (aq) + PO 4 3- (aq) Fe(PO 4 )(s) (2) 3 Ca 2+ (aq) + 2 PO 4 3- (aq) Ca 3 (PO 4 ) 2 (s) (3) Kidevedellinen ferrofosfaatti on käytännöllisesti katsoen liukenematon. Ferrisulfaattia on menestyksellisesti kokeiltu esim. ojavesien liukoisen fosforin poistossa, /4/, jossa raportoitiin jopa 91 %:n reduktioista. Kalsiumfosfaatin vesiliukoisuus on vain n g/l, /5/.
8 8 3 FOSFORIN MÄÄRITYSMENETELMÄ 3.1 Käytetty menetelmä Fosforipitoisuuden määrittämiseen käytettiin laboratoriossa SFS-standardia 3025 Veden fosfaatin määritys. Standardi on tarkoitettu veden fosfaattipitoisuuden määrittämiseen. Sitä voidaan käyttää lähes kaikenlaisille vesille, muttei kuitenkaan teollisuuden jätevesille, joissa on paljon orgaanista ainetta. Menetelmä perustuu siihen, että liuoksessa, joka sisältää rikkihappoa noin 0,2mol/l, muodostaa ortofosfaatti molybdaatin (Mo) ja kolmiarvoisen antimonin kanssa antimoni-12- fosforimolybdeenihappoa. Askorbiinihappo (C 6 H 8 O 6 ) pelkistää sen siniseksi kolloidiseksi kompleksiyhdisteeksi. Ortofosfaattipitoisuus on verrannollinen kompleksiyhdisteen absorbanssiin, joka mitataan aallonpituudella 880nm. Määritystä varten tehdään fosfaatin työliuoksella pitoisuuksilla 10, 20, 50, 100, 250, 500 ja 750μg P/l vertailukäyrä, jonka suoran yhtälöstä voidaan laskea näytteen absorbanssin perusteella näytteen fosforipitoisuus. Lisäksi tehdään kestävöimättömässä tapauksessa ionivaihdetusta vedestä nollanäyte, jonka absorbanssi vähennetään kaikista muista mitatuista absorbansseista. /6/ Yleensä menetelmää käytetään kestävöidyille näytteille, mutta laboratorissa tutkittiin kokeellisia fosforiliuoksia, joten näytteitä ei tarvinnut kestävöidä. Menetelmän mukaan mitataan absorbanssi reagenssi lisäysten jälkeen aikaisintaan 10 minuutin ja viimeistään 30 minuutin kuluttua. Silloin sinisen värin muodostuminen ja absorbanssiarvot ovat luotettavia. 3.2 Menetelmän testaukset Ennen fosforin poistamiskokeita tutkittiin fosforipitoisuuden määritysmenetelmän luotettavuutta. Ensin tehtiin vertailukäyrä ohjeiden mukaan ja sitten tehtiin liuos, jonka fosforipitoisuus tiedettiin ja mitattiin absorbanssi. Laskettiin suoran yhtälöstä absorbanssin mukainen fosforipitoisuus ja verrattiin sitä teoreettiseen pitoisuuteen. Lisäksi tutkittiin onko absorbanssimittauksen ajankohdalla merkitystä mittaamalla absorbanssit kalibrointiliuoksista heti, 15 minuutin, 30 minuutin ja tunnin päästä ja
9 9 vertailtiin vertailukäyriä keskenään. Lisäksi testattiin, onko liuosten jäähdyttämisellä noin 5-asteiseksi vaikutusta sinisen värin muodostumiseen ja vertailukäyrän pysymiseen samanlaisena kuin standardin mukaisilla analysointiviiveillä Fosforipitoisuuden testaaminen Menetelmän luotettavuutta näytteen fosforipitoisuuden määrittämisessä testattiin liuoksella, joka tehtiin Na 2 HPO 4 x 2 H 2 O -yhdistettä käyttäen. Fosforin määrä prosentteina yhdisteessä saatiin moolimassoista laskemalla: M(P)/M(Na 2 HPO 4 x 2 H 2 O) = 30,97g/mol / 177,99g/mol = 0,174 (4) Näin ollen, haluttaessa liuos jonka fosforipitoisuus on 10mg/l, tuli Na 2 HPO 4 x 2 H 2 O -yhdistettä liuottaa litraan: X * 0,174 = 10mg X = 57,47mg = 0,575g Koska 10mg/l fosforia menee yli vertailukäyrän suurimman hyväksytyn arvon, tehtiin liuoksesta vielä kaksi laimennosta, joiden pitoisuuksiksi asetettiin 0,38mg/l (S1) ja 0,63mg/l (S2). Vertailukäyrä tehtiin työliuoksen laimennoksilla ja saatiin seuraavanlaisia arvoja 15min päästä reagenssien lisäyksestä: Taulukko 1. Mittaustulokset fosforipitoisuuden testaamiseksi Pitoisuus µg P/L Absorbanssi 0-näyte , , , , , , ,489 S1 0,262 S2 0,426
10 10 Työliuoksen absorbanssien perusteella tehtiin vertailukäyrä: Kuva 1. Vertailukäyrä 15 min reagenssien lisäyksen jälkeen Työliuoksen 20µg/L absorbanssi jätettiin käyrästä pois epäluotettavana. Suoran yhtälöstä saadaan laskettua näytteiden (S1 ja S2) absorbanssien mukainen fosforipitoisuusarvo. Pitoisuuksiksi saatiin: 0,262 = 0,0006*S1 S1= 0,262/0,0006= 437µg/L (vertaa 380 µg/l) 0,426 = 0,0006*S2 S2= 0,426/0,0006= 710µg/L (vertaa 630 µg/l) Pitoisuudet ovat hieman korkeammat kuin teoreettisesti, mutta ero ei kuitenkaan ole niin suuri, etteikö tuloksia voisi pitää luotettavina. Samoja näytteitä (S1 ja S2) käytettiin myös tutkittaessa analysointiviiveen vaikutusta mittausmenetelmän tarkkuuteen. Näytteiden pitoisuudet ovat laskettu seuraavassa osiossa taulukoihin valmiiksi.
11 Analysointiviiveen testaaminen Tehtiin vertailukäyrää varten fosforin työliuoksesta laimennokset ja lisättiin reagenssit sekä niihin että näytteisiin S1 ja S2. Absorbanssit mitattiin heti, 15min, 30min ja 1h kuluttua ja arvot olivat seuraavanlaisia. Taulukko 2. Vertailukäyrän absorbanssit eri analysointiviiveillä Pitoisuus µg P/L Absorbanssi <5min Absorbanssi 15min kuluttua Absorbanssi 30min Absorbanssi 1h kuluttua kuluttua kuluttua 0-näyte ,027 0,012 0,021 0, ,041 0,01 0,017 0, ,058 0,026 0,034 0, ,09 0,057 0,065 0, ,181 0,15 0,16 0, ,327 0,309 0,32 0, ,464 0,489 0,479 0,697 S1 (pitoisuus μg/l) 0,2 (285) 0,262 (445) 0,276 (451) 0,436 (507) S2 (pitoisuus μg/l) 0,407 (630) 0,426 (718) 0,428 (704) 0,527 (609) Arvoista tehdyt vertailukäyrät löytyvät liitteestä 1. Käyristä nähdään heti, että heti mitatuissa, 15 minuutin kuluttua mitatuissa ja 30 minuutin kuluttua mitatuissa on suoran yhtälö suurin piirtein sama, kun taas 1 tunnin kuluttua mitatuissa suoran yhtälö on täysin eri ja mitatut arvot eivät sijoitu lähellekään saatua suoraa. Käyrien suoran yhtälöön on jätetty y= ax + b arvo b, jotta nähdään paremmin eroavatko käyrät toisistaan. Tuntemattomien näytteiden arvoja mitatessa käyrät on pakotettava menemään origon kautta, jolloin yhtälö olisi kaikissa y = 0,0006x paitsi 1 tunnin kuluttua mitatussa y = 0,0009x. Kuitenkin alle 5 minuutin kuluttua mitatussa käyrässä ovat näytteiden S1 ja S2 täysin erilaiset kuin 15 minuutin kuluttua mitatussa ja 30 minuutin kuluttua mitatussa. Pienillä fosforipitoisuuksilla alle 5 minuutin kuluttua mitatut absorbanssit olivat selvästi myöhemmin mitattuja suurempia, reagenssit eivät olleet välttämättä reagoineet tarpeeksi.
12 12 Liitteestä 2 löytyy sama testi uudelleen tehtynä, analysointiviiveinä 30 minuuttia, 1 tunti ja 2 tuntia. Arvot olivat seuraavanlaisia (jos nollanäytteen arvo ei ollut 0, on mitatuista arvoista on vähennetty valmiiksi nollanäytteen arvo). Taulukko 3. Vertailukäyrän absorbanssit eri analysointiviiveillä Pitoisuus µg P/L Absorbanssi 30min kuluttua Absorbanssi 1h kuluttua Absorbanssi 2h kuluttua 0-näyte 0 0,001 0, ,015 0,015 0, ,014 0,017 0, ,03 0,038 0, ,064 0,074 0, ,16 0,169 0, ,324 0,333 0, ,479 0,489 0,477 S1 (pitoisuus μg/l) 0,275 (456) 0,283 (458) 0,274 (448) S2 (pitoisuus μg/l) 0,426 (708) 0,433 (708) 0,427 (700) Liitteen 2 vertailukäyristä nähdään, että tällä kertaa suorien yhtälöt ovat lähempänä toisiaan, vaikka reagenssien annettiin reagoida jopa kaksikin tuntia. Näytteiden S1 ja S2 arvot ovat kaikista käyrien yhtälöistä laskettuna lähes samat. Kuitenkin huomataan y= ax + b arvosta b, että 30 minuutin kohdalla mitattu käyrä kulkee kaikkein lähimpää origoa ja on näin ollen luotettavin näistä kolmesta käyrästä Analysointiviiveen testaaminen jäähdytyksellä Jäähdytystä testattiin absorbanssien mittauksessa eri analysointiviiveillä siten, että työliuoksesta tehdyt liuokset ja näytteet laitettiin korkillisiin lasipulloihin reagenssi lisäysten jälkeen ja lasipurkit upotettiin sangossa olevaan 5ºC-asteiseen veteen. Absorbanssit mitattiin 30 minuutin, tunnin ja 2 tunnin kuluttua. Liitteessä 3 on saadut
13 13 vertailukäyrät. Saatiin seuraavanlaisia arvoja (nollanäytteen arvo on vähennetty muista arvoista). Taulukko 4. Vertailukäyrän absorbanssit eri analysointiviiveillä liuosten ollessa jäähdytyksessä Pitoisuus/Näyte Absorbanssi 30min kuluttua Absorbanssi 1h kuluttua Absorbanssi 2h kuluttua 0-näyte 0 0,008 0, ,012 0,01 0, ,016 0,013 0, ,035 0,033 0, ,068 0,065 0, ,167 0,168 0, ,341 0,339 0, ,501 0,502 0,491 S1 (pitoisuus μg/l) 0,271 (383) 0,274 (391) 0,269 (378) S2 (pitoisuus μg/l) 0,432 (631) 0,428 (611) 0,42 (594) Vertailukäyrien suorien yhtälöt liitteessä 3 ovat hyvin lähellä toisiaan. Yhden tunnin kuluttua reagenssien lisäyksestä mitattu vertailukäyrä menee kuitenkin lähimpää origoa. Mutta kun verrataan näytteitä S1 ja S2, niin 30 minuutin kuluttua mitatun vertailukäyrän suoran yhtälön perusteella lasketut arvot ovat lähimpänä teoreettisia arvoja. Kaksi tuntia reagenssien lisäyksen jälkeen mitatut arvot ovat kaikki pienempiä kuin muiden ajankohtien arvot. Jäähdytys ei näyttäisi juurikaan vaikuttavan reaktionopeuteen. Kuitenkin jäähdytyksellä saadut suoran yhtälöt ovat y = 0,0007x eivätkä y = 0,0006x kuten ilman jäähdytystä. Päädyttiin siihen lopputulokseen, että fosforia poistattaessa käytetään suoran yhtälöä y = 0,0006x, kun lasketaan absorbanssista fosforimääriä. Uusia vertailukäyriä ei tarvinnut tehdä, sillä kaikki käyrät olivat lähes samanlaisia.
14 14 4 FOSFORIN POISTAMINEN SAOSTAMALLA 4.1 Saostaminen ja saostamiseen käytetty kemikaali Yleensä fosforin saostamiseen käytetään alumiini- tai rautasuoloja, kuten alumiinikloridia, alumiinisulfaattia, ferrikloridisulfaattia tai ferrisulfaattia. /7/ Näiden pitäisi kemiallisen saostuksen tapahtuessa saada fosfori sedimentoitumaan nestefaasin pohjalle. Vaikka nuo kemikaalit ovatkin yleisempiä, tutkittiin laboratoriossa kalkin toimimista saostajana. Kalkki sitoo fosforin kalsiumfosfaatiksi: 3 CaO (s) + 3 H 2 O (l) 3 Ca(OH) 2 (aq) (5) 3 Ca(OH) 2 (aq) + 2 PO 3-4 (aq) Ca 3 (PO 4 ) OH - (aq) (6) Yhtälössä on otettu huomioon se osa reaktiosta, kun fosfaatti on jostakin yhdisteestä irronnut ioniksi liuokseen ja se reagoi sitten kalsiumhydroksidin kanssa. Testeissä käytettiin fosfaattiyhdisteenä Na 2 HPO 4 x 2 H 2 O-yhdistettä. Näin ollen reaktioyhtälöistä katsottuna kalkkia tulee 3/2 * Na 2 HPO 4 x 2 H 2 O-yhdisteen moolimäärä. Jos Na 2 HPO 4 x 2 H 2 O-yhdistettä on 1g, on se mooleina: n(na 2 HPO 4 x 2 H 2 O) = m/m = 1g / 178g/mol = 0,00562mol Silloin kalkkia tarvitaan: n(cao) = 3/2 * n(na 2 HPO 4 x 2 H 2 O) = 0,00843mol m(cao) = n * M = 0,00843mol * 56,1g/mol = 0,473g Kalkin ja Na 2 HPO 4 x 2 H 2 O-yhdisteen suhde on siis: 1g Na 2 HPO 4 x 2 H 2 O:a sitoo 0,473g kalkkia. 4.2 Saostamiskokeet Kalkin toimimista fosforin saostamiseen tutkittiin siten, että otettiin 2000ml dekantteriin 1000ml vettä ja käynnistettiin magneettisekoitus. Lisättiin Na 2 HPO 4 x 2 H 2 O-yhdistettä 0,5g (fosforipitoisuus 0,087g P/L) ja annettiin sen liueta kunnolla (30 minuuttia). Tämän jälkeen otettiin liuoksesta näyte (näyte 1) ja sitten lisättiin kalkkia ylimäärin: kalkkia tarvittiin 0,237g, joten sitä laitettiin hieman ylimäärin eli 0,3g (eli noin 1,3-kertainen määrä).
15 15 Annettiin kalkin reagoida kunnolla (30 minuuttia) ja sitten sammutettiin sekoitus. Sedimentoitumista annettiin tapahtua noin 30 minuuttia, jonka jälkeen otettiin näyte (näyte 2) pinnasta. Näytteet laimennettiin 1:500. Näytteitä otettiin 25ml lasipurkkeihin, lisättiin reagenssit ja otettiin absorbanssit 15 minuutin kuluttua. Saaduista arvoista pääteltiin, että sedimentoitumista ei ollut tapahtunut tarpeeksi, joten annettiin saostumisen jatkua seuraavaan päivään ja sitten otettiin uusi näyte (näyte 3). Näytteeseen 3 tehtiin tarvittavat reagenssi lisäykset ja absorbanssi mitattiin 15 minuutin kuluttua. Taulukko 5. Kalkkisaostuskokeen absorbanssit Pitoisuus/Näyte Absorbanssi 15min Pitoisuus mg P/L kuluttua (Laskettu käyrällä (suluissa arvo, kun 0- y=0,0006x) näyte on vähennetty) 0-näyte 1,263 - Näyte 1 1,397 (0,134) 112 (vrt. 87) Näyte 2 1,386 (0,123) näyte 2 1,444 - Näyte 3 1,459 (0,015) 13
16 16 Arvoista nähdään hyvinkin selvästi että fosforin määrä on laskenut noin 12 prosenttiin alkuperäisestä pitoisuudesta. Kuvasta nähdään että sedimentoitumista on todella tapahtunut. Kuva 2. Fosforin sedimentoituminen kalkkilisäyksen jälkeen. Pohjalle on erottunut valkoinen kalkki-kalsiumfosfaattisakka Kalkki saostajana sovellettuna haja-asutusalueelle Fosfori saatiin saostettua liuoksen pohjalle lisäämällä kalkkia fosforiliuokseen. Fosforia tuottaa yksi henkilö noin 2,2g päivässä. /8/ Vettä ihminen käyttää noin 180l päivässä. /9/ Tällöin olisi nelihenkisen perheen fosfori määrä 8,8g/720l (=12,2mg/l). Litraa kohden kalkkia menisi 33,2mg ja 720 litraan 23,95g. Jos haja-asutus alueella asuu noin 200 ihmistä (eli keskimäärin 50 nelihenkistä perhettä), tulee fosforia silloin 440g/56000l ja kalkkia tarvitaan silloin 1,2kg. Puutarhakalkinkin hinta on vain 8,5 /25kg, joten kalkkikustannukset eivät olisi kovinkaan suuria. /10/
17 17 5 YHTEENVETO JA VIRHEARVIOINTI Tulokset näyttivät varsin selvästi että kalkki sitoo fosforia vesiliuoksesta ja pienentää liuoksen fosforipitoisuutta huomattavasti. Fosforin määritys standardilla SFS3025 onnistuu, kun analysointiviive pidetään sellaisena kuin standardi sen määrittää. Viimeisissä mittauksissa absorbanssiarvot nousivat jopa nollanäytteessäkin hyvin suuriksi, yli 1,0abs. Aluksi ei saatu hyväksyttäviä tuloksia. Reagenssit uusittiin ja ionivaihdetun veden ph ja sähkönjohtokyky tarkistettiin. Sähkönjohtokyky oli luokkaa 15µS/cm mikä on korkeahko ionivaihdetulle vedelle. Veden ph oli hyväksyttävissä rajoissa. Reaktioastiat pestiin huolellisesti 4-M suolahapolla ja 2-M NaOH-liuoksella. Mikään näistä toimenpiteistä ei pienentänyt nollanäytteen ja näytteiden sinistä väriä. Kuitenkin pian tästä saatiin tuloksia, joihin voitiin luottaa ja päätettiin jatkaa määrityksiä. Suuri absorbanssi tuo toki virhettä mittauksiin, mutta mittauksista nähdään kuitenkin oikea suunta ja arvot ovat suurinpiirtein niinkuin pitääkin.
18 18 LÄHTEET 1. Elonkehä ry, Fosforia on käytettävä järkevästi (2011), Viitattu , 2. Biologian ja maantieteen opettajien liitto, Rehevöityminen, Viitattu , 3. Länsi-Uudenmaan vesi ja ympäristö ry, Fosforin kiertokulku (2013), Viitattu , 4. Närvänen, A ja Jansson, Håkan., Ferrisulfaatti saostaa ojavesistä liuenneet fosforit, Maaseudun tiede, 64. vuosikerta, N:o 2, s. 13 (2007) 5. Fabricius-Liukkonen ja Sundholm, G., Fysikaalisen kemian taulukoita, Otatieto, N:o 548 (1994) 6. Suomen standardoimisliitto, SFS3025 Veden fosfaatin määritys, SFS-Käsikirja Vedenlaatu osa 3 (2011) 7. Kemira Oyj, Järvien puhdistus, Viitattu , 8. Pekka Lahtinen, Haja-asutus alueiden jäteveden käsittely, opinnäytetyö, Tampereen ammattikorkeakoulu (2010), Viitattu , =1 9. Motiva Oy, Vedenkulutus (2015), Viitattu Hankkija Oy, Kekkilä Puutarhakalkki 25kg, Viitattu
19 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 1A
20 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 1B
21 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 2A
22 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 2B
23 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 3A
24 FOSFORIN MÄÄRITYKSEN VERTAILUKÄYRIÄ LIITE 3B
25
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA
 ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
FOSFORIPITOISUUS PESUAINEESSA KOHDERYHMÄ: Työ soveltuu yläkouluun kurssille elollinen luonto ja yhteiskunta. Lukiossa työ soveltuu parhaiten kurssille KE4. KESTO: Työ kestää n.1-2h MOTIVAATIO: Vaatteita
Vinkkejä opettajille ja odotetut tulokset SIVU 1
 Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
FOSFORIPITOISUUS PESUAINEESSA
 FOSFORIPITOISUUS PESUAINEESSA TAUSTAA Pehmeä vesi on hyvän pesutuloksen edellytys. Tavallisissa pesupulvereissa fosfori esiintyy polyfosfaattina, joka suhteellisen nopeasti hydrolisoituu vedessä ortofosfaatiksi.
FOSFORIPITOISUUS PESUAINEESSA TAUSTAA Pehmeä vesi on hyvän pesutuloksen edellytys. Tavallisissa pesupulvereissa fosfori esiintyy polyfosfaattina, joka suhteellisen nopeasti hydrolisoituu vedessä ortofosfaatiksi.
Spektrofotometria ja spektroskopia
 11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
Kokemuksia kemikaalikunnostuksista Lahden seudun järvillä. Ismo Malin Vesiensuojelupäällikkö Lahden ympäristöpalvelut
 Kokemuksia kemikaalikunnostuksista Lahden seudun järvillä Ismo Malin Vesiensuojelupäällikkö Lahden ympäristöpalvelut HS 11.11.2017 tiistai, 12. joulukuuta 2017 2 Kemiallisia käsittelyjä Oja Matjärvi Järvi
Kokemuksia kemikaalikunnostuksista Lahden seudun järvillä Ismo Malin Vesiensuojelupäällikkö Lahden ympäristöpalvelut HS 11.11.2017 tiistai, 12. joulukuuta 2017 2 Kemiallisia käsittelyjä Oja Matjärvi Järvi
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Rakennekalkki Ratkaisu savimaiden rakenneongelmiin VYR viljelijäseminaari 2018 Kjell Weppling ja Anne-Mari Aurola / Nordkalk Oy Ab
 Rakennekalkki Ratkaisu savimaiden rakenneongelmiin VYR viljelijäseminaari 2018 Kjell Weppling ja Anne-Mari Aurola / Nordkalk Oy Ab Sisältö 1. Rakennekalkituksen tausta mitä tiedämme? 2. Kalkkituotteet
Rakennekalkki Ratkaisu savimaiden rakenneongelmiin VYR viljelijäseminaari 2018 Kjell Weppling ja Anne-Mari Aurola / Nordkalk Oy Ab Sisältö 1. Rakennekalkituksen tausta mitä tiedämme? 2. Kalkkituotteet
TKK, TTY, LTY, OY, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 31.5.2006
 TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
peltovaltaiselta ja luonnontilaiselta valuma
 Ravinnehuuhtoumien muodostuminen peltovaltaiselta ja luonnontilaiselta valuma alueelta Tuloksia vedenlaadun seurannasta RaHa hankkeessa Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHahankkeen
Ravinnehuuhtoumien muodostuminen peltovaltaiselta ja luonnontilaiselta valuma alueelta Tuloksia vedenlaadun seurannasta RaHa hankkeessa Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHahankkeen
Heinijärven vedenlaatuselvitys 2016
 Heinijärven vedenlaatuselvitys 2016 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 13.12.2016 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin Helsingin yliopiston Lammin
Heinijärven vedenlaatuselvitys 2016 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 13.12.2016 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin Helsingin yliopiston Lammin
Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011
 Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto Johdanto Tämä raportti on selvitys Luoteis-Tammelan Heinijärven ja siihen laskevien ojien
Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto Johdanto Tämä raportti on selvitys Luoteis-Tammelan Heinijärven ja siihen laskevien ojien
Ei ole olemassa jätteitä, on vain helposti ja hieman hankalammin uudelleen käytettäviä materiaaleja
 Jätehuolto Ei ole olemassa jätteitä, on vain helposti ja hieman hankalammin uudelleen käytettäviä materiaaleja Jätteiden käyttötapoja: Kierrätettävät materiaalit (pullot, paperi ja metalli kiertävät jo
Jätehuolto Ei ole olemassa jätteitä, on vain helposti ja hieman hankalammin uudelleen käytettäviä materiaaleja Jätteiden käyttötapoja: Kierrätettävät materiaalit (pullot, paperi ja metalli kiertävät jo
 Vastaanottaja Ramboll Finland Niko Rissanen Asiakirjatyyppi Nitrifikaation ja hapenkulutuksen inhibitio - Tutkimusraportti Päivämäärä 22.2.2016 Viite 1510025001 KUUSAKOSKI OY RAJAVUOREN KAATO- PAIKKAVEDEN
Vastaanottaja Ramboll Finland Niko Rissanen Asiakirjatyyppi Nitrifikaation ja hapenkulutuksen inhibitio - Tutkimusraportti Päivämäärä 22.2.2016 Viite 1510025001 KUUSAKOSKI OY RAJAVUOREN KAATO- PAIKKAVEDEN
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Järviveden happamoitumiseen vaikuttavat tekijät. Tulokset: KaiHali-projekti
 Järviveden happamoitumiseen vaikuttavat tekijät Tulokset: 1.3.-31.8.2017 KaiHali-projekti Hanna Runtti 17.11.2017 Sisällysluettelo 1 Taustaa... 3 2 Tutkittavat järvivedet... 3 3 Koesuunnitelmat... 3 3.1
Järviveden happamoitumiseen vaikuttavat tekijät Tulokset: 1.3.-31.8.2017 KaiHali-projekti Hanna Runtti 17.11.2017 Sisällysluettelo 1 Taustaa... 3 2 Tutkittavat järvivedet... 3 3 Koesuunnitelmat... 3 3.1
Ohjeita opettamiseen ja odotettavissa olevat tulokset SIVU 1
 Ohjeita opettamiseen ja odotettavissa olevat tulokset SIVU 1 Toiminta aloitetaan johdattelulla. Tarkoituksena on rakentaa konteksti oppilaiden tutkimukselle ja kysymykselle (Boldattuna oppilaiden työohjeessa),
Ohjeita opettamiseen ja odotettavissa olevat tulokset SIVU 1 Toiminta aloitetaan johdattelulla. Tarkoituksena on rakentaa konteksti oppilaiden tutkimukselle ja kysymykselle (Boldattuna oppilaiden työohjeessa),
Olli-Matti Kärnä: UPI-projektin alustavia tuloksia kesä 2013 Sisällys
 Olli-Matti Kärnä: UPI-projektin alustavia tuloksia kesä 213 Sisällys 1. Vedenlaatu... 2 1.1. Happipitoisuus ja hapen kyllästysaste... 3 1.2. Ravinteet ja klorofylli-a... 4 1.3. Alkaliniteetti ja ph...
Olli-Matti Kärnä: UPI-projektin alustavia tuloksia kesä 213 Sisällys 1. Vedenlaatu... 2 1.1. Happipitoisuus ja hapen kyllästysaste... 3 1.2. Ravinteet ja klorofylli-a... 4 1.3. Alkaliniteetti ja ph...
UUDET LANNOITEFOSFORIN LÄHTEET
 UUDET LANNOITEFOSFORIN LÄHTEET Ari Väisänen 20.9.2017 TUTKIMUSRYHMÄMME HANKKEITA Harvinaisten maametallien talteenotto puun- ja turpeenpolton tuhkasta (Jyväskylän Energia Oy) INKI Innovatiivinen kiertotalous
UUDET LANNOITEFOSFORIN LÄHTEET Ari Väisänen 20.9.2017 TUTKIMUSRYHMÄMME HANKKEITA Harvinaisten maametallien talteenotto puun- ja turpeenpolton tuhkasta (Jyväskylän Energia Oy) INKI Innovatiivinen kiertotalous
KIRKNIEMEN PIKKUJÄRVEN VEDEN LAATU TALVELLA Åke Lillman Kirkniemen kartano Lohja
 8.3.2017 Åke Lillman Kirkniemen kartano 08800 Lohja KIRKNIEMEN PIKKUJÄRVEN VEDEN LAATU TALVELLA 2017 Vesinäytteet kahdelta havaintopaikalta otettiin 28.2.2017. Työ tehtiin Kirkniemen kartanon toimeksiannosta.
8.3.2017 Åke Lillman Kirkniemen kartano 08800 Lohja KIRKNIEMEN PIKKUJÄRVEN VEDEN LAATU TALVELLA 2017 Vesinäytteet kahdelta havaintopaikalta otettiin 28.2.2017. Työ tehtiin Kirkniemen kartanon toimeksiannosta.
Liuenneen silikaatin spektrofotometrinen määritys
 Liuenneen silikaatin spektrofotometrinen määritys 1. Työn periaate Liuenneen silikaatin määritys perustuu keltaisen silikomolybdeenihapon muodostumiseen. Keltainen kompleksi pelkistetään oksaalihapolla
Liuenneen silikaatin spektrofotometrinen määritys 1. Työn periaate Liuenneen silikaatin määritys perustuu keltaisen silikomolybdeenihapon muodostumiseen. Keltainen kompleksi pelkistetään oksaalihapolla
Alajärven ja Takajärven vedenlaatu
 Alajärven ja Takajärven vedenlaatu 1966-16 Alajärvi Alajärven vedenlaatua voidaan kokonaisuudessaan pitää hyvänä. Veden ph on keskimäärin 7,3 (Jutila 1). Yleisellä tasolla alusvesi on lievästi rehevää
Alajärven ja Takajärven vedenlaatu 1966-16 Alajärvi Alajärven vedenlaatua voidaan kokonaisuudessaan pitää hyvänä. Veden ph on keskimäärin 7,3 (Jutila 1). Yleisellä tasolla alusvesi on lievästi rehevää
Liite 1. Saimaa. Immalanjärvi. Vuoksi. Mellonlahti. Joutseno. Venäjä
 Liite 1 Saimaa Immalanjärvi Vuoksi Mellonlahti Joutseno Venäjä Liite 2 1 5 4 3 2 Liite 3 puron patorakennelma Onnelan lehto Onnelan lehto Mellonlahden ranta Liite 4 1/7 MELLONLAHDEN TILAN KEHITYS VUOSINA
Liite 1 Saimaa Immalanjärvi Vuoksi Mellonlahti Joutseno Venäjä Liite 2 1 5 4 3 2 Liite 3 puron patorakennelma Onnelan lehto Onnelan lehto Mellonlahden ranta Liite 4 1/7 MELLONLAHDEN TILAN KEHITYS VUOSINA
Saarijärven reitin järvien sinileväkartoitus. Iso Suojärvi Pyhäjärvi Kyyjärvi
 Saarijärven reitin järvien sinileväkartoitus Iso Suojärvi yhäjärvi Kyyjärvi Sinilevämittari Mittaussyvyys 30 cm Mittausvene Uusi mittarisuojus Kyyjärvellä Mittausmenetelmä äyte 1,5 sekunnin välein GS-Koordinaatit
Saarijärven reitin järvien sinileväkartoitus Iso Suojärvi yhäjärvi Kyyjärvi Sinilevämittari Mittaussyvyys 30 cm Mittausvene Uusi mittarisuojus Kyyjärvellä Mittausmenetelmä äyte 1,5 sekunnin välein GS-Koordinaatit
ISO-KAIRIN VEDEN LAATU Kesän 2015 tutkimus ja vertailu vuosiin 1978, 1980 ja 1992
 LUVY/149 4.8.215 Minna Sulander Ympäristönsuojelu, Vihti ISO-KAIRIN VEDEN LAATU Kesän 215 tutkimus ja vertailu vuosiin 1978, 198 ja 1992 Vihdin pohjoisosassa sijaitsevasta Iso-Kairista otettiin vesinäytteet
LUVY/149 4.8.215 Minna Sulander Ympäristönsuojelu, Vihti ISO-KAIRIN VEDEN LAATU Kesän 215 tutkimus ja vertailu vuosiin 1978, 198 ja 1992 Vihdin pohjoisosassa sijaitsevasta Iso-Kairista otettiin vesinäytteet
Kokemuksia suomalaisten järvien kemikaloinnista
 16.6.2017 Limnologi Reijo Oravainen Kokemuksia suomalaisten järvien kemikaloinnista Kokemäenjoen vesistön vesiensuojeluyhdistys ry REHEVYYDEN SYYT Tutkimukset ovat kiistatta osoittaneet, että pääravinteet
16.6.2017 Limnologi Reijo Oravainen Kokemuksia suomalaisten järvien kemikaloinnista Kokemäenjoen vesistön vesiensuojeluyhdistys ry REHEVYYDEN SYYT Tutkimukset ovat kiistatta osoittaneet, että pääravinteet
Jussi Klemola 3D- KEITTIÖSUUNNITTELUOHJELMAN KÄYTTÖÖNOTTO
 Jussi Klemola 3D- KEITTIÖSUUNNITTELUOHJELMAN KÄYTTÖÖNOTTO Opinnäytetyö KESKI-POHJANMAAN AMMATTIKORKEAKOULU Puutekniikan koulutusohjelma Toukokuu 2009 TIIVISTELMÄ OPINNÄYTETYÖSTÄ Yksikkö Aika Ylivieska
Jussi Klemola 3D- KEITTIÖSUUNNITTELUOHJELMAN KÄYTTÖÖNOTTO Opinnäytetyö KESKI-POHJANMAAN AMMATTIKORKEAKOULU Puutekniikan koulutusohjelma Toukokuu 2009 TIIVISTELMÄ OPINNÄYTETYÖSTÄ Yksikkö Aika Ylivieska
KALKKIA VEDENPUHDISTUKSEEN
 KALKKIA VEDENPUHDISTUKSEEN Vesi tärkein elintarvikkeemme SMA Mineral on Pohjoismaiden suurimpia kalkkituotteiden valmistajia. Meillä on pitkä kokemus kalkista ja kalkin käsittelystä. Luonnontuotteena kalkki
KALKKIA VEDENPUHDISTUKSEEN Vesi tärkein elintarvikkeemme SMA Mineral on Pohjoismaiden suurimpia kalkkituotteiden valmistajia. Meillä on pitkä kokemus kalkista ja kalkin käsittelystä. Luonnontuotteena kalkki
Veikö syksyn sateet ravinteet mennessään?
 Veikö syksyn sateet ravinteet mennessään? - Tuloksia vedenlaadun seurannasta RaHahankkeessa Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry Esityksen sisältö Vedenlaadun seuranta
Veikö syksyn sateet ravinteet mennessään? - Tuloksia vedenlaadun seurannasta RaHahankkeessa Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry Esityksen sisältö Vedenlaadun seuranta
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
Rinnakkaissaostuksesta biologiseen fosforinpoistoon
 Rinnakkaissaostuksesta biologiseen fosforinpoistoon Sakari Pitkäjärvi Huittisten puhdistamo oy 1 1 Perinteinen rinnakkaissaostus Fosfori saostetaan jätevedestä kemiallisesti Esimerkiksi ferrisulfaattia
Rinnakkaissaostuksesta biologiseen fosforinpoistoon Sakari Pitkäjärvi Huittisten puhdistamo oy 1 1 Perinteinen rinnakkaissaostus Fosfori saostetaan jätevedestä kemiallisesti Esimerkiksi ferrisulfaattia
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo. Luento 8 CHEM-A1250
 Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Varsinais-Suomen vesien tila: mitä vesistä mitataan ja mitä tulokset kertovat? Raisio Janne Suomela
 Varsinais-Suomen vesien tila: mitä vesistä mitataan ja mitä tulokset kertovat? Raisio 1.12.211 Janne Suomela Varsinais-Suomen päävesistöalueet Kiskonjoki Perniönjoki 147 km 2 Uskelanjoki 566 km 2 Halikonjoki
Varsinais-Suomen vesien tila: mitä vesistä mitataan ja mitä tulokset kertovat? Raisio 1.12.211 Janne Suomela Varsinais-Suomen päävesistöalueet Kiskonjoki Perniönjoki 147 km 2 Uskelanjoki 566 km 2 Halikonjoki
Ohjeita opettajille ja odotetut tulokset
 Ohjeita opettajille ja odotetut tulokset SIVU 1 Aktiviteetti alkaa toimintaan johdattelulla. Tarkoituksena on luoda konteksti oppilaiden tutkimukselle ja tutkimusta ohjaavalle kysymykselle (Boldattuna
Ohjeita opettajille ja odotetut tulokset SIVU 1 Aktiviteetti alkaa toimintaan johdattelulla. Tarkoituksena on luoda konteksti oppilaiden tutkimukselle ja tutkimusta ohjaavalle kysymykselle (Boldattuna
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
KaiHali & DROMINÄ hankkeiden loppuseminaari
 KaiHali & DROMINÄ hankkeiden loppuseminaari Kaivosvesien muuttamien vesistöjen aktiiviset puhdistusmenetelmät Esther Takaluoma / Kimmo Kemppainen, KAMK 04.12.2018 Aktiiviset puhdistusmenetelmät 1. Luontainen
KaiHali & DROMINÄ hankkeiden loppuseminaari Kaivosvesien muuttamien vesistöjen aktiiviset puhdistusmenetelmät Esther Takaluoma / Kimmo Kemppainen, KAMK 04.12.2018 Aktiiviset puhdistusmenetelmät 1. Luontainen
YTO-aineiden integrointi: Kemian toteutus Työskentely maatalousalalla tutkinnon osaan
 YTO-aineiden integrointi: Kemian toteutus 2017 - Työskentely maatalousalalla tutkinnon osaan Hämeen ammatti-instituutti, Mustiala Maatilatalouden osaamisala Lehtori Kirsi Lähde Osaamistavoitteet (OPS 2014)
YTO-aineiden integrointi: Kemian toteutus 2017 - Työskentely maatalousalalla tutkinnon osaan Hämeen ammatti-instituutti, Mustiala Maatilatalouden osaamisala Lehtori Kirsi Lähde Osaamistavoitteet (OPS 2014)
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
Ravinnehuuhtoumien mittaaminen. Kirsti Lahti ja Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry
 Ravinnehuuhtoumien mittaaminen Kirsti Lahti ja Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHa-hankkeen loppuseminaari 17.6.2014 18.6.2014 1 Mitä hankkeessa tavoiteltiin? Kehittää
Ravinnehuuhtoumien mittaaminen Kirsti Lahti ja Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHa-hankkeen loppuseminaari 17.6.2014 18.6.2014 1 Mitä hankkeessa tavoiteltiin? Kehittää
17VV VV 01021
 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
MÄDÄTYSJÄÄNNÖKSEN LABORATORIOTASON VALUMAVESIKOKEET
 MÄDÄTYSJÄÄNNÖKSEN LABORATORIOTASON VALUMAVESIKOKEET Biojäte- ja lietepohjainen Laura Kannisto 214 Bioliike-projektia (v. 213-214) rahoitetaan Etelä-Suomen EAKR-ohjelmasta SISÄLLYS 1 JOHDANTO... 1 2 KOEJÄRJESTELY...
MÄDÄTYSJÄÄNNÖKSEN LABORATORIOTASON VALUMAVESIKOKEET Biojäte- ja lietepohjainen Laura Kannisto 214 Bioliike-projektia (v. 213-214) rahoitetaan Etelä-Suomen EAKR-ohjelmasta SISÄLLYS 1 JOHDANTO... 1 2 KOEJÄRJESTELY...
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
KaiHali & DROMINÄ hankkeiden loppuseminaari
 KaiHali & DROMINÄ hankkeiden loppuseminaari Sedimentin geokemiallisten olojen muuttuminen kaivoskuormituksessa (KaiHali-projektin työpaketin 2 osatehtävä 3), Jari Mäkinen, Tommi Kauppila ja Tatu Lahtinen
KaiHali & DROMINÄ hankkeiden loppuseminaari Sedimentin geokemiallisten olojen muuttuminen kaivoskuormituksessa (KaiHali-projektin työpaketin 2 osatehtävä 3), Jari Mäkinen, Tommi Kauppila ja Tatu Lahtinen
Lumetuksen ympäristövaikutukset
 Lumetuksen ympäristövaikutukset KeMMI -osatutkimus Lumetus Lumetuksessa vesi paineilman avulla pieniksi pisaroiksi, jotka riittävän kylmässä jäätyvät ennen maahan laskeutumista Mm. IPCC ja OECD huomioineet
Lumetuksen ympäristövaikutukset KeMMI -osatutkimus Lumetus Lumetuksessa vesi paineilman avulla pieniksi pisaroiksi, jotka riittävän kylmässä jäätyvät ennen maahan laskeutumista Mm. IPCC ja OECD huomioineet
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
ISO HEILAMMEN VEDEN LAATU Kesän 2015 tutkimus ja vertailu aikaisempiin vuosiin
 LUVY/121 18.8.215 Lohjan kaupunki Ympäristönsuojelu ISO HEILAMMEN VEDEN LAATU Kesän 215 tutkimus ja vertailu aikaisempiin vuosiin Sammatin Iso Heilammen länsiosan 6 metrin syvänteeltä otettiin vesinäytteet
LUVY/121 18.8.215 Lohjan kaupunki Ympäristönsuojelu ISO HEILAMMEN VEDEN LAATU Kesän 215 tutkimus ja vertailu aikaisempiin vuosiin Sammatin Iso Heilammen länsiosan 6 metrin syvänteeltä otettiin vesinäytteet
KaliVesi hankkeen keskustelutilaisuus. KE klo 18 alkaen
 KaliVesi hankkeen keskustelutilaisuus KE 14.11.2018 klo 18 alkaen Ohjelma Tilaisuuden avaus Hannu Marttila Kalimenjoen vedenlaadun vaihtelu ja monitoroinnin tulokset Hannu Marttila Mitä jatkuvatoiminen
KaliVesi hankkeen keskustelutilaisuus KE 14.11.2018 klo 18 alkaen Ohjelma Tilaisuuden avaus Hannu Marttila Kalimenjoen vedenlaadun vaihtelu ja monitoroinnin tulokset Hannu Marttila Mitä jatkuvatoiminen
ROMUMETALLIA OSTAMASSA (OSA 1)
 ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
Neutraloituminen = suolan muodostus
 REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
VEDENLAADUN SEURANTA JA RAVINNEVALUMIEN EHKÄISY
 VEDENLAADUN SEURANTA JA RAVINNEVALUMIEN EHKÄISY TIINA TULONEN, SARI UUSHEIMO, LAURI ARVOLA, EEVA EINOLA Lammin biologinen asema, Helsingin yliopisto Ravinneresurssi päivä 11.4.2017 Mustiala HANKKEEN TAVOITE:
VEDENLAADUN SEURANTA JA RAVINNEVALUMIEN EHKÄISY TIINA TULONEN, SARI UUSHEIMO, LAURI ARVOLA, EEVA EINOLA Lammin biologinen asema, Helsingin yliopisto Ravinneresurssi päivä 11.4.2017 Mustiala HANKKEEN TAVOITE:
Kaitalammin (Hajakka) veden laatu Elokuu 2017
 4.9.2017 Karkkilan kaupunki, ympäristönsuojelu Kaitalammin (Hajakka) veden laatu Elokuu 2017 Karkkilan Hajakassa Kaupinojan valuma-alueella (23.087) sijaitsevan Kaitalammin vesinäytteet otettiin 3.8.2017
4.9.2017 Karkkilan kaupunki, ympäristönsuojelu Kaitalammin (Hajakka) veden laatu Elokuu 2017 Karkkilan Hajakassa Kaupinojan valuma-alueella (23.087) sijaitsevan Kaitalammin vesinäytteet otettiin 3.8.2017
Hollolan pienjärvien tila ja seuranta. Vesiensuojelusuunnittelija Matti Kotakorpi, Lahden ympäristöpalvelut
 Hollolan pienjärvien tila ja seuranta Vesiensuojelusuunnittelija Matti Kotakorpi, Lahden ympäristöpalvelut 2016 2017 2018 2019 2020 2021 Pienjärvien seuranta Pienjärvien vedenlaadun seuranta Hollolassa
Hollolan pienjärvien tila ja seuranta Vesiensuojelusuunnittelija Matti Kotakorpi, Lahden ympäristöpalvelut 2016 2017 2018 2019 2020 2021 Pienjärvien seuranta Pienjärvien vedenlaadun seuranta Hollolassa
Wiitaseudun Energia Oy jätevedenpuhdistamon ylimääräiset vesistövesinäytteet 10.4.2014
 Lausunto 8.5.2014 Wiitaseudun Energia Oy jätevedenpuhdistamon ylimääräiset vesistövesinäytteet 10.4.2014 Tausta: Kalastajat olivat 6.4.2014 tehneet havainnon, että jäällä oli tummaa lietettä lähellä Viitasaaren
Lausunto 8.5.2014 Wiitaseudun Energia Oy jätevedenpuhdistamon ylimääräiset vesistövesinäytteet 10.4.2014 Tausta: Kalastajat olivat 6.4.2014 tehneet havainnon, että jäällä oli tummaa lietettä lähellä Viitasaaren
Ravinnehuuhtoumien muodostuminen peltovaltaiselta ja luonnontilaiselta valumaalueelta
 Ravinnehuuhtoumien muodostuminen peltovaltaiselta ja luonnontilaiselta valumaalueelta - Tuloksia vedenlaadun seurannasta RaHahankkeessa Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHahankkeen
Ravinnehuuhtoumien muodostuminen peltovaltaiselta ja luonnontilaiselta valumaalueelta - Tuloksia vedenlaadun seurannasta RaHahankkeessa Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry RaHahankkeen
PUUJÄRVEN VEDEN LAATU Vuoden 2013 loppukesän tulokset ja vertailu vuoteen 2012
 LUVY/119 6.9.213 Puujärven VSY Olli Kilpinen Hulluksentie 1 e 25 243 Masala PUUJÄRVEN VEDEN LAATU Vuoden 213 loppukesän tulokset ja vertailu vuoteen 212 Näytteet Puujärven kahdelta syvännehavaintopaikalta
LUVY/119 6.9.213 Puujärven VSY Olli Kilpinen Hulluksentie 1 e 25 243 Masala PUUJÄRVEN VEDEN LAATU Vuoden 213 loppukesän tulokset ja vertailu vuoteen 212 Näytteet Puujärven kahdelta syvännehavaintopaikalta
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Sammatin Lihavajärven veden laatu Heinäkuu 2017
 10.8.2017 Lohjan kaupunki, ympäristönsuojelu Sammatin Lihavajärven veden laatu Heinäkuu 2017 Lohjan Sammatissa sijaitsevan Lihavan vesinäytteet otettiin 19.7.2017 Lohjan kaupungin ympäristönsuojeluosaston
10.8.2017 Lohjan kaupunki, ympäristönsuojelu Sammatin Lihavajärven veden laatu Heinäkuu 2017 Lohjan Sammatissa sijaitsevan Lihavan vesinäytteet otettiin 19.7.2017 Lohjan kaupungin ympäristönsuojeluosaston
Säynäislammin vedenlaatututkimus 2016
 5.9.2016 Karkkilan kaupunki, ympäristönsuojelu Säynäislammin vedenlaatututkimus 2016 Vesinäytteet Karkkilan itäosassa sijaitsevalta Säynäislammilta otettiin Karkkilan kaupungin ympäristönsuojeluosaston
5.9.2016 Karkkilan kaupunki, ympäristönsuojelu Säynäislammin vedenlaatututkimus 2016 Vesinäytteet Karkkilan itäosassa sijaitsevalta Säynäislammilta otettiin Karkkilan kaupungin ympäristönsuojeluosaston
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
Kemiaa tekemällä välineitä ja työmenetelmiä
 Opiskelijalle 1/4 Kemiaa tekemällä välineitä ja työmenetelmiä Ennen työn aloittamista huomioi seuraavaa Tarkista, että sinulla on kaikki tarvittavat aineet ja välineet. Kirjaa tulokset oikealla tarkkuudella
Opiskelijalle 1/4 Kemiaa tekemällä välineitä ja työmenetelmiä Ennen työn aloittamista huomioi seuraavaa Tarkista, että sinulla on kaikki tarvittavat aineet ja välineet. Kirjaa tulokset oikealla tarkkuudella
HUNTTIJÄRVEN VEDENLAADUNSEURANTA Eteläinen laskuoja
 1 LAUREA-AMMATTIKORKEAKOULU Hyvinkää HUNTTIJÄRVEN VEDENLAADUNSEURANTA Eteläinen laskuoja Heidi Rantala Syyskuu 2008 2 SISÄLLYS 1 JOHDANTO... 3 2 SÄHKÖNJOHTOKYKY... 3 3 VEDEN HAPPAMUUS... 4 4 VÄRILUKU...
1 LAUREA-AMMATTIKORKEAKOULU Hyvinkää HUNTTIJÄRVEN VEDENLAADUNSEURANTA Eteläinen laskuoja Heidi Rantala Syyskuu 2008 2 SISÄLLYS 1 JOHDANTO... 3 2 SÄHKÖNJOHTOKYKY... 3 3 VEDEN HAPPAMUUS... 4 4 VÄRILUKU...
Paskolammin vedenlaatututkimus 2016
 5.9.2016 Karkkilan kaupunki, ympäristönsuojelu Paskolammin vedenlaatututkimus 2016 Vesinäytteet Karkkilan Vuotinaisissa sijaitsevalta Paskolammilta otettiin Karkkilan kaupungin ympäristönsuojeluosaston
5.9.2016 Karkkilan kaupunki, ympäristönsuojelu Paskolammin vedenlaatututkimus 2016 Vesinäytteet Karkkilan Vuotinaisissa sijaitsevalta Paskolammilta otettiin Karkkilan kaupungin ympäristönsuojeluosaston
Espoon kaupunki Pöytäkirja 32. Ympäristölautakunta Sivu 1 / 1
 Ympäristölautakunta 13.03.2014 Sivu 1 / 1 2412/11.01.03/2012 32 Espoon vesistötutkimus vuonna 2013 Valmistelijat / lisätiedot: Ilppo Kajaste, puh. 043 826 5220 etunimi.sukunimi@espoo.fi Päätösehdotus Va.
Ympäristölautakunta 13.03.2014 Sivu 1 / 1 2412/11.01.03/2012 32 Espoon vesistötutkimus vuonna 2013 Valmistelijat / lisätiedot: Ilppo Kajaste, puh. 043 826 5220 etunimi.sukunimi@espoo.fi Päätösehdotus Va.
Tammelan Jäni- ja Heinijärven vedenlaatuselvitys v. 2017
 Tammelan Jäni- ja Heinijärven vedenlaatuselvitys v. 2017 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 11.12.2017 Johdanto Lammin biologinen asema selvitti Tammelan Jäni- ja Heinijärven sekä
Tammelan Jäni- ja Heinijärven vedenlaatuselvitys v. 2017 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 11.12.2017 Johdanto Lammin biologinen asema selvitti Tammelan Jäni- ja Heinijärven sekä
Lahnajärven, Suomusjärven ja Myllylammen vedenlaatututkimus 2016
 8.9.2016 Lahna- ja Suomusjärven hoitoyhdistys Mauri Mäntylä Lahnajärven, Suomusjärven ja Myllylammen vedenlaatututkimus 2016 Vesinäytteet otettiin Lahna- ja Suomusjärven suojeluyhdistyksen toimesta 28.8.2016
8.9.2016 Lahna- ja Suomusjärven hoitoyhdistys Mauri Mäntylä Lahnajärven, Suomusjärven ja Myllylammen vedenlaatututkimus 2016 Vesinäytteet otettiin Lahna- ja Suomusjärven suojeluyhdistyksen toimesta 28.8.2016
Humuksen vaikutukset järvien hiilenkiertoon ja ravintoverkostoihin. Paula Kankaala FT, dos. Itä Suomen yliopisto Biologian laitos
 Humuksen vaikutukset järvien hiilenkiertoon ja ravintoverkostoihin Paula Kankaala FT, dos. Itä Suomen yliopisto Biologian laitos Hiilenkierto järvessä Valuma alueelta peräisin oleva orgaaninen aine (humus)
Humuksen vaikutukset järvien hiilenkiertoon ja ravintoverkostoihin Paula Kankaala FT, dos. Itä Suomen yliopisto Biologian laitos Hiilenkierto järvessä Valuma alueelta peräisin oleva orgaaninen aine (humus)
Limsan sokeripitoisuus
 KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
KOHDERYHMÄ: Työn kohderyhmänä ovat lukiolaiset ja työ sopii tehtäväksi esimerkiksi työkurssilla tai kurssilla KE1. KESTO: N. 45 60 min. Työn kesto riippuu ryhmän koosta. MOTIVAATIO: Sinun tehtäväsi on
VALKJÄRVEN VEDEN LAATU Kesän 2015 tutkimus ja vertailu kesiin 2010-2014
 LUVY/121 6.7.215 Anne Linnonmaa Valkjärven suojeluyhdistys ry anne.linnonmaa@anne.fi VALKJÄRVEN VEDEN LAATU Kesän 215 tutkimus ja vertailu kesiin 21-214 Sammatin Valkjärvestä otettiin vesinäytteet 25.6.215
LUVY/121 6.7.215 Anne Linnonmaa Valkjärven suojeluyhdistys ry anne.linnonmaa@anne.fi VALKJÄRVEN VEDEN LAATU Kesän 215 tutkimus ja vertailu kesiin 21-214 Sammatin Valkjärvestä otettiin vesinäytteet 25.6.215
Heinijärven vedenlaatuselvitys 2014
 Heinijärven vedenlaatuselvitys 2014 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 3.12.2014 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin vuonna 2014 Helsingin yliopiston
Heinijärven vedenlaatuselvitys 2014 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 3.12.2014 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin vuonna 2014 Helsingin yliopiston
Bioenergia ry TURVETUOTANTOALUEIDEN YLIVIRTAAMASELVITYS
 Bioenergia ry TURVETUOTANTOALUEIDEN YLIVIRTAAMASELVITYS 2014-2015 15.2.2017 ESITYKSEN SISÄLTÖ 1. Selvityksen tausta ja lähtöainesto 2. Ylivirtaamatilanteet ja niiden määritys 3. Virtaaman vaikutus vedenlaatuun
Bioenergia ry TURVETUOTANTOALUEIDEN YLIVIRTAAMASELVITYS 2014-2015 15.2.2017 ESITYKSEN SISÄLTÖ 1. Selvityksen tausta ja lähtöainesto 2. Ylivirtaamatilanteet ja niiden määritys 3. Virtaaman vaikutus vedenlaatuun
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
α-amylaasi α-amylaasin eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Tärkkelys Oligosakkaridit Maltoosi + glukoosi
 n eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Työssä eristetään ja puhdistetaan merkittävä ja laajalti käytetty teollisuusentsyymi syljestä. pilkkoo tärkkelystä ensin oligosakkarideiksi
n eristäminen syljestä ja spesifisen aktiivisuuden määritys. Johdanto Työssä eristetään ja puhdistetaan merkittävä ja laajalti käytetty teollisuusentsyymi syljestä. pilkkoo tärkkelystä ensin oligosakkarideiksi
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1)
 MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
MAIDON PROTEIININ MÄÄRÄN SELVITTÄMINEN (OSA 1) Johdanto Maito on tärkeä eläinproteiinin lähde monille ihmisille. Maidon laatu ja sen sisältämät proteiinit riippuvat useista tekijöistä ja esimerkiksi meijereiden
FOSFORINPOISTON KEHITTYMINEN
 FOSFORINPOISTON KEHITTYMINEN 1980 2020 Risto Saarinen Toimitusjohtaja Porvoon vesi Yhteenveto Fosforinpoisto osataan Suomessa Osaaminen ja tekniset ratkaisut ovat parantuneet On aika arvioida, tarvitaanko
FOSFORINPOISTON KEHITTYMINEN 1980 2020 Risto Saarinen Toimitusjohtaja Porvoon vesi Yhteenveto Fosforinpoisto osataan Suomessa Osaaminen ja tekniset ratkaisut ovat parantuneet On aika arvioida, tarvitaanko
Kemialliset vesiensuojelumenetelmät
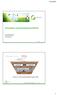 Kemialliset vesiensuojelumenetelmät Aaro Närvänen 07.03.2013 12.3.2013 1 Vesistöjen anemia PO 4 -P, P Lääkkeeksi + Fe 3+ tai Al 3+ Liuennut P Kiintoaine P Leville käyttökelpoinen P x Sedimentti P Fosforin
Kemialliset vesiensuojelumenetelmät Aaro Närvänen 07.03.2013 12.3.2013 1 Vesistöjen anemia PO 4 -P, P Lääkkeeksi + Fe 3+ tai Al 3+ Liuennut P Kiintoaine P Leville käyttökelpoinen P x Sedimentti P Fosforin
VANJOEN JA SEN SIVU-UOMIEN MAIJANOJAN JA ORHINOJAN VEDEN LAATU
 19.7.216 Ympäristönsuojelu, Vihti VANJOEN JA SEN SIVU-UOMIEN MAIJANOJAN JA ORHINOJAN VEDEN LAATU 7.7.216 Vihdin puolelta Vanjokeen laskevasta kahdesta sivu-uomasta Maijanojasta ja Orhinojasta otettiin
19.7.216 Ympäristönsuojelu, Vihti VANJOEN JA SEN SIVU-UOMIEN MAIJANOJAN JA ORHINOJAN VEDEN LAATU 7.7.216 Vihdin puolelta Vanjokeen laskevasta kahdesta sivu-uomasta Maijanojasta ja Orhinojasta otettiin
Rasvattoman maidon laktoosipitoisuuden määritys entsymaattisesti
 Rasvattoman maidon laktoosipitoisuuden määritys entsymaattisesti 1. Työn periaate Esikäsitellyn näyteliuoksen sisältämä laktoosi hajotetaan (hydrolysoidaan) entsymaattisesti D-glukoosiksi ja D-galaktoosiksi
Rasvattoman maidon laktoosipitoisuuden määritys entsymaattisesti 1. Työn periaate Esikäsitellyn näyteliuoksen sisältämä laktoosi hajotetaan (hydrolysoidaan) entsymaattisesti D-glukoosiksi ja D-galaktoosiksi
Nummelan hulevesikosteikon puhdistusteho
 Nummelan hulevesikosteikon puhdistusteho Pasi ivlk Valkama, Emmi imäkinen, Anne Ojala, Ojl Heli HliVht Vahtera, Kirsti tilhti Lahti, Kari irantakokko, tkkk Harri Vasander, Eero Nikinmaa & Outi Wahlroos
Nummelan hulevesikosteikon puhdistusteho Pasi ivlk Valkama, Emmi imäkinen, Anne Ojala, Ojl Heli HliVht Vahtera, Kirsti tilhti Lahti, Kari irantakokko, tkkk Harri Vasander, Eero Nikinmaa & Outi Wahlroos
Eksimeerin muodostuminen
 Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Fysikaalisen kemian Syventävät-laboratoriotyöt Eksimeerin muodostuminen 02-2010 Työn suoritus Valmista pyreenistä C 16 H 10 (molekyylimassa M = 202,25 g/mol) 1*10-2 M liuos metyylisykloheksaaniin.
Jaksollinen järjestelmä
 Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille
 Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille 25.1.2018 Kemian tehtävät Kirjoita nimesi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin
Fysiikan, kemian, matematiikan ja tietotekniikan kilpailu lukiolaisille 25.1.2018 Kemian tehtävät Kirjoita nimesi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin
Vihdin Tuohilammen vedenlaatututkimus, heinäkuu 2016
 26.8.2016 Vihdin kunta, ympäristönsuojelu Vihdin Tuohilammen vedenlaatututkimus, heinäkuu 2016 Vesinäytteet Vihdin Otalammella sijaitsevasta Tuohilammesta otettiin 20.7.2016 Vihdin kunnan ympäristönsuojeluosaston
26.8.2016 Vihdin kunta, ympäristönsuojelu Vihdin Tuohilammen vedenlaatututkimus, heinäkuu 2016 Vesinäytteet Vihdin Otalammella sijaitsevasta Tuohilammesta otettiin 20.7.2016 Vihdin kunnan ympäristönsuojeluosaston
Varsinais-Suomen suurten jokien nykyinen tila ja siihen vaikuttavat tekijät
 Varsinais-Suomen suurten jokien nykyinen tila ja siihen vaikuttavat tekijät Veera-hankkeen loppuseminaari 2.11.216 Janne Suomela Varsinais-Suomen ELY-keskus 1 Esityksen sisältö Yleistä alueen joista Jokien
Varsinais-Suomen suurten jokien nykyinen tila ja siihen vaikuttavat tekijät Veera-hankkeen loppuseminaari 2.11.216 Janne Suomela Varsinais-Suomen ELY-keskus 1 Esityksen sisältö Yleistä alueen joista Jokien
Sekoitushapetus Vesijärven Enonselällä - Kolmen vuoden kokemuksia
 Sekoitushapetus Vesijärven Enonselällä - Kolmen vuoden kokemuksia Limnologipäivät 1.-11..13, Helsinki Pauliina Salmi Lammin biologinen asema Ismo Malin Lahden seudun ympäristöpalvelut Kalevi Salonen Jyväskylän
Sekoitushapetus Vesijärven Enonselällä - Kolmen vuoden kokemuksia Limnologipäivät 1.-11..13, Helsinki Pauliina Salmi Lammin biologinen asema Ismo Malin Lahden seudun ympäristöpalvelut Kalevi Salonen Jyväskylän
Tulosten analysointi. Liite 1. Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma
 Liite 1 Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma Tulosten analysointi Liite loppuraporttiin Jani Isokääntä 9.4.2015 Sisällys 1.Tutkimustulosten
Liite 1 Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma Tulosten analysointi Liite loppuraporttiin Jani Isokääntä 9.4.2015 Sisällys 1.Tutkimustulosten
Miten maatalouden vesiensuojelutoimien tehoa voidaan mitata? Pasi Valkama Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry
 Miten maatalouden vesiensuojelutoimien tehoa voidaan mitata? Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry Esityksen sisältö Kuormituksen muodostuminen Automaattinen veden laadun seuranta ja
Miten maatalouden vesiensuojelutoimien tehoa voidaan mitata? Vantaanjoen ja Helsingin seudun vesiensuojeluyhdistys ry Esityksen sisältö Kuormituksen muodostuminen Automaattinen veden laadun seuranta ja
KERTARAPORTTI Oravin vesiosuuskunta C 4484 Tapio Rautiainen Tappuvirrantie Oravi
 ORAVIN JÄTEVEDENPUHDISTAMO Tutkimus: 2.7.2017 (4484). Oravin vesiosuuskunta C 4484 Tapio Rautiainen Tappuvirrantie 776 58130 Oravi ORAVIN VESIOSUUSKUNNAN PANOSPUHDISTAMON KUORMITUSTARKKAILU 2.7.2017 OLOSUHTEET
ORAVIN JÄTEVEDENPUHDISTAMO Tutkimus: 2.7.2017 (4484). Oravin vesiosuuskunta C 4484 Tapio Rautiainen Tappuvirrantie 776 58130 Oravi ORAVIN VESIOSUUSKUNNAN PANOSPUHDISTAMON KUORMITUSTARKKAILU 2.7.2017 OLOSUHTEET
Vihdin Lapoon vedenlaatututkimus, elokuu 2016
 26.8.2016 Vihdin kunta, ympäristönsuojelu Vihdin Lapoon vedenlaatututkimus, elokuu 2016 Vesinäytteet Vihdin Lapoosta otettiin 16.8.2016 Vihdin kunnan ympäristönsuojeluosaston toimeksiannosta. Työ perustuu
26.8.2016 Vihdin kunta, ympäristönsuojelu Vihdin Lapoon vedenlaatututkimus, elokuu 2016 Vesinäytteet Vihdin Lapoosta otettiin 16.8.2016 Vihdin kunnan ympäristönsuojeluosaston toimeksiannosta. Työ perustuu
Ruokjärven veden laatu Maalis- ja elokuu 2017
 30.8.2017 Karkkilan kaupunki, ympäristönsuojelu Ruokjärven veden laatu Maalis- ja elokuu 2017 Karkkilan Vuotnaisissa sijaitsevan Ruokjärven vesinäytteet otettiin 1.3.2017 ja 2.8.2017 Karkkilan kaupungin
30.8.2017 Karkkilan kaupunki, ympäristönsuojelu Ruokjärven veden laatu Maalis- ja elokuu 2017 Karkkilan Vuotnaisissa sijaitsevan Ruokjärven vesinäytteet otettiin 1.3.2017 ja 2.8.2017 Karkkilan kaupungin
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Elintarviketeollisuuden hapan vaahtopesuneste
 P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Näytteenotto ja tulosten analysointi
 Haja-asutuksen jätevedet Näytteenotto ja tulosten analysointi Mirva Levomäki Lounais-Suomen vesi- ja ympäristötutkimus Oy Näytteenoton tärkeys VN asetus 542/2003, hajajätevesiasetus kuormitusta vähennettävä
Haja-asutuksen jätevedet Näytteenotto ja tulosten analysointi Mirva Levomäki Lounais-Suomen vesi- ja ympäristötutkimus Oy Näytteenoton tärkeys VN asetus 542/2003, hajajätevesiasetus kuormitusta vähennettävä
