Lähialueen suolaisen. referenssiveden kehitys
|
|
|
- Jarno Ahola
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Työraportti Lähialueen suolaisen. referenssiveden kehitys Arto Muurinen Ulla Vuorinen.Jarmo Lehikoinen Hannu Aalto VTT Kemiantekniikka Tammikuu 1998 POSJVA OY Mikonkatu 15 A, FIN HELSINKI Puhelin (09) Fax (09)
2 Työ raportti Lähialueen suolaisen referenssiveden kehitys Arto Muurinen Ulla Vuorinen ~armo Lehikoinen Hannu Aalto VTT Kemiantekniikka Tammikuu 1998
3 ~,,..,. KEMIANTEKNIIKKA V 1 1 Teollisuusfysiikka 1 (1) TUTKIMUSSELOSTUS NRO KET2090/97 Tilaaja Tilaus Käsittelijä Tehtävä Tulokset Posiva Oy Mikonkatu 15 A HELSINKI 9757/97/MVS Erikoistutkija Arto Muurinen, (09) Käytetyn polttoaineen loppusijoitustilan lähialueen referenssiveden arviointi ja reseptin kehittäminen Raportissa "Lähialueen suolaisen referenssiveden kehitys" Espoo Tutkimuspäällikön sijainen Erikoistutkija n-~~~ Antero Tiitta #h A~ L Arto Muurinen JAKELU Posiva Oy VTT Kemiantekniikka 1 arkisto VIT KEMIANTEKNIIKKA Teollisuusfysiikka Otakaari 3 A, Espoo PL VIT Puh. vaihde (09) 4561 Faksi (09) vtt.fi/
4 Pasivan työraporteissa käsitellään käynnissä olevaa tai keskeneräistä työtä. Esitetyt tulokset ovat alustavia. Raportissa esitetyt johtopäätökset ja näkökannat ovat kirjoittajien omia, eivätkä välttämättä vastaa Posiva Oy:n kantaa
5 LÄHIALUEEN SUOLAISEN REFERENSSIVEDEN KEHITYS TllVISTELMÄ Tässä tutkimuksessa kehitettiin kaksi referenssivettä käytetyn polttoaineen loppusijoitustilan lähialueelle suolaisessa (67 g/l) pohjavesiympäristössä ja testattiin niiden pysyvyyttä erilaisissa koeolosuhteissa. Toinen referenssivesistä, joka oli kalsiitin suhteen selvästi ylikylläinen, oli verraten stabiili suljetun systeemin kuukauden testissä, mutta epästabiili avoimessa systeemissä typpikaapissa. Toinen, ilman hiilidioksidin ja kalsiitin kanssa tasapainossa oleva referenssivesi oli stabiili suljetussa systeemissä ja ilman kanssa tasapainossa olevassa avoimessa systeemissä, mutta epästabiili avoimessa systeemissä typpikaapissa. Tutkimuksessa on esitetty valmistusohjeet referenssivesille ja niiden käyttöön liittyviä rajoituksia. Avainsanat: Referenssivesi, loppusijoitus, lähialue, stabiilisuus, liukoisuus, kalsiitti, karbonaatti
6 DEVELOPMENT OF SALINE NEAR-FIELD REFERENCE WATER ABSTRACT In this study two reference waters for the near-field of a repository in saline (67 g/l) groundwater conditions were developed and tested for a month in various experimental conditions. One ofthe reference waters, which was clearly over-saturated in respect of calcite, was rather stabile in a closed system but unstable in an open system in a nitrogen glove-box. The other reference water, which was in equilibrium with calcite and pc02 of air, was stabile in a closed system and in a system open to the air, but unstable in an open system in a nitrogen glove-box. The study gives recipes for the reference waters and discusses the limitations of their use. Keywords: Reference water, disposal, near-field, stability, solubility, calcite, carbonate,
7 SISÄLLYSLUETTELO Tiivistelmä 3 Abstract 4 1 JOHDANTO 7 2 TUTKIMUKSEN TOTEUTUS Pohjavesisimulantin koostumuksen määrittely ja valmistus Lähialueen referenssiveden koostumuksen määrittely ja valmistus Lähialueen referenssiveden Stabiilisuuden tutkiminen Kalsiitin suhteen ylikylläisen veden stabiilisuustarkastelu Ilman ja kalsiitin suhteen tasapainotetun veden stabiilisuustarkastelu 13 3 YHTEENVETO Sivu KIRJALLISUUSVIITTEET LIITE I: Mallinnuksessa käytetty tietokanta LIITE II: Lähialueen suolaisen referenssiveden valmistusohje (A-vesi) LIITE UI: Lähialueen suolaisen referenssiveden valmistusohje (B-vesi)
8 7 1. JOHDANTO Synteettisiä referenssivesiä tarvitaan laboratoriokokeissa takaamaan veden muuttumaton koostumus eri koekerroilla. Tunnettu tarkka koostumus helpottaa mallinnusta, kokeiden tulkintaa ja eri kokeiden välistä vertailua. Käytetyn polttoaineen loppusijoitustilan lähialueen veden koostumusta arvioitaessa on lähtökohtana ympäröivä pohjavesi, johon vuorovaikutukset lähialueen materiaalien kanssa aiheuttavat muutoksia. Näillä vaikutuksilla on myös aikariippuvuus mm. sen mukaan milloin eri vapautumisesteet osallistuvat vuorovaikutusprosessiin. Alkuvaiheessa merkittävin pohjaveteen vaikuttava tekijä on bentoniitti. Kemiallisten muutosten syynä ovat bentoniitin liukenevat komponentit ja sen pääkomponentin, montmorilloniitin, aiheuttamat ioninvaihtoprosessit. Vaikutukset ovat suurimmillaan loppusijoituksen alkuvaiheessa ja laimenevat ajan myötä niin, että ennen pitkää lähestytään pohjaveden olosuhteita. Pohjaveden ja bentoniitin välisiä kemiallisia vuorovaikutuksia on aiemmin tutkittu kokeellisesti esimerkiksi makealla referenssipohjavedellä (Allard vesi), jonka liuenneen kiintoaineen pitoisuus (TDS) on noin 0, 14 g/l, ja Olkiluodon suolaisella referenssivedellä, jonka TDS on noin 24 g/l (Muurinen & Lehikoinen 1997, Muurinen 1997). Näiden tutkimusten pohjalta on olemassa alustava käsitys veden ja bentoniitin välisistä vuorovaikutusprosesseista. Olkiluodon syvän pohjaveden analyysien perusteella näyttäisi TDS kuitenkin nousevan jopa 67 g/l tasolle. Näin väkevillä liuoksilla ei vuorovaikutuskokeita Suomessa ole tähän mennessä tehty. Tämän tutkimuksen tarkoituksena oli arvioida käytetyn polttoaineen loppusijoitustilan lähialueelle muodostuvan veden koostumusta pääkomponenttien osalta suolaisessa pohjavesiympäristössä, laatia ohje referenssiveden valmistusta varten ja tutkia referenssiveden pysyvyyttä koeolosuhteissa. 2. TUTKIMUKSEN TOTEUTUS 2.1 Pohjavesisimolantio koostumuksen määrittely ja valmistus Lähialueen veden perustana olevan suolaisen pohjaveden koostumus määritteltiin Olkiluodosta otetun näyteen (OL-KR4, , syvyys m) pohjalta. Näytteelle tehdyn analyysin perusteella laskettiin EQ3/6-mallilla suolaisen pohjavesisimulantin koostumus ilmakehän hiilidioksidipitoisuutta ja typpikaapin hiilidioksidipitoisuutta vastaavissa olosuhteissa. Taulukossa 1 on esitetty IVO:lta saadut veden alustavat analyysitulokset sekä mallinnustulokset. Mallilaskennassa käytettiin EQ3/6-mallin versiota 7.2b ja sen termodynaamista tietokantaa V8-EQ8-DATAO.HMW.R2 ja Pitzer-mallia aktiivisuuskertaimien laskentaan. Lämpötilana laskennassa oli 25 C koska kyseinen tietokanta on määritelty vain tälle lämpötilalle. Käytetty tietokanta on varsin suppea (Liite 1) sisältäen kuitenkin hiilidioksidin, joten karbonaattitasapainon määrittäminen on mahdollista. Mallilaskennan
9 8 tavoitteena oli saada sellainen vest, JOSsa et tapahtuisi ylikylläisyyden seurauksena saostumisia. Analyysin tuloksena saatu pohjaveden koostumus ei ollut varaustasapainossa, koska koostumukseen otettiin mukaan vain pääkomponentit ja niistäkin oli vasta alustavat tulokset olemassa. Lisäksi sulfaatti jätettiin mallinnuksessa pois varsin epävarmana pidetyn tuloksen johdosta. Varaustasapainotus vedessä tehtiin lisäämällä natriumin määrää noin 52 mmol/l (1 200 mg/l). Riippumatta käytetystä ph:sta aragoniitti, kaisiitti ja dolomiitti ovat ylikylläisiä analyysiin perustuvassa vedessä. Hiilidioksidin fugasiteetin logaritmi kenttä-ph:n arvolla on -3,6 ja kennostossa mitatulla ph:n arvolla - 4,5. Hapellinen suolainen simulantti mallinnettiin lisäämällä ilman hiilidioksidin kanssa tasapainossa olevaan veteen (log Pco2= -3,5) pohjavettä vastaavat määrät kemikaaleja ja tasapainottamalla liuos kalsiitin suhteen, jolloin 5,1 mg kalsiittia saostui. Tällaisen veden ph:ksi saatiin 7, 1. Hapeton suolainen vesisimulantti mallinnettiin vastaavasti lisäämällä tarvittavat määrät kemikaaleja veteen, joka oli tasapainossa atmosfåärin kanssa, jonka log Pc 02 = -6,5 ( typpikaapin atmosfåäri). Vesi tasapainotettiin kalsiitin suhteen, jolloin 8,2 mg kalsiittia saostui. Tällaisen veden ph:ksi saatiin 8,6. Hiilen määrää ja ph:ta lukuunottamatta ovat vesien koostumukset käytännöllisesti katsoen samat. Näistä vesistä valmistettiin vuorovaikutuskokeita varten vain ilmatasapainoa vastaava versio (OL-BRINE), jonka valmistuksessa tarvittavat kemikaalimäärät on esitetty Taulukossa 2. Taulukko 1. Olkiluodon suolaisen pohjavesinäytteen OL-KR4 ( ) koostumus ja sen pohjalta EQ3/6 mallinnuksen tuloksena saatu, ilman kanssa tasapainossa olevan (log Pc 02 = -3,5) ja typpikaapin atmosfäärin kanssa tasapainossa olevan ( log P co 2 = -6, 0) veden koostumus. ph 7,5 (kenttä) 7,1 8,6 7,8 (kenno) 8,2 (laboratorio) Na mmol/l Ca mmol/l Mg mmol/l 4,52 4,52 4,52 Cl mmol/l so4 mmol/l 0,81 (?) Alkaliteetti mekv/l 0,20 Crot mmol/l 1,2 0,1 logpco2-3,6 (kenttä) -3,5-6,0-4,5 (kenno)
10 9 Taulukko 2. Hapellisen suolaisen pohjaveden simulantin (OL-BRINE) valmistuksessa tarvittavat kemikaalimäärät. NaCl ,2 Kuten muidenkin simulanttivesien valmistuksessa liuotetaan kemikaalit erikseen ensin tarvittavaan määrään vettä, jotka sitten yhdistetään yhdeksi liuokseksi. Valmistetun suolaisen pohjavesisimulantin ph:ksi muodostui 6,6. Se säädettiin 0,1 M NaOHliuoksella arvoon 7, Lähialueen referenssiveden koostumuksen määrittely ja valmistus Lähialueen veden koostumuksen määrittelyssä lähdettiin tilanteesta, joka vallitsee loppusijoitustilassa pian sen jälkeen, kun hentoniitti on kyllästynyt pohjavedellä, mutta liuenneet komponentit eivät ole merkittävästi kulkeutuneet po1s. Tätä kuvattiin hentoniitti/vesi-suhteella 1,5 g/ml, mikä vastaa tilannetta, JOSsa hentoniitti on tasapainossa 2,25 kertaa huokosvetensä suuruisen liuostilavuuden kanssa. Lähialueelle muodostuvan veden koostumus arvioitiin pohjaveden koostumuksen, lyhyen hentoniittivesi-vuorovaikutuskokeen Ja liuokselle tehdyn EQ3/6-mallinnustarkastelun sekä aikaisemmista vesi-bentoniittivuorovaikutuskokeista kertyneen tiedon pohjalta. Lyhytaikaisella vesibentoniittivuorovaikutuskokeella selvitettiin suolaisen pohjaveden (OL-BRINE) ja bentoniitin välisiä nopeita vuorovaikutusprosesseja ja sen tuloksena muodostuvan liuoksen koostumusta. Koe tehtiin suljetussa systeemissä batch-kokeena sekoittamalla MX-80 bentoniiti taulukon 2 mukaan valmistettuun suolaiseen simulanttiveteen. Koe tehtiin 50 ml:n sentrifugiputkissa (16 kpl), joihin punnittiin kuhunkin 32,6 g huonekuivaa MX-80 bentoniittia (kuivapaino = 30 g). Bentoniitin päälle lisättiin 20 ml pohjavesisimulanttia ja vesi ja hentoniitti sekoitettiin. Systeemin annetiin tasapainottua kaksi viikkoa laboratorio-olosuhteissa, jonka jälkeen liuos erotettiin sentrifugoimalla. Erottuneet liuokset yhdistettiin yhdeksi näytteeksi, joka suodatettiin 0,45 IJ.m suodattimella. Liuoksesta mitattiin ph sekä analysoitiin Na+, Ca 2 +, Mg 2 +, cr ja SO/- ionikromatografisesti ja HC0 3 - titraamalla. Taulukossa 3 on esitetty veden muuttuminen kahden viikon vuorovaikutuskokeen aikana ja vertailun vuoksi aikaisemmin, vähemmän suolaisen Olkiluodon pohjavesisimulantin OL-SR Ja kompaktoidun bentoniitin vuorovaikutuskokeesta saadut tulokset. Muutokset veden kemiassa ovat verraten yhdenmukaisia. Kationien osalta muutosta hallitsee ioninvaihto, jolloin natriumin, magnesiumin ja kaliumin pitoisuus liuoksessa kasvaa ja kalsiumin pitoisuus vastaavasti pienenee. Pieniä määriä sulfaatti- ja karbonaattimineraaleja myös liukenee. Sekä kationien että anionien pitoisuutta kasvattaa myös ekskluusio, jonka vaikutus kloridin pitoisuuden perusteella arvioituna on % lähtötasosta. Muutokset ph: ssa ovat pieniä.
11 10 Taulukko 3. Liuoksen koostumuksen muuttuminen kompaktoimattomalla bentoniitilla ja OL-BRINE-vedellä tehdyssä kahden viikon vuorovaikutuskokeessa (hapellinen, suljettu) ja kompaktoidulla bentoniitilla ja OL-SR-vedellä tehdyssä 324 päivän vuorovaikutuskokeessa (typpikaappi, suljettu, Muurinen 1997). ph 7,1 7,4 8,2 8,1 Na mmol!l Ca - II Mg - II - 4, ,3 13 K - II - 0 4,8 0,51 2,4 Cl - II HC03 - II - 0,097 1,3 0 2,7 so4 - II Br - II ,30 1,6 Tarkistetut analyysitulokset Kahden viikon vuorovaikutuskokeesta saadun suolaisen hentoniittiveden analyysituloksen (Taulukko 3) perusteella tehtiin mallitarkastelut lähialueen suolaisen referenssiveden määrittämiseksi. Koska veden analyysi ei ollut sähköisesti tasapainossa, se tasapainotettiin lisäämällä natriumia noin 148 mmol/l. (Myöhempi tarkistus osoitti, että sekä natrium- että kalsiumpitoisuudet olivat liian pieniä. Oikeat pitoisuudet ovat [Na] = 940 mmol/l ja [Ca] = 270 mmol/l) Mallitarkastelussa suljetun systeemin hentoniittivedessä kalsiumkarhonaattifaasit aragoniitti ja kaisiitti ovat ylikylläisiä sekä kalsiumsulfaattifaasit anhydriitti ja kipsi sekä magnesiitti (MgC0 3 ) kylläisiä. Suljetun systeemin log Pco2:n arvoksi saadaan -2, 7. Kun hapellisen suljetun systeemin vesi (Taulukko 3) tasapainotetaan ilman hiilidioksin, kalsiitin ja kipsin kanssa saadaan ph:ksi 7,2. Tällöin vedestä on saastunut 0,63 mmol kalsiittia ja 0,60 mmol kipsiä. Kun tasapainotus tehdään vastaamaan typpikaapin atmosfåäriä (logpc02 = -6,0), saastuneet määrät ovat hieman suuremmat ja ph:ksi saadaan 8,5. Merkittävimmät erot näiden vesien kemiallisessa koostumuksessa ovat ph: ssa ja hiilen määrässä. Koostumukset on esitetty taulukossa 4. Erilaisten hiilidioksidipitoisuuksien kanssa tasapainossa olevien lähialueen simulanttivesien valmistuksessa tarvittavat kemikaalimäärät on esitetty taulukossa 5. Valmistettaessa liuoksia muut kemikaalit, paitsi NaHC0 3, liuotetaan erikseen tarpeelliseen määrään vettä ja yhdistetään yhdeksi liuokseksi. Lopuksi lisätään natriumhikarhonaatti.
12 11 Taulukko 4. Bentoniitin ja suolaisen veden (OL-BRINE) vuorovaikutuksessa muodostuneen veden mal/innustulokset. A: suljetu, ylikylläinen systeemi. B: ilman ja kalsiitin kanssa tasapainotettu systeemi. C: typpikaapin atmosfäärin ja kalsiitin kanssa tasapainotettu systeemi.... : j ~pg j ~iliöj : Taulukko 5. Suljetun ylikylläisen systeemin sekä ilman ja typpikaapin atmosfäärin ja kalsiitin kanssa tasapainossa olevan lähialueen suolaisen simulanttiveden valmistuksessa tarvittavat kemikaalimäärät. 2.3 Lähialueen referenssiveden Stabiilisuuden tutkiminen Stabiilisuuden seurantaa varten valmistettiin kaksi taulukon 5 mukaista bentoniittivesisimulanttia, joista toinen (A) edustaa kalsiitin suhteen selvästi ylikylläistä suljetun systeemin vettä ja toinen (B) ilman hiilidioksidin ja kalsiitin kanssa tasapainossa olevaa vettä. Mallinnuksen mukaan ylikylläinen vesi (vesi A) otettiin stabiilisuustestiin mukaan siksi, että sellaisen muodostumisesta oli selvää kokeellista havaintoa olemassa. Toisaalta typpikaappia vastaavan veden (vesi C) jättäminen pois testattavien joukosta perustui sen erittäin alhaiseen karbonaattipitoisuuteen, jonka merkitys loppusijoituksen kannalta oletettiin vähäiseksi. Kemikaalit (paitsi NaHC03) liuotettiin deionisoituun veteen laboratoriossa, jonka jälkeen liuoksia typetettiin neljä tuntia hapen ja hiilidioksidin poistamiseksi. Typetyksen jälkeen liuokset siirrettiin typpikaappiin, jossa liuoksiin lisättiin NaHC03. Liuosten
13 12 annettiin seisoa yli yön, jolloin kummankin liuoksen ph oli 7,1. Vaikka ph:n arvot poikkesivat mallin antamista (Taulukko 4) ei ph:ta kuitenkaan säädetty. Liuokset suodatettiin 0,45 J.tm:n suodattimella ja jaettiin 100 gramman erissä 125 ml:n Nalgene polypropyleeni pulloihin eri olosuhteissa suoritettavia stabiilisuustestejä varten. Stabiilisuustestissä näytepullot varastoitiin ilmassa tai typpikaapissa tiiviisti suljetussa (sulj.) tai löyhästi suljetussa (av.) pullossa. Säilytysajat olivat 2 viikkoa ja 4 viikkoa. Pullojen painoja seurattiin ja avoimista pulloista haihtunut vesi korvattiin viikottain deionisoidulla vedellä. Koejakson lopussa kustakin liuoksesta otettiin 30 ml:n erä, joka suodatettiin 0,45 1Jm:n suodattimella. Liuoksesta analysoitiin Na+, Ca 2 +, cr, solionikromatografisesti, Mg 2 + ja K+ atomiabsorptiospektrofotometrisesti liekkitekniikalla ja karbonaattihiili alkaliteettititrauksella. Taulukossa 6 on esitetty A-veden pitoisuudet eri koeolosuhteille ja koeajoille. Vastaavat tiedot B-vedelle ovat Taulukossa 7. Merkittäviä muutoksia tapahtuu vain ph:ssa, karbonaattihiilen pitoisuuksissa ja alkaliteetissa. Muut komponentit säilyvät analyysitarkkuuden puitteissa muuttumattomina. Karbonaattikemian havainnollistamiseksi on kuvissa 1 ja 2 esitetty A- ja B-vedelle mallilla laskettu ph:n, alkaliteetin ja karbonaattihiilen (HC03- + CO/) pitoisuuden riippuvuus hiilidioksidin fugasiteetista. Laskelma on tehty kahdella olettamuksella, joista ensimmäisessä (1) oletetaan systeemin säilyvän ylikylläisenä ja toisessa (2) systeemin oletetaan olevan tasapainossa kalsiitin kanssa, jolloin liukoisuusrajan ylittyessä kaisiitti saostuu. 2.4 Kalsiitin suhteen ylikylläisen veden stabiilisuustarkastelu (A-vesi) A-vesi on alunperin tehty ylikylläiseksi kalsiitin suhteen. Mallilla laskettuna sen karbonaattikemiaan liittyvät pitoisuudet suljetussa systeemissä ovat alkutilanteessa Ctot = 1,3 mmol!l, log pc02 = -2,7 ja ph = 7,4 (Taulukko 4). Systeemissä tapahtuvia muutoksia voidaan tarkastella vertaamalla mallinnuksen ennustuksia (Kuva 1) kokeissa havaittuihin muutoksiin (Taulukko 6). Seuraavassa on tarkasteltu erilaisia tilanteita A vedellä. a) Systeemi on suliettu ia kalsiitin annetaan saostua niin. että ylikylläisyys poistuu. Mallinnustulosten mukaan tällaisessa tilanteessa karbonaattihiilen p1to1suus, kokonaisalkaliteetti ja ph pienenevät selvästi. Kuvassa 1 se vastaa tilannetta, jossa siirrytään käyriitä (1) käyrille (2), log pc02:n pysyessä vakiona. Koejärjestelyssä tämä vastaisi ilma/suljettu ja typpi/suljettu tilanteita, joissa ylikylläinen kaisiitti alkaisi saostua. Taulukosta 6 havaitaan kuitenkin, että näillä näytteillä ei kokonaisalkaliteetissa tapahdu muutosta neljän viikon koejakson aikana. Karbonaattihiilen osalta muutos ilmaolosuhteissa on vähäinen, typpikaapissa vähän selvempi, mutta pieni. Samoin ph:n arvot asettuvat tasolle 7,3-7,4 vastaten kohtuullisen hyvin suljetun ylikylläisen systeemin mallinnustulosta. Suljetussa systeemissä A-vesi näyttäisi siten pysyvän verraten stabiilina, vaikka se on selvästi ylikylläinen.
14 13 b) Systeemi on avoin niin, että pc02 pienenee. mutta ylikylläisyyden annetaan säilyä. Mallinnustulosten mukaan kokonaisalkaliteetti säilyy lähes muuttumattomana, karbonaattihiilen pitoisuus pienenee ja ph kasvaa. Koejätjestelyssä tämä vastaisi ilma/avoin ja typpi/avoin tilanteita, kun ylikylläisyys säilyy. Taulukosta 6 havaitaan, että näillä näytteillä ei kokonaisalkaliteetissa tapahdu muutosta neljän viikon koejakson aikana muissa kuin typpi/avoin näytteessä. Karbonaattihiilen pitoisuus ilmaolosuhteissa pienenee vähän, typpikaapissa lasku on selvä jo kahden viikon kuluttua ja kasvaa säilytysajan pidetessä. ph:n arvot kasvavat hiukan ilmaolosuhteissa, mutta selvästi typpikaapissa. Avoimista pulloista ilma/avoin/2-4 vko ja typpi/avoin/2 vko vastaavat siten melko hyvin avointa ylikylläistä systeemiä, jossa tasapainottuminen ympäristön alemman hiilidioksidipitoisuuden kanssa on meneillään, mutta saastuminen ei vielä ole alkanut. c) Systeemi on avoin niin. että. pc02 pienenee ja lisäksi karbonaatti saostuu. Mallinnuksen mukaan pienenevät kokonaisalkaliteetti ja karbonaattihiilen pitoisuus selvästi ja ph kasvaa, mutta vähemmän kuin edellisessä ylikylläisessä tapauksessa. Koejärjestelyssä tämä vastaa avoimia pulloja, jossa kaisiitti saostuu. Taulukosta 6 havaitaan, että kokonaisalkaliteetti ja karbonaatti pienenevät ja ph kasvaa selvästi typpi/avoin/4 vko tapauksessa. Nämä pullot vastaavat siten systeemiä, jossa tasapainottuminen ympäristön alemman hiilidioksidipitoisuuden kanssa on meneillään ja samanaikaisesti kaisiitti saostuu. Yhteenvetona voidaan todeta, että lyhyen vesi-hentoniitti-vuorovaikutuskokeen perusteella saatu lähialueen suolainen hentoniittivesi (A-vesi, Taulukko 5) on ylikylläinen kalsiitin ja aragoniitin suhteen ja epätasapainossa myös ilman ja typpikaapin, hiilidioksidiin nähden. Tasapainon saavuttaminen ympäristön hiilidioksidia säätämällä vaatisi pc02:n nostamista tasolle -1, jolloin ph laskisi alle kuuden. Ylikylläinen vesi näyttäisi kuitenkin säilyvän suljetun systeemin lyhytaikaisissa kokeissa verraten muuttumattomana. Kokeet tällaisella vedellä edellyttävät kuitenkin karbonaattikemian huolellista seurantaa. Avoin systeemi, jossa pc02 on pienempi kuin liuoksen vastaava arvo, pyrkii tasapainoon ympäristön hiilidioksidin kanssa ja samalla taipumus ylikylläisen kalsiitin saastumiseen kasvaa. Näissä olosuhteissa A-vettä ei voi pitää stabiilina edes lyhytaikaisessa kokeessa. Liitteessä II on esitetty valmistusohje lähialueen suljetun systeemin ylikylläiselle referenssivedelle. 2.5 Dman ja kalsiitin suhteen tasapainotetun veden stabiilisuustarkastelu (B-vesi) B-vesi valmistettiin niin, että se oli tasapainossa ilman hiilidioksidipitoisuuden ja kalsiitin kanssa. Mallilla laskettuna sen karbonaattikemiaan liittyvät pitoisuudet suljetussa systeemissä ovat alkutilanteessa Ctot = 0,14 mmol/l, log pc02 = -3,5 ja ph = 7,2 (Taulukko 4). Systeemissä tapahtuvia muutoksia voidaan tarkastella vertaamalla mallinnuksen ennustuksia (Kuva 2) kokeissa havaittuihin muutoksiin (Taulukko 7). Seuraavassa kohdissa d), e) ja f) on tarkasteltu B-vedellä samoja kolmea tilannetta kuin A-vedellä edellä.
15 14 d) Systeemi pidetään suljettuna. Koska systeemi on tasapainossa kalsiitin kanssa ei suljetussa systeemissä pitäisi tapahtua muutoksia. Koejärjestelyssä tämä vastaisi ilma/suljettu ja typpi/suljettu tilanteita. Koska vesi on suunniteltu vastaamaan ilman hiilidioksidipitoisuutta, pitäisi sen olla tasapainossa myös ilma/avoin kokeessa. Kuten Taulukosta 7 havaitaan ovat ph:t ilmaolosuhteissa hiukan alempia kuin typpikaapissa. Alkaliteetin arvot ovat verraten vakioita typpi/sulj./4 vko lukuunottamatta, jolloin se lievästi laskee. Kaikissa neljän viikon näytteissä karbonaattipitoisuudet ovat lievästi alentuneet. Erot ilma ja typpikaapin välillä viittaavat siihen, että pullot eivät ole täysin tiiviitä tai näytteen käsittely typpikaapissa, voi vaikuttaa lievästi karbonaattikemiaan. B vesi on kuitenkin verraten stabiili suljetussa systeemissä. e) Systeemi on avoin niin. että pc02 pienenee. mutta ylikylläisyyden annetaan säilyä. Mallinnustulosten mukaan kokonaisalkaliteetti säilyy lähes muuttumattomana, karbonaattihiilen pitoisuus pienenee ja ph kasvaa. Koejärjestelyssä tämä vastaa typpi/avoin tilanteita, kun ylikylläisyys säilyy. Taulukosta 7 havaitaan että typpi/avoin näytteillä alkaliteetti pysyy lähes muuttumattomana, karbonaattihiili laskee ja ph nousee. Koe vastaa siten hyvin avointa systeemiä, joka on tasapainottumassa alhaisen hiilidioksidipitoisuuden kanssa, mutta jossa kalsiitin saastuminen ei ole alkanut. f) Systeemi on avoin niin. että. pc02 pienenee ja lisäksi karbonaatin annetaan saostua. Mallinnuksen mukaan pienenevät kokonaisalkaliteetti ja karbonaattihiilen pitoisuus selvästi ja ph kasvaa, mutta vähemmän kuin edellisessä ylikylläisessä tapauksessa. Koejärjestelyssä tämä vastaa avoimia pulloja, jossa kaisiitti saostuu. B-vedellä ei tätä tapausta havaittu. Yhteenvetona voidaan todeta, että B-vesi (Taulukko 5) valmistettiin siten, että se on tasapainossa kalsiitin ja ilmakehän hiilidioksidin kanssa. Vesi näyttäisi verraten stabiililta suljetussa systeemissä ja ilman kanssa tasapainossa olevassa avoimessa systeemissä. Jos avoin systeemi on tasapainossa alhaisen hiilidioksidipitoisuuden kanssa, pyrkii karbonaattihiili poistumaan ja samalla ph nousee. Yhden kuukauden seurannassa ei kuitenkaan vielä havaittu kalsiitin alkavan saostua. Pitkäaikaiset kokeet tällä vedellä tulisi tehdä suljetussa systeemissä ja mielellään siten, että ympäristön hiilidioksidipitoisuus järjestetään vastaamaan ilman hiilidioksidipitoisuutta. Liitteessä III on esitetty valmistusohje lähialueen referenssivedelle, joka on tasapainossa kalsiitin ja ilman hiilidioksidipitoisuuden kanssa (pc0 2 = -3,5).
16 15 Taulukko 6. Pitoisuudet kalsiitin suhteen ylikylläisen veden (A-vesi) näytteissä eri olosuhteissa ja eripituisten koejaksojen jälkeen ,- 1.0E E (1) ph, kun systeemi on ylikylläinen :a E-04 ei ~ ----l:s (2) ph, kun systeemi tasapainossa kalsiitin kanssa o - (1) C (HC03 + C02).s --D-(2) C (HC03 + C02) ---e-- (1) Alk. tot (ekv/kg) ()-- (2) Alk. tot (ekv/kg) 4.0.,._ ; E log pc02 Kuva 1. EQ3/6 mallilla tarkasteltu ph:n ja karbonaattihii/en pitoisuuden (HC CO/) riippuvuus hiilidioksidinfugasiteetista (pc0 2 ) A-vedellä.
17 16 Taulukko 7. Pitoisuudet kalsiitin ja ilman kanssa tasapainossa olevan veden (B-vesi) näytteissä eri olosuhteissa ja eripituisten koejaksojen jälkeen : ~<oeaika ::::::::::::::..... Na mmoi/l Ca mmoi/l Mg mmoi/l K mmoi/l 4,8 4,6 Cl mmoi/l C tot mmoi/l 0,14 0,14 Alk. tot mekvll 0,14 0,14 S04 mmoi/l 12,7 12 ph ,7 4, ,13 0,14 0,15 0, , ,11 0, ::,:~pg~i~~ ::::::: :: Na mmoi/l Ca mmoi/l Mg mmoi/l K mmoi/l 4,8 4,6 Cl mmoi/l C tot mmoi/l 0,14 0,14 Alk. tot mekvll 0,14 0,15 S04 mmoi/l 12,7 13 ph ,7 4, ,10 0,09 0,14 0, , ,07 0, , ,- 1.0E _ ' ' n.. -_-_-_---.._, 8.0 'å, ---, 1.0E-03 l.-.-,,_ :a 7.0 ' ~ ~ E-04 'tt (1) ph, kun systeemi on ylikyllainen (2) ph, kun systeemi on tasapainossa kalsiitin kanssa - (1) C(HC03+C02) --o-(2) C (HC03 + C02) --e-- (1) Alk. tot (ekv/kg) o-- (2) Alk. tot (ekv/kg) 4.0 ~ E log PC0 2 Kuva 2. EQ3/6 mallilla tarkasteltu ph:n ja karbonaattihiilen pitoisuuden (HC CO/) riippuvuus hiilidioksidin jugasiteetista (pc0 2 ) B-vedellä.
18 17 3. YHTEENVETO Tässä tutkimuksessa arv1o1tnn käytetyn polttoaineen loppusijoitustilan lähialueelle muodostuvan veden koostumusta sen pääkomponenttien osalta suolaisessa ( 67 gil) pohjavesiympäristössä, laadittiin ohje referenssiveden valmistusta varten ja tutkittiin referenssiveden pysyvyyttä erilaisissa koeolosuhteissa. Lähialueen veden koostumusta arvioitaessa oli lähtökohtana Olkiluodosta otetun näytteen (OL-KR4, , syvyys m) vesi. Lyhytaikaisella vesibentoniittivuorovaikutuskokeella selvitettiin suolaisen pohjaveden ja bentoniitin välisiä nopeita vuorovaikutusprosesseja ja sen tuloksena muodostuvan liuoksen koostumusta. Kationien osalta muutosta hallitsee ioninvaihto, jolloin natriumin, magnesiumin ja kaliumin pitoisuus liuoksessa kasvaa ja kalsiumin pitoisuus vastaavasti pienenee. Pieniä määriä sulfaatti- ja karbonaattimineraaleja myös liukenee. Sekä kationien että anionien pitoisuutta kasvattaa myös ekskluusio, jonka vaikutus kloridin pitoisuuden perusteella arvioituna on % lähtötasosta. Muutokset ph: ssa on pieniä. Analyysituloksen perusteella tehtiin mallitarkastelut lähialueen suolaisen referenssiveden määrittämiseksi. Stabiilisuuden seurantaa varten valmistettiin kaksi bentoniittivesisimulanttia, joista toinen edustaa kalsiitin suhteen selvästi ylikylläistä, suljetun systeemin vettä ja toinen ilman hiilidioksidin ja kalsiitin kanssa tasapainossa olevaa vettä. Stabiilisuustestissä näytepullot varastoitiin ilmassa tai typpikaapissa tiiviisti suljetussa tai löyhästi suljetussa pullossa. Säilytysajat olivat 2 viikkoa ja 4 viikkoa. Stabiilisuustestin lopussa liuoksista määritettiin Na +, K+, Ca 2 +, Mg 2 +, cr, SO/-,alkaliteetti ja ph. Kalsiitin suhteen ylikylläinen vesi näyttäisi säilyvän suljetun systeemin lyhytaikaisissa kokeissa verraten muuttumattomana. Kokeet tällaisella vedellä edellyttävät kuitenkin karbonaattikemian huolellista seurantaa. Avoimessa systeemissä, jossa pc0 2 :n arvo on pienempi kuin liuoksen vastaava arvo, pyrkii liuos tasapainoon ympäristön hiilidioksidin kanssa ja samalla taipumus ylikylläisen kalsiitin saastumiseen kasvaa. Näissä olosuhteissa vettä ei voi pitää stabiilina edes lyhytaikaisessa kokeessa. Kalsiitin ja ilmakehän hiilidioksidin kanssa tasapainossa oleva vesi näyttäisi verraten stabiililta suljetussa systeemissä ja ilman kanssa tasapainossa olevassa avoimessa systeemissä. Jos avoin systeemi on tasapainossa alhaisen hiilidioksidipitoisuuden kanssa, pyrkii karbonaattihiili poistumaan ja samalla ph nousee. Yhden kuukauden seurannassa ei kuitenkaan vielä havaittu kalsiitin alkavan saostua. Pitkäaikaiset kokeet tällä vedellä tulisi tehdä suljetussa systeemissä ja mielellään siten, että ympäristön hiilidioksidipitoisuus jätjestetään vastaamaan ilman hiilidioksidipitoisuutta. Tutkimuksessa on esitetty valmistusohje lähialueen kahdelle simulantille ja niiden käyttöön liittyviä rajoituksia.
19 18 KIRJALLISUUSVllTTEET Muurinen, A. & Lehikoinen, J Model for diffusion and porewater chemistry in compacted bentonite. Experimental arrangements and preliminary results of the porewater chemistry studies. Helsinki: Posiva Oy. 31 s. POSIV A ISBN Muurinen, A Model for diffusion and porewater chemistry in compacted bentonite. Preliminary results of the porewater chemistry studies. Helsinki: Posiva Oy. 26 s. Työraportti-97-62e.
20 LIITE! MALLINNUKSESSA KÄYTETTY TIETOKANTA EQPT Species List File: no. of elements on the data file = 9 no. of aqueous species in the master set = 10 the dimensioned limit = 1 00 the dimensioned limit = 500 datao.hmw.r2 Cll: GEMBOCHS.V2- EQ8- DATAO.HMW.R2 THERMODYNAMIC DATABASE generated by GEMBOCHS.v2-JEWEL.SRC.R3 02-aug :16:55 Output package: eq3 D~as~ hmw element = o element = ca element = cl element = h element = c element = k element = mg element = na element = s aqueous, atwt =, atwt =, atwt =, atwt =, atwt =, atwt =, atwt =, atwt =, atwt = ca++ h+ k+ na+ o2(g) co3-- hso4- mgoh+ 1 h2o 3 cl- 5 hco3-7 mg++ 9 so co2(aq) 13 caco3( aq) 15 mgco3(aq) 17 ohminerals 1 anhydrite 3 aphthitalite 5 arcanite 7 bloedite 9 burkeite 11 ca4cl2(oh)6: 13h2o 13 calcite 15 dolomite 17 gaylussite 19 gypsum 21 hexahydrite 23 k3h(so4)2 25 knaco3:6h2o 27 kalicinite 29 leonite 31 mercallite 33 misenite 35 na3h(so4)2 37 nahcolite 39 nesquehonite 41 picromerite 43 polyhalite 45 sylvite 47 tachyhydrite antarcticite aragonite bischofite brucite ca2cl2( oh )2: h2o cacl2:4h2o carnallite epsomite glauberite halite k2co3: 3/2h2o k8h4(co3)6:3h2o kainite kieserite magnesite mirabilite na2co3:7h2o na4ca(so4)3:2h2o natron oxychloride-mg pirssonite syngenite thenardite portlandite
21 LIITE I/2 49 thermonatrite 51 trona-k trona liquids 0 none * note- (eqpt/pcrsg) The pure liquids block has not been written on the data1 and data1f files, because the EQ3NR and EQ6 codes presently do not treat non-aqeuous liquids. Gases solid solutions 1 co2(g) 3 o2(g) h2(g) 0 none
22 LIITE II LÄHIALUEEN SUOLAISEN REFERENSSIVEDEN VALMISTUSOHJE (A-vesi) Ominaisuudet: Vesi on ylikylläinen kalsiitin suhteen ja tasapainossa pc0 2 = - 2, 7 kanssa. Vettä tulee käyttää vain suljetussa systeemissä. Karbonaattipitoisuuden, alkaliteetin ja ph:n muutosta tulee seurata. Liuoksen ollessa yhteydessä alhaiseen hiilidioksidipitoisuuteen karbonaatti pyrkii poistumaan, ph nousee ja kalsiiti voi saostua. Valmistus: Yhden litran valmistamiseen tarvitaan seuraavat määrät kemikaaleja KCI 0,360 g CaCI22H20 36,49 g NaCI 57,53 g MgS0 4 7H20 3,261 g MgC/2 6H20 3,157 g NaHC03 0,110 g Kukin kemikaali (paitsi NaHC0 3 ) liuotettaan erikseen deionisoituun veteen, jonka jälkeen liuokset yhdistetään ja laimennetaan tilavuus litraksi. Liuosta typetetään neljä tuntia hiilidioksidin poistamiseksi. Typetyksen jälkeen lisätään NaHC0 3 ja korvataan typetyksessä haihtunut vesi. Viikon stabiloitumisen jälkeen mitataan ph, jonka tulisi olla 7,4. Tarvittaessa säädetään ph laimealla HCl- tai NaOH-liuoksella.
23 LIITE III LÄHIALUEEN SUOLAISEN REFERENSSIVEDEN VALMISTUSOHJE (B-vesi) Ominaisuudet: Vesi on kylläinen kalsiitin suhteen ja tasapainossa hiilidioksidipitoisuuden pc0 2 = - 3,5 kanssa. Vettä tulee käyttää suljetussa systeemissä tai olosuhteissa, joissa ympäristön hiilidioksidipitoisuus vastaa tasapainopitoisuutta. Karbonaattipitoisuuden, alkaliteetin ja ph:n muutosta tulee seurata. Liuoksen ollessa yhteydessä alhaiseen hiilidioksidipitoisuuteen karbonaatti pyrkii poistumaan, ph nousee ja kalsiiti voi saostua. Valmistus: Yhden litran valmistamiseen tarvitaan seuraavat määrät kemikaaleja KCl 0,360 g CaCl22H20 36,33 g NaCl 57,60 g MgS04 7H20 3,144 g MgCl2 6H20 3,254 g NaHC03 0,0115 g Kukin kemikaali (paitsi NaHC03) liuotettaan erikseen deionisoituun, jonka jälkeen liuokset yhdistetään ja laimennetaan tilavuus litraksi. Liuosta typetettään neljä tuntia hiilidioksidin poistamiseksi. Typetyksen jälkeen lisätään NaHC03 ja korvataan typetyksessä haihtunut vesi. Viikon stabiloitumisen jälkeen mitataan ph, jonka tulisi olla 7,2. Tarvittaessa säädetään ph laimealla HCl- tai NaOH-liuoksella.
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
125,0 ml 0,040 M 75,0+125,0 ml Muodostetaan ionitulon lauseke ja sijoitetaan hetkelliset konsentraatiot
 4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa
 Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa Jari Aromaa, Lotta Rintala Teknillinen korkeakoulu Materiaalitekniikan laitos 1. Taustaa, miksi kupari syöpyy ja kuinka
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa Jari Aromaa, Lotta Rintala Teknillinen korkeakoulu Materiaalitekniikan laitos 1. Taustaa, miksi kupari syöpyy ja kuinka
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä
 Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Oppikirjan tehtävien ratkaisut
 Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Kenttätutkimus hiiliteräksen korroosiosta kaukolämpöverkossa
 1 (17) Tilaajat Suomen KL Lämpö Oy Sari Kurvinen Keisarinviitta 22 33960 Pirkkala Lahti Energia Olli Lindstam PL93 15141 Lahti Tilaus Yhteyshenkilö VTT:ssä Sähköposti 30.5.2007, Sari Kurvinen, sähköposti
1 (17) Tilaajat Suomen KL Lämpö Oy Sari Kurvinen Keisarinviitta 22 33960 Pirkkala Lahti Energia Olli Lindstam PL93 15141 Lahti Tilaus Yhteyshenkilö VTT:ssä Sähköposti 30.5.2007, Sari Kurvinen, sähköposti
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
Testata kalkinhajottajan toimivuutta laboratorio-olosuhteissa.
 TUTKIMUSSELOSTUS NRO PRO 463/02 1 (4) Tilaaja Oy Metro Therm Ab Kuutamokatu 8A Karri Siren 02210 ESPOO ja Nordkalk Oyj Abp Jari Laakkonen Tytyri 08100 Lohja Tilaus Käsittelijä Kohde Tehtävä Palaveri 24.3.2002
TUTKIMUSSELOSTUS NRO PRO 463/02 1 (4) Tilaaja Oy Metro Therm Ab Kuutamokatu 8A Karri Siren 02210 ESPOO ja Nordkalk Oyj Abp Jari Laakkonen Tytyri 08100 Lohja Tilaus Käsittelijä Kohde Tehtävä Palaveri 24.3.2002
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
C-14 vapautuminen loppusijoituksessa (HIILI-14) C-14 vapautuminen aktivoituneesta metallijätteestä loppusijoituksessa Kaija Ollila, VTT
 C-14 vapautuminen loppusijoituksessa (HIILI-14) C-14 vapautuminen aktivoituneesta metallijätteestä loppusijoituksessa Kaija Ollila, VTT C-14 pidättyminen kalsiittiin Jukka Lehto, HY Radiokemian laboratorio
C-14 vapautuminen loppusijoituksessa (HIILI-14) C-14 vapautuminen aktivoituneesta metallijätteestä loppusijoituksessa Kaija Ollila, VTT C-14 pidättyminen kalsiittiin Jukka Lehto, HY Radiokemian laboratorio
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko klo 8-10
 Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
Kertausluennot: Mahdollisuus pisteiden korotukseen ja rästisuorituksiin Keskiviikko 25.10 klo 8-10 Jokaisesta oikein ratkaistusta tehtävästä voi saada yhden lisäpisteen. Tehtävä, joilla voi korottaa kotitehtävän
TUTKIMUSSELOSTE. Tutkimuksen lopetus pvm. Näkösyv. m
 TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 3 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 3 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
Jaksollinen järjestelmä
 Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
Jaksollinen järjestelmä (a) Mikä on hiilen järjestysluku? (b) Mikä alkuaine kuuluu 15:een ryhmään ja toiseen jaksoon? (c) Montako protonia on berylliumilla? (d) Montako elektronia on hapella? (e) Montako
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
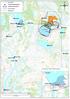 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
17VV VV 01021
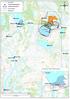 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Ympäristölupahakemuksen täydennys
 Ympäristölupahakemuksen täydennys Täydennyspyyntö 28.9.2012 19.10.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-10-19 2 / 6 Ympäristölupahakemuksen täydennys Pohjois-Suomen
Ympäristölupahakemuksen täydennys Täydennyspyyntö 28.9.2012 19.10.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-10-19 2 / 6 Ympäristölupahakemuksen täydennys Pohjois-Suomen
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA
 ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
ASPIRIININ MÄÄRÄN MITTAUS VALOKUVAAMALLA Jaakko Lohenoja 2009 Johdanto Asetyylisalisyylihapon määrä voidaan mitata spektrofotometrisesti hydrolysoimalla asetyylisalisyylihappo salisyylihapoksi ja muodostamalla
Seokset ja liuokset. 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen
 Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
FINAS-akkreditoitu testauslaboratorio T 025. SELVITYS ENDOMINES OY:n SIVUKIVINÄYTTEIDEN LIUKOISUUDESTA
 FINAS-akkreditoitu testauslaboratorio T 0 SELVITYS ENDOMINES OY:n SIVUKIVINÄYTTEIDEN LIUKOISUUDESTA LABTIUM OY Endomines Oy Selvitys sivukivinäytteiden liukoisuudesta Tilaaja: Endomines Oy Juha Reinikainen
FINAS-akkreditoitu testauslaboratorio T 0 SELVITYS ENDOMINES OY:n SIVUKIVINÄYTTEIDEN LIUKOISUUDESTA LABTIUM OY Endomines Oy Selvitys sivukivinäytteiden liukoisuudesta Tilaaja: Endomines Oy Juha Reinikainen
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo. Luento 8 CHEM-A1250
 Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Bentoniittipuskurin jääkauden jälkeinen eroosio
 Bentoniittipuskurin jääkauden jälkeinen eroosio Matti Liukkonen & Markus Olin # # Nykyinen osoite: Science consulting cheq&diff BENTONIITTIPUSKURIN JÄÄKAUSIEROOSIO Jääkausi- eli glasiaalieroosio voi heikentää
Bentoniittipuskurin jääkauden jälkeinen eroosio Matti Liukkonen & Markus Olin # # Nykyinen osoite: Science consulting cheq&diff BENTONIITTIPUSKURIN JÄÄKAUSIEROOSIO Jääkausi- eli glasiaalieroosio voi heikentää
Siilinjärven kaivoksen rikastushiekan hyödyntäminen pilaantuneen maaperän kunnostamisessa
 Siilinjärven kaivoksen rikastushiekan hyödyntäminen pilaantuneen maaperän kunnostamisessa Salla Venäläinen Helsingin yliopisto Maatalous-metsätieteellinen tiedekunta Elintarvike- ja ympäristötieteiden
Siilinjärven kaivoksen rikastushiekan hyödyntäminen pilaantuneen maaperän kunnostamisessa Salla Venäläinen Helsingin yliopisto Maatalous-metsätieteellinen tiedekunta Elintarvike- ja ympäristötieteiden
Liitetaulukko 1/11. Tutkittujen materiaalien kokonaispitoisuudet KOTIMAINEN MB-JÄTE <1MM SAKSAN MB- JÄTE <1MM POHJAKUONA <10MM
 Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Lupahakemuksen täydennys
 Lupahakemuksen täydennys 26.4.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-04-26 2 / 6 Lupahakemuksen täydennys Täydennyskehotuksessa (11.4.2012) täsmennettäväksi pyydetyt
Lupahakemuksen täydennys 26.4.2012 Talvivaara Sotkamo Oy Talvivaarantie 66 88120 Tuhkakylä Finland 2012-04-26 2 / 6 Lupahakemuksen täydennys Täydennyskehotuksessa (11.4.2012) täsmennettäväksi pyydetyt
Luku 3. Protolyysireaktiot ja vesiliuoksen ph
 Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
TUTKIMUSSELOSTE. Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: Tarkkailukierros: vko 2. Tutkimuksen lopetus pvm
 TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 2 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 2 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Sähkökemialliset tarkastelut HSC:llä
 Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
Sähkökemialliset tarkastelut HSC:llä Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 5 Tavoite Oppia hyödyntämään HSC-ohjelmistoa sähkökemiallisissa tarkasteluissa 1 Sisältö Sähkökemiallisiin
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
VXLIRAPORTTI LOVIISAN H~~STHOLMENIN POHJAVEDEN GEOKEMIALLISESTA TUTKIMUKSESTA
 ARKISTOKAPPALE I / Juho Hyyppa Geologinen tutkimuslaitos Maaperaosasto VXLIRAPORTTI LOVIISAN H~~STHOLMENIN POHJAVEDEN GEOKEMIALLISESTA TUTKIMUKSESTA 31.8.19 82 Imatran Voima Oy ja Geologinen tutkimuslaitos
ARKISTOKAPPALE I / Juho Hyyppa Geologinen tutkimuslaitos Maaperaosasto VXLIRAPORTTI LOVIISAN H~~STHOLMENIN POHJAVEDEN GEOKEMIALLISESTA TUTKIMUKSESTA 31.8.19 82 Imatran Voima Oy ja Geologinen tutkimuslaitos
TUTKIMUSTODISTUS 2012E
 TUTKIMUSTODISTUS 2012E- 21512-1 Tarkkailu: Talvivaara kipsisakka-altaan vuoto 2012 Tarkkailukierros: vko 51 Tilaaja: Pöyry Finland Oy Otto pvm. Tulo pvm. Tutkimuksen lopetus pvm. Havaintopaikka Tunnus
TUTKIMUSTODISTUS 2012E- 21512-1 Tarkkailu: Talvivaara kipsisakka-altaan vuoto 2012 Tarkkailukierros: vko 51 Tilaaja: Pöyry Finland Oy Otto pvm. Tulo pvm. Tutkimuksen lopetus pvm. Havaintopaikka Tunnus
Kuparin korroosio hapettomissa olosuhteissa
 Kuparin korroosio hapettomissa olosuhteissa Olof Forsén, Antero Pehkonen, Jari Aromaa Aalto-yliopisto Timo Saario VTT 1 Kuparin korroosio hapettomissa olosuhteissa Taustaa Aikaisemmat tutkimukset Tutkimuksen
Kuparin korroosio hapettomissa olosuhteissa Olof Forsén, Antero Pehkonen, Jari Aromaa Aalto-yliopisto Timo Saario VTT 1 Kuparin korroosio hapettomissa olosuhteissa Taustaa Aikaisemmat tutkimukset Tutkimuksen
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
TESTAUSSELOSTE Vesilaitosvesi
 LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 3.8.2017 17-2767 #1 1 (6) Vihdin kunta / Vihdin Vesi Saarikko Santeri vesilaitoksen johtaja PL 13 03101 NUMMELA Tilausnro
LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 3.8.2017 17-2767 #1 1 (6) Vihdin kunta / Vihdin Vesi Saarikko Santeri vesilaitoksen johtaja PL 13 03101 NUMMELA Tilausnro
Olkiluodon pohjavesikemia - suolainen ja murtovesi - suolaisen referenssiveden resepti
 Työ r a p o r t t i- 9 7-2 5 Olkiluodon pohjavesikemia - suolainen ja murtovesi - suolaisen referenssiveden resepti Ulla Vuorinen, Kaija Ollila VTT Kemiantekniikka Margit Snellman Posiva Oy Elokuu 1997
Työ r a p o r t t i- 9 7-2 5 Olkiluodon pohjavesikemia - suolainen ja murtovesi - suolaisen referenssiveden resepti Ulla Vuorinen, Kaija Ollila VTT Kemiantekniikka Margit Snellman Posiva Oy Elokuu 1997
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Järviveden happamoitumiseen vaikuttavat tekijät. Tulokset: KaiHali-projekti
 Järviveden happamoitumiseen vaikuttavat tekijät Tulokset: 1.3.-31.8.2017 KaiHali-projekti Hanna Runtti 17.11.2017 Sisällysluettelo 1 Taustaa... 3 2 Tutkittavat järvivedet... 3 3 Koesuunnitelmat... 3 3.1
Järviveden happamoitumiseen vaikuttavat tekijät Tulokset: 1.3.-31.8.2017 KaiHali-projekti Hanna Runtti 17.11.2017 Sisällysluettelo 1 Taustaa... 3 2 Tutkittavat järvivedet... 3 3 Koesuunnitelmat... 3 3.1
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Heinijärven vedenlaatuselvitys 2014
 Heinijärven vedenlaatuselvitys 2014 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 3.12.2014 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin vuonna 2014 Helsingin yliopiston
Heinijärven vedenlaatuselvitys 2014 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto 3.12.2014 Johdanto Heinijärven ja siihen laskevien ojien vedenlaatua selvitettiin vuonna 2014 Helsingin yliopiston
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Hiilidioksidin hyötykäyttö betonin valmistuksessa
 Hiilidioksidin hyötykäyttö betonin valmistuksessa Bio-CO 2 hankkeen päätösseminaari Sampo Mäkikouri 30.8.2018 Esityksen sisältö Johdanto. Hiilidioksidin hyötykäyttö betonin valmistuksessa. Termodynaaminen
Hiilidioksidin hyötykäyttö betonin valmistuksessa Bio-CO 2 hankkeen päätösseminaari Sampo Mäkikouri 30.8.2018 Esityksen sisältö Johdanto. Hiilidioksidin hyötykäyttö betonin valmistuksessa. Termodynaaminen
Ellinghamin diagrammit
 Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
Ellinghamin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 1 - Luento 2 Tavoite Oppia tulkitsemaan (ja laatimaan) vapaaenergiapiirroksia eli Ellinghamdiagrammeja 1 Tasapainopiirrokset
SULFIDIEN AIHEUTTAMA KUPARIN JÄNNITYSKORROOSIO
 SULFIDIEN AIHEUTTAMA KUPARIN JÄNNITYSKORROOSIO Timo Saario VTT Temaattinen KYT-seminaari 29.04.2010 1 TAUSTAA - 1 Japanilainen tutkimusryhmä raportoi vuonna 2007 että CuOFP on altis sulfidien aiheuttamalle
SULFIDIEN AIHEUTTAMA KUPARIN JÄNNITYSKORROOSIO Timo Saario VTT Temaattinen KYT-seminaari 29.04.2010 1 TAUSTAA - 1 Japanilainen tutkimusryhmä raportoi vuonna 2007 että CuOFP on altis sulfidien aiheuttamalle
TALVIVAARA SOTKAMO OY. Laimennuslaskelmat
 17.1.2013 TALVIVAARA SOTKAMO OY Laimennuslaskelmat 1 Pöyry Finland Oy Kari Kainua, FM Heimo Vepsä, FM Yhteystiedot PL 20, Tutkijantie 2 A 90571 Oulu puh. 010 33280 sähköposti etunimi.sukunimi@poyry.com
17.1.2013 TALVIVAARA SOTKAMO OY Laimennuslaskelmat 1 Pöyry Finland Oy Kari Kainua, FM Heimo Vepsä, FM Yhteystiedot PL 20, Tutkijantie 2 A 90571 Oulu puh. 010 33280 sähköposti etunimi.sukunimi@poyry.com
TUTKIMUSTODISTUS. Jyväskylän Ympäristölaboratorio. Sivu: 1(1) Päivä: 09.10.14. Tilaaja:
 Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Kevitsan vesistötarkkailu, perus, syyskuu 2018
 Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-002382-01 12.10.2018 Tutkimusnro EUAA56-00002241 Asiakasnro RZ0000092 Näytteenottaja
Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-002382-01 12.10.2018 Tutkimusnro EUAA56-00002241 Asiakasnro RZ0000092 Näytteenottaja
Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus.
 Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus. 2012 Envitop Oy Riihitie 5, 90240 Oulu Tel: 08375046 etunimi.sukunimi@envitop.com www.envitop.com 2/5 KUUSAKOSKI OY Janne Huovinen Oulu 1 Tausta Valtioneuvoston
Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus. 2012 Envitop Oy Riihitie 5, 90240 Oulu Tel: 08375046 etunimi.sukunimi@envitop.com www.envitop.com 2/5 KUUSAKOSKI OY Janne Huovinen Oulu 1 Tausta Valtioneuvoston
Myös normaali sadevesi on hieman hapanta (ph n.5,6) johtuen ilman hiilidioksidista, joka liuetessaan veteen muodostaa hiilihappoa.
 sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
Verikaasuanalyysi. Esitys (anestesia)hoitajille. Vesa Lappeteläinen 3.10.2013
 Verikaasuanalyysi Esitys (anestesia)hoitajille Vesa Lappeteläinen 3.10.2013 Yleistä Yleensä valtimoverestä otettava verinäyte, joka analysoidaan vieritestianalysaattorilla Nopein tapa saada keskeistä tietoa
Verikaasuanalyysi Esitys (anestesia)hoitajille Vesa Lappeteläinen 3.10.2013 Yleistä Yleensä valtimoverestä otettava verinäyte, joka analysoidaan vieritestianalysaattorilla Nopein tapa saada keskeistä tietoa
Liukoisuus
 Liukoisuus REAKTIOT JA TASAPAINO, KE5 Kertausta: Eri suolojen liukeneminen veteen on tärkeä arkipäivän ilmiö. Yleensä suolan liukoisuus veteen kasvaa, kun lämpötila nousee. Tosin esimerkiksi kalsiumkarbonaatti,
Liukoisuus REAKTIOT JA TASAPAINO, KE5 Kertausta: Eri suolojen liukeneminen veteen on tärkeä arkipäivän ilmiö. Yleensä suolan liukoisuus veteen kasvaa, kun lämpötila nousee. Tosin esimerkiksi kalsiumkarbonaatti,
Ilmakanaviston äänenvaimentimien (d=100-315 mm) huoneiden välisen ilmaääneneristävyyden määrittäminen
 TESTAUSSELOSTE NRO VTT-S-02258-06 1 (2) Tilaaja IVK-Tuote Oy Helmintie 8-10 2 Jyväskylä Tilaus Tuomas Veijalainen, 9.1.2006 Yhteyshenkilö VTT:ssä VTT, Valtion teknillinen tutkimuskeskus Erikoistutkija
TESTAUSSELOSTE NRO VTT-S-02258-06 1 (2) Tilaaja IVK-Tuote Oy Helmintie 8-10 2 Jyväskylä Tilaus Tuomas Veijalainen, 9.1.2006 Yhteyshenkilö VTT:ssä VTT, Valtion teknillinen tutkimuskeskus Erikoistutkija
Tiedelimsa. KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä.
 KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
Tutkimustodistus Projekti: /10
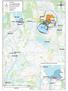 1/4 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2018, heinäkuu Asiakkaan viite: PO45696 Näytteenottopvm: 16.7.2018 Näyte saapui: 18.7.2018 Näytteenottaja:
1/4 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2018, heinäkuu Asiakkaan viite: PO45696 Näytteenottopvm: 16.7.2018 Näyte saapui: 18.7.2018 Näytteenottaja:
Tips for teachers and expected results
 Tips for teachers and expected results Työskentely aloitetaan JOHDANNOLLA, jonka aikana annetaan tietoa vatsahappoihin liittyvistä ongelmista ja antasideista. Lisäksi esitetään kysymys, joka ohjaa oppilaiden
Tips for teachers and expected results Työskentely aloitetaan JOHDANNOLLA, jonka aikana annetaan tietoa vatsahappoihin liittyvistä ongelmista ja antasideista. Lisäksi esitetään kysymys, joka ohjaa oppilaiden
Top Analytica Oy Ab. XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio
 XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio Röntgenfluoresenssi Röntgensäteilyllä irroitetaan näytteen atomien sisäkuorilta (yleensä K ja L kuorilta) elektroneja. Syntyneen vakanssin paikkaa
XRF Laite, menetelmät ja mahdollisuudet Teemu Paunikallio Röntgenfluoresenssi Röntgensäteilyllä irroitetaan näytteen atomien sisäkuorilta (yleensä K ja L kuorilta) elektroneja. Syntyneen vakanssin paikkaa
Määritelmät. Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin
 Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Í%SC{ÂÂ!5eCÎ. Korvaa* Kevitsan vesistötarkkailu, PERUS, marraskuu 2018
 Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-008423-02 Tutkimusnro EUAA56-00006080 Asiakasnro RZ0000092 Näytteenottaja Timo Putkonen
Boliden Kevitsa Mining Oy Anniina Salonen Kevitsantie 730 99670 PETKULA s-posti: anniina.salonen@boliden.com AR-18-RZ-008423-02 Tutkimusnro EUAA56-00006080 Asiakasnro RZ0000092 Näytteenottaja Timo Putkonen
TESTAUSSELOSTE Nro VTT-S Pro Clima Acrylat Solid liiman tartuntakokeet
 TESTAUSSELOSTE Nro VTT-S-25-14.9. Pro Clima Acrylat Solid liiman tartuntakokeet Tilaaja: Redi-Talot Oy TESTAUSSELOSTE NRO VTT-S-25-1 (5) Tilaaja Redi-Talot Oy Jarmo Puronlahti Yrittäjäntie 23 18 KLAUKKALA
TESTAUSSELOSTE Nro VTT-S-25-14.9. Pro Clima Acrylat Solid liiman tartuntakokeet Tilaaja: Redi-Talot Oy TESTAUSSELOSTE NRO VTT-S-25-1 (5) Tilaaja Redi-Talot Oy Jarmo Puronlahti Yrittäjäntie 23 18 KLAUKKALA
Ioniselektiivinen elektrodi
 ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
KE5 Kurssikoe Kastellin lukio 2012 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko.
 KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011
 Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto Johdanto Tämä raportti on selvitys Luoteis-Tammelan Heinijärven ja siihen laskevien ojien
Luoteis-Tammelan vesistöjen vedenlaatuselvitys v. 2011 Tiina Tulonen Lammin biologinen asema Helsingin yliopisto Johdanto Tämä raportti on selvitys Luoteis-Tammelan Heinijärven ja siihen laskevien ojien
Suolaliuoksen ph
 Suoaiuoksen ph REAKTIOT JA TASAPAINO, KE5 Liuoksen ph-arvoon vaikuttaa oksonium- ja hydroksidi-ionien ainemäärien isäksi neutraoitumisessa muodostuvan suoan protoyysi sen mukaan mistä suoasta on kyse.
Suoaiuoksen ph REAKTIOT JA TASAPAINO, KE5 Liuoksen ph-arvoon vaikuttaa oksonium- ja hydroksidi-ionien ainemäärien isäksi neutraoitumisessa muodostuvan suoan protoyysi sen mukaan mistä suoasta on kyse.
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Tulosten analysointi. Liite 1. Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma
 Liite 1 Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma Tulosten analysointi Liite loppuraporttiin Jani Isokääntä 9.4.2015 Sisällys 1.Tutkimustulosten
Liite 1 Ympäristöministeriö - Ravinteiden kierrätyksen edistämistä ja Saaristomeren tilan parantamista koskeva ohjelma Tulosten analysointi Liite loppuraporttiin Jani Isokääntä 9.4.2015 Sisällys 1.Tutkimustulosten
KE4, KPL. 3 muistiinpanot. Keuruun yläkoulu, Joonas Soininen
 KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KE4, KPL. 3 muistiinpanot Keuruun yläkoulu, Joonas Soininen KPL 3: Ainemäärä 1. Pohtikaa, miksi ruokaohjeissa esim. kananmunien ja sipulien määrät on ilmoitettu kappalemäärinä, mutta makaronit on ilmoitettu
KÄYTTÖTURVALLISUUSTIEDOTE
 Sivu: 1/5 Etiketti 2.2: Palamattomat, myrkyttömät kaasut. 1. AINEEN TAI VALMISTEEN JA YHTIÖN TAI YRITYKSEN TUNNISTETIEDOT 1.1 Kemikaalin tunnistustiedot Kauppanimi 1.2 Kemikaalin käyttötarkoitus 1.2.1
Sivu: 1/5 Etiketti 2.2: Palamattomat, myrkyttömät kaasut. 1. AINEEN TAI VALMISTEEN JA YHTIÖN TAI YRITYKSEN TUNNISTETIEDOT 1.1 Kemikaalin tunnistustiedot Kauppanimi 1.2 Kemikaalin käyttötarkoitus 1.2.1
Peltojen kipsikäsittelyn vaikutukset maahan ja veteen
 Kuva: Eliisa Punttila Peltojen kipsikäsittelyn vaikutukset maahan ja veteen Petri Ekholm Suomen ympäristökeskus SYKE 3.4.2019 1 Miten kipsi vaikuttaa? CaSO 4 2H 2 O Sato ja viljely Paljon rikkiä ja kalsiumia,
Kuva: Eliisa Punttila Peltojen kipsikäsittelyn vaikutukset maahan ja veteen Petri Ekholm Suomen ympäristökeskus SYKE 3.4.2019 1 Miten kipsi vaikuttaa? CaSO 4 2H 2 O Sato ja viljely Paljon rikkiä ja kalsiumia,
Rak Betonitekniikka 2 Harjoitus Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys
 Rak-82.3131 Betonitekniikka 2 Harjoitus 2 23.9.2010 Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys Portlandsementti Portlandsementin kemiallinen koostumus KOMPONENTTI LYHENNE PITOISUUS
Rak-82.3131 Betonitekniikka 2 Harjoitus 2 23.9.2010 Rakennussementit, klinkkerimineraalikoostumus ja lämmönkehitys Portlandsementti Portlandsementin kemiallinen koostumus KOMPONENTTI LYHENNE PITOISUUS
CHEM-C2230 Pintakemia. Työ 2: Etikkahapon adsorptio aktiivihiileen. Työohje
 CHEM-C2230 Pintakemia Tö 2: Etikkahapon orptio aktiivihiileen Töohje 1 Johdanto Kaasun ja kiinteän aineen rajapinnalla tapahtuu leensä kaasun orptiota. Mös liuoksissa tapahtuu usein liuenneen aineen orptiota
CHEM-C2230 Pintakemia Tö 2: Etikkahapon orptio aktiivihiileen Töohje 1 Johdanto Kaasun ja kiinteän aineen rajapinnalla tapahtuu leensä kaasun orptiota. Mös liuoksissa tapahtuu usein liuenneen aineen orptiota
KEHÄVALU OY Mattilanmäki 24 TAMPERE
 PENTTI PAUKKONEN VALUHIEKAN HAITTA-AINETUTKIMUS KEHÄVALU OY Mattilanmäki 24 TAMPERE Työ nro 82102448 23.10.2002 VALUHIEKAN HAITTA-AINETUTKIMUS Kehävalu Oy 1 SISÄLLYS 1. JOHDANTO 2 2. TUTKIMUSKOHDE 2 2.1
PENTTI PAUKKONEN VALUHIEKAN HAITTA-AINETUTKIMUS KEHÄVALU OY Mattilanmäki 24 TAMPERE Työ nro 82102448 23.10.2002 VALUHIEKAN HAITTA-AINETUTKIMUS Kehävalu Oy 1 SISÄLLYS 1. JOHDANTO 2 2. TUTKIMUSKOHDE 2 2.1
Spektrofotometria ja spektroskopia
 11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
11 KÄYTÄNNÖN ESIMERKKEJÄ INSTRUMENTTIANALYTIIKASTA Lisätehtävät Spektrofotometria ja spektroskopia Esimerkki 1. Mikä on transmittanssi T ja transmittanssiprosentti %T, kun absorbanssi A on 0, 1 ja 2. josta
KaiHali & DROMINÄ hankkeiden loppuseminaari
 KaiHali & DROMINÄ hankkeiden loppuseminaari Sedimentin geokemiallisten olojen muuttuminen kaivoskuormituksessa (KaiHali-projektin työpaketin 2 osatehtävä 3), Jari Mäkinen, Tommi Kauppila ja Tatu Lahtinen
KaiHali & DROMINÄ hankkeiden loppuseminaari Sedimentin geokemiallisten olojen muuttuminen kaivoskuormituksessa (KaiHali-projektin työpaketin 2 osatehtävä 3), Jari Mäkinen, Tommi Kauppila ja Tatu Lahtinen
GeoChem. Havainnot uraanin käyttäytymisestä kiteisissä kivissä 2006-2010 Mira Markovaara-Koivisto Teknillinen korkeakoulu, Geoympäristötekniikka
 GeoChem Havainnot uraanin käyttäytymisestä kiteisissä kivissä 2006-2010 Mira Markovaara-Koivisto Teknillinen korkeakoulu, Geoympäristötekniikka 15.2.2008 KYT2010 seminaari - Kalliokulkeutuminen Helsingin
GeoChem Havainnot uraanin käyttäytymisestä kiteisissä kivissä 2006-2010 Mira Markovaara-Koivisto Teknillinen korkeakoulu, Geoympäristötekniikka 15.2.2008 KYT2010 seminaari - Kalliokulkeutuminen Helsingin
Kallioperän redox-olosuhteiden muutosten tutkiminen
 Kallioperän redox-olosuhteiden muutosten tutkiminen Radiokemian laboratorio Kemian laitos Juhani Suksi KYT 21 Kalliokulkeutuminen-seminaari 15.2.28 Kallioperän redox-olosuhteiden muutosten tutkiminen Uraanin
Kallioperän redox-olosuhteiden muutosten tutkiminen Radiokemian laboratorio Kemian laitos Juhani Suksi KYT 21 Kalliokulkeutuminen-seminaari 15.2.28 Kallioperän redox-olosuhteiden muutosten tutkiminen Uraanin
Í%R]'ÂÂÂVqEÎ. Päivämäärä Sivu 1 / 2
![Í%R]'ÂÂÂVqEÎ. Päivämäärä Sivu 1 / 2 Í%R]'ÂÂÂVqEÎ. Päivämäärä Sivu 1 / 2](/thumbs/70/63468890.jpg) 113-2016-00010172 Päivämäärä 14.9.2016 Sivu 1 / 2 Reisjärven Vesiosuuskunta Asiakasnro: KF0000653 Reisjärven Vesiosuuskunta Kirkkotie 6 A 1 85900 Reisjärvi Jakelu : Jorma Turunen (jorma.turunen@selanne.net),
113-2016-00010172 Päivämäärä 14.9.2016 Sivu 1 / 2 Reisjärven Vesiosuuskunta Asiakasnro: KF0000653 Reisjärven Vesiosuuskunta Kirkkotie 6 A 1 85900 Reisjärvi Jakelu : Jorma Turunen (jorma.turunen@selanne.net),
Reaktiosarjat
 Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hemosol B0 käsittää kaksitilaisen PVC (polyvinyyli) pussin, joka sisältää
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hemosol B0 hemofiltraatio- ja hemodialyysineste. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hemosol B0 käsittää kaksitilaisen PVC (polyvinyyli) pussin, joka sisältää
Pohjavesinäytteiden otto Eurajoen Olkiluodon kairanrei'istä Ol-KR3,0l-KR4,0l-KR7,0l-KR9 ja Ol-KR 10 vuosina 1998-1 999
 Työraportti 9 9-7 Pohjavesinäytteiden otto Eurajoen Olkiluodon kairanrei'istä Ol-KR,l-KR4,l-KR7,l-KR9 ja Ol-KR vuosina 998-999 Virpi Karttunen Mia Mäntynen Outi Salonen.Joulukuu 999 POSIVA OY Mikonkatu
Työraportti 9 9-7 Pohjavesinäytteiden otto Eurajoen Olkiluodon kairanrei'istä Ol-KR,l-KR4,l-KR7,l-KR9 ja Ol-KR vuosina 998-999 Virpi Karttunen Mia Mäntynen Outi Salonen.Joulukuu 999 POSIVA OY Mikonkatu
Osasto: Materiaalin käsittely, Rikkihapon annostelu agglomeraattiin kuljettimella
 1/6 Osasto: Projekti: TK Materiaalin käsittely, Rikkihapon annostelu agglomeraattiin kuljettimella Pvm. 17.12.2015 jatkettu 7.4.2016 Tekijä: Ville Heikkinen, Matti Okkonen, Herkko Kylli Asiakirja: Tulokset
1/6 Osasto: Projekti: TK Materiaalin käsittely, Rikkihapon annostelu agglomeraattiin kuljettimella Pvm. 17.12.2015 jatkettu 7.4.2016 Tekijä: Ville Heikkinen, Matti Okkonen, Herkko Kylli Asiakirja: Tulokset
Kasvatuskokeet mädätysjäännös- ja kompostiseoksilla
 Kasvatuskokeet mädätysjäännös- ja kompostiseoksilla Selvitys Lepaa 17.12.2014 Teo Kanniainen Bioliike-projektia (v. 2013-2014) rahoitetaan Etelä-Suomen EAKR-ohjelmasta. SISÄLLYS 1 KASVATUSKOE JA TAVOITTEET...
Kasvatuskokeet mädätysjäännös- ja kompostiseoksilla Selvitys Lepaa 17.12.2014 Teo Kanniainen Bioliike-projektia (v. 2013-2014) rahoitetaan Etelä-Suomen EAKR-ohjelmasta. SISÄLLYS 1 KASVATUSKOE JA TAVOITTEET...
VILJAVUUSTUTKIMUS s-posti: Päivämäärä Asiakasnro Tutkimusnro
 1/7 Näytteen numero 1 2 3 4 5 6 7 Peruslohkotunnus 04749-48 04757-56 04765-64 04777-76 04778-77 04779-78 04784-83 Nimi A1 A5 B6 KA KB S BB Pintamaan maalaji a) HHt HHt HHt HHt HHt HHt HHt Multavuus a)
1/7 Näytteen numero 1 2 3 4 5 6 7 Peruslohkotunnus 04749-48 04757-56 04765-64 04777-76 04778-77 04779-78 04784-83 Nimi A1 A5 B6 KA KB S BB Pintamaan maalaji a) HHt HHt HHt HHt HHt HHt HHt Multavuus a)
TESTAUSSELOSTE Vesilaitosvesi Tilausnro (1001/VIHTIVL), saapunut , näytteet otettu Näytteenottaja: Tilaaja, JM
 LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 12.12.2016 16-4749 #1 1 (4) Vihdin kunta / Vihdin Vesi PL 13 03101 NUMMELA Tilausnro 98290 (1001/VIHTIVL), saapunut 21.11.2016,
LÄNSI-UUDENMAAN VESI JA YMPÄRISTÖ RY Laboratorio TESTAUSSELOSTE Vesilaitosvesi 12.12.2016 16-4749 #1 1 (4) Vihdin kunta / Vihdin Vesi PL 13 03101 NUMMELA Tilausnro 98290 (1001/VIHTIVL), saapunut 21.11.2016,
Vinkkejä opettajille ja odotetut tulokset SIVU 1
 Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Kosteikkojen puhdistustehokkuuden parantaminen sorptiomateriaaleilla
 Kosteikkojen puhdistustehokkuuden parantaminen sorptiomateriaaleilla Satu Maaria Karjalainen SYKE TuKos-hankkeen loppuseminaari 1.9.2011 Oulussa Tausta Osassa turvetuotannon t t valumavesiä puhdistavissa
Kosteikkojen puhdistustehokkuuden parantaminen sorptiomateriaaleilla Satu Maaria Karjalainen SYKE TuKos-hankkeen loppuseminaari 1.9.2011 Oulussa Tausta Osassa turvetuotannon t t valumavesiä puhdistavissa
Arseeniriskin hallinta kiviainesliiketoiminnassa. Pirjo Kuula TTY/Maa- ja pohjarakenteet
 Arseeniriskin hallinta kiviainesliiketoiminnassa Pirjo Kuula TTY/Maa- ja pohjarakenteet Sisältö Faktat Arseenin esiintyminen kallioperässä ja pohjavedessä Mitä pitää mitata ja milloin? Arseenipitoisuuden
Arseeniriskin hallinta kiviainesliiketoiminnassa Pirjo Kuula TTY/Maa- ja pohjarakenteet Sisältö Faktat Arseenin esiintyminen kallioperässä ja pohjavedessä Mitä pitää mitata ja milloin? Arseenipitoisuuden
Halax WC-istuimen ilmanvaihtojärjestelmän vaikutus WC-tilan sisäilman laatuun
 TUTKIMUSSELOSTUS Nro VTT-S-08510-13 15.07.2014 Halax WC-istuimen ilmanvaihtojärjestelmän vaikutus WC-tilan sisäilman laatuun Tilaaja: Halax Oy TUTKIMUSSELOSTUS NRO VTT-S-08510-13 1 (7) Tilaaja Tilaus Yhteyshenkilö
TUTKIMUSSELOSTUS Nro VTT-S-08510-13 15.07.2014 Halax WC-istuimen ilmanvaihtojärjestelmän vaikutus WC-tilan sisäilman laatuun Tilaaja: Halax Oy TUTKIMUSSELOSTUS NRO VTT-S-08510-13 1 (7) Tilaaja Tilaus Yhteyshenkilö
Liukeneminen 31.8.2016
 Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Orimattilan Vesi Oy:n Vääräkosken jätevedenpuhdistamon velvoitetarkkailu, tuloslausunto tammikuu 2016
 Orimattilan kaupunki / vesilaitos Tokkolantie 3 16300 ORIMATTILA Orimattilan Vesi Oy:n Vääräkosken jätevedenpuhdistamon velvoitetarkkailu, tuloslausunto tammikuu 2016 Vääräkosken jätevedenpuhdistamon tarkkailunäytteet
Orimattilan kaupunki / vesilaitos Tokkolantie 3 16300 ORIMATTILA Orimattilan Vesi Oy:n Vääräkosken jätevedenpuhdistamon velvoitetarkkailu, tuloslausunto tammikuu 2016 Vääräkosken jätevedenpuhdistamon tarkkailunäytteet
