RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
|
|
|
- Anne Saaristo
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Neotigason (asitretiini) 10 mg kapseli, kova Neotigason (asitretiini) 25 mg kapseli, kova Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Psoriaasin vaikea-asteiset muodot mukaan lukien: erytroderminen psoriaasi ja lokalisoitunut tai generalisoitunut pustulaarinen psoriaasi; (krooninen vaikea-asteinen ihosairaus, jolle luonteenomaista ovat iholla esiintyvät punaiset laikut, joihin liittyy usein hopeanvalkoisia suomumaisia kuolleita ihosoluja) Psoriaasi on pitkäaikainen ihosairaus, jota sairastaa noin 2 4 % länsimaiden väestöstä. Valkoihoiset ovat muita etnisiä ryhmiä alttiimpia sairaudelle. 1 Psoriaasi on usein perinnöllistä, mutta sen voivat laukaista tai oireita voivat pahentaa myös tupakointi, ylipaino, alkoholin kulutus, ruokavalio, infektiot, lääkitys ja stressaavat elämäntilanteet. 2 Vaikka psoriaasi ei yleensä ole hengenvaarallinen sairaus, se on krooninen sairaus, jossa on remissiovaiheita ja vaiheita, jolloin tauti pahenee. Toisinaan hoidolla ei saavuteta hoitovastetta. Vaikea-asteisissa tapauksissa se voi edetä niveltulehduksiin. Noin %:lla psoriaasin oireet helpottuvat eri pituisiksi jaksoiksi. 5 Vaikea-asteiset keratinisaatiohäiriöt, kuten: synnynnäinen iktyoosi, pityriasis rubra pilaris, Darierin tauti, muut keratinisaatiohäiriöt, jotka voivat olla vastustuskykyisiä muille hoidoille (vaikeat sairaudet, joihin liittyy ihon kuivumista ja suomuisuutta). Synnynnäinen iktyoosi Ichthyosis vulgaris on synnynnäinen ihosairaus, jossa kuolleet ihosolut kerääntyvät ihon pintaan paksuiksi, kuiviksi suomuiksi. Tautia esiintyy noin yhdellä 300 henkilöstä Yhdysvalloissa. Sitä esiintyy yhtä paljon kummallakin sukupuolella ja kaikissa etnisissä ryhmissä. Sairaus todetaan yleisesti ensimmäisen elinvuoden aikana ja valtaosassa tapauksista 5. elinvuoteen mennessä. Ihon suomuisuus lisääntyy yleensä murrosikään saakka, ja tämän jälkeen oireet yleisesti ottaen vähenevät iän myötä. Kyseessä on krooninen sairaus, joka usein vaatii jatkuvaa hoitoa. 6 Pityriasis rubra pilaris Pityriasis rubra pilaris on harvinainen ihosairaus, joka aiheuttaa jatkuvan tulehduksen ja ihon kuoriutumista. Tautia voi esiintyä millä tahansa etnisellä ryhmällä, ja sitä esiintyy yhtä paljon kummallakin sukupuolella. Sairaus voi puhjeta lapsena (perinnöllinen muoto) tai aikuisena (hankittu muoto).
2 Pityriasis rubra pilarista sairastavien potilaiden kämmenet ja jalkapohjat voivat paksuuntua kivuliaasti ja aiheuttaa invalidisoitumista. Näiden potilaiden kuntoon vaikuttaa ihon punaisuuden mahdollinen generalisoituminen. 7 Keratodermia palmoplantaris Perinnöllinen keratodermia palmoplantaris (liikasarveistuminen) on ihosairaus, jolle on luonteenomaista kämmenien ja jalkapohjien ihon paksuuntuminen. Sairautta on raportoitu esiintyvän harvoin (5,2 henkilöllä :sta) ja useammin miehillä kuin naisilla. Sairaus voi olla perinnöllinen tai hankittu, ja jos tähän liittyy muita oireyhtymiä, liikasarveistuminen on näistä vallitseva. Perinnölliset muodot voivat paikantua käsiin ja jalkoihin tai liittyä enemmän generalisoituneisiin ihosairauksiin. 42 Darierin tauti Darierin tauti on melko harvinainen ja sitä esiintyy yleensä myöhäislapsuudessa tai varhaisaikuisuudessa. Se on perinnöllinen sairaus, jota esiintyy saman verran kummallakin sukupuolella. Oireita voivat olla kutiava iho ja joissain tapauksissa kutiavien ihoalueiden kipu. Potilaat, joilla on tämä sairaus, ovat herkempiä saamaan ihotulehduksia. 8 Lichen planus Lichen planusta (punajäkälää) esiintyy yleisesti keski-ikäisillä naisilla ja miehillä. Oireita voi esiintyä iholla, suussa tai genitaalialueilla. Iholla esiintyvän sairauden syöpäriski on matala, mutta suussa se on korkeampi. Yleisesti ottaen riski on kuitenkin matala (alle 2 %). 43 VI.2.2 Yhteenveto hoidon hyödyistä Yhteensä 12 kliinistä tutkimusta on osoittanut, että mg:n asitretiinin vuorokausiannokset ovat sopivia psoriaasin hoitoon. Näiden tutkimusten tulokset osoittivat, että psoriaasin oireet poistuivat kokonaan 31,5 %:lla potilaista, parantuivat merkitsevästi 16,5 %:lla potilaista ja parantuivat hieman 12,5 %:lla potilaista. 8,5 %:lla potilaista muutosta ei tapahtunut tai sairauden oireet pahenivat. Tulokset osoittivat myös, että parhaat hoitotulokset saavutettiin psoriaasin vaikea-asteisimmissa ja harvinaisemmissa muodoissa (pustulaarinen ja erytroderminen) kuin yleisimmissä läiskäpsoriaaseissa potilaalla 30:sta (26 miestä ja neljä naista, iältään vuotiaita) psoriaasi saavutti remissiovaiheen tai oireet paranivat merkitsevästi tutkimuksessa, johon osallistuvilla potilailla oli vaikea-asteisia keratinisaatiohäiriöitä ja joita hoidettiin 35 mg:n asitretiiniannoksella neljän viikon ajan ja tämän jälkeen mg:n vuorokausiannoksilla. Hoidolla oli myönteisiä vaikutuksia ihon suomuisuuden, punoituksen, kutinan sekä kämmenien ja jalkapohjien ihon paksuuntumisen vähenemiseen. Tutkimuksessa pystyttiin todistamaan, että asitretiini vaikuttaa tehokkaasti moniin keratinisaatiohäiriöihin, joiden hoitoon ainoastaan systeemiset retinoidit ovat tätä nykyä tuoneet merkitsevää parannusta punajäkälää sairastavaa potilasta osallistui kahdeksan viikkoa kestävään tutkimukseen. Niiden potilaiden tila, joita hoidettiin 30 mg:n asitretiinivuorokausiannoksella (64 %), kohentui merkitsevästi verrattuna potilaisiin, jotka eivät saaneet mitään hoitoa (13 %). Lisäksi seuraavien kahdeksan viikon aikana 83 %:lla aiemmin hoitamattomista potilaista saavutettiin hoitovaste asitretiinihoitoon. Tämä tutkimus osoitti, että asitretiini on tehokas ja hyväksyttävä hoitomuoto vaikea-asteisen punajäkälän hoitoon. 44 VI.2.3 Hoidon hyötyihin liittyvät asiat, joita ei tunneta Tällä hetkellä olemassa olevien tietojen pohjalta ei tunnistettu aukkoja kohderyhmän tietämyksessä tehokkuuteen liittyen, mikä antaisi syyn luvan myöntämisen jälkeisiin tehokkuustutkimuksiin. Tämän lisäksi ei myöskään ole näyttöä, joka viittaisi erilaisiin
3 hoitotuloksiin kohdeväestön alaryhmissä, kun huomioidaan eri tekijät, kuten ikä, sukupuoli, rotu tai elinvamma. VI.2.4 Yhteenveto turvallisuustiedoista Tärkeät tunnistetut riskit Riski Mitä tiedetään Ehkäistävyys Lisääntynyt Asitretiini aiheuttaa Raskaudenehkäisy ja raskaustestien epämuodostumien riski, joka syntymättömälle lapselle tekeminen ovat välttämättömiä hoidon liittyy alkoholin epämuodostumia (kallon ja aikana ja kolme vuotta asitretiinihoidon käyttörajoituksen kasvojen luiden vaurioita, lopettamisen jälkeen. noudattamatta jättämiseen ja sydämen, verisuoniston ja Hedelmällisessä iässä oleville naisille etretinaattiyhdisteen aivojen epämuodostumia, ei saa antaa verta potilaalta, jota muodostumiseen, joka voi luustovaurioita). Jos hoidetaan tai on hoidettu asitretiinilla olla haitallista raskaana olevalle naiselle kuluneen kolmen vuoden aikana. syntymättömälle lapselle annetaan verta asitretiinilla Hedelmällisessä iässä olevat naiset (Teratogeenisuus, hoidetulta potilaalta, eivät saa käyttää alkoholia (juomissa, lisääntynyt riski, joka liittyy syntymättömään lapseen ruuissa tai lääkkeissä) asitretiinihoidon alkoholin käyttörajoituksen kohdistuu myös tällöin suuri aikana tai kahteen kuukauteen hoidon noudattamatta jättämiseen epämuodostumien riski. lopettamisen jälkeen. (muuntuminen etretinaatiksi)) Asitretiinin ja alkoholin Hedelmällisessä iässä olevien naisten samanaikainen käyttö voi on käytettävä tehokasta johtaa syntymättömälle ehkäisymenetelmää keskeytyksettä lapselle mahdollisesti ainakin neljä viikkoa ennen haitallisen yhdisteen asitretiinihoidon aloittamista, hoidon (etretinaatin) aikana ja kolmen vuoden ajan hoidon muodostumiseen. Jos sitä lopettamisen jälkeen. Ensisijaisena muodostuu, sen poistuminen ehkäisymenetelmänä on käytettävä elimistöstä kokonaisuudessaan hormonaalisia kestää yhdistelmäehkäisyvalmisteita tai suhteellisen pitkään. kierukkaa, ja lisäksi suositellaan kondomin tai pessaarin käyttöä. Ns. minipillereitä ei suositella. Enintään kolme päivää ennen hoidon aloittamista on tehtävä raskaustesti, jonka on oltava negatiivinen. Asitretiini aloitetaan negatiivisen raskaustestin jälkeen, seuraavan kuukautiskierron toisena tai kolmantena päivänä. Asitretiinihoidon aikana on tehtävä raskaustestejä säännöllisesti 28 päivän välein. Lääkärin on tarkastettava raskaustestin tulos ja todettava se negatiiviseksi aina ennen lääkemääräyksen uusimista. Testi ei saa olla kolmea päivää vanhempi. Kun asitretiinihoito lopetetaan, raskaustestit on tehtävä 1 3 kuukauden välein kolmen vuoden ajan viimeisestä asitretiiniannoksesta.
4 Imetys: lapseen kohdistuva Asitretiinin poistumista Imettäminen on vasta-aiheista toksisuus ihmisen rintamaidosta asitretiinihoidon aikana. tutkittiin, ja tutkimuksessa todettiin, että 1,5 % äidin saamasta annoksesta kulkeutuu rintamaitoon. Lisääntynyt kallonsisäinen Asitretiini voi aiheuttaa Lääkärin on puututtava tähän paine: lääkkeen kallonsisäisen paineen viittaaviin oireisiin mahdollisimman yhteisvaikutus tetrasykliinien nousua. Oireita voivat olla: nopeasti. kanssa johtaa kallonsisäisen vaikea-asteinen päänsärky, Asitretiinin ja muiden mahdollisesti paineen nousuun pahoinvointi, oksentelu ja kallonsisäistä painetta nostavien (Hyvänlaatuinen näköhäiriöt. lääkkeiden (tetrasykliinien) kallonsisäisen paineen samanaikainen käyttö on vastaaiheista. nousu; lääkkeen yhteisvaikutus tetrasykliinien kanssa johtaa lisääntyneeseen riskiin) Maksaongelmat: lääkkeen Asitretiini voi aiheuttaa ihon Maksan toiminta on varmistettava yhteisvaikutus ja silmänvalkuaisten verikokein ennen hoidon aloittamista metotreksaatin kanssa johtaa keltaisuutta, joka voi olla ja säännöllisesti hoidon aikana. maksatulehdusriskin merkki keltataudista (hyvin Erityinen riski on potilailla, joilla on kasvamiseen harvinainen, voi esiintyä vaikea-asteinen maksan vajaatoiminta (Maksan toimintahäiriö; enintään yhdellä käyttäjällä (vasta-aiheista). lääkkeen yhteisvaikutus :sta) tai Metotreksaatin ja asitretiinin metotreksaatin kanssa johtaa maksatulehduksesta (melko yhdistelmäkäyttö on myös vastaaiheista lisääntyneen hepatiittiriskin kasvamiseen) harvinainen, voi esiintyä enintään yhdellä käyttäjällä maksatulehdusriskin vuoksi. sadasta). Muita oireita voivat olla ruokahaluttomuus, kuume, yleinen huonovointisuus, pahoinvointi, tummavirtsaisuus ja epämukavuuden tunne vatsan alueella. Veren rasva-arvot (Hyperkolesterolemia ja hypertriglyseridemia) Kun potilaita on hoidettu Veren rasva-arvot on mitattava ennen korkeilla asitretiiniannoksilla, hoidon aloittamista ja säännöllisesti on havaittu palautuvaa veren hoidon aikana. rasva-arvojen kohoamista Asitretiini on vasta-aiheista potilailla, erityisesti korkean riskin joilla on kroonisesti raja-arvojen yli potilailla ja pitkäkestoisessa kohonneet veren rasva-arvot. hoidossa. Epänormaali uuden Asitretiini voi aiheuttaa Lääkäri voi seurata luustoa luukudoksen muodostuminen muutoksia luiden kasvuun, säännöllisesti, sillä asitretiini voi luiden pintaan (eksostoosi) ts. muodostaa uutta luuta aiheuttaa luustomuutoksia erityisesti aikuisilla, erityisesti iäkkäillä luiden pinnalle. lapsilla ja iäkkäillä potilailla, jotka potilailla, pitkäkestoisen saavat pitkäkestoista hoitoa. hoidon jälkeen (luutumiseen liittyvät häiriöt aikuisilla, etenkin iäkkäillä potilailla, pitkäkestoisen hoidon jälkeen) Etretinaatista lapsille aiheutuneet luumuutokset
5 Glukoositoleranssin Diabeetikoilla retinoidit voivat Siksi verensokeripitoisuus on muutokset (muutokset parantaa tai heikentää mitattava tavallista useammin hoidon glukoosin metaboliassa) glukoositoleranssia. alkuvaiheessa. Tärkeät mahdolliset riskit Riski Mitä tiedetään Mielialamuutokset (mukaan Korkeilla annoksilla toteutettu asitretiinihoito voi aiheuttaa lukien ärtyneisyys, mielialamuutoksia (mukaan lukien ärtyneisyyttä, aggressiivisuus ja aggressiivisuutta ja masennusta). masennus)
6 Puuttuvat tiedot Riski Mitä tiedetään Riskit suhteessa krooniseen Pitkäaikaisessa käytössä asitretiini voi aiheuttaa muutoksia käyttöön luiden kasvuun, ts. muodostaa uutta luuta luiden pinnalle. Palautuvaa veren rasva-arvojen kohoamista on havaittu erityisesti korkean riskin potilailla ja pitkäkestoisessa hoidossa. Tällä hetkellä kaikkia asitretiinin kroonisen käytön seurauksia ei tiedetä. VI.2.5 Yhteenveto toimenpiteistä riskien minimoimiseksi Kaikista lääkevalmisteista laaditaan valmisteyhteenveto, joka sisältää lääkäreille, apteekkihenkilökunnalle ja muille terveydenhuollon ammattilaisille suunnattua yksityiskohtaista tietoa lääkkeen käytöstä, riskeistä ja suosituksista riskien minimoimiseksi. Pakkausselosteessa kerrotaan valmisteyhteenvedon tiedot lyhyesti maallikkokielellä. Valmisteyhteenvedossa ja pakkausselosteessa mainitut toimet ovat tavanomaisia riskienminimointitoimia. Lääkkeen valmisteyhteenveto ja pakkausseloste ovat saatavissa Fimean verkkosivujen kautta Tämän lääkkeen turvalliseen ja tehokkaaseen käyttöön liittyy erityisehtoja ja rajoituksia (riskien minimoinnin lisätoimia). Kattavat tiedot näistä ehdoista ja mahdollisen koulutusmateriaalin keskeisistä osista on julkaistu Euroopan lääkeviraston lääkevalmisteasiakirjoissa, joihin on löydettävissä linkki Fimean verkkosivujen kautta. Näiden lisätoimien toteuttamisesta kussakin maassa sovitaan kuitenkin yhdessä lääkkeen valmistajan ja kansallisen viranomaisen kanssa. Tällaisia lisätoimia seuraavien riskien minimoimiseksi ovat: Epämuodostumien riski ja etretinaattiyhdisteen muodostumisen riski, joka voi olla haitallista syntymättömälle lapselle Terveydenhuollon ammattilaisille tarkoitetun suoran tiedotteen jakelu (Distribution of Direct Healthcare Professional Communication, DHPC) Tavoite ja perustelut Tavoitteena on korostaa keskeisiä seikkoja ja tiedottaa niistä suoraan valmistetta määrääville lääkäreille. Yhteenveto pääasiallisista riskien minimoinnin lisätoimista DHPC:ssä korostetaan samanaikaiseen alkoholin kulutukseen, verenluovutukseen ja teratogeenisuuteen liittyviä riskejä. Terveydenhuollon ammattilaisten ja potilaiden koulutus Tavoite ja perustelut Tavoitteena on varmistaa asitretiinin turvallinen käyttö suhteessa raskauteen ja syntymättömän lapsen altistumiseen. Siinä kerrotaan, kuinka hedelmällisessä iässä olevat naiset voivat välttyä raskaudelta ja kuinka muut potilasryhmät voivat pienentää sikiöaltistuksen riskiä. Riskien minimoinnin lisätoimet ovat tarpeen, jotta lääkäreille ja potilaille voidaan kertoa entistä paremmin tästä tärkeästä riskistä, johon liittyy syntymättömään lapseen kohdistuvia vakavia seurauksia.
7 Terveydenhuollon ammattilaisille tarkoitetun suoran tiedotteen jakelu (Distribution of Direct Healthcare Professional Communication, DHPC) Tavoite ja perustelut Tavoitteena on korostaa keskeisiä seikkoja ja tiedottaa niistä suoraan valmistetta määrääville lääkäreille. Yhteenveto pääasiallisista riskien minimoinnin lisätoimista DHPC:ssä korostetaan samanaikaiseen alkoholin kulutukseen, verenluovutukseen ja teratogeenisuuteen liittyviä riskejä. Terveydenhuollon ammattilaisten ja potilaiden koulutus Yhteenveto pääasiallisista riskien minimoinnin lisätoimista Koulutusmateriaalin jakelu, jotta pystytään korostamaan ehkäisyn tarpeellisuutta asitretiinihoidon aikana, kuukausittaisten raskaustestien tarpeellisuutta ennen lääkemääräyksen uusimista ja hedelmällisessä iässä olevien naisten tarvetta allekirjoittaa suostumuslomake. Raskaudenehkäisyohjelma koostuu seuraavista: - Lääkärin opas asitretiinin määräämiseen - Lääkärin tarkastuslista määrättäessä lääkettä naispotilaille - Apteekkihenkilökunnan opas asitretiinin luovutukseen - Potilaan opas asitretiinin käyttöön - Vahvistuslomake naispotilaille - Vahvistuslomake miespotilaille VI.2.6 Kehityssuunnitelma myyntiluvan myöntämisen jälkeen Tutkimus (tutkimuksen numero) Monikansallinen, havaintoihin perustuva poikkileikkaustutkimus Tavoitteet Käsiteltävät turvallisuuteen tai tehoon liittyvät seikat Tutkimuksen tavoitteena Teratogeenisuus, on lisääntynyt riski, arvioida raskauden joka liittyy ja sikiöaltistuksen alkoholin ehkäisyohjelman käyttörajoituksen vaikutusta potilaan noudattamatta tietotasoon ja jättämiseen mahdolliseen toimintaan (muuntuminen etretinaatiksi) suhteessa tarpeeseen välttää raskaaksi tulemista asitretiinihoidon aikana ja kolmen vuoden ajan hoidon lopettamisen jälkeen. Tila Suunniteltu (yhteenveto liitteenä) Väli- ja loppuraporttien aikataulu Ei vahvistettu Myyntiluvan ehdoissa mainitut tutkimukset Mikään yllä olevista tutkimuksista ei ole myyntiluvan ehtona.
8 VI.2.7 Yhteenveto riskienhallintasuunnitelman päivityksistä Merkittävät riskienhallintasuunnitelman päivitykset Version Päivämäärä Turvallisuustiedot Kommentti numero Tunnistetut riskit Teratogeenisuus Ensimmäinen versio valmisteltu ja ainoastaan Ranskaan muuntuminen etretinaatiksi Imetys Hyvänlaatuinen kallonsisäisen paineen nousu Lääkkeen yhteisvaikutus tetrasykliinien kanssa, joka johtaa kallonsisäisen paineen nousuun Maksan toimintahäiriö Lääkkeen yhteisvaikutus metotreksaatin kanssa, joka johtaa hepatiittiriskin kasvamiseen Seerumin kolesteroli- ja triglyseridipitoisuuden nousu Luutumiseen liittyvät häiriöt aikuisilla, etenkin iäkkäillä potilailla, pitkäkestoisen hoidon jälkeen Etretinaatista lapsille aiheutuneet luumuutokset Mahdolliset riskit Psyykkiset häiriöt (mielialamuutokset, mukaan lukien ärtyneisyys, aggressiivisuus ja masennus), joiden tiedetään liittyvän korkeisiin retinoidiannoksiin Puuttuvat tiedot Riskit suhteessa krooniseen käyttöön Samat tärkeät riskit Riskienhallintasuunnitelma kattaa kaikki Actaviksen tuotteet, eikliinisten ja kliinisten tutkimusten tiedot lisättiin.
9 Yksi riski lisättiin: Riskienhallintasuunnitelman Tärkeät tunnistetut riskit: muutokset alustavan Glukoosimetabolian arviointiraportin mukaan. muutokset Tutkimusta ehdotettiin keinoksi arvioida raskaudenehkäisyohjelman tehoa. Raskaudenehkäisyohjelman muutokset tehtiin ihmislääkekomitean suosituksen mukaisesti, jossa suositetaan käyttämään raskauden ehkäisyä kolmen vuoden ajan asitretiinihoidon lopettamisen jälkeen kahden vuoden sijaan.
Proscar. 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0
 PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi)
 Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Propecia (finasteridi 0,2 ja 1 mg) tabletti , versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 22 helmikuuta 2016 Drospirenoni/etinyyliestradioli Versionumero: 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Suun kautta
22 helmikuuta 2016 Drospirenoni/etinyyliestradioli Versionumero: 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Suun kautta
Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto
 EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Ibandronat Stada 150 mg kalvopäällysteiset tabletit. 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Olmesartan medoxomil STADA. 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
19.2.2014, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto
 EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Pregabalin Krka 17.2.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Täydellisyyden vuoksi, viitaten Direktiivin 2001/83 artiklaan 11, hakija varaa mahdollisuuden
Pregabalin Krka 17.2.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Täydellisyyden vuoksi, viitaten Direktiivin 2001/83 artiklaan 11, hakija varaa mahdollisuuden
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
CYPRETYL RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 CYPRETYL Päivämäärä: 29.6.2015, Versio: 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Akne on yleinen ihovaiva, jonka tunnusmerkkejä
CYPRETYL Päivämäärä: 29.6.2015, Versio: 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Akne on yleinen ihovaiva, jonka tunnusmerkkejä
Nucala. 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/671186/2015 Nucala 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Nucalan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/671186/2015 Nucala 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Nucalan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 JAYDESS 13,5 mg, kohdunsisäinen ehkäisin 5/2014 versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2. VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Jaydess-hormonkierukkaa
JAYDESS 13,5 mg, kohdunsisäinen ehkäisin 5/2014 versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2. VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Jaydess-hormonkierukkaa
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
Remeron. 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Remeron 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Masennus on sairaus, jossa surullisuuden tunne ja
Remeron 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Masennus on sairaus, jossa surullisuuden tunne ja
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
POTILAAN OPAS MAVENCLAD. Potilaan opas. Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä
 MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/188850/2014 Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Jardiance-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla
EMA/188850/2014 Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Jardiance-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Erivedge 150 mg kovat kapselit RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Lokakuu 2013, v. 8.0 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ihon tyvisolusyöpä on yleisin
Erivedge 150 mg kovat kapselit RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Lokakuu 2013, v. 8.0 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ihon tyvisolusyöpä on yleisin
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 11 maaliskuuta 2016 Desloratadiini Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Heinänuha Pohjoismaiset tutkimukset
11 maaliskuuta 2016 Desloratadiini Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Heinänuha Pohjoismaiset tutkimukset
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski
 mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Akne Aikuisiän aknea esiintyy 25 prosentilla aikuisista miehistä ja 50 prosentilla
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Akne Aikuisiän aknea esiintyy 25 prosentilla aikuisista miehistä ja 50 prosentilla
RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT
 RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT ORION CORPORATION PÄIVÄMÄÄRÄ: 15-6-2015, VERSIO 2 VI.2 Julkisen yhteenvedon osiot VI.2.1
RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT ORION CORPORATION PÄIVÄMÄÄRÄ: 15-6-2015, VERSIO 2 VI.2 Julkisen yhteenvedon osiot VI.2.1
Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa. Tietoa terveydenhuollon ammattilaisille
 Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa Tietoa terveydenhuollon ammattilaisille Suositukset seuraavissa tilanteissa: - maksan toiminnan seuraaminen - yhteisvaikutukset
Valdoxan (agomelatiini) aikuispotilaiden vakavien masennustilojen hoidossa Tietoa terveydenhuollon ammattilaisille Suositukset seuraavissa tilanteissa: - maksan toiminnan seuraaminen - yhteisvaikutukset
NuvaRing. N.V. Organon. 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 NuvaRing N.V. Organon 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Etonogestreelia ja etinyyliestradiolia
NuvaRing N.V. Organon 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Etonogestreelia ja etinyyliestradiolia
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Pramipexol Stada. 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Pramipexol Stada 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Pramipexol STADA 0,088 mg tabletti Pramipexol STADA 0,18 mg tabletti Pramipexol STADA
Pramipexol Stada 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Pramipexol STADA 0,088 mg tabletti Pramipexol STADA 0,18 mg tabletti Pramipexol STADA
Apteekkihenkilökunnan
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio)
 28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
Hoidon hyötyihin liittyvät asiat, joita ei tunneta (yksi lyhyt kappale kustakin käyttöaiheesta, enintään 50 sanaa)
 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Numeta G16E, Numeta G19E 2332015, Versio 30 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2 Julkisen yhteenvedon osiot VI21 Tietoa sairauden esiintyvyydestä Joillakin sairaalapotilailla ei välttämättä
Numeta G16E, Numeta G19E 2332015, Versio 30 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2 Julkisen yhteenvedon osiot VI21 Tietoa sairauden esiintyvyydestä Joillakin sairaalapotilailla ei välttämättä
Riskienhallintasuunnitelman julkinen yhteenveto Repatha (evolokumabi)
 EMA/577184/2015 Riskienhallintasuunnitelman julkinen yhteenveto Repatha (evolokumabi) Tämä on Repatha-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden avulla
EMA/577184/2015 Riskienhallintasuunnitelman julkinen yhteenveto Repatha (evolokumabi) Tämä on Repatha-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden avulla
Riskienhallintasuunnitelman julkinen yhteenveto Kyprolis (karfiltsomibi)
 EMA/639793/2015 Riskienhallintasuunnitelman julkinen yhteenveto Kyprolis (karfiltsomibi) Tämä on Kyprolis-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/639793/2015 Riskienhallintasuunnitelman julkinen yhteenveto Kyprolis (karfiltsomibi) Tämä on Kyprolis-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Elidel 10 mg/g emulsiovoide 8.12.2015, Versio 11 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ekseemaa esiintyy lähinnä lapsilla
Elidel 10 mg/g emulsiovoide 8.12.2015, Versio 11 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ekseemaa esiintyy lähinnä lapsilla
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Lääkärin opas. Raskauden ja sikiöaltistuksen ehkäisyohjelma
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO. Lynparza-valmisteen (olaparibi) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/681881/2014 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Lynparza-valmisteen (olaparibi) riskienhallintasuunnitelman (RMP) yhteenveto VI.2 Julkisen yhteenvedon osiot Tämä on Lynparza-valmisteen
EMA/681881/2014 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Lynparza-valmisteen (olaparibi) riskienhallintasuunnitelman (RMP) yhteenveto VI.2 Julkisen yhteenvedon osiot Tämä on Lynparza-valmisteen
Bimatoprosti. 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Bimatoprosti 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Kohonneen silmänpaineen alentaminen kroonista avokulmaglaukoomaa
Bimatoprosti 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Kohonneen silmänpaineen alentaminen kroonista avokulmaglaukoomaa
Lipanthyl Penta 145 mg , versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Lipanthyl Penta 145 mg 15.9.2015, versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Fenofibraatti: Julkisen yhteenvedon osiot Fenofibraatti: Tietoa sairauden esiintyvyydestä Arviolta
Lipanthyl Penta 145 mg 15.9.2015, versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Fenofibraatti: Julkisen yhteenvedon osiot Fenofibraatti: Tietoa sairauden esiintyvyydestä Arviolta
Isotretinoin Actavis
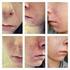 Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Erityisturvallisuustiedote
 Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Julkisen yhteenvedon osiot
 Olmestad Comp 20 mg/12,5 mg kalvopäällysteinen tabletti Olmestad Comp 20 mg/25 mg kalvopäällysteinen tabletti 17.12.2015, versio V1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon
Olmestad Comp 20 mg/12,5 mg kalvopäällysteinen tabletti Olmestad Comp 20 mg/25 mg kalvopäällysteinen tabletti 17.12.2015, versio V1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon
Enstilar , Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Enstilar 21.1.2016, Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Psoriaasi on yleinen ihosairaus, jossa iholle ilmestyy
Enstilar 21.1.2016, Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Psoriaasi on yleinen ihosairaus, jossa iholle ilmestyy
Nexplanon. 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Nexplanon 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Implanon ja Implanon NXT/Nexplanon ovat pitkävaikutteisia
Nexplanon 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Implanon ja Implanon NXT/Nexplanon ovat pitkävaikutteisia
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos. 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin Actavis
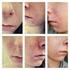 Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Abstral, EU:n riskienhallintasuunnitelma, versio 4.0
 Vaikuttavat aineet (kansainvälinen INN-nimi tai Fentanyyli (fentanyylisitraattina) yleinen nimi): Farmakoterapeuttinen ryhmä (ATC-koodi): Opioidianalgeetit, fenyylipiperidiinijohdannaiset, N02ABO3 Myyntiluvan
Vaikuttavat aineet (kansainvälinen INN-nimi tai Fentanyyli (fentanyylisitraattina) yleinen nimi): Farmakoterapeuttinen ryhmä (ATC-koodi): Opioidianalgeetit, fenyylipiperidiinijohdannaiset, N02ABO3 Myyntiluvan
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Mydrane 0,2 mg/ml + 3,1 mg/ml + 10 mg/ml injektioneste, liuos 3.7.2015, Versio 2.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Mydrane 0,2 mg/ml + 3,1 mg/ml + 10 mg/ml injektioneste, liuos 3.7.2015, Versio 2.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Julkisen yhteenvedon osiot
 EU RMP alitretinoiini v8 toukokuu 2014 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Puhelin- tai sähköpostikyselyissä 6 14 % pohjois- ja keskieurooppalaisista aikuisista vastasi,
EU RMP alitretinoiini v8 toukokuu 2014 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Puhelin- tai sähköpostikyselyissä 6 14 % pohjois- ja keskieurooppalaisista aikuisista vastasi,
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Osa A. Täytetään kaikkien naispotilaiden kohdalla
 Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Praluent. 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Praluent 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Praluent-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Praluent 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Praluent-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Apteekkihenkilökunnan opas
 Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Riskienhallintasuunnitelman julkinen yhteenveto Blincyto (blinatumomabi)
 EMA/642231/2015 Riskienhallintasuunnitelman julkinen yhteenveto Blincyto (blinatumomabi) Tämä on Blincyto-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/642231/2015 Riskienhallintasuunnitelman julkinen yhteenveto Blincyto (blinatumomabi) Tämä on Blincyto-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 11.5.2016 Fludarabin Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Vaikka kroonisen lymfaattisen leukemian (KLL) esiintyvyys
11.5.2016 Fludarabin Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Vaikka kroonisen lymfaattisen leukemian (KLL) esiintyvyys
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Lescol / Lescol Depot. 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Lescol / Lescol Depot 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Korkea kolesteroli tarkoittaa kolesterolin
Lescol / Lescol Depot 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Korkea kolesteroli tarkoittaa kolesterolin
, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
Toctino (alitretinoiini)
 Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Perusseikkoja julkista yhteenvetoa varten
 Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
INFLECTRA SEULONTAKORTTI
 Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit , Versio 1.3
 Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Ihopsoriaasin hoitaminen. Anna Jussila, LL, erikoistuvan vaiheen lääkäri SATSHP, Ihotautien poliklinikka
 Ihopsoriaasin hoitaminen Anna Jussila, LL, erikoistuvan vaiheen lääkäri SATSHP, Ihotautien poliklinikka Hoidon tavoitteet 1. Oireiden minimointi 2. Elämänlaadun parantaminen 3. Työ- ja toimintakyvyn säilyttäminen
Ihopsoriaasin hoitaminen Anna Jussila, LL, erikoistuvan vaiheen lääkäri SATSHP, Ihotautien poliklinikka Hoidon tavoitteet 1. Oireiden minimointi 2. Elämänlaadun parantaminen 3. Työ- ja toimintakyvyn säilyttäminen
Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
(alitretinoiini) Potilaskortti RASKAUDENEHKÄISYOHJELMA. Potilaan nimi. alitretinoiini
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210mm Pages: 8 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 RASKAUDENEHKÄISYOHJELMA
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210mm Pages: 8 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 RASKAUDENEHKÄISYOHJELMA
Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi
 Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
Tarkastuslista määrättäessä asitretiinia naispotilaille
 Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
PAKKAUSSELOSTE. VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa
 PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
Menjugate. 22.06.2016, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Menjugate 22.06.2016, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä N. meningitidis -bakteeri voi aiheuttaa infektion
Menjugate 22.06.2016, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä N. meningitidis -bakteeri voi aiheuttaa infektion
Primovist (dinatriumgadoksetaatti) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Primovist (dinatriumgadoksetaatti) 05/2013, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 2. Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Magneettikuvaus (MK) on yksi useasta
Primovist (dinatriumgadoksetaatti) 05/2013, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 2. Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Magneettikuvaus (MK) on yksi useasta
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/natrii chloridum B. Braun 1,5 mg/ml
Kalii chloridum/glucosum B. Braun 1,5 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/glucosum B. Braun 3 mg/ml + 50 mg/ml infuusioneste, liuos Kalii chloridum/natrii chloridum B. Braun 1,5 mg/ml
LIITE. Tieteelliset osat
 LIITE Tieteelliset osat 3 LIITE Tieteelliset osat A) JOHDANTO Sparfloksasiini on kinoloneihin kuuluva antibiootti, joka on indikoitu seuraavien tilojen hoitoon: - avohoitopneumonia annostuksella 400/200
LIITE Tieteelliset osat 3 LIITE Tieteelliset osat A) JOHDANTO Sparfloksasiini on kinoloneihin kuuluva antibiootti, joka on indikoitu seuraavien tilojen hoitoon: - avohoitopneumonia annostuksella 400/200
- aktiivisen nivelreuman hoitoon aikuisille silloin, kun hoito sairauden kulkuun vaikuttavilla lääkkeillä (DMARD) on aiheellinen
 RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO TREXAN 25 MG/ML, INJEKTIONESTE, LIUOS, ESITÄYTETTY RUISKU ORION CORPORATION PÄIVÄMÄÄRÄ: 12-01-2015, VERSIO 1.2 VI.2 Julkisen yhteenvedon osiot Metotreksaatti
RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO TREXAN 25 MG/ML, INJEKTIONESTE, LIUOS, ESITÄYTETTY RUISKU ORION CORPORATION PÄIVÄMÄÄRÄ: 12-01-2015, VERSIO 1.2 VI.2 Julkisen yhteenvedon osiot Metotreksaatti
Julkisen yhteenvedon osiot
 Leflunomide STADA Versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Leflunomide STADA 10 mg tabletti, kalvopäällysteinen Leflunomide STADA 20 mg tabletti, kalvopäällysteinen
Leflunomide STADA Versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Leflunomide STADA 10 mg tabletti, kalvopäällysteinen Leflunomide STADA 20 mg tabletti, kalvopäällysteinen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 17 helmikuuta 2016 isotretinoiini Versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Aknetyyppejä on useita, ja eräät vaikea-asteiset
17 helmikuuta 2016 isotretinoiini Versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Aknetyyppejä on useita, ja eräät vaikea-asteiset
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Paracetamol B. Braun 10 mg/ml infuusioneste, liuos 22.10.2014, versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Parasetamolia
Paracetamol B. Braun 10 mg/ml infuusioneste, liuos 22.10.2014, versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Parasetamolia
Pakkausseloste: Tietoa potilaalle
 Pakkausseloste: Tietoa potilaalle Otezla tabletti, kalvopäällysteinen Otezla 20 mg tabletti, kalvopäällysteinen Otezla 30 mg tabletti, kalvopäällysteinen apremilasti Tähän lääkkeeseen kohdistuu lisäseuranta.
Pakkausseloste: Tietoa potilaalle Otezla tabletti, kalvopäällysteinen Otezla 20 mg tabletti, kalvopäällysteinen Otezla 30 mg tabletti, kalvopäällysteinen apremilasti Tähän lääkkeeseen kohdistuu lisäseuranta.
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
LIITE EMEAN TIETEELLISET JOHTOPÄÄTÖKSET JA HYLKÄYSPERUSTEET
 LIITE EMEAN TIETEELLISET JOHTOPÄÄTÖKSET JA HYLKÄYSPERUSTEET LÄÄKEVALMISTEKOMITEAN () 19. HEINÄKUUTA 2007 ANTAMAN VALMISTETTA NIMELTÄ NATALIZUMAB ELAN PHARMA KOSKEVAN LAUSUNNON UUDELLEENARVIOINTI Heinäkuussa
LIITE EMEAN TIETEELLISET JOHTOPÄÄTÖKSET JA HYLKÄYSPERUSTEET LÄÄKEVALMISTEKOMITEAN () 19. HEINÄKUUTA 2007 ANTAMAN VALMISTETTA NIMELTÄ NATALIZUMAB ELAN PHARMA KOSKEVAN LAUSUNNON UUDELLEENARVIOINTI Heinäkuussa
RMP section VI.2 Elements for Public Summary
 RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
Harvoni RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/702765/2014 Harvoni RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Harvoni-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/702765/2014 Harvoni RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Harvoni-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Suositukset maksan haittavaikutusten välttämiseksi. Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan.
 Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
