(alitretinoiini) Potilaskortti RASKAUDENEHKÄISYOHJELMA. Potilaan nimi. alitretinoiini
|
|
|
- Tyyne Laine
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Cutterguide: No Printing Process: Offset GD: RR Size: 148 x 210mm Pages: 8 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 RASKAUDENEHKÄISYOHJELMA (alitretinoiini) Potilaskortti Potilaan nimi alitretinoiini Toctino_LP_148x210_GSKEDC-FB _D2.indd 1 12/4/2014 6:37:22 PM
2 Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien vaara on erittäin suuri, jos Toctinovalmistetta käytetään raskauden aikana, vaikka vain lyhytaikaisestikin. Siksi Toctino-hoitoa ei saa antaa raskaana oleville naisille eikä naisille, jotka voivat tulla raskaaksi. Lääkkeen määräävänä lääkärinä teidän on varmistettava, että seuraavat ehdot täyttyvät ennen kuin Toctino-hoito aloitetaan (tai hoitoa jatketaan). Raskaustestien kirjaaminen Raskaustestit on tehtävä lääketieteellisesti valvotuissa olosuhteissa, ja testin herkkyyden on oltava vähintään 25 miu/ml. Merkitkää raskaustestien päivämäärät ja tulokset seuraavaan taulukkoon. Nimikirjaimet 1. raskaustesti ennen hoitoa 2. raskaustesti ennen hoitoa Viimeinen raskaustesti hoidon jälkeen Edelliset kuukautiset (pvm) Raskaustestin ajankohta (pvm) Raskaustestin tulos Nimikirjaimet Muistilista Toctino-hoitoa määräävälle lääkärille Ennen lääkkeen määräämistä Varmista käyttöaihe: vaikea krooninen käsi-ihottuma, kun paikallisella voimakkaalla korikosteroidihoidolla ei saada aikaan hoitovastetta Tarkista vasta-aiheet, sillä Toctino-hoitoa ei saa määrätä seuraavissa tilanteissa: Raskaana oleville tai imettäville naisille Maksan vajaatoiminta Huonossa hoitotasapainossa oleva hyperkolesterolemia Huonossa hoitotasapainossa oleva hypertriglyseridemia Huonossa hoitotasapainossa oleva kilpirauhasen vajaatoiminta A-hypervitaminoosi Yliherkkyys alitretinoiinille, muille retinoideille tai apuaineille Samanaikainen tetrasykliinihoito Varmista, että potilaalle on kerrottu (suullisesti ja kirjallisesti) Toctinohoitoon liittyvästä sikiöepämuodostumien vaarasta ja että hän ymmärtää sen täysin. Kerro potilaalle, että hän ei saa luovuttaa verta Toctino-hoidon aikana eikä yhden kuukauden aikana hoidon päättymisen jälkeen eikä antaa kapseleita kenellekään muulle. Anna jokaiselle potilaalle Toctino-potilasesite. Anna kaikille naispotilaille, jotka voivat tulla raskaaksi, Toctino-esite Tietoa raskauden ehkäisystä. Toctino_LP_148x210_GSKEDC-FB _D2.indd 2-3
3 Varmista, että naispotilaat, jotka voivat tulla raskaaksi, ymmärtävät kuukausittaisten seurantakäyntien välttämättömyyden. Varmista, että naispotilas ymmärtää, miksi on välttämätöntä käyttää jatkuvasti raskaudenehkäisyohjelman mukaista tehokasta ehkäisyä yhden kuukauden ajan ennen hoidon alkamista, hoidon aikana ja yhden kuukauden ajan hoidon päättymisen jälkeen. Varmista, että myös ne naispotilaat, joilla ei ole kuukautisia tai jotka eivät ole seksuaalisesti aktiivisia, noudattavat Tietoa raskauden ehkäisystä - esitteen ohjeita. Poikkeus: potilaat, joille on tehty hysterektomia. Ensimmäinen raskaustesti: määrää tarpeen mukaan ensimmäinen raskaustesti, jonka herkkyys on vähintään 25 mlu/ml, kierron 3 ensimmäisen päivän aikana tai, jos kuukautiset ovat epäsäännölliset, 3 viikon kuluttua viimeisestä suojaamattomasta yhdynnästä. Jos ensimmäisen testin tulos on negatiivinen, potilaan on alettava käyttää hänelle valittua (mieluummin kahta samanaikaista) ehkäisymenetelmää. Toinen raskaustesti: kun tehokasta ehkäisyä on käytetty vähintään 4 viikon ajan, tehdään toinen lääketieteellisesti valvottu raskaustesti samana päivänä, jona lääke määrätään, tai tätä vastaanottokäyntiä edeltävien 3 päivän aikana. Varmista, että potilas ymmärtää mahdollisen raskauden seuraukset. Jos hän epäilee olevansa raskaana, hänen on lopetettava heti Toctinovalmisteen käyttö ja otettava yhteyttä lääkäriin. Varmista, että potilas ymmärtää raskaustestien välttämättömyyden ja hyväksyy sen, että raskaustestejä tehdään hoidon aikana tarvittaessa kuukausittain ja lisäksi 5 viikon kuluttua hoidon päättymisestä. Varmista, että potilaasi on saanut kaiken suullisen ja kirjallisen tiedon mahdollisista riskeistä ja varotoimista ja on vahvistanut tämän allekirjoittamalla kirjallisen vakuutuksen. Säilytä tämä kirjallinen vakuutus omassa kansiossasi. Toctino-hoito voidaan aloittaa vasta, kun potilas on käyttänyt ehkäisyä vähintään 4 viikon ajan ja kun lääketieteellisesti valvotusta raskaustestistä on saatu negatiivinen tulos. Hoidon aikana Jos kaikki edellä mainitut ehdot täyttyvät, potilaalle voidaan määrätä Toctino-hoitoa. Naisille, jotka voivat tulla raskaaksi, lääke on määrättävä 3 vuorokauden kuluessa viimeisimmästä negatiivisesta raskaustestistä, ja lääkemääräys on rajoitettava 30 vuorokauteen. Muut raskaustestit: lääketieteellisesti valvottuja raskaustestejä, joiden herkkyys on vähintään 25 miu/ml, tehdään hoidon aikana paikallisen käytännön mukaisesti ja kerran kuukaudessa samana päivänä, jona uusi lääkemääräys kirjoitetaan, tai sitä edeltävien 3 päivän aikana. Sikiöepämuodostumien vaaraa on korostettava, ja potilaan kaikkiin raskauden ehkäisyä koskeviin kysymyksiin on vastattava. Jos potilas kaikista varotoimenpiteistä huolimatta tulee raskaaksi hoidon aikana tai hoidon päättymistä seuraavan kuukauden aikana, hoito on lopetettava heti ja potilaan on otettava yhteyttä lääkäriin, jotta voidaan neuvotella jatkotoimenpiteistä. Ilmoita Toctino-hoidon yhteydessä ilmenevät raskaustapaukset asianomaisille terveysviranomaisille ja GSK -yhtiölle. Hoidon päättyessä Kehota potilasta jatkamaan raskaudenehkäisyä ja muistuta häntä, että hän ei saa luovuttaa verta kuukauden aikana hoidon päättymisen jälkeen. Jäljelle jääneitä kapseleita ei saa antaa kenellekään muulle, vaan ne on palautettava apteekkiin tai lääkkeet antaneelle lääkärille. Kehota potilasta tulemaan uudelleen vastaanotolle 5 viikon kuluttua hoidon päättymisestä viimeistä raskaustestiä varten. Toctino_LP_148x210_GSKEDC-FB _D2.indd 4-5
4 Hoitavien lääkäreiden vakuutus Potilas (sukunimi, etunimi), syntymäaika, tuli vastaanotolleni (pvm). Hänellä on (merkitse diagnoosi), jossa seuraavilla hoidoilla ei ole saatu aikaan hoitovastetta (ilmoita aikaisemmat hoidot). Siksi on harkittu Toctino-hoidon aloittamista. Potilaalle on annettu aikaisemmalla vastaanottokäynnillä Toctino-potilasesite ja Toctino-esite Tietoa raskauden ehkäisystä. Tämän päivän vastaanottokäynnillä olen selostanut potilaalle yksityiskohtaisesti kaikki Toctino-hoidon vaatimat varotoimenpiteet ja mahdolliseen raskauteen liittyvät riskit Toctino-hoidon yhteydessä. Potilaalla on ollut tilaisuus esittää kysymyksiä. Arvioni mukaan potilaan tiedot riskeistä ovat: kattavat riittämättömät Olen selittänyt, että raskauden ehkäisy on välttämätöntä sikiöepämuodostumien vaaran vuoksi, ja potilas on saanut lähetteen gynekologin vastaanotolle, jossa hänelle valitaan mielellään kaksi sopivaa ehkäisymenetelmää ja keskustellaan niiden käytöstä. Käsitykseni mukaan kyseinen potilas: on riittävän vastuuntuntoinen ei ole vastuuntuntoinen Potilaalle on kerrottu hoidosta ja kaikista siihen liittyvistä riskeistä ja hän on halukas aloittamaan Toctino-hoidon. Raskaustestit Ennen hoitoa Ensimmäinen raskaustesti on tehtävä tarpeen mukaan ennen ehkäisyn aloittamista (paitsi jos jatkuva ehkäisy on jo käytössä). Jos kuukautiset ovat epäsäännölliset, raskaustesti tehdään noin 3 viikon kuluttua viimeisestä suojaamattomasta yhdynnästä. Toinen raskaustesti on tehtävä hoidon aloittamista edeltävien 3 päivän aikana, kun kahta tehokasta ehkäisymenetelmää on käytetty 4 viikon ajan. Hoidon aikana Raskaustestit on tehtävä tarvittaessa kuukauden välein uuden lääkemääräyksen kirjoittamiseen liittyvillä vastaanottokäynneillä tai näitä käyntejä edeltävien 3 päivän aikana. Hoidon päättyessä Raskauden ehkäisyä on jatkettava vähintään 1 kuukauden ajan hoidon päättymisen jälkeen. Viimeinen raskaustesti tehdään 5 viikon kuluttua Toctino-hoidon päättymisestä. Tämän perusteella suostun antamaan kyseiselle potilaalle Toctino-hoitoa kieltäydyn antamasta kyseiselle potilaalle Toctino-hoitoa Allekirjoitus: Päiväys: Toctino_LP_148x210_GSKEDC-FB _D2.indd 6-7
5 Piispansilta 9 A, Espoo Puh , GSK-tuoteinfo /2014, FIN/DERM/0001/12(1) Toctino_LP_148x210_GSKEDC-FB _D2.indd 8
Toctino (alitretinoiini)
 Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Toctino (alitretinoiini)
 Raskauden ehkäisyohjelma TOC-FI-003-04032009-B OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet
Raskauden ehkäisyohjelma TOC-FI-003-04032009-B OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
Toctino (alitretinoiini)
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CC Windows Generated in: Acrobat Distiller XI OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CC Windows Generated in: Acrobat Distiller XI OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE
Toctino (alitretinoiini)
 OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet huolellisesti ennen kuin
OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet huolellisesti ennen kuin
Osa A. Täytetään kaikkien naispotilaiden kohdalla
 Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä asitretiinia naispotilaille
 Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Hoitopäiväkirja REVOLADE. (eltrombopagi) Tutustu huolella myös pakkausselosteeseen
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148x158 mm Pages: 52 Colors: C M Y K (4 Color) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 10.0 Hoitopäiväkirja REVOLADE
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148x158 mm Pages: 52 Colors: C M Y K (4 Color) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 10.0 Hoitopäiväkirja REVOLADE
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE. (alitretinoiini) Lääkärin materiaalit. Potilaan nimi.
 LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
Apteekkihenkilökunnan
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Isotretinoin Actavis
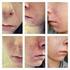 Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Lääkärin opas. Raskauden ja sikiöaltistuksen ehkäisyohjelma
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin Orifarm Tietoja lääkärille. Raskaudenehkäisyohjelma Hoito-ohjeet
 Isotretinoin Orifarm Tietoja lääkärille Raskaudenehkäisyohjelma Hoito-ohjeet Johdanto Isotretinoin Orifarm -valmisteen hyväksytty käyttöaihe on vaikea, asianmukaiseen systeemiseen antibioottihoitoon ja
Isotretinoin Orifarm Tietoja lääkärille Raskaudenehkäisyohjelma Hoito-ohjeet Johdanto Isotretinoin Orifarm -valmisteen hyväksytty käyttöaihe on vaikea, asianmukaiseen systeemiseen antibioottihoitoon ja
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Apteekkihenkilökunnan opas
 Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä
 mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
Isotretinoin Actavis
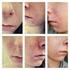 Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Erivedge -valmisteen raskaudenehkäisyohjelma
 Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Liite III. Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom. Nämä muutokset valmistetietojen asianmukaisiin kohtiin on laadittu referraalimenettelyssä. Direktiivin 2001/83/EY III otsikon 4. luvussa
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom. Nämä muutokset valmistetietojen asianmukaisiin kohtiin on laadittu referraalimenettelyssä. Direktiivin 2001/83/EY III otsikon 4. luvussa
Lääkärin opas. Acitretin Orifarm 10 mg ja 25 mg kovat kapselit. Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Lääkärin opas Acitretin Orifarm 10 mg ja 25 mg kovat kapselit Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Acitretin Orifarm sisältää vaikuttavana aineena asitretiinia, joka
Lääkärin opas Acitretin Orifarm 10 mg ja 25 mg kovat kapselit Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Acitretin Orifarm sisältää vaikuttavana aineena asitretiinia, joka
Erivedge -valmisteen raskaudenehkäisyohjelma. Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle
 Erivedge -valmisteen raskaudenehkäisyohjelma Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle 1 2 Sisällysluettelo: 1. Johdanto 1.1 Lääkärin rooli Erivedge -valmisteen raskaudenehkäisyohjelmassa
Erivedge -valmisteen raskaudenehkäisyohjelma Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle 1 2 Sisällysluettelo: 1. Johdanto 1.1 Lääkärin rooli Erivedge -valmisteen raskaudenehkäisyohjelmassa
Tietovihkonen potilaille, joille on määrätty Volibris-valmistetta
 Printing Process: Offset Cutterguide: No GD: RR 37861 Size: 148X210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietovihkonen potilaille,
Printing Process: Offset Cutterguide: No GD: RR 37861 Size: 148X210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietovihkonen potilaille,
Toctino (alitretinoiini)
 TIETOA RASKAUDEN EHKÄISYSTÄ Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-E Sisällys 1. Luuloja ja tieroa 3 2. Raskauden ehkäisy ja Toctino 4 3. Raskaustestit 6 4. Teille soveltuvat
TIETOA RASKAUDEN EHKÄISYSTÄ Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-E Sisällys 1. Luuloja ja tieroa 3 2. Raskauden ehkäisy ja Toctino 4 3. Raskaustestit 6 4. Teille soveltuvat
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski
 mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
EU Core koulutusmateriaali. Asitretiini, 10 mg ja 25 mg, kovat kapselit
 Versio Nro 4.0 Päiväys 04.05.2016 Korvaa version Nro 3.0 Päiväys 29.01.2016 Viite CCSI Versionro 8 10.12.2015 EU Core koulutusmateriaali Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini,
Versio Nro 4.0 Päiväys 04.05.2016 Korvaa version Nro 3.0 Päiväys 29.01.2016 Viite CCSI Versionro 8 10.12.2015 EU Core koulutusmateriaali Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini,
5 RASKAUDENILMOITUSLOMAKE
 5 RASKAUDENILMOITUSLOMAKE RO-GNE: RASKAUDEN ILMOITUSLOMAKE ILMOITTAJAN TIEDOT Ensimmäinen Seuranta Ilmoittajan nimi: Tyyppi: Lääkäri (erikoisala) Farmaseutti/proviisori Kuluttaja Muu (mikä) Yhteydenotto-osoite:
5 RASKAUDENILMOITUSLOMAKE RO-GNE: RASKAUDEN ILMOITUSLOMAKE ILMOITTAJAN TIEDOT Ensimmäinen Seuranta Ilmoittajan nimi: Tyyppi: Lääkäri (erikoisala) Farmaseutti/proviisori Kuluttaja Muu (mikä) Yhteydenotto-osoite:
Tärkeää tietoa GILENYA -hoidosta
 Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
POTILASOPAS. Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä
 POTILASOPAS Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä Tämä opas on tarkoitettu tytöille ja naisille, jotka käyttävät valproaattia
POTILASOPAS Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä Tämä opas on tarkoitettu tytöille ja naisille, jotka käyttävät valproaattia
Liite II. Tieteelliset päätelmät
 Liite II Tieteelliset päätelmät 74 Tieteelliset päätelmät Britannia käynnisti lääketurvatietojen perusteella direktiivin 2001/83/EY 31 artiklan mukaisen lausuntopyyntömenettelyn 7. heinäkuuta 2016. Se
Liite II Tieteelliset päätelmät 74 Tieteelliset päätelmät Britannia käynnisti lääketurvatietojen perusteella direktiivin 2001/83/EY 31 artiklan mukaisen lausuntopyyntömenettelyn 7. heinäkuuta 2016. Se
Tietoja terveydenhuollon ammattilaiselle
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 mm X 210 mm Pages: 12 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietoja terveydenhuollon
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 mm X 210 mm Pages: 12 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietoja terveydenhuollon
Liite III. Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huomaa: Näistä muutoksista valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on päätetty lausuntopyyntömenettelyssä. Jäsenmaiden
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huomaa: Näistä muutoksista valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on päätetty lausuntopyyntömenettelyssä. Jäsenmaiden
Potilasturvallisuuden edistämisen ohjausryhmä. Potilasturvallisuus on yhteinen asia! Potilasturvallisuus. Kysy hoidostasi vastaanotolla!
 Potilasturvallisuus on yhteinen asia! Potilasturvallisuus on osa hyvää hoitoa kattaa tutkimuksen, hoidon ja laitteiden turvallisuuden tarkoittaa myös sitä, ettei hoidosta aiheutuisi potilaalle haittaa
Potilasturvallisuus on yhteinen asia! Potilasturvallisuus on osa hyvää hoitoa kattaa tutkimuksen, hoidon ja laitteiden turvallisuuden tarkoittaa myös sitä, ettei hoidosta aiheutuisi potilaalle haittaa
LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA
 PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
SARAN JA TUOMAKSEN TARINA
 SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Kansalliset toimintamallit. Sähköinen lääkemääräys
 Kansalliset toimintamallit Sähköinen lääkemääräys 16.11.2015 Sähköinen resepti kotihoidossa ja palveluasumisessa Sähköisen lääkemääräyksen käytännöt kotihoidossa ja palveluasumisessa Kotihoidossa ja palveluasumisessa
Kansalliset toimintamallit Sähköinen lääkemääräys 16.11.2015 Sähköinen resepti kotihoidossa ja palveluasumisessa Sähköisen lääkemääräyksen käytännöt kotihoidossa ja palveluasumisessa Kotihoidossa ja palveluasumisessa
ASTMAN OMAHOITOKORTTI
 ASTMAN OMAHOITOKORTTI www.hengitys.fi www.astmatesti.fi www.pef.fi Erikieliset astmatestit löydät osoitteesta: www.asthmacontroltest.com GSK, Piispansilta 9 A 00 Espoo Puh. 00 0 0 0, www.gsk.fi GSK-tuoteinfo
ASTMAN OMAHOITOKORTTI www.hengitys.fi www.astmatesti.fi www.pef.fi Erikieliset astmatestit löydät osoitteesta: www.asthmacontroltest.com GSK, Piispansilta 9 A 00 Espoo Puh. 00 0 0 0, www.gsk.fi GSK-tuoteinfo
Sairaanhoitajan, terveydenhoitajan ja kätilön määrättävissä olevat lääkkeet
 3432 Liitteet Liite 1 Sairaanhoitajan, terveydenhoitajan ja kätilön määrättävissä olevat lääkkeet Lääkityksen aloittaminen ATC-luokka Lääke Tautitila Rajaus N01BB20 Lidokaiini-prilokaiini laastari ihon
3432 Liitteet Liite 1 Sairaanhoitajan, terveydenhoitajan ja kätilön määrättävissä olevat lääkkeet Lääkityksen aloittaminen ATC-luokka Lääke Tautitila Rajaus N01BB20 Lidokaiini-prilokaiini laastari ihon
POTILAAN OPAS MAVENCLAD. Potilaan opas. Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä
 MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Potilasohje. Sinulle on määrätty Donaxyl (dekvaliniumkloridi) -valmistetta bakteerivaginoosin hoitoon
 Potilasohje Sinulle on määrätty Donaxyl (dekvaliniumkloridi) -valmistetta bakteerivaginoosin hoitoon Bakteerivaginoosi Epämiellyttävän hajuisen valkovuodon yleisin aiheuttaja on bakteerivaginoosi. 1 Sinulle
Potilasohje Sinulle on määrätty Donaxyl (dekvaliniumkloridi) -valmistetta bakteerivaginoosin hoitoon Bakteerivaginoosi Epämiellyttävän hajuisen valkovuodon yleisin aiheuttaja on bakteerivaginoosi. 1 Sinulle
Varhainen Raskaustesti Tikku
 FI Varhainen Raskaustesti Tikku Käyttöopas Kotikäyttöön. Version 1.0 FI 17012017 Cat.No. W1-S 10mIU Babyplan varhainen raskaustestin voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
FI Varhainen Raskaustesti Tikku Käyttöopas Kotikäyttöön. Version 1.0 FI 17012017 Cat.No. W1-S 10mIU Babyplan varhainen raskaustestin voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
TÄRKEITÄ TURVALLISUUSTIETOJA RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE
 RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
REVOLADE-hoidon (eltrombopagi) hoitopäiväkirja POTILAALLE
 REVOLADE-hoidon (eltrombopagi) hoitopäiväkirja POTILAALLE Omat TIETONI Nimi: Osoite: Puhelin: Syntymäaika: REVOLADE (eltrombopagi) -annos: 2 Oma HOITOTIIMINI Lääkärin nimi: Hoitajan nimi: Osoite: Puhelin:
REVOLADE-hoidon (eltrombopagi) hoitopäiväkirja POTILAALLE Omat TIETONI Nimi: Osoite: Puhelin: Syntymäaika: REVOLADE (eltrombopagi) -annos: 2 Oma HOITOTIIMINI Lääkärin nimi: Hoitajan nimi: Osoite: Puhelin:
sivu 1 (6) Sähköinen lääkemääräys vaatimusmäärittely versio 2.7
 sivu 1 () Sähköinen lääkemääräys vaatimusmäärittely 19.9.2014 versio 2. LIITE 1: Lääkemääräyksiin ja toimitussanomaan liittyvät oikeudet 1 Lääkemääräyksiin liittyvät oikeudet tila Toimittamaton lääkemääräys
sivu 1 () Sähköinen lääkemääräys vaatimusmäärittely 19.9.2014 versio 2. LIITE 1: Lääkemääräyksiin ja toimitussanomaan liittyvät oikeudet 1 Lääkemääräyksiin liittyvät oikeudet tila Toimittamaton lääkemääräys
Sähköinen lääkemääräys pitkäaikaisessa avo- tai laitoshoidossa Kansalliset toimintamallit alkaen Päivitetty
 Sähköinen lääkemääräys pitkäaikaisessa avo- tai laitoshoidossa Kansalliset toimintamallit 1.1.2017 alkaen Päivitetty 7.8.2017 Asiakkaan reseptit pitkäaikaisessa avo- tai laitoshoidossa Kun asiakas saa
Sähköinen lääkemääräys pitkäaikaisessa avo- tai laitoshoidossa Kansalliset toimintamallit 1.1.2017 alkaen Päivitetty 7.8.2017 Asiakkaan reseptit pitkäaikaisessa avo- tai laitoshoidossa Kun asiakas saa
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Sosiaali- ja terveysministeriö E-KIRJE STM STO Närhi Ulla(STM) Eduskunta
 Sosiaali- ja terveysministeriö E-KIRJE STM2013-00035 STO Närhi Ulla(STM) 30.01.2013 Eduskunta Viite Asia EU; terveys; komission täytäntööpanodirektiivi 2012/52/EU toimenpiteistä toisessa jäsenvaltiossa
Sosiaali- ja terveysministeriö E-KIRJE STM2013-00035 STO Närhi Ulla(STM) 30.01.2013 Eduskunta Viite Asia EU; terveys; komission täytäntööpanodirektiivi 2012/52/EU toimenpiteistä toisessa jäsenvaltiossa
LISÄTIETOLOMAKE 3 Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52
 Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) keskenmenohetkellä Sikiöiden lukumäärä Keskenmenoon mahdollisesti vaikuttaneet tekijät
Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) keskenmenohetkellä Sikiöiden lukumäärä Keskenmenoon mahdollisesti vaikuttaneet tekijät
Raskauden ehkäisy synnytyksen jälkeen Katja Hämeenoja, ylilääkäri Lapin keskussairaala
 Raskauden ehkäisy synnytyksen jälkeen 3.5.2017 Katja Hämeenoja, ylilääkäri Lapin keskussairaala Miksi tärkeä asia? Vuonna 2015 Suomessa tehtiin 9441 raskaudenkeskeytystä, mikä on pienin määrä vuonna 1970
Raskauden ehkäisy synnytyksen jälkeen 3.5.2017 Katja Hämeenoja, ylilääkäri Lapin keskussairaala Miksi tärkeä asia? Vuonna 2015 Suomessa tehtiin 9441 raskaudenkeskeytystä, mikä on pienin määrä vuonna 1970
Version 6, 5 October TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus
 TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä apteekkilainen
TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä apteekkilainen
ESIMERKKIPAKKAUS AIVASTUX. Erä 1058350. MTnr 0000 Myyntiluvan haltija: Lääketehdas Oy, Lääkekylä, Suomi. Vnr 39 71 65. Vnr 39 71 65. tit q.s.
 ESIMERKKIPAKKAUS AIVASTUX 12 2015 1058350 Käyt. viim.: 12 2015 Erä 1058350 Aivastux 10 mg 10 tabl. Vnr 04 36 79 Ibuprofen 400 mg Glycerol (85%) Sacchar Constit q.s. Käyttötarkoitus: Allergisen nuhan, allergisten
ESIMERKKIPAKKAUS AIVASTUX 12 2015 1058350 Käyt. viim.: 12 2015 Erä 1058350 Aivastux 10 mg 10 tabl. Vnr 04 36 79 Ibuprofen 400 mg Glycerol (85%) Sacchar Constit q.s. Käyttötarkoitus: Allergisen nuhan, allergisten
MUNASOLUJEN LUOVUTTAJAN HAASTATTELU HENKILÖTIEDOT. Sukunimi: Henkilötunnus: Ikä: Etunimet: Osoite: Tilinumero kulujen korvaamiseksi: Puhelin: Ammatti:
 MUNASOLUJEN LUOVUTTAJAN HAASTATTELU HENKILÖTIEDOT Sukunimi: Etunimet: Henkilötunnus: Ikä: Osoite: Puhelin: Tilinumero kulujen korvaamiseksi: Ammatti: Elätkö vakituisessa parisuhteessa: Parisuhde vuodesta:
MUNASOLUJEN LUOVUTTAJAN HAASTATTELU HENKILÖTIEDOT Sukunimi: Etunimet: Henkilötunnus: Ikä: Osoite: Puhelin: Tilinumero kulujen korvaamiseksi: Ammatti: Elätkö vakituisessa parisuhteessa: Parisuhde vuodesta:
Version 6, 14 August Etukansi. MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute
 Etukansi MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute Sisäsivut TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Etukansi MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute Sisäsivut TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Raskauden ehkäisy. Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää.
 Raskauden ehkäisy Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää. Jokaisella on oikeus saada oikeaa tietoa ja neuvontaa raskauden ehkäisyn keinoista sekä niiden hyödyistä,
Raskauden ehkäisy Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää. Jokaisella on oikeus saada oikeaa tietoa ja neuvontaa raskauden ehkäisyn keinoista sekä niiden hyödyistä,
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Version 6, 5 October MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus
 MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota
MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota
LISÄTIETOLOMAKE 1 Synnynnäinen epämuodostuma (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52
 Synnynnäinen epämuodostuma (sivu /4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 4 77 0 5 Raskauden kesto (viikkoa) Syntyneiden lapsien lukumäärä Synnytystapa Alatie Keisarileikkaus LUETTELO SYNNYNNÄISISTÄ
Synnynnäinen epämuodostuma (sivu /4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 4 77 0 5 Raskauden kesto (viikkoa) Syntyneiden lapsien lukumäärä Synnytystapa Alatie Keisarileikkaus LUETTELO SYNNYNNÄISISTÄ
Version 7, 5 October MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute
 MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota huomioon seuraavat tärkeät turvallisuustiedot
MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota huomioon seuraavat tärkeät turvallisuustiedot
Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin
 Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
TERVEYDENHUOLLON AMMATTILAISTEN OPAS
 TERVEYDENHUOLLON AMMATTILAISTEN OPAS Tietoa riskeistä, jotka liittyvät valproaatin (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) käyttöön naispotilaille ja raskauden aikana. Raskauden ehkäisy
TERVEYDENHUOLLON AMMATTILAISTEN OPAS Tietoa riskeistä, jotka liittyvät valproaatin (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) käyttöön naispotilaille ja raskauden aikana. Raskauden ehkäisy
Minun psori päiväkirjani
 Tähän päiväkirjaasi voit kirjoittaa henkilökohtaisesti psoristasi, psorin hoidoistasi ja niiden vaikutuksista. Voit hyödyntää päiväkirjaa kirjoittamalla myös muista psoriin vaikuttavista asioista, sillä
Tähän päiväkirjaasi voit kirjoittaa henkilökohtaisesti psoristasi, psorin hoidoistasi ja niiden vaikutuksista. Voit hyödyntää päiväkirjaa kirjoittamalla myös muista psoriin vaikuttavista asioista, sillä
1. LÄÄKEVALMISTEEN NIMI. Toctino 10 mg kapselit, pehmeä Toctino 30 mg kapselit, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Toctino 10 mg kapselit, pehmeä Toctino 30 mg kapselit, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 10 mg tai 30 mg alitretinoiinia. Apuaineet,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Toctino 10 mg kapselit, pehmeä Toctino 30 mg kapselit, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 10 mg tai 30 mg alitretinoiinia. Apuaineet,
Versio 8, TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute
 TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia?
 Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia? Reetta Kälviäinen Professori, ylilääkäri EPILEPSIAKESKUS 15.10.2014 Valproaatin käytön rajoituksia naisilla ja tytöillä
Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia? Reetta Kälviäinen Professori, ylilääkäri EPILEPSIAKESKUS 15.10.2014 Valproaatin käytön rajoituksia naisilla ja tytöillä
LISÄTIETOLOMAKE 2 Neonataalikuolema (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52
 Neonataalikuolema (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) Syntyneiden lapsien lukumäärä Synnytystapa Alatie Keisarileikkaus LAPSI VASTASYNTYNEEN
Neonataalikuolema (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) Syntyneiden lapsien lukumäärä Synnytystapa Alatie Keisarileikkaus LAPSI VASTASYNTYNEEN
X/2013 LÄÄKKEIDEN TOIMITTAMINEN EUROOPPA- LAISEN LÄÄKEMÄÄRÄYKSEN PERUSTEELLA. Määräys pp.kk.vvvv Dnro
 Määräys pp.kk.vvvv Dnro X/2013 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys LÄÄKKEIDEN TOIMITTAMINEN EUROOPPA- LAISEN LÄÄKEMÄÄRÄYKSEN PERUSTEELLA Lääkealan turvallisuus- ja kehittämiskeskus Säkerhets-
Määräys pp.kk.vvvv Dnro X/2013 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys LÄÄKKEIDEN TOIMITTAMINEN EUROOPPA- LAISEN LÄÄKEMÄÄRÄYKSEN PERUSTEELLA Lääkealan turvallisuus- ja kehittämiskeskus Säkerhets-
Suomeksi Näin käytät ereseptiä
 Suomeksi Näin käytät ereseptiä Kaikkialla Suomessa siirrytään vaiheittain käyttämään sähköistä reseptiä eli ereseptiä. Tarkista, mitkä apteekit ja terveydenhuollon toimipaikat käyttävät jo ereseptiä. Saat
Suomeksi Näin käytät ereseptiä Kaikkialla Suomessa siirrytään vaiheittain käyttämään sähköistä reseptiä eli ereseptiä. Tarkista, mitkä apteekit ja terveydenhuollon toimipaikat käyttävät jo ereseptiä. Saat
Version 6, 14 August Etukansi. TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute
 Etukansi TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Etukansi TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
+ + Lapsesta ei ole mitään henkilöllisyyttä tai kansalaisuusasemaa osoittavaa todistusta tai asiakirjaa KAN_1C_100214PP +
 KAN_1C 1 *1169601* KANSALAISUUSHAKEMUKSEN KANSSAHAKIJANA OLEVAN 15-17 -VUOTIAAN LAPSEN LIITELOMAKE Tämä liitelomake on tarkoitettu 15-17 -vuotiaalle lapselle (kanssahakija), jolle haetaan Suomen kansalaisuutta
KAN_1C 1 *1169601* KANSALAISUUSHAKEMUKSEN KANSSAHAKIJANA OLEVAN 15-17 -VUOTIAAN LAPSEN LIITELOMAKE Tämä liitelomake on tarkoitettu 15-17 -vuotiaalle lapselle (kanssahakija), jolle haetaan Suomen kansalaisuutta
Julkisen yhteenvedon osiot
 EU RMP alitretinoiini v8 toukokuu 2014 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Puhelin- tai sähköpostikyselyissä 6 14 % pohjois- ja keskieurooppalaisista aikuisista vastasi,
EU RMP alitretinoiini v8 toukokuu 2014 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Puhelin- tai sähköpostikyselyissä 6 14 % pohjois- ja keskieurooppalaisista aikuisista vastasi,
sivu 1 (8) Sähköinen lääkemääräys vaatimusmäärittely versio 2.8
 sivu 1 (8) LIITE 1: Lääkemääräyksiin ja toimitussanomaan liittyvät oikeudet 1 Lääkemääräyksiin liittyvät oikeudet (lääkemääräysten käsittelyyn liittyvät käyttöoikeudet) tila Toimittamaton lääkemääräys
sivu 1 (8) LIITE 1: Lääkemääräyksiin ja toimitussanomaan liittyvät oikeudet 1 Lääkemääräyksiin liittyvät oikeudet (lääkemääräysten käsittelyyn liittyvät käyttöoikeudet) tila Toimittamaton lääkemääräys
Raskaustesti Puikko. Käyttöopas. Version 1.0 FI Cat.No. W1-M(5.0mm)
 FI Raskaustesti Puikko Käyttöopas Version 1.0 FI 18102017 Cat.No. W1-M(5.0mm) Babyplan raskaustesti on nopea raskaustesti, jonka voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
FI Raskaustesti Puikko Käyttöopas Version 1.0 FI 18102017 Cat.No. W1-M(5.0mm) Babyplan raskaustesti on nopea raskaustesti, jonka voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
Liite III. Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset
 Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä MAVENCLAD LÄÄKÄRIN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI - FI/CLA/1117/0049
 Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Sairaalan talousjohtaja. 3. Rekisterin nimi Niuvanniemen sairaalan potilaslaskutusrekisteri
 REKISTERISELOSTE 1 (5) 1. Rekisterin pitäjä Nimi Niuvanniemen sairaala (valtion mielisairaala) Postiosoite Niuvankuja 65 70240 KUOPIO Puhelin 0295 242 111 (vaihde) 2. Rekisteriasioita hoitava henkilö tai
REKISTERISELOSTE 1 (5) 1. Rekisterin pitäjä Nimi Niuvanniemen sairaala (valtion mielisairaala) Postiosoite Niuvankuja 65 70240 KUOPIO Puhelin 0295 242 111 (vaihde) 2. Rekisteriasioita hoitava henkilö tai
Tarkistuslista 1: Metyylifenidaatin määräämistä edeltävä tarkistuslista. Ennen metyylifenidaattihoidon aloittamista
 Tarkistuslista 1: Metyylifenidaatin määräämistä edeltävä tarkistuslista Seuraava tarkistuslista on tarkoitettu auttamaan metyylifenidaattia sisältävän lääkkeen määräämisessä vähintään 6-vuotiaille lapsille
Tarkistuslista 1: Metyylifenidaatin määräämistä edeltävä tarkistuslista Seuraava tarkistuslista on tarkoitettu auttamaan metyylifenidaattia sisältävän lääkkeen määräämisessä vähintään 6-vuotiaille lapsille
Sähköisen lääkemääräyslain muutokset HE 219/ /251 THL/OPER lakimies Joni Komulainen Joni Komulainen, lakimies, OPER
 Sähköisen lääkemääräyslain muutokset HE 219/2013 28.3.2014/251 THL/OPER lakimies Joni Komulainen 1.9.2015 Joni Komulainen, lakimies, OPER Muutetut lait 1) Lääkemääräyslaki Laki sähköisestä lääkemääräyksestä
Sähköisen lääkemääräyslain muutokset HE 219/2013 28.3.2014/251 THL/OPER lakimies Joni Komulainen 1.9.2015 Joni Komulainen, lakimies, OPER Muutetut lait 1) Lääkemääräyslaki Laki sähköisestä lääkemääräyksestä
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
ASTMAPOTILAAN HOITOPOLKU: HENGITYSHOITAJA/ASTMALÄÄKÄRI
 Astmapotilaan hoidon aloitus ja hoitopolku Simon terveysasemalla ASTMAPOTILAAN HOITOPOLKU: HENGITYSHOITAJA/ASTMALÄÄKÄRI Terveyskeskuksessa on jo ennestään käytössä suhteellisen hyvin toimiva astmapotilaan
Astmapotilaan hoidon aloitus ja hoitopolku Simon terveysasemalla ASTMAPOTILAAN HOITOPOLKU: HENGITYSHOITAJA/ASTMALÄÄKÄRI Terveyskeskuksessa on jo ennestään käytössä suhteellisen hyvin toimiva astmapotilaan
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
esimerkkipakkaus aivastux
 esimerkkipakkaus aivastux Pakkausseloste: Tietoa käyttäjälle Aivastux 10 mg tabletit setiritsiini Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle
esimerkkipakkaus aivastux Pakkausseloste: Tietoa käyttäjälle Aivastux 10 mg tabletit setiritsiini Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle
VALMISTEYHTEENVETO. Tämä lääkevalmiste on tarkoitettu ainoastaan diagnostiseen käyttöön.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Indium ( 111 In) chloride kantaliuos radioaktiivista lääkettä varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yhden millilitran koostumus referenssiajankohtana:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Indium ( 111 In) chloride kantaliuos radioaktiivista lääkettä varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yhden millilitran koostumus referenssiajankohtana:
XGEVA. (denosumabi) POTILASOPAS
 XGEVA (denosumabi) POTILASOPAS SISÄLLYS Sisällysluettelo 2 Miksi saat XGEVAa 3 Ennen XGEVA-hoitoa sekä hoidon aikana 5 Raskaus ja imetys 8 XGEVAn haittavaikutukset 8 Mitä on hyvä muistaa 10 Anna tämä kortti
XGEVA (denosumabi) POTILASOPAS SISÄLLYS Sisällysluettelo 2 Miksi saat XGEVAa 3 Ennen XGEVA-hoitoa sekä hoidon aikana 5 Raskaus ja imetys 8 XGEVAn haittavaikutukset 8 Mitä on hyvä muistaa 10 Anna tämä kortti
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot

