Jännittävät metallit
|
|
|
- Heikki Lahtinen
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Jännittävät metallit Tästä alkaa tutkimusmatkamme sähkön syntymiseen! Varmaan tiedätkin, että sähköä saadaan sekä pistorasioista että erilaisista paristoista. Pistorasioista saatava sähkö tuotetaan fysikaalisesti, mutta paristojen sähkö syntyy kemiallisesti. Sähkön synnyttämiseen kemiallisesti tarvitaan metalleja. Metalleja on monia erilaisia, mutta niillä on keskenään samanlaisia ominaisuuksia. Olen Mammu ja olen tutkimusapulaisesi. En ehkä tiedä paljoa, mutta ainakin minulla on paljon hyviä kysymyksiä. Alkajaisiksi muistelemme, minkä nimisiä metalleja on olemassa ja teemme niistä listan tähän: Metallin nimi Kemiallinen merkki Metallin nimi Kemiallinen merkki Psst tiesitkö, että elohopea, uraani ja kalsium ovat myös metalleja? Tiedätkö metallien yhteisiä ominaisuuksia? Kerro minullekin! Tiedän vain, että niitä on suurin piirtein viisi. Muistatko vielä, mikä aiheuttaa metallien yhteiset ominaisuudet? Osaatko selittää miksi metallit ovat hyviä sähkönjohteita? Huh! Luulisi näillä tiedoilla homman hoituvan. Milloinkas se välitunti oikein oli?
2 Nyt on aika käydä tutkimaan. Älä sitten ainakaan paljoa hutki, sillä muuten Mammua pelottaa. Muista käyttää suojalaseja ja työtakkia, jotta vahingot eivät olisi vaaraksi! Tarkoituksenamme on tutustua hieman lähemmin seuraaviin metalleihin: kupari, tina, sinkki, magnesium, kulta, hopea, rauta, nikkeli Päämääränämme on laittaa metallit järjestykseen niiden ominaisuuksien mukaan ja samalla löytää sähkön kemiallinen alkuperä. Tutkimus nro 1: Metallien palaminen eli miten saadaan aikaan sähinää Tämä on kyllä sellainen homma, jonka opettaja tekee ja te katsotte! Listaa tähän, mitä metalleja näit poltettavan ja mitä havaintoja teit Oliko metallien palamisreaktioiden nopeuksissa eroja? Laita metallit järjestykseen niiden palamisreaktion kiivauden mukaan. Mitä syntyy, kun metallit palavat? Kirjoita reaktioyhtälö jollekin näkemällesi metallin palamisreaktiolle.
3 Hapettunut metalli on aina ionimuodossa ja pelkistynyt atomimuodossa! Seuraavaksi tutustumme hapettumiseen ja pelkistymiseen. Hapettuminen ja pelkistyminen tapahtuvat aina yhtä aikaa. Aine hapettuu, kun se luovuttaa elektroneja. Kun aine vastaanottaa elektroneja, sen sanotaan pelkistyvän. Katsotanpa vähän lähemmin muutamaa esimerkkitapausta. Täydennäthän kuviot piirtämällä puuttuvat elektronit ja merkitsemällä atomien sekä ionien varaukset näkyviin. Tässä sinkki hapettuu Psst Kuvioihin on piirretty vain uloimmat elektronikuoret Zn Poistetaan Zn Sinkkiatomi Sinkki-ioni Nyt laitetaan kupari pelkistymään! Lisätään Cu Cu Kupari-ioni Kupariatomi Mitenköhän elektronit liikkuvat, kun yksi sinkkiatomi pelkistää kaksi kupari-ionia? Zn Cu Cu Kappas, yhtään elektronia ei mene hukkaan! Muistithan merkitä alku- ja lopputilanteen varaukset näkyviin?
4 Olemme valmiita seuraavaan koitokseen Tutkimus nro 2: Rauta vs. kupari eli kiista elektroneista Jos sinulla ei ole kuparisulfaattiliuosta, saat tehdä sen liuottamalla kuparisulfaattia veteen. Tässä työssä tutkitaan metallien hapettumista ja pelkistymistä. Tarvitset koeputken, siihen sopivan korkin sekä suodatuslaitteiston. Täytä koeputki noin puolilleen kuparisulfaattiliuoksella ja lisää vajaa teelusikallinen rautajauhetta. Sulje koeputki tiiviisti ja ravistele. Mitä havaitset? Mikä aiheuttaa kuparisulfaattiliuoksen sinisen värin? Mitä atomeja ja ioneja koeputkessa oli ennen reaktiota? Mitä atomeja ja ioneja koeputkessa on reaktion jälkeen? Suodata metallihippuset pois liuoksesta ja tutki niitä tarkemmin. Mitä huomaat? Selitä havaintosi siten, että Mammukin sen ymmärtää. Voit ottaa metallihippuset talteen. Liuoksen voit kaataa viemäriin runsaan veden kanssa.
5 Katsotaan seuraavaksi, mitä metallit tykkäävät haposta Tutkimus nro 3: Metallit suolahapossa eli liueta vai ei Tässä työssä tarvitset erilaisia metalleja, koeputkia sekä koeputkitelineen. Tulitikutin ovat tarpeellisia. Laita kuhunkin koeputkeen pieni luraus 10 % suolahappoa. Lisää jokaiseen koeputkeen vielä ripaus jotakin metallijauhetta tai pieni pala metallia. Jotta tuloksesi olisivat mahdollisimman tieteellisiä, pyri käyttämään joko metallijauheita tai -paloja. Yritä pitää metallien määrät samoina! Huolehdi, että tiedät aina, mitä metallia missäkin koeputkessa on! Tee havaintoja reaktioiden voimakkuuksista. Yritä tunnistaa koeputkista kupliva kaasu päättelemällä tai viemällä palava tulitikku varovasti koeputken yläpuolelle. Kuvaile eri metallien reaktiota suolahapon kanssa Laita metallit järjestykseen sen mukaan, kuinka kiivaasti ne regoivat suolahapon kanssa ja vertaa tuloksia tutkimuksen 1 tuloksiin. Mitä huomaat? Psst Open pöydällä on perintökoruja happokylvyssä Oletkin varmaan kuullut jalometalleista. Miten ne ovat erilaisia kuin muut metallit? Mitkä tutkimuksessa käytetyistä metalleista olivat jalometalleja? Miten ne reagoivat suolahapon kanssa? Huh! Miksei rauta ole jalometalli?
6 Kirjoita jossakin koeputkessa tapahtuneen reaktion reaktioyhtälö. Mitä metallille on tapahtunut? Entä vedylle? Voit kaataa koeputkien sisällöt viemäriin runsaan veden kanssa. Ota liukenemattomat metallit talteen! Metallit voidaan luokitella kahteen ryhmään eli jaloihin ja epäjaloihin metalleihin. Jos metallit halutaan laittaa tarkempaan järjestykseen, on avuksi otettava jännitemittari. Olemme jo oppineet, että metalliatomien ja -ionien välillä voi liikkua elektroneja. Elektronit siirtyvät aina hapettuvalta metalliatomilta pelkistyvälle metalli-ionille. Jos voisimme ohjata elektronit kulkemaan tiettyä reittiä pitkin, saisimme aikaan sähkövirran. Tämä onnistuu esimerkiksi tällaisella järjestelyllä: Sähkövirta on elektronien liikettä! Jotta elektronit liikkuisivat, tarvitaan jännite. Kaksi metallilevyä Johdin Elektrolyyttiliuos Johdin Tämä on sähkökemiallisen parin kaavakuva. Sähkökemiallisessa parissa kaksi eri metallin palaa ovat ioneja sisältävässä elektrolyyttiliuoksessa, kuten suola- tai happoliuoksessa. Sähkökemiallinen pari toimii vaikka sitruunassa! Metallilevyt yhdistetään toisiinsa johtimilla, joita pitkin elektronit kulkevat. Sähkön kulkua voidaan mitata jännitemittarin avulla tai kytkemällä virtapiiriin pieni lamppu. Seuraavaksi saat itse rakentaa oman sähköparin!
7 Tutkimus nro 4: Sähkökemiallinen pari eli sähköä metalleista Tarkoituksenasi on koota sähkökemiallinen pari kupari- ja sinkkilevystä. Tarvitset ainakin johtimia ja hauenleukoja. Mitä muuta tarvitset? Huolehdi, etteivät metallilevyt kosketa toisiaan jännitten mittaamisen aikana! Kun olet koonnut sähkökemiallisen parin, tee tarvittavia kokeita ja selvitä seuraavat seikat: Mikä on metallilevyjen välinen jännite? Riittääkö tämä jännite hehkulampun sytyttämiseen? Miten jännite muuttuu, kun vaihdat hauenleukojen paikkaa metallista toiseen? Mitä jännitteelle tapahtuu, kun levyt koskettavat toisiaan? Miksi? Vertaa jännitettä tavallisen pariston jännitteeseen. Yritä saada lamppu syttymään tavallisen pariston avulla. Mitä huomaat? Huolehdi jätteiden asiallisesta loppukäsittelystä! Metalleista todellakin saadaan sähköä! Se, kuinka suuri jännite metallilevyjen välille saadaan, riippuu metalleista. Metallit on järjestetty jännitesarjaksi sen mukaan, kuinka suuri jännite metallien välille saadaan. Sähkökemiallisessa parissa syntyvä jännite on sitä suurempi, mitä kauempana metallit ovat toisistaan jännitesarjassa. Jestas! Aika hurjalta kuulostaa. Seuraavaksi sinun on tutkittava eri sähköpareja ja järjestettävä metallit jännitesarjaksi sen perusteella, kuinka suuri jännite sähköparissa syntyy.
8 Tutkimus nro 5: Galvaaniset solut eli monenmoisten sähköparien tutkimista pienessä mittakaavassa Tarvitset seuraavia välineitä: kennolevy, johtimia, jännitemittari, hauenleukoja, suodatinpaperia (1x2 cm:n pala riittää mainiosti), pinsetit. Lisäksi tarvitset pieniä paloja metalleja, joita aiot tutkia. Hyviä tutkimuskohteita ovat esimerkiksi sinkki, magnesium, rauta, nikkeli, kupari ja tina. Tarvitset myös metallien suolojen liuoksia, esimerkiksi näitä: ZnSO 4, MgSO 4, CuSO 4, SnCl 2, FeCl 2,NiSO 4. Tämä työ kannattaa suunnitella ja tehdä huolella! Joudut käyttämään myös muutaman pisaran jotain sellaista suolaliuosta, jossa ei ole tutkimaasi metallia, esimerkiksi kaliumnitraattia tai ruokasuolaliuosta. Suunnittele metallien paikat kennolevylle siten, että saat helposti mitattua jokaisen metalliparin välisen jännitteen. Tutkittavien metallien tulee olla vierekkäisissä kennoissa. Tähän voit merkitä, mitä metalleita aiot mihinkin kennoon laittaa. Kun olet valinnut metallien paikat, laita jokaiseen kennoon sen metallin suolan liuosta, jota aiot kennoon laittaa. Esimerkiksi niihin kennoihin, joihin aiot laittaa rautapalan, laitat raudan suolan liuosta. Ole huolellinen, ettet mene sekaisin, mitä suolaa missäkin kennossa on! Seuraavaksi teemme suodatinpaperista suolasillan. Laita suodatinpaperipalanen petrimaljalle ja kostuta se muutamalla pisaralla kaliumnitraattia tai ruokasuolaliuosta. Mittaa jokaisen metalliparin jännite näin: 1: valitse tutkittavat metallit 2: aseta suolasilta tutkittavien metallien kennojen välille pinseteillä ja huolehdi, että suolasilta osuu kumpaankin liuokseen 3: kiinnitä hauenleuat tutkittaviin metalleihin ja aseta ne oman suolansa liuokseen 4: mittaa jännite jännitemittarilla Kun mittaat jännitettä, kytke musta johto mittarin COM-kohtaan ja punainen johto mittarin V-kohtaan. Tiesithän, että mittaat tasajännitettä?
9 Voit kirjata tutkimustuloksesi tähän taulukkoon Metallit kiinni punaisessa johtimessa Zn Mg Cu Ni Fe Sn Zn Metallit kiinni mustassa johtimessa Mg Cu Ni Fe Sn Miksi samalle metalliparille saadaan kaksi eri jännitettä? Mikä on näiden kahden jännitteen ero? Mitä merkitystä on suolasillalla? Kokeile mitata jonkin sähköparin jännite ilman suolasiltaa. Metallien jännitesarjassa metallit on asetettu järjestykseen sen mukaan, kuinka suuri jännite niiden välille saadaan. Mitä suurempi jännite metallien välillä on, sitä kauempana ne ovat toisistaan jännitesarjassa. Järjestä tutkimasi metallit mittaamiesi jännitteiden perusteella jännitesarjaksi. Pitkälle ollaan jo päästy, mutta vielä pitäisi hieman pinnistellä. Jätteet viemäriin runsaan veden kanssa!
10 Metallien hapettumista ja pelkistymistä voidaan tutkia jännitesarjan avulla. Toisessa päässä jännitesarjaa ovat jalometallit, jotka pelkistyvät mielellään ja reagoivat hitaasti. Mitä enemmän jännitesarjassa edetään kohti toista päätä, sitä helpommin metalliatomit hapettuvat ja sitä kiivammin ne reagoivat. Voimmekin siis todeta, että mitä epäjalompi metalli on, sitä helpommin se hapettuu, ja mitä jalompi metalli on, sitä paremmin se pelkistyy. Reaktionopeus kasvaa Jalous kasvaa Mg Zn Fe Ni Sn Cu Ag Au Epäjalot metallit Hapettuvat helposti Liukenevat suolahappoon Jalot metallit Pelkistyvät mielellään Eivät liukene suolahappoon Jos sähköparissa metallien välillä on positiivinen jännite, mustassa johtimessa kiinni oleva metalli pelkistää punaisesa johtimessa olevan metallin ionin. Jos sähköparissa metallien välillä oleva jännite on negatiivinen, mustassa johtimessa kiinni oleva metalli ei voi pelkistää punaisessa johtimessa kiinni olevan metallin ionia. Tämä nähdään helpommin tutkimalla jännitesarjaa. Metalli-ionin vasemmalla puolella oleva metalli voi pelkistää metalli-ionin, mutta oikealla puolella oleva ei. Esimerkiksi sinkki voi pelkistää kupari-ionin, sillä sinkki on kuparin vasemmalla puolella. Kupari sen sijaan ei voi pelkistää sinkki-ionia, sillä kupari on sinkin oikealla puolella. Tutki jännitesarjaa ja päättele, ovatko seuraavat reaktiot mahdollisia: Tina pelkistää magnesiumionit Rauta pelkistää hopeaionit Magnesium pelkistää nikkeli-ionit Onpas monimutkaista. Minä kyllä ajattelisin niin, että epäjalompi metalli pelkistää jalomman metallin ionin. Sinkki pelkistää kupari-ionit Sinkki pelkistää kultaionit Nikkeli pelkistää kupri-ionit Rauta pelkistää sinkki-ionit Mikäs nyt olikaan syy sille, että epäjalot metallit reagoivat jalometalleja nopeammin? Hopea pelkistää kultaionit Kulta pelkistää hopeaionit
11 Tutkimus nro 6: Metallien suolaliuosten tunnistaminen eli jännitesarja kovassa käytössä Saat eteesi kolme koeputkellista metallisuolojen liuoksia. Tehtävänäsi on selvittää, minkä metallin suolaa missäkin koeputkessa on. Liuokset voivat olla hopean, tinan, sinkin ja kuparin liuoksia. Selvitystyössäsi saat käyttää apuna ainoastaan metallien jännitesarjaa sekä rauta- ja kuparipalasia. Suunnitele tutkimuksesi huolellisesti ja kirjaa havaintosi ylös. Ole huolellinen, ettet mene koeputkissa sekaisin! Osasin, osasin! Mammu osasi melkein ihan itse!
Jännittävät metallit Opettajan ohje
 Jännittävät metallit Opettajan ohje Koonnut Oili Kemppainen Tämän työn tarkoituksena on opettaa sähkökemiaa. Työn tiimellyksessä kerrataan metallien ominaisuudet, tutustutaan hapettumiseen ja pelkistymiseen
Jännittävät metallit Opettajan ohje Koonnut Oili Kemppainen Tämän työn tarkoituksena on opettaa sähkökemiaa. Työn tiimellyksessä kerrataan metallien ominaisuudet, tutustutaan hapettumiseen ja pelkistymiseen
Käsitteitä. Hapetusluku = kuvitteellinen varaus, jonka atomi saa elektronin siirtyessä
 Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Metallien ominaisuudet ja rakenne
 Metallien Kemia 25 Metallien ominaisuudet ja rakenne Metallit ovat käyttökelpoisia materiaaleja. Niiden ominaisuudet johtuvat metallin rakennetta koossa pitävästä metallisidoksesta. Metalleja käytetään
Metallien Kemia 25 Metallien ominaisuudet ja rakenne Metallit ovat käyttökelpoisia materiaaleja. Niiden ominaisuudet johtuvat metallin rakennetta koossa pitävästä metallisidoksesta. Metalleja käytetään
1. Malmista metalliksi
 1. Malmista metalliksi Metallit esiintyvät maaperässä yhdisteinä, mineraaleina Malmiksi sanotaan kiviainesta, joka sisältää jotakin hyödyllistä metallia niin paljon, että sen erottaminen on taloudellisesti
1. Malmista metalliksi Metallit esiintyvät maaperässä yhdisteinä, mineraaleina Malmiksi sanotaan kiviainesta, joka sisältää jotakin hyödyllistä metallia niin paljon, että sen erottaminen on taloudellisesti
Sähkökemia. Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali
 Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Normaalipotentiaalit
 Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
luku2 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen
 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella
 Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella Tarvittavat ennakkotiedot ja käsitteet: Atomi, anioni, kationi, atomien yleisimmät hapetustilat, metallien jännitesarja,
Metallien sähkökemiallisen jännitesarjan opettaminen draaman avulla yläasteella Tarvittavat ennakkotiedot ja käsitteet: Atomi, anioni, kationi, atomien yleisimmät hapetustilat, metallien jännitesarja,
 Työn toteutus Lisää pullosta kolmeen koeputkeen 1 2 cm:n kerros suolahappoa. Pudota ensimmäiseen koeputkeen kuparinaula, toiseen sinkkirae ja kolmanteen magnesiumnauhan pala. Tulosten käsittely Mikä aine
Työn toteutus Lisää pullosta kolmeen koeputkeen 1 2 cm:n kerros suolahappoa. Pudota ensimmäiseen koeputkeen kuparinaula, toiseen sinkkirae ja kolmanteen magnesiumnauhan pala. Tulosten käsittely Mikä aine
Vesi. Pintajännityksen Veden suuremman tiheyden nesteenä kuin kiinteänä aineena Korkean kiehumispisteen
 Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Perunapellosta virtaa! Jenna Salmijärvi ja Maija Torttila
 Perunapellosta virtaa! Jenna Salmijärvi ja Maija Torttila Johdanto Kuva 1: Pokepallo Olet lähtenyt pelaamaan Pokèmon Go peliä. Päädyit keskelle perunapeltoa etsimään pokemoneja. Eteesi ilmestyi Snorlax!
Perunapellosta virtaa! Jenna Salmijärvi ja Maija Torttila Johdanto Kuva 1: Pokepallo Olet lähtenyt pelaamaan Pokèmon Go peliä. Päädyit keskelle perunapeltoa etsimään pokemoneja. Eteesi ilmestyi Snorlax!
Kemia 7. luokka. Nimi
 Kemia 7. luokka Nimi 1. Turvallinen työskentely Varoitusmerkit Kaasupolttimen käyttö Turvallinen työskentely Turvallinen työskentely Kaasupolttimen käyttö 1. Varmista että ilma-aukot ovat kiinni. 2. Sytytä
Kemia 7. luokka Nimi 1. Turvallinen työskentely Varoitusmerkit Kaasupolttimen käyttö Turvallinen työskentely Turvallinen työskentely Kaasupolttimen käyttö 1. Varmista että ilma-aukot ovat kiinni. 2. Sytytä
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Sähkökemiaa. Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio
 Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio Hapettuminen ja pelkistyminen 1. Hapetin ja pelkistin 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi
Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio Hapettuminen ja pelkistyminen 1. Hapetin ja pelkistin 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi
Tutkimusmateriaalit -ja välineet: kaarnan palaset, hiekan murut, pihlajanmarjat, juuripalat, pakasterasioita, vettä, suolaa ja porkkananpaloja.
 JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
Jaksollinen järjestelmä ja sidokset
 Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
Booriryhmä Hiiliryhmä Typpiryhmä Happiryhmä Halogeenit Jalokaasut Jaksollinen järjestelmä ja sidokset 13 Jaksollinen järjestelmä on tärkeä kemian työkalu. Sen avulla saadaan tietoa alkuaineiden rakenteista
Sähkökemiaa. Hapettuminen Jännitesarja Elektrolyysi Korroosio
 Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Korroosio Hapettuminen ja pelkistyminen 1. Määritelmät 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi ja sen sovelluksia
Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Korroosio Hapettuminen ja pelkistyminen 1. Määritelmät 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi ja sen sovelluksia
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Elektrolyysi Anodilla tapahtuu aina hapettuminen ja katodilla pelkistyminen!
 Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
7. luokan kemia. Nimi
 7. luokan kemia Nimi Kurssin arviointi arvosana socrative 1: turvallinen työskentely hyväksytty/hylätty socrative 2: työvälineet 410 socrative 3: kemialliset merkit 410 socrative 4: alkuaine, yhdiste,
7. luokan kemia Nimi Kurssin arviointi arvosana socrative 1: turvallinen työskentely hyväksytty/hylätty socrative 2: työvälineet 410 socrative 3: kemialliset merkit 410 socrative 4: alkuaine, yhdiste,
Workshop: Tekniikan kemia OAMK:ssa
 1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
2.1 Sähköä kemiallisesta energiasta
 2.1 Sähköä kemiallisesta energiasta Monet hapettumis ja pelkistymisreaktioista on spontaaneja, jolloin elektronien siirtyminen tapahtuu itsestään. Koska reaktio on spontaani, vapautuu siinä energiaa, yleensä
2.1 Sähköä kemiallisesta energiasta Monet hapettumis ja pelkistymisreaktioista on spontaaneja, jolloin elektronien siirtyminen tapahtuu itsestään. Koska reaktio on spontaani, vapautuu siinä energiaa, yleensä
AKKU- JA PARISTOTEKNIIKAT
 AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
Sähkökemian perusteita, osa 1
 Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
(Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen)
 KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
KE2-kurssi: Kemian mikromaalima Osio 1 (Huom! Oikeita vastauksia voi olla useita ja oikeasta vastauksesta saa yhden pisteen) Monivalintatehtäviä 1. Etsi seuraavasta aineryhmästä: ioniyhdiste molekyyliyhdiste
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Kemian eriyttävä tunti. Tekijät Riina Karppinen, Klaus Mäki-Petäys ja Kirsi Söderberg Aihe: sähkökemiallinen pari. Johdanto
 Kemian eriyttävä tunti Tekijät Riina Karppinen, Klaus Mäki-Petäys ja Kirsi Söderberg Aihe: sähkökemiallinen pari Johdanto Eriytettäväksi aiheeksi on valittu sähkökemiallinen pari, ja tunti on suunniteltu
Kemian eriyttävä tunti Tekijät Riina Karppinen, Klaus Mäki-Petäys ja Kirsi Söderberg Aihe: sähkökemiallinen pari Johdanto Eriytettäväksi aiheeksi on valittu sähkökemiallinen pari, ja tunti on suunniteltu
Käytännön esimerkkejä on lukuisia.
 PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012
 Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Aine koostuu atomeista Nimitys tulee sanasta atomos = jakamaton (400 eaa, Kreikka) Atomin kuvaamiseen käytetään atomimalleja Pallomalli
Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Aine koostuu atomeista Nimitys tulee sanasta atomos = jakamaton (400 eaa, Kreikka) Atomin kuvaamiseen käytetään atomimalleja Pallomalli
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
sivu 1/6 KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää myös yläkoululaisille, kunhan
VÄRIKÄSTÄ KEMIAA. MOTIVAATIO: Mitä tapahtuu teelle kun lisäät siihen sitruunaa? Entä mitä havaitset kun peset mustikan värjäämiä sormia saippualla?
 VÄRIKÄSTÄ KEMIAA KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. Parhaiten työ soveltuu alakouluun kurssille aineet ympärillämme tai yläkouluun kurssille
VÄRIKÄSTÄ KEMIAA KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. Parhaiten työ soveltuu alakouluun kurssille aineet ympärillämme tai yläkouluun kurssille
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA Työskentelet metallinkierrätyslaitoksella. Asiakas tuo kierrätyslaitokselle 1200 kilogramman erän kellertävää metallimateriaalia, joka on löytynyt purettavasta
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA Työskentelet metallinkierrätyslaitoksella. Asiakas tuo kierrätyslaitokselle 1200 kilogramman erän kellertävää metallimateriaalia, joka on löytynyt purettavasta
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
Johdanto... 3. Tavoitteet... 3. Työturvallisuus... 3. Polttokennoauton rakentaminen... 4. AURINKOPANEELITUTKIMUS - energiaa aurinkopaneelilla...
 OHJEKIRJA SISÄLLYS Johdanto... 3 Tavoitteet... 3 Työturvallisuus... 3 Polttokennoauton rakentaminen... 4 AURINKOPANEELITUTKIMUS - energiaa aurinkopaneelilla... 5 POLTTOKENNOAUTON TANKKAUS - polttoainetta
OHJEKIRJA SISÄLLYS Johdanto... 3 Tavoitteet... 3 Työturvallisuus... 3 Polttokennoauton rakentaminen... 4 AURINKOPANEELITUTKIMUS - energiaa aurinkopaneelilla... 5 POLTTOKENNOAUTON TANKKAUS - polttoainetta
Tehtäviä sähkökemiasta
 Tehtäviä sähkökemiasta 1. Millainen on sähkökemiallinen jännitesarja? Mitä sen avulla voidaan kuvata? Jännitesarjalla kuvataan metallien taipumusta muodostaa kemiallisia yhdisteitä. Metallit on järjestetty
Tehtäviä sähkökemiasta 1. Millainen on sähkökemiallinen jännitesarja? Mitä sen avulla voidaan kuvata? Jännitesarjalla kuvataan metallien taipumusta muodostaa kemiallisia yhdisteitä. Metallit on järjestetty
Työohjeet Jippo- polkuun
 Työohjeet Jippo- polkuun TUTKIMUSPISTE 1: Kelluuko? Tarvikkeet: kaarnan palaset, hiekan murut, pihlajanmarjat, juuripalat, pakasterasioita, vettä, suolaa ja porkkananpaloja. Tutkimus 1a: Tee hypoteesi
Työohjeet Jippo- polkuun TUTKIMUSPISTE 1: Kelluuko? Tarvikkeet: kaarnan palaset, hiekan murut, pihlajanmarjat, juuripalat, pakasterasioita, vettä, suolaa ja porkkananpaloja. Tutkimus 1a: Tee hypoteesi
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
Sähköparin oppimista tukeva tietokonesimulaatio kemian lukioopetukseen
 Sähköparin oppimista tukeva tietokonesimulaatio kemian lukioopetukseen Taina Sirkiä Pro gradu -tutkielma 7/2015 Kemian opettajankoulutusyksikkö Kemian laitos Matemaattis-luonnontieteellinen tiedekunta
Sähköparin oppimista tukeva tietokonesimulaatio kemian lukioopetukseen Taina Sirkiä Pro gradu -tutkielma 7/2015 Kemian opettajankoulutusyksikkö Kemian laitos Matemaattis-luonnontieteellinen tiedekunta
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
Sukunimi: Etunimi: Henkilötunnus:
 K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
K1. Onko väittämä oikein vai väärin. Oikeasta väittämästä saa 0,5 pistettä. Vastaamatta jättämisestä tai väärästä vastauksesta ei vähennetä pisteitä. (yhteensä 10 p) Oikein Väärin 1. Kaikki metallit johtavat
KUPARIASPIRINAATIN VALMISTUS
 TAUSTAA KUPARIASPIRINAATIN VALMISTUS Kupariaspirinaatti eli dikuparitetra-asetyylisalisylaatti on epäorgaaninen yhdiste, jonka käyttöä nivelreuman hoidossa ja toisen sukupolven lääkevalmistuksessa on tutkittu
TAUSTAA KUPARIASPIRINAATIN VALMISTUS Kupariaspirinaatti eli dikuparitetra-asetyylisalisylaatti on epäorgaaninen yhdiste, jonka käyttöä nivelreuman hoidossa ja toisen sukupolven lääkevalmistuksessa on tutkittu
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet
 Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet Kari Sormunen Syksy 2014 Kemiallinen reaktio Kemiallinen reaktio on prosessi, jossa aineet muuttuvat toisiksi aineiksi: atomien
Kemiallisia reaktioita ympärillämme Fysiikan ja kemian pedagogiikan perusteet Kari Sormunen Syksy 2014 Kemiallinen reaktio Kemiallinen reaktio on prosessi, jossa aineet muuttuvat toisiksi aineiksi: atomien
Myös normaali sadevesi on hieman hapanta (ph n.5,6) johtuen ilman hiilidioksidista, joka liuetessaan veteen muodostaa hiilihappoa.
 sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
TÄS ON PROTSKUU! PROTEIINIEN KEMIAA
 sivu 1/8 TÄS ON PROTSKUU! PROTEIINIEN KEMIAA LUOKKA-ASTE/KURSSI TAUSTA Työ soveltuu peruskoulun yläasteelle ja lukioon. Työn tavoite on tutustua proteiinien kokeellisiin tunnistusmenetelmiin. POHDITTAVAKSI
sivu 1/8 TÄS ON PROTSKUU! PROTEIINIEN KEMIAA LUOKKA-ASTE/KURSSI TAUSTA Työ soveltuu peruskoulun yläasteelle ja lukioon. Työn tavoite on tutustua proteiinien kokeellisiin tunnistusmenetelmiin. POHDITTAVAKSI
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA
 SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää
SUMUINEN AAMU METALLINKIERRÄTYSLAITOKSELLA KOHDERYHMÄ: Työ on suunniteltu lukion kurssille KE4, jolla käsitellään teollisuuden tärkeitä raaka-aineita sekä hapetus-pelkitysreaktioita. Työtä voidaan käyttää
ROMUMETALLIA OSTAMASSA (OSA 1)
 ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
ROMUMETALLIA OSTAMASSA (OSA 1) Johdanto Kupari on metalli, jota käytetään esimerkiksi sähköjohtojen, tietokoneiden ja putkiston valmistamisessa. Korkean kysynnän vuoksi kupari on melko kallista. Kuparipitoisen
7. luokan kemia. Nimi
 7. luokan kemia Nimi Tavoitteet ja arviointi Tässä on esitetty seitsemännen luokan kemian tavoitteet ja niihin liittyvät taitotasot. Voit näiden avulla seurata omaa oppimistasi ja pohtia omia tavoitteitasi.
7. luokan kemia Nimi Tavoitteet ja arviointi Tässä on esitetty seitsemännen luokan kemian tavoitteet ja niihin liittyvät taitotasot. Voit näiden avulla seurata omaa oppimistasi ja pohtia omia tavoitteitasi.
kipinäpurkauksena, josta salama on esimerkki.
 Sähkö 25 Esineet saavat sähkövarauksen hankauksessa kipinäpurkauksena, josta salama on esimerkki. Hankauksessa esineet voivat varautua sähköisesti. Varaukset syntyvät, koska hankauksessa kappaleesta siirtyy
Sähkö 25 Esineet saavat sähkövarauksen hankauksessa kipinäpurkauksena, josta salama on esimerkki. Hankauksessa esineet voivat varautua sähköisesti. Varaukset syntyvät, koska hankauksessa kappaleesta siirtyy
Arvioin omaa työskentelyäni ja pyydän apua, kun sitä tarvitsen. Asetan omia tavoitteita ja. työskentelyn. niiden saavuttamiseksi.
 Nimi Tavoitteet ja arviointi Tässä on esitetty seitsemännen luokan kemian tavoitteet ja niihin liittyvät taitotasot. Voit näiden avulla seurata omaa oppimistasi ja pohtia omia tavoitteitasi. 2 T2 Tiedän,
Nimi Tavoitteet ja arviointi Tässä on esitetty seitsemännen luokan kemian tavoitteet ja niihin liittyvät taitotasot. Voit näiden avulla seurata omaa oppimistasi ja pohtia omia tavoitteitasi. 2 T2 Tiedän,
Stipendiaattityöt Jyväskylän yliopiston kemian laitos
 Stipendiaattityöt Jyväskylän yliopiston kemian laitos Juha Siitonen 14. Elokuuta 2011 Alkuaineita jos tunne sä et Niiden kykyjä vähättelet minaisuudet peittelet Turha sun on koittaa Sieluja voittaa Goethe
Stipendiaattityöt Jyväskylän yliopiston kemian laitos Juha Siitonen 14. Elokuuta 2011 Alkuaineita jos tunne sä et Niiden kykyjä vähättelet minaisuudet peittelet Turha sun on koittaa Sieluja voittaa Goethe
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
JAKSOLLINEN JÄRJESTELMÄ
 JASOLLINEN JÄRJESTELMÄ Oppitunnin tavoite: Oppitunnin tavoitteena on opettaa jaksollinen järjestelmä sekä sen historiaa alkuainepelin avulla. Tunnin tavoitteena on, että oppilaat oppivat tieteellisen tutkimuksen
JASOLLINEN JÄRJESTELMÄ Oppitunnin tavoite: Oppitunnin tavoitteena on opettaa jaksollinen järjestelmä sekä sen historiaa alkuainepelin avulla. Tunnin tavoitteena on, että oppilaat oppivat tieteellisen tutkimuksen
Alikuoret eli orbitaalit
 Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Alkuaineiden jaksollinen järjestelmä Alkuaineen kemialliset ominaisuudet määräytyvät sen ulkokuoren elektronirakenteesta. Seuraus: Samanlaisen ulkokuorirakenteen omaavat alkuaineen ovat kemiallisesti sukulaisia
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
b) Reaktio Zn(s) + 2 Ag + (aq) Zn 2+ (aq) + 2 Ag (s) tapahtuu galvaanisessa kennossa. Kirjoita kennokaavio eli kennon lyhennetty esitys.
 KE4-KURSSIN KOE Kastellin lukio 2013 Vastaa kuuteen (6) kysymykseen. Tee pisteytysruudukko. 1. Tarkastele jaksollista järjestelmää ja valitse siitä a) jokin jalometalli. b) jokin alkuaine, joka reagoi
KE4-KURSSIN KOE Kastellin lukio 2013 Vastaa kuuteen (6) kysymykseen. Tee pisteytysruudukko. 1. Tarkastele jaksollista järjestelmää ja valitse siitä a) jokin jalometalli. b) jokin alkuaine, joka reagoi
YLEINEN KEMIA. Alkuaineiden esiintyminen maailmassa. Alkuaineet. Alkuaineet koostuvat atomeista. Atomin rakenne. Copyright Isto Jokinen
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
vi) Oheinen käyrä kuvaa reaktiosysteemin energian muutosta reaktion (1) etenemisen funktiona.
 3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
Kemian opiskelun avuksi
 Kemian opiskelun avuksi Ilona Kuukka Mukana: Petri Järvinen Matti Koski Euroopan Unionin Kotouttamisrahasto osallistuu hankkeen rahoittamiseen. AINE JA ENERGIA Aine aine, nominatiivi ainetta, partitiivi
Kemian opiskelun avuksi Ilona Kuukka Mukana: Petri Järvinen Matti Koski Euroopan Unionin Kotouttamisrahasto osallistuu hankkeen rahoittamiseen. AINE JA ENERGIA Aine aine, nominatiivi ainetta, partitiivi
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
JÄTTEET HARVINAISTEN LUONNONVAROJEN LÄHTEENÄ
 JÄTTEET HARVINAISTEN LUONNONVAROJEN LÄHTEENÄ Ari Väisänen 8.5.2019 Sisältö Kriittisten materiaalien tuotanto Potentiaalisia raaka-ainelähteitä Raaka-aineiden talteenotto lietteestä 3D tulostetut metallisiepparit
JÄTTEET HARVINAISTEN LUONNONVAROJEN LÄHTEENÄ Ari Väisänen 8.5.2019 Sisältö Kriittisten materiaalien tuotanto Potentiaalisia raaka-ainelähteitä Raaka-aineiden talteenotto lietteestä 3D tulostetut metallisiepparit
Kaikki ympärillämme oleva aine koostuu alkuaineista.
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
FyKe 7 9 Kemia ja OPS 2016
 Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
Kuvat: vas. Fotolia, muut Sanoma Pro Oy FyKe 7 9 Kemia ja OPS 2016 Kemian opetuksen tehtävänä on tukea oppilaiden luonnontieteellisen ajattelun sekä maailmankuvan kehittymistä. Kemian opetus auttaa ymmärtämään
KE04. Kurssikalvot. Tuomas Hentunen. Kevät Tuomas Hentunen KE04 Kevät / 24
 KE04 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE04 Kevät 2016 1 / 24 Metallien jännitesarja Metallien sähkökemiallinen jännitesarja on muodostettu metallien ja vedyn kasvavan pelkistymiskyvyn
KE04 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE04 Kevät 2016 1 / 24 Metallien jännitesarja Metallien sähkökemiallinen jännitesarja on muodostettu metallien ja vedyn kasvavan pelkistymiskyvyn
HAPANTA HUNAJAA. KESTO: Työn teoriaosion, mahdollisten alkuvalmistelujen ja siivousten lisäksi työn suoritukseen menee noin 15 minuuttia aikaa.
 HAPANTA HUNAJAA KOHDERYHMÄ: Työ on suunniteltu alakouluun, mutta sitä voi soveltaa muillekin luokka-asteille. Yläkouluissa ja lukiossa voidaan käyttää vahvoja happoja ja emäksiä ja laskea tarkemmin pitoisuudet
HAPANTA HUNAJAA KOHDERYHMÄ: Työ on suunniteltu alakouluun, mutta sitä voi soveltaa muillekin luokka-asteille. Yläkouluissa ja lukiossa voidaan käyttää vahvoja happoja ja emäksiä ja laskea tarkemmin pitoisuudet
Reaktioyhtälö. Sähköisen oppimisen edelläkävijä www.e-oppi.fi. Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava
 Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
POHDITTAVAKSI ENNEN TYÖTÄ
 MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
Tekijä lehtori Zofia Bazia-Hietikko
 Tekijä lehtori Zofia Bazia-Hietikko Tarkoituksena on tuoda esiin, että kemia on osa arkipäiväämme, siksi opiskeltavat asiat kytketään tuttuihin käytännön tilanteisiin. Ympärillämme on erilaisia kemiallisia
Tekijä lehtori Zofia Bazia-Hietikko Tarkoituksena on tuoda esiin, että kemia on osa arkipäiväämme, siksi opiskeltavat asiat kytketään tuttuihin käytännön tilanteisiin. Ympärillämme on erilaisia kemiallisia
HAPANTA HUNAJAA POHDITTAVAKSI ENNEN TYÖTÄ
 HAPANTA HUNAJAA POHDITTAVAKSI ENNEN TYÖTÄ Mitä hunaja sisältää? Hunaja sisältää noin 200 yhdistettä, muun muassa erilaisia sokereita, vettä, happoja, vettä proteiineja, vitamiineja, hivenaineita, entsyymejä
HAPANTA HUNAJAA POHDITTAVAKSI ENNEN TYÖTÄ Mitä hunaja sisältää? Hunaja sisältää noin 200 yhdistettä, muun muassa erilaisia sokereita, vettä, happoja, vettä proteiineja, vitamiineja, hivenaineita, entsyymejä
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
ILOTULITUSRAKETTIEN KEMIAA TUTKIMUKSELLINEN OPPIMISKOKONAISUUS YLÄKOULUN KEMIAN OPETUKSEEN
 ILOTULITUSRAKETTIEN KEMIAA TUTKIMUKSELLINEN OPPIMISKOKONAISUUS YLÄKOULUN KEMIAN OPETUKSEEN Topias Ikävalko 1 & Roosa Pylvänen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Aihe: Metallien liekin
ILOTULITUSRAKETTIEN KEMIAA TUTKIMUKSELLINEN OPPIMISKOKONAISUUS YLÄKOULUN KEMIAN OPETUKSEEN Topias Ikävalko 1 & Roosa Pylvänen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Aihe: Metallien liekin
7. Resistanssi ja Ohmin laki
 Nimi: LK: SÄHKÖ-OPPI Tarmo Partanen Teoria (Muista hyödyntää sanastoa) 1. Millä nimellä kuvataan sähköisen komponentin (laitteen, johtimen) sähkön kulkua vastustavaa ominaisuutta? 2. Miten resistanssi
Nimi: LK: SÄHKÖ-OPPI Tarmo Partanen Teoria (Muista hyödyntää sanastoa) 1. Millä nimellä kuvataan sähköisen komponentin (laitteen, johtimen) sähkön kulkua vastustavaa ominaisuutta? 2. Miten resistanssi
Liitetaulukko 1/11. Tutkittujen materiaalien kokonaispitoisuudet KOTIMAINEN MB-JÄTE <1MM SAKSAN MB- JÄTE <1MM POHJAKUONA <10MM
 Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
sivu 1/7 OPETTAJALLE Työn motivaatio
 sivu 1/7 PETTAJALLE Työn motivaatio Työssä saadaan kemiallinen reaktio näkyväksi käyttämällä katalyyttiä. Työssä katalyyttinä toimii veren hemoglobiinin rauta tai yhtä hyvin liuos joka sisältää esimerkiksi
sivu 1/7 PETTAJALLE Työn motivaatio Työssä saadaan kemiallinen reaktio näkyväksi käyttämällä katalyyttiä. Työssä katalyyttinä toimii veren hemoglobiinin rauta tai yhtä hyvin liuos joka sisältää esimerkiksi
Kemia ja ympäristö opintojakso
 1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
Nanoteknologian kokeelliset työt vastauslomake
 vastauslomake 1. Hydrofobiset pinnat Täydennä taulukkoon käyttämäsi nesteet tutkittavat materiaalit. Merkitse taulukkoon huomioita nesteiden käyttäytymisestä tutkittavalla materiaalilla. Esim muodostaa
vastauslomake 1. Hydrofobiset pinnat Täydennä taulukkoon käyttämäsi nesteet tutkittavat materiaalit. Merkitse taulukkoon huomioita nesteiden käyttäytymisestä tutkittavalla materiaalilla. Esim muodostaa
PULLEAT VAAHTOKARKIT
 PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
Lkm keski- maksimi Lkm keski- maksimi. Lkm keski- maksimi Lkm keski- maksimi
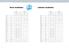 Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
ATOMIN JA IONIN KOKO
 ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
ATOMIN JA IONIN KOKO MATERIAALIT JA TEKNOLOGIA, KE4 Alkuaineen sijainti jaksollisessa järjestelmässä ja koko (atomisäde ja ionisäde) helpottavat ennustamaan kuinka helposti ja miten ko. alkuaine reagoi
Vihreän kemian 12 pääperiaatetta:
 Kemian opettajankoulutusyksikkö Helsingin yliopisto Vihreä laboratorio Opettajan ohje Topias Ikävalko, Oona Kiviluoto, Iines Kuosmanen ja Toni Silvennoinen Vihreä laboratorio KOHDERYHMÄ: Työ soveltuu lukion
Kemian opettajankoulutusyksikkö Helsingin yliopisto Vihreä laboratorio Opettajan ohje Topias Ikävalko, Oona Kiviluoto, Iines Kuosmanen ja Toni Silvennoinen Vihreä laboratorio KOHDERYHMÄ: Työ soveltuu lukion
Ionisidos ja ionihila:
 YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
YHDISTEET KEMIAA KAIK- KIALLA, KE1 Ionisidos ja ionihila: Ionisidos syntyy kun metalli (pienempi elek.neg.) luovuttaa ulkoelektronin tai elektroneja epämetallille (elektronegatiivisempi). Ionisidos on
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
12. Amiinit. Ammoniakki 1 amiini 2 amiini 3 amiini kvarternäärinen ammoniumioni
 12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
SÄHKÖ KÄSITTEENÄ. Yleisnimitys suurelle joukolle ilmiöitä ja käsitteitä:
 FY6 SÄHKÖ Tavoitteet Kurssin tavoitteena on, että opiskelija ymmärtää sähköön liittyviä peruskäsitteitä, tutustuu mittaustekniikkaan osaa tehdä sähköopin perusmittauksia sekä rakentaa ja tutkia yksinkertaisia
FY6 SÄHKÖ Tavoitteet Kurssin tavoitteena on, että opiskelija ymmärtää sähköön liittyviä peruskäsitteitä, tutustuu mittaustekniikkaan osaa tehdä sähköopin perusmittauksia sekä rakentaa ja tutkia yksinkertaisia
KESKIPITKIÄ ANALYYSEJÄ
 KESKIPITKIÄ ANALYYSEJÄ versio 2 Jaakko Lohenoja 2009 Alkusanat Tähän tekstiin on koottu muutama useamman vaiheen sisältävä harjoitustyö, joiden suorittamiseen kuluu yli puoli tuntia. Harjoitustyöt ovat
KESKIPITKIÄ ANALYYSEJÄ versio 2 Jaakko Lohenoja 2009 Alkusanat Tähän tekstiin on koottu muutama useamman vaiheen sisältävä harjoitustyö, joiden suorittamiseen kuluu yli puoli tuntia. Harjoitustyöt ovat
Helsingin yliopiston kemian valintakoe. Keskiviikkona klo Vastausselvitykset: Tehtävät:
 1 elsingin yliopiston kemian valintakoe Keskiviikkona 9.5.2018 klo 10-13. Vastausselvitykset: Tehtävät: 1. Kirjoita seuraavat reaktioyhtälöt olomuotomerkinnöin: a. Sinkkipulveria lisätään kuparisulfaattiliuokseen.
1 elsingin yliopiston kemian valintakoe Keskiviikkona 9.5.2018 klo 10-13. Vastausselvitykset: Tehtävät: 1. Kirjoita seuraavat reaktioyhtälöt olomuotomerkinnöin: a. Sinkkipulveria lisätään kuparisulfaattiliuokseen.
2. Koska f(5) > 8 ja yhdeksän pisteen varaan voidaan virittää kupera viisikulmio, niin f(5) = 9.
 Dimension 1/2018 pulmasivu Ratkaisuja 1. Viiden pisteen joukosta voidaan aina valita neljä, jotka ovat kuperan monikulmion kärkipisteitä, mutta neljästä pisteestä ei muodostu aina kuperaa monikulmiota.
Dimension 1/2018 pulmasivu Ratkaisuja 1. Viiden pisteen joukosta voidaan aina valita neljä, jotka ovat kuperan monikulmion kärkipisteitä, mutta neljästä pisteestä ei muodostu aina kuperaa monikulmiota.
1. (*) Luku 90 voidaan kirjoittaa peräkkäisen luonnollisen luvun avulla esimerkiksi
 Matematiikan pulmasivu Koonnut Martti Heinonen martti.heinonen@luukku.com Vaikeustaso on merkitty tähdillä: yhden tähden (*) tehtävä on helpoin ja kolmen (***) haastavin. 1. (*) Luku 90 voidaan kirjoittaa
Matematiikan pulmasivu Koonnut Martti Heinonen martti.heinonen@luukku.com Vaikeustaso on merkitty tähdillä: yhden tähden (*) tehtävä on helpoin ja kolmen (***) haastavin. 1. (*) Luku 90 voidaan kirjoittaa
Määritelmä, metallisidos, metallihila:
 ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
ALKUAINEET KEMIAA KAIK- KIALLA, KE1 Metalleilla on tyypillisesti 1-3 valenssielektronia. Yksittäisten metalliatomien sitoutuessa toisiinsa jokaisen atomin valenssielektronit tulevat yhteiseen käyttöön
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
KÄYTTÄJÄN OPAS. Yksityiskohtainen käyttöoppaasi. BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten
 KÄYTTÄJÄN OPAS Yksityiskohtainen käyttöoppaasi BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten Jos sinulla on kysymyksiä BYDUREON-valmisteen käytöstä Katso Tavallisia kysymyksiä ja
KÄYTTÄJÄN OPAS Yksityiskohtainen käyttöoppaasi BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten Jos sinulla on kysymyksiä BYDUREON-valmisteen käytöstä Katso Tavallisia kysymyksiä ja
 PROSESSI - JA YM P ÄRI STÖTEKNII K AN OS ASTO I lmi ömalli nnus prosessi metallurgi assa, 201 2 Teema 4 Tehtävänanto ja työselostusohje 21.9.2012 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA
PROSESSI - JA YM P ÄRI STÖTEKNII K AN OS ASTO I lmi ömalli nnus prosessi metallurgi assa, 201 2 Teema 4 Tehtävänanto ja työselostusohje 21.9.2012 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA
BIOMUOVIA TÄRKKELYKSESTÄ
 BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
2.1.3 Pitoisuus. 4.2 Hengitys Tuotetta hengittänyt toimitetaan raittiiseen ilmaan. Tarvittaessa tekohengitystä, viedään lääkärin hoitoon.
 KÄYTTÖTURVALLISUUSTIEDOTE Sivu 1 / 5 1. KEMIKAALIN JA SEN VALMISTAJAN, MAAHANTUOJAN TAI MUUN TOIMINNANHARJOITTAJAN TUNNISTUSTIEDOT 1.1 Kemikaalin tunnistustiedot 1.1.1 Kauppanimi 1.2 Kemikaalin käyttötarkoitus
KÄYTTÖTURVALLISUUSTIEDOTE Sivu 1 / 5 1. KEMIKAALIN JA SEN VALMISTAJAN, MAAHANTUOJAN TAI MUUN TOIMINNANHARJOITTAJAN TUNNISTUSTIEDOT 1.1 Kemikaalin tunnistustiedot 1.1.1 Kauppanimi 1.2 Kemikaalin käyttötarkoitus
KÄYTÖN JÄLKEEN HUOLEHDI, ETTÄ KAIKKI PALAUTETAAN PAIKALLEEN JA LAITTEET SAMMUTETAAN ASIANMUKAISESTI.
 KÄYTÖN JÄLKEEN HUOLEHDI, ETTÄ KAIKKI PALAUTETAAN PAIKALLEEN JA LAITTEET SAMMUTETAAN ASIANMUKAISESTI. Sisällys 1. Perusvalaistus ja valkokangas... 1 2. Tietokone, dokumenttikamera, kevyt äänentoisto, netti
KÄYTÖN JÄLKEEN HUOLEHDI, ETTÄ KAIKKI PALAUTETAAN PAIKALLEEN JA LAITTEET SAMMUTETAAN ASIANMUKAISESTI. Sisällys 1. Perusvalaistus ja valkokangas... 1 2. Tietokone, dokumenttikamera, kevyt äänentoisto, netti
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
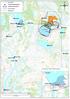 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
17VV VV 01021
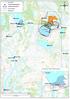 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Kiteet kimpaleiksi (Veli-Matti Ikävalko)
 Kiteet kimpaleiksi (Veli-Matti Ikävalko) VINKKEJÄ OPETTAJALLE: Työ voidaan suorittaa 8 luokalla ionisidosten yhteydessä. Teoria ja kysymysosa osa voidaan suorittaa kotitehtävänä. Kirjallisuudesta etsimiseen
Kiteet kimpaleiksi (Veli-Matti Ikävalko) VINKKEJÄ OPETTAJALLE: Työ voidaan suorittaa 8 luokalla ionisidosten yhteydessä. Teoria ja kysymysosa osa voidaan suorittaa kotitehtävänä. Kirjallisuudesta etsimiseen
Sisällys. Vesi... 9. Avaruus... 65. Voima... 87. Ilma... 45. Oppilaalle... 4 1. Fysiikkaa ja kemiaa oppimaan... 5
 Sisällys Oppilaalle............................... 4 1. Fysiikkaa ja kemiaa oppimaan........ 5 Vesi................................... 9 2. Vesi on ikuinen kiertolainen........... 10 3. Miten saamme puhdasta
Sisällys Oppilaalle............................... 4 1. Fysiikkaa ja kemiaa oppimaan........ 5 Vesi................................... 9 2. Vesi on ikuinen kiertolainen........... 10 3. Miten saamme puhdasta
