Keuhkosyövän uudet lääkkeet
|
|
|
- Toivo Mäkelä
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Keuhkosyövän uudet lääkkeet Jarkko Ahvonen Syöpätautien erikoislääkäri Tampereen yliopistollinen sairaala
2 Sidonnaisuudet Asiantuntijapalkkio Boehringer Ingelheim, Bristol-Myers Squibb, Lilly, MSD, Roche Koulutusmatka Bristol-Myers Squibb, Roche
3 Esityksen sisältö ALK-estäjät seritinibi alektinibi EGFR-estäjät osimertinibi nesitumumabi VEGFR-estäjät nintedanibi ramusirumabi PD-1-estäjät nivolumabi pembrolitsumabi
4 Mikä on kliinisesti merkityksellinen hyöty?
5 Kliinisesti merkityksellinen hyöty
6 Kliinisesti merkityksellinen hyöty
7 Seritinibi Zykadia LDK x potentimpi ALK-estäjä kritsotinibiin verrattuna Kritsotinibista poiketen ei estä MET-kinaasia Annostus 750 mg x 1 po.
8 Seritinibi Faasi I 130 ALK-positiivista maligniteettia 94 %:lla keuhkosyöpä ECOG 0-2 Aikaisempi kritsotinibihoito 68 %:lla MTD 750 mg x 1 Annosta rajoittavat haittavaikutukset: ripuli, oksentelu, Alatnousu, hypofosfatemia 114 potilasta sai seritinibiä 400 mg Shaw et al. N Engl J Med 2014;370:
9 Seritinibi Faasi I ORR 58 % mdor 8,2 kk. mpfs 7,5 kk. Shaw et al. N Engl J Med 2014;370:
10 Alektinibi Alecensa (?) CH/RO x potentimpi ALK-estäjä kritsotinibiin verrattuna Kritsotinibista poiketen ei estä MET- tai ROS1- kinaaseja Erinomainen keskushermostopenetraatio Annostus 600 mg x 2 po.
11 Alektinibi Faasi II (NP28673) ALK-mutaatiopos. potilaita, joiden tauti edennyt kritsotinibin aikana Platinapohjainen solunsalpaajahoito sallittu n = %:lla aivometastaasit Ou et al. J Clin Oncol 2015;34:611-8
12 Alektinibi Faasi II (NP28673) ORR 50 % DCR 79 % mdor 11,2 kk mpfs 8,9 kk Ou et al. J Clin Oncol 2015;34:611-8
13 Alektinibi Faasi II (NP28673) ORR 57 % DCR 83 % mdor 10,3 kk Ou et al. J Clin Oncol 2015;34:611-8
14 Alektinibi Faasi II (NP28673) Haittavaikutukset Ummetus 33 % Uupumus 26 % Perifeerinen turvotus 25 % Yksi hoitoon liitetty kuolema (suoliperforaatio) Ou et al. J Clin Oncol 2015;34:611-8
15 Osimertinibi Tagrisso AZD polven irreversiibeli EGFR:n tyrosiinikinaasi-inhibiittori Suunniteltu kohdistumaan T790M-mutatoituneeseen reseptoriin Ei vaikuta villin tyypin EGFR:iin Penetroituu keskushermostoon Annostus 80 mg x 1 po.
16 Osimertinibi Faasi I/II (AURA) EGFR-mutaatiopos. potilaita, jotka saaneet kliin. hyötyä EGFR-TKI-lääkkeelle, mutta tauti edennyt sen aikana n = 253 T790M-mutaatio 138/222 (62 %) Jänne et al. N Engl J Med 2015;372:
17 Osimertinibi Faasi I/II (AURA) ORR 51 % DCR 84 % mpfs 8,2 kk Jänne et al. N Engl J Med 2015;372:
18 Osimertinibi Faasi I/II (AURA) ORR 61 % DCR 95 % mpfs 9,6 kk Jänne et al. N Engl J Med 2015;372:
19 Osimertinibi Faasi I/II (AURA) ORR 21 % DCR 61 % mpfs 2,8 kk Jänne et al. N Engl J Med 2015;372:
20 Osimertinibi Faasi I/II (AURA) Haittavaikutukset Ripuli 47 % Ihottuma 40 % Pahoinvointi 22 % Väh. ruokahalu 20 % 11 QT-ajan pidentymistä 6 pneumoniittia Jänne et al. N Engl J Med 2015;372:
21 Nesitumumabi Portrazza Monoklonaalinen humaani EGFR-vasta-aine 800 mg vakioannos iv. päivänä 1 ja 8, yhdessä sisplatiini-gemsitabiini-solunsalpaajahoidon kanssa Hoitoa jatketaan taudin etenemiseen tai sietämättömiin haittavaikutuksiin saakka
22 Nesitumumabi Faasi III (SQUIRE) Levinneisyysluokan IV levyepiteelikarsinooma Ei aikaisempaa solunsalpaajahoitoa ECOG 0-2 n = 1093 Sisplatiini-gemsitabiini +/- nesitumumabi (avoin) Thacher et al. Lancet Oncol 2015;16:763-74
23 Nesitumumabi Faasi III (SQUIRE) Thacher et al. Lancet Oncol 2015;16:763-74
24 Nesitumumabi Faasi III (SQUIRE) Thacher et al. Lancet Oncol 2015;16:763-74
25 Nesitumumabi Faasi III (SQUIRE) Thacher et al. Lancet Oncol 2015;16:763-74
26 Nesitumumabi Faasi III (SQUIRE) Nesitumumabihaarassa enemmän Hypomagnesemiaa Ihoreaktioita ja ihottumaa Laskimotukoksia Thacher et al. Lancet Oncol 2015;16:763-74
27 Nintedanibi Vargatef (Ofev keuhkofibroosi-indikaatiossa) BIBF 1120 Multikinaasiestäjä VEGFR 1-3, PDGFR, FGFR 1-3, RET, Flt-3 Annostus: 200 mg x 2 po. syklin päivinä 2-21 yhdessä dosetakselin kanssa (päivänä 1)
28 Reck et al. Lancet Oncol 2014;15: Nintedanibi Faasi III (LUME-Lung 1) Levinneisyysluokan IIIB tai IV NSCLC (kaikki histologiat) Aiempi platinapohjainen solunsalpaajahoito Bevasitsumabi sallittu ECOG 0-1 Poissulkukriteerejä: invaasio suuriin suoniin, kavitaatio, veriyskä, tromboosi, vuoto Dosetakseli +/- nintedanibi (kaksoissokkoutus, lumekontrolloitu)
29 Reck et al. Lancet Oncol 2014;15: Nintedanibi Faasi III (LUME-Lung 1) OS, ITT-populaatio
30 Reck et al. Lancet Oncol 2014;15: Nintedanibi Faasi III (LUME-Lung 1) OS, adenokarsinoomat mos 12.6 vs kk.
31 Reck et al. Lancet Oncol 2014;15: Nintedanibi Faasi III (LUME-Lung 1) OS, adenokarsinoomat, tauti edennyt 9 kk. mos 10.9 vs. 7.9 kk.
32 Reck et al. Lancet Oncol 2014;15: Nintedanibi Faasi III (LUME-Lung 1) Nintedanibiryhmässä oli haittavaikutuksina enemmän Ripulia Maksa-arvojen nousua Pahoinvointia ja oksentelua Ruokahaluttomuutta
33 Ramusirumabi Cyramza Monoklonaalinen humaani VEGFR-2-vasta-aine Bevasitsumabi on VEGF-A:n vasta-aine 10 mg/kg iv. 3 viikon välein yhdessä dosetakselin kanssa
34 Garon et al. Lancet 2014;384: Ramusirumabi Faasi III (REVEL) Levinneisyysluokan IV ei-pienisoluinen keuhkosyöpä Aikaisempi platinapohjainen solunsalpaajahoito ECOG 0-1 n = 1253 Poissulkukriteerejä: invaasio suuriin suoniin, kavitaatio, veriyskä, tuore valtimotapahtuma, korkea verenpaine, maha-suolikanavan verenvuoto Dosetakseli +/- ramusirumabi (lumekontrolloitu)
35 Ramusirumabi Faasi III (REVEL) ORR 23 % vs. 14 % DCR 64 % vs. 53 % Garon et al. Lancet 2014;384:665-73
36 Ramusirumabi Faasi III (REVEL) Ramusirumabiryhmässä lumeryhmää enemmän Kuumeista neutropeniaa Vuotoja (29 % vs. 15 %) Vakavia vuotoja yhtä paljon molemmissa ryhmissä Verenpaineen nousua (11 % vs. 5 %) Garon et al. Lancet 2014;384:665-73
37 Nivolumabi Opdivo Monoklonaalinen humaani PD-1-vasta-aine 3 mg/kg iv. 2 viikon välein taudin etenemiseen tai sietämättömiin haittavaikutuksiin saakka Kaksi faasin III tutkimusta, jossa nivolumabia verrattu dosetakseliin platinapohjaisen solunsalpaajahoidon jälkeen ECOG-luokan 0-1 potilailla CheckMate 017 (levyepiteelikarsinooma) CheckMate 057 (ei-levyepiteelikarsinooma)
38 Nivolumabi Faasi III (CheckMate 017) Brahmer et al. N Engl J Med 2015;373:123-35
39 Nivolumabi Faasi III (CheckMate 017) Brahmer et al. N Engl J Med 2015;373:123-35
40 Nivolumabi Faasi III (CheckMate 057) Borghaei et al. N Engl J Med 2015;373:
41 Nivolumabi Faasi III (CheckMate 057) Borghaei et al. N Engl J Med 2015;373:
42 Pembrolitsumabi Keytruda Monoklonaalinen humanisoitu PD-1-vasta-aine Annostus 2 mg/kg(?) iv. 3 viikon välein
43 Herbst et al. Lancet (online) Pembrolitsumabi Faasi II/III (KEYNOTE-010) Levinneisyysluokan IV ei-pienisoluinen keuhkosyöpä (kaikki histologiat) 1-2 aiempaa hoitolinjaa ECOG 0-1 PD-L1-ekspressio vähintään 1 % kasvainsoluista n = 1034 Pembrolitsumabi 2 mg/kg vs. 10 mg/kg vs. dosetakseli
44 Pembrolitsumabi Faasi II/III (KEYNOTE-010) PD-L1 1 % PD-L1 50 % Pembro 2 mg/kg Pembro 10 mg/kg Dosetakseli Pembro 2 mg/kg Pembro 10 mg/kg Dosetakseli mos 10.4 kk. HR 0.71 p= kk. HR 0.61 p< kk. mos 14.9 kk. HR 0.54 p= kk. HR 0.50 p< kk. mpfs 3.9 kk. HR 0.88 p= kk. HR 0.79 p= kk. mpfs 5.0 kk. HR 0.59 p= kk. HR 0.59 p< kk. ORR 18 % p= % p= % ORR 30 % p< % p< % Herbst et al. Lancet (online)
45 Herbst et al. Lancet (online) Pembrolitsumabi Faasi II/III (KEYNOTE-010)
46 Herbst et al. Lancet (online) Pembrolitsumabi Faasi II/III (KEYNOTE-010)
47 Herbst et al. Lancet (online) Pembrolitsumabi Faasi II/III (KEYNOTE-010)
48 Yhteenveto mos-ero HR Hinta /kk.* 80 kg potilas Nesitumumabi 1.6 kk. 0.84? Nintedanibi 3.0 kk.** 0.75? Ramusirumabi 1.4 kk Nivolumabi (levyepit) Nivolumabi (adeno) 3.2 kk kk Pembrolitsumabi 6.7 kk *) Terveysportti hintatiedot **) Adenokarsinooma, progressio 9 kk.
JULKAISUSARJA 6/2016 NIVOLUMABI EI- PIENISOLUISEN KEUHKO- SYÖVÄN HOIDOSSA
 JULKAISUSARJA 6/2016 NIVOLUMABI EI- PIENISOLUISEN KEUHKO- SYÖVÄN HOIDOSSA NIVOLUMABI EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 6/2016 Lääkealan turvallisuus-
JULKAISUSARJA 6/2016 NIVOLUMABI EI- PIENISOLUISEN KEUHKO- SYÖVÄN HOIDOSSA NIVOLUMABI EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 6/2016 Lääkealan turvallisuus-
MITÄ UUTTA SARKOOMIEN HOIDOSSA?
 MITÄ UUTTA SARKOOMIEN HOIDOSSA? O S A S T O N Y L I L Ä Ä K Ä R I M A I J A T A R K K A N E N H Y K S S Y Ö P Ä K E S K U S LUENNON SISÄLTÖ luu- ja pehmytkudossarkoomat ei pediatrisia tutkimuksia ei gynekologisia
MITÄ UUTTA SARKOOMIEN HOIDOSSA? O S A S T O N Y L I L Ä Ä K Ä R I M A I J A T A R K K A N E N H Y K S S Y Ö P Ä K E S K U S LUENNON SISÄLTÖ luu- ja pehmytkudossarkoomat ei pediatrisia tutkimuksia ei gynekologisia
OPDIVO (nivolumabi) Immuunivälitteisten haittavaikutusten hoito-opas. Infuusiokonsentraatti, liuosta varten. Käyttöaiheet Melanooma 1
 OPDIVO (nivolumabi) Infuusiokonsentraatti, liuosta varten Immuunivälitteisten haittavaikutusten hoito-opas Käyttöaiheet Melanooma 1 OPDIVO (nivolumabi) monoterapiana on tarkoitettu aikuisten edenneen melanooman
OPDIVO (nivolumabi) Infuusiokonsentraatti, liuosta varten Immuunivälitteisten haittavaikutusten hoito-opas Käyttöaiheet Melanooma 1 OPDIVO (nivolumabi) monoterapiana on tarkoitettu aikuisten edenneen melanooman
INPULSIS -ON: Nintedanibin pitkäaikainen turvallisuus idiopaattista keuhkofibroosia (IPF) sairastavilla potilailla
 INPULSIS -ON: Nintedanibin pitkäaikainen turvallisuus idiopaattista keuhkofibroosia (IPF) sairastavilla potilailla Tämä on yhteenveto kliinisestä tutkimuksesta IPF:ää sairastavilla potilailla. Se on kirjoitettu
INPULSIS -ON: Nintedanibin pitkäaikainen turvallisuus idiopaattista keuhkofibroosia (IPF) sairastavilla potilailla Tämä on yhteenveto kliinisestä tutkimuksesta IPF:ää sairastavilla potilailla. Se on kirjoitettu
OPDIVO (nivolumabi) Infuusiokonsentraatti, liuosta varten. Immuunivälitteisten haittavaikutusten hoito-opas
 Immuunivälitteisten haittavaikutusten hoito-opas Käyttöaiheet Melanooma 1 OPDIVO monoterapiana tai yhdistelmähoitona ipilimumabin kanssa on tarkoitettu aikuisten edenneen melanooman hoitoon (jota ei voida
Immuunivälitteisten haittavaikutusten hoito-opas Käyttöaiheet Melanooma 1 OPDIVO monoterapiana tai yhdistelmähoitona ipilimumabin kanssa on tarkoitettu aikuisten edenneen melanooman hoitoon (jota ei voida
keuhkosyövän uusista hoitotutkimuksista Jussi Koivunen, el dos OYS/Syöpätaudit
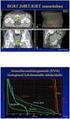 keuhkosyövän uusista hoitotutkimuksista Jussi Koivunen, el dos OYS/Syöpätaudit 30.8.2014 Sidonnaisuudet Taloudelliset riippuvuudet: Konsultointi: - Tutkimusrahoitus: - Osakkeet: - Honorariat: Eli Lilly,
keuhkosyövän uusista hoitotutkimuksista Jussi Koivunen, el dos OYS/Syöpätaudit 30.8.2014 Sidonnaisuudet Taloudelliset riippuvuudet: Konsultointi: - Tutkimusrahoitus: - Osakkeet: - Honorariat: Eli Lilly,
Levinneen keuhkosyövän nykyaikainen lääkehoito mitä totunnaisten solunsalpaajien lisäksi?
 KATSAUS TEEMA Jussi Koivunen, Aija Knuuttila ja Pekka Mali Levinneen keuhkosyövän nykyaikainen lääkehoito mitä totunnaisten solunsalpaajien lisäksi? Ei-pienisoluisen keuhkosyövän hoitoon on tullut viime
KATSAUS TEEMA Jussi Koivunen, Aija Knuuttila ja Pekka Mali Levinneen keuhkosyövän nykyaikainen lääkehoito mitä totunnaisten solunsalpaajien lisäksi? Ei-pienisoluisen keuhkosyövän hoitoon on tullut viime
Molekyylidiagnostiikka keuhkosyövän hoidossa. Jussi Koivunen, el, dos. Syöpätautien ja sädehoidon klinikka/oys
 Molekyylidiagnostiikka keuhkosyövän hoidossa Jussi Koivunen, el, dos. Syöpätautien ja sädehoidon klinikka/oys Sidonnaisuudet Taloudelliset riippuvuudet: Konsultointi: - Tutkimusrahoitus: - Honorariat:
Molekyylidiagnostiikka keuhkosyövän hoidossa Jussi Koivunen, el, dos. Syöpätautien ja sädehoidon klinikka/oys Sidonnaisuudet Taloudelliset riippuvuudet: Konsultointi: - Tutkimusrahoitus: - Honorariat:
KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman hoitoon.
 KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
Neuroendokriinisten syöpien lääkehoito
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
Page 1 of 5 JULKAISTU NUMEROSSA 3/2015 TEEMAT Neuroendokriinisten syöpien lääkehoito Maija Tarkkanen / Kirjoitettu 16.6.2015 / Julkaistu 13.11.2015 Neuroendokriinisten (NE) syöpien ilmaantuvuus lisääntyy,
JULKAISUSARJA 13/2016 PEMBROLITSUMABI PD-L1-POSITIIVISEN EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA. Arviointikooste
 JULKAISUSARJA 13/2016 PEMBROLITSUMABI PD-L1-POSITIIVISEN EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Arviointikooste PEMBROLITSUMABI PD-L1- POSITIIVISEN EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Fimea kehittää,
JULKAISUSARJA 13/2016 PEMBROLITSUMABI PD-L1-POSITIIVISEN EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Arviointikooste PEMBROLITSUMABI PD-L1- POSITIIVISEN EI-PIENISOLUISEN KEUHKOSYÖVÄN HOIDOSSA Fimea kehittää,
Bevasitsumabi on rekombinantti humanisoitu monoklonaalinen vasta-aine, joka on tuotettu kiinankääpiöhamsterin munasarjasoluissa DNA-tekniikalla.
 1. LÄÄKEVALMISTEEN NIMI Avastin 25 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 25 mg bevasitsumabia. Jokainen 4 ml:n injektiopullo sisältää
1. LÄÄKEVALMISTEEN NIMI Avastin 25 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 25 mg bevasitsumabia. Jokainen 4 ml:n injektiopullo sisältää
JULKISEN YHTEENVEDON OSAT. Yleistä tietoa taudin epidemiologiasta
 OSA VI.2 Osa VI.2.1 JULKISEN YHTEENVEDON OSAT Yleistä tietoa taudin epidemiologiasta Maailmanlaajuisesti ajatellen valtaosa keuhkosyövistä on ei-pienisoluista keuhkosyöpää (NSCLC). Tutkimusten mukaan taudin
OSA VI.2 Osa VI.2.1 JULKISEN YHTEENVEDON OSAT Yleistä tietoa taudin epidemiologiasta Maailmanlaajuisesti ajatellen valtaosa keuhkosyövistä on ei-pienisoluista keuhkosyöpää (NSCLC). Tutkimusten mukaan taudin
Uutta lääkkeistä: Palbosiklibi
 Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
Page 1 of 5 JULKAISTU NUMEROSSA 1/2017 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Palbosiklibi Annikka Kalliokoski / Kirjoitettu 25.1.2017 / Julkaistu Ibrance 75 mg, 100 mg, 125 mg kovat kapselit, Pfizer Limited
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
Opas terveydenhuollon ammattilaisille. Kadcyla (trastutsumabiemtansiini)
 Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto
 EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
Mitä tutkimus koskee? Miksi tutkimus tehtiin? Mitä lääkkeitä tutkittiin? BI
 Tämä on yhteenveto kliinisestä tutkimuksesta idiopaattista keuhkofibroosia, harvinaista keuhkosairautta, sairastavilla potilailla. Se on kirjoitettu tavalliselle lukijalle ja helposti ymmärrettävää kieltä
Tämä on yhteenveto kliinisestä tutkimuksesta idiopaattista keuhkofibroosia, harvinaista keuhkosairautta, sairastavilla potilailla. Se on kirjoitettu tavalliselle lukijalle ja helposti ymmärrettävää kieltä
Immuno-onkologiaa. Tiina Tuomisto-Huttunen, LT, eval KYS/Syöpäkeskus
 Immuno-onkologiaa Tiina Tuomisto-Huttunen, LT, eval KYS/Syöpäkeskus Sisältö tulehdus syövän synnyssä epäspesifi immunoterapia checkpoint inhibiittorit - vaikutusmekanismi - esimerkkejä eri syöpien hoidossa
Immuno-onkologiaa Tiina Tuomisto-Huttunen, LT, eval KYS/Syöpäkeskus Sisältö tulehdus syövän synnyssä epäspesifi immunoterapia checkpoint inhibiittorit - vaikutusmekanismi - esimerkkejä eri syöpien hoidossa
Uutta melanoomasta. Pia Vihinen TYKS/Syöpäklinikka. Tutkimukset kun epäilet melanooman leviämistä
 Uutta melanoomasta Pia Vihinen TYKS/Syöpäklinikka Tutkimukset kun epäilet melanooman leviämistä Vartalon TT tutkimus tai PET-TT Verikokeet; Hb, maksa-arvot, krea Korkea LDH huonon ennusteen merkki PAD:
Uutta melanoomasta Pia Vihinen TYKS/Syöpäklinikka Tutkimukset kun epäilet melanooman leviämistä Vartalon TT tutkimus tai PET-TT Verikokeet; Hb, maksa-arvot, krea Korkea LDH huonon ennusteen merkki PAD:
Julkisen yhteenvedon osiot
 Pemetrexed STADA 25 mg/ml infuusiokonsentraatti, liuosta varten 7.5.2015, versio V1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Pemetrexed STADA 25 mg/ml infuusiokonsentraatti, liuosta varten 7.5.2015, versio V1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
JULKAISUSARJA 4/2016 PD-1- JA PD-L1-VASTA-AINEET. Uudet mahdolliset käyttöaiheet ja käyttöönoton kustannukset lähivuosina
 JULKAISUSARJA 4/2016 PD-1- JA PD-L1-VASTA-AINEET Uudet mahdolliset käyttöaiheet ja käyttöönoton kustannukset lähivuosina PD-1- JA PD-L1-VASTA-AINEET. UUDET MAHDOLLISET KÄYTTÖAIHEET JA KÄYTTÖÖNOTON KUSTANNUKSET
JULKAISUSARJA 4/2016 PD-1- JA PD-L1-VASTA-AINEET Uudet mahdolliset käyttöaiheet ja käyttöönoton kustannukset lähivuosina PD-1- JA PD-L1-VASTA-AINEET. UUDET MAHDOLLISET KÄYTTÖAIHEET JA KÄYTTÖÖNOTON KUSTANNUKSET
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI CIAMBRA 100 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää pemetreksedidinatriumhemipentahydraattia
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI CIAMBRA 100 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää pemetreksedidinatriumhemipentahydraattia
Levinneen suolistosyövän hoito
 Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Levinneen suolistosyövän hoito Yhteyshoitajakoulutus 29.9. LT ylilääkäri Pirkanmaan Syöpäyhdistys Uusien tapausten lukumäärät, yleisimpien syöpien mennyt ja ennustettu trendi, miehet Uusien tapausten lukumäärät,
Ruokatorvisyöpä. Ruokatorvisyöpä 2013. Ruokatorven syövän yleisyyden alueelliset vaihtelut. Ruokatorven levyepiteelisyövän etiologia
 Ruokatorvisyöpä Ruokatorvisyöpä 2013 Eero Sihvo Dos KSKS Nielemisvaikeus Suomessa vajaa 300/v 14. yleisin ca >20. yleisin ca 2 histologista päätyyppiä Distaalinen ruokatorvi 40,0 35,0 30,0 25,0 20,0 15,0
Ruokatorvisyöpä Ruokatorvisyöpä 2013 Eero Sihvo Dos KSKS Nielemisvaikeus Suomessa vajaa 300/v 14. yleisin ca >20. yleisin ca 2 histologista päätyyppiä Distaalinen ruokatorvi 40,0 35,0 30,0 25,0 20,0 15,0
Yksi kalvopäällysteinen tabletti sisältää 150 mg erlotinibia (erlotinibihydrokloridina).
 1. LÄÄKEVALMISTEEN NIMI Tarceva 15 mg kalvopäällysteiset tabletit. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 15 mg erlotinibia (erlotinibihydrokloridina). Apuaineet:
1. LÄÄKEVALMISTEEN NIMI Tarceva 15 mg kalvopäällysteiset tabletit. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 15 mg erlotinibia (erlotinibihydrokloridina). Apuaineet:
Opdivo 10 mg/ml infuusiokonsentraatti, liuosta varten, Bristol-Myers Squibb Pharma EEIG.
 Page 1 of 7 JULKAISTU NUMEROSSA 3/2015 UUTTA LÄÄKKEISTÄ Nivolumabi Päivi Ruokoniemi, Olli Tenhunen / Kirjoitettu 29.9.2015 / Julkaistu 2.10.2015 Opdivo 10 mg/ml infuusiokonsentraatti, liuosta varten, Bristol-Myers
Page 1 of 7 JULKAISTU NUMEROSSA 3/2015 UUTTA LÄÄKKEISTÄ Nivolumabi Päivi Ruokoniemi, Olli Tenhunen / Kirjoitettu 29.9.2015 / Julkaistu 2.10.2015 Opdivo 10 mg/ml infuusiokonsentraatti, liuosta varten, Bristol-Myers
Pienisoluisen keuhkosyövän (SCLC) hoito. Jussi Koivunen, el, dos Syöpätau<en ja sädehoidon klinikka OYS/OY
 Pienisoluisen keuhkosyövän (SCLC) hoito Jussi Koivunen, el, dos Syöpätau
Pienisoluisen keuhkosyövän (SCLC) hoito Jussi Koivunen, el, dos Syöpätau
Aripiprazole Sandoz (aripipratsoli)
 Aripiprazole Sandoz (aripipratsoli) Esite potilaille/heistä huolehtiville henkilöille Tämä esite sisältää tärkeitä turvallisuustietoja, joihin sinun on tutustuttava ennen aripipratsolihoidon aloittamista
Aripiprazole Sandoz (aripipratsoli) Esite potilaille/heistä huolehtiville henkilöille Tämä esite sisältää tärkeitä turvallisuustietoja, joihin sinun on tutustuttava ennen aripipratsolihoidon aloittamista
Uutta lääkkeistä: Vemurafenibi
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Vemurafenibi Kristiina Airola / Julkaistu 28.9.2012. Zelboraf 240 mg kalvopäällysteinen tabletti, Roche Registration Ltd. Zelboraf-valmistetta
Kissa: Leikkauksen jälkeisen kivun lievitys kohdun ja munasarjojen poistoleikkauksen sekä pienten pehmytkudoskirurgisten toimenpiteiden jälkeen.
 1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
JULKAISUSARJA 7/2017 ATETSOLITSUMABI EI- PIENISOLUISEN KEUHKOSYÖ- VÄN TOISEN LINJAN HOIDOS- SA. Uusien sairaalalääkkeiden nopea arviointi
 JULKAISUSARJA 7/2017 ATETSOLITSUMABI EI- PIENISOLUISEN KEUHKOSYÖ- VÄN TOISEN LINJAN HOIDOS- SA Uusien sairaalalääkkeiden nopea arviointi ATETSOLITSUMABI EI- PIENISOLUISEN KEUHKOSYÖVÄN TOISEN LINJAN HOIDOSSA
JULKAISUSARJA 7/2017 ATETSOLITSUMABI EI- PIENISOLUISEN KEUHKOSYÖ- VÄN TOISEN LINJAN HOIDOS- SA Uusien sairaalalääkkeiden nopea arviointi ATETSOLITSUMABI EI- PIENISOLUISEN KEUHKOSYÖVÄN TOISEN LINJAN HOIDOSSA
Follikulaarisen lymfooman nykyhoito
 Follikulaarisen lymfooman nykyhoito Follikulaariseen lymfoomaan sairastui Suomen syöpärekisterin tuoreimpien tilastojen mukaan vuonna 2014 kaikkiaan 228 potilasta. 1 Tämä tarkoittaa noin viidesosaa kaikista
Follikulaarisen lymfooman nykyhoito Follikulaariseen lymfoomaan sairastui Suomen syöpärekisterin tuoreimpien tilastojen mukaan vuonna 2014 kaikkiaan 228 potilasta. 1 Tämä tarkoittaa noin viidesosaa kaikista
GIOTRIF (afatinibi) Monoterapiana paikallisesti edennyttä tai etäpesäkkeistä ei-pienisoluista keuhkosyöpää sairastaville aikuispotilaille
 GIOTRIF (afatinibi) Monoterapiana paikallisesti edennyttä tai etäpesäkkeistä ei-pienisoluista keuhkosyöpää sairastaville aikuispotilaille Joita ei ole aiemmin hoidettu epidermaalisen kasvutekijän reseptorin
GIOTRIF (afatinibi) Monoterapiana paikallisesti edennyttä tai etäpesäkkeistä ei-pienisoluista keuhkosyöpää sairastaville aikuispotilaille Joita ei ole aiemmin hoidettu epidermaalisen kasvutekijän reseptorin
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin 38/46 A. Valmisteyhteenveto 4.1 Käyttöaiheet [tällä hetkellä hyväksytyt käyttöaiheet on poistettava ja korvattava seuraavilla]
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin 38/46 A. Valmisteyhteenveto 4.1 Käyttöaiheet [tällä hetkellä hyväksytyt käyttöaiheet on poistettava ja korvattava seuraavilla]
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
Arviointien hyödyntäminen käytännön työssä Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue
 Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Arviointien hyödyntäminen käytännön työssä 19.9.2018 Ayl Katariina Klintrup Syöpätautien ja hematologian vastuualue 1 Uuden lääkkeen käyttöönotto Alle 35 000? Menettelytapa alle 35 000 kustannuksissa?
Potilaan päiväkirja. Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi
 Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
JULKAISUSARJA 5/2016 NIVOLUMABI EDENNEEN MUNUAISSYÖVÄN HOIDOSSA
 JULKAISUSARJA 5/2016 NIVOLUMABI EDENNEEN MUNUAISSYÖVÄN HOIDOSSA NIVOLUMABI EDENNEEN MUNUAISSYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 5/2016 Lääkealan turvallisuus- ja kehittämiskeskus
JULKAISUSARJA 5/2016 NIVOLUMABI EDENNEEN MUNUAISSYÖVÄN HOIDOSSA NIVOLUMABI EDENNEEN MUNUAISSYÖVÄN HOIDOSSA Fimea kehittää, arvioi ja informoi -julkaisusarja 5/2016 Lääkealan turvallisuus- ja kehittämiskeskus
Syöpäkeskuksen tutkimusmahdollisuudet Heikki Minn
 Syöpäkeskuksen tutkimusmahdollisuudet Heikki Minn Sidonnaisuudet Konsulttina ja/tai kliinisenä tutkijana seuraavissa lääketieteellistä toimintaa harjoittavissa yrityksissä viimeisen 3-v aikana: Amgen,
Syöpäkeskuksen tutkimusmahdollisuudet Heikki Minn Sidonnaisuudet Konsulttina ja/tai kliinisenä tutkijana seuraavissa lääketieteellistä toimintaa harjoittavissa yrityksissä viimeisen 3-v aikana: Amgen,
RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA
 RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA Johanna Mattson dosentti ylilääkäri, vs. toimialajohtaja HYKS Syöpäkeskus 28.11.2016 1 RINTASYÖPÄ SUOMESSA 5008 uutta tapausta vuonna 2014 Paikallinen rintasyöpä
RINNAN NGS PANEELIEN KÄYTTÖ ONKOLOGIN NÄKÖKULMA Johanna Mattson dosentti ylilääkäri, vs. toimialajohtaja HYKS Syöpäkeskus 28.11.2016 1 RINTASYÖPÄ SUOMESSA 5008 uutta tapausta vuonna 2014 Paikallinen rintasyöpä
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Aripiprazole Accord (aripipratsoli)
 Aripiprazole Accord (aripipratsoli) Esite terveydenhuoltohenkilöstölle Aripiprazole Accord (aripipratsoli) on tarkoitettu keskivaikean tai vaikean maniavaiheen enintään 12 viikkoa kestävään hoitoon 13
Aripiprazole Accord (aripipratsoli) Esite terveydenhuoltohenkilöstölle Aripiprazole Accord (aripipratsoli) on tarkoitettu keskivaikean tai vaikean maniavaiheen enintään 12 viikkoa kestävään hoitoon 13
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP
 Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
Miten syövän hoidon hyötyä mitataan? Olli Tenhunen LT FIMEA/PPSHP Disclosures No interests in pharmaceutical industry Member of EMA Scientific Advice Working Party, Oncology Working Party, Committee for
EUROOPAN LÄÄKEVIRASTON TIETEELLISET JOHTOPÄÄTÖKSET JA PERUSTEET VALMISTEYHTEENVEDON, MYYNTIPÄÄLLYSMERKINTÖJEN JA PAKKAUSSELOSTEEN MUUTTAMISELLE
 LIITE II EUROOPAN LÄÄKEVIRASTON TIETEELLISET JOHTOPÄÄTÖKSET JA PERUSTEET VALMISTEYHTEENVEDON, MYYNTIPÄÄLLYSMERKINTÖJEN JA PAKKAUSSELOSTEEN MUUTTAMISELLE 11 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä
LIITE II EUROOPAN LÄÄKEVIRASTON TIETEELLISET JOHTOPÄÄTÖKSET JA PERUSTEET VALMISTEYHTEENVEDON, MYYNTIPÄÄLLYSMERKINTÖJEN JA PAKKAUSSELOSTEEN MUUTTAMISELLE 11 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä
Yksi kalvopäällysteinen tabletti sisältää 150 mg erlotinibia (erlotinibihydrokloridina).
 1. LÄÄKEVALMISTEEN NIMI Tarceva 15 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 15 mg erlotinibia (erlotinibihydrokloridina). Apuaineet,
1. LÄÄKEVALMISTEEN NIMI Tarceva 15 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 15 mg erlotinibia (erlotinibihydrokloridina). Apuaineet,
Julkisen yhteenvedon osiot
 Erlotinib STADA 25 mg, 100 mg ja 150 mg kalvopäällysteiset tabletit 17.3.2017, versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Erlotinib STADA 25 mg, 100 mg ja 150 mg kalvopäällysteiset tabletit 17.3.2017, versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Vectibix (panitumumabi) levinneessä suolistosyövässä
 Vectibix (panitumumabi) levinneessä suolistosyövässä Opas potilaan ohjaukseen lääkärille ja hoitajalle HOITOHENKILÖKUNNALLE Ensikäynnille Sisältö Mikä lääke Vectibix on? Miten se annostellaan? Odotettavissa
Vectibix (panitumumabi) levinneessä suolistosyövässä Opas potilaan ohjaukseen lääkärille ja hoitajalle HOITOHENKILÖKUNNALLE Ensikäynnille Sisältö Mikä lääke Vectibix on? Miten se annostellaan? Odotettavissa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml konsentraattia sisältää 20 mg dosetakselia. Yksi 1 ml:n
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml konsentraattia sisältää 20 mg dosetakselia. Yksi 1 ml:n
Eturauhassyövän uudet lääkehoidot
 Eturauhassyövän uudet lääkehoidot 24.04.2015 Petteri Hervonen, LT, Syöpätautien erikoislääkäri Docrates Syöpäsairaala, TAYS Yleistä Eturauhassyöpä on miesten yleisin syöpätyyppi Lähes 5000 uutta diagnoosia/vuosi
Eturauhassyövän uudet lääkehoidot 24.04.2015 Petteri Hervonen, LT, Syöpätautien erikoislääkäri Docrates Syöpäsairaala, TAYS Yleistä Eturauhassyöpä on miesten yleisin syöpätyyppi Lähes 5000 uutta diagnoosia/vuosi
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
Yksi kerta-annosinjektiopullo sisältää vedetöntä etanolia 182 mg/ml (23% v/v). Täydellinen apuaineluettelo, ks. kohta 6.1
 VALMISTEYHTEENVETO 1 LÄÄKEVALMISTEEN NIMI Docetaxel Hospira 10 mg/ml infuusiokonsentraatti, liuosta varten 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 10 mg
VALMISTEYHTEENVETO 1 LÄÄKEVALMISTEEN NIMI Docetaxel Hospira 10 mg/ml infuusiokonsentraatti, liuosta varten 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 10 mg
JULKAISUSARJA 4/2015 RAMUSIRUMABI EDENNEEN MAHASYÖVÄN JA RUOKATORVI- MAHALAUKKURAJAN ADENOKARSINOOMAN HOIDOSSA
 JULKAISUSARJA 4/2015 RAMUSIRUMABI EDENNEEN MAHASYÖVÄN JA RUOKATORVI- MAHALAUKKURAJAN ADENOKARSINOOMAN HOIDOSSA RAMUSIRUMABI EDENNEEN MAHASYÖVÄN JA RUOKATORVI- MAHALAUKKURAJAN ADENOKARSINOOMAN HOIDOSSA
JULKAISUSARJA 4/2015 RAMUSIRUMABI EDENNEEN MAHASYÖVÄN JA RUOKATORVI- MAHALAUKKURAJAN ADENOKARSINOOMAN HOIDOSSA RAMUSIRUMABI EDENNEEN MAHASYÖVÄN JA RUOKATORVI- MAHALAUKKURAJAN ADENOKARSINOOMAN HOIDOSSA
Eläimiä koskevat erityiset varotoimet Jos haittavaikutuksia ilmenee, tulee hoito keskeyttää ja ottaa yhteys eläinlääkäriin.
 1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
Gefitinibi ei-pienisoluisen keuhkosyövän täsmähoitona?
 Katsaus AIJA KNUUTTILA, EEVA-MAIJA KARJALAINEN, ANNAMARI ROUHOS JA PEKKA MALI Gefitinibi ei-pienisoluisen keuhkosyövän täsmähoitona? Levinneeseen tai paikallisesti edenneeseen, leikkaukseen soveltumattomaan,
Katsaus AIJA KNUUTTILA, EEVA-MAIJA KARJALAINEN, ANNAMARI ROUHOS JA PEKKA MALI Gefitinibi ei-pienisoluisen keuhkosyövän täsmähoitona? Levinneeseen tai paikallisesti edenneeseen, leikkaukseen soveltumattomaan,
Lääkkeet muistisairauksissa
 Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
Lääkkeet muistisairauksissa Muistihoitajat 27.4.2016 Vanheneminen muuttaa lääkkeiden farmakokinetiikkaa Lääkeaineen vaiheet elimistössä: Imeytyminen: syljen eritys vähenee, mahalaukun ph nousee, maha-suolikanavan
B. PAKKAUSSELOSTE 45
 B. PAKKAUSSELOSTE 45 PAKKAUSSELOSTE Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen ottamisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos Sinulla on lisäkysymyksiä, käänny lääkärisi
B. PAKKAUSSELOSTE 45 PAKKAUSSELOSTE Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen ottamisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos Sinulla on lisäkysymyksiä, käänny lääkärisi
MRI ja kohdunrunkosyövän leikkauksen suunnittelu 1 GKS. 26.09.2013 Helsinki. Arto Leminen
 MRI ja kohdunrunkosyövän leikkauksen suunnittelu 1 GKS 26.09.2013 Helsinki Arto Leminen 2 Yleisimmät syövät Suomessa 2011 3 Naiset N Miehet N Rinta 4865 Eturauhanen 4719 Paksusuoli 874 Keuhko + ht 1570
MRI ja kohdunrunkosyövän leikkauksen suunnittelu 1 GKS 26.09.2013 Helsinki Arto Leminen 2 Yleisimmät syövät Suomessa 2011 3 Naiset N Miehet N Rinta 4865 Eturauhanen 4719 Paksusuoli 874 Keuhko + ht 1570
Eteisvärinän antikoagulaatiohoito. Seija Paakkinen LL, sisätautien ja kardiologian erikoislääkäri Kardiologian alueylilääkäri PHHYKY
 Eteisvärinän antikoagulaatiohoito Seija Paakkinen LL, sisätautien ja kardiologian erikoislääkäri Kardiologian alueylilääkäri PHHYKY Sidonnaisuudet Tukea esimiehen määräämiin koulutuksiin Bayer, Boehringer
Eteisvärinän antikoagulaatiohoito Seija Paakkinen LL, sisätautien ja kardiologian erikoislääkäri Kardiologian alueylilääkäri PHHYKY Sidonnaisuudet Tukea esimiehen määräämiin koulutuksiin Bayer, Boehringer
Miten tehostan sepelvaltimotaudin lääkehoitoa?
 Miten tehostan sepelvaltimotaudin lääkehoitoa? Dosentti, kardiologi Erkki Ilveskoski Yleislääkäripäivät 27.11.2015 1 Sidonnaisuudet Luennoitsija ja/tai muut asiantuntijatehtävät St. Jude Medical, Novartis,
Miten tehostan sepelvaltimotaudin lääkehoitoa? Dosentti, kardiologi Erkki Ilveskoski Yleislääkäripäivät 27.11.2015 1 Sidonnaisuudet Luennoitsija ja/tai muut asiantuntijatehtävät St. Jude Medical, Novartis,
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen
 Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Tärkeä lääketurvatiedote terveydenhuollon ammattilaisille. RAS-villityyppistatuksen (KRAS- ja NRAS-statuksen eksoneissa 2, 3 ja 4) varmistaminen on tärkeää ennen Erbitux (setuksimabi) -hoidon aloittamista
Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten
 1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva 80 mg konsentraatin kerta-annosinjektiopullo sisältää
1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva 80 mg konsentraatin kerta-annosinjektiopullo sisältää
Orionilainen lääketutkimus ja -kehitys. 13.5.2014 Mikko Kuoppamäki, neurologian dosentti Lääketieteellisen yksikön päällikkö
 Orionilainen lääketutkimus ja -kehitys 13.5.2014 Mikko Kuoppamäki, neurologian dosentti Lääketieteellisen yksikön päällikkö Maailman paras T&K vuonna 2017 tavoite vuodesta 2008 Paras rakenne Paras johtajuus
Orionilainen lääketutkimus ja -kehitys 13.5.2014 Mikko Kuoppamäki, neurologian dosentti Lääketieteellisen yksikön päällikkö Maailman paras T&K vuonna 2017 tavoite vuodesta 2008 Paras rakenne Paras johtajuus
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Vectibix 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml konsentraattia sisältää 20 mg panitumumabia.
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Vectibix 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml konsentraattia sisältää 20 mg panitumumabia.
Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku
 1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
1 Mitä uutta eturauhassyövän sädehoidosta? Mauri Kouri HUS Syöpätautien klinikka Onkologiapäivät 31.8.13 Turku 2 ASCO GU 2013 Radikaali prostatektomian jälkeinen sädehoito ARO 92-02 / AUO AP 09/95 10v
VASTA-AIHEET (kts. tarkemmin Terveysportti Duodecim lääketietokanta )
 MS-TAUDIN IMMUNOMODULOIVA LÄÄKITYS Lähteenä Käypähoito-suositus (3.12.2014, kohdennettu päivitys 16.12.2015). MS-tauti käypähoito suositus Lisäksi hoitojen toteutuksessa ja seurannassa huomioitava sairaalakohtaiset
MS-TAUDIN IMMUNOMODULOIVA LÄÄKITYS Lähteenä Käypähoito-suositus (3.12.2014, kohdennettu päivitys 16.12.2015). MS-tauti käypähoito suositus Lisäksi hoitojen toteutuksessa ja seurannassa huomioitava sairaalakohtaiset
Yleisimmät idiopaattiset interstitiaalipneumoniat ja tavalliset keuhkovauriot - avainasemassa moniammatillisuus
 Yleisimmät idiopaattiset interstitiaalipneumoniat ja tavalliset keuhkovauriot - avainasemassa moniammatillisuus 12.11.2015 IAP Tampere Airi Jartti Elisa Lappi-Blanco Sidonnaisuudet Luentopalkkioita Oy
Yleisimmät idiopaattiset interstitiaalipneumoniat ja tavalliset keuhkovauriot - avainasemassa moniammatillisuus 12.11.2015 IAP Tampere Airi Jartti Elisa Lappi-Blanco Sidonnaisuudet Luentopalkkioita Oy
Kenelle täsmähoitoja ja millä hinnalla?
 Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
Kenelle täsmähoitoja ja millä hinnalla? Heikki Joensuu ylilääkäri, Syöpätautien klinikka, HYKS, ja professori, Lääketieteellinen tiedekunta, Helsingin yliopisto EUROCARE-4 tutkimus Syöpäpotilaiden eloonjääminen
VALMISTEYHTEENVETO. Yli 33 kg painavat lapset (noin 11-vuotiaat), alle 50 kg painavat nuoret ja aikuiset:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
Vaaleankeltainen, opalisoiva piparmintun tuoksuinen ja makuinen suspensio.
 1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen 8 ml:n injektiopullo konsentraattia sisältää 160 mg dosetakselia.
 1. LÄÄKEVALMISTEEN NIMI TAXOTERE 160 mg/8 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
1. LÄÄKEVALMISTEEN NIMI TAXOTERE 160 mg/8 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
Keytruda 50 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos, Merck Sharp & Dohme Limited.
 Page 1 of 6 JULKAISTU NUMEROSSA 3/2015 UUTTA LÄÄKKEISTÄ Pembrolitsumabi Päivi Ruokoniemi, Olli Tenhunen / Kirjoitettu 29.9.2015 / Julkaistu 2.10.2015 Keytruda 50 mg kuiva-aine välikonsentraatiksi infuusionestettä
Page 1 of 6 JULKAISTU NUMEROSSA 3/2015 UUTTA LÄÄKKEISTÄ Pembrolitsumabi Päivi Ruokoniemi, Olli Tenhunen / Kirjoitettu 29.9.2015 / Julkaistu 2.10.2015 Keytruda 50 mg kuiva-aine välikonsentraatiksi infuusionestettä
Mitä uutta keuhkosyövän käyvässä hoidossa
 Mitä uutta keuhkosyövän käyvässä hoidossa Antti Jekunen Kliinisen lääketutkimuksen dosentti, kliininen farmakologia HY Soveltavan onkologian dosentti, syöpätautien klinikka, TY Kliinisen onkologian professori,
Mitä uutta keuhkosyövän käyvässä hoidossa Antti Jekunen Kliinisen lääketutkimuksen dosentti, kliininen farmakologia HY Soveltavan onkologian dosentti, syöpätautien klinikka, TY Kliinisen onkologian professori,
Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
 1. LÄÄKEVALMISTEEN NIMI Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
1. LÄÄKEVALMISTEEN NIMI Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
PAKKAUSSELOSTE: TIETOJA KÄYTTÄJÄLLE. Granisetron Teva 1 mg kalvopäällysteinen tabletti Granisetron Teva2 mg kalvopäällysteinen tabletti Granisetroni
 PAKKAUSSELOSTE: TIETOJA KÄYTTÄJÄLLE Granisetron Teva 1 mg kalvopäällysteinen tabletti Granisetron Teva2 mg kalvopäällysteinen tabletti Granisetroni Lue tämä seloste huolellisesti ennen kuin aloitat lääkkeen
PAKKAUSSELOSTE: TIETOJA KÄYTTÄJÄLLE Granisetron Teva 1 mg kalvopäällysteinen tabletti Granisetron Teva2 mg kalvopäällysteinen tabletti Granisetroni Lue tämä seloste huolellisesti ennen kuin aloitat lääkkeen
Pakkausseloste: Tietoa käyttäjälle. Vectibix 20 mg/ml infuusiokonsentraatti, liuosta varten panitumumabi
 Pakkausseloste: Tietoa käyttäjälle Vectibix 20 mg/ml infuusiokonsentraatti, liuosta varten panitumumabi Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää
Pakkausseloste: Tietoa käyttäjälle Vectibix 20 mg/ml infuusiokonsentraatti, liuosta varten panitumumabi Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
VALMISTEYHTEENVETO. 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 2,5 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 2,5 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito. Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen
 KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen www.hematology.fi KLL:n diagnostiikka, seuranta ja hoito-ohjeet löytyvät täältä: -> Hoito-ohjeet
KLL Lymfosytoosin selvittely KLL:n seuranta ja hoito Hematologian alueellinen koulutuspäivä 14.4.2016 Anu Laasonen www.hematology.fi KLL:n diagnostiikka, seuranta ja hoito-ohjeet löytyvät täältä: -> Hoito-ohjeet
Kuolevan lapsen kivunhoito
 Kuolevan lapsen kivunhoito Jukka Pouttu Lasten ja nuorten sairaala HUS SULAT 28.01.2016 Lisää aiheesta: DUODECIM: Kuolevan potilaan oireiden hoito Käypä hoito -suositus Julkaistu: 28.11.2012 Kuolevan lapsen
Kuolevan lapsen kivunhoito Jukka Pouttu Lasten ja nuorten sairaala HUS SULAT 28.01.2016 Lisää aiheesta: DUODECIM: Kuolevan potilaan oireiden hoito Käypä hoito -suositus Julkaistu: 28.11.2012 Kuolevan lapsen
LIITE VALMISTEYHTEENVETO
 LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
Lääkevalmisteella ei enää myyntilupaa
 PAKKAUSSELOSTE Zenapax 5 mg/ml infuusiokonsentraatti Daklitsumabi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos Sinulla
PAKKAUSSELOSTE Zenapax 5 mg/ml infuusiokonsentraatti Daklitsumabi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos Sinulla
Herceptin on tarkoitettu HER2:ta yli-ilmentävän metastasoituneen rintasyövän hoitoon:
 1. LÄÄKEVALMISTEEN NIMI Herceptin 150 mg infuusiokuiva-aine konsentraattiliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 150 mg trastutsumabia, joka on humanisoitu monoklonaalinen
1. LÄÄKEVALMISTEEN NIMI Herceptin 150 mg infuusiokuiva-aine konsentraattiliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 150 mg trastutsumabia, joka on humanisoitu monoklonaalinen
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
PAKKAUSSELOSTE. Comtess 200 mg tabletti, kalvopäällysteinen Entakaponi
 PAKKAUSSELOSTE Comtess 200 mg tabletti, kalvopäällysteinen Entakaponi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen ottamisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos sinulla
PAKKAUSSELOSTE Comtess 200 mg tabletti, kalvopäällysteinen Entakaponi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen ottamisen. - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos sinulla
1. ELÄINLÄÄKKEEN NIMI. Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Yksi millilitra sisältää: Vaikuttava aine:
 1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
Bevasitsumabi ei-pienisoluisen keuhkosyövän hoidossa
 Aija Knuuttila, Annamari Rouhos, Eeva-Maija Karjalainen, Matti Pietiläinen, Niina Paunu, Eija-Riitta Salomaa ja Henrik Riska KATSAUS KATSAUS Bevasitsumabi ei-pienisoluisen keuhkosyövän hoidossa Edenneen
Aija Knuuttila, Annamari Rouhos, Eeva-Maija Karjalainen, Matti Pietiläinen, Niina Paunu, Eija-Riitta Salomaa ja Henrik Riska KATSAUS KATSAUS Bevasitsumabi ei-pienisoluisen keuhkosyövän hoidossa Edenneen
PD-hoidon komplikaatiot
 Sisäinen ohje 1 (5) PD-hoidon komplikaatiot Peritoniitti eli vatsakalvon tulehdus: Peritoniitin yleisin aiheuttaja on staphylococcus aureus. Staphylococcus epidermiksen osuus on pienempi. Harvinaisempia
Sisäinen ohje 1 (5) PD-hoidon komplikaatiot Peritoniitti eli vatsakalvon tulehdus: Peritoniitin yleisin aiheuttaja on staphylococcus aureus. Staphylococcus epidermiksen osuus on pienempi. Harvinaisempia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, ks. 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, ks. 6.1. 3. LÄÄKEMUOTO
Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
