Orgaanisen kemian laboratoriotöiden yleisohje
|
|
|
- Esko Pesonen
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 Orgaanisen kemian laboratoriotöiden yleisohje 2006 Ari Koskinen, Petri Pihko, Tiina Putkonen, Päivi Koskinen, Emmi Valkonen, Taina Salo 2007 Aapo Tammisto, Aki Abe
2 Sisällysluettelo Johdanto... 3 Laboratoriopäiväkirja... 3 Aineiden siirtäminen, mittaaminen ja punnitseminen... 7 Astioiden pesu... 8 Erikoistapaukset... 9 Uuden reaktion suunnittelu Reaktion seuranta TLC:n ajaminen Värjäysreagenssit Synteesin päävaiheet Eristyksen ja puhdistuksen yksikköoperaatiot Uutto Kuivaus Haihdutus Puhdistuksen yksikköoperaatiot Tislaus Fraktiotislaus Alipainetislaus Kiteytys Tuotteiden karakterisointi Turvallisuus orgaanisen kemian laboratoriossa: Laboratoriojätteiden käsittely... 52
3 3 Johdanto Orgaanisen kemian laboratoriotyökurssien tarkoituksena on opettaa turvallisia ja siistejä työtapoja sekä oikeita työmenetelmiä. Lisäksi tavoitteena on, että laboratoriossa opitaan kemiaa. Uusia asioita ihminen oppii kaikkein parhaiten käsillään tekemänsä työn avulla ja haluamme osaltamme auttaa tätä oppimisprosessia. Tämän kirjasen tarkoitus on perehdyttää orgaanisen kemian työmenetelmiin ja laboratoriokäytäntöihin. Laboratoriopäiväkirja Laboratoriopäiväkirja ei ole vain työntekijän omaa käyttöä varten, vaan sitä käytetään dokumenttina toisille tutkijoille, jotta he tietäisivät, mitä kyseinen työntekijä on tehnyt. Tarvittaessa muiden tulee voida toistaa kokeet ilmoitettujen ohjeiden perusteella. Laboratoriopäiväkirja on myös laillinen dokumentti tehdystä työstä, joka vaaditaan esim. patenttia puolustettaessa. Muistiinpanot on siis syytä tehdä selkeällä käsialalla. Työohjeen kopioiminen suoraan kirjallisuudesta omiin muistiinpanoihin ei ole hyvä käytäntö se antaa vaikutelman, ettet ole ymmärtänyt, mitä olet tekemässä. Alusta alkaen on syytä opetella siisti, johdonmukainen ja ytimekäs esitystapa, jotta muistiinpanot pysyisivät työn tasalla ja muiden on helppo tarkistaa, miten työ on tehty. Virallinen laboratoriopäiväkirja on kovakantinen A4-kokoinen sidottu kirjanen. Orgaanisen kemian oppilaslaboratoriotöitä varten riittää vihko, josta ei saa revittyä lehtiä irti. Kaikki merkinnät tehdään suoraan kirjaan, ei koskaan irtopaperille tms. myöhempää tiedonsiirtoa varten, koska tärkeät irtolappuset katoavat helposti. Yleensä lyijykynä on sopivin kynä muistiinpanojen tekemiseen, sillä laboratorion hapan ilma tuhoaa vähitellen kuulakärkikynällä kirjoitetun tekstin. Jos päiväkirja on tarkoitettu pysyväksi ja lailliseksi dokumentiksi, on muistiinpanot tehtävä pysyvää jälkeä jättävällä kynällä eli kuulakärki- tai mustekynä. Tällöin päiväkirjaa ei säilytetä laboratoriossa. Muistiinpanot kirjoitetaan vain oikeanpuoleisille numeroiduille sivuille. Vasemmanpuoleiset sivut on varattu suttupaperiksi laskutoimituksia varten. Virheellisiä merkintöjä ei saa pyyhkiä tai sotkea vaan niiden yli vedetään siisti viiva ja korjaukset kirjoitetaan virheen yläpuolelle tai perään.
4 4 Kokeiden raportointi Kokeet raportoidaan alla kuvatulla tavalla. Ennen kokeen aloittamista päiväkirjassa pitää olla merkinnät reagenssitaulukkoon asti. Kokeelle annetaan nimi, esim. Asetofenonin hydratsonin valmistus. Vältä kuitenkin pitkiä IUPAC-nimiä otsikoissa. Kirjoita reaktioyhtälö näkyviin, esim. O CH 3 H 2 NNH 2 KOH HN NH 2 CH 3 Anna kirjallisuusviite, jonka mukaan olet tehnyt työn (jos mahdollista). Sen alapuolelle kirjoitetaan taulukko reagensseista. Taulukkoon laitetaan vain reaktioon osallistuvat yhdisteet. Uutto- ja pesuliuokset, kuivausaineet jne. kirjataan päiväkirjaan asianmukaiseen kohtaan. reagenssi mol.wt. mmol mol-% g(ml) Huom. asetofenoni ,0 g dietyleeniglykoli 60 ml liuotin hydratsiinihydraatti 50, ,0 ml d=1.011; 90% KOH 56, g Kaikki tämä pitää olla tehtynä ennen synteesin aloittamista. Jos reagenssien todelliset määrät poikkeavat lasketuista, yliviiva jälkimmäiset ja kirjoita todelliset määrät niiden yläpuolelle. Voit myös numeroida reagenssit ja käyttää näitä numeroita. Tämän jälkeen kirjoitetaan kokeen todellinen kuvaus. Kokeiden kuvaus kirjoitetaan aina passiivin imperfektiä ja pluskvamperfektiä käyttäen. Esim. Asetofenoni liuotettiin dietyleeniglykoliin 100 ml:n pyörökolvissa, joka varustettiin refluksointilaitteistolla ja lämpömittarilla. Hydratsiinihydraatti ja KOH-rakeet lisättiin ja seos lämmitettiin varovasti kiehuvaksi... Kokeen kuvauksen viereen piirretään kaaviokuva reaktion kulusta ja sen jälkeisistä toimenpiteistä (erotuskaavio, katso esimerkkisivua, s. 6).
5 5 Merkitse päiväys ja kellonaika ylös aina, kun aloitat reaktion, ajat TLC:n, huomaat muutoksia reaktiossa, lisäät reagensseja ja kun sammutat reaktion. Kirjoita ylös sammutusliuos ja uuttoliuos sekä näiden määrät (katso esimerkkisivua, s 6). Kopioi kaikki TLC-levyt päiväkirjaasi 1:1 mittakaavassa niin täsmällisesti kuin mahdollista. Merkitse ylös eluointi- ja visualisointiolosuhteet. Kun saat tuotteen, kirjoita kuvaus siitä: Tuotteeksi saatiin kellertävää nestettä, jonka kiehumispiste on C. Ilmoita puhdistusolosuhteet: esim. kiteytysliuottimet, kiehumispiste ja paine. Merkitse lopuksi muistiin omat tuloksesi: todellinen saanto grammoina, mooleina ja prosentteina sekä kirjallisuuden saanto, jos sellainen on olemassa.
6 6 Esimerkki laboratoriopäiväkirjan sivun ulkonäöstä: 9 March Reduction of Aldehyde BB A21a H H OHC H OBn OBn NaBH4/CeCl3 MeOH, 0 C HO H OBn OBn Ref. Luche, J.-L.; Rodriguez-Hahn, L.; Crabbe, P.J. J. Chem. Soc., Chem. Commun. 1978, 601. MeOH I II III CH 2 Cl 2 aq HCl Substance mw mmol mol-% mg/ml notes I BB A21a p. A21 III NaBH II CeCl 3 (0.4M/MeOH) Aldrich II MeOH ml solvent The aldehyde and CeCl 3 solution in MeOH (25 ml) was cooled to 0 C, then treated with NaBH 4 (in 2 ml MeOH) TLC (20 % EtOAc in hexane): vanillin staining 10 min 30 min aq org BB A23a (red/brown) aq NaHCO 3 dried Na 2 SO 4 BB A23b (blue) product L L+R R L L+R R After 30 min the tlc shows no SM but two products. MeOH was evaporated, CH 2 Cl 2 (30 ml) was added and the mixture was washed with 10 % HCl (10 ml) followed by sat NaHCO 3 (3 x 10 ml), dried (Na 2 SO 4 ) and evaporated to give 210 mg crude (104 %). After separation: BB A23a 27 mg (12 %) BB A23b 140 mg (69%) by NMR by NMR MeO H H OMe OBn OBn Comment: Next time use aqueous solvent - may avoid ketal formation HO H H OBn OBn
7 7 Aineiden siirtäminen, mittaaminen ja punnitseminen Jotta reaktiot onnistuisivat hyvin ja laboratorio säilyisi siistinä ja mahdollisimman hajuttomana: Mieti etukäteen, miten siirrät lähtöaineesi reaktioastiaan. Siivoa heti jälkesi punnituspaikoilta. Käytä oikeanlaisia mitta- ja punnitusastioita. Älä saastuta reagensseja likaisilla välineillä! Sulje aina astiat heti punnituksen jälkeen! Siirrä kemikaalit omaan vetokaappiisi ainoastaan suljetuissa astioissa. Nesteet Liuottimet, useimmat reagenssit Käytä mittalasia (tai ruiskua ja neulaa) Ilma- ja kosteusherkät reagenssit Käytä ruiskua ja neulaa (ja suojakaasua) Jäykät siirappimaiset öljyt Siirretään mieluiten liuoksina Pienet näytemäärät (esim. näytetippa IR:lle) Käytä pasteurpipettiä Ruiskujen käyttö opetetaan laboratoriossa. Pasteurpipettejä käytettäessä on muistettava, että höyrynpaineen tulee antaa tasaantua pipetissä ennen siirtoa. Vedä liuosta pipettiin ja purista ulos muutaman kerran, ennen kuin ryhdyt siirtämään liuosta tai liuotinta pipetillä. Kiinteät aineet, jotka lisätään reaktioastiaan Kiteiset aineet Punnitse spaattelilla pieneen näytepurkkiin tai punnituspaperille (EI dekantterilaseihin!) Vahamaiset tai alhaalla sulavat aineet Siirretään mieluiten liuoksina tai sulatettuina Kiinteiden aineiden punnitsemisesta Kuivina talvipäivinä kiinteiden aineiden punnitseminen voi olla hankalaa. Astiat varautuvat staattisella sähköllä ja aineet saattavat käyttäytyä vastahakoisesti. Staattisen sähkön vaikutuksia voi välttää, jos koskettaa spaattelilla punnitusastiaa ennen aineen siirtämistä. Muoviastioita kannattaa välttää.
8 8 Astioiden pesu Laboratoriotyöskentelyn onnistumisen takaa puhtaus. Kaikki lasiastiat ja muut laitteet on huolellisesti puhdistettava heti käytön jälkeen. Seuraavassa on esitetty hyvien laboratoriokäytäntöjen mukaisia ohjeita. Laboratorion siisteys tuo mukanaan turvallisuutta ja puhtailla astioilla reaktiotkin onnistuvat paremmin. Muista, että vahingot kiertävät: likaiset astiat ja välineet voivat pilata monen muunkin työn ja aiheuttaa jopa vaaratilanteita! Pidä huolta, että muutkin tekevät oman osansa siisteyden eteen. Useimmiten orgaanisen kemian laboratoriossa lasiastioihin kertyy orgaanista likaa ja epäpuhtauksia. Vesi ei välttämättä ole niille paras liuotin. Esipesu Huuhtele huolellisesti kaikki käyttämäsi lasiastiat pienellä määrällä teknistä etanolia jäteastiaan. Tarvittaessa voit käyttää muitakin liuottimia, kuten asetonia tai etyyliasetaattia (käytä näitä vetokaapissa!) Nämä ovat parempia erilaisten rasvojen ja öljyjen irrottamiseen. Rasvat ja öljyt puhdistuvat vain pyyhkimällä astian pintaa etyyliasetaattiin kostutetulla paperipyyhkeellä tai vanupuikolla. Pesu Jos esipesty astia ei ole puhdas, pese se uudestaan liuottimella. Tee viimeinen huuhtelu aina etanolilla, johon liukenee myös pieniä määriä epäorgaanisia suoloja. Jos astia täytyy saada nopeasti kuivaksi, asetonihuuhtelu aivan viimeiseksi auttaa. Vesipesu Jos reaktio on ollut heterogeeninen tai astioissa on ollut suoloja, myös vesipesu saattaa olla tarpeen. Käytä vettä, laboratoriopesuainetta ja tarvittaessa sopivia pesuharjoja. Vältä astioiden naarmuttamista! Pesuharjojen kanssa tulee olla varovainen, ettei puhkaise kolvin pohjaan reikää. Huuhdo pesuaine lopuksi hyvin pois vedellä ja pese vielä kerran etanolilla. Joissakin tapauksissa lievästi happamat (0.1 M HCl) tai emäksiset (0.1 M NaOH) pesuliuokset voivat olla tarpeen. Myös nämä on muistettava huuhdella pois huolella. Happo- ja emäskylvyt Tislausjäännökset ovat usein ongelmallisia tapauksia (polymeerejä ja pahimmassa tapauksessa kärähtäneitä jäännöksiä). Usein liotus sopivalla orgaanisella liuottimella riittää irrottamaan jäännöksen. Hyviä liuottimia ovat etyyliasetaatti ja dimetyyliformamidi. Jos nämä eivät toimi, kannattaa käyttää happo- tai emäskylpyjä (valmistusohjeet saa assistenteilta).
9 9 Erikoistapaukset Ruiskut ja neulat Ruiskut ja neulat on huuhdeltava aina heti käytön jälkeen sopivalla liuottimella (reaktioliuotin) ja inertillä liuottimella (THF, etyyliasetaatti) sekä lopuksi etanolilla tai asetonilla. Seuraavassa taulukossa on annettu ohjeita erityyppisten ruiskujen pesuun. Jos ruiskuissa on ollut organometallireagensseja, on oltava varovainen: reagenssijäämät voivat reagoida kiivaasti veden kanssa ja vesi saattaa saostaa niukkaliukoisia suoloja, jotka tukkivat ruiskun ja neulat. Liuotinhuuhtelun jälkeen kannattaa käyttää laimeaa happoa (0.1 M HCl) veden asemesta. Muista neutraloida happo ruiskusta ennen lopullista pesua! Tukkeutuneita neuloja voi avata ultraäänipesurilla tai teräslangan avulla. Jos ruiskussa on ollut vain liuotinta tai muuta pelkästään orgaanista reagenssia, vettä ei kannata käyttää pesuun ollenkaan. TAVALLISET LASIRUISKUT KAASUTIIVIIT LASIRUISKUT MUOVIRUISKUT 1. Huuhdo liuottimella Huuhdo liuottimella Huuhdo liuottimella (2.) Vesipesu tai 0.1 M HCl Vesipesu tai 0.1 M HCl Vesipesu tai 0.1 M HCl 3. EtOH (tai asetoni) EtOH (tai asetoni) EtOH (tai asetoni) 4. Kuivaus uunissa yön yli, Kuiva eetteri, puhalletaan Kuivataan ilmassa säilytetään eksikkaattorissa kuivaksi argonilla, säilytetään eksikkaattorissa ÄLÄ KUIVAA UUNISSA ÄLÄ KUIVAAUUNISSA Juuttuneet hiokset Lasihiokset voivat juuttua erityisesti vakuumitislauksissa ja reaktioissa, joissa on emäksisiä vesiliuoksia. Jos hiokset ovat juuttuneet kiinni, kevyt taputtelu joka puolelta saattaa riittää. Varo vääntämästä niin kovasti, että astia särkyy! Seuraavana keinona kannattaa kokeilla hioksen kuumentamista kuumailmapuhaltimella (VARO kuumaa lasia!). Tämän tarkoituksena on laajentaa naarashiosta enemmän kuin koirashiosta, jolloin hiosten pitäisi irrota toisistaan. Jos hiokset pysyvät itsepintaisesti juuttuneina, voi joko kokeilla yön yli liotusta jossain pesukylvyssä tai sitten viedä astiat lasinpuhaltajalle hän yleensä onnistuu toivottomiltakin tuntuneissa tapauksissa.
10 10 Kuivaus Anna lasiastioiden ensin kuivua ilmassa. Jos on tarpeen, kuivaus lämpökaapissa ( C) muutaman tunnin ajan tai yön yli riittää. Älä säilytä lasiastioita uunissa! Uuden reaktion suunnittelu Synteetikon tärkeimpiin tehtäviin kuuluu uusien reaktioiden suunnittelu. Joissain tapauksissa kirjallisuudesta löytyy reaktio-olosuhteet reaktiolle, joka läheisesti muistuttaa kehitteillä olevaa reaktiota. Hyvin usein joudutaan reaktio kuitenkin suunnittelemaan aivan alusta. Tällöin käytetään teoriaa, käytännössä opittuja taitoja ja kokemusta hyväksi. Tästä syystä taitavaksi synteetikoksi kehittyminen vie aikaa ja vaatii paljon kokeellista työtä. Seuraavassa on lueteltu hyvän suunnittelun pääkohdat: Suhtaudu kriittisesti kirjallisuuden reaktio-ohjeisiin. Reaktion tulee olla mahdollisimman yksinkertainen toteuttaa. Reaktion tulee olla varmasti toistettavissa. Reaktion saannon tulee olla mahdollisimman korkea. Reaktiossa tulee syntyä mahdollisimman vähän jätettä. Huomioitava ennen uuden reaktion ajoa: Lämpötila Eksoterminen reaktio Käytä jäähdytyshaudetta Lämmitettävä reaktio Käytä vesi- tai öljyhaudetta Tislaus / Kiteytys Käytä vesi- tai öljyhaudetta Sekoitus Homogeeninen reaktio Käytä magneettisekoitusta Heterogeeninen reaktio Käytä mekaanista sekoitusta tai Morton-kolvia. HUOM! Pienessä mittakaavassa tehdyissä reaktioissa (< 10 mmol) magneettisekoitus on yleensä riittävä. Liuottimen valinta Liuottimen valintaan vaikuttavat lähtöaineet, tuotteet ja reaktion siirtymätilat. Valitse liuotin, joka parhaiten stabiloi siirtymätilaa ja / tai tuotetta. Käytä pääsääntöisesti vedettömiä liuottimia. (Jos reaktion voi tehdä vedessä tai vesipitoisessa liuotinseoksessa, vettä kannattaa kokeilla yhtenä vaihtoehtona.) Hydrolyyseissä ei tarvita vedettömiä liuottimia. Suojakaasujen käyttö
11 11 Pyri käyttämään suojakaasuja, kuten argon (Ar) tai typpi (N 2 ). Monet reaktiot ovat hyvin herkkiä sekä ilman hapelle että kosteudelle. Hapetusreaktiot ja hydrolyysit eivät yleensä tarvitse suojakaasua. Mittakaava Kun teet uuden reaktion ensimmäisen kerran, käytä 1 mmol mittakaavaa. Kun toistat reaktiota, kasvata sen mittakaavaa aina enintään 2-3 kertaiseksi,. Konsentraatio Kun teet uuden reaktion ensimmäisen kerran, käytä 10 mm konsentraatiota eli 1 mmol lähtöainetta 10 ml:ssa liuotinta. Reaktion seuranta Kirjallisuudessa ilmoitetut reaktioajat ovat ainoastaan ohjeellisia. Jokaisen reaktion etenemistä on seurattava sopivalla tavalla. Useimmissa tapauksissa reaktio on tapahtunut täydellisesti, kun reagenssit ovat kuluneet loppuun (muista tasapainoreaktiot). Menetelmä, joka valitaan, riippuu reaktiosta ja lähtöaineiden sekä tuotteiden (myös sivutuotteiden) kemiallisesta luonteesta. Ohutkerroskromatografia, TLC (Thin Layer Chromatography) Yksinkertaisin ja useimmiten käytetty menetelmä on ohutkerroskromatografia, TLC, jota pitäisi aina kokeilla ensin. TLC:llä voidaan seurata reaktioiden etenemistä kvalitatiivisesti. Sana kromatografia tulee kreikasta ja tarkoittaa väreillä piirtämistä. Kromatografia perustuu siihen, että eri aineet tarttuvat (adsorboituvat) eri tavoin huokoisiin aineisiin. Kun seos liikkuu (eluoituu) huokoisen aineen (stationäärifaasi) läpi siten, että liuotin (eluentti) ajaa sitä eteenpäin, tapahtuu erottumista. Jotkut aineet adsorboituvat paremmin stationäärifaasiin ja toiset taas huonommin. Ohuella levyllä nämä aineet muodostavat täpliä, jotka vaeltavat sitä pidemmälle, mitä huonommin ne tarttuvat levyn pinnalla olevaan adsorboivaan stationäärifaasiin. Tyypillisesti stationäärifaasina käytetään esim. silikageeliä tai alumiinioksidia, jotka adsorboivat polaarisia aineita hyvin. Mitä polaarisempi aine, sitä lyhyemmän matkan se liikkuu silikalla päällystetyn ohutlevyn pinnalla.
12 12 Sopiva eluentti, stationäärisen faasin väliaine ja detektointitapa valitaan jo ennen reaktion aloittamista. Jokainen TLC piirretään oikeassa mittakaavassa laboratoriopäiväkirjaan. Myös kellonaika, jolloin TLC on ajettu, eluentti ja visualisointitapa merkitään ylös. Ensimmäinen TLC ajetaan heti, kun reagenssit on lisätty reaktioastiaan. Tämä on reaktion alkupiste. Toinen TLC otetaan noin minuuttia reaktion alusta, ja tämän jälkeen sopivin väliajoin. Viimeiset kaksi TLC:tä ajetaan juuri ennen reaktion sammuttamista ja ylöstyöskentelyä (reaktion loppupiste) ja heti ylöstyöskentelyn jälkeen. Muista tarkistaa myös vesifaasi! Huom! Reaktion sammutuksen jälkeen ajettavalle levylle tulee neljäs täplä, joka otetaan uuton vesifaasista. TLC-levyt TLC-levyillä on olemassa pääasiassa kahdenlaisia päällysteitä: piidioksidi (silika) ja alumiinioksidi (alumina). Silikalevyt ovat yleisimmin käytettyjä. Ne ovat lähes neutraaleja ja sopivat monenlaisten aineiden ajamiseen. Aluminalevyt ovat emäksisiä, ja niitä käytetään emäksisten, huonosti silikalla liikkuvien aineiden analysoinnissa. Yleisesti käytetyt TLClevyt ovat alumiinilevyjä, jotka on päällystetty 0,25 mm:n kerroksella silikaa (ja tavallisesti fluoresoivalla UV-indikaattorilla, joka sisältää Zn-reagensseja). Eluentin valinta Sopivan liuottimen valinta vaatii aina tietynlaista vaistoa ja vaatii harjoittelua. Yhdisteiden eluoitumisjärjestys riippuu niiden polaarisuudesta suhteessa eluentin polaarisuuteen. Pyritään valitsemaan sellainen eluentti, jolla toivotun tuotteen Rfarvoksi saadaan (ks. R f-arvo, alla). Näytteiden aplikointi Kun reaktiota seurataan, yhdelle levylle aplikoidaan aina vähintään kolme näytettä: L) lähtöaine, L+R) lähtöaineen ja reaktioseoksen co-spot ja R) reaktioseos. Valmista lähtöaineesta referenssi liuottamalla sitä (1-10%) johonkin alhaalla kiehuvaan liuottimeen (esim. CH 2Cl 2 tai Et 2O). Näytteiden aplikoinnissa käytetään ohutta lasikapillaaria (valmistetaan itse). Täplien visualisointi Näytteet saadaan näkyviin TLC-levyillä kolmella yleisesti käytetyllä menetelmällä. Mitä tahansa näistä tavoista voidaan käyttää, mutta niitä pitäisi kokeilla alla olevassa järjestyksessä. 1. Levyä voidaan katsoa ultraviolettilampun alla, jolloin UV-aktiiviset täplät näkyvät. 2. Levy voidaan värjätä jodilla.
13 13 3. Levy voidaan käsitellä jollain värjäysreagenssilla. Aineiden käyttäytymistä TLC levyllä tietyllä liuotinsysteemillä merkitään R f-arvolla: R f = Täplän keskipisteen etäisyys lähtöviivasta Liuottimen etäisyys lähtöviivasta Muistettavia asioita: Kylmässä tilassa suoritettavan reaktion (< -20 o C) todellista tilaa ei voida määrittää TLC:llä, koska näyte lämpenee kapillaarissa. Ionien reaktioita ei voi suoraan seurata TLC:llä. Näytteelle on suoritettava mini - sammutus ja uutto. Huom! Näytteen applikointi levylle suoraan tällaisesta reaktiosta vastaa hapanta reaktion sammutusta. Hyvin happoherkät yhdisteet saattavat tuhoutua silikalevyllä. Helposti haihtuvat yhdisteet saattavat haihtua. Korkealla kiehuvat liuottimet voivat vaikuttaa eluointiin. Varmista, että liuotin on kokonaan haihtunut tai suorita mini - ylöstyöskentely. TLC ei ole aina paras tai ainoa menetelmä. Yhdessä TLC:n kanssa tai yksistään voit käyttää seuraavia menetelmiä. Infrapuna- ja ultraviolettispektrometria (IR ja UV) IR ja UV ovat erinomaisia menetelmiä funktionaalisten ryhmien muutosreaktioiden seuraamisessa, esim. alkoholin reaktio karbonyyliksi. Molemmat ovat nopeita ja helppoja ajaa. Menetelmät ovat kvalitatiivisia ja sivureaktiot ja/tai reagenssit saattavat häiritä ajoa. IR:n ja UV:n käytöstä on kerrottu tarkemmin monisteen lopussa tuotteiden karakterisoinnin yhteydessä. TLC:n ajaminen TLC-levyt ajetaan ja värjätään aina vetokaapissa! 1. Ajoastia TLC:n ajoastiana voidaan käyttää erityisesti tarkoitukseen suunniteltua säiliötä, sopivaa kannellista lasipurkkia. Oppilaslaboratoriossa käytetään ajoastiana
14 14 lasipurkkeja (esim. pilttipurkit). Sillipurkit tai voimakkaasti maustettuja aineita sisältäneet purkit eivät kelpaa. Kaada astian pohjalle liuotinta n. 3 mm kerros. Vuoraa osa astiasta suodatinpaperilla, jotta astian sisäpuoli tasapainottuu nopeammin liuottimen höyrynpaineeseen. Sulje kansi ja anna seisoa, kun valmistelet TLC-levyn. Kuva 1. Erilaisia ajoastioita 2. Levyt Orgaanisen kemian laboratoriossa TLC levyt on leikattu 5 cm 20 cm kokoisiksi levyiksi. Jokainen levy leikataan sopivan levyiseksi palaksi; kolmelle tai neljälle näytteelle sopiva leveys on 3 cm (korkeus aina 5 cm). Käsittele levyjä varoen, jotta et tuhoa silikakerrosta levyn pinnalla tai likaa sitä. Varo erityisesti murtamasta tai taittamasta levyä. Mittaa n. 7 mm pohjasta, ja piirrä lyijykynällä poikkiviiva tälle korkeudelle. Älä paina kynällä liikaa, jotta levyn pinta ei hajoaisi. Merkitse pisteillä viivan kohdalle näytteiden paikat Merkitse viivan alle näytteiden nimet: L = lähtöaine, L + R = seostäplä, R = reaktio. Jätä tarpeeksi tilaa näytteiden väliin äläkä laita näytettä liian lähelle reunaa; noin 4 näytettä mahtuu 3 cm leveälle levylle. Käytä lyijykynää.
15 15 Kuva 2. TLC levyn valmistelu 3. Näytteiden aplikointi Aplikoi näyte levylle. Jos näyte ei ole liuottimessa, liuota noin 1 mg näytettä muutamaan pisaraan haihtuva liuotinta, kuten heksaani, etyyliasetaatti tai dikloorimetaani. Yleisesti 1 % pitoisuus (1g/100 ml) on hyvä näytteen pitoisuus TLC-analyysiä varten. Liuos aplikoidaan TLC-levylle kapillaarilla. Oppilaslaboratoriossa ja orgaanisen kemian laboratoriossa yleensäkin käytetään pipetistä itse valmistettuja kapillaareja. Kasta kapillaari näyteliuokseen. Varmista, että kapillaarissa on liuosta. Kosketa kapillaarilla TLC levyä niin, että levylle syntyy pieni täplä (enintään 3-4 mm halkaisijaltaan). Kosketa levyä niin monta kertaa, että kapillaari on tyhjä. Kuva 3. Näytteen aplikointi 4. Kehitä levy Käytä pinsettejä! Aseta TLC-levy pystyssä kehitysastiaan (aplikoidut täplät alas!) ja sulje kansi. Varmista, että liuotinpinta jää viivan alapuolelle. Jätä astia rauhassa vetokaappiin.
16 16 Kuva 4. TLC levyn kehitys. Anna liuotinrintaman nousta, kunnes se on enää puolen sentin päässä levyn yläreunasta. Poista levy kehitysastiasta ja merkitse lyijykynällä viiva liuotinrintaman kohdalle. Kuva 5. TLC levy poistetaan ajoastiasta Anna liuottimen haihtua levyltä. 5. Visualisoi täplät Merkitse värilliset täplät lyijykynällä ympäröimällä ne. 6. Katso levyä UV lampun alla. Ympäröi UV-aktiiviset täplät. Älä katso suoraan UV-lamppuun.
17 17 Kuva 6. Visualisointi UV-lampun alla 7. Värjää levy sopivalla värjäysreagenssilla. niisto dippaus lämmitys lopputulos Kuva 7. TLC levyn värjäys
18 18 Värjäysreagenssit Muista merkitä kaikki täplät TLC levylle, kun käytät ei-pysyvää visualisointimenetelmää. Värjääminen jodilla I2 Jodi värjää useimmat yhdisteet, joilla on jokin funktionaalinen ryhmä, joten se on erityisen hyvä tyydyttymättömien yhdisteiden värjäämiseen. Tämä menetelmä ei jätä pysyvää väriä; jodi haihtuu muutamassa minuutissa. Haihtumista voidaan nopeuttaa varovaisella kuumennuksella. Jodia käytetään usein sen jälkeen, kun TLC:tä on katsottu UV:n alla ja ennen kuin se värjätään pysyvillä värjäysreagensseilla. Jodi saattaa häiritä joitakin värjäysreagensseja, joten sitä ei kannata käyttää jokaiselle levylle. Valmistus: Pane muutama jodikide ja 2 teelusikallista hiekkaa lasiastiaan, jossa on tiivis kansi. Käyttö: Laita TLC levy hiekka-jodi astiaan ja pyöritä astiaa ympäri muutaman kerran. Täplät värjäytyvät eri sävyisiksi ruskeiksi. Kun olet merkinnyt värjäytyneet täplät, jätä levy vetokaappiin haihtumaan tai lämmitä levyllä kunnes jodin ruskea väri katoaa. Huom! Jodihöyryt ovat myrkyllisiä. Muista pitää astia huolellisesti suljettuna ja työskentele aina vetokaaapissa. Värjääminen liuoksilla Värjäysliuoksia käytetään UV:n (ja jodin) jälkeen, koska ne ovat pysyviä: värjäytyminen on kemiallisesti irreversiibeliä ja visualisointi muilla keinoilla on mahdotonta liuosten jälkeen. Värit eivät kuitenkaan ole pysyviä, vaan häviävät ajan kanssa. Levyistä on piirrettävä kopio 1:1 laboratoriopäiväkirjaan heti värjäyksen jälkeen. Huom! Jos levyllä ei näy jotakin, se ei tarkoita, ettei sitä ole levyllä! On tärkeä valita oikea värjäysreagenssi reaktiota varten. Väri on seurausta TLC-levyllä olevien komponenttien ja värjäysreagenssin välisestä kemiallisesta reaktiosta, joten värjäys tapahtuu vain, jos reaktio tapahtuu. Jos reaktiossa on kemiallisesti hyvin erilaisia yhdisteitä, täytyy ajaa kaksi tai useampia TLC-levyjä yhtäaikaa ja värjätä ne eri reagensseilla. Värjäysreagenssit säilyvät rajallisen ajan (kuukaudesta muutamaan kuukauteen). Niitä säilytetään aina tummissa lasiastioissa, joissa on tiiviit kannet. Kun reagenssi vaihdetaan, astia on pestävä huolellisesti ja valmistuspäivä merkittävä astiaan.
19 19 Käyttö: Anna liuottimen (eluentin tai I2) haihtua levyltä. Pitele levyä yläkulmasta pinseteillä, kasta levy kokonaan väriin ja nosta se nopeasti pois. Pyyhi levyn reuna paperiin ylimääräisen värin poistamiseksi ennenkuin kuumennat sitä levyllä. Älä ylikuumenna! Eri täplät reagoivat eri nopeuksilla värjäysreagenssien kanssa riippuen niiden kemiallisesta luonteesta. Seuraa kuumennusta huolellisesti. Jotta levyt eivät sotkisi paikkoja, kannattaa levyjen tausta pyyhkäistä kostealla paperilla värjäyksen jälkeen puhtaaksi. Yleisiä TLC-värjäysreagensseja Kaikki vaativat kuumennusta. Fosfomolybdeenihappo (Phosphomolybdic acid, PMA) Hyvä yleinen reagenssi hapettuville aineille, erityisesti ei-haihtuville alkoholeille. Sinivihreät täplät. Valmistus: 5.0 g fosfomolybdeenihappoa liuotetaan EtOH:n (100 ml). Säilytys: Valolta suojattuna. Pidä kansi tiukasti suljettunsa. Säilyy < 1 kuukausi. Hapan fosfomolybdeenihappo (Hapan PMA) Hyvä yleisreagenssi. Valmistus: 2.3 g fosfomolybdeenihappoa liuotetaan tislattuun veteen (90 ml). Lisätään varovasti väkevää rikkihappoa (4.5 ml) sekä 85% fosforihappoa (1.5 ml). Säilytys: Tiiviisti suljettu, valolta suojattu lasiastia. Anisaldehydi Hyvä yleisreagenssi, joka antaa erilaisia värejä. Täplät katoavat nopeammin kuin PMA:lla värjätyt. Valmistus: 2.8 ml anisaldehydiä liotetaan etanoliin (100 ml) ja lisätään varovasti väkevää rikkihappoa (2 ml) ja jääetikkaa CH3COOH (1.2 ml). Säilytys: Valolta suojattuna. Varastoliuos säilyy ainoastaan kylmässä. H 2 SO 4 Hyvä yleisreagenssi. Valmistus: 5 ml konsentroitua rikkihappoa etanoliin (100 ml) Säilytys: Tiiviisti suljettu tumma lasiastia.
20 20 Vanilliini Hyvä yleisreagenssi, joka antaa erilaisia värejä. Valmistus: 2.4 g vanilliinia liuotetaan etanoliin (100 ml) ja lisätään varovasti väkevää rikkihappoa (2 ml) sekä väkevää etikkahappoa (1.2 ml). Säilytys: Tummassa lasiastiassa. Cerium fosfomolybdeenihappo (Cerium PMA) Valmistus: 2.0 g fosfomolybdeenihappoa sekä 1.0 g cerium(iv)sulfaattia liuotetaan tislattuun veteen (90 ml). Lisätään varovasti väkevää rikkihappoa (10 ml). Säilytys: Tummassa lasiastiassa. Tyydyttymättömät yhdisteet: Permanganaatti Useimmat alkeenit ja alkyynit värjäytyvät nopeasti (keltainen täplä). Aldehydit ja alkoholit värjäytyvät myös keltaisiksi, mutta ketonit ja monet esterit saadaan näkyviin vasta kuumennuksen jälkeen tai muutaman minuutin kuluttua. Valmistus: KMnO 4 (0.9 g) + K 2CO 3 (6 g) + 1M NaOH (1.5 ml) laimennetaan veteen (90 ml). Reaktio: HO OH KMnO H 2 O MnO KOH Erikoisvärjäysreagenssit: Nämä värit eivät vaadi aina lämmittämistä. Varovainen lämmitys antaa kuitenkin usein paremman tuloksen. Aldehydit ja ketonit: 2,4-dinitrofenyylihydratsiini (DNP) VAROITUS: 2,4-dinitrofenyylihydratsiini on myrkyllistä. Käsittele reagenssia erityisen huolellisesti. Jätä reagenssilla värjätyt levyt vetokaappiin omaan astiaansa ja piirrä levy työpäiväkirjaasi värjäyspisteen luona. Oranssit täplät. Hyvin nopea reaktio aldehydien kanssa, jotkut estyneemmät ketonit voivat reagoida hitaammin. Valmistus: 0.6 g DNP:ta liuotetaan etanolin (60 ml) ja veden seokseen (24 ml), ja lisätään väkevää rikkihappoa (18 ml)
21 21 Reaktio: R C R' O 2 N O + HN NO 2 H 2 N H + R R' HN N O 2 N NO 2 2,4-dinitrofenyylihydratsiini + H 2 O Amiinit: Ninhydriinireagenssi Primääriset amiinit värjäytyvät kellanoransseiksi (tai keltaiseksi) ja sekundääriset amiinit värjäytyvät punaisiksi melkein heti. Valmistus: 1.0 g ninhydriiniä liuotetaan etanoliin (100 ml) ja lisätään 0,2 ml jääetikkahappoa. Reaktio: O R O O OH OH H + O OH R-NH 2 O NH 2 OH O NH + R keltainen O ninhydriini O RR -NH O O R N R OH 2 O O R N R punainen
22 22 Synteesin päävaiheet Oheinen kaavio kuvaa synteesin kulkua ja ainetasetta pääpiirteittäin. Orgaanisen synteesin ainetase Puhdas aine Karakterisointi: TLC R f, sp., kp., [a] D, n D 20, UV, IR, NMR ( 1 H, 13 C) Alkuaineanalyysi Tarkka massa (HRMS) Reagenssit Reaktio! Reaktion seuranta: TLC, GC, HPLC, NMR Reaktioseos Reaktion sammutusliuos Sivutuotteet Puhdistus: tislaus, kiteytys tai kromatografia Eristys uuttamalla liukoisuuden ja/tai pk a :n perusteella (erotuskaavio) -emäliuokset -tislausjäännökset -liuotinjäte Raakatuote (epäpuhdas tuote) suolat Saanto lasketaan aina puhtaan tuotteen ainemäärästä. Uudet aineet karakterisoidaan täydellisesti. Raakatuotteen perusteella laskettu raakasaanto kuvaa eristyksen tehokkuutta. Kaikkia reaktioita ei tarvitse sammuttaa eikä uuttaa! Jos tuote voidaan kiteyttää tai tislata suoraan reaktioseoksesta, sammutusta ja uuttoa ei tarvita. Synteesin suorittaminen Synteesin teko voidaan jakaa kahdeksaan vaiheeseen: 1. Alustavat työt: Tutustu lähtöaineisiin ja reaktion suorittamiseen ja alusta laboratoriopäiväkirja (reaktiokaavio, ainetaulukko). 2. Kokoa laitteisto. 3. Liuota lähtöaineet reaktioliuottimeen reaktiokolvissa. (Normaali lisäys; joskus käytetään myös käänteistä lisäysjärjestystä, jolloin lähtöaine lisätään reaktioasiassa oleviin reagensseihin). 4. Lisää huoneenlämmössä lisättävät reagenssit. 5. Säädä reaktiolämpötila ja sekoitusnopeus. 6. Lisää reagenssit ohjeen mukaisesti. 7. Seuraa reaktion edistymistä (esim. TLC).
23 23 8. Kun reaktio on saavuttanut toivotun edistymisasteen (lähtöaine kulunut kokonaan, tuotejakauma toivottu, sivutuotetta alkaa syntyä tms kriteeri), on aika tehdä päätös reaktion pysäyttämisestä. (ks. alla erillinen kohta reaktion pysäyttämisestä) Reaktion jälkeen kolvissa on reaktioseos, joka sisältää päätuotteen, erilaisia sivutuotteita, reagoimattomia lähtöaineita, liuottimia ja muita mahdollisia epäpuhtauksia (mm. suoloja) eli kaiken mitä olet reaktiokolviin laittanut ja mitä reaktiot ovat tuottaneet. Reaktioissa käytettävä sekoitus Sekoituksella on useimmissa orgaanisissa synteeseissä varsin tärkeä tehtävä: sen avulla voidaan lyhentää reaktioaikaa, parantaa lopputuotteen määrää, edistää reaktion käynnistymistä ja estää ylikuumenemista. Magneettisekoitusta voidaan käyttää, kun reaktio tehdään pienessä mitakaavassa ja reaktioseos on homogeeninen. Reaktioseosten kuumentaminen ja jäähdyttäminen Jos reaktiossa tarvitaan sekoituksen lisäksi kuumennusta (palautuskeittoa eli refluksointia) on laitteisto varustettava palautusjäähdyttimellä. Reaktiosta riippuen voidaan kuumennukseen käyttää joko vesi- tai öljyhaudetta. Lämmityksen tulee olla tasaista, sillä pyöreäpohjaisen kolvin pistemäinen kuumennus saattaa rikkoa koko astian. Monet orgaanisen kemian reaktiot voivat olla liian hitaita tai liian kiivaita huoneenlämpötilassa. Tämän vuoksi reaktioseoksen lämpötilaa on voitava kontrolloida. Lämpötilan kohottaminen lisää reaktionopeutta ja alentaminen vastaavasti hidastaa. Kuumennettaessa reaktioseosta tai tislattaessa on huolehdittava siitä, että ylikuumenemista ei pääse tapahtumaan!
24 24 vesi palautusjäähdytin vesi kolvi haude magneett magneettisekoitin Kuva. Refluksointi laitteisto ÄLÄ KOSKAAN LÄMMITÄ SULJETTUA LAITTEISTOA! Kuumennushauteet Jos liuotin on alhaalla kiehuva neste (esim. eetteri), voidaan käyttää vesihaudetta (+keittolevyä). Yleensä paras haude on öljyhaude (parafiiniöljy) noin 220 C:een saakka. Öljyhauteen lämpötilaa on jatkuvasti tarkkailtava. Öljyhauteeseen ei saa päästää vettä. Jos reaktioseoksessa on metallista natriumia, ei vesihaudetta saa missään tapauksessa käyttää. Kylmähauteet Kylmä- tai jäähdytyshauteita tarvitaan mm. seuraavissa tilanteissa: alentamaan reaktionopeutta, estämään reaktion väli- tai lopputuotteen hajoamista ja parantamaan kiteytyksen saantoa. Esimerkkejä kylmähauteista: virtaava kylmä vesi jäähaude (jäitä + vettä) C NaCl/jää (1:3) C
25 25 Reaktion pysäytys Useimmat reaktiot ovat tasapainoreaktioita. Kun reaktiossa on saavutettu toivottu tasapainotila, se on pysäytettävä. Reaktio voidaan pysäyttää: kontrolloimalla reaktioaikaa kontrolloimalla reaktiolämpötilaa (erityisesti endotermiset reaktiot) sammuttamalla Sammutuksen tarkoituksena on sammuttaa vielä jäljelle jääneet reaktiiviset reagenssit neutraloida reaktioseos Yleensä sammutukseen käytetään vesiliuoksia, jotka säätävät (puskuroivat) ph:n lähelle neutraalia (usein lievästi happamaksi tai lievästi emäksiseksi). Tyypillisiä sammutusliuoksia ovat esim. lievästi emäksinen, kylläinen NaHCO3 tai lievästi hapan, kylläinen NH 4Cl. Valitse sammutusliuos siten, että tuote on täysin stabiili lopullisessa ph:ssa. Sekä vesikerroksen että orgaanisen kerroksen ph on hyvä tarkistaa kostealla phpaperilla. Mitä sammutusliuosta käytän? Neutraalit tai vain lievästi happamat/emäksiset reaktiot: Lievästi emäksiset reaktiot: kylläinen NH 4Cl tai vesi (jäähdytä samalla) Lievästi happamat reaktiot: laimea NaHCO 3 (jäähdytä samalla) Happamat tai emäksiset reaktiot: Neutraloi laimealla emäksellä tai hapolla (esim. NaHCO 3, sitruunahappo, fosforihappo) Vahvasti happamat reaktiot sammutetaan usein ensin vedellä, jolloin ylimääräinen happo voidaan uuttaa pois. Tämän jälkeen orgaanisen kerroksen neutraalius varmistetaan lisäämällä natriumvetykarbonaattia. Kaikkia reaktioita ei välttämättä tarvitse sammuttaa. Mieti, kestääkö tuote vettä tai vesiliuosta? Voiko tuotteen tislata tai kiteyttää suoraan reaktioseoksesta? Sammuta kaikki kylmässä tehtävät reaktiot kylmässä! Jäähdytä kuumennetut reaktiot huoneenlämpöön tai jopa sen alle ennen sammutusta. Sammutusliuos tulee aina lisätä hyvin varovaisesti! Jos sammutettaessa kehittyy kaasuja (esim. hiilidioksidia natriumvetykarbonaatista), saattaa olla turvallisempaa kaataa reaktioseos sammutusliuokseen.
26 26 Eristyksen ja puhdistuksen yksikköoperaatiot Sammutuksen jälkeen orgaaniset tuotteet yleensä eristetään uuttamalla eli vesikerros (jonne suolat ym. liukenevat hyvin) erotetaan orgaanisesta kerroksesta (johon tuote on pääsääntöisesti liuennut). Usein orgaanista kerrosta lisäksi pestään erilaisilla liuoksilla, joiden tehtävänä on säätää ph:ta halutuksi ja/tai uuttaa pois happamia tai emäksisiä reagensseja ja sivutuotteita. Uutto Uutto on tavallisin toimenpide reaktion suorittamisen jälkeen. Nyrkkisääntönä voidaan pitää, että orgaaniset yhdisteet liukenevat paremmin orgaanisiin liuottimiin ja vastaavasti epäorgaaniset yhdisteet veteen. Synteesissä on usein epäorgaanisia aineita: happoja, emäksiä, suoloja, katalyyttejä tai reagensseja, jotka on erotettava reaktioseoksesta, useimmiten uuttamalla, ennen jatkopuhdistusta. Suoritus: 1. Valitse uuttoon kaksi lähes toisiinsa liukenematonta nestettä (esim. eetteri/vesi). Reaktioseoksen eri komponentit jakautuvat liukoisuuksiensa perusteella jompaan kumpaan liuotinkerrokseen. Syntyy liukoisuuksien tasapainotila. 2. Valitse erotussuppilo nestemäärien mukaan. Erotussuppilon tulee olla tilavuudeltaan n. kaksi kertaa uutettavan liuoksen ja uuttoliuoksen yhteenlaskettu tilavuus. 3. Siirrä reaktioseos erotussuppiloon. Huuhtele reaktiokolvi pienellä määrällä käyttämääsi orgaanista liuotinta. 4. Tarkista orgaanisen ja vesifaasien suhteelliset määrät. Tarvittaessa voit lisätä orgaanista liuotinta tai sammutus- tai pesuliuosta. 5. Sulje tulppa. 6. Käännä suppilo ylösalaisin ja avaa hana varovasti. Erotussuppilosta saattaa tällöin vapautua kaasuja. 7. Sulje hana. 8. Ravista kerran ja toista kohdat Ravistele voimakkaasti useita kertoja, ja toista kohdat Aseta erotussuppilo statiivirenkaaseen, poista tulppa ja odota kunnes faasien rajapinta on kirkas.
27 27 Erotussuppilo jätetään seisomaan muutamaksi minuutiksi, jotta eri liuoskerrokset erottuisivat selvästi toisistaan. Joskus syntyy emulsio eli eri liuottimet eivät eroa selvästi toisistaan. Emulsio syntyy helposti varsinkin silloin, kun vesifaasi on emäksinen. Sen hajoamista voidaan nopeuttaa seuraavilla toimenpiteillä: kyllästetään vesifaasi NaCl:lla lisätään reaktioseoksessa olevaa liuotinta heilutetaan samalla pyörittäen (ei ravistelua) jätetään erotussuppilo seisomaan esim. yön yli Kun liuosten rajapinta on selvästi havaittavissa, alempi kerros lasketaan johonkin astiaan! Koskaan ei pidä laskea luulemaansa vesikerrosta suoraan viemäriin. Jos on epävarma, kumpi on vesikerros, kannattaa asia varmistaa yksinkertaisella kokeella: tiputetaan muutama pisara jompaakumpaa liuotinta erotussuppiloon ja katsotaan kumpaan faasiin pisarat asettuvat. 11. Ota molemmat kerrokset talteen. Valitse faaseista käsiteltävä faasi: tavallisesti peset orgaanista faasia vesiliuoksilla tai uutat vesifaasista tuotettasi orgaaniseen faasiin. Jos orgaaninen liuottimesi on raskaampaa kuin vesi, se on myös alempi faasi, jolloin joudut siirtämään sen Erlenmeyer-kolvin kautta takaisin erotussuppiloon. 12. Palaa kohtaan 3. Uuta mieluummin usealla erällä orgaanista liuotinta kuin käyttämällä koko liuotinmäärä kerrallaan, jotta lopputuote saataisiin mahdollisimman hyvin talteen. Nyrkkisääntö: Uuton kokonaisliuotinmäärä on kaksi kertaa alkuperäisen uutettavan liuoksen määrä. Jokaisella uuttokerralla käytettävän liuottimen määrä puolitetaan. Mittaustarkkuudeksi riittää hyvin Erlenmeyereiden asteikko. Mikäli et ole varma onko tuote uuttunut orgaaniseen kerrokseen, aja TLC molemmista kerroksista. Pieni levy (3x4 cm) riittää. Ravistelussa saattaa kehittyä ylipainetta. Ylipainetta syntyy erityisesti tilanteissa, joissa vapautuu kaasuja, esim. CO 2, kun hapanta reaktioseosta pestään natriumkarbonaattiliuoksella. Ylipaineen estämiseksi ravistellaan ensin varovasti; erityisesti CO 2:n kehitys vaatii, että paine saa laueta välillä. Vasta sen jälkeen, kun ylipainetta ei synny, ravistellaan voimakkaasti.
28 28 Uuton vaiheita: Paineen tasaus (hana auki) Hana kiinni ja ravistelu Kerrokset erottumassa Kerrokset erottuneet
29 29 erotussuppilo vesifaasi (tai orgaaninen faa orgaaninen faasi (tai vesifaasi) erla Faasin talteenotto Aktiivinen uutto Edellä kuvattu uuttaminen kahdella eri liuottimella perustuu aineiden liukoisuuksien eroon eri liuottimien välillä. Yleensä haluttu päätuote liukenee paremmin orgaaniseen liuottimeen. Aktiivinen uutto perustuu siihen, että komponentit reagoivat liuottimen kanssa; useimmiten syntyy suola. Yleensä suolat ovat vesiliukoisia, mikä tarkoittaa sitä, että orgaaninen aine (happo tai emäs) muodostaessaan suolan siirtyy aktiivisessa uutossa vesifaasiin. Kun eri kerrokset on erotettu toisistaan, voidaan orgaaniset komponentit erottaa vesifaasista tekemällä se joko happamaksi (2 M HCl) tai emäksiseksi (2 M NaOH) riippuen synteesistä. Esimerkki: 1-fenyylietyyliamiinin erottaminen asetofenonista Reaktioseoksesta, jossa on 1-fenyylietyyliamiinia NH 3 Cl O (hydrokloridisuolana) ja asetofenonia voidaan + asetofenoni uuttaa pois tolueenilla, jolloin 1- liukenee veteen NaOH liukenee tolueeniin (uutetaan pois) fenyylietyyliamiinin HCl-suola jää vesiliuokseen. Kun vesiliuos tehdään emäksiseksi, 1-fenyylietyyliamiini. HCl deprotonoituu (pk a n. 10) ja vapaa amiini voidaan tislata NH 2 tai uuttaa pois vesiliuoksesta asetofenonin häiritsemättä.
30 30 Kuivaus Orgaaniset uutteet täytyy kuivata ennen haihdutusta. Kuivauksella on kaksi päätehtävää: poistaa orgaanisessa faasissa mahdollisesti pisaroina olevat suolaliuokset, jotta raakatuotteeseen ei jäisi mitään vesifaasista peräisin olevia aineita imeä itseensä suurin osa orgaaniseen faasiin liuenneesta vedestä. Vesi voi aiheuttaa räiskymistä haihdutettaessa ja pahimmassa tapauksessa raakatuotteeseen jää vettä pisaroina. Veden haihduttaminen on aina hankalampaa ja hitaampaa kuin tyypillisten orgaanisten liuottimien haihduttaminen. Yleensä kuivausaineina käytetään natriumsulfaattia (Na2SO4) tai magnesiumsulfaattia (MgSO 4). Nämä muodostavat nopeasti veden kanssa huoneenlämmössä stabiileja hydraatteja (esim. Na2SO4. 10H2O), mutta eivät liukene käytännössä lainkaan orgaanisiin liuottimiin (poikkeuksena alkoholit). Hydraatit hajoavat kuumennettaessa, joten natriumsulfaattia tai magnesiumsulfaattia ei voi käyttää tislauksen yhteydessä. Magnesiumsulfaatti on heikko Lewis-happo. Yleiskäyttöön kannattaa sen vuoksi käyttää natriumsulfaattia. Suoritus 1. Lisää kuivattavaan liuokseen (uutteeseen) n. 1-2 teelusikallista (n. 3-6 grammaa) natriumsulfaattia / 100 ml kuivattavaa liuosta. 2. Pyöräytä astiaa varovaisesti. Jos natriumsulfaatti paakkuuntuu astian pohjalle tai pohjalla näkyy vielä pisaroita, lisää vielä 1-2 teelusikallista natriumsulfaattia. Kuivausainetta on tarpeeksi, kun seoksessa ei enää näy pisaroita. 3. Odota 5-10 minuuttia. Tällä välin voit valmistella kuivausaineen suodatuksen. 4. Paina kartiomaiseen lasisuppiloon pieni sormenpään kokoinen pumpulituppo tiiviisti, mutta ei liian tiiviisti, kiinni esim. spaattelilla.
31 31 5. Valitse haihdutuskolviksi sellainen kolvi, jonka tilavuus on vähintään kaksinkertainen kuivatun liuoksen tilavuuteen nähden. Tue kolvi kouralla ja aseta suppilo kolviin. HUOM: Suppilon ja kolvin kaulan väliin tulee jäädä ilmarako! 6. Suodata kuivausaine pois pumpulin läpi. Kun kaadat liuosta suppiloon, varo nesteen mukana tulevia kuivausainepaakkuja, jotka saattavat räiskyttää liuosta. 7. Huuhtele astiat ja kuivausaine 3-4 kertaa pienellä määrällä uuttoliuotinta. Voit tarkistaa TLC:llä, jäikö kuivausaineen sekaan vielä tuotetta. Haihdutus Kuivauksen jälkeen orgaanisesta kerroksesta voidaan poistaa liuotin joko tavallisella tislauksella, alipainetislauksella tai rotavaporilla (pyöröhaihdutin). Tislaus ja alipainetislaus ovat hyviä menetelmiä, mikäli tuote kestää kuumennusta. Rotavapori on näitä hellävaraisempi menetelmä. Kun liuotin on poistettu, saadaan raakatuote, jota usein joudutaan vielä puhdistamaan eri menetelmillä (esim. tislaus, kiteytys). Raakatuotteen määrä on syytä punnita aina! Näin pystyt seuraamaan reaktion ainetasetta! Rotavapori vastaa nopeutettua alipainetislausta. Magneettisekoituksen asemesta kolvia pyöritetään moottorilla, jolloin lämmönsiirto nopeutuu ja haihtuminen tehostuu. Alipainelähteenä käytetään pumppua.
32 32 Rotavaporin käyttö 1. Tarkasta, että rotavaporissa on roiskesuoja ja että se on puhdas. Tarkasta myös, että keruukolvi on tyhjä. Keruukolvit tyhjennetään liuotinjäteastioihin. 2. Laita rotavaporin vakuumipumppu päälle. Varmista, että pumpun ja rotavaporin välinen venttiili on kiinni. 3. Avaa jäähdytysvesikierto. 4. Kiinnitä haihdutuskolvi rotavaporiin. Käytä muoviklipsiä varmistamaan, ettei kolvi putoa.
33 33 5. Sulje rotavaporin ylähana ja käynnistä pyöritys. Sopiva pyöritysnopeus on n. 60 rpm. 6. Avaa varovasti pumpun ja rotavaporin välinen venttiili. Seuraa paineen alenemista pumpun painemittarista. Jos liuos kuohuu, ole valmiina avaamaan heti rotavaporin ylähana ja sulkemaan pumpun ja rotavaporin välinen venttiili. 7. Laske kolvi vesihauteeseen. Haihdutusta voi nopeuttaa lämmittämällä vesihaudetta (hauteen max. lämpötila n. +35 C). 8. Lopeta haihdutus, kun tislettä ei enää kerry lisää. Päästä ilma hitaasti laitteistoon: Sulje pumpun ja rotavaporin välinen venttiili. Lopeta pyöritys ja avaa rotavaporin ylähana pitäen samalla kiinni kolvista. Sulje jäähdytysvesikierto. 9. Tyhjennä keruukolvit. Pyöröhaihduttajan pumppuosa
34 34 Puhdistuksen yksikköoperaatiot Tislaus lämpömittari tislausvälikappale jäähdytin tislauskolvi vesi vesi tislausmutka haude keräysastia magneettisekoitin Kuva. Tislauslaitteisto Tislaus on käyttökelpoisin menetelmä nesteiden puhdistamiseksi ja sitä käytetään rutiinina liuottimien ja reagenssien puhdistamisessa. Tislauksen käyttö: liuottimen pois haihduttaminen synteesin jälkeen nesteiden erottaminen, kun niiden kiehumispisteet eroavat tarpeeksi toisistaan. Normaalipainetislauksessa kiehumispisteiden eron on oltava 50 o C, jakotislauksessa o C. Lämpöherkät aineet tislataan alipaineessa. nestemäisen aineen puhdistaminen.
35 35 Joitakin turvallisuusohjeita ennen kuin aloitat: Älä koskaan lämmitä suljettua systeemiä. Pidä syttyvät orgaaniset liuottimet kaukana liekistä, kipinälähteistä ja hyvin kuumista pinnoista (kauempana kuin 1,5 m eli eri vetokaapissa). Älä koskaan päästä tislauskolvia täysin kuivaksi. Tarkista, että yhdiste, jonka tislaat on termisesti stabiili. Tislauksen vaiheet 1. Täytä sopivan kokoinen tislauskolvi korkeintaan 2/3-tilavuuden verran. 2. Lisää tislauskolviin magneettisauva (tai keitinkiviä normaalipainetislauksessa). 3. Valitse sopiva lämmityshaude, joko vesi- tai öljyhaude. Hauteen lämpötilan tulee olla n. 20 C korkeampi kuin tislattavan aineen kiehumispiste. 4. Valitse tislattavan aineen kiehumispisteen perusteella sopiva jäähdytys: - kp. alle 120 C: virtaava vesi - kp. yli 120 C: seisova vesi jäähdyttimessä - kp. yli 150 C: ilmajäähdytys, jos on pelättävissä, että tislattava aine kiinteytyy. 5. Aloita lämmitys. Hauteen lämpötilan voi nostaa kohtalaisen nopeasti tislauslämpötilaan (ks. kohta3). 6. Tarkkaile tislautumisnopeutta. Nopeus on hyvä, kun tislettä syntyy n. 1 tippa/sekunti. 7. Jos kiehumispiste on korkea (>150 C), tislausmutka voidaan peittää foliolla. 8. Tislauksessa saadaan eri lämpötiloissa kiehuvia nestemääriä eli jakeita, jotka voidaan jakaa seuraavasti: 1. esi- tai alkutisle = liuotin ja alempana kiehuvat epäpuhtaudet 2. varsinainen tisle 3. jälkitisle = ylempänä kiehuvat epäpuhtaudet 4. tislausjäännös Tislauskolvia ei saa koskaan päästää täysin kuivaksi! 9. Jos seoksen eri komponenttien kiehumispisteet eroavat toisistaan alle 50 C käytetään fraktiointikolonneja (ks. jako- eli fraktiotislaus, alla).
36 36 Fraktiotislaus Yhdisteiden, joiden kiehumispisteet eroavat C, erottamisessa täytyy käyttää laitteistoa, jossa tiivistyminen ja höyrystyminen tapahtuu useita kertoja eli tislauskolonnia. Tislauskolonnissa tapahtuvien tiivistymis- ja höyrystymiskertojen määrää kuvataan käsitteellä teoreettinen pohja. Hyvässä teollisessa tislauskolonnissa teoreettisia pohjia voi olla useita kymmeniä; laboratoriokolonneissa useimmiten kuitenkin vain muutamia. Laboratoriossa käytetään yleisesti Vigreux-kolonnia, jollaisia on käytössä myös oppilaslaboratoriossa. Kolonnina voidaan käyttää myös lasikappaleilla täytettyä lasiputkea, jolloin voidaan saavuttaa parempi erotus. Tällöin kuitenkin pieniä määriä tislattaessa kolonniin jää melko paljon tislattavaa ainetta. Alipainetislaus Monet aineet hajoavat kuumennettaessa kiehumispisteeseen, joten niiden tislaaminen ilmanpaineessa ei onnistu. Joissakin tapauksissa hajoaminen voidaan välttää tislaamalla alipaineessa. Kiehumispiste riippuu paineesta, ja se voidaan arvioida paine-lämpötila nomogrammista ( Alipaineen aikaansaamiseksi käytetään öljy- (n. 0,1 mmhg) tai vesisuihkupumppua (n. 15 mmhg). Oppilaslaboratoriossa on käytössä öljypumppuja, joihin on suora liitäntä jokaisesta vetokaapista. Alipainetislauslaitteisto on lähes samanlainen kuin normaalitislauslaitteisto. Laitteistossa on huomiotava useamman fraktion kerääminen ilman, että alipaine häviää laitteistosta. Yksinkertaisinta on käyttää tisleenjakajaa (ns. Saarijärven Liisa, cow adapter). Alipainetislauksen suorittaminen 1. Kaada tislattava aine kolviin (korkeintaan 2/3 kolvin tilavuudesta) ja lisää magneettisauva (keitinkivet eivät riitä alipaineessa). 2. Kokoa laitteisto. Varmista, että keräysastia ja tisleenjakaja pysyvät paikoillaan käyttäen klipsejä ja yhdistä laitteisto sekä pumppuun että manometriin kolmitiehanalla. 3. Tarkista, että manometrin hana on kiinni ennen kuin imet laitteistoon vakuumin. 4. Varmista, että tislauskolvissa on magneettisekoitus päällä. 5. Alipaineen aikaansaamiseksi laitteistoon
37 37 a) Öljypumpulla (käytössä oppilaslabrassa) Kolmitiehanan pumppuun menevä alipaineletku liitetään suoraan vetokaapissa olevaan pumppuliitäntään Käynnistetään pumppu Avataan pumppuliitäntä (kääntämällä kahvasta) ja säädetään alipainetta venttiilin avulla Odota hetki paineen alenemista ja avaa sitten manometrin hana seurataksesi paineen stabiloitumista b) vesisuihkupumpulla (ei käytössä oppilaslabrassa): Avaa Wulffin pullon hana ja sulje manometrin hana Kierrä vesisuihkupumpun hana täysin auki Sulje Wulffin pullon hana kun paine on alentunut (mikä kuullaan vesisuihkupumpun äänestä), avaa manometrin hana ja seuraa paineen alenemista ja stabiloitumista 6. Lämmitä kolvia hitaasti, jotta haihtuvat epäpuhtaudet tislautuvat ensin ja tämän jälkeen tuote. Tarkkaile lämpötilaa ja painetta. Kerää esitisle sekä pääfraktio, joka tislautuu vakiolämpötilassa. 7. Lopeta tislaus poistamalla lämmitys, kun nestemäärä tislauskolvissa on pieni. 8. Päästä ilma hitaasti laitteistoon seuraavasti: manometrin hana suljetaan Pumpun venttiili suljetaan ja ilma päästetään laitteistoon irroittamalla pumppuliitännässä kiinni oleva alipaineletku (kun käytössä öljypumppu) TAI Wulffin pullon hana avataan ja vesisuihkupumppu suljetaan (kun käytössä vesisuihkupumppu) manometrin hana avataan hitaasti, jotta se ei vaurioidu ja elohopeaa ei joudu laboratorion tiloihin
38 38 tislauslaitteisto vesi vesi kolmitiehana liitetän vesisuihkupumppuun Wulffin pullo muista sekoitus! paksuseinäinen alipaineletku manometri Kuva. Alipainetislauslaitteisto Kiteytys Kiinteän, kiteisen tuotteen puhdistukseen riittää joskus pelkkä kiteiden pesu kylmällä liuottimella. Useimmiten tarvitaan uudelleenkiteytys, jotta päästäisiin eroon liukenemattomista tai värillisistä epäpuhtauksista. Menetelmä perustuu puhdistettavan aineen ja epäpuhtauksien liukoisuuseroon sekä epäpuhtauksien suhteellisen pieneen määrään. Uudelleenkiteytyksessä synteesin raakatuote pyritään liuottamaan palautusjäähdyttimellä varustetussa kiteytyskolvissa mahdollisimman pieneen määrään kuumaa liuotinta, jotta saadaan tulokseksi kylläinen liuos. Liuokseen lisätään siemenkide (jos sellaisia on käytettävissä) ja annetaan seoksen jäähtyä hitaasti, jolloin tuote kiteytyy ja epäpuhtaudet jäävät emäliuokseen. Kiteytysliuottimen kiehumispisteen on oltava vähintään 10 o C alempi kuin kiteytettävän aineen sulamispisteen, jotta kiteytettävä aine ei sula ennen liukenemistaan. Jos tuotteessa on liukenemattomia epäpuhtauksia, ne suodatetaan pois kuumasta liuoksesta. Tämä on usein hankalaa (liuos ei pysykään kuumana suodatettaessa, jolloin myös tuote alkaa
LÄÄKETEHTAAN UUMENISSA
 LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
LÄÄKETEHTAAN UUMENISSA KOHDERYHMÄ: Soveltuu lukion KE1- ja KE3-kurssille. KESTO: n. 1h MOTIVAATIO: Työskentelet lääketehtaan laadunvalvontalaboratoriossa. Tuotantolinjalta on juuri valmistunut erä aspiriinivalmistetta.
Liukeneminen 31.8.2016
 Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
sulfatiatsoli meripihkahappoanhydridi eli dihydro-2,5- furaanidioni etanoli (EtaxA, 99 %)
 ANTIBIOOTTISYNTEESI TAUSTAA Olet kesätöissä lääketehtaalla. Lääkefirman kemistit ovat kehittäneet antibiootin, sulfiatsolin, joka estää bakteerien foolihapon synteesiä. Foolihappoa tarvitaan esimerkiksi
ANTIBIOOTTISYNTEESI TAUSTAA Olet kesätöissä lääketehtaalla. Lääkefirman kemistit ovat kehittäneet antibiootin, sulfiatsolin, joka estää bakteerien foolihapon synteesiä. Foolihappoa tarvitaan esimerkiksi
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt
 KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
KEMS448 Fysikaalisen kemian syventävät harjoitustyöt Jakaantumislaki 1 Teoriaa 1.1 Jakaantumiskerroin ja assosioituminen Kaksi toisiinsa sekoittumatonta nestettä ovat rajapintansa välityksellä kosketuksissa
c) Nimeä kaksi alkuainetta, jotka kuuluvat jaksollisessa järjestelmässä samaan ryhmään kalsiumin kanssa.
 Kurssikoe KE1.2, Ihmisen ja elinympäristön kemia, ke 6.4. 2016 Vastaa vain kuuteen tehtävään. Jokaisessa tehtävässä maksimi pistemäärä on kuusi pistettä (paitsi tehtävässä 7 seitsemän pistettä). Voit vapaasti
Kurssikoe KE1.2, Ihmisen ja elinympäristön kemia, ke 6.4. 2016 Vastaa vain kuuteen tehtävään. Jokaisessa tehtävässä maksimi pistemäärä on kuusi pistettä (paitsi tehtävässä 7 seitsemän pistettä). Voit vapaasti
Jos eristysvaiheessa saadaan erotettua tuote kiinteänä, kiteytyy esimerkiksi kaadettaessa reaktioseos veteen, käytetään imusuodatusta.
 Eristysvaihe: Perusmenetelmä orgaanisten yhdisteiden eristämisessä reaktioseoksesta on uutto orgaanisella liuottimella jota yleensä seuraa aktiivinen uutto. Menetelmä luonnollisesti perustuu siihen, että
Eristysvaihe: Perusmenetelmä orgaanisten yhdisteiden eristämisessä reaktioseoksesta on uutto orgaanisella liuottimella jota yleensä seuraa aktiivinen uutto. Menetelmä luonnollisesti perustuu siihen, että
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
SIPSEISSÄKÖ RASVAA? KOKEELLINEN TYÖ: PERUNALASTUJA VAI JUUSTONAKSUJA? Tämän työn tavoite on vertailla eri sipsilaatuja ja erottaa sipsistä rasva.
 SIPSEISSÄKÖ RASVAA? TAUSTAA Saamme rasvaa joka päivä ja monissa muodoissa. Osa rasvasta on välttämätöntä, koska elimistömme tarvitsee rasvaa elintoimintojemme ylläpitoon. Saamme hyvin paljon rasvaa piilossa
SIPSEISSÄKÖ RASVAA? TAUSTAA Saamme rasvaa joka päivä ja monissa muodoissa. Osa rasvasta on välttämätöntä, koska elimistömme tarvitsee rasvaa elintoimintojemme ylläpitoon. Saamme hyvin paljon rasvaa piilossa
SAIPPUALIUOKSEN SÄHKÖKEMIA 09-2009 JOHDANTO
 SAIPPUALIUOKSEN SÄHKÖKEMIA 09-009 JOHDANTO 1 lainaus ja kuvat lähteestä: Työssä tutkitaan johtokyky- ja ph-mittauksilla tavallisen palasaippuan kemiallista koostumusta ja misellien ja aggregaattien muodostumista
SAIPPUALIUOKSEN SÄHKÖKEMIA 09-009 JOHDANTO 1 lainaus ja kuvat lähteestä: Työssä tutkitaan johtokyky- ja ph-mittauksilla tavallisen palasaippuan kemiallista koostumusta ja misellien ja aggregaattien muodostumista
Kasvien piilotetut väriaineet
 KOHDERYHMÄ: Työ sopii parhaiten lukioon kursseille KE1 tai KE2. Työn voi tehdä myös yläkoululaisten kanssa kurssilla raaka-aineet ja tuotteet, jolloin keskitytään poolittomuuden sijaan erotusmenetelmiin.
KOHDERYHMÄ: Työ sopii parhaiten lukioon kursseille KE1 tai KE2. Työn voi tehdä myös yläkoululaisten kanssa kurssilla raaka-aineet ja tuotteet, jolloin keskitytään poolittomuuden sijaan erotusmenetelmiin.
ABT 2000kg Haarukkavaunun käyttöohje
 ABT 2000kg Haarukkavaunun käyttöohje HUOM! Käyttäjän tulee lukea käyttöohje ennen käytön aloittamista. 1. YLEISKUVAUS Kapasiteetti Max. haarukoiden korkeus Min. haarukoiden korkeus Haarukoiden pituus Vaunun
ABT 2000kg Haarukkavaunun käyttöohje HUOM! Käyttäjän tulee lukea käyttöohje ennen käytön aloittamista. 1. YLEISKUVAUS Kapasiteetti Max. haarukoiden korkeus Min. haarukoiden korkeus Haarukoiden pituus Vaunun
KOHDERYHMÄ KESTO: MOTIVAATIO: TAVOITE: AVAINSANAT: - TAUSTAA
 ANTIBIOOTTISYNTEESI KOHDERYHMÄ: Työ soveltuu ensisijaisesti lukiolaisille. Lukiossa työn voi toteuttaa kurssilla KE3 tai työkurssilla. KESTO: Työ kestää 90 min (refluksointi 60min) (120 min tislauksen
ANTIBIOOTTISYNTEESI KOHDERYHMÄ: Työ soveltuu ensisijaisesti lukiolaisille. Lukiossa työn voi toteuttaa kurssilla KE3 tai työkurssilla. KESTO: Työ kestää 90 min (refluksointi 60min) (120 min tislauksen
SIPSEISSÄKÖ RASVAA? KOKEELLINEN TYÖ: PERUNALASTUJA VAI JUUSTONAKSUJA?
 SIPSEISSÄKÖ RASVAA? TAUSTAA Saamme rasvaa joka päivä ja monissa muodoissa. Osa rasvasta on välttämätöntä, koska elimistömme tarvitsee rasvaa elintoimintojemme ylläpitoon. Saamme hyvin paljon rasvaa piilossa
SIPSEISSÄKÖ RASVAA? TAUSTAA Saamme rasvaa joka päivä ja monissa muodoissa. Osa rasvasta on välttämätöntä, koska elimistömme tarvitsee rasvaa elintoimintojemme ylläpitoon. Saamme hyvin paljon rasvaa piilossa
Juha Siitonen Jyväskylän yliopisto. Syntetiikan töitä
 Juha Siitonen Jyväskylän yliopisto Syntetiikan töitä Orgaanisen kemian työmenetelmistä Reuksointi Reuksointi käsittää reaktioseoksen keittämisen palautusjäähdyttimen alla niin, että höyrystyvät reagenssit
Juha Siitonen Jyväskylän yliopisto Syntetiikan töitä Orgaanisen kemian työmenetelmistä Reuksointi Reuksointi käsittää reaktioseoksen keittämisen palautusjäähdyttimen alla niin, että höyrystyvät reagenssit
Sisällys. Opitaan fysiikkaa ja kemiaa 7. 1 Fysiikka ja kemia tutkivat luonnon tapahtumia...8 2 Tutkitaan turvallisesti...12. Lähdetään liikkeelle 17
 Sisällys Opitaan fysiikkaa ja kemiaa 7 1 Fysiikka ja kemia tutkivat luonnon tapahtumia...8 2 Tutkitaan turvallisesti...12 Lähdetään liikkeelle 17 3 Mitä pidemmälle, sitä nopeammin...18 4 Ilman voimaa liike
Sisällys Opitaan fysiikkaa ja kemiaa 7 1 Fysiikka ja kemia tutkivat luonnon tapahtumia...8 2 Tutkitaan turvallisesti...12 Lähdetään liikkeelle 17 3 Mitä pidemmälle, sitä nopeammin...18 4 Ilman voimaa liike
Kemiaa tekemällä välineitä ja työmenetelmiä
 Opiskelijalle 1/4 Kemiaa tekemällä välineitä ja työmenetelmiä Ennen työn aloittamista huomioi seuraavaa Tarkista, että sinulla on kaikki tarvittavat aineet ja välineet. Kirjaa tulokset oikealla tarkkuudella
Opiskelijalle 1/4 Kemiaa tekemällä välineitä ja työmenetelmiä Ennen työn aloittamista huomioi seuraavaa Tarkista, että sinulla on kaikki tarvittavat aineet ja välineet. Kirjaa tulokset oikealla tarkkuudella
780301A TUTKIMUSHARJOITTELU: ORGAANISEN KEMIAN LABORATORIO-OSUUS TYÖLUENTO SYKSY 2015
 780301A TUTKIMUSHARJOITTELU: ORGAANISEN KEMIAN LABORATORIO-OSUUS TYÖLUENTO SYKSY 2015 Kurssilla tarvitaan työohjemoniste (tulostetaan Nopasta) välttämättömät: laboratoriotakki, suojalasit (lainattavissa
780301A TUTKIMUSHARJOITTELU: ORGAANISEN KEMIAN LABORATORIO-OSUUS TYÖLUENTO SYKSY 2015 Kurssilla tarvitaan työohjemoniste (tulostetaan Nopasta) välttämättömät: laboratoriotakki, suojalasit (lainattavissa
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
KLOORIJÄÄMÄT JUOMAVE- DESSÄ
 KLOORIJÄÄMÄT JUOMAVE- DESSÄ KOHDERYHMÄ: Työ on suunniteltu lukiolaisille, mutta työtä voi soveltaa myös yläkouluun. Tällöin kuvaajan piirtäminen ja spektrofotometrin teoria jätetään pois tai sitä supistetaan
KLOORIJÄÄMÄT JUOMAVE- DESSÄ KOHDERYHMÄ: Työ on suunniteltu lukiolaisille, mutta työtä voi soveltaa myös yläkouluun. Tällöin kuvaajan piirtäminen ja spektrofotometrin teoria jätetään pois tai sitä supistetaan
12. Amiinit. Ammoniakki 1 amiini 2 amiini 3 amiini kvarternäärinen ammoniumioni
 12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
12. Amiinit Amiinit ovat ammoniakin alkyyli- tai aryylijohdannaisia. e voivat olla primäärisiä, sekundäärisiä tai tertiäärisiä ja lisäksi ne voivat muodostaa kvaternäärisiä ammoniumioneja. Ammoniakki 1
ALKOHOLIT SEKAISIN KOHDERYHMÄ:
 ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
ALKOHOLIT SEKAISIN KOHDERYHMÄ: Työ soveltuu lukion kursseille KE1, KE2 ja KE4. KESTO: Työ kestää n.1h MOTIVAATIO: Työ on havainnollinen ja herättää pohtimaan kaasujen kemiaa. TAVOITE: Työssä opiskelija
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
Seosten erotusmenetelmiä
 Seosten erotusmenetelmiä KEMIAA KAIKKIALLA, KE1 Kemiassa on usein tarve erottaa niin puhtaita aineita kuin myös seoksia toisistaan. Seoksesta erotetaan sen komponentteja (eli seoksen muodostavia aineita)
Seosten erotusmenetelmiä KEMIAA KAIKKIALLA, KE1 Kemiassa on usein tarve erottaa niin puhtaita aineita kuin myös seoksia toisistaan. Seoksesta erotetaan sen komponentteja (eli seoksen muodostavia aineita)
Sunwind Cuisine 50cm pöytäliesi
 Sunwind Cuisine 50cm pöytäliesi Asennus- ja käyttöohje Tuotenumero: 340002/340004 Yleisiä ohjeita ja suosituksia: 1. Kaasulieden asennuksen yhteydessä 1. Poista pakkausmateriaalit lieden sisäpuolelta ja
Sunwind Cuisine 50cm pöytäliesi Asennus- ja käyttöohje Tuotenumero: 340002/340004 Yleisiä ohjeita ja suosituksia: 1. Kaasulieden asennuksen yhteydessä 1. Poista pakkausmateriaalit lieden sisäpuolelta ja
Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan?
 2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
2.1 Kolme olomuotoa Mitkä ovat aineen kolme olomuotoa ja miksi niiden välisiä olomuodon muutoksia kutsutaan? pieni energia suuri energia lämpöä sitoutuu = endoterminen lämpöä vapautuu = eksoterminen (endothermic/exothermic)
ALKOHOLIT SEKAISIN TAUSTAA
 ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
ALKOHOLIT SEKAISIN TAUSTAA Kaasukromatografia on menetelmä, jolla voidaan tutkia haihtuvia, orgaanisia yhdisteitä. Näyte syötetään tavallisesti ruiskulla injektoriin, jossa se höyrystyy ja sekoittuu inerttiin
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Kestopreparaatin tekeminen. Antti Haarto 27.2.2013
 Kestopreparaatin tekeminen Antti Haarto 27.2.2013 Genitaalien rakenne Esiesivalmistelut Koiraat Levitystä tehtäessä vaikeasti määritettäviltä lajeilta kannattaa levittää myös sivulämssät genitaaleista
Kestopreparaatin tekeminen Antti Haarto 27.2.2013 Genitaalien rakenne Esiesivalmistelut Koiraat Levitystä tehtäessä vaikeasti määritettäviltä lajeilta kannattaa levittää myös sivulämssät genitaaleista
Stipendiaattityöt Jyväskylän yliopiston kemian laitos
 Stipendiaattityöt Jyväskylän yliopiston kemian laitos Juha Siitonen 14. Elokuuta 2011 Alkuaineita jos tunne sä et Niiden kykyjä vähättelet minaisuudet peittelet Turha sun on koittaa Sieluja voittaa Goethe
Stipendiaattityöt Jyväskylän yliopiston kemian laitos Juha Siitonen 14. Elokuuta 2011 Alkuaineita jos tunne sä et Niiden kykyjä vähättelet minaisuudet peittelet Turha sun on koittaa Sieluja voittaa Goethe
Törmäysteoria. Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa
 Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Paula Kajankari 2015. LUMA-kerho Kokeellista kemiaa. Kohderyhmä 5 6 luokkalaiset. Laajuus 90 minuuttia x 5 kerhokertaa
 LUMA-kerho Kokeellista kemiaa Kohderyhmä 5 6 luokkalaiset Laajuus 90 minuuttia x 5 kerhokertaa Tavoite Tavoitteena on osoittaa oppilaille, että luonnontieteiden opiskelu voi olla muutakin kuin kirjasta
LUMA-kerho Kokeellista kemiaa Kohderyhmä 5 6 luokkalaiset Laajuus 90 minuuttia x 5 kerhokertaa Tavoite Tavoitteena on osoittaa oppilaille, että luonnontieteiden opiskelu voi olla muutakin kuin kirjasta
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Biodiesel Tuotantomenetelmien kemiaa
 Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Biodiesel Tuotantomenetelmien kemiaa Tuotantomenetelmät Kasviöljyjen vaihtoesteröinti Kasviöljyjen hydrogenointi Fischer-Tropsch-synteesi Kasviöljyt Rasvan kemiallinen rakenne Lähde: Malkki, Rypsiöljyn
Tiedelimsa. KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä.
 KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
KOHDERYHMÄ: Työ voidaan tehdä kaikenikäisien kanssa. Teorian laajuus riippuu ryhmän tasosta/iästä. KESTO: 15min 1h riippuen työn laajuudesta ja ryhmän koosta. MOTIVAATIO: Arkipäivän kemian ilmiöiden tarkastelu
TÄS ON PROTSKUU! PROTEIINIEN KEMIAA
 sivu 1/8 TÄS ON PROTSKUU! PROTEIINIEN KEMIAA LUOKKA-ASTE/KURSSI TAUSTA Työ soveltuu peruskoulun yläasteelle ja lukioon. Työn tavoite on tutustua proteiinien kokeellisiin tunnistusmenetelmiin. POHDITTAVAKSI
sivu 1/8 TÄS ON PROTSKUU! PROTEIINIEN KEMIAA LUOKKA-ASTE/KURSSI TAUSTA Työ soveltuu peruskoulun yläasteelle ja lukioon. Työn tavoite on tutustua proteiinien kokeellisiin tunnistusmenetelmiin. POHDITTAVAKSI
kemiallisesti puhdas vesi : tislattua vettä käytetään mm. höyrysilitysraudoissa (saostumien ehkäisy)
 Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
MOTIVAATIO: Olet harjoittelijana vedenpuhdistuslaitoksella. Juomavedeksi käsiteltävän veden desinfiointivaiheesta
 KOHDERYHMÄ: Työ on suunniteltu lukiolaisille, mutta työtä voi soveltaa myös yläkouluun. Tällöin kuvaajan piirtäminen ja spektrofotometrin teoria jätetään pois tai sitä supistetaan sopivasti. Lukiossa työ
KOHDERYHMÄ: Työ on suunniteltu lukiolaisille, mutta työtä voi soveltaa myös yläkouluun. Tällöin kuvaajan piirtäminen ja spektrofotometrin teoria jätetään pois tai sitä supistetaan sopivasti. Lukiossa työ
Marjan makuisia koruja rautalangasta ja helmistä -Portfolio
 Marjan makuisia koruja rautalangasta ja helmistä -Portfolio Saara Lohi 2007 Suunnittelu ja tavoitteet Suunnittelun lähtökohtana oli kuva pihlajanmarjoista pajumatolla. Tavoitteena on suunnitella ja toteuttaa
Marjan makuisia koruja rautalangasta ja helmistä -Portfolio Saara Lohi 2007 Suunnittelu ja tavoitteet Suunnittelun lähtökohtana oli kuva pihlajanmarjoista pajumatolla. Tavoitteena on suunnitella ja toteuttaa
Merkintöjen tekeminen pohjakuvaan Libre Officella v.1.2
 v.1.2 Tämän ohjeen avulla voit piirtää omia merkintöjäsi olemassa olevan pohjakuvan päälle. Ohje on tehty käyttäen LibreOfficen versiota 5.0, mutta se toimii melko hyvin myös vanhempien versioiden kanssa.
v.1.2 Tämän ohjeen avulla voit piirtää omia merkintöjäsi olemassa olevan pohjakuvan päälle. Ohje on tehty käyttäen LibreOfficen versiota 5.0, mutta se toimii melko hyvin myös vanhempien versioiden kanssa.
BIOMUOVIA TÄRKKELYKSESTÄ
 BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
BIOMUOVIA TÄRKKELYKSESTÄ KOHDERYHMÄ: Soveltuu peruskoulun 9.luokan kemian osioon Orgaaninen kemia. KESTO: 45 60 min. Kemian opetuksen keskus MOTIVAATIO: Muovituotteet kerääntyvät helposti luontoon ja saastuttavat
P-Frami sopimusasiakkaan käyttöohje
 TALON KÄYTTÄJÄT - 1- ja 2- kerros ammattikorkeakoulun henkilökunta (+vieraspysäköinti) - 1-kerrokseen kulku sekä pohjois- että eteläpäästä - 2-kerrokseen suositellaan kulkua pohjoispäästä (kierrerampin
TALON KÄYTTÄJÄT - 1- ja 2- kerros ammattikorkeakoulun henkilökunta (+vieraspysäköinti) - 1-kerrokseen kulku sekä pohjois- että eteläpäästä - 2-kerrokseen suositellaan kulkua pohjoispäästä (kierrerampin
7992FI WG 80 Talvipuutarhan liukuosat Talvipuutarhan kiinteät osat ks. sivu 16
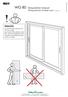 7992FI WG 80 Talvipuutarhan liukuosat Talvipuutarhan kiinteät osat ks. sivu 16 Willab Garden 2015-11 TÄRKEÄÄ! Lue asennusohje kokonaan ennen kuin aloitat asennuksen! Ellei ohjeita noudateta, osat eivät
7992FI WG 80 Talvipuutarhan liukuosat Talvipuutarhan kiinteät osat ks. sivu 16 Willab Garden 2015-11 TÄRKEÄÄ! Lue asennusohje kokonaan ennen kuin aloitat asennuksen! Ellei ohjeita noudateta, osat eivät
joka voidaan määrittää esim. värinmuutosta seuraamalla tai lukemalla
 REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
Sähköpostiohjeet. Tehokas ja huoleton sähköposti
 Sähköpostiohjeet 1 Uuden PST tiedoston luominen sähköposteille... 3 Tärkeää!... 3 Tiedoston luominen... 3 Kansioiden luominen datatiedostoon... 5 Pikatoimintojen luominen... 8 Odottaa vastausta allekirjoitus...
Sähköpostiohjeet 1 Uuden PST tiedoston luominen sähköposteille... 3 Tärkeää!... 3 Tiedoston luominen... 3 Kansioiden luominen datatiedostoon... 5 Pikatoimintojen luominen... 8 Odottaa vastausta allekirjoitus...
RAUTAFOSFATOINNIN VESIEN SIIRROT. Copyright Isto Jokinen
 RAUTAFOSFATOINNIN VESIEN SIIRROT VESIEN SIIRTÄMISEN SYYT Vesien siirtoa tehdään kahdesta syystä: 1. Rautafosfatointialtaasta ja huuhtelu 1:stä haihtuu runsaasti vettä koska nesteet ovat kuumia ja niitä
RAUTAFOSFATOINNIN VESIEN SIIRROT VESIEN SIIRTÄMISEN SYYT Vesien siirtoa tehdään kahdesta syystä: 1. Rautafosfatointialtaasta ja huuhtelu 1:stä haihtuu runsaasti vettä koska nesteet ovat kuumia ja niitä
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
KEMA221 2009 KEMIALLINEN TASAPAINO ATKINS LUKU 7
 KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
Kaasu Neste Kiinteä aine Plasma
 Olomuodot Kaasu: atomeilla/molekyyleillä suuri nopeus, vuorovaikuttavat vain törmätessään toisiinsa Neste: atomit/molekyylit/ionit liukuvat toistensa lomitse, mutta pysyvät yhtenä nestetilavuutena (molekyylien
Olomuodot Kaasu: atomeilla/molekyyleillä suuri nopeus, vuorovaikuttavat vain törmätessään toisiinsa Neste: atomit/molekyylit/ionit liukuvat toistensa lomitse, mutta pysyvät yhtenä nestetilavuutena (molekyylien
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
KUPARIASPIRINAATIN VALMISTUS
 TAUSTAA KUPARIASPIRINAATIN VALMISTUS Kupariaspirinaatti eli dikuparitetra-asetyylisalisylaatti on epäorgaaninen yhdiste, jonka käyttöä nivelreuman hoidossa ja toisen sukupolven lääkevalmistuksessa on tutkittu
TAUSTAA KUPARIASPIRINAATIN VALMISTUS Kupariaspirinaatti eli dikuparitetra-asetyylisalisylaatti on epäorgaaninen yhdiste, jonka käyttöä nivelreuman hoidossa ja toisen sukupolven lääkevalmistuksessa on tutkittu
Ongelma sellutehtaalla
 Olette luokkanne kanssa yritysvierailulla sellutehtaalla ja tutustumiskierroksella törmäätte tehtaalla ilmenevään ongelmaan. Sellunvalmistusprosessi on jouduttu keskeyttämään putkistoa tukkivien ligniinisaostumien
Olette luokkanne kanssa yritysvierailulla sellutehtaalla ja tutustumiskierroksella törmäätte tehtaalla ilmenevään ongelmaan. Sellunvalmistusprosessi on jouduttu keskeyttämään putkistoa tukkivien ligniinisaostumien
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
ASENNUSOHJE UPONOR UMPISÄILIÖ 3 M 3. Uponor umpisäiliö 3 m 3. Helppo käsitellä helppo asentaa.
 ASENNUSOHJE UPONOR UMPISÄILIÖ 3 M 3 Uponor umpisäiliö 3 m 3. Helppo käsitellä helppo asentaa. Uponor umpisäiliö 3 m 3 Kaivanto Umpisäiliön kaivanto mitoitetaan niin, että ankkurointilevyt mahtuvat sen
ASENNUSOHJE UPONOR UMPISÄILIÖ 3 M 3 Uponor umpisäiliö 3 m 3. Helppo käsitellä helppo asentaa. Uponor umpisäiliö 3 m 3 Kaivanto Umpisäiliön kaivanto mitoitetaan niin, että ankkurointilevyt mahtuvat sen
Tutkimusmateriaalit -ja välineet: kaarnan palaset, hiekan murut, pihlajanmarjat, juuripalat, pakasterasioita, vettä, suolaa ja porkkananpaloja.
 JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
Kondensaatio ja hydrolyysi
 Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
AIR-MIX-RUISKUN PERUSKÄYTTÖ
 AIR-MIX-RUISKUN PERUSKÄYTTÖ 1. Ruiskun pesu ennen käyttöönottoa 2. Maalin lisäys ja maalaus 3. Ruiskunpesu maalauksen jälkeen RUISKUN KÄYTTÖ MAALAUKSISSA Air-Mix-ruiskua käytetään lähinnä kalusteovien
AIR-MIX-RUISKUN PERUSKÄYTTÖ 1. Ruiskun pesu ennen käyttöönottoa 2. Maalin lisäys ja maalaus 3. Ruiskunpesu maalauksen jälkeen RUISKUN KÄYTTÖ MAALAUKSISSA Air-Mix-ruiskua käytetään lähinnä kalusteovien
vi) Oheinen käyrä kuvaa reaktiosysteemin energian muutosta reaktion (1) etenemisen funktiona.
 3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA
 ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
ALKOHOLIEN TUNNISTUS KAASUKROMATOGRAFIAN AVULLA Kohderyhmä: Työ on suunniteltu lukiolaisille sekä ammattikoululaisille ja sopii hyvin erotus- ja tunnistusmenetelmien opetuksen yhteyteen. Työn teoriassa
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
HORNADY LOCK-N-LOAD SONIC CLEANER LOCK-N-LOAD MAGNUM SONIC CLEANER KÄYTTÖOHJE
 HORNADY LOCK-N-LOAD SONIC CLEANER LOCK-N-LOAD MAGNUM SONIC CLEANER KÄYTTÖOHJE Hornady Lock-N-Load Sonic/Magnum Sonic Cleaner poistaa ruutijäämät hylsyn sisä-ja ulkopuolelta ultraäänienergian ja erityisen
HORNADY LOCK-N-LOAD SONIC CLEANER LOCK-N-LOAD MAGNUM SONIC CLEANER KÄYTTÖOHJE Hornady Lock-N-Load Sonic/Magnum Sonic Cleaner poistaa ruutijäämät hylsyn sisä-ja ulkopuolelta ultraäänienergian ja erityisen
Kemia s10 Ratkaisut. b) Kloorin hapetusluvun muutos: +VII I, Hapen hapetusluvun muutos: II 0. c) n(liclo 4 ) = =
 1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
1. 2. a) Yhdisteen molekyylikaava on C 6 H 10 : A ja E b) Yhdisteessä on viisi CH 2 yksikköä : D ja F c) Yhdisteet ovat tyydyttyneitä ja syklisiä : D ja F d) Yhdisteet ovat keskenään isomeereja: A ja E
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 28.1.2016 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
KÄYTTÄJÄN OPAS. Yksityiskohtainen käyttöoppaasi. BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten
 KÄYTTÄJÄN OPAS Yksityiskohtainen käyttöoppaasi BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten Jos sinulla on kysymyksiä BYDUREON-valmisteen käytöstä Katso Tavallisia kysymyksiä ja
KÄYTTÄJÄN OPAS Yksityiskohtainen käyttöoppaasi BYDUREON 2 mg injektiokuiva-aine ja liuotin depotsuspensiota varten Jos sinulla on kysymyksiä BYDUREON-valmisteen käytöstä Katso Tavallisia kysymyksiä ja
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä. FT Satu Ikonen, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola
 Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Orgaanisten epäpuhtauksien määrittäminen jauhemaisista näytteistä FT, Teknologiakeskus KETEK Oy Analytiikkapäivät 2012, Kokkola TEKNOLOGIAKESKUS KETEK OY Kokkolassa sijaitseva yritysten osaamisen kehittämiseen
Ylioppilastutkintolautakunta S tudentexamensnämnden
 Ylioppilastutkintolautakunta S tudentexamensnämnden KEMIAN KOE 22.3.2013 HYVÄN VASTAUKSEN PIIRTEITÄ Alla oleva vastausten piirteiden ja sisältöjen luonnehdinta ei sido ylioppilastutkintolautakunnan arvostelua.
Ylioppilastutkintolautakunta S tudentexamensnämnden KEMIAN KOE 22.3.2013 HYVÄN VASTAUKSEN PIIRTEITÄ Alla oleva vastausten piirteiden ja sisältöjen luonnehdinta ei sido ylioppilastutkintolautakunnan arvostelua.
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille
 Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 22.1.2015 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Fysiikan, kemian ja matematiikan kilpailu lukiolaisille 22.1.2015 Kemian tehtävät Kirjoita nimesi, luokkasi ja lukiosi tähän tehtäväpaperiin. Kirjoita vastauksesi selkeällä käsialalla tehtäväpaperiin vastauksille
Neutraloituminen = suolan muodostus
 REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
REAKTIOT JA TASAPAINO, KE5 Neutraloituminen = suolan muodostus Taustaa: Tähän asti ollaan tarkasteltu happojen ja emästen vesiliuoksia erikseen, mutta nyt tarkastellaan mitä tapahtuu, kun happo ja emäs
MENETELMÄ POISTETTU KÄYTÖSTÄ Sideaineet, yleistä
 Sideaineet, yleistä PANK-1003 PANK SIDEAINEEN TALTEENOTTO ASFALTISTA PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: Korvaa menetelmän: 15.11.1996-1. MENETELMÄN TARKOITUS 2. MENETELMÄN SOVELTAMISALUE Menetelmässä
Sideaineet, yleistä PANK-1003 PANK SIDEAINEEN TALTEENOTTO ASFALTISTA PÄÄLLYSTEALAN NEUVOTTELUKUNTA Hyväksytty: Korvaa menetelmän: 15.11.1996-1. MENETELMÄN TARKOITUS 2. MENETELMÄN SOVELTAMISALUE Menetelmässä
Alumiinista alunaa TAUSTAA
 KOHDERYHMÄ: Työ soveltuu yläkouluun tai lukion kursseille KE3 ja KE4. Teorian laajuus riippuu siitä mille kohderyhmälle työ vedetään. KESTO: Noin 1-1,5h. Kesto riippuu siitä, tehdäänkö tuotteelle imusuodatus
KOHDERYHMÄ: Työ soveltuu yläkouluun tai lukion kursseille KE3 ja KE4. Teorian laajuus riippuu siitä mille kohderyhmälle työ vedetään. KESTO: Noin 1-1,5h. Kesto riippuu siitä, tehdäänkö tuotteelle imusuodatus
PULLEAT VAAHTOKARKIT
 PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
PULLEAT VAAHTOKARKIT KOHDERYHMÄ: Työ soveltuu alakouluun kurssille aineet ympärillämme ja yläkouluun kurssille ilma ja vesi. KESTO: Työ kestää n.30-60min MOTIVAATIO: Työssä on tarkoitus saada positiivista
Matematiikan tukikurssi
 Matematiikan tukikurssi Kurssikerta 8 1 Derivaatta Tarkastellaan funktion f keskimääräistä muutosta tietyllä välillä ( 0, ). Funktio f muuttuu tällä välillä määrän. Kun tämä määrä jaetaan välin pituudella,
Matematiikan tukikurssi Kurssikerta 8 1 Derivaatta Tarkastellaan funktion f keskimääräistä muutosta tietyllä välillä ( 0, ). Funktio f muuttuu tällä välillä määrän. Kun tämä määrä jaetaan välin pituudella,
MORDAX -horminkorjausmenetelmä
 MORDAX -horminkorjausmenetelmä MORDAX PLUS - käyttöohje Eskon Oy Ajomiehentie 13 00390 HELSINKI puh. 09-863 4161 fax. 09-867 38271 sähköposti: internet: eskon@eskon.fi www.eskon.fi Vuotavat hormit ovat
MORDAX -horminkorjausmenetelmä MORDAX PLUS - käyttöohje Eskon Oy Ajomiehentie 13 00390 HELSINKI puh. 09-863 4161 fax. 09-867 38271 sähköposti: internet: eskon@eskon.fi www.eskon.fi Vuotavat hormit ovat
Juoksumaton huolto-ohje
 Juoksumaton huolto-ohje Maton huoltaminen on tärkeää Matto on juoksumaton tärkein osa. Sen kunnossa pitäminen takaa sen, että laite toimii moitteettomasti vuosikausia eteenpäin. Säännöllisin väliajoin
Juoksumaton huolto-ohje Maton huoltaminen on tärkeää Matto on juoksumaton tärkein osa. Sen kunnossa pitäminen takaa sen, että laite toimii moitteettomasti vuosikausia eteenpäin. Säännöllisin väliajoin
Epäyhtälön molemmille puolille voidaan lisätä sama luku: kaikilla reaaliluvuilla a, b ja c on voimassa a < b a + c < b + c ja a b a + c b + c.
 Epäyhtälö Kahden lausekkeen A ja B välisiä järjestysrelaatioita A < B, A B, A > B ja A B nimitetään epäyhtälöiksi. Esimerkiksi 2 < 6, 9 10, 5 > a + + 2 ja ( + 1) 2 2 + 2 ovat epäyhtälöitä. Epäyhtälössä
Epäyhtälö Kahden lausekkeen A ja B välisiä järjestysrelaatioita A < B, A B, A > B ja A B nimitetään epäyhtälöiksi. Esimerkiksi 2 < 6, 9 10, 5 > a + + 2 ja ( + 1) 2 2 + 2 ovat epäyhtälöitä. Epäyhtälössä
Tutustu merkintöihin! Tärkeää tietoa siitä, miten varmistat pesu- ja puhdistusaineiden käytön turvallisuuden kotona
 Tutustu merkintöihin! Tärkeää tietoa siitä, miten varmistat pesu- ja puhdistusaineiden käytön turvallisuuden kotona Kodin puhdistusaineisiin on lähiaikoina tulossa uudet varoitusmerkinnät. Osa symboleista
Tutustu merkintöihin! Tärkeää tietoa siitä, miten varmistat pesu- ja puhdistusaineiden käytön turvallisuuden kotona Kodin puhdistusaineisiin on lähiaikoina tulossa uudet varoitusmerkinnät. Osa symboleista
Käyttöohjeet LA-VA V300 / Premium Line VAKUUMIPAKKAUSLAITE
 Käyttöohjeet LA-VA V300 / Premium Line VAKUUMIPAKKAUSLAITE Hankkimallasi Lava vakuumipakkauslaitteella on 2 vuoden takuu. Takuu ei kata vahinkoa, mikäli ilmapumppuun on päästetty nestettä. On tärkeä tietää,
Käyttöohjeet LA-VA V300 / Premium Line VAKUUMIPAKKAUSLAITE Hankkimallasi Lava vakuumipakkauslaitteella on 2 vuoden takuu. Takuu ei kata vahinkoa, mikäli ilmapumppuun on päästetty nestettä. On tärkeä tietää,
Vetokoukun johdinkimppu, 7 napainen
 Ohje nro Versio Osa nro 9172640 1.2 9499587, 9499589, 9499590, 9441161 Vetokoukun johdinkimppu, 7 napainen M3702107 Sivu 1 / 11 Varuste A0000162 M3702108 Sivu 2 / 11 JOHDANTO Lue läpi koko ohje ennen asennuksen
Ohje nro Versio Osa nro 9172640 1.2 9499587, 9499589, 9499590, 9441161 Vetokoukun johdinkimppu, 7 napainen M3702107 Sivu 1 / 11 Varuste A0000162 M3702108 Sivu 2 / 11 JOHDANTO Lue läpi koko ohje ennen asennuksen
Heikot sidokset voimakkuusjärjestyksessä: -Sidos poolinen, kun el.neg.ero on 0,5-1,7. -Poolisuus merkitään osittaisvarauksilla
 Heikot sidokset voimakkuusjärjestyksessä: 1. Ioni-dipoli sidokset 2. Vetysidokset 3. 4. Dipoli-dipoli sidokset Dispersiovoimat -Sidos poolinen, kun el.neg.ero on 0,5-1,7 -Poolisuus merkitään osittaisvarauksilla
Heikot sidokset voimakkuusjärjestyksessä: 1. Ioni-dipoli sidokset 2. Vetysidokset 3. 4. Dipoli-dipoli sidokset Dispersiovoimat -Sidos poolinen, kun el.neg.ero on 0,5-1,7 -Poolisuus merkitään osittaisvarauksilla
Käyttöjärjestelmät: Virtuaalimuisti
 Käyttöjärjestelmät: Virtuaalimuisti Teemu Saarelainen Tietotekniikka teemu.saarelainen@kyamk.fi Lähteet Stallings, W. Operating Systems Haikala, Järvinen, Käyttöjärjestelmät Eri Web-lähteet Muistinhallinta
Käyttöjärjestelmät: Virtuaalimuisti Teemu Saarelainen Tietotekniikka teemu.saarelainen@kyamk.fi Lähteet Stallings, W. Operating Systems Haikala, Järvinen, Käyttöjärjestelmät Eri Web-lähteet Muistinhallinta
TILASTOLLINEN LAADUNVALVONTA
 1 Aki Taanila TILASTOLLINEN LAADUNVALVONTA 31.10.2008 2 TILASTOLLINEN LAADUNVALVONTA Tasalaatuisuus on hyvä tavoite, jota ei yleensä voida täydellisesti saavuttaa: asiakaspalvelun laatu vaihtelee, vaikka
1 Aki Taanila TILASTOLLINEN LAADUNVALVONTA 31.10.2008 2 TILASTOLLINEN LAADUNVALVONTA Tasalaatuisuus on hyvä tavoite, jota ei yleensä voida täydellisesti saavuttaa: asiakaspalvelun laatu vaihtelee, vaikka
KÄYTTÖOHJE VPI7A- LASIKANNUKEITIN
 KÄYTTÖOHJE VPI7A- LASIKANNUKEITIN SISÄLLYS 1. Laitetoimituksen sisältö s.2 2. Turvaohjeet s.2 3. Varotoimenpiteet s.2 3.1 Toimenpiteet ennen laitteen liittämistä sähköverkkoon s.3 4. Merkkivalot s.4 5.
KÄYTTÖOHJE VPI7A- LASIKANNUKEITIN SISÄLLYS 1. Laitetoimituksen sisältö s.2 2. Turvaohjeet s.2 3. Varotoimenpiteet s.2 3.1 Toimenpiteet ennen laitteen liittämistä sähköverkkoon s.3 4. Merkkivalot s.4 5.
Seokset ja liuokset. 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen
 Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
YMPÄRISTÖKEMIAN LABORATORIOHARJOITUSTEN ANALYYSIOHJEET
 YMPÄRISTÖKEMIAN LABORATORIOHARJOITUSTEN ANALYYSIOHJEET 26.2.2016 Aino Peltola VEDEN ph-arvon MÄÄRITYS Suomen vedet ovat luontaisesti happamia. Tämä johtuu liuenneesta hiilidioksidista, humuspitoisuudesta
YMPÄRISTÖKEMIAN LABORATORIOHARJOITUSTEN ANALYYSIOHJEET 26.2.2016 Aino Peltola VEDEN ph-arvon MÄÄRITYS Suomen vedet ovat luontaisesti happamia. Tämä johtuu liuenneesta hiilidioksidista, humuspitoisuudesta
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
8. Alkoholit, fenolit ja eetterit
 8. Alkoholit, fenolit ja eetterit SM -08 Alkoholit ovat orgaanisia yhdisteitä, joissa on yksi tai useampia -ryhmiä. Fenoleissa -ryhmä on kiinnittynyt aromaattiseen renkaaseen. Alkoholit voivat olla primäärisiä,
8. Alkoholit, fenolit ja eetterit SM -08 Alkoholit ovat orgaanisia yhdisteitä, joissa on yksi tai useampia -ryhmiä. Fenoleissa -ryhmä on kiinnittynyt aromaattiseen renkaaseen. Alkoholit voivat olla primäärisiä,
Viihdejärjestelmä, RSE, kaksi näyttöä, kahdella soittimella, (alnro 175379-)
 Installation instructions, accessories Ohje nro Versio 1319908 1.3 Osa nro 1319734, 1319735, 1319736, 1319737, 1319738, 1319746, 1319747, 1319748, 1319749, 31414410, 31373296, 31373300, 31399103, 31399104,
Installation instructions, accessories Ohje nro Versio 1319908 1.3 Osa nro 1319734, 1319735, 1319736, 1319737, 1319738, 1319746, 1319747, 1319748, 1319749, 31414410, 31373296, 31373300, 31399103, 31399104,
Installation instructions, accessories. Kattolaatikko. Volvo Car Corporation Gothenburg, Sweden. Ohje nro Versio Osa nro 9491340 1.0.
 Ohje nro Versio Osa nro 9491340 1.0 Kattolaatikko A8901430 Sivu 1 / 8 B8901445 Sivu 2 / 8 JOHDANTO Lue läpi koko ohje ennen asennuksen aloittamista. Huomautukset ja varoitustekstit ovat turvallisuuden
Ohje nro Versio Osa nro 9491340 1.0 Kattolaatikko A8901430 Sivu 1 / 8 B8901445 Sivu 2 / 8 JOHDANTO Lue läpi koko ohje ennen asennuksen aloittamista. Huomautukset ja varoitustekstit ovat turvallisuuden
Lue ohjeet huolellisesti ennen laitteen käyttöä.
 1 Väliaikaisen tallennuskansion käyttö Lue ohjeet huolellisesti ennen laitteen käyttöä. Kun skannaat kuvia, dioja, asiakirjoja jne. sekä digitoit LP-levyjä tai C-kasetteja, sinulla on mahdollisuus tallentaa
1 Väliaikaisen tallennuskansion käyttö Lue ohjeet huolellisesti ennen laitteen käyttöä. Kun skannaat kuvia, dioja, asiakirjoja jne. sekä digitoit LP-levyjä tai C-kasetteja, sinulla on mahdollisuus tallentaa
Luku 3. Protolyysireaktiot ja vesiliuoksen ph
 Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
luku 1.notebook Luku 1 Mooli, ainemäärä ja konsentraatio
 Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
Luku 1 Mooli, ainemäärä ja konsentraatio 1 Kemian kvantitatiivisuus = määrällinen t ieto Kemian kaavat ja reaktioyhtälöt sisältävät tietoa aineiden rakenteesta ja aineiden määristä esim. 2 H 2 + O 2 2
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
Sähkötoiminen moottorinlämmitin, 230 V, (R-design)
 Installation instructions, accessories Ohje nro 31414484 Versio 1.1 Osa nro 31373665 Sähkötoiminen moottorinlämmitin, 230 V, (R-design) IMG-386602 Volvo Car Corporation Sähkötoiminen moottorinlämmitin,
Installation instructions, accessories Ohje nro 31414484 Versio 1.1 Osa nro 31373665 Sähkötoiminen moottorinlämmitin, 230 V, (R-design) IMG-386602 Volvo Car Corporation Sähkötoiminen moottorinlämmitin,
Vaarallinen jäte. Pakkaaminen, merkintä ja kuljettaminen
 Vaarallinen jäte Pakkaaminen, merkintä ja kuljettaminen Mitä vaarallinen jäte on? Vaarallisella jätteellä tarkoitetaan jätettä, jolla on palo- tai räjähdysvaarallinen, tartuntavaarallinen, muu terveydelle
Vaarallinen jäte Pakkaaminen, merkintä ja kuljettaminen Mitä vaarallinen jäte on? Vaarallisella jätteellä tarkoitetaan jätettä, jolla on palo- tai räjähdysvaarallinen, tartuntavaarallinen, muu terveydelle
Lisää segmenttipuusta
 Luku 24 Lisää segmenttipuusta Segmenttipuu on monipuolinen tietorakenne, joka mahdollistaa monenlaisten kyselyiden toteuttamisen tehokkaasti. Tähän mennessä olemme käyttäneet kuitenkin segmenttipuuta melko
Luku 24 Lisää segmenttipuusta Segmenttipuu on monipuolinen tietorakenne, joka mahdollistaa monenlaisten kyselyiden toteuttamisen tehokkaasti. Tähän mennessä olemme käyttäneet kuitenkin segmenttipuuta melko
SÄILYTÄ KÄYTTÖOPAS HUOLELLISESTI MYÖHEMPÄÄ KÄYTTÖÄ VARTEN.
 LUE TÄMÄ KÄYTTÖOPAS HUOLELLISESTI ENNEN LAITTEEN KÄYTTÖÖNOTTOA. OHJEITA NOUDATTAMALLA SAAT PARHAAN TU- LOKSEN JA VOIT KÄYTTÄÄ LAITETTA TURVALLISESTI. SF TURVAVAROITUKSIA - Varmista pakkauksen poistamisen
LUE TÄMÄ KÄYTTÖOPAS HUOLELLISESTI ENNEN LAITTEEN KÄYTTÖÖNOTTOA. OHJEITA NOUDATTAMALLA SAAT PARHAAN TU- LOKSEN JA VOIT KÄYTTÄÄ LAITETTA TURVALLISESTI. SF TURVAVAROITUKSIA - Varmista pakkauksen poistamisen
Lue jäljempänä oleva ohje synteesikaavakkeen täyttäminen. Synteesikaavakkeita voi tulostaa Nettilabrasta.
 Kemian perustyöt (orgaanisen kemian osuus), orgaanisen kemian I & II työt sekä Synthetic chemistry labworks OHJE TYÖSELOSTUKSEN LAATIMISEEN KURSSILLA KEMIAN PERUSTYÖT (orgaanisen kemian osuus) Synteeseistä
Kemian perustyöt (orgaanisen kemian osuus), orgaanisen kemian I & II työt sekä Synthetic chemistry labworks OHJE TYÖSELOSTUKSEN LAATIMISEEN KURSSILLA KEMIAN PERUSTYÖT (orgaanisen kemian osuus) Synteeseistä
