Opas terveydenhuollon ammattilaisille
|
|
|
- Riitta-Liisa Laaksonen
- 6 vuotta sitten
- Katselukertoja:
Transkriptio
1 Opas terveydenhuollon ammattilaisille LEMTRADA -valmisteen (alemtutsumabin) käyttö aaltomaista multippeliskleroosia (RRMS) sairastavien potilaiden hoidossa Tärkeitä turvallisuutta koskevia tietoja
2
3 Sisällysluettelo 1. LEMTRADA -valmisteen esittely 5 2. Mitä riskejä LEMTRADA -valmisteen käyttöön liittyy? 7 3. LEMTRADA -hoitoa saavien potilaiden seuranta Usein kysytyt kysymykset 13 3
4 Yleiskatsaus LEMTRADA -valmisteeseen LEMTRADA (alemtutsumabi) on tarkoitettu aaltomaista (relapsoivaa-remittoivaa, RRMS) multippeliskleroosia sairastaville aikuisille potilaille, joilla on aktiivinen tauti kliinisen taudinkuvan tai kuvantamislöydösten perusteella määriteltynä. Tämä opas terveydenhuollon ammattilaisille on laadittu osana LEMTRADA - koulutusohjelmaa ja se on tarkoitettu LEMTRADA -hoitoa määrääville ja valvoville terveydenhuollon ammattilaisille. Tämän oppaan tarkoituksena on parantaa LEMTRADA - hoitoa suotuisasti vaikuttavilla asianmukaisilla toimilla. Oppaan sisältö: 1. Kuvaus LEMTRADA -valmisteen käyttöön liittyvistä välittömistä ja viivästyneistä riskeistä, joita saattaa ilmetä usean vuoden kuluttua hoidosta ja jotka saattavat olla vakavia tai hengenvaarallisia ja joita ovat: > vakavat infektiot > autoimmuunisairaudet: > kilpirauhasen toimintahäiriöt > immuuni trombosytopenia (ITP) > munuaissairaudet, kuten tyvikalvovasta-aineglomerulonefriitti (anti-gbm-tauti) 2. Suositukset siitä, miten näitä riskejä voidaan pienentää neuvomalla, seuraamalla ja hoitamalla potilaita asianmukaisella tavalla 3. Usein kysyttyjen kysymysten osio. Terveydenhuollon ammattilaisten muistilistaa käytetään myös potilaan ensimmäisellä käynnillä, jolloin LEMTRADA -hoito määrätään, ja seurantakäynneillä. Lisäksi on laadittu potilaan opas ja potilasvaroituskortti, jotka annetaan potilaalle, kun LEMTRADA -hoito aloitetaan. > Potilaan opas: käytävä huolellisesti läpi yhdessä potilaan kanssa hoitoa määrättäessä ja säännöllisesti seurantakäynneillä. Sen tarkoituksena on kertoa potilaille autoimmuunisairauksien ja vakavien infektioiden oireista ja kokeisiin osallistumisen tarpeellisuudesta sekä kehottaa potilaita olemaan valppaina oireiden varalta ja hakeutumaan välittömästi hoitoon, jos oireita ilmenee. > Potilasvaroituskortti: yhteydenpitoväline, joka kertoo potilasta hoitavalle terveydenhuollon ammattilaiselle, että potilas saa LEMTRADA -valmistetta. Potilaan (tai tarvittaessa huoltajan) on pidettävä tämä kortti aina mukanaan ja näytettävä se terveydenhuollon ammattilaiselle. Tämän materiaalin voi pyytää Sanofin lääketurva- ja neuvontayksiköstä: pharmacovigilance.finland@sanofi.com tai puh Huomaa, että tässä oppaassa ei ole kuvattu kaikkia LEMTRADA -valmisteen käyttöön liittyviä riskejä eikä se korvaa valmisteyhteenvetoa (SmPC).
5 1> LEMTRADA -valmisteen esittely LEMTRADA (alemtutsumabi) on tarkoitettu aaltomaista (relapsoivaa-remittoivaa, RRMS) multippeliskleroosia sairastaville aikuisille potilaille, joilla on aktiivinen tauti kliinisen taudinkuvan tai kuvantamislöydösten perusteella määriteltynä. LEMTRADA on laskimonsisäisesti annettava monoklonaalinen vasta-aine. Se kiinnittyy CD52:ksi kutsuttuun antigeeniin, jota esiintyy runsaasti T- ja B-lymfosyyttien pinnalla ja vähemmän luonnollisissa tappajasoluissa, monosyyteissä ja makrofageissa. LEMTRADA -valmisteen vaikutusmekanismia MS-taudin hoidossa ei täysin tunneta. Tutkimukset kuitenkin viittaavat immuunivastetta muuntaviin (immunomodulatorisiin) vaikutuksiin lymfosyyttikadon ja populaation uudelleen muodostumisen kautta. Lääke aiheuttaa muun muassa seuraavia muutoksia: > Muutokset joidenkin lymfosyyttien alatyyppien määrässä, suhteellisessa määrässä ja ominaisuuksissa hoidon jälkeen > Regulatoristen T-solualatyyppien lisääntyminen > Muisti-T- ja B-lymfosyyttien lisääntyminen > Ohimenevät vaikutukset luontaisen immuniteetin osa-alueisiin (ts. neutrofiileihin, makrofageihin, luonnollisiin tappajasoluihin). Terapeuttinen vaikutus saattaa selittyä kiertävien B- ja T-solujen määrän vähenemisellä ja solupopulaation uudelleenmuodostumisella. LEMTRADA -hoito on aloitettava MS-potilaiden hoitoon perehtyneen neurologin valvonnassa. Mahdollisten LEMTRADA -valmisteen aiheuttamien riskien ja haittavaikutusten minimoimiseksi sekä lääkettä määräävien lääkäreiden että potilaiden on sitouduttava seurantaan, joka kestää 48 kuukautta (4 vuotta) viimeisen LEMTRADA -infuusion jälkeen. Potilaiden on tärkeää ymmärtää, että heidän täytyy jatkaa seurantaa, vaikka heidän vointinsa olisikin hyvä ja vaikka MS-tauti olisi saatu hyvin hallintaan. Luomalla toimivan hoitosuhteen sinun, potilaan ja MS-taudin hoidosta vastaavan henkilökunnan välille sekä tutustumalla huolella potilaan opastamiseen tarkoitettuihin työkaluihin, voit auttaa potilastasi: > Noudattamaan säännöllistä seuranta-aikataulua > Tunnistamaan oireita ja raportoimaan niistä ajoissa > Saamaan tarvittaessa nopeasti asianmukaista hoitoa. 5
6 Katso lisätietoja tämän oppaan kohdasta LEMTRADA -hoitoa saavien potilaiden seuranta. Saat vielä selkeämmän käsityksen hoidon vaikutusten ja vaadittavan seurannan kestosta tutustumalla kuvaan 1 ja taulukkoon 1. Kuva 1 - Yleiskatsaus LEMTRADA -hoitoon ja seurantaan ALOITUSHOITO, JOKA SISÄLTÄÄ KAKSI HOITOJAKSOA LISÄHOITOJAKSOT TARPEEN MUKAAN* Jakso Vähintään Vähintään 12 kk Jakso Jakso Jakso ensimmäisen hoitojakson hoitojakson jälkeen kolmannen hoitojakson 5 päivän hoito jälkeen 3 päivän hoito 3 päivän hoito jälkeen 3 päivän hoito Aloita veri- ja virtsakokeet ennen hoitoa Jatkuva seuranta 4 vuoden ajan viimeisen hoitojakson päätyttyä *HUOMAA Tutkimuksessa, jossa seurattiin potilaita 6 vuoden ajan ensimmäisen infuusion (jakso 1) jälkeen, osoitettiin, että suurin osa potilaista ei tarvitse jatkohoitoa kahden ensimmäisen hoitojakson jälkeen. Taulukko 1 - Yleiskatsaus LEMTRADA -hoidon seurantaan Autoimmuunisairaus Laboratoriokoe Ennen hoitoa Kerran kuukaudessa 3 kuukauden välein Jatka 48 kuukauden ajan Kilpirauhasen toimintahäiriöt Kilpirauhasen toimintakokeet (kuten TSHmittaukset) X - X X Immuuni trombosytopenia (ITP) ja muut sytopeniat Täydellinen verenkuva ja erittelylaskenta X X - X Munuaissairaudet, kuten tyvikalvovastaaineglomerulonefriitti Seerumin kreatiniinin mittaus Virtsakoe, mukaan lukien virtsan mikroskopointi X X - X X X - X 6
7 2> Mitä riskejä LEMTRADA -valmisteen käyttöön liittyy? On huomattava, että tämä opas ei kata kaikkia LEMTRADA -valmisteen käyttöön liittyviä riskejä eikä korvaa valmisteyhteenvetoa. Vakavat infektiot LEMTRADA -valmisteen käyttöön liittyy vakavien infektioiden riski. Riskin minimoimiseksi on tärkeää: > siirtää hoidon aloitusta potilailla, joilla on aktiivinen infektio, sen paranemiseen asti > tehdä HIV-seulonta, arvioida sekä aktiivisen että inaktiivisen (latentin) tuberkuloosin riski paikallisten ohjeiden mukaisesti ja tehdä hepatiitti B (HBV ) ja hepatiitti C -virus (HCV ) -seulonta > tehdä ihmisen papilloomavirusseulonta (HPV-seulonta) ja toistaa seulonta vuosittain. Rokotteen antamista ennen hoitoa on harkittava. > saattaa rokotusohjelma loppuun vähintään 6 viikkoa ennen hoidon aloittamista > suositella listerioosiriskiä pienentävää ruokavaliota kahdeksi viikoksi ennen infuusiota, infuusion aikana ja vähintään yhden kuukauden ajaksi infuusion jälkeen > aloittaa herpestä ennaltaehkäisevä lääkitys hoidon ensimmäisenä päivänä ja jatkaa sitä vähintään yhden kuukauden ajan jokaisen hoitojakson jälkeen > välttää samanaikaisia hoitoja muilla immunomoduloivilla lääkeaineilla. Autoimmuunisairaudet LEMTRADA -valmisteen käyttöön on todettu liittyvän riski sairastua muun muassa seuraaviin autoimmuunisairauksiin (lueteltu esiintymistiheyden mukaan yleisimmästä harvinaisimpaan): a. Kilpirauhasen toimintahäiriöt b. ITP c. Munuaissairaus (kuten tyvikalvovasta-aineglomerulonefriitti). Nämä sairaudet voivat olla vakavia ja aiheuttaa lisääntynyttä sairastavuutta ja/tai johtaa kuolemaan. Autoimmuunisairaudet saattavat puhjeta vasta useita vuosia hoidon jälkeen. Varhainen seuranta ja toteaminen voivat parantaa potilaiden hoitotuloksia. 7
8 On tärkeää seurata laboratoriokokeiden tuloksia huolellisesti ja tarkkailla näihin sairauksiin viittaavia oireita ja löydöksiä. Käy seuraavat osiot huolella läpi, jotta oppisit ymmärtämään näitä riskejä entistä paremmin. a. Kilpirauhasen toimintahäiriöt Kliinisissä tutkimuksissa raportoitiin autoimmuunisairaudesta johtuvia kilpirauhasen toimintahäiriöitä, kuten hypertyroidismia ja hypotyroidismia. Kilpirauhasen toimintahäiriöt olivat hyvin yleisiä näissä tutkimuksissa. Niistä suurin osa oli vakavuudeltaan lieviä tai keskivaikeita ja ilmeni 48 kuukauden sisällä ensimmäisestä LEMTRADA -hoidosta. Osa tapauksista oli ohimeneviä eikä vaatinut hoitoa. Useimmat kilpirauhaseen liittyvät tapahtumat saatiin hallintaan tavanomaisella lääkityksellä, mutta joillekin potilaille oli tehtävä leikkaustoimenpide. On tärkeää kertoa potilaalle, että havaitusta kilpirauhasen toimintahäiriön tyypistä riippuen tämä saattaa tarvita hoitoa koko loppuelämänsä. > Kilpirauhasen toimintakokeet, kuten TSH-mittaukset, on tehtävä ennen hoidon aloittamista ja sen jälkeen kolmen kuukauden välein, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. Jos TSH-arvo on poikkeava, on tutkittava vapaa T3 ja T4. > Lisäksi on tarkkailtava kilpirauhasen toimintahäiriöistä kertovia oireita ja löydöksiä. > Kilpirauhasen toimintahäiriöt ovat riski erityisesti raskaaksi tuleville naisille. Hoitamaton kilpirauhassairaus voi aiheuttaa vahinkoa syntymättömälle ja vastasyntyneelle lapselle. Erityistä varovaisuutta on noudatettava, jos raskaana oleva nainen sairastaa Basedowin tautia (jota kutsutaan myös Gravesin taudiksi), sillä äidin elimistössä olevat TSH-reseptorin vasta-aineet voivat siirtyä kehittyvään sikiöön ja aiheuttaa tälle tilapäisen vastasyntyneen Basedowin taudin. Potilaan raskauden seurannasta vastaavien terveydenhuollon ammattilaisten on oltava tietoisia potilaan LEMTRADA -hoitoon liittyvästä kilpirauhasen toimintahäiriöriskistä ja häiriöiden asianmukaisesta hoidosta. 8
9 b. Immuuni trombosytopenia (ITP) Immuuni trombosytopenia on autoimmuunisairaus, joka liittyy yleensä verihiutaleiden toimintaa estäviin vasta-aineisiin. Se on kliininen oireyhtymä, jossa verenkierrossa olevien verihiutaleiden pienentynyt määrä (trombosytopenia) ilmenee verenvuototaipumuksena mustelma-alttiutena (purppura) tai veren ekstravasaationa hiussuonista ihoon ja limakalvoille (petekiat). Kuvassa 2 on esimerkkejä immuunin trombosytopenian ilmenemisestä. ITP:n oireita voivat olla muun muassa (mutta eivät yksinomaan) mustelma-alttius, verenvuotoherkkyys ja tavallista runsaammat tai epäsäännölliset kuukautiset. Näitä kliinisiä ITP:n oireita saattaa esiintyä, mutta ei välttämättä esiinny, jo ennen kuin verenvuoto muuttuu vakavaksi. ITP voi olla vakava sairaus, ja se saattaa lisätä sairastavuutta tai johtaa kuolemaan. Sairaus voi puhjeta vasta useiden vuosien kuluttua lääkkeen antamisesta potilaalle. Kliinisissä tutkimuksissa ITP voitiin diagnosoida ja hoitaa ajoissa. Useimmille potilaille tehosi ensilinjan hoitona annettu lääkitys. Kaikkia potilaita on seurattava ITP:n varalta noudattamalla seuraavia ohjeita: > Täydellinen verenkuva tulee ottaa ja erittelylaskenta suorittaa ennen hoidon aloittamista sekä sen jälkeen kuukauden välein, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. > Varmista, ettei potilaalla ole havaittavissa kliinisiä ITP:n oireita. > Kerro potilaalle, miten tärkeää on käydä kuukausittain verikokeissa ja jatka seurantaa 48 kuukauden ajan viimeisen infuusion jälkeen. > Opasta potilasta tunnistamaan ITP:hen liittyviä oireita ja muistuta, kuinka tärkeää niiden tarkkaileminen on. > Mikäli potilaalla epäillään ITP:tä, ryhdy välittömästi tarvittaviin hoitotoimenpiteisiin ja ohjaa potilas välittömästi hematologin vastaanotolle. Vakava ja runsas vuoto on hengenvaarallista ja vaatii välitöntä hoitoa. Katso oppaan osasta 3. LEMTRADA -hoitoa saavien potilaiden seuranta tärkeitä tietoja valmisteen turvallisesta käytöstä. Mahdollisia LEMTRADA -hoidon uusimiseen liittyviä riskejä sen jälkeen, kun potilas on kerran sairastunut ITP:hen, ei tunneta. 9
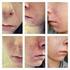
10 Kuva 2 - Esimerkkejä ITP:stä Purppura Tämä on esimerkki säärestä, johon on kehittynyt herkästi tai runsaasti mustelmia. Sijainti Saattaa ilmetä missä tahansa kehon osassa, ei vain säärissä. Petekiat Tämä on esimerkki sääristä, joissa on petekioita ja purppuraa. Petekiat ovat pieniä, nuppineulanpään kokoisia hajanaisia punaisia, vaaleanpunaisia tai violetteja pisteitä iholla. Sijainti Saattaa ilmetä missä tahansa kehon osassa. Tämä on esimerkki kielen alla olevasta purppurasta. Sijainti Petekioita ja purppuraa saattaa ilmetä missä tahansa limakalvoilla, mukaan lukien kaikkialla suussa (kielen alla, kitalaessa, poskien sisäpinnalla, kielessä tai ikenissä). Huomaa: Nämä kuvat ovat esimerkkejä mustelmista ja petekioista. Potilaan oireet voivat olla näissä kuvissa esitettyä lievempiä, ja hänellä voi silti olla ITP. 10
11 c. Munuaissairaudet (kuten tyvikalvovasta-aineglomerulonefriitti) Kliinisissä tutkimuksissa, joissa LEMTRADA -valmistetta annettiin MStautia sairastaville potilaille, munuaissairaustapauksia, kuten tyvikalvovastaaineglomerulonefriittiä, raportoitiin vain harvoin. Yleensä ne todettiin 39 kuukauden kuluessa viimeisestä LEMTRADA -infuusiosta. Munuaissairauden kliinisiä oireita voivat olla seerumin kreatiniiniarvojen kohoaminen, hematuria ja/tai proteinuria. Vaikka alveolaarista verenvuotoa ei tavattukaan kliinisissä tutkimuksissa, veriyskä voi olla yksi tyvikalvovasta-aineglomerulonefriitin (Goodpasturen oireyhtymän) oireista. Koska potilaat voivat olla oireettomia, säännöllisten laboratoriokokeiden suorittaminen on erittäin tärkeää: > Seerumin kreatiniiniarvot mitataan ennen hoidon aloittamista sekä sen jälkeen kuukauden välein, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. Menstruoivilla naisilla virtsa-analyysit tulee ajoittaa sopivasti, jotta vältyttäisiin virheellisiltä positiivisilta tuloksilta. > Virtsakoe, mukaan lukien virtsan mikroskopointi, tulee tehdä ennen hoidon aloittamista sekä sen jälkeen kuukauden välein, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. Tämän jälkeen testi tulee tehdä munuaissairauteen viittaavien kliinisten löydösten perusteella. > Mikäli seerumin kreatiniiniarvoissa havaitaan kliinisesti merkittäviä poikkeamia lähtötason arvoista tai jos potilaalla havaitaan selittämätöntä hematuriaa ja/tai proteinuriaa, on välittömästi tehtävä jatkotutkimukset mahdollisen munuaissairauden selvittämiseksi sekä ohjattava potilas munuaistautien erikoislääkärin vastaanotolle. Kun munuaissairaus pystytään toteamaan ja hoitamaan varhaisessa vaiheessa, huonon hoitotuloksen riski saattaa pienentyä. Tyvikalvovasta-aineglomerulonefriitti on hoitamattomana hengenvaarallinen ja vaatii siksi välitöntä hoitoa. Ellei potilas pääse viipymättä hoitoon, hänelle saattaa kehittyä nopeasti dialyysihoitoa ja/tai elinsiirtoa vaativa munuaisten vajaatoimintahäiriö, joka voi johtaa kuolemaan. Epäillyistä haittavaikutuksista ilmoittaminen On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle: > Fimea, Lääkkeiden haittavaikutusrekisteri, PL 55, FIMEA, tai > Sanofi Oy, puh:
12 3> LEMTRADA -hoitoa saavien potilaiden seuranta > On erittäin tärkeää, että potilas ymmärtää olevansa velvollinen käymään säännöllisesti laboratoriokokeissa (48 kuukauden ajan viimeisen LEMTRADA - infuusion jälkeen), vaikka olisikin oireeton ja vaikka MS-tauti olisi saatu hyvin hallintaan. > Suunnittele ja koordinoi säännöllistä seurantaa yhdessä potilaan kanssa. > Mikäli potilas ei noudata seuranta-aikataulua, hän saattaa tarvita lisäohjeita siitä, mitä riskejä laboratoriokokeiden jättäminen väliin saattaa aiheuttaa. > Arvioi koetulokset ja tarkkaile oireita mahdollisista haittavaikutuksista. > Käykää LEMTRADA -valmisteeseen liittyvä potilaan opas ja pakkausseloste läpi yhdessä potilaan kanssa aluksi hoidon määräämisen yhteydessä ja säännöllisesti seurantakäynneillä. Potilasta tulee informoida hoidon riskeistä ja hyödyistä ennen hoidon aloitusta. Muistuta potilasta tarkkailemaan autoimmuunisairauksiin liittyviä oireita ja hakeutumaan hoitoon, mikäli ongelmia ilmenee. > Kehota potilasta pitämään potilasvaroituskortti aina mukana. Hänen tulee näyttää potilasvaroituskorttia kaikille terveydenhuollon ammattilaisille, jotka hoitavat häntä mistä syystä tahansa, ja erityisesti kiireellisessä hoitotilanteessa. > Useimmin esiintyvien haittavaikutusten, erityisesti autoimmuunitilojen ja infektioiden, oikea-aikaiseen diagnosointiin ja hoitoon erikoistuneita lääkäreitä ja tarvittavia laitteita tulee olla saatavilla. 12
13 4> Usein kysytyt kysymykset Ennen LEMTRADA -valmisteen määräämistä potilaalle on otettava huomioon seuraavat seikat: Mitä laboratoriokokeita on tehtävä ennen LEMTRADA -hoidon aloittamista? Tarvittavat kokeet ovat: > Täydellinen verenkuva ja erittelylaskenta > Seerumin kreatiniinin mittaus > Virtsakoe, mukaan lukien virtsan mikroskopointi > Kilpirauhasen toimintakokeet, kuten TSH-mittaukset Katso lisätietoja taulukosta 1 Yleiskatsaus LEMTRADA -hoidon seurantaan. Voinko määrätä LEMTRADA -valmistetta potilaille, jotka käyttävät jotakin muuta MSlääkitystä? LEMTRADA -valmistetta ei ole käytetty immunosuppresiivisten lääkkeiden rinnalla MStaudin hoidossa. Kuten muidenkin immuunijärjestelmää säätelevien hoitojen kohdalla, mahdollinen yhteisvaikutus potilaan immuunijärjestelmään tulee ottaa huomioon, kun LEMTRADA -hoitoa harkitaan. Edellä mainittujen lääkkeiden ja LEMTRADA -valmisteen rinnakkaiskäyttö saattaa lisätä immunosuppression riskiä. Jos LEMTRADA -valmistetta käytetään muiden MS-taudin kulkua muuntavien hoitojen jälkeen, hoito on toteutettava LEMTRADA -valmisteen ja kyseessä olevan muun lääkkeen valmisteyhteenvedon mukaisesti. Jatketaanko laboratoriokokeiden tekemistä LEMTRADA -hoitojen aikana sekä niiden jälkeen? Kuinka kauan? Kyllä. Kokeet alkavat ennen hoidon aloittamista (lähtötason testit) ja kokeita on jatkettava, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. Lisätietoja siitä, mitä kokeita tulee suorittaa, milloin, ja kuinka pitkään, on kohdassa Yleiskatsaus LEMTRADA -hoidon seurantaan. Entä jos potilaallani on jokin infektio juuri silloin, kun olin aikonut aloittaa LEMTRADA -hoidon? Mikäli potilaalla on vaikea-asteinen aktiivinen infektio, LEMTRADA -hoidon aloittamista on siirrettävä, kunnes infektio on parantunut. HIV-infektio on LEMTRADA -valmisteen käytön vasta-aihe. 13
14 Hoito Miten LEMTRADA -valmistetta annetaan ja kuinka kauan infuusio kestää? LEMTRADA -hoito aloitetaan laskimonsisäisellä infuusiolla kahden eri hoitojakson aikana, jotka järjestetään vuoden välein. Ensimmäisellä hoitojaksolla infuusioita annetaan päivittäin viitenä peräkkäisenä päivänä. Toinen hoitojakso järjestetään 12 kuukauden kuluttua, jolloin potilaalle annetaan infuusioita päivittäin kolmena peräkkäisenä päivänä. Jos kliinisiin löydöksiin ja kuvantamislöydöksiin perustuvien kriteerien mukaan saadaan näyttöä MS-taudin aktiivisuudesta, voidaan harkita tarpeen mukaan annettavaa kolmatta ja neljättä lisähoitojaksoa. Näillä hoitojaksoilla annetaan infuusioita päivittäin kolmena peräkkäisenä päivänä vähintään 12 kuukauden kuluttua aiemmasta hoitojaksosta. Mikäli ilmenee infuusioon liittyviä reaktioita, tarvittaessa on annettava oireen mukaista hoitoa. Jos potilas sietää huonosti infuusiota, sen kestoa voidaan pidentää. Vakavien infuusioon liittyvien reaktioiden ilmetessä on harkittava infuusion välitöntä keskeyttämistä. Kliinisissä tutkimuksissa anafylaksiatapaukset tai vakavat hoidon keskeyttämistä vaatineet reaktiot olivat erittäin harvinaisia. Saatavilla tulisi aina olla tarvittavat resurssit anafylaksian tai vakavien reaktioiden hoitamiseksi. Lääkäreiden on oltava tietoisia potilaan sydänsairauksista, koska infuusioon voi liittyä sydänoireita, kuten bradykardiaa tai takykardiaa. Anafylaktisten tai vakavien reaktioiden hoitoon tarvittavien hoitomahdollisuuksien on oltava saatavilla. Tarvitaanko jotakin estolääkitystä? Potilaille annetaan esilääkityksenä kortikosteroideja (1 000 mg metyyliprednisolonia tai vastaavaa) juuri ennen LEMTRADA -infuusiota kunkin hoitojakson kolmena ensimmäisenä päivänä. Lisäksi voidaan harkita antihistamiinien ja/tai antipyreettien antamista ennen LEMTRADA -infuusiota. Herpesinfektioiden ehkäisemiseksi kaikille potilaille tulisi antaa oraalista estolääkitystä sekä hoitojakson aikana että ainakin kuukauden ajan sen jälkeen. Kliinisissä tutkimuksissa potilaille annettiin 200 mg asikloviiria [tai vastaavaa] kahdesti päivässä. 14 Haittavaikutusten seuranta Mitä oireita ITP aiheuttaa? ITP:stä aiheutuvia oireita voivat olla muun muassa (mutta eivät yksinomaan) mustelmaalttius, petekiat (hiussuonipurkaumat), spontaani mukokutaaninen verenvuoto (esim. ikenistä tai nenästä) sekä tavallista runsaammat tai epäsäännölliset kuukautiset. Näitä kliinisiä ITP:n oireita saattaa esiintyä jo ennen kuin verenvuoto muuttuu vaikeaasteiseksi. Alhainen verihiutaleiden määrä tai kliinisesti merkittävät poikkeamat täydellisen verenkuvan ja erittelylaskennan lähtötason arvoista voivat myös olla merkki ITP:stä. Katso lisätietoja kuvasta 2.
15 Miten minun tulisi hoitaa potilasta, jolla epäillään ITP:tä? Kaikkia potilaita on tärkeää monitoroida ITP:n varalta, jotta sairaus voidaan diagnosoida ja saada hallintaan ajoissa. Tästä syystä potilaalta tulisi ottaa täydellinen verenkuva ennen hoidon aloittamista sekä sen jälkeen kuukauden välein, kunnes viimeisestä infuusiosta on kulunut 48 kuukautta. Mikäli potilaalla epäillään ITP:tä, verihiutaleiden määrä on tutkittava välittömästi. Jos sairaus on varmistettu, ryhdy välittömästi tarvittaviin hoitotoimenpiteisiin ja ohjaa potilas hematologin vastaanotolle. Vakava ja runsas vuoto on hengenvaarallista ja vaatii välitöntä hoitoa. Mitä oireita munuaissairauteen, kuten tyvikalvovasta-aineglomerulonefriittiin, voi liittyä? Oireita munuaissairaudesta voivat olla seerumin kreatiniiniarvojen kohoaminen, hematuria ja/tai proteinuria. Vaikka alveolaarista verenvuotoa ei tavattukaan kliinisissä tutkimuksissa, veriyskää voi esiintyä tyvikalvovasta-aineglomerulonefriitin yhteydessä. Koska potilaat voivat olla oireettomia, on säännöllisten laboratoriokokeiden (seerumin kreatiniiniarvojen mittauksen sekä virtsa-analyysien) suorittaminen tärkeää. Miten minun tulisi hoitaa potilasta, jolla epäillään munuaissairautta? Mikäli havaitaan kliinisesti merkittäviä muutoksia seerumin kreatiniiniarvoissa, selittämätöntä hematuriaa ja/tai proteinuriaa, munuaissairauden lisäarviointi on aloitettava ja potilas lähetettävä viipymättä erikoislääkärille. Munuaissairauksien varhainen tunnistus ja hoito voi pienentää huonojen hoitotulosten vaaraa. Raskautta, ehkäisyä ja imetystä koskeva neuvonta Onko naispotilaiden käytettävä ehkäisyä? Alemtutsumabin alkuvaiheen puoliintumisaika oli noin 4 5 päivää, ja se oli vastaava eri hoitojaksoilla. Seerumipitoisuudet laskivat mataliksi tai olemattomiksi noin 30 päivän kuluessa kunkin hoitojakson jälkeen. Tästä syystä hedelmällisessä iässä olevien naisten tulee käyttää tehokasta ehkäisyä sekä hoidon aikana että neljä kuukautta kunkin LEMTRADA -hoitojakson jälkeen. On otettava huomioon, että koko LEMTRADA -hoito muodostuu kahdesta hoitojaksosta, joiden välillä on 12 kuukautta. Naisten, jotka voivat tulla raskaaksi, on oltava tietoisia tästä ja heitä on kehotettava jatkamaan ehkäisyn käyttöä kahden hoitojakson välillä. Voiko LEMTRADA -hoitoa antaa raskauden aikana? LEMTRADA -valmistetta saa antaa raskauden aikana ainoastaan, kun mahdolliset hyödyt ylittävät sikiölle mahdollisesti koituvan haitan. Ihmisen IgG:n tiedetään läpäisevän istukan; myös alemtutsumabi voi läpäistä istukan ja siten mahdollisesti aiheuttaa riskin sikiölle. Ei tiedetä, voiko LEMTRADA aiheuttaa haittaa sikiölle, kun sitä annetaan raskaana olevalle naiselle, tai voiko se vaikuttaa lisääntymiskykyyn. 15
16 Kilpirauhassairaus aiheuttaa erityisen riskin raskaana oleville naisille. Mikäli kilpirauhasen vajaatoimintaa ei hoideta raskauden aikana, on olemassa suurentunut keskenmenon ja sikiöön kohdistuvien vaikutusten, kehitysvammaisuuden ja lyhytkasvuisuuden, vaara. Gravesin tautia (tunnetaan myös Basedowin tautina) sairastavilla äideillä TSH-reseptorin vasta-aineet voivat siirtyä kehittyvään sikiöön ja aiheuttaa vastasyntyneelle ohimenevän Gravesin taudin. Jos nainen haluaa tulla raskaaksi, miten pitkään on odotettava LEMTRADA - hoitojakson jälkeen? Naisten on käytettävä tehokkaita ehkäisymenetelmiä 4 kuukauden ajan kunkin LEMTRADA -hoitojakson jälkeen, joten heidän on odotettava vähintään 4 kuukautta, ennen kuin yrittävät tulla raskaaksi. On otettava huomioon, että koko alemtutsumabihoito muodostuu kahdesta hoitojaksosta, joiden välillä on 12 kuukautta. Naisten, jotka voivat tulla raskaaksi, on oltava tietoisia tästä ja heitä on kehotettava jatkamaan ehkäisyn käyttöä kahden hoitojakson välillä. Vaikuttaako LEMTRADA naisten tai miesten hedelmällisyyteen jatkossa? Ei ole olemassa riittäviä kliinisiä turvallisuustietoja LEMTRADA -valmisteen vaikutuksesta hedelmällisyyteen. Alatutkimuksessa, johon osallistui 13 alemtutsumabilla hoidettua miespotilasta (joita hoidettiin joko 12 mg:n tai 24 mg:n annoksella), ei esiintynyt merkkejä siemennesteen puuttumisesta, siittiökadosta, jatkuvasti matalasta siittiömäärästä, liikkumishäiriöistä tai siittiöiden morfologisten poikkeavuuksien lisääntymisestä. Ihmisen ja jyrsijöiden lisääntymiskudoksissa tiedetään olevan CD52:ta. Eläinkokeet ovat osoittaneet vaikutuksia humanisoitujen hiirten hedelmällisyyteen (ks. valmisteyhteenvedon kohta 5.3). Kuitenkaan saatavilla olevien tietojen perusteella mahdollista vaikutusta ihmisen hedelmällisyyteen altistusaikana ei tunneta. Voiko lastaan imettävälle potilaalle antaa LEMTRADA -hoitoa? Ei tiedetä, erittyykö alemtutsumabi ihmisen rintamaitoon. Imeväiseen kohdistuvia riskejä ei voida sulkea pois. Siksi imetys on keskeytettävä jokaisen LEMTRADA - hoitojakson ajaksi ja 4 kuukauden ajaksi kunkin hoitojakson viimeisen infuusion jälkeen. Rintamaidon kautta saadun immuniteetin hyödyt voivat kuitenkin olla suurempia imeväiselle kuin potentiaalisen alemtutsumabialtistuksen aiheuttamat riskit. 16 Rokotteet Mitä rokotuksiin liittyviä asioita tulisi ottaa huomioon LEMTRADA -hoitoa suunniteltaessa? Eläviä viruksia sisältävillä rokotteilla tehdyn immunisaation turvallisuutta LEMTRADA - hoidon jälkeen ei ole tutkittu, eikä eläviä viruksia sisältäviä rokotteita saa antaa potilaille, jotka ovat äskettäin saaneet LEMTRADA -hoitojakson. On suositeltavaa, että potilas on saanut kaikki paikallisen rokotusohjelman mukaiset rokotukset vähintään kuusi viikkoa ennen LEMTRADA -hoidon aloittamista. Ennen LEMTRADA -hoidon aloittamista on harkittava rokotusta varicella zoster -virus (VZV) vastaan, jos potilaan elimistössä ei ole kyseisen viruksen vasta-aineita.
17 Muistiinpanot 17
18 18 Muistiinpanot
19
20 GZFI.LEMT , hyväksytty (Fimea) Sanofi Oy puh: ,
Opas terveydenhuollon ammattilaisille
 Opas terveydenhuollon ammattilaisille LEMTRADA -valmisteen (alemtutsumabin) käyttö aaltomaisesti etenevää multippeliskleroosia (RRMS) sairastavien potilaiden hoidossa Sisällysluettelo 1> LEMTRADA -valmisteen
Opas terveydenhuollon ammattilaisille LEMTRADA -valmisteen (alemtutsumabin) käyttö aaltomaisesti etenevää multippeliskleroosia (RRMS) sairastavien potilaiden hoidossa Sisällysluettelo 1> LEMTRADA -valmisteen
Potilaan opas. Tärkeää tietoa LEMTRADA -hoitoa aloittaville potilaille
 Potilaan opas Tärkeää tietoa LEMTRADA -hoitoa aloittaville potilaille Sisällysluettelo 1> LEMTRADA -valmisteen esittely 04 2> Yleiskatsaus LEMTRADA -hoitoon 04 3> Haittavaikutukset 07 4> Muita hyödyllisiä
Potilaan opas Tärkeää tietoa LEMTRADA -hoitoa aloittaville potilaille Sisällysluettelo 1> LEMTRADA -valmisteen esittely 04 2> Yleiskatsaus LEMTRADA -hoitoon 04 3> Haittavaikutukset 07 4> Muita hyödyllisiä
POTILAAN OPAS MAVENCLAD. Potilaan opas. Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä
 MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä MAVENCLAD LÄÄKÄRIN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI - FI/CLA/1117/0049
 Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä
 mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
TÄRKEITÄ TURVALLISUUSTIETOJA RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE
 RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
INFLECTRA SEULONTAKORTTI
 Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE. (alitretinoiini) Lääkärin materiaalit. Potilaan nimi.
 LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
RMP section VI.2 Elements for Public Summary
 RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun
 HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun HIV-positivisilla potilailla on suurentunut munuaisten vajaatoiminnan riski, joka edellyttää
HIV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun HIV-positivisilla potilailla on suurentunut munuaisten vajaatoiminnan riski, joka edellyttää
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0
 PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Proscar. 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
Osa A. Täytetään kaikkien naispotilaiden kohdalla
 Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski
 mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI LEMTRADA 12 mg infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 12 mg alemtutsumabia 1,2 ml:ssa
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI LEMTRADA 12 mg infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 12 mg alemtutsumabia 1,2 ml:ssa
Pioglitazone Actavis
 Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
Tutustu Pioglitazone Actavis -valmisteyhteenvetoon ennen lääkkeen määräämistä Hoidollisten riskien minimointiohje Pioglitazone Actavis 15 mg ja 30 mg tabletit Päivitetty viimeksi 10/2018 Pioglitazone minimointiohje
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
LIITE I VALMISTEYHTEENVETO 1 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Olmesartan medoxomil STADA. 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
VASTA-AIHEET (kts. tarkemmin Terveysportti Duodecim lääketietokanta )
 MS-TAUDIN IMMUNOMODULOIVA LÄÄKITYS Lähteenä Käypähoito-suositus (3.12.2014, kohdennettu päivitys 16.12.2015). MS-tauti käypähoito suositus Lisäksi hoitojen toteutuksessa ja seurannassa huomioitava sairaalakohtaiset
MS-TAUDIN IMMUNOMODULOIVA LÄÄKITYS Lähteenä Käypähoito-suositus (3.12.2014, kohdennettu päivitys 16.12.2015). MS-tauti käypähoito suositus Lisäksi hoitojen toteutuksessa ja seurannassa huomioitava sairaalakohtaiset
HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun
 HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun Tärkeitä seikkoja huomioitavaksi: Tarkasta kaikkien potilaiden kreatiniinipuhdistuma ennen
HBV-tartuntaan liittyvien munuaisongelmien koulutusesite, joka sisältää myös kreatiniinin poistuman mittatikun Tärkeitä seikkoja huomioitavaksi: Tarkasta kaikkien potilaiden kreatiniinipuhdistuma ennen
Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista
 Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista Valmisteyhteenveto on luettava huolellisesti ennen Bupropion Sandoz -valmisteen
Lääkäreille ja apteekkihenkilökunnalle lähetettävät tiedot Bupropion Sandoz 150 mg ja 300 mg säädellysti vapauttavista tableteista Valmisteyhteenveto on luettava huolellisesti ennen Bupropion Sandoz -valmisteen
Suositukset maksan haittavaikutusten välttämiseksi. Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan.
 Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto
 EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI LEMTRADA 12 mg infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 12 mg alemtutsumabia 1,2 ml:ssa
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI LEMTRADA 12 mg infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi injektiopullo sisältää 12 mg alemtutsumabia 1,2 ml:ssa
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi)
 Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto
 EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Apteekkihenkilökunnan
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/188850/2014 Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Jardiance-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla
EMA/188850/2014 Jardiance-valmisteen (empagliflotsiini) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Jardiance-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman hoitoon.
 KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit
Propecia (finasteridi 0,2 ja 1 mg) tabletti , versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
LIITE III. Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin
 HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi
 20 mg/ml infuusiokonsentraatti, liuosta varten Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Terveydenhuollon ammattilainen Usein kysytyt kysymykset
20 mg/ml infuusiokonsentraatti, liuosta varten Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Terveydenhuollon ammattilainen Usein kysytyt kysymykset
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana
 Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Erivedge -valmisteen raskaudenehkäisyohjelma
 Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
Erityisturvallisuustiedote
 Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Laskimonsisäisiin rautavalmisteisiin liittyvien vakavien yliherkkyysreaktioiden riskiä koskevat vahvistetut suositukset
 Lokakuuta 2013 Laskimonsisäisiin rautavalmisteisiin liittyvien vakavien yliherkkyysreaktioiden riskiä koskevat vahvistetut suositukset Hyvä terveydenhuollon ammattilainen, laskimonsisäisten rautavalmisteiden
Lokakuuta 2013 Laskimonsisäisiin rautavalmisteisiin liittyvien vakavien yliherkkyysreaktioiden riskiä koskevat vahvistetut suositukset Hyvä terveydenhuollon ammattilainen, laskimonsisäisten rautavalmisteiden
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 25 BROMOKRIPTIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON MERKITYKSELLISIIN KOHTIIN TEHTÄVÄT MUUTOKSET 4.2 Annostus ja antotapa
Liite III. Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset
 Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
Ethambutol Orion 500 mg tabletit Päivämäärä: , Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Ethambutol Orion 500 mg tabletit Päivämäärä: 21.10.2016, Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Etambutoli on
Ethambutol Orion 500 mg tabletit Päivämäärä: 21.10.2016, Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Etambutoli on
Tarkastuslista määrättäessä asitretiinia naispotilaille
 Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Opas Tietoja potilaille
 Opas Tietoja potilaille Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti
Opas Tietoja potilaille Tärkeää turvallisuutta koskevaa tietoa immuunivälitteisten haittavaikutusten riskin minimoimiseksi Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA
 PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
Hoidon hyötyihin liittyvät asiat, joita ei tunneta (yksi lyhyt kappale kustakin käyttöaiheesta, enintään 50 sanaa)
 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
Perusseikkoja julkista yhteenvetoa varten
 Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
Opas laboratoriohenkilökunnalle
 Opas laboratoriohenkilökunnalle HEMLIBRA (emisitsumabi) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Opas laboratoriohenkilökunnalle HEMLIBRA (emisitsumabi) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
TÄRKEITÄ TURVALLISUUSTIETOJA
 TÄRKEITÄ TURVALLISUUSTIETOJA Tärkeitä Truvada -valmisteen turvallisuustietoja lääkkeen määrääjille altistusta edeltävän estohoidon (Pre-exposure Prophylaxis, PrEP) käyttöaiheessa Truvada (emtrisitabiini/tenofoviiridisoproksiilifumaraatti)
TÄRKEITÄ TURVALLISUUSTIETOJA Tärkeitä Truvada -valmisteen turvallisuustietoja lääkkeen määrääjille altistusta edeltävän estohoidon (Pre-exposure Prophylaxis, PrEP) käyttöaiheessa Truvada (emtrisitabiini/tenofoviiridisoproksiilifumaraatti)
Mikä on HER2-positiivinen rintasyöpä?
 Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Perinnöllinen välimerenkuume
 www.printo.it/pediatric-rheumatology/fi/intro Perinnöllinen välimerenkuume 2. DIAGNOOSI JA HOITO 2.1 Miten tauti todetaan? Yleensä taudin määrittelyssä edetään seuraavasti: Kliininen epäily: Perinnöllistä
www.printo.it/pediatric-rheumatology/fi/intro Perinnöllinen välimerenkuume 2. DIAGNOOSI JA HOITO 2.1 Miten tauti todetaan? Yleensä taudin määrittelyssä edetään seuraavasti: Kliininen epäily: Perinnöllistä
Miten Truvadaa otetaan
 Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Lääkärin opas. Raskauden ja sikiöaltistuksen ehkäisyohjelma
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Ibandronat Stada 150 mg kalvopäällysteiset tabletit. 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
EMA/198014/2014 Sylvant (siltuksimabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on Sylvant-valmistetta koskevan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joiden
Liite I. Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle
 Liite I Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle Tieteelliset johtopäätökset Kun otetaan huomioon lääketurvallisuuden riskinarviointikomitean (PRACin) arviointiraportti
Liite I Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle Tieteelliset johtopäätökset Kun otetaan huomioon lääketurvallisuuden riskinarviointikomitean (PRACin) arviointiraportti
Lääkealan turvallisuus- ja kehittämiskeskuksen ohje HAITTAVAIKUTUSTEN ILMOITTAMINEN
 Ohje 27.2.2017 6895/00.01.02/2016 1/2017 Lääkealan turvallisuus- ja kehittämiskeskuksen ohje HAITTAVAIKUTUSTEN ILMOITTAMINEN Kohderyhmät Lääkkeen määräämiseen tai toimittamiseen oikeutetut henkilöt Voimassaoloaika
Ohje 27.2.2017 6895/00.01.02/2016 1/2017 Lääkealan turvallisuus- ja kehittämiskeskuksen ohje HAITTAVAIKUTUSTEN ILMOITTAMINEN Kohderyhmät Lääkkeen määräämiseen tai toimittamiseen oikeutetut henkilöt Voimassaoloaika
Lääkealan turvallisuus- ja kehittämiskeskuksen ohje LÄÄKKEIDEN HAITTAVAIKUTUSTEN ILMOIT- TAMINEN
 Ohje x.x.2017 6895/00.01.02/2016 x/2017 Lääkealan turvallisuus- ja kehittämiskeskuksen ohje LÄÄKKEIDEN HAITTAVAIKUTUSTEN ILMOIT- TAMINEN Kohderyhmät Lääkkeen määräämiseen tai toimittamiseen oikeutetut
Ohje x.x.2017 6895/00.01.02/2016 x/2017 Lääkealan turvallisuus- ja kehittämiskeskuksen ohje LÄÄKKEIDEN HAITTAVAIKUTUSTEN ILMOIT- TAMINEN Kohderyhmät Lääkkeen määräämiseen tai toimittamiseen oikeutetut
Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin
 Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
Uutta lääkkeistä: Ulipristaali
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
19.2.2014, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen
 Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen Huom! Nämä muutokset sisällytetään voimassa oleviin valmisteyhteenvetoon, myyntipäällysmerkintöihin ja pakkausselosteeseen, jotka ovat koordinaatioryhmämenettelyssä
Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen Huom! Nämä muutokset sisällytetään voimassa oleviin valmisteyhteenvetoon, myyntipäällysmerkintöihin ja pakkausselosteeseen, jotka ovat koordinaatioryhmämenettelyssä
Potilaan päiväkirja. Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi
 Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
Potilaan päiväkirja Avuksi maksa-arvojen ja käyntiaikojen seurantaan ensimmäisen hoitovuoden ajaksi POTILAAN TIEDOT Nimi: Osoite: Puh.: Erikoislääkäri: Erikoislääkärin puh.: Parkinsonhoitaja: Parkinsonhoitajan
Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten tenofoviiridisoproksiilifumaraattihoidon aikana
 Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten fumaraattihoidon aikana HIV-positiivisilla potilailla on suurentunut heikentyneen munuaistoiminnan
Ohjeita terveydenhuollon ammattilaisille munuaistoiminnan hallintaan ja annoksen säätämiseen aikuisten fumaraattihoidon aikana HIV-positiivisilla potilailla on suurentunut heikentyneen munuaistoiminnan
Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio)
 28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit , Versio 1.3
 Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista
 Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista Diasesitys terveydenhuollon ammattilaisten koulutukseen 1 Benepali (etanersepti) Tähän lääkkeeseen kohdistuu lisäseuranta. On tärkeää
Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista Diasesitys terveydenhuollon ammattilaisten koulutukseen 1 Benepali (etanersepti) Tähän lääkkeeseen kohdistuu lisäseuranta. On tärkeää
Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa , Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa 6.7.2016, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden
Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa 6.7.2016, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden
Exviera-valmisteen (dasabuviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775993/2014 Exviera-valmisteen (dasabuviiri) enhallintasuunnitelman yhteenveto Tämä on Exviera-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/775993/2014 Exviera-valmisteen (dasabuviiri) enhallintasuunnitelman yhteenveto Tämä on Exviera-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
NLRP12-geeniin liittyvä toistuva kuume
 www.printo.it/pediatric-rheumatology/fi/intro NLRP12-geeniin liittyvä toistuva kuume 1. MIKÄ ON NLRP12-GEENIIN LIITTYVÄ TOISTUVA KUUME? 1.1 Mikä se on? NLRP12-geeniin liittyvä toistuva kuume on perinnöllinen
www.printo.it/pediatric-rheumatology/fi/intro NLRP12-geeniin liittyvä toistuva kuume 1. MIKÄ ON NLRP12-GEENIIN LIITTYVÄ TOISTUVA KUUME? 1.1 Mikä se on? NLRP12-geeniin liittyvä toistuva kuume on perinnöllinen
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteiden asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteiden asianmukaisiin kohtiin Huomautus: Seuraavat muutokset valmisteyhteenvedon ja pakkausselosteen tiettyihin kohtiin tehdään sovittelumenettelyn
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteiden asianmukaisiin kohtiin Huomautus: Seuraavat muutokset valmisteyhteenvedon ja pakkausselosteen tiettyihin kohtiin tehdään sovittelumenettelyn
