Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa
|
|
|
- Juho-Matti Hakala
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa Raskauden ja sikiöaltistuksen ehkäisyohjelma
2 Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia, joka on erittäin teratogeenistä. Sikiön isotretinoiinille altistumiseen liittyy erittäin korkea hengenvaarallisten synnynnäisten epämuodostumien riski. Isotretinoiinin raskauden ja sikiöaltistuksen ehkäisyohjelma on kehitetty varmistamaan, että naispotilaat eivät ole raskaana isotretinoiinihoitoa aloitettaessa eivätkä tule raskaaksi isotretinoiinihoidon aikana ja ainakaan kuukauteen hoidon lopettamisen jälkeen. Ohjelmassa kuvataan myös muita potilasryhmiä koskevat toimet, joilla sikiöaltistuksen riskiä voidaan pienentää. Tämä esite toimii oppaana isotretinoiinia toimitettaessa raskauden ja sikiöaltistuksen ehkäisyohjelman mukaisesti. Yksityiskohtaisempi kuvaus raskauden ja sikiöaltistuksen ehkäisyohjelmasta on luettavissa isotretinoiinin hyväksytystä valmisteyhteenvedosta kohdasta 4.4. Varoitukset ja käyttöön liittyvät varotoimet. Huomaa, että tässä oppaassa on tietoa liittyen vain raskauden ja sikiöaikaisen altistuksen ehkäisemisestä yksityiskohtaisemmat tiedot lääkkeen määräämiseen, mukaan lukien tiedot haittavaikutuksista on luettavissa isotretinoiinin valmisteyhteenvedosta.
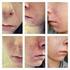
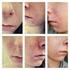
3 Isotretinoiinin teratogeeniset riskit Jos nainen tulee raskaaksi isotretinoiinihoidon aikana tai kuukauden sisällä isotretinoiinihoidon lopettamisen jälkeen, hyvin vaikea-asteisten ja vakavien sikiön epämuodostumien riski on suuri. Myös spontaaneja keskenmenoja esiintyy useammin.
4 Isotretinoiinin raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiinin raskauden ja sikiöaltistuksen ehkäisyohjelmaa on noudatettava kaikkien niiden naispotilaiden kohdalla, jotka voivat tulla raskaaksi. Ohjelma koostuu kolmesta osasta: Koulutusohjelma Hoidon hallinta Lääkkeen toimituksen kontrollointi Koulutusohjelma Koulutusohjelman tarkoituksena on: lisätä sekä potilaiden että lääkärien tietoa isotretinoiinin teratogeenisistä riskeistä lisätä naispotilaiden tietoisuutta ja ymmärrystä. Koulutusohjelman osana toimitetaan seuraavat esitteet: Lääkärin opas isotretinoiinin määräämiseen Lääkärin tarkastuslista määrättäessä isotretinoiinia naispotilaille Apteekkihenkilökunnan opas isotretinoiinia toimitettaessa (tämä asiakirja) Potilaan opas
5 Hoidon hallinta Hoidon hallinta isotretinoiinin raskauden ja sikiöaltistuksen ehkäisyohjelmassa perustuu: koulutusmateriaalin jakamiseen potilaille terveydenhoitohenkilöstön valvomaan raskaustestiin ennen hoitoa, sen aikana ja 5 viikkoa hoidon loppumisen jälkeen ainakin yhden tehokkaan ehkäisymenetelmän käyttöön. Potilaan on suositeltavaa käyttää kahta toisiaan täydentävää ehkäisymenetelmää, mukaan lukien estemenetelmä, ainakin yhden kuukauden ajan ennen hoidon aloittamista ja jatkaa näin koko hoitojakson ajan ja ainakin yhden kuukauden ajan hoidon lopettamisen jälkeen. Lääkkeen toimituksen kontrollointi Raskauden ja sikiöaltistuksen ehkäisyohjelmassa naisten isotretinoiinilääkemääräys saa sisältää vain 30 päivän annoksen ja lääkemääräys on voimassa vain seitsemän päivää.
6 Ehdot isotretinoiinin määräämiselle naispotilaille, joiden kohdalla raskaus on mahdollinen Isotretinoiinin käyttö on vasta-aiheista hedelmällisessä iässä olevien naisten hoidossa, elleivät kaikki seuraavat raskaudenehkäisyohjelman ehdot täyty: Naisella on vaikea-asteinen akne (nodulaarinen akne, onteloakne (acne conglobata) tai akne, johon liittyy pysyvä arpeutumisvaara), joka on resistentti asianmukaisille systeemisesti käytettäville antibakteerisille lääkkeille ja paikallisella hoidolla toteutetulle vakiohoidolle. Nainen ymmärtää teratogeenisuuden riskin. Nainen ymmärtää tiiviin kuukausittaisen seurannan tarpeen. Nainen ymmärtää ja hyväksyy tehokkaan ja keskeytyksettömän ehkäisyn tarpeellisuuden, joka aloitetaan kuukausi ennen hoidon aloittamista ja jota jatketaan koko hoidon keston ajan sekä yhden kuukauden ajan hoidon lopettamisen jälkeen. Hoidon aikana on käytettävä ainakin yhtä ja mieluiten kahta toisiaan täydentävää ehkäisymenetelmää mukaan lukien estemenetelmä. Naisen on noudatettava kaikkia annettuja tehokkaaseen ehkäisyyn liittyviä neuvoja, vaikkei hänellä olisikaan kuukautisvuotoa (amenorrea). Naisen on kyettävä huolehtimaan tehokkaasta ehkäisystä. Naiselle on kerrottu raskauden mahdollisista seurauksista ja hän ymmärtää ne. Hän ymmärtää myös, miksi on otettava nopeasti yhteys lääkäriin, jos epäilee olevansa raskaana. Nainen ymmärtää raskaustestin tarpeellisuuden ennen hoitoa, hoidon aikana ja viisi viikkoa hoidon lopettamisen jälkeen ja hyväksyy asian. Nainen on vahvistanut ymmärtäneensä vaarat ja välttämättömät varotoimet, joita isotretinoiinin käyttöön liittyy.
7 Nämä ehdot koskevat myös naisia, jotka eivät sillä hetkellä ole seksuaalisesti aktiivisia, ellei lääkemääräyksen antaja ole sitä mieltä, että on olemassa pakottavia syitä, jotka sulkevat raskauden mahdollisuuden pois. Lääkemääräyksen antajan on varmistettava seuraavat seikat: Potilas noudattaa edellä mainittuja raskaudenehkäisyyn liittyviä ehtoja ja vahvistaa, että hän on riittävässä määrin ymmärtänyt asian. Potilas hyväksyy ja vahvistaa yllä mainitut ehdot. Potilas on käyttänyt ainakin yhtä ja mieluiten kahta tehokasta ehkäisymenetelmää, mukaan lukien estemenetelmä, ainakin yhden kuukauden ajan ennen hoidon aloittamista ja jatkaa näin koko hoitojakson ajan ja ainakin yhden kuukauden ajan hoidon lopettamisen jälkeen. Raskaustestistä on saatu negatiivinen tulos ennen hoitoa, sen aikana ja viisi viikkoa hoidon lopettamisen jälkeen. Raskaustestien päivämäärät ja tulokset on dokumentoitava.
8 Lisävarotoimet Naispotilaat, joiden kohdalla raskaus ei ole mahdollinen On tärkeää, että myös naisia, jotka eivät voi tulla raskaaksi, varoitetaan isotretinoiinin teratogeenisistä vaaroista. Ehkäisyn tärkeydestä on keskusteltava myös näiden potilaiden kanssa, sillä olosuhteet voivat muuttua, vaikka nainen ei voisikaan tulla raskaaksi isotretinoiinihoitoa aloitettaessa. Naisille, jotka voivat tulla raskaaksi, on annettava kattavat tiedot isotretinoiinin teratogeenisestä riskistä ja tiukoista raskaudenehkäisyvaatimuksista. Miespotilaat Saatavilla olevat tiedot osoittavat, että isotretinoiinia käyttävien miespotilaiden siemennesteestä aiheutuneen äitiin kohdistuvan altistuksen taso ei ole riittävän suuri, jotta siihen liittyisi isotretinoiinin teratogeenisiä vaikutuksia. Miespotilaita on kuitenkin muistutettava siitä, että he eivät saa jakaa lääkkeitään kenenkään kanssa, varsinkaan naisten. Miespotilaille on annettava kattavat tiedot isotretinoiinin teratogeenisestä riskistä ja tiukoista raskaudenehkäisyvaatimuksista. Kaikki potilaat Potilaille on kerrottava, että he eivät saa koskaan antaa isotretinoiinia toiselle henkilölle ja että heidän on hoidon päätyttyä palautettava mahdolliset käyttämättömät kapselit apteekkiin. Kaikille potilaille on kerrottava, että he eivät saa luovuttaa verta hoidon aikana eivätkä yhteen kuukauteen isotretinoiinihoidon päättymisen jälkeen, sillä verensiirrosta voi aiheutua riskejä raskaana olevan naisen sikiölle.
9 Isotretinoiinin toimittamiseen liittyvät rajoitukset Isotretinoiinilääkemääräyksiä koskevat seuraavat toimitusrajoitukset raskauden ja sikiöaltistuksen ehkäisyohjelman mukaisesti: 1. Naisille kirjoitettu isotretinoiinin lääkemääräys saa sisältää vain 30 päivän lääkeannoksen ja se on voimassa seitsemän päivän ajan. Raskauden ja sikiöaltistuksen ehkäisyohjelman mukaisesti yli seitsemän päivää vanhat lääkemääräykset ovat vanhentuneet ja potilasta on tällöin kehotettava hakemaan lääkäriltään uusi lääkemääräys. Joidenkin naispotilaiden kohdalla tämä saattaa edellyttää myös uutta raskaustestiä ja negatiivista testitulosta. Jos naispotilaalla on lääkemääräys, joka sisältää yli 30 päivän lääkeannoksen, lääkkeen määrääjään on otettava yhteys ja varmistettava, kuuluuko potilas raskauden ja sikiöaltistuksen ehkäisyohjelman piiriin. Jos potilasta ei hoideta raskauden ja sikiöaltistuksen ehkäisyohjelman mukaisesti, isotretinoiini voidaan toimittaa. Jos olet epävarma, varmista asia lääkkeen määränneeltä lääkäriltä. 2. Miehille kirjoitetuissa lääkemääräyksissä ei ole rajoitusta hoidon keston tai lääkemääräyksen voimassaolon suhteen. 3. Ihanteellisessa tapauksessa raskaustesti, lääkemääräyksen kirjoittaminen ja isotretinoiinin toimittaminen apteekista tapahtuu samana päivänä. 4. Älä hyväksy seuraavia: Puhelimessa tehdyt isotretinoiinilääkemääräykset Uusitut lääkemääräykset Ilmaiset lääkenäytteet 5. Kaikille potilaille on kerrottava seuraavat tiedot: Tätä lääkettä ei saa koskaan antaa toiselle henkilölle. Mahdolliset käyttämättömät kapselit on palautettava apteekkiin hoidon päätyttyä. Potilas ei saa luovuttaa verta hoidon aikana tai yhteen kuukauteen isotretinoiinihoidon päättymisen jälkeen, koska siitä aiheutuu mahdollinen riski sikiölle, jos verensiirtopotilas on raskaana.
10 Lisätietoja Koulutusmateriaalit ovat saatavilla Tuotekohtainen riskienhallintamateriaali Fimean verkkosivuilla: ( Terveysportissa sekä Galenoksen ( verkkosivuilla. Painetun potilasoppaan tilaaminen Markkinointimateriaalit Tilaa valmiita materiaaleja Reseptilääkkeet Laatimispäivämäärä: XX.XX.2015
11
12 Orion Oyj, Orion Pharma, PL 400, Espoo Orion Pharma 6/2015, MXXXX
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Lääkärin opas. Raskauden ja sikiöaltistuksen ehkäisyohjelma
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Lääkärin opas Raskauden ja sikiöaltistuksen ehkäisyohjelma Johdanto Isotretinoiinikapselit sisältävät vaikuttavana aineena isotretinoiinia,
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Raskauden ja sikiöaltistuksen ehkäisyohjelma Apteekkihenkilökunnan opas isotretinoiininia toimitettaessa Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Apteekkihenkilökunnan
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Raskauden ja sikiöaltistuksen ehkäisyohjelma Lääkärin opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Lääkärin opas Johdanto Isotretinoin Actavis sisältää vaikuttavana
Apteekkihenkilökunnan
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Apteekkihenkilökunnan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on
Apteekkihenkilökunnan opas
 Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Apteekkihenkilökunnan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Asitretiinin teratogeeniset riskit Acitretin Orifarm sisältää vaikuttavana
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Lääkärin opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Johdanto Neotigason sisältää vaikuttavana aineena asitretiinia, joka on erittäin teratogeenistä.»
Osa A. Täytetään kaikkien naispotilaiden kohdalla
 Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Raskauden ja sikiöaltistuksen ehkäisyohjelma Tarkastuslista määrättäessä isotretinoiinia naispotilaille Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Tarkastuslista
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Lääkärin opas. Acitretin Orifarm 10 mg ja 25 mg kovat kapselit. Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Lääkärin opas Acitretin Orifarm 10 mg ja 25 mg kovat kapselit Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Acitretin Orifarm sisältää vaikuttavana aineena asitretiinia, joka
Lääkärin opas Acitretin Orifarm 10 mg ja 25 mg kovat kapselit Raskauden ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Johdanto Acitretin Orifarm sisältää vaikuttavana aineena asitretiinia, joka
Tarkastuslista määrättäessä asitretiinia naispotilaille
 Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Tarkastuslista määrättäessä asitretiinia naispotilaille Acitretin Orifarm 10 mg:n ja 25 mg:n kovat kapselit Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini on erittäin teratogeenistä
Isotretinoin Actavis
 Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Raskauden ja sikiöaltistuksen ehkäisyohjelma Potilaan opas Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Isotretinoin Potilaan opas Tämän esitteen tarkoitus Tämä esite sisältää
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE. (alitretinoiini) Lääkärin materiaalit. Potilaan nimi.
 LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
LÄÄKÄRIN TARKISTUSLISTA/VAHVISTUSLOMAKE MÄÄRÄTTÄESSÄ LÄÄKETTÄ NAISPOTILAILLE (alitretinoiini) Lääkärin materiaalit Potilaan nimi alitretinoiini Lääkärin materiaalit Lääkärin tarkistuslista/vahvistuslomake
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin Orifarm Tietoja lääkärille. Raskaudenehkäisyohjelma Hoito-ohjeet
 Isotretinoin Orifarm Tietoja lääkärille Raskaudenehkäisyohjelma Hoito-ohjeet Johdanto Isotretinoin Orifarm -valmisteen hyväksytty käyttöaihe on vaikea, asianmukaiseen systeemiseen antibioottihoitoon ja
Isotretinoin Orifarm Tietoja lääkärille Raskaudenehkäisyohjelma Hoito-ohjeet Johdanto Isotretinoin Orifarm -valmisteen hyväksytty käyttöaihe on vaikea, asianmukaiseen systeemiseen antibioottihoitoon ja
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta sikiöepämuodostumien
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
EU Core koulutusmateriaali. Asitretiini, 10 mg ja 25 mg, kovat kapselit
 Versio Nro 4.0 Päiväys 04.05.2016 Korvaa version Nro 3.0 Päiväys 29.01.2016 Viite CCSI Versionro 8 10.12.2015 EU Core koulutusmateriaali Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini,
Versio Nro 4.0 Päiväys 04.05.2016 Korvaa version Nro 3.0 Päiväys 29.01.2016 Viite CCSI Versionro 8 10.12.2015 EU Core koulutusmateriaali Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Asitretiini,
Toctino (alitretinoiini)
 Raskauden ehkäisyohjelma TOC-FI-003-04032009-B OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet
Raskauden ehkäisyohjelma TOC-FI-003-04032009-B OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet
(alitretinoiini) Potilaskortti RASKAUDENEHKÄISYOHJELMA. Potilaan nimi. alitretinoiini
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210mm Pages: 8 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 RASKAUDENEHKÄISYOHJELMA
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210mm Pages: 8 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 RASKAUDENEHKÄISYOHJELMA
Toctino (alitretinoiini)
 Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Potilaskortti Potilaan nimi TOC-FI-003-04032009-C RASKAUDENEHKÄISYOHJELMA Toctino (alitretinoiini) Toctino kuuluu lääkeaineryhmään, jonka tiedetään aiheuttavan synnynnäisiä epämuodostumia. Sikiöepämuodostumien
Erivedge -valmisteen raskaudenehkäisyohjelma
 Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
Erivedge -valmisteen raskaudenehkäisyohjelma Tärkeää tietoa Erivedge -valmistetta käyttäville mies- ja naispotilaille raskauden ehkäisemisestä ja ehkäisystä. 1 2 Sisältö 1. Johdanto 1.1. Mitä Erivedge
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä
 mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
mykofenolaattimefotiili Opas potilaalle Tietoa syntymättömään lapseen kohdistuvista riskeistä Laatimispäivä: Huhtikuu 2016 Sisällysluettelo Johdanto... 3 Mitkä hoidon riskit ovat?... 3 Ketä riski koskee?...
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski
 mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
mykofenolaattimefotiili Opas terveydenhuoltoalan ammattilaisille Teratogeenisyysriski Laatimispäivä: Huhtikuu 2016 Johdanto Tämä esite, Myfenax (mykofenolaattimofetiili) Opas terveydenhuoltoalan ammattilaisille,
Liite III. Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom. Nämä muutokset valmistetietojen asianmukaisiin kohtiin on laadittu referraalimenettelyssä. Direktiivin 2001/83/EY III otsikon 4. luvussa
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom. Nämä muutokset valmistetietojen asianmukaisiin kohtiin on laadittu referraalimenettelyssä. Direktiivin 2001/83/EY III otsikon 4. luvussa
POTILASOPAS. Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä
 POTILASOPAS Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä Tämä opas on tarkoitettu tytöille ja naisille, jotka käyttävät valproaattia
POTILASOPAS Valproaatti* (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) Ehkäisy ja raskaus: Mitä sinun on tiedettävä Tämä opas on tarkoitettu tytöille ja naisille, jotka käyttävät valproaattia
Erivedge -valmisteen raskaudenehkäisyohjelma. Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle
 Erivedge -valmisteen raskaudenehkäisyohjelma Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle 1 2 Sisällysluettelo: 1. Johdanto 1.1 Lääkärin rooli Erivedge -valmisteen raskaudenehkäisyohjelmassa
Erivedge -valmisteen raskaudenehkäisyohjelma Tietoa Erivedge -hoitoa määräävälle terveydenhuollon ammattilaiselle 1 2 Sisällysluettelo: 1. Johdanto 1.1 Lääkärin rooli Erivedge -valmisteen raskaudenehkäisyohjelmassa
Liite III. Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huomaa: Näistä muutoksista valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on päätetty lausuntopyyntömenettelyssä. Jäsenmaiden
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huomaa: Näistä muutoksista valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on päätetty lausuntopyyntömenettelyssä. Jäsenmaiden
Liite II. Tieteelliset päätelmät
 Liite II Tieteelliset päätelmät 74 Tieteelliset päätelmät Britannia käynnisti lääketurvatietojen perusteella direktiivin 2001/83/EY 31 artiklan mukaisen lausuntopyyntömenettelyn 7. heinäkuuta 2016. Se
Liite II Tieteelliset päätelmät 74 Tieteelliset päätelmät Britannia käynnisti lääketurvatietojen perusteella direktiivin 2001/83/EY 31 artiklan mukaisen lausuntopyyntömenettelyn 7. heinäkuuta 2016. Se
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä MAVENCLAD LÄÄKÄRIN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI - FI/CLA/1117/0049
 Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä 31.10.2017 MAVENCLAD LÄÄKÄRIN OPAS Sisältö MAVENCLAD-valmisteen esittely Hoito-ohjelmat Hoidonaikainen seuranta Lymfosyyttien määrä Vaikeat infektiot
Toctino (alitretinoiini)
 OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet huolellisesti ennen kuin
OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE Toctino (alitretinoiini) Raskaudenehkäisyohjelma Ohjeita Toctino-hoitoa määrääville lääkäreille Pyydämme teitä lukemaan nämä ohjeet huolellisesti ennen kuin
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Ensimmäisen annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta
Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia?
 Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia? Reetta Kälviäinen Professori, ylilääkäri EPILEPSIAKESKUS 15.10.2014 Valproaatin käytön rajoituksia naisilla ja tytöillä
Fertiili-ikäisen naisen epilepsian hyvä hoito Milloin ja miten käytän valproaattia? Reetta Kälviäinen Professori, ylilääkäri EPILEPSIAKESKUS 15.10.2014 Valproaatin käytön rajoituksia naisilla ja tytöillä
Toctino (alitretinoiini)
 Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CC Windows Generated in: Acrobat Distiller XI OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE
Cutterguide: No Printing Process: Offset GD: RR 37861 Size: 148 x 210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CC Windows Generated in: Acrobat Distiller XI OHJEET LÄÄKÄREILLE JA APTEEKKIHENKILÖKUNNALLE
Tärkeää tietoa GILENYA (fingolimodi) -hoidosta
 Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
Tähän lääkkeeseen kohdistuu lisäseuranta. Tärkeää tietoa GILENYA (fingolimodi) -hoidosta Vanhemmille/huoltajille Ensimmäisen annoksen jälkeen lääkäri pyytää lasta jäämään vastaanotolle vähintään kuuden
POTILAAN OPAS MAVENCLAD. Potilaan opas. Kladribiini (MAVENCLAD) RMP, versio 1.0 Fimean hyväksymä
 MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
MAVENCLAD Potilaan opas POTILAAN OPAS RISKIENHALLINNAN KOULUTUSMATERIAALI FI/CLA/1117/0050 Tärkeää tietoa MAVENCLAD-hoidon aloittaville potilaille Sisällys MAVENCLAD-valmisteen esittely Kuinka MAVENCLAD-hoito
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
Tärkeää tietoa GILENYA -hoidosta
 Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
Tärkeää tietoa GILENYA -hoidosta Ensimmäisen GILENYA-annoksen jälkeen lääkärisi pyytää sinua jäämään vastaanotolle vähintään kuuden tunnin ajaksi, jotta tarvittaviin toimenpiteisiin voidaan ryhtyä, jos
Propecia (finasteridi 0,2 ja 1 mg) tabletti , versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA
 PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
PROTELOS OSSEOR LÄÄKETTÄ MÄÄRÄÄVÄN LÄÄKÄRIN OPAS JA TARKISTUSLISTA (strontiumranelaatti) Tämä opas on osa Protelos -valmisteen riskinhallintasuunnitelmaa. Oppaan on tarkoitus antaa tietoa Protelos -valmisteen
NIMET, LÄÄKEMUODOT, LÄÄKEVALMISTEIDEN VAHVUUDET, ANNOSTELUREITIT, MYYNTILUVAN HAKIJAT, MYYNTILUVAN HALTIJAT, PAKKAUKSET JA PAKKAUSKOOT JÄSENVALTIOISSA
 LIITE I NIMET, LÄÄKEMUODOT, LÄÄKEVALMISTEIDEN VAHVUUDET, ANNOSTELUREITIT, MYYNTILUVAN HAKIJAT, MYYNTILUVAN HALTIJAT, PAKKAUKSET JA PAKKAUSKOOT JÄSENVALTIOISSA 1 Jäsenvaltio Hakija / myyntiluvan haltija
LIITE I NIMET, LÄÄKEMUODOT, LÄÄKEVALMISTEIDEN VAHVUUDET, ANNOSTELUREITIT, MYYNTILUVAN HAKIJAT, MYYNTILUVAN HALTIJAT, PAKKAUKSET JA PAKKAUSKOOT JÄSENVALTIOISSA 1 Jäsenvaltio Hakija / myyntiluvan haltija
Ohje 6/2018 1(5) THL/1579/ /2018. Operatiivisen toiminnan ohjaus (OPER)
 Ohje 6/2018 1(5) LÄÄKKEEN MÄÄRÄÄMINEN RESEPTILLÄ LÄÄKEHOIDON KESTOAJALLE TULEE PERUSTUA HOIDOLLISEEN TARPEESEEN Valtuutussäännökset Sähköisestä lääkemääräyksestä annetun lain (61/2007) 24 :n 2 momentti
Ohje 6/2018 1(5) LÄÄKKEEN MÄÄRÄÄMINEN RESEPTILLÄ LÄÄKEHOIDON KESTOAJALLE TULEE PERUSTUA HOIDOLLISEEN TARPEESEEN Valtuutussäännökset Sähköisestä lääkemääräyksestä annetun lain (61/2007) 24 :n 2 momentti
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Liite III. Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset
 Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
Liite III Valmisteyhteenvetojen ja pakkausselosteiden tiettyihin kohtiin tehtävät korjaukset 55 Monovalenttisten tuhkarokkorokotteiden valmisteyhteenvetojen tiettyihin kohtiin tehtävät korjaukset Kohta
SARAN JA TUOMAKSEN TARINA
 SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Erityisturvallisuustiedote
 Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Erityisturvallisuustiedote Arava (leflunomidi) on tautiprosessia hidastava antireumaattinen lääke (DMARD), joka on tarkoitettu aikuisten aktiivista nivelreumaa tai aktiivista nivelpsoriaasia sairastavien
Opas terveydenhuollon ammattilaisille. Kadcyla (trastutsumabiemtansiini)
 Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Opas terveydenhuollon ammattilaisille Kadcyla (trastutsumabiemtansiini) Riskienhallintamateriaali, versio 3.0. Hyväksytty Fimeassa 20.11.2018 2 Riskienhallintamateriaali marraskuu 2018 VAROITUS: Riski
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille Riskienhallintamateriaali syyskuu 2016 Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta
ESIMERKKIPAKKAUS AIVASTUX. Erä 1058350. MTnr 0000 Myyntiluvan haltija: Lääketehdas Oy, Lääkekylä, Suomi. Vnr 39 71 65. Vnr 39 71 65. tit q.s.
 ESIMERKKIPAKKAUS AIVASTUX 12 2015 1058350 Käyt. viim.: 12 2015 Erä 1058350 Aivastux 10 mg 10 tabl. Vnr 04 36 79 Ibuprofen 400 mg Glycerol (85%) Sacchar Constit q.s. Käyttötarkoitus: Allergisen nuhan, allergisten
ESIMERKKIPAKKAUS AIVASTUX 12 2015 1058350 Käyt. viim.: 12 2015 Erä 1058350 Aivastux 10 mg 10 tabl. Vnr 04 36 79 Ibuprofen 400 mg Glycerol (85%) Sacchar Constit q.s. Käyttötarkoitus: Allergisen nuhan, allergisten
Potilasesite. Jinarc (tolvaptaani)
 Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Jinarc (tolvaptaani) Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti uutta turvallisuutta koskevaa tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista.
Tietovihkonen potilaille, joille on määrätty Volibris-valmistetta
 Printing Process: Offset Cutterguide: No GD: RR 37861 Size: 148X210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietovihkonen potilaille,
Printing Process: Offset Cutterguide: No GD: RR 37861 Size: 148X210 mm Pages: 16 Colors: C M Y K (4 Colors) Native File: Indesign CS5 Windows Generated in: Acrobat Distiller 9.0 Tietovihkonen potilaille,
Version 6, 5 October TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus
 TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä apteekkilainen
TOIMITTAMISOHJE APTEEKEILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä apteekkilainen
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN
 LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
LIITE III MUUTOKSET VALMISTEYHTEENVETOON JA PAKKAUSSELOSTEESEEN 41 KABERGOLIINIA SISÄLTÄVIEN LÄÄKEVALMISTEIDEN VALMISTEYHTEENVEDON 4.2 Annostus ja antotapa: Seuraava tieto tulee lisätä sopivalla tavalla:
Naisella on vapaus valita SINULLE SOPIVIN EHKÄISY
 Naisella on vapaus valita SINULLE SOPIVIN EHKÄISY Jos lasten hankinta ei ole ajankohtaista, on ehkäisyä käytettävä yhdyntöjen aloittamisesta vaihdevuosiin saakka. Niin hormonaalisia kuin muitakin ehkäisyvaihtoehtoja
Naisella on vapaus valita SINULLE SOPIVIN EHKÄISY Jos lasten hankinta ei ole ajankohtaista, on ehkäisyä käytettävä yhdyntöjen aloittamisesta vaihdevuosiin saakka. Niin hormonaalisia kuin muitakin ehkäisyvaihtoehtoja
EU Core koulutusmateriaali. Isotretinoin Actavis, 10 mg ja 20 mg, kapseli, pehmeä
 Versio Nro 2.0 Päiväys 08.12.2015 Korvaa version 1.0 Päiväys 03.09.2013 Viite RMP Versionro 4.0 19.08.2013 EU Core koulutusmateriaali Isotretinoin Actavis, 10 mg ja 20 mg, kapseli, pehmeä 1 Sisältö 1.
Versio Nro 2.0 Päiväys 08.12.2015 Korvaa version 1.0 Päiväys 03.09.2013 Viite RMP Versionro 4.0 19.08.2013 EU Core koulutusmateriaali Isotretinoin Actavis, 10 mg ja 20 mg, kapseli, pehmeä 1 Sisältö 1.
Potilasturvallisuuden edistämisen ohjausryhmä. Potilasturvallisuus on yhteinen asia! Potilasturvallisuus. Kysy hoidostasi vastaanotolla!
 Potilasturvallisuus on yhteinen asia! Potilasturvallisuus on osa hyvää hoitoa kattaa tutkimuksen, hoidon ja laitteiden turvallisuuden tarkoittaa myös sitä, ettei hoidosta aiheutuisi potilaalle haittaa
Potilasturvallisuus on yhteinen asia! Potilasturvallisuus on osa hyvää hoitoa kattaa tutkimuksen, hoidon ja laitteiden turvallisuuden tarkoittaa myös sitä, ettei hoidosta aiheutuisi potilaalle haittaa
Liite III. Muutokset valmisteyhteenvedon, myyntipäällysmerkintöjen ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon, myyntipäällysmerkintöjen ja pakkausselosteen asianmukaisiin kohtiin 20 VALMISTEYHTEENVETO Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita
Liite III Muutokset valmisteyhteenvedon, myyntipäällysmerkintöjen ja pakkausselosteen asianmukaisiin kohtiin 20 VALMISTEYHTEENVETO Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita
TOIMINTA KANTA-PALVELUJEN HÄIRIÖTILANTEESSA
 Sisällysluettelo 1 Johdanto 2 2 Kanta-palvelujen toiminnassa tai yhteyksissä havaitaan häiriö 4 3 Ilmoitus käyttötukeen 5 4 Tiedota häiriöstä muuta henkilöstöä 6 5 Häiriön laajuus 6 6 Toimintamalli Kanta-palvelujen
Sisällysluettelo 1 Johdanto 2 2 Kanta-palvelujen toiminnassa tai yhteyksissä havaitaan häiriö 4 3 Ilmoitus käyttötukeen 5 4 Tiedota häiriöstä muuta henkilöstöä 6 5 Häiriön laajuus 6 6 Toimintamalli Kanta-palvelujen
Proscar. 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Optimointi muutokset vaatimuksissa
 Optimointi muutokset vaatimuksissa STUKin Säteilyturvallisuuspäivät Jyväskylä 24.-25.5.2018 Ylitarkastaja Petra Tenkanen-Rautakoski Optimoinnista säädetään jatkossa SätL 2 luku, 6 Optimointiperiaate Tarkemmat
Optimointi muutokset vaatimuksissa STUKin Säteilyturvallisuuspäivät Jyväskylä 24.-25.5.2018 Ylitarkastaja Petra Tenkanen-Rautakoski Optimoinnista säädetään jatkossa SätL 2 luku, 6 Optimointiperiaate Tarkemmat
LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA
 LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA 1 Jäsenvaltio Myyntiluvanhaltija Käytetty nimi Vahvuus
LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA 1 Jäsenvaltio Myyntiluvanhaltija Käytetty nimi Vahvuus
Versio 8, TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute
 TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana
 Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA
 LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA CPMP/2846/03 1/21 EMEA 2003 Jäsenvaltio Myyntiluvanhaltija
LIITE I LISTA LÄÄKKEEN NIMISTÄ, ANNOSMUODOISTA, VAHVUUKSISTA, ANTOREITEISTÄ, MYYNTILUVANHALTIJOISTA, PAKKAUKSISTA JA PAKKAUSKOISTA JÄSENVALTIOISSA CPMP/2846/03 1/21 EMEA 2003 Jäsenvaltio Myyntiluvanhaltija
Tähän lääkkeeseen kohdistuu lisäseuranta. Usein kysytyt kysymykset. Terveydenhuollon ammattilaisten esite.
 Tähän lääkkeeseen kohdistuu lisäseuranta. Usein kysytyt kysymykset. Terveydenhuollon ammattilaisten esite. Sisältö 1. Mikä on esitteen tarkoitus? 4 2. Mitä OPSUMIT on? 4 3. Mitkä ovat OPSUMITin käyttöaiheet?
Tähän lääkkeeseen kohdistuu lisäseuranta. Usein kysytyt kysymykset. Terveydenhuollon ammattilaisten esite. Sisältö 1. Mikä on esitteen tarkoitus? 4 2. Mitä OPSUMIT on? 4 3. Mitkä ovat OPSUMITin käyttöaiheet?
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Isotretinoin Orifarm 20 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 20 mg Yksi kapseli, pehmeä, sisältää 20 mg isotretinoiinia. Apuaineet, joiden
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Isotretinoin Orifarm 20 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 20 mg Yksi kapseli, pehmeä, sisältää 20 mg isotretinoiinia. Apuaineet, joiden
LISÄTIETOLOMAKE 3 Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52
 Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) keskenmenohetkellä Sikiöiden lukumäärä Keskenmenoon mahdollisesti vaikuttaneet tekijät
Keskenmeno (sivu 1/4) Palauta tämä lomake faksilla HRA Pharmaan numeroon + 33 1 42 77 03 52 Raskauden kesto (viikkoa) keskenmenohetkellä Sikiöiden lukumäärä Keskenmenoon mahdollisesti vaikuttaneet tekijät
Kadcyla (trastutsumabiemtansiini)
 Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
Kadcyla (trastutsumabiemtansiini) Opas terveydenhuollon ammattilaisille 2 VAROITUS: Riski Kadcylan ja Herceptinin vaihtumisesta Lääkkeen määräämiseen, käyttökuntoon saattamiseen ja antoon liittyvissä vaiheissa
Tästä asiasta tiedottamisesta on sovittu Euroopan lääkeviraston (EMA) ja Lääkealan turvallisuus- ja kehittämiskeskuksen (Fimea) kanssa.
 24.10.2011 Helsinki TÄRKEÄÄ TURVALLISUUSTIETOA HÄDENSA -PERÄPUIKOISTA Hyvä terveydenhuollon ammattilainen Terpeenijohdoksia sisältävien peräpuikkojen käyttö on vastaaiheista alle 2½-vuotialla lapsilla
24.10.2011 Helsinki TÄRKEÄÄ TURVALLISUUSTIETOA HÄDENSA -PERÄPUIKOISTA Hyvä terveydenhuollon ammattilainen Terpeenijohdoksia sisältävien peräpuikkojen käyttö on vastaaiheista alle 2½-vuotialla lapsilla
VALMISTEYHTEENVETO. Apuaineet: puhdistettu soijaöljy, hydrattu soijaöljy, osittain hydrattu soijaöljy Täydellinen apuaineluettelo, ks. kohta 6.1.
 1. LÄÄKEVALMISTEEN NIMI Isotretinoin Orion 20 mg kapseli, pehmeä VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 20 mg isotretinoiinia. Apuaineet: puhdistettu soijaöljy,
1. LÄÄKEVALMISTEEN NIMI Isotretinoin Orion 20 mg kapseli, pehmeä VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 20 mg isotretinoiinia. Apuaineet: puhdistettu soijaöljy,
Version 6, 14 August Etukansi. TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute
 Etukansi TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Etukansi TOIMITTAMISOHJE APTEEKEILLE Instanyl -nenäsumute TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
esimerkkipakkaus aivastux
 esimerkkipakkaus aivastux Pakkausseloste: Tietoa käyttäjälle Aivastux 10 mg tabletit setiritsiini Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle
esimerkkipakkaus aivastux Pakkausseloste: Tietoa käyttäjälle Aivastux 10 mg tabletit setiritsiini Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle
Version 6, 5 October MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus
 MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota
MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl nenäsumute, kerta annospakkaus TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL NENÄSUMUTE KERTA ANNOSPAKKAUKSESSA SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON Hyvä lääkäri Lue ja ota
Valmisteyhteenveto. 1. Lääkevalmisteen nimi. Isotretinoin ratiopharm 20 mg kapseli, pehmeä. 2. Vaikuttavat aineet ja niiden määrät
 Valmisteyhteenveto Isotretinoin ratiopharm 20 mg kapseli, pehmeä 1. Lääkevalmisteen nimi Isotretinoin ratiopharm 20 mg kapseli, pehmeä 2. Vaikuttavat aineet ja niiden määrät Isotretinoiini 20 mg Apuaineet:
Valmisteyhteenveto Isotretinoin ratiopharm 20 mg kapseli, pehmeä 1. Lääkevalmisteen nimi Isotretinoin ratiopharm 20 mg kapseli, pehmeä 2. Vaikuttavat aineet ja niiden määrät Isotretinoiini 20 mg Apuaineet:
TERVEYDENHUOLLON AMMATTILAISTEN OPAS
 TERVEYDENHUOLLON AMMATTILAISTEN OPAS Tietoa riskeistä, jotka liittyvät valproaatin (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) käyttöön naispotilaille ja raskauden aikana. Raskauden ehkäisy
TERVEYDENHUOLLON AMMATTILAISTEN OPAS Tietoa riskeistä, jotka liittyvät valproaatin (Absenor, Deprakine, Orfiril, Orfiril Long, Valproat Sandoz) käyttöön naispotilaille ja raskauden aikana. Raskauden ehkäisy
Kokemuksia sähköisestä lääkemääräyksestä
 Kokemuksia sähköisestä lääkemääräyksestä TERVE-SOS 2011 Johanna Andersson 23.5.2011 Medi-IT Oy Heikinkatu 7, 48100 Kotka Puh. 05-211 1888 Fax. 05-220 5919 www.medi-it.fi 1 Potilasohje Tiedot toimitetusta
Kokemuksia sähköisestä lääkemääräyksestä TERVE-SOS 2011 Johanna Andersson 23.5.2011 Medi-IT Oy Heikinkatu 7, 48100 Kotka Puh. 05-211 1888 Fax. 05-220 5919 www.medi-it.fi 1 Potilasohje Tiedot toimitetusta
Miten Truvadaa otetaan
 Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
Miten Truvadaa otetaan Ota Truvada-valmistetta juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma. Suositeltu annos on yksi Truvada-tabletti kerran vuorokaudessa
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Kysymyksiä ja vastauksia terveydenhuoltohenkilöstölle Voriconazole Orion (vorikonatsoli)
 Kysymyksiä ja vastauksia terveydenhuoltohenkilöstölle Voriconazole Orion (vorikonatsoli) Laadittu: Kesäkuu 2016 1. Mikä on tämän esitteen tarkoitus? Tämä esite on tarkoitettu terveydenhuoltohenkilöstölle
Kysymyksiä ja vastauksia terveydenhuoltohenkilöstölle Voriconazole Orion (vorikonatsoli) Laadittu: Kesäkuu 2016 1. Mikä on tämän esitteen tarkoitus? Tämä esite on tarkoitettu terveydenhuoltohenkilöstölle
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
Version 6, 14 August Etukansi. MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute
 Etukansi MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute Sisäsivut TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
Etukansi MÄÄRÄÄMISOHJE LÄÄKÄRILLE Instanyl -nenäsumute Sisäsivut TÄRKEÄÄ TURVALLISUUSTIETOA: INSTANYL -NENÄSUMUTE SYÖPÄÄN LIITTYVÄN LÄPILYÖNTIKIVUN HOITOON ------------------------------------------------------------------------------
SÄHKÖISEN LÄÄKEMÄÄRÄYKSEN MUUTOKSIA JA TOIMINTAMALLIN TARKENTAMINEN 01.11.2015 ALKAEN
 Ohje 8/2015 1(5) SÄHKÖISEN LÄÄKEMÄÄRÄYKSEN MUUTOKSIA JA TOIMINTAMALLIN TARKENTAMINEN 01.11.2015 ALKAEN Kohderyhmät Voimassaoloaika Julkisen sosiaali- ja terveydenhuollon palvelujen tarjoajat Yksityisen
Ohje 8/2015 1(5) SÄHKÖISEN LÄÄKEMÄÄRÄYKSEN MUUTOKSIA JA TOIMINTAMALLIN TARKENTAMINEN 01.11.2015 ALKAEN Kohderyhmät Voimassaoloaika Julkisen sosiaali- ja terveydenhuollon palvelujen tarjoajat Yksityisen
Kapselit otetaan ruokailun yhteydessä kerran tai kaksi kertaa vuorokaudessa.
 1. LÄÄKEVALMISTEEN NIMI Roaccutan 10 mg pehmeät kapselit Roaccutan 20 mg pehmeät kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen pehmeä kapseli sisältää 10 mg tai 20 mg isotretinoiinia Apuaineet,
1. LÄÄKEVALMISTEEN NIMI Roaccutan 10 mg pehmeät kapselit Roaccutan 20 mg pehmeät kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen pehmeä kapseli sisältää 10 mg tai 20 mg isotretinoiinia Apuaineet,
Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin
 Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
Liite III Muutoksia valmisteyhteenvedon merkittäviin kohtiin ja pakkausselosteisiin Huom.: Nämä muutokset valmisteyhteenvetoon, pakkausmerkintöihin ja pakkausselosteeseen saatetaan päivittää myöhemmin
Mikä on HER2-positiivinen rintasyöpä?
 Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
Tietoa potilaalle HER2-positiivisen rintasyövän KANJINTI*-hoidosta *KANJINTI on trastutsumabi-biosimilaari. Ensimmäinen trastutsumabilääke, jonka kauppanimi on Herceptin, on ollut saatavilla jo useita
VALMISTEYHTEENVETO. Kapselit otetaan ruokailun yhteydessä kerran tai kaksi kertaa vuorokaudessa.
 1. LÄÄKEVALMISTEEN NIMI Isotretinoin Actavis 10 mg, kapseli, pehmeä Isotretinoin Actavis 20 mg, kapseli, pehmeä VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi pehmeä kapseli sisältää 10
1. LÄÄKEVALMISTEEN NIMI Isotretinoin Actavis 10 mg, kapseli, pehmeä Isotretinoin Actavis 20 mg, kapseli, pehmeä VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi pehmeä kapseli sisältää 10
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
INFLECTRA SEULONTAKORTTI
 Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Suositukset maksan haittavaikutusten välttämiseksi. Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan.
 Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
Potilaan opas VALDOXAN Suositukset maksan haittavaikutusten välttämiseksi Valdoxan voi aiheuttaa haittavaikutuksena mm. muutoksia maksan toimintaan. Tässä oppaassa kerrotaan suosituksista maksan haittavaikutusten
AMGEVITA (adalimumabi)
 AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
AMGEVITA (adalimumabi) Potilaskortti - Lapset Tässä kortissa on tärkeitä turvallisuustietoja Amgevitavalmisteesta. Huom: Näytä tämä kortti aina, kun asioit lapsesi lääkärin tai muun terveydenhuoltohenkilöstön
