Paclitaxel_FI_SPC_Clean_ VALMISTEYHTEENVETO
|
|
|
- Susanna Aho
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 VALMISTEYHTEENVETO 1
2 1. LÄÄKEVALMISTEEN NIMI Paclitaxel Stragen 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia. Yksi 5 ml injektiopullo sisältää 30 mg paklitakselia. Yksi 16,7 ml injektiopullo sisältää 100 mg paklitakselia. Yksi 25 ml injektiopullo sisältää 150 mg paklitakselia. Yksi 50 ml injektiopullo sisältää 300 mg paklitakselia. Apuaineet: Vedetön etanoli: 396 mg/ml Makrogoliglyserolirisiinioleaatti: 527 mg/ml Täydellinen apuaineluettelo, ks. kohta LÄÄKEMUOTO Infuusiokonsentraatti, liuosta varten. Kirkas, väritön tai hieman kellertävä viskoosi liuos. 4. KLIINISET TIEDOT 4.1 Käyttöaiheet Munasarjasyöpä Munasarjasyöpää sairastavien potilaiden ensilinjan kemoterapiana yhdessä sisplatiinin kanssa Paclitaxin on tarkoitettu potilaille, joilla on edennyt munasarjakarsinooma tai jäännöstuumori (>1 cm) ensimmäisen laparotomian jälkeen Paclitaxel Stragen on tarkoitettu etäpesäkkeisen munasarjasyövän toisen linjan hoidoksi platinaa sisältäneen tavanomaisen hoidon epäonnistuttua. Rintasyöpä Paclitaxel Stragen on tarkoitettu imusolmukkeisiin levinneen rintasyövän liitännäishoidoksi antrasykliinisyklofosfamidihoidon jälkeen. Paclitaxel Stragen -liitännäishoito tulee katsoa antrasykliinisyklofosfamidihoidon jatkamisen vaihtoehdoksi. Paclitaxel Stragen on tarkoitettu paikallisesti levinneen tai etäpesäkkeisen rintasyövän alkuhoidoksi yhdessä jonkin antrasykliinin kanssa potilailla, joilla voidaan käyttää antrasykliinihoitoa, tai käytettäväksi yhdessä trastutsumabin kanssa potilailla,jotka yli-ilmentävät HER-2:ta (human epidermal growth factor receptor 2) tasolla 3+, määritettynä immunohistokemiallisin menetelmin ja joille antrasykliinihoito ei sovi (ks. kohdat 4.4 ja 5.1). 2
3 Paclitaxel Stragen on tarkoitettu käytettäväksi ainoana lääkkeenä etäpesäkkeisen rintasyövän hoitoon potilailla, joilla antrasykliiniä sisältävä hoito on epäonnistunut tai ei ole mahdollista tavanomaisessa muodossaan. Pitkälle edennyt ei-pienisoluinen keuhkosyöpä Paclitaxel Stragen on tarkoitettu ei-pienisoluisen keuhkosyövän hoitoon yhdistettynä sisplatiiniin potilailla, joille ei voida antaa potentiaalisesti kuratiivista leikkaus- ja/tai sädehoitoa. AIDSiin liittyvä Kaposin sarkooma Paclitaxel Stragen on tarkoitettu pitkälle edennyttä AIDSiin liittyvää Kaposin sarkoomaa sairastavien potilaiden hoitoon, jos aiempi liposomaalinen antrasykliinihoito on epäonnistunut. Tätä käyttöaihettakoskevia tutkimuksia lääkkeen tehosta on rajallisesti. Tiivistelmä relevanteista tutkimustuloksista, ks. kohta Annostus ja antotapa Kaikille potilaille on annettava ennen Paclitaxel Stragenia esilääkitys, johon kuuluu kortikosteroideja, antihistamiineja ja H 2 -antagonisteja, esimerkiksi seuraavasti: Lääke Annos Anto ennen Paclitaxel Stragenia deksametasoni 20 mg suun kautta* tai laskimoon difenhydramiini** 50 mg laskimoon min simetidiini tai ranitidiini 300 mg laskimoon 50 mg laskimoon * 8 20 mg, jos käyttöaiheena on Kaposin sarkooma ** tai vastaava antihistamiini, esim. kloorifeniramiini Suun kautta annettaessa noin 6 ja 12 h aiemmin, laskimoon annettaessa min aiemmin min Paclitaxel Stragen annetaan laskimoon käyttäen infuusiosuodatinta, jonka kalvon mikrohuokoskoko on 0.22 μm (ks. kohta 6.6). Munasarjasyövänensilinjan lääkitys Muitakin hoitoja tutkitaan parhaillaan, mutta suositeltava yhdistelmähoito on paklitakselin ja sisplatiinin yhdistelmä. Suositeltava annos on infuusion kestosta riippuen jompikumpi seuraavista: joko 175 mg/m 2 paklitakselia laskimoon 3 tunnin aikana ja sen jälkeen 75 mg/m 2 sisplatiinia kolmen viikon välein toistettuna hoitojaksona tai vaihtoehtoisesti 135 mg/m 2 paklitakselia 24 tuntia kestävänä infuusiona ja sen jälkeen 75 mg/m 2 sisplatiinia kolmen viikon välein toistettuna hoitojaksona (ks. kohta 5.1). Munasarjasyöväntoisen linjan lääkitys Suositeltava paklitakseliannos on 175 mg/m 2 annettuna 3 tunnin aikana 3 viikon välein. Rintasyövän liitännäishoito Suositeltava paklitakseliannos on 175 mg/m 2 annettuna 3 tunnin aikana 3 viikon välein yhteensä 4 kertaa antrasykliini-syklofosfamidihoidon jälkeen. Rintasyövän ensilinjan lääkitys 3
4 Jos paklitakselia käytetään yhdessä doksorubisiinin (50 mg/m 2 ) kanssa, paklitakseli annetaan 24 tuntia doksorubisiinin jälkeen. Suositeltava paklitakseliannos on 220 mg/m 2 annettuna 3 tunnin aikana laskimoon 3 viikon välein (ks. kohdat 4.5 ja 5.1). Jos paklitakselia käytetään yhdessä trastutsumabin kanssa, suositeltava paklitakseliannos on 175 mg/m 2 annettuna 3 tunnin aikana laskimoon 3 viikon välein (ks. kohta 5.1). Paklitakseli-infuusio voidaan aloittaa ensimmäisen trastutsumabiannoksen jälkeisenä päivänä tai välittömästi myöhempien trastutsumabiannosten jälkeen, jos aiempi trastutsumabiannos oli hyvin siedetty (trastutsumabin yksityiskohtaiset annostustiedot, ks. trastutsumabin valmisteyhteenveto). Rintasyöväntoisen linjan lääkitys Suositeltava paklitakseliannos on 175 mg/m 2 annettuna 3 tunnin aikana 3 viikon välein. Pitkälle edenneen ei-pienisoluisen keuhkosyövän hoito Suositeltava paklitakseliannos on 175 mg/m 2 annettuna 3 tunnin aikana ja sen jälkeen 80 mg/m 2 sisplatiinia 3 viikon välein toistettuna hoitojaksona. AIDSiin liittyvän Kaposin sarkooman hoito Suositeltava paklitakseliannos on 100 mg/m 2 annettuna 3 tuntia kestävänä laskimoinfuusiona 2 viikon välein. Myöhemmät paklitakseliannokset annetaan potilaan yksilöllisen sietokyvyn mukaisesti. Paklitakselia ei tule antaa uudelleen ennen kuin potilaan neutrofiiliarvot ovat 1,5 x 10 9 /l ( 1 x 10 9 /l Kaposin sarkooman hoidossa) ja trombosyyttiarvot 100 x 10 9 /l ( 75 x 10 9 /l Kaposin sarkooman hoidossa). Jos potilaalle kehittyy vaikea neutropenia (neutrofiiliarvot < 0,5 x 10 9 /l 7 päivän ajan) tai vaikea perifeerinen neuropatia, myöhempiä annoksia tulee pienentää 20 % (Kaposin sarkoomaa hoidettaessa 25 %) (ks. kohta 4.4). Maksan vajaatoimintapotilaat Riittämättömien tietojen vuoksi ei voida antaa suosituksia annostuksen muuttamisesta potilailla, joilla on lievä tai keskivaikea maksan vajaatoiminta (ks. kohdat 4.4 ja 5.2). Vaikeaa maksan vajaatoimintaa sairastaville potilaille ei pidä antaa paklitakselihoitoa. Antotapa: Infuusiokonsentraatti liuosta varten tulee laimentaa ennen käyttöä (ks. kohta 6.6) ja antaa vain laskimoon. 4.3 Vasta-aiheet Paclitaxel Stragen on vasta-aiheinen potilailla, joilla on vaikea yliherkkyys paklitakselille tai apuaineille, etenkin makrogoliglyserolirisiinioleaatille (ks. kohta 4.4). Paclitaxel Stragen on vasta-aiheinen raskauden ja imetyksen aikana (ks. kohta 4.6), eikä sitä tule antaa potilaille, joiden lähtötilanteen neutrofiiliarvo on < 1,5 x 10 9 /l (< 1 x 10 9 /l Kaposin sarkoomaa hoidettaessa). Kaposin sarkoomaa hoidettaessa Paclitaxel Stragen on vasta-aiheinen myös potilailla, joilla on samanaikaisia vakavia kontrolloimattomia infektioita. 4.4 Varoitukset ja käyttöön liittyvät varotoimet Paclitaxel Stragenia saa antaa vain syövän lääkehoitoon perehtyneen lääkärin valvonnassa. Huomattavia yliherkkyysreaktioita voi esiintyä, joten asianmukaisten tukihoitovälineiden on oltava saatavilla. 4
5 Potilaille on annettava kortikosteroideja, antihistamiineja ja H 2 -antagonisteja sisältävä esilääkitys (ks. kohta 4.2). Jos Paclitaxel Stragenia käytetään yhdessä sisplatiinin kanssa, se tulee antaa ennen sisplatiinia (ks. kohta 4.5). Alle 1 %:lla paklitakselihoitoa saaneista potilaista, joille on annettu asianmukainen esilääkitys, on esiintynyt huomattavia yliherkkyysreaktioita, joihin on liittynyt hoitoa vaativaa hengenahdistusta ja verenpaineen laskua, angioedeemaa ja yleistynyttä nokkosihottumaa. Reaktiot ovat todennäköisesti histamiinivälitteisiä. Jos potilaalle kehittyy vaikea yliherkkyysreaktio, paklitakseli-infuusio on lopetettava välittömästi ja oireenmukainen hoito on aloitettava. Tämän jälkeen potilasta ei saa enää altistaa paklitakselille. Luuydinsuppressio (lähinnä neutropenia) on annosta rajoittava haittavaikutus. Potilaan veriarvoja on alettava seurata säännöllisesti. Paklitakselia ei tule antaa uudelleen ennen kuin potilaan neutrofiiliarvot ovat korjautuneet tasolle 1,5 x 10 9 /l ( 1 x 10 9 /l Kaposin sarkooman hoidossa) ja trombosyyttiarvot tasolle 100 x 10 9 /l ( 75 x 10 9 /l Kaposin sarkooman hoidossa). Kaposin sarkoomaa koskevassa kliinisessä tutkimuksessa valtaosa potilaista sai granulosyyttikasvutekijää (G-CSF). Vaikeita sydämen johtumishäiriöitä on ilmoitettu harvoin, kun paklitakselia on käytetty ainoana lääkkeenä. Jos potilaalle kehittyy paklitakselia annettaessa huomattava johtumishäiriö, hänelle on annettava asianmukaista hoitoa, ja sydäntoimintaa on seurattava jatkuvasti myöhempien Paclitaxel Stragen -hoitojen yhteydessä. Paklitakselia annettaessa on havaittu hypotensiota, hypertensiota ja bradykardiaa. Potilaat ovat yleensä oireettomia eivätkä yleensä tarvitse hoitoa. Usein toistuvaa elintoimintojen seurantaa suositellaan etenkin Paclitaxel Stragen -infuusion ensimmäisen tunnin aikana. Vaikeita sydän- ja verisuonistotapahtumia havaittiin useammin ei-pienisoluista keuhkosyöpää kuin rinta- tai munasarjasyöpää sairastavilla potilailla. AIDSiin liittyvää Kaposin sarkoomaa koskeneessa kliinisessä tutkimuksessa havaittiin yksi paklitakseliin liittynyt sydämen vajaatoimintatapaus. Kun paklitakselia käytetään yhdessä doksorubisiinin tai trastutsumabin kanssa etäpesäkkeisen rintasyövän alkuvaiheen hoitona, on kiinnitettävä huomiota potilaan sydäntoiminnan seurantaan. Jos potilaalle harkitaan paklitakselihoitoa näiden lääkeyhdistelmien puitteissa, hänelle on tehtävä lähtötilanteessa sydäntoiminnan arvio, johon kuuluu anamneesi, lääkärintarkastus, EKG, kaikukardiografia ja/tai Multiple Gated Acquisition (MUGA)-tutkimus. Sydäntoimintaa tulee seurata edelleen hoidon aikana (esim. 3 kk välein). Seurannan avulla voidaan tunnistaa potilaat, joille saattaa kehittyä sydämen toimintahäiriö. Heitä hoitavien lääkärien on arvioitava huolellisesti potilaan saama kumulatiivinen antrasykliiniannos (mg/m 2 ) ja päätettävä sen perusteella, miten usein potilaan kammiotoimintaa tulee arvioida. Jos tutkimuksissa havaitaan sydäntoiminnan (edes oireetonta) huononemista, hoitavien lääkärien tulee arvioida huolellisesti hoidon jatkamisen kliiniset edut suhteessa mahdollisesti peruuttamattomien sydänlihasvaurioiden vaaraan. Jos potilas saa lisää hoitoa, sydäntoimintaa on seurattava entistä useammin (esim. 1 2 hoitojakson välein). Lisätietoa, ks. trastutsumabin tai doksorubisiinin valmisteyhteenveto. Perifeeristä neuropatiaa esiintyy usein, mutta vaikeat oireet ovat harvinaisia. Vaikeissa tapauksissa on suositeltavaa pienentää kaikkia myöhempiä Paclitaxel Stragen -annoksia 20 % (Kaposin sarkoomaa hoidettaessa 25 %). Ei-pienisoluista keuhkosyöpää sairastavilla potilailla ja potilailla, jotka saivat paklitakselia munasarjasyövän ensilinjan hoitona, todettiin, että vaikeaa neurotoksisuutta esiintyi useammin silloin, kun potilaille annettiin 3 tuntia kestävä paklitakseli-infuusio ja sisplatiinia, kuin käytettäessä joko paklitakselimonoterapiaa tai syklofosfamidia, jonka jälkeen annettiin sisplatiinia. Maksan vajaatoimintapotilailla voi olla tavallista suurempi toksisuusriski, etenkin asteen III/IV luuydinsuppression riski. Paklitakselin toksisuuden ei ole osoitettu olevan tavallista voimakkaampaa, kun lääke 5
6 annetaan 3 tuntia kestävänä infuusiona potilaille, joilla on lieviä maksatoiminnan poikkeavuuksia. Kun paklitakseli annetaan pidempänä infuusiona, keskivaikeaa tai vaikeaa maksan vajaatoimintaa sairastavilla potilailla saattaa esiintyä tavallista enemmän luuydinsuppressiota. Potilaita tulee seurata tarkoin voimakkaan luuydinsuppression varalta (ks. kohta 4.2). Riittämättömien tietojen vuoksi ei voida antaa suosituksia annostuksen muuttamisesta potilailla, joilla on lievä tai keskivaikea maksan vajaatoiminta (ks. kohdat 5.2). Valmisteen käytöstä potilailla, joilla on lähtötilanteessa vaikea kolestaasi, ei ole tietoja. Vaikeaa maksan vajaatoimintaa sairastaville potilaille ei pidä antaa paklitakselihoitoa. Paclitaxel Stragen sisältää etanolia (396 mg/ml), joten sen mahdolliset vaikutukset keskushermostoon ja muut vaikutukset on otettava huomioon. Paclitaxel Stragen sisältää myös makrogoliglyserolirisiinioleaattia, joka voi aiheuttaa vaikeita allergiareaktioita. Paklitakselin antamista valtimoon on vältettävä erityisen tarkoin, sillä paikallista toleranssia koskeneissa eläinkokeissa havaittiin vaikeita kudosreaktioita, kun lääkettä annettiin valtimoon. Pseudomembranoottista koliittia on ilmoitettu harvoin, myös potilailla, jotka eivät ole saaneet samanaikaisesti antibioottihoitoa. Tämän reaktion mahdollisuus on otettava huomioon erotusdiagnoosissa, jos potilaalle kehittyy vaikea tai pitkäaikainen ripuli paklitakselihoidon aikana tai pian sen jälkeen. Paklitakselin ja sädehoidon yhdistelmä (hoitojen järjestyksestä riippumatta) voi vaikuttaa interstitiaalisen keuhkosairauden kehittymiseen. Paklitakselin on todettu olevan teratogeeninen, alkiotoksinen ja mutageeninen monissa eri koejärjestelmissä. Tästä syystä hedelmällisessä iässä olevien nais- ja miespotilaiden ja/tai heidän kumppaniensa tulee käyttää ehkäisyä vähintään 6 kk ajan paklitakselihoidon jälkeen. Kaposin sarkoomapotilailla esiintyy harvoin vaikeaa mukosiittia. Jos vaikeita reaktioita kehittyy, paklitakseliannosta tulee pienentää 25 %. 4.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset Simetidiiniesilääkitys ei vaikuta paklitakselin puhdistumaan. Kun Paclitaxel Stragenia käytetään munasarjasyövän ensilinjan hoitona, on suositeltavaa antaa Paclitaxel Stragen ennen sisplatiinia. Jos paklitakseli annetaan ennen sisplatiinia, sen turvallisuusprofiili on samankaltainen kuin paklitakselimonoterapiaa käytettäessä. Kun paklitakseli annettiin sisplatiinin jälkeen, potilailla esiintyi voimakkaampaa luuydinsuppressiota, ja paklitakselin puhdistuma pieneni noin 20 %. Gynekologisia syöpiä sairastavilla potilailla, jotka saavat paklitakseli- ja sisplatiinihoitoa, voi olla suurempi munuaisten vajaatoiminnan riski kuin potilailla, jotka saavat pelkkää sisplatiinia. Doksorubisiinin ja sen aktiivisten metaboliittien eliminaatio voi heikentyä, jos paklitakselin ja doksorubisiinin annostelun välinen aika lyhenee. Tästä syystä Paclitaxel Stragen tulee antaa 24 tuntia doksorubisiinin jälkeen etäpesäkkeisen rintasyövän alkuvaiheen hoidossa (ks. kohta 5.2). Paklitakselin metabolia tapahtuu osittain CYP2C8- ja CYP3A4-välitteisesti (ks. kohta 5.2). Kliiniset tutkimukset ovat osoittaneet, että paklitakselin CYP2C8-välitteinen metaboloituminen 6αhydroksipaklitakseliksi on lääkkeen tärkein metaboliareitti ihmisellä. Ketokonatsolin (jonka tiedetään olevan voimakas CYP3A4-estäjä) samanaikainen anto ei estä paklitakselin eliminaatiota potilailla, joten lääkeaineet 6
7 voidaan antaa samanaikaisesti ilman annosmuutoksia. Paklitakselin mahdollisista yhteisvaikutuksista muiden CYP3A4:n substraattien/estäjien kanssa on vain rajallisesti muuta tietoa. Tästä syystä on noudatettava varovaisuutta, kun paklitakselia annetaan samanaikaisesti sellaisten lääkkeiden kanssa, joiden tiedetään estävän (esim. erytromysiini, fluoksetiini, gemfibrotsiili) tai indusoivan (esim. rifampisiini, karbamatsepiini, fenytoiini, efavirentsi, nevirapiini) joko CYP2C8:n tai CYP3A4:n toimintaa. Kaposin sarkoomaa sairastaneilla potilailla, jotka käyttivät samanaikaisesti useita muita lääkkeitä, saadut tutkimustulokset viittaavat siihen, että paklitakselin systeeminen puhdistuma pieneni merkitsevästi nelfinaviirin ja ritonaviirin käytön yhteydessä, mutta ei indinaviirin käytön yhteydessä. Yhteisvaikutuksista muiden proteaasinestäjien kanssa on vain rajallisesti tietoa. Tästä syystä paklitakselin käytössä on noudatettava varovaisuutta, jos potilas käyttää samanaikaisesti myös proteaasinestäjiä. 4.6 Raskaus ja imetys Käyttö raskauden aikana Paklitakselin on osoitettu olevan alkio- ja sikiötoksinen kanilla ja heikentävän hedelmällisyyttä rotalla. Paklitakselin käytöstä raskauden aikana ei ole tietoa. Kuten muutkin sytotoksiset lääkevalmisteet, Paclitaxel Stragen voi vahingoittaa sikiötä ja on siksi vasta-aiheinen raskausaikana. Naisia tulee kehottaa välttämään raskaaksi tulemista Paclitaxel Stragen -hoidon aikana ja kertomaan välittömästi hoitavalle lääkärille, jos he tulevat raskaaksi. Käyttö imetyksen aikana Ei tiedetä, erittyykö paklitakseli maitoon ihmisellä. Paclitaxel Stragen on vasta-aiheinen imetyksen aikana. Imetys tulee lopettaa hoidon ajaksi. 4.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn Paklitakselilla ei ole haitallista vaikutusta ajokykyyn ja koneiden käyttökykyyn. Tulee kuitenkin huomata, että valmiste sisältää alkoholia (ks. kohdat 4.4 ja 6.1). 4.8 Haittavaikutukset Ellei toisin ole mainittu, seuraavassa tekstissä viitataan koko turvallisuustietokantaan. Siihen kuului 812 potilasta, joilla oli kiinteitä kasvaimia ja jotka saivat paklitakselihoitoa monoterapiana kliinisissä tutkimuksissa. Kaposin sarkooman potilaspopulaatio on hyvin spesifinen, joten näitä potilaita koskevat, 107 potilasta kattaneesta kliinisestä tutkimuksesta saadut tiedot esitetään erillisessä kappaleessa tämän luvun lopussa. Ellei muuta ole mainittu, haittavaikutusten esiintymistiheys ja vaikeusaste olivat yleisesti ottaen samanlaisia potilailla, jotka saavat paklitakselia munasarjasyövän, rintasyövän tai ei-pienisoluisen keuhkosyövän hoitoon. Ikä ei vaikuttanut selkeästi mihinkään mainituista haittavaikutuksista. Luuydinsuppressio oli yleisin merkitsevä haittavaikutus. Vaikeaa neutropeniaa (< 0,5 x 10 9 /l) esiintyi 28 %:lla potilaista, mutta siihen ei liittynyt kuumejaksoja. Vain 1 %:lla potilaista oli vaikeaa neutropenia 7 vrk ajan. Trombosytopeniaa ilmoitettiin 11 %:lla potilaista. Kolmella prosentilla potilaista trombosyyttiarvot laskivat tasolle < 50 x 10 9 /l ainakin kerran tutkimuksen aikana. Anemiaa havaittiin 64 %:lla potilaista, mutta se oli vaikeaa (Hb < 5 mmol/l) vain 6 %:lla potilaista. Anemian ilmaantuvuus ja vaikeusaste ovat yhteydessä potilaan hemoglobiiniarvoihin lähtötilanteessa. Neurotoksisuutta, lähinnä perifeeristä neuropatiaa, esiintyi nähtävästi useammin ja se oli vaikeampaa käytettäessä 175 mg/m 2 infuusiota annettuna 3 tunnin aikana (neurotoksisuutta 85 %:lla, vaikeaa 15 %:lla) 7
8 kuin käytettäessä 135 mg/m 2 infuusiota annettuna 24 tunnin aikana (perifeeristä neuropatiaa 25 %:lla, vaikeaa 3 %:lla), kun paklitakselia käytettiin yhdessä sisplatiinin kanssa. Vaikean neurotoksisuuden ilmaantuvuus näyttää suurenevan, jos ei-pienisoluista keuhkosyöpää tai munasarjasyöpää sairastava potilas saa paklitakselia 3 tuntia kestävänä infuusiona ja sen jälkeen sisplatiinia. Perifeeristä neuropatiaa voi esiintyä ensimmäisen hoidon jälkeen, ja se voi pahentua paklitakselialtistuksen suurentuessa. Perifeerinen neuropatia johti muutamassa tapauksessa paklitakselihoidon lopettamiseen. Sensoriset oireet lievittyivät tai hävisivät yleensä useiden kuukausien kuluessa paklitakselihoidon lopettamisesta. Aiempien hoitojen aiheuttamat, edelleen jatkuvat neuropatiat eivät ole paklitakselihoidon vasta-aihe. Nivelkipua tai lihaskipua esiintyi 60 %:lla potilaista, ja se oli vaikeaa 13 %:lla potilaista. Kahdelle potilaalle (< 1 %:lle potilaista) kehittyi merkittävä ja mahdollisesti kuolemaan johtava yliherkkyysreaktio (määritelmä: hoitoa vaativa hypotensio, angioedeema, keuhkoputkia avaavaa lääkitystä vaativa hengenahdistus tai yleistynyt nokkosihottuma). 34 %:lla potilaista (17 %:ssa kaikista hoitojaksoista) esiintyi vähäisiä yliherkkyysreaktioita. Nämä vähäiset reaktiot, lähinnä punastuminen ja ihottuma, eivät vaatineet hoitoa eivätkä estäneet paklitakselihoidon jatkamista. Laskimoon annon yhteydessä kehittyvät pistoskohdan reaktiot voivat aiheuttaa paikallista turvotusta, kipua, punoitusta ja kovettumista. Ekstravasaatio voi joskus aiheuttaa selluliittia. Ihon kuoriutumista ja/tai kesimistä on ilmoitettu, joskus ekstravasaation yhteydessä. Myös ihon värimuutokset ovat mahdollisia. Harvinaisissa tapauksissa on ilmoitettu aiemman ekstravasaation yhteydessä havaittujen ihoreaktioiden uusiutumista, kun paklitakselia on annettu toiseen kohtaan (ns. recall-ilmiö). Ekstravasaation aiheuttamiin reaktioihin ei tunneta mitään erityistä hoitoa. Seuraavassa taulukossa luetellaan pelkän paklitakselin antoon liittyneet haittavaikutukset niiden vaikeusasteesta riippumatta, kun lääke annettiin 3 tuntia kestäneenä infuusiona potilaille, joilla oli etäpesäkkeisiä syöpiä (812 kliinisissä tutkimuksissa hoidettua potilasta) sekä valmisteen markkinoille tulon jälkeen saatujen tietojen perusteella (merkitty *). Alla lueteltujen haittavaikutusten esiintymistiheys on määritelty seuraavan luokittelun mukaisesti: hyvin yleiset ( 1/10), yleiset ( 1/100, < 1/10), melko harvinaiset ( 1/1 000, < 1/100), harvinaiset ( 1/10 000, < 1/1 000), hyvin harvinaiset (< 1/10 000). Infektiot: Veri ja imukudos: Immuunijärjestelmä: Aineenvaihdunta ja ravitsemus: Psyykkiset häiriöt: Hyvin yleiset: infektiot (lähinnä virtsatie- tai ylähengitystieinfektiot), joiden on joissakin tapauksissa ilmoitettu johtaneen kuolemaan Melko harvinaiset: septinen sokki Harvinaiset*: keuhkokuume, peritoniitti, sepsis Hyvin yleiset: luuydinsuppressio, neutropenia, anemia, trombosytopenia, leukopenia, verenvuoto Harvinaiset*: kuumeinen neutropenia Hyvin harvinaiset*: akuutti myelooinen leukemia, myelodysplastinen oireyhtymä Hyvin yleiset: vähäiset yliherkkyysreaktiot (lähinnä punastuminen ja ihottuma) Melko harvinaiset: merkittävät, hoitoa vaativat yliherkkyysreaktiot (esim. hypotensio, angioedeema, hengitysvaikeudet, yleistynyt nokkosihottuma, vilunväreet, selkäkipu, rintakipu, takykardia, vatsakipu, raajakipu, voimakas hikoilu ja hypertensio) Harvinaiset*: anafylaktiset reaktiot Hyvin harvinaiset*: anafylaktinen sokki Hyvin harvinaiset*: ruokahaluttomuus Hyvin harvinaiset*: sekavuustilat 8
9 Hermosto: Silmät: Kuulo ja tasapainoelin: Sydän: Verisuonisto: Hengityselimet, rintakehä ja välikarsina: Ruoansulatuselimistö: Maksa ja sappi: Iho ja ihonalainen kudos: Luusto, lihakset ja sidekudos: Yleisoireet ja antopaikassa todettavat haitat: Tutkimukset: Hyvin yleiset: neurotoksisuus (lähinnä perifeerinen neuropatia) Harvinaiset*: motorinen neuropatia (ja sen aiheuttama vähäinen distaaliosien heikkous) Hyvin harvinaiset*: autonominen neuropatia (joka johtaa paralyyttiseen ileukseen ja ortostaattiseen hypotensioon), grand mal -kohtaukset, kouristukset, enkefalopatia, huimaus, päänsärky, ataksia Hyvin harvinaiset*: näköhermon ja/tai näön häiriöt (välähdykset, näkökenttäpuutokset), etenkin potilailla, jotka ovat saaneet suositusannokset ylittäviä annoksia Hyvin harvinaiset*: ototoksisuus, kuulon menetys, tinnitus, kiertohuimaus Yleiset: bradykardia Melko harvinaiset: kardiomyopatia, oireeton ventrikulaarinen takykardia, takykardia, johon liittyy bigeminiaa, AV-katkos ja pyörtyminen, sydäninfarkti Hyvin harvinaiset*: eteisvärinä, supraventrikulaarinen takykardia Hyvin yleiset: hypotensio Melko harvinaiset: hypertensio, tromboosi, tromboflebiitti Hyvin harvinaiset*: sokki Harvinaiset*: hengenahdistus, pleuraeffuusio, interstitiaalinen keuhkosairaus, keuhkofibroosi, keuhkoembolia, hengitysvajaus Hyvin harvinaiset*: yskä Hyvin yleiset: pahoinvointi, oksentelu, ripuli, limakalvotulehdus Harvinaiset*: suolitukkeuma, suolen perforaatio, iskeeminen koliitti, haimatulehdus Hyvin harvinaiset*: suoliliepeen tromboosi, pseudomembranoottinen koliitti, ruokatorvitulehdus, ummetus, askites, neutropeninen koliitti Hyvin harvinaiset*: maksanekroosi, hepaattinen enkefalopatia (molempien on ilmoitettu johtaneen joissakin tapauksissa kuolemaan) Hyvin yleiset: hiustenlähtö Yleiset: ohimenevät, lievät kynsien ja ihon muutokset Harvinaiset*: kutina, ihottuma, punoitus Hyvin harvinaiset*: Stevens-Johnsonin oireyhtymä, epidermaalinen nekrolyysi, erythema multiforme, eksfoliatiivinen dermatiitti, nokkosihottuma, kynsien irtoaminen (hoitoa saavien potilaiden tulee suojata kätensä ja jalkansa auringolta) Hyvin yleiset: Nivelkipu, lihaskipu Yleiset: pistoskohdan reaktiot (kuten paikallinen turvotus, kipu, punoitus, kovettuminen; ekstravasaatio voi joskus aiheuttaa selluliittia, ihon fibroosia ja ihonekroosia) Harvinaiset*: voimattomuus, kuume, nestehukka, turvotus, huonovointisuus Yleiset: ASAT-arvojen ja alkalisen fosfataasin arvojen voimakas kohoaminen Melko harvinaiset: bilirubiiniarvojen voimakas kohoaminen Harvinaiset*: veren kreatiniinipitoisuuden suureneminen Antrasykliini-syklofosfamidihoitoa saaneilla rintasyöpäpotilailla, jotka saivat paklitakselia liitännäishoitona, esiintyi enemmän neurosensorista toksisuutta, yliherkkyysreaktioita, nivelkipua/lihaskipua, anemiaa, 9
10 infektioita, kuumetta, pahoinvointia/oksentelua ja ripulia kuin potilailla, jotka saivat vain antrasykliinisyklofosfamidihoitoa. Näiden tapahtumien esiintymistiheys oli kuitenkin samankaltainen kuin pelkkää paklitakselia käytettäessä, kuten edellä kerrottiin. Yhdistelmähoito Seuraavassa viitataan kahteen munasarjasyövän ensilinjan lääkitystä koskeneeseen suureen tutkimukseen (paklitakseli + sisplatiini: yli potilasta), kahteen etäpesäkkeisen rintasyövän ensilinjan hoitoa koskeneeseen faasin III tutkimukseen, joista toisessa käytettiin paklitakselin ja doksorubisiinin yhdistelmää (paklitaseli + doksorubisiini: 267 potilasta) ja toisessa paklitakselin ja trastutsumabin yhdistelmää (suunniteltu alaryhmäanalyysi: paklitakseli + trastutsumabi: 188 potilasta) sekä kahteen pitkälle edenneen eipienisoluisen keuhkosyövän hoitoa koskeneeseen faasin III tutkimukseen (paklitakseli + sisplatiini: yli 360 potilasta) (ks. kohta 5.1). Kun munasarjasyövän ensilinjan hoitoa saavat potilaat saivat paklitakselia 3 tuntia kestävänä infuusiona, neurotoksisuutta, nivelkipua/lihaskipua ja yliherkkyysreaktioita ilmoitettiin useammin ja ne olivat vaikeampia siinä tapauksessa, että potilaat saivat ensin paklitakselia ja sen jälkeen sisplatiinia kuin siinä tapauksessa, että potilaat saivat ensin syklofosfamidia ja sen jälkeen sisplatiinia. Luuydinsuppressiota esiintyi nähtävästi harvemmin ja se oli lievempää potilailla, jotka saivat paklitakselia 3 tuntia kestäneenä infuusiona ja sen jälkeen sisplatiinia, kuin potilailla, jotka saivat syklofosfamidia ja sen jälkeen sisplatiinia. Potilailla, jotka saivat ensilinjan lääkitystä etäpesäkkeiseen rintasyöpään, ilmoitettiin useammin ja vaikeampaa neutropeniaa, anemiaa, perifeeristä neuropatiaa, nivel-/lihaskipua, voimattomuutta, kuumetta ja ripulia, kun hoitona oli 220 mg/m 2 paklitakselia 3 tunnin infuusiona 24 tuntia doksorubisiinin jälkeen (50 mg/m 2 ), kuin siinä tapauksessa, että he saivat tavanomaista FAC-hoitoa (5-fluorourasiili, 500 mg/m 2, doksorubisiini, 50 mg/m 2 ja syklofosfamidi, 500 mg/m 2 ). Pahoinvointia ja oksentelua esiintyi nähtävästi harvemmin ja lievempänä potilailla, jotka saivat paklitakselia sisältänyttä hoitoa (220 mg/m 2 paklitakselia / 50 mg/m 2 doksorubisiinia), kuin tavanomaisen FAC-hoidon yhteydessä. Paklitakseli-/doksorubisiiniryhmässä saattoi esiintyä vähemmän ja lievempää oksentelua ja pahoinvointia myös ryhmän saaman kortikosteroidihoidon vuoksi. Kun paklitakselia käytettiin 3 tuntia kestävänä infuusiona yhdessä trastutsumabin kanssa etäpesäkkeisen rintasyövän ensilinjan hoitona, seuraavia tapahtumia ilmoitettiin useammin kuin pelkkää paklitakselia käytettäessä (riippumatta siitä, johtuivatko nämä tapahtumat paklitakselista tai trastutsumabista): sydämen vajaatoiminta (8 % paklitakseli-trastutsumabiryhmässä ja 1 % paklitakseliryhmässä), infektiot (46 % ja 27 %), vilunväreet (42 % ja 4 %), kuume (47 % ja 23 %), yskä (42 % ja 22 %), ihottuma (39 % ja 18 %), nivelkipu (37 % ja 21 %), takykardia (12 % ja 4 %), ripuli (45 % ja 30 %), hypertensio (11 % ja 3 %), nenäverenvuoto (18 % ja 4 %), akne (11 % ja 3 %), herpes simplex (12 % ja 3 %), tapaturmat (13 % ja 3 %), unettomuus (25 % ja 13 %), nuha (22 % ja 5 %), sinuiitti (21 % ja 7 %) ja pistoskohdan reaktiot (7 % ja 1 %). Jotkin esiintymistiheyksien eroista voivat johtua siitä, että paklitakseli/trastutsumabihoito kesti pidempään ja siihen kuului enemmän hoitokertoja kuin pelkkään paklitakselihoitoon. Vaikeita tapahtumia esiintyi yhtä usein paklitakseli/trastutsumabihoitoa ja pelkkää paklitakselihoitoa käytettäessä. Kun doksorubisiinia annettiin yhdessä paklitakselin kanssa potilaille, joilla oli etäpesäkkeinen rintasyöpä, sydämen supistumispoikkeavuuksia ( 20 % alenema vasemman kammion ejektiofraktiossa) havaittiin 15 %:lla potilaista, kun taas tavanomaista FAC-hoitoa käytettäessä niitä esiintyi 10 %:lla. Kongestiivista sydämen vajaatoimintaa todettiin < 1 %:lla sekä paklitakseli/doksorubisiiniryhmän että tavanomaista FAChoitoa saaneen ryhmän potilaista. Kun trastutsumabin ja paklitakselin yhdistelmää annettiin aiempaa antrasykliinihoitoa saaneille potilaille, sydämen toimintahäiriöitä esiintyi useammin ja ne olivat vaikeampia kuin potilailla, jotka saivat paklitakselimonoterapiaa (NYHA-luokat I/II, 10 % paklitakselitrastutsumabiryhmässä ja 0 % paklitakseliryhmässä; NYHA-luokat III/IV, 2 % ja 1 %). Ilmiöön on harvinaisissa tapauksissa liittynyt kuolemantapauksia (ks. trastutsumabin valmisteyhteenveto). Kaikissa 10
11 tapauksissa näitä harvinaisia tapauksia lukuun ottamatta potilaiden tila reagoi asianmukaiseen lääketieteelliseen hoitoon. Säteilyn aiheuttamaa pneumoniittia on ilmoitettu potilailla, jotka ovat saaneet samanaikaisesti sädehoitoa. AIDSiin liittyvä Kaposin sarkooma Hematologisia ja maksaan kohdistuvia haittavaikutuksia lukuun ottamatta (ks. alla) haittavaikutusten esiintymistiheys ja vaikeusaste ovat yleisesti ottaen olleet samanlaisia Kaposin sarkoomaa sairastavilla potilailla ja potilailla, jotka saivat paklitakselimonoterapiaa muiden kiinteiden kasvainten hoitoon. Tiedot perustuvat 107 potilaalla tehtyyn kliiniseen tutkimukseen. Veri ja imukudos: luuydinsuppressio on tärkein annosta rajoittava haittavaikutus. Hematologisen toksisuuden tärkein muoto on neutropenia. Ensimmäisen hoitojakson aikana vaikeaa neutropeniaa (< 0,5 x 10 9 /l) esiintyi 20 %:lla potilaista. Koko hoitoaikana vaikeaa neutropeniaa esiintyi 39%:lla potilaista. Neutropenia kesti yli 7 päivän ajan 41 %:lla potilaista ja vrk ajan 8 %:lla potilaista. Se lievittyi kaikilla seuratuilla potilailla 35 päivän kuluessa. Asteen 4 neutropeniaa, joka kesti 7 päivää, esiintyi 22 %:lla potilaista. Paklitakseliin liittyvää neutropenista kuumetta ilmoitettiin 14 %:lla potilaista, ja sitä esiintyi 1,3 %:ssa hoitojaksoista. Paklitakselin aikana esiintyi 3 lääkevalmisteeseen liittyvää sepsistapausta (2,8 %), jotka johtivat kuolemaan. Trombosytopeniaa esiintyi 50 %:lla potilaista, ja se oli vaikeaa (< 50 solua x 10 9 /l) 9 %:lla. Vain 14 prosentilla esiintyi trombosyyttiarvojen laskua tasolle < 75 solua x 10 9 /l ainakin kerran hoidon aikana. Paklitakseliin liittyvää verenvuotoa ilmoitettiin < 3 %:lla potilaista, mutta verenvuotoepisodit olivat paikallisia. Anemiaa (Hb < 11 g/dl) havaittiin 61 %:lla potilaista, ja se oli vaikeaa (Hb < 8 g/dl) 10 %:lla. 21 % potilaista tarvitsi punasolusiirtoja. Maksa ja sappi: Bilirubiiniarvojen kohoamista esiintyi 28 %:lla, alkalisen fosfataasin arvojen kohoamista 43 %:lla ja ASAT-arvojen kohoamista 44 %:lla potilaista, joiden maksatoiminta oli lähtötilanteessa normaali (> 50 % käytti proteaasinestäjiä). Kunkin arvon kohoaminen oli vaikeaa 1 %:ssa tapauksista. 4.9 Yliannostus Paklitakselin yliannostukselle ei tunneta vastalääkettä. Yliannostuksen tärkeimmät komplikaatiot olisivat oletettavasti luuydinsuppressio, perifeerinen neurotoksisuus ja mukosiitti. 5. FARMAKOLOGISET OMINAISUUDET 5.1 Farmakodynamiikka Farmakoterapeuttinen ryhmä: Taksaanit ATC-koodi: L01CD01 Paklitakseli on mikrotubuluksiin vaikuttava aine, joka edistää mikrotubulusten muodostumista tubuliinidimeereistä ja stabiloi mikrotubuluksia estämällä niiden depolymerisaatiota. Stabilisaatio estää mikrotubulusverkoston normaalia dynaamista uudelleenjärjestäytymistä, jota tarvitaan elintärkeissä solusyklin interfaasi- ja mitoosivaiheissa. Lisäksi paklitakseli aiheuttaa poikkeavien mikrotubulusrykelmien tai -kimppujen muodostumista koko solusyklin ajan sekä useiden mikrotubulushaarojen muodostumista mitoosin aikana. 11
12 Paklitakselin turvallisuutta ja tehoa munasarjasyövän ensilinjan lääkityksenä arvioitiin kahdessa suuressa satunnaistetussa, kontrolloidussa kliinisessä tutkimuksessa (vertailukohteena syklofosfamidi, 750 mg/m 2 / sisplatiini, 75 mg/m 2 ). Intergroup-tutkimuksessa (BMS CA ) yli 650 potilasta, joilla oli tason II b-c, III tai IV primaarinen munasarjasyöpä, sai enintään 9 Taxol-hoitojaksoa (175 mg/m 2 3 tunnin aikana) ja sen jälkeen sisplatiinia (75 mg/m 2 ) tai vertailuvalmistetta. Toisessa suuressa tutkimuksessa (GOG-111/B-MS CA ) arvioitiin enintään 6 hoitojakson tehoa yli 400 potilaalla, joilla oli asteen III/IV primaarinen munasarjasyöpä ja laparotomian jälkeen > 1 cm jäännöskasvain tai etäpesäkkeitä. Hoitojaksoihin kuului joko paklitakselia (135 mg/m 2 24 tunnin kuluessa) ja sen jälkeen sisplatiinia (75 mg/m 2 ) tai vertailuvalmistetta. Näitä kahta paklitakseliannostusta ei verrattu suoraan toisiinsa. Molemmissa tutkimuksissa potilailla, jotka saivat paklitakselia yhdessä sisplatiinin kanssa, saavutettiin kuitenkin merkitsevästi suuremmat vasteprosentit, pidempi aika taudin etenemiseen ja pidempi elinaika kuin tavanomaista hoitoa käytettäessä. Potilailla, joilla oli pitkälle edennyt munasarjasyöpä ja jotka saivat 3 tunnin paklitakseli-infuusion ja sisplatiinia, havaittiin enemmän neurotoksisuutta, nivelkipua ja lihaskipua mutta vähemmän luuydinsuppressiota kuin potilailla, jotka saivat syklofosfamidia ja sisplatiinia. Rintasyövän liitännäishoitoa koskeneessa tutkimuksessa potilasta, joilla oli imusolmukkeisiin levinnyt rintasyöpä, sai ensin neljä jaksoa doksorubisiini- ja syklofosfamidihoitoa ja sen jälkeen joko paklitakseliliitännäishoitoa tai ei lainkaan kemoterapiaa (CALGB 9344, BMS CA ). Seuranta-ajan mediaani oli 69 kk. Yleisesti ottaen paklitakseli vähensi taudin uusiutumisriskiä merkitsevästi (18 %, p = 0,0014) verrattuna potilaisiin, jotka saivat vain antrasykliiniä ja syklofosfamidia. Se pienensi merkitsevästi myös kuolemantapausten riskiä (19 %, p = 0,0044) verrattuna potilaisiin, jotka saivat vain antrasykliiniä ja syklofosfamidia. Retrospektiiviset analyysit osoittavat, että kaikkien alaryhmien potilaat hyötyivät hoidosta. Potilailla, joiden syöpä oli hormonireseptorinegatiivinen tai hormonireseptoristatukseltaan tuntematon, taudin uusiutumisriski pieneni 28 % (95 % luottamusväli 0,59 0,86). Potilailla, joiden syöpä oli hormonireseptoripositiivinen, taudin uusiutumisriski pieneni 9 % (95 % luottamusväli 0,78 1,07). Tutkimusasetelmassa ei kuitenkaan tutkittu yli 4 hoitojakson pituisen antrasykliini-syklofosfamidihoidon vaikutusta. Tästä syystä tämän tutkimuksen perusteella ei voida sulkea pois mahdollisuutta, että vaikutukset voisivat johtua osittain hoitoryhmien saaman lääkehoidon pituuserosta (antrasykliini-syklofosfamidi, 4 hoitojaksoa; antrasykliini, syklofosfamidi ja paklitakseli, 8 hoitojaksoa). Tästä syystä paklitakseliliitännäishoito tulee katsoa antrasykliini-syklofosfamidihoidon jatkamisen vaihtoehdoksi. Toisessa suuressa kliinisessä tutkimuksessa, joka koski imusolmukkeisiin levinneen rintasyövän liitännäishoitoa ja jonka tutkimusasetelma oli samanlainen, potilasta sai neljä antrasykliinisyklofosfamidihoitojaksoa, ja heidät satunnaistettiin saamaan tai olemaan saamatta tämän jälkeen vielä 4 hoitojaksoa paklitakselia suuremmalla 225 mg/m 2 annoksella (NSABP B-28, BMS CA ). Seurantaajan mediaani oli 64 kk. Paklitakselia saaneilla potilailla taudin uusiutumisriski pieneni merkitsevästi (17 %, p = 0,006) verrattuna potilaisiin, jotka saivat vain antrasykliini-syklofosfamidihoitoa. Paklitakselihoidon yhteydessä myös kuolemantapausten riski pieneni 7 % (95 % luottamusväli 0,78 1,12). Kaikkien alaryhmien analyyseissä todettiin, että paklitakseliryhmässä saavutettiin paremmat tulokset. Tässä tutkimuksessa taudin riski pieneni 23 % (95 % luottamusväli 0,6 0,92), jos potilaan kasvain oli hormonireseptoripositiivinen. Hormonireseptorinegatiivisessa potilasryhmässä taudin uusiutumisriski pieneni 10 % (95 % luottamusväli 0,7 1,11). Paklitakselin turvallisuutta ja tehoa rintasyövän ensilinjan lääkityksenä arvioitiin kahdessa keskeisessä satunnaistetussa, kontrolloidussa, avoimessa faasin III tutkimuksessa. Ensimmäisessä tutkimuksessa (BMS CA ) doksorubisiinin bolusannosta (50 mg/m 2 ), jonka jälkeen annettiin 24 tunnin kuluttua 220 mg/m 2 paklitakselia 3 tuntia kestävänä infuusiona (AT-ryhmä), verrattiin tavanomaiseen FAC-hoitoon (5- fluorourasiili 500 mg/m 2, doksorubisiini 50 mg/m 2, syklofosfamidi 500 mg/m 2 ). Molempia hoitoja annettiin kolmen viikon välein 8 hoitojakson ajan. Satunnaistettuun tutkimukseen otettiin 267 potilasta, joilla oli etäpesäkkeinen rintasyöpä ja jotka joko eivät olleet saaneet aiemmin lainkaan kemoterapiaa tai olivat saaneet vain muuta kuin antrasykliinihoitoa sisältävää kemoterapiaa liitännäishoitona. Tulokset osoittivat, että AT- 12
13 ryhmässä aika taudin etenemiseen oli merkitsevästi pidempi kuin FAC-ryhmässä (8,2 kk ja 6,2 kk; p = 0,029). Elinajan mediaani oli paklitakseli/doksorubisiiniryhmässä pidempi kuin FAC-ryhmässä (23,0 kk ja 18,3 kk; p = 0,004). AT-ryhmässä 44 % ja FAC-ryhmässä 48 % potilaista sai vielä myöhempää kemoterapiaa, johon kuului taksaaneja 7 %:lla AT-ryhmän potilaista ja 50 %:lla FAC-ryhmän potilaista. Myös kokonaisvasteprosentti oli AT-ryhmässä merkitsevästi suurempi kuin FAC-ryhmässä (68 % ja 55 %). Täydellinen vaste saavutettiin 19 %:lla paklitakseli/doksorubisiiniryhmän potilaista ja 8 %:lla FAC-ryhmän potilaista. Kaikki tehokkuustulokset on vahvistettu sokkoutetun riippumattoman arvioinnin avulla. Toisessa keskeisessä tutkimuksessa arvioitiin paklitakselin ja trastutsumabin yhdistelmän tehoa ja turvallisuutta tutkimuksen HO648g alaryhmäanalyysissä (etäpesäkkeistä rintasyöpää sairastavat potilaat, jotka olivat aiemmin saaneet antrasykliiniliitännäishoitoa). Trastutsumabin ja paklitakselin yhdistelmän tehoa ei ole osoitettu potilailla, jotka eivät ole saaneet aiempaa antrasykliinihoitoa. Trastutsumabin (4 mg/kg aloitusannos, sitten 2 mg/kg kerran viikossa) ja 3 tuntia kestäneen, 3 viikon välein annetun paklitakseliinfuusion (175 mg/m 2 ) tehoa verrattiin pelkän 3 tuntia kestäneen, 3 viikon välein annetun paklitakseliinfuusion tehoon (175 mg/m 2 ). Tutkimukseen osallistui 188 potilasta, joiden etäpesäkkeinen rintasyöpä yliilmensi HER2:ta (immunohistokemiallinen tulos 2+ tai 3+) ja jotka olivat saaneet aiemmin antrasykliinejä. Paklitakselia annettiin kolmen viikon välein vähintään 6 hoitojakson ajan, kun taas trastutsumabi annettiin kerran viikossa taudin etenemiseen saakka. Tutkimus osoitti, että paklitakseli/trastutsumabiyhdistelmähoitoa saaneilla potilailla saatiin merkitsevästi parempia tuloksia kuin pelkällä paklitakselilla taudin etenemiseen kuluneen ajan suhteen (6,9 kk ja 3,0 kk), vasteprosentin suhteen (41 % ja 17 %) ja hoitovasteen keston suhteen (10,5 kk ja 4,5 kk). Merkitsevin paklitakselin ja trastutsumabin yhdistelmän käyttöön liittynyt toksisuusilmiö olivat sydämen toimintahäiriöt (ks. kohta 4.8). Paklitakselin (175 mg/m 2 ) ja sen jälkeen annettavan sisplatiinin (80 mg/m 2 ) käyttöä pitkälle edenneen eipienisoluisen keuhkosyövän hoidossa on arvioitu kahdessa faasin III tutkimuksessa (367 potilasta sai paklitakselia sisältävää hoitoa). Molemmat tutkimukset olivat satunnaistettuja. Toisessa vertailuhoitona oli sisplatiini (100 mg/m 2 ) ja toisessa teniposidi (100 mg/m 2 ), jonka jälkeen annettiin sisplatiinia (80 mg/m 2 ). 367 potilasta sai vertailuhoitoja. Molemmissa tutkimuksissa saatiin samanlaisia tuloksia. Ensisijainen päätetapahtuma oli kuolleisuus, jonka suhteen paklitakselia sisältäneen hoidon ja vertailuhoidon välillä ei ollut merkitsevää eroa (elinajan mediaanit 8,1 kk ja 9,5 kk paklitakselia sisältänyttä hoitoa käytettäessä ja 8,6 kk ja 9,9 kk vertailuhoitoa käytettäessä). Hoitojen välillä ei ollut merkitsevää eroa myöskään taudin etenemiseen kuluneen ajan suhteen. Kliinisten vasteprosenttien välillä oli merkitsevä ero paklitakselin hyväksi. Elämänlaatua koskevat tulokset viittaavat siihen, että paklitakselia sisältäviin hoitoihin liittyi vähemmän ruokahaluttomuutta, ja osoittavat selvästi, että paklitakselia sisältäviin hoitoihin liittyi enemmän perifeeristä neuropatiaa (p < 0,008). Paklitakselin tehoa ja turvallisuutta AIDSiin liittyvän Kaposin sarkooman hoidossa tutkittiin ei-vertailevassa tutkimuksessa, johon osallistuneilla potilailla oli pitkälle edennyt Kaposin sarkooma, jota oli aiemmin hoidettu systeemisellä kemoterapialla. Ensisijainen päätetapahtuma oli paras kasvainvaste. 63 potilaan 107:stä katsottiin olevan resistenttejä liposomaalisille antrasykliineille. Tämän alaryhmän katsotaan olevan keskeinen tehokkuuspopulaatio. 15 hoitojakson jälkeen kokonaisvasteprosentti (täydellinen/osittainen vaste) liposomaalisille antrasykliineille resistenteillä potilailla oli 57 % (luottamusväli %). Yli 50 % vasteista oli havaittavissa jo ensimmäisten 3 hoitojakson jälkeen. Liposomaalisille antrasykliineille resistenteillä potilailla saavutetut vasteprosentit olivat vertailukelpoisia sekä potilailla, jotka eivät olleet koskaan saaneet proteaasinestäjiä (55,6 %), että potilailla, jotka saivat yhtä proteaasinestäjää vähintään 2 kk ennen paklitakselihoitoa (60,9 %). Taudin etenemiseen kuluneen ajan mediaani keskeisessä potilaspopulaatiossa oli 468 vrk (95 % luottamusväli 257 ei voida arvioida). Elinajan mediaania ei voitu laskea, mutta keskeisessä potilaspopulaatiossa 95 % luottamusvälin alaraja oli 617 vrk. 5.2 Farmakokinetiikka 13
14 Laskimoon annetun paklitakselin pitoisuudet plasmassa pienenevät kaksivaiheisesti. Paklitakselin farmakokinetiikkaa selvitettiin 3 tunnin infuusion jälkeen (annos 135 mg/m 2 ) ja 24 tunnin infuusion jälkeen (annos 175 mg/m 2 ). Arvioidun terminaalisen puoliintumisajan keskiarvot vaihtelivat välillä 3,0 52,7 h, ja kokonaispuhdistuman tilamallittomalla menetelmällä määritetyt keskiarvot vaihtelivat välillä 11,6 24,0 l/h/m 2. Kokonaispuhdistuma vaikutti pienenevän, kun paklitakselin pitoisuus plasmassa suureni. Vakaan tilan jakaantumistilavuuden keskiarvo vaihteli välillä l/m 2, mikä viittaa siihen, että lääke jakautuu voimakkaasti ekstravaskulaariseen tilaan ja/tai sitoutuu voimakkaasti kudoksiin. 3 tunnin infuusiota käytettäessä farmakokinetiikka muuttuu ei-lineaariseksi annoksen suurentuessa. Kun annosta suurennettiin 30 % (tasolta 135 mg/m 2 tasolle 175 mg/m 2 ), huippupitoisuus seerumissa suureni 75 % ja AUC-arvo suureni 81 %. Kun 19 Kaposin sarkoomaa sairastavalle potilaalle annettiin 100 mg/m 2 annos 3 tunnin infuusiona laskimoon, C max -keskiarvo oli 1, 530 ng/ml (vaihteluväli 0,761 2, 860 ng/ml) ja AUC-keskiarvo 5, 619 ng/h/ml (vaihteluväli 2, 609 9, 428 ng/h/ml). Puhdistuma oli 20,6 l/h/m 2 (vaihteluväli 11 38) ja jakautumistilavuus 291 l/m 2 (vaihteluväli ). Terminaalinen eliminaation puoliintumisaika oli keskimäärin 23,7 tuntia (vaihteluväli tuntia). Systeeminen paklitakselialtistus vaihteli kunkin potilaan kohdalla vain hyvin vähän. Paklitakselin kumuloitumisesta elimistöön useita hoitojaksoja annettaessa ei saatu näyttöä. In vitro tutkimukset lääkeaineen sitoutumisesta ihmisen seerumin proteiineihin viittaavat siihen, että sitoutumisprosentti on %. Simetidiini, ranitidiini, deksametasoni ja difenhydramiini eivät vaikuttaneet paklitakselin sitoutumiseen. Paklitakselin eliminaatiota ihmisellä ei ole selvitetty täysin. Keskimäärin 1,3 12,6 % annoksesta on erittynyt muuttumattomana virtsaan, mikä viittaa siihen, että lääke eliminoituu suuressa määrin jotakin muuta kautta kuin munuaisteitse. Paklitakselin eliminaatio saattaa tapahtua pääasiassa maksametabolian ja sappiteitse tapahtuvan eliminaation kautta. Paklitakselin metabolia vaikuttaa olevan pääasiassa CYP450- entsyymivälitteistä. Radioaktiivisesti merkityn paklitakselin annon jälkeen keskimäärin 26 % radioaktiivisuudesta erittyi 6α-hydroksipaklitakselina ulosteeseen, 2 % 3 -p-hydroksipaklitakselina ulosteeseen ja 6 % 6α-3 p-dihydroksipaklitakselina ulosteeseen. Näiden hydroksyloituneiden metaboliittien muodostus tapahtuu CYP2C8-välitteisesti (6α-hydroksipaklitakseli), CYP3A4-välitteisesti (3 -phydroksipaklitakseli) ja sekä CYP2C8- että CYP3A4-välitteisesti (6α-3 p-dihydroksipaklitakseli). Munuaisten tai maksan vajaatoiminnan vaikutusta 3 tunnin infuusiona annetun paklitakselin eliminaatioon ei ole tutkittu muodollisesti. Kun yksi hemodialyysipotilas sai 3 tunnin paklitakseli-infuusion (annos 135 mg/m 2 ), farmakokineettiset parametrit olivat samoissa rajoissa kuin potilailla, jotka eivät saa dialyysihoitoa. Kliinisissä tutkimuksissa, joissa paklitakselia ja doksorubisiinia annettiin yhtä aikaa, doksorubisiinin ja sen metaboliittien jakautuminen elimistöön ja niiden eliminaatio hidastuivat. Kun paklitakseli annettiin välittömästi doksorubisiinin jälkeen, plasman kokonaisaltistus doksorubisiinille oli 30 % suurempi kuin siinä tapauksessa, että lääkkeiden välillä pidettiin 24 tunnin tauko. Jos Paclitaxel Stragenia käytetään yhdessä muiden hoitojen kanssa, on tutustuttava sisplatiinin tai trastutsumabin valmisteyhteenvetoon näiden valmisteiden käyttöä koskevien tietojen saamiseksi. 5.3 Prekliiniset tiedot turvallisuudesta 14
15 Paklitakselin karsinogeenista potentiaalia ei ole tutkittu. Paklitakseli on kuitenkin farmakodynaamisen toimintamekanisminsa vuoksi potentiaalisesti karsinogeeninen ja geenitoksinen. Paklitakselin on osoitettu mutageeninen nisäkkäillä tehdyissä tutkimuksissa in vitro ja in vivo. 6. FARMASEUTTISET TIEDOT 6.1 Apuaineet Vedetön etanoli Makrogoliglyserolirisiinioleaatti 6.2 Yhteensopimattomuudet Makrogoliglyserolirisiinioleaatti voi johtaa DEHP:in (di-(2-etyyliheksyyli)ftalaatin) irtoamiseen pehmeistä PVC-säiliöistä. Pitoisuudet suurenevat makrogoliglyserolirisiinioleaatin pitoisuuden ja ajan myötä. Tästä syystä Paclitaxel Stragen -liuoksen käyttöönvalmistuksessa, säilytyksessä ja annostelussa ei saa käyttää PVC:tä sisältäviä tarvikkeita eikä välineitä. Koska yhteensopivuustutkimuksia ei ole tehty, lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa. 6.3 Kestoaika Avaamaton injektiopullo: 2 vuotta Pakkauksen avaamisen jälkeen ennen laimennusta: Valmisteen on osoitettu säilyvän käytön aikana kemiallisesti ja fysikaalisesti stabiilina 28 vuorokauden ajan 25 C:n lämpötilassa, kun injektiopullosta vedetään useaan otteeseen valmistetta neulalla. Mikrobiologiselta kannalta avattua valmistetta voidaan säilyttää enintään 28 päivän ajan 25 C:n lämpötilassa. Muut käytönaikaiset säilytysajat ja säilytysolosuhteet ovat käyttäjän vastuulla. Laimennuksen jälkeen: Käyttövalmiin infuusionesteen on osoitettu säilyvän kemiallisesti ja fysikaalisesti stabiilina 96 tunnin ajan alle 25 C:n lämpötilassa, kun valmisteen laimentamiseen on käytetty 0,9 % NaCl-infuusionestettä, 5 % glukoosi-infuusionestettä, 0,9 % NaCl-infuusionesteen ja 5 % glukoosi-infuusionesteen sekoitusta tai Ringerin infuusionestettä, jossa on 5 % glukoosia. Mikrobiologiselta kannalta valmiste tulee käyttää välittömästi. Jos valmistetta ei käytetä välittömästi, käytönaikainen säilytysaika ja säilytysolosuhteet ovat käyttäjän vastuulla. Ne ovat kuitenkin yleensä enintään 24 tuntia 2 8 C:n lämpötilassa, ellei laimennus tapahdu kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa. 6.4 Säilytys Säilytä alkuperäispakkauksessa. Herkkä valolle. Laimennettu liuos: Ks. kohta Pakkaustyyppi ja pakkauskoko 15
16 Kirkas, väritön, tyypin I (Ph Eur) lasista valmistettu injektiopullo, jossa klorobutyylikumitulppa ja alumiininen sinetti ja repäisyosa. Injektiopullojen koot: 5 ml, 16,7 ml, 25 ml ja 50 ml. Kaikkia pakkauskokoja ei välttämättä ole myynnissä. 6.6 Erityiset varotoimet hävittämiselle ja muut käsittelyohjeet Käsittely Kuten kaikkia syöpälääkkeitä käsiteltäessä, Paclitaxel Stragenin käsittelyssä on noudatettava varovaisuutta. Koulutetun henkilöstön tulee laimentaa valmiste aseptisissa oloissa tähän tarkoitukseen varatulla alueella. Asianmukaisia suojakäsineitä on käytettävä. Valmisteen joutumista iholle tai limakalvoille on vältettävä, ja sen estämiseksi on ryhdyttävä varotoimiin. Jos valmistetta joutuu iholle, alue pestään vedellä ja saippualla. Paikallisen altistuksen jälkeen on havaittu pistelyä, poltetta ja punoitusta. Jos valmistetta joutuu limakalvoille, alue huuhdellaan huolellisesti vedellä. Kun valmistetta on hengitetty, on havaittu hengenahdistusta, rintakipua, nielun poltetta ja pahoinvointia. Raskaana olevat naiset eivät saa käsitellä paklitakselia. Jos avaamattomia injektiopulloja säilytetään jääkaapissa tai pakastimessa, niihin voi muodostua sakkaa, joka liukenee uudelleen valmisteen lämmetessä huoneenlämpöön, vaikka valmistetta ei sekoitettaisi lainkaan tai sitä sekoitettaisiin vain vähän. Tämä ei vaikuta valmisteen laatuun. Jos liuos pysyy sameana tai siinä havaitaan liukenematonta sakkaa, injektiopullo tulee hävittää. Valmistelu laskimoon antamista varten Ennen infuusiota Paclitaxel Stragen laimennetaan aseptisesti johonkin seuraavista infuusionesteistä: 0,9 % NaCl-infuusioneste, 5 % glukoosi-infuusioneste, 0,9 % NaCl-infuusionesteen ja 5 % glukoosi-infuusionesteen sekoitus tai Ringerin infuusioneste, jossa on 5 % glukoosia. Lopullisen pitoisuuden tulee olla 0,3 1,2 mg/ml. Laimennetun liuoksen kemiallinen ja fysikaalinen stabiliteetti, ks. kohta 6.3. Käyttöönvalmistuksen yhteydessä liuos voi olla hieman samea, mikä johtuu valmisteen vehikkelistä. Sameutta ei voi poistaa suodattamalla. Paclitaxel Stragen annetaan käyttäen infuusiosuodatinta, jonka mikrohuokoisen kalvon huokoskoko on 0,22 μm. Valmisteen tehon ei havaittu heikkenevän merkitsevästi simuloidussa annostelussa, jossa valmiste annettiin infuusiosuodattimella varustetun laskimoannosteluletkuston kautta. Harvinaisissa tapauksissa on ilmoitettu paklitakseli-infuusion sakkautumista, yleensä 24 tunnin infuusioajan loppuvaiheissa. Vaikka sakkautumisen syytä ei olekaan selvitetty, ilmiö on todennäköisesti yhteydessä laimennetun liuoksen ylisaturaatioon. Sakkautumisriskin vähentämiseksi Paclitaxel Stragen tulee käyttää mahdollisimman pian laimentamisen jälkeen, ja sen voimakasta sekoittamista, täristämistä tai ravistelua tulee välttää. Infuusioletkusto tulee huuhdella huolellisesti ennen käyttöä. Infuusion aikana liuoksen ulkonäkö on tarkastettava säännöllisesti, ja infuusio tulee keskeyttää, jos liuoksessa havaitaan sakkaa. Pehmeistä PVC-infuusiovälineistä voi irrota DEHP:iä [di-(2-etyyliheksyyli)ftalaatti]. DEHP-altistuksen minimoimiseksi laimennetut paklitakseliliuokset on säilytettävä pulloissa tai pusseissa, jotka eivät sisällä PVC:tä (lasi- tai polypropyleenipullot; polypropyleeni- tai polyolefiinipussit), ja niiden antamiseen tulee käyttää polyetyleenipinnoitettuja välineitä. DEHP:iä ei ole irronnut merkitsevässä määrin, kun käytetyissä suodattimissa on ollut lyhyt, pehmeä PVC-letku (jompaankumpaan tai molempiin suuntiin). 16
17 Hävittäminen Kaikki Paclitaxel Stragenin käyttöönvalmistukseen ja antamiseen käytetyt esineet sekä esineet, jotka joutuvat muutoin kosketuksiin lääkkeen kanssa, tulee hävittää sytotoksisten yhdisteiden käsittelyä koskevien paikallisten ohjeiden mukaisesti. 7. MYYNTILUVAN HALTIJA Stragen Nordic A/S Hesselvej 41 Ganlose 3660 Stenlose Tanska puh.: faksi: sähköposti: 8. MYYNTILUVAN NUMERO(T) MYYNTILUVAN MYÖNTÄMISPÄIVÄMÄÄRÄ/UUDISTAMISPÄIVÄMÄÄRÄ <{PP/KK/VVVV}> <{PP kuukautta VVVV}> [Täytetään kansallisesti] 10. TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
Apuaineet: Vedetön etanoli (401,7 mg/ml), polyoksyylirisiiniöljy (makrogoliglyserolirisiinioleaatti) (522,4 mg/ml)
 1. LÄÄKEVALMISTEEN NIMI Pacligen 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia. Yksi 5 ml injektiopullo
1. LÄÄKEVALMISTEEN NIMI Pacligen 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia. Yksi 5 ml injektiopullo
PAKKAUSSELOSTE Paclitaxel Stragen 6 mg/ml infuusiokonsentraatti, liuosta varten Paklitakseli
 PAKKAUSSELOSTE 1 PAKKAUSSELOSTE Paclitaxel Stragen 6 mg/ml infuusiokonsentraatti, liuosta varten Paklitakseli Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste.
PAKKAUSSELOSTE 1 PAKKAUSSELOSTE Paclitaxel Stragen 6 mg/ml infuusiokonsentraatti, liuosta varten Paklitakseli Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia.
Paclitaxel Fresenius Kabi 6 mg/ml infuusiokonsentraatti, liuosta varten
 1. LÄÄKEVALMISTEEN NIMI Paclitaxel Fresenius Kabi 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 millilitra infuusiokonsentraattia, liuosta varten, sisältää 6 mg
1. LÄÄKEVALMISTEEN NIMI Paclitaxel Fresenius Kabi 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 millilitra infuusiokonsentraattia, liuosta varten, sisältää 6 mg
VALMISTEYHTEENVETO. Paclitaxel Hospira 6 mg/ml infuusiokonsentraatti, liuosta varten
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxel Hospira 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra infuusiokonsentraattia sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxel Hospira 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra infuusiokonsentraattia sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Paclitaxel STADA 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxel STADA 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxel STADA 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
Valmisteyhteenveto. Paclitaxel Accord 6 mg/ml infuusiokonsentraatti, liuosta varten
 1. LÄÄKEVALMISTEEN NIMI Valmisteyhteenveto Paclitaxel Accord 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra infuusiokonsentraattia, liuosta varten,
1. LÄÄKEVALMISTEEN NIMI Valmisteyhteenveto Paclitaxel Accord 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra infuusiokonsentraattia, liuosta varten,
VALMISTEYHTEENVETO. Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti. Osmolaliteetti: noin 4 000 mosm/kg vettä ph: noin 4
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Kaliumkloridia sisältää: Kaliumkloridi 150 mg/ml, joka vastaa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Kaliumkloridia sisältää: Kaliumkloridi 150 mg/ml, joka vastaa
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. TAXOL 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TAXOL 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Paklitakseli 6 mg/ml. 5 ml:n injektiopullo sisältää 30 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TAXOL 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Paklitakseli 6 mg/ml. 5 ml:n injektiopullo sisältää 30 mg paklitakselia.
VALMISTEYHTEENVETO. Valmisteen kuvaus: Valkoinen tai melkein valkoinen talkkimainen jauhe.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 9 mg natriumkloridia. 100 ml sisältää 15,4 mmol (vastaten 354 mg) natriumia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 9 mg natriumkloridia. 100 ml sisältää 15,4 mmol (vastaten 354 mg) natriumia.
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia vastaten 1,5 g glukosamiinisulfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
Histadin- valmisteen tehoa ja turvallisuutta ei ole osoitettu alle 2-vuotiailla lapsilla.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Metronidatsoli 0,75 paino-%, 7,5 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.1 Käyttöaiheet. 4.2 Annostus ja antotapa
 1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
Hivenaineiden perustarpeen sekä hiukan lisääntyneen tarpeen tyydyttämiseen laskimoravitsemuksen yhteydessä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
VALMISTEYHTEENVETO. Ruiskeina annettavien jauheiden, konsentraattien ja liuosten liuottamiseen ja laimentamiseen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Fresenius Kabi 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9,0 mg/ml Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Fresenius Kabi 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9,0 mg/ml Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO. Päänahan seborrooinen ekseema ja muu päänahan hilseily (pityriasis capitis). Pityriasis versicolor.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Steriili vesi Baxter Viaflo, liuotin parenteraaliseen käyttöön
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Steriili vesi Baxter Viaflo, liuotin parenteraaliseen käyttöön 2. VAIKUTTAVAT AINEET NIIDEN MÄÄRÄT JA Injektionesteisiin käytettävä vesi. 3. LÄÄKEMUOTO Liuotin
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Steriili vesi Baxter Viaflo, liuotin parenteraaliseen käyttöön 2. VAIKUTTAVAT AINEET NIIDEN MÄÄRÄT JA Injektionesteisiin käytettävä vesi. 3. LÄÄKEMUOTO Liuotin
VALMISTEYHTEENVETO. Apuaine: Yksi kerta-annosinjektiopullo infuusiokonsentraattia sisältää 27 painoprosenttia 96-prosenttista etanolia.
 1. LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Docetaxel Ebewe 10 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia sisältää 10 mg dosetakselia.
1. LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Docetaxel Ebewe 10 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia sisältää 10 mg dosetakselia.
VALMISTEYHTEENVETO. Valkoinen, pyöreä, kummaltakin puolelta litteä viistoreunainen tabletti, jossa jakouurre toisella puolella.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
Kissa: Leikkauksen jälkeisen kivun lievitys kohdun ja munasarjojen poistoleikkauksen sekä pienten pehmytkudoskirurgisten toimenpiteiden jälkeen.
 1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
VALMISTEYHTEENVETO. Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia, joka vastaa 2,68 mg bentsydamiinia.
 1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
VALMISTEYHTEENVETO. Lievän tai kohtalaisen vaikean polven nivelrikon oireiden lievittäminen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO. Yli 33 kg painavat lapset (noin 11-vuotiaat), alle 50 kg painavat nuoret ja aikuiset:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO. Huom. Emätinpuikko tulee työntää syvälle emättimeen, ei mielellään kuukautisten aikana.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
Vaaleankeltainen, opalisoiva piparmintun tuoksuinen ja makuinen suspensio.
 1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
VALMISTEYHTEENVETO. Aikuiset (myös iäkkäät): Suositeltu annos on 800 mg eli 2 kapselia vuorokaudessa kerta-annoksena kolmen kuukauden ajan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Yksi tippa silmän sidekalvopussiin 4 kertaa päivässä tai tarpeen mukaan tilan vaikeusasteesta riippuen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Oculac 50 mg/ml silmätipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml: 50 mg povidoni K 25 Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Silmätipat,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Oculac 50 mg/ml silmätipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml: 50 mg povidoni K 25 Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Silmätipat,
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO. Addex-Magnesiumsulfaatti 246 mg/ml infuusiokonsentraatti, liuosta varten
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Magnesiumsulfaatti 246 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Magnesiumsulfaatti infuusiokonsentraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Magnesiumsulfaatti 246 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Magnesiumsulfaatti infuusiokonsentraattia
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. Revertor vet 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Revertor vet 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml injektionestettä sisältää: Vaikuttava aine: Atipametsolihydrokloridi
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Revertor vet 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml injektionestettä sisältää: Vaikuttava aine: Atipametsolihydrokloridi
VALMISTEYHTEENVETO. Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia 20 mg (2 %).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
VALMISTEYHTEENVETO. Akrivastiinia ei pidä määrätä potilaille, joiden munuaistoiminta on merkittävästi heikentynyt.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO. Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112 mg feksofenadiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
LIITE VALMISTEYHTEENVETO
 LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml konsentraattia sisältää 20 mg dosetakselia. Yksi 1 ml:n
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Qvidadotax 20 mg/ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml konsentraattia sisältää 20 mg dosetakselia. Yksi 1 ml:n
4.1 Käyttöaihe Akuutteihin tai kroonisiin keuhko- ja keuhkoputkisairauksiin liittyvän limaa erittävän yskän limaa irrottava hoito.
 V A LMIS T EYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 60 mg poretabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi poretabletti sisältää 60 mg ambroksolihydrokloridia. Apuaineet: 110,00 mg vedetöntä
V A LMIS T EYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 60 mg poretabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi poretabletti sisältää 60 mg ambroksolihydrokloridia. Apuaineet: 110,00 mg vedetöntä
VALMISTEYHTEENVETO. Neste- ja elektrolyyttihukka esim. leikkauksen, trauman tai palovammojen yhteydessä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ringer-acetat Fresenius Kabi, infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml infuusionestettä sisältää: Natr. chlorid. 5,9 g Natr. acet.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ringer-acetat Fresenius Kabi, infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml infuusionestettä sisältää: Natr. chlorid. 5,9 g Natr. acet.
1. ELÄINLÄÄKKEEN NIMI. Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
VALMISTE YHT E ENVET O
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
VALMISTEYHTEENVETO. Maksimivuorokausiannos 40 ml (120 mg dekstrometorfaania)
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resilar 3 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml sisältää 3 mg dekstrometorfaanihydrobromidia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resilar 3 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml sisältää 3 mg dekstrometorfaanihydrobromidia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO. Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml. Valmisteen kuvaus: miedosti tuoksuva, väritön tai hieman kellertävä liuos
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
Tuulix tabletit on tarkoitettu allergisen nuhan sekä kroonisen idiopaattisen urtikarian oireiden hoitoon.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tuulix 10 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tuulix 10 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
Yksi kerta-annosinjektiopullo sisältää vedetöntä etanolia 182 mg/ml (23% v/v). Täydellinen apuaineluettelo, ks. kohta 6.1
 VALMISTEYHTEENVETO 1 LÄÄKEVALMISTEEN NIMI Docetaxel Hospira 10 mg/ml infuusiokonsentraatti, liuosta varten 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 10 mg
VALMISTEYHTEENVETO 1 LÄÄKEVALMISTEEN NIMI Docetaxel Hospira 10 mg/ml infuusiokonsentraatti, liuosta varten 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 10 mg
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO. Tämä lääkevalmiste on tarkoitettu vain IgE-välitteisen allergian spesifiseen diagnostiseen käyttöön.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI SOLUPRICK SQ hyönteismyrkyt, liuos ihopistotestiin - 801 Mehiläisen myrkky (Apis mellifera) - 802 Ampiaisen myrkky (Vespula spp.) 2. VAIKUTTAVAT AINEET JA NIIDEN
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI SOLUPRICK SQ hyönteismyrkyt, liuos ihopistotestiin - 801 Mehiläisen myrkky (Apis mellifera) - 802 Ampiaisen myrkky (Vespula spp.) 2. VAIKUTTAVAT AINEET JA NIIDEN
Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen 8 ml:n injektiopullo konsentraattia sisältää 160 mg dosetakselia.
 1. LÄÄKEVALMISTEEN NIMI TAXOTERE 160 mg/8 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
1. LÄÄKEVALMISTEEN NIMI TAXOTERE 160 mg/8 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
Eläimiä koskevat erityiset varotoimet Jos haittavaikutuksia ilmenee, tulee hoito keskeyttää ja ottaa yhteys eläinlääkäriin.
 1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg karmelloosinatriumia. Yksi tippa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg karmelloosinatriumia. Yksi tippa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO. Valmisteen kuvaus: pyöreä, merkintä BEPANTHEN kehässä, halkaisija n. 18 mm, paksuus n. 3,5 mm, harmaankeltainen, sitruunan tuoksu.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle tai apuaineille.
 1. ELÄINLÄÄKKEEN NIMI Ancesol 10 mg/ml injektioneste, liuos, naudoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Kloorifenamiinimaleaatti (vastaa 7,03 mg kloorifenamiinia)
1. ELÄINLÄÄKKEEN NIMI Ancesol 10 mg/ml injektioneste, liuos, naudoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Kloorifenamiinimaleaatti (vastaa 7,03 mg kloorifenamiinia)
Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
VALMISTEYHTEENVETO. Nuhaan ja poskiontelotulehdukseen liittyvän limakalvojen turvotuksen lievittäminen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT - ksylometatsoliinihydrokloridi 0,5 mg/ml - ksylometatsoliinihydrokloridi 1 mg/ml Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT - ksylometatsoliinihydrokloridi 0,5 mg/ml - ksylometatsoliinihydrokloridi 1 mg/ml Täydellinen apuaineluettelo, ks. kohta
1. ELÄINLÄÄKKEEN NIMI. Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Yksi millilitra sisältää: Vaikuttava aine:
 1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
PAKKAUSSELOSTE. VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa
 PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
VALMISTEYHTEENVETO. Yliherkkyys mikonatsolille, muille imidatsolijohdannaisille tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 20 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää mikonatsolinitraattia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 20 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää mikonatsolinitraattia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää: Glukoosi, vedetön 6,75 g Natriumkloridi 1,30 g Natriumsitraatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää: Glukoosi, vedetön 6,75 g Natriumkloridi 1,30 g Natriumsitraatti
VALMISTEYHTEENVETO. Tabletit ovat pyöreitä, harmaansinisiä ja sokeripäällysteisiä, halkaisija n. 11 mm.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
VALMISTEYHTEENVETO. Täydellisen parenteraalisen ravitsemuksen täydennyksenä vesiliukoisten vitamiinien päivittäisen tarpeen tyydyttämiseksi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Docetaxel Orion 20 mg/1 ml infuusiokonsentraatti, liuosta varten Docetaxel Orion 80 mg/4 ml infuusiokonsentraatti, liuosta varten Docetaxel Orion 160 mg/8 ml
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Docetaxel Orion 20 mg/1 ml infuusiokonsentraatti, liuosta varten Docetaxel Orion 80 mg/4 ml infuusiokonsentraatti, liuosta varten Docetaxel Orion 160 mg/8 ml
VALMISTEYHTEENVETO. Shampoo Viskoosi liuos, joka on väriltään kirkkaan oljenkeltainen tai vaaleanoranssi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Vaminolac infuusioneste 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT ml sisältää:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vaminolac infuusioneste 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml sisältää: Vaikuttavat aineet Alaniini Arginiini Asparagiinihappo Kysteiini (+ kystiini)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vaminolac infuusioneste 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml sisältää: Vaikuttavat aineet Alaniini Arginiini Asparagiinihappo Kysteiini (+ kystiini)
VALMISTEYHTEENVETO. Koira Lievän tai kohtalaisen sisäelimiin liittyvän kivun lievittämiseen. Rauhoittamiseen yhdessä medetomidiinin kanssa.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Torphasol vet 4 mg/ml injektioneste, liuos koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Butorfanoli (butorfanolitartraattina
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Torphasol vet 4 mg/ml injektioneste, liuos koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Butorfanoli (butorfanolitartraattina
Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille
 1. ELÄINLÄÄKKEEN NIMI Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra injektionestettä sisältää: Vaikuttava
1. ELÄINLÄÄKKEEN NIMI Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra injektionestettä sisältää: Vaikuttava
VALMISTEYHTEENVETO. Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g
 1 LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen annospussi sisältää seuraavat määrät vaikuttavia
1 LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen annospussi sisältää seuraavat määrät vaikuttavia
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Mylan 20 mg/1 ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml infuusiokonsentraattia, liuosta varten
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Mylan 20 mg/1 ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml infuusiokonsentraattia, liuosta varten
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Accord 20 mg/1 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Accord 20 mg/1 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg
Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten
 1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva 80 mg konsentraatin kerta-annosinjektiopullo sisältää
1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva 80 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva 80 mg konsentraatin kerta-annosinjektiopullo sisältää
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Hospira UK Limited 20 mg/1 ml infuusiokonsentraatti, liuosta varten Docetaxel Hospira UK Limited 80 mg/4 ml infuusiokonsentraatti, liuosta
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Hospira UK Limited 20 mg/1 ml infuusiokonsentraatti, liuosta varten Docetaxel Hospira UK Limited 80 mg/4 ml infuusiokonsentraatti, liuosta
Apuaineet: Yksi gramma sisältää 1,56 mg metyyliparahydroksibentsoaattia (E 218) ja 0,17 mg propyyliparahydroksibentsoaattia (E 216), ks. kohta 4.4.
 1. LÄÄKEVALMISTEEN NIMI REGRANEX 0,01 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma geeliä sisältää 100 μg bekaplermiiniä*. * Rekombinantti-DNA-tekniikalla tuotettu ihmisen BB-verihiutalekasvutekijä
1. LÄÄKEVALMISTEEN NIMI REGRANEX 0,01 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma geeliä sisältää 100 μg bekaplermiiniä*. * Rekombinantti-DNA-tekniikalla tuotettu ihmisen BB-verihiutalekasvutekijä
VALMISTEYHTEENVETO. Liialliseen kaasunmuodostukseen liittyvät mahan ja suoliston vaivat
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Espumisan 100 mg/ml tipat, emulsio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Vaikuttava aine: simetikoni 1 ml sisältää 100 mg simetikonia. Apuaine: sorbitoli (E420),
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Espumisan 100 mg/ml tipat, emulsio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Vaikuttava aine: simetikoni 1 ml sisältää 100 mg simetikonia. Apuaine: sorbitoli (E420),
VALMISTEYHTEENVETO. Yksi 8,5 ml ampulli sisältää 1 mg terlipressiiniasetaattia, vastaten 0,85mg terlipressiiniä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GLYPRESSIN 1 mg injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 8,5 ml ampulli sisältää 1 mg terlipressiiniasetaattia, vastaten 0,85mg terlipressiiniä.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GLYPRESSIN 1 mg injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi 8,5 ml ampulli sisältää 1 mg terlipressiiniasetaattia, vastaten 0,85mg terlipressiiniä.
Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
 1. LÄÄKEVALMISTEEN NIMI Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
1. LÄÄKEVALMISTEEN NIMI Docetaxel Actavis 20 mg/ml infuusiokonsentraatti liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen Docetaxel Actavis injektiopullo sisältää dosetakselia 20 mg/ml.
INFLECTRA SEULONTAKORTTI
 Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
Demyelinoiva sairaus Jos potilaalla on aiempi tai äskettäin puhjennut demyelinioiva sairaus, anti-tnf-hoidon hyödyt ja haitat on arvioitava huolellisesti ennen INFLECTRA -hoidon aloitusta. INFLECTRA -hoidon
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. Norocarp vet 50 mg/ml injektioneste, liuos koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Norocarp vet 50 mg/ml injektioneste, liuos koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Karprofeeni 50
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Norocarp vet 50 mg/ml injektioneste, liuos koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Karprofeeni 50
VALMISTEYHTEENVETO. Valmistetta ei saa antaa kanille, marsulle, hamsterille, gerbiilille eikä muille pienille jyrsijöille.
 1. ELÄINLÄÄKKEEN NIMI Amovet vet 150 mg/ml injektioneste, suspensio VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Amoksisilliinitrihydraatti (172,1 mg) vastaten
1. ELÄINLÄÄKKEEN NIMI Amovet vet 150 mg/ml injektioneste, suspensio VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Amoksisilliinitrihydraatti (172,1 mg) vastaten
VALMISTEYHTEENVETO. Hiuspohja pestään Ketoconazol ratiopharm shampoolla, jonka annetaan vaikuttaa 3-5 minuutin ajan ennen huuhtelua.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
Liite III Valmisteyhteenvetoon ja pakkausselosteeseen tehtävät muutokset
 Liite III Valmisteyhteenvetoon ja pakkausselosteeseen Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen jäsenvaltioiden
Liite III Valmisteyhteenvetoon ja pakkausselosteeseen Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen jäsenvaltioiden
Lääkevalmisteella ei enää myyntilupaa
 PAKKAUSSELOSTE Nespo 15 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo 25 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo 40 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo
PAKKAUSSELOSTE Nespo 15 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo 25 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo 40 mikrogrammaa, injektioneste, liuos injektiopullossa Nespo
VALMISTEYHTEENVETO. Malignit lymfooma:. Hodgkinin tauti, retikkelisolusarkooma, lymfosarkooma.
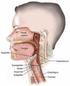 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 20 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidi 20 mg/ml Apuaineet, ks 6.1 3. LÄÄKEMUOTO Infuusiokonsentraatti,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 20 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidi 20 mg/ml Apuaineet, ks 6.1 3. LÄÄKEMUOTO Infuusiokonsentraatti,
Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina.
 1. LÄÄKEVALMISTEEN NIMI TAXOTERE 20 mg/1 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
1. LÄÄKEVALMISTEEN NIMI TAXOTERE 20 mg/1 ml infuusiokonsentraatti, liuosta varten. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml konsentraattia sisältää 20 mg dosetakselia trihydraattina. Jokainen
Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Basiron AC 5 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Basiron AC 5 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
Neste- ja NaCl- vajaus. Infuusioiden ja injektioiden valmistamiseen.
 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Baxter 9 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9 mg/ml mmol/l: Na + 154 Cl - 154 Täydellinen apuaineluettelo, ks. kohta
1. LÄÄKEVALMISTEEN NIMI Natriumklorid Baxter 9 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9 mg/ml mmol/l: Na + 154 Cl - 154 Täydellinen apuaineluettelo, ks. kohta
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Wartec 5 mg/ml liuos penslaukseen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra liuosta sisältää 5 mg podofyllotoksiinia. Täydellinen apuaineluettelo,
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Wartec 5 mg/ml liuos penslaukseen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra liuosta sisältää 5 mg podofyllotoksiinia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Ketokonatsoli 20 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ketokonatsoli 20 mg/g Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Emulsiovoide Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ketokonatsoli 20 mg/g Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Emulsiovoide Valmisteen
Metotreksaattihoidon toksisen vaikutuksen kumoaminen. Pitkälle edennyt kolorektaalisyöpä yhdessä 5- fluorourasiilin kanssa.
 1. LÄÄKEVALMISTEEN NIMI Isovorin 10 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Levofoliinihappo 10 mg/ml kalsiumlevofolinaattina Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
1. LÄÄKEVALMISTEEN NIMI Isovorin 10 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Levofoliinihappo 10 mg/ml kalsiumlevofolinaattina Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Riniitti. Sinuiitti. Lisälääkityksenä välikorvatulehduksessa vähentämään nenä-nielualueen limakalvon turvotusta. Rinoskopia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Otrivin Säilytysaineeton 0,5 mg/ml nenäsumute, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ksylometatsoliinihydrokloridi 0,5 mg/ml. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Otrivin Säilytysaineeton 0,5 mg/ml nenäsumute, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ksylometatsoliinihydrokloridi 0,5 mg/ml. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Normofusin 50 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Normofusin 50 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml Normofusin 50 mg/ml infuusionestettä sisältää: Vaikuttava aine Määrä
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Normofusin 50 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml Normofusin 50 mg/ml infuusionestettä sisältää: Vaikuttava aine Määrä
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Natriumklorid Braun 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Braun 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml injektionestettä sisältää natriumkloridia Elektrolyyttipitoisuudet
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Braun 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml injektionestettä sisältää natriumkloridia Elektrolyyttipitoisuudet
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva Pharma 20 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva Pharma 20 mg
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Docetaxel Teva Pharma 20 mg infuusiokonsentraatti ja liuotin, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Docetaxel Teva Pharma 20 mg
Annosta tulee muuttaa eläimillä, joilla on munuaisten tai maksan vajaatoiminta, koska haittavaikutusriski on suurentunut.
 1. ELÄINLÄÄKKEEN NIMI Metomotyl vet 2,5 mg/ml injektioneste, liuos kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 millilitra sisältää: Vaikuttava aine: metoklopramidi (hydrokloridimonohydraattina)
1. ELÄINLÄÄKKEEN NIMI Metomotyl vet 2,5 mg/ml injektioneste, liuos kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 millilitra sisältää: Vaikuttava aine: metoklopramidi (hydrokloridimonohydraattina)
VALMISTEYHTEENVETO. Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten on tarkoitettu aikuisten potilaiden hoitoon.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Paclitaxin 6 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml infuusiokonsentraattia liuosta varten sisältää 6 mg paklitakselia.
VALMISTEYHTEENVETO. 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LIVOSTIN 0,5 mg/ml nenäsumute, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LIVOSTIN 0,5 mg/ml nenäsumute, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
