Augmentin on tarkoitettu seuraavien infektioiden hoitoon aikuisille ja lapsille (ks. kohdat 4.2, 4.4 ja 5.1).
|
|
|
- Eeva-Kaarina Kinnunen
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 1. LÄÄKEVALMISTEEN NIMI Augmentin 875 mg/125 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää amoksisilliinitrihydraattia vastaten 875 mg amoksisilliinia, ja kaliumklavulanaattia vastaten 125 mg klavulaanihappoa. Täydellinen apuaineluettelo, ks. kohta LÄÄKEMUOTO Kalvopäällysteinen tabletti. Tabletit ovat valkoisia tai luonnonvalkoisia ja kapselin muotoisia. Tabletin molemmilla puolilla on kaiverrus AC ja toisella puolella on jakouurre. Jakouurre on tarkoitettu ainoastaan tabletin puolittamiseen nielemisen helpottamiseksi, ei tabletin jakamiseen keskenään yhtä suuriin annoksiin. 4. KLIINISET TIEDOT 4.1 Käyttöaiheet Augmentin on tarkoitettu seuraavien infektioiden hoitoon aikuisille ja lapsille (ks. kohdat 4.2, 4.4 ja 5.1). akuutti bakteerin aiheuttama sinuiitti (asianmukaisesti diagnosoitu) akuutti välikorvan tulehdus akuutti kroonisen bronkiitin pahenemisvaihe (asianmukaisesti diagnosoitu) kotisyntyinen keuhkokuume kystiitti pyelonefriitti iho- ja pehmytkudosinfektiot, erityisesti selluliitti, eläinten puremat, vaikeat hammasperäiset abskessit, joihin liittyy etenevä selluliitti luu- ja nivelinfektiot, erityisesti osteomyeliitti. Antibioottihoidon toteutuksessa on huomioitava antibakteerisen lääkehoidon tarkoituksenmukaista käyttöä koskevat viralliset ohjeet. 4.2 Annostus ja antotapa Annostus Annokset ilmaistaan kauttaaltaan amoksisilliinina/klavulaanihappona paitsi silloin kun annokset ilmoitetaan yksittäisinä komponentteina. Seuraavat asiat on huomioitava valittaessa Augmentinin annosta tietyn infektion hoitoon: oletetut patogeenit ja niiden todennäköinen herkkyys antibakteerisille lääkeaineille (ks. kohta 4.4) infektion vaikeus ja paikka potilaan ikä, paino ja munuaistoiminta, kuten alla on kuvattu. 1
2 Aikuisten ja 40 kg painavien lasten kokonaisvuorokausiannos on tätä Augmentinin lääkemuotoa käytettäessä 1750 mg amoksisilliinia/250 mg klavulaanihappoa kaksi kertaa vuorokaudessa annosteltuna ja 2625 mg amoksisilliinia/375 mg klavulaanihappoa kolme kertaa vuorokaudessa annosteltuna, kun lääke annetaan alla olevan suosituksen mukaisesti. Alle 40 kg painavien lasten enimmäisannos vuorokaudessa on tätä Augmentinin lääkemuotoa käytettäessä mg amoksisilliinia/ mg klavulaanihappoa, kun lääke annetaan alla olevan suosituksen mukaisesti. Hoidon keston tulee määräytyä potilaan vasteen mukaan. Jotkut infektiot (esim. osteomyeliitti) vaativat pitempiä hoitoaikoja. Hoitoa ei tule jatkaa yli 14 päivää ilman uudelleenarviointia (ks. kohta 4.4 koskien pitkäkestoista hoitoa). Aikuiset ja 40 kg painavat lapset Suositeltu annos: standardiannos (kaikki käyttöaiheet): 875 mg/125 mg kaksi kertaa vuorokaudessa korotettu annos (erityisesti välikorvan-, poskiontelon-, alempien hengitysteiden ja virtsatietulehduksessa): 875 mg/125 mg kolme kertaa vuorokaudessa Alle 40 kg painavat lapset Lapsille Augmentin voidaan antaa tabletteina tai oraalisuspensiona. Suositeltu annos: 25 mg/3,6 mg/kg/vrk 45 mg/6,4 mg/kg/vrk jaettuna kahteen annokseen joissakin infektioissa (kuten välikorvan, poskiontelon ja alempien hengitysteiden infektioissa) annos voi olla enintään 70 mg/10 mg/kg/vrk jaettuna kahteen annokseen. Augmentin-tabletteja ei voi jakaa, joten niitä ei tule antaa alle 25 kg painaville lapsille. Alla olevassa taulukossa on esitetty lasten saamat amoksisilliini- ja klavulaanihappoannokset (mg/painokilo) kg painavilla lapsilla yhden 875 mg/125 mg tabletin kerta-annoksen jälkeen. Paino [kg] Amoksisilliiniannos [mg/painokilo] yhtä kerta-annosta kohden (1 kalvopäällysteinen tabletti) Klavulaanihappoannos [mg/painokilo] yhtä kerta-annosta kohden (1 kalvopäällysteinen tabletti) 21, 9 25,0 29,2 35,0 3,1 3,6 4,2 5,0 Suositeltu kerta-annos [mg/painokilo] (ks. yllä) 12,5 22,5 (korkeintaan 35) 1,8 3,2 (korkeintaan 5) Alle 25 kg painaville lapsille suositellaan annettavaksi Augmentin-oraalisuspensiota. 2
3 Kliinistä tutkimustietoa ei ole saatavilla koskien Augmentinin 7:1 formulaatioiden käyttöä alle 2-vuotiailla lapsilla, kun annos on yli 45 mg/6,4 mg/kg vuorokaudessa. Kliinistä tutkimustietoa ei ole saatavilla koskien Augmentinin 7:1 formulaatioiden käyttöä alle 2 kuukauden ikäisillä lapsilla. Annossuosituksia ei sen vuoksi voida antaa tälle potilasryhmälle. Iäkkäät potilaat Annoksen muuttaminen ei ole tarpeen. Munuaisten vajaatoiminta Annoksen muuttaminen ei ole tarpeen hoidettaessa potilaita, joiden kreatiniinipuhdistuma (CrCl) on yli 30 ml/min. Potilaille, joiden kreatiinipuhdistuma on alle 30 ml/min, ei suositella käytettäväksi Augmentin-valmisteita, joissa amoksisilliinin ja klavulaanihapon suhde on 7:1, koska annoksen sovittamista koskevia suosituksia ei ole saatavilla. Maksan vajaatoiminta Annettava varoen. Maksan toimintaa tulee seurata säännöllisin väliajoin (ks. kohdat 4.3 ja 4.4). Antotapa Augmentin otetaan suun kautta. Augmentin tulee annostella aterian yhteydessä, jotta voidaan minimoida mahdollinen gastrointestinaalinen intoleranssi. 4.3 Vasta-aiheet Yliherkkyys vaikuttaville aineille, jollekin penisilliinille tai kohdassa 6.1 mainituille apuaineille. Aiempi vaikea välitön yliherkkyysreaktio (esim. anafylaksi) toiselle beetalaktaamivalmisteelle (esim. kefalosporiinille, karbapeneemille tai monobaktaamille). Aiempi amoksisilliini-klavulaanihaposta johtunut keltatauti/maksan vajaatoiminta (ks. kohta 4.8). 4.4 Varoitukset ja käyttöön liittyvät varotoimet Ennen amoksisilliini-klavulaanihappohoidon aloittamista mahdolliset aiemmat penisilliinien, kefalosporiinien tai muiden beetalaktaamien aiheuttamat yliherkkyysreaktiot on selvitettävä tarkkaan (ks. kohdat 4.3 ja 4.8). Penisilliinihoitoa saavilla potilailla on kuvattu vakavia ja joskus kuolemaan johtavia yliherkkyysreaktioita (anafylaksin kaltaisia). Nämä reaktiot ovat todennäköisempiä potilailla, joilla on aiemmin todettu penisilliiniyliherkkyys sekä atooppisilla henkilöillä. Jos potilas saa allergisen reaktion, amoksisilliiniklavulaanihappohoito on lopetettava ja aloitettava sopiva vaihtoehtoinen hoito. Jos infektion aiheuttajamikrobi(e)n on osoitettu olevan herkk(i)ä amoksisilliinille, on harkittava siirtymistä amoksisilliini-klavulaanihaposta amoksisilliiniin virallisia hoitosuosituksia noudattaen. 3
4 Tämä Augmentin-valmiste ei sovellu käytettäväksi silloin kun on olemassa suuri riski, että oletetut patogeenit ovat resistenttejä beetalaktaamivalmisteille, eikä tämä resistenssi välity sellaisten beetalaktamaasien kautta, jotka ovat herkkiä klavulaanihappoinhibitiolle. Tätä valmistetta ei pidä käyttää penisilliinille resistentin S. pneumoniae -kannan aiheuttamissa infektioissa. Kouristuksia voi ilmetä munuaisten vajaatoimintaa sairastavilla tai suuria annoksia saavilla potilailla (ks. kohta 4.8). Amoksisilliiini-klavulaanihapon käyttöä tulee välttää, jos epäillään mononukleoosi-infektiota, koska sen yhteydessä on ilmennyt tuhkarokkoa muistuttavaa ihottumaa amoksisilliinia saaneilla potilailla. Allopurinolin samanaikainen käyttö amoksisilliinihoidon aikana voi lisätä allergisten ihoreaktioiden mahdollisuutta. Pitkäaikainen käyttö voi toisinaan aiheuttaa valmisteelle resistenttien mikrobien lisääntymistä. Hoidon aloitusvaiheessa esiintyvä kuumeinen yleistynyt eryteema, johon liittyy märkärakkuloita, saattaa olla oire akuutista yleistyneestä märkärakkulaisesta eksanteemasta (ks. kohta 4.8). Tämä reaktio vaatii Augmentin-hoidon lopettamista ja on jatkossa amoksisilliinihoidon vasta-aihe. Amoksisilliini-klavulaanihapon käytössä on noudatettava varovaisuutta, jos potilaalla on todettu merkkejä maksan vajaatoiminnasta (ks. kohdat 4.2, 4.3 ja 4.8). Maksaan kohdistuvia haittavaikutuksia on todettu pääasiassa miehillä ja iäkkäillä potilailla, ja ne saattavat liittyä pitkäaikaiseen hoitoon. Näitä tapahtumia on raportoitu hyvin harvoin lapsilla. Kaikissa väestöryhmissä oireet ja löydökset tulevat esiin yleensä hoidon aikana tai pian sen jälkeen, mutta joskus ne saattavat ilmaantua vasta useiden viikkojen kuluttua hoidon päättymisestä. Maksavaikutukset ovat yleensä korjaantuvia, mutta ne voivat olla vaikeita, ja erittäin harvoin on raportoitu kuolemantapauksia. Tällöin potilaalla on lähes aina ollut jokin vakava perussairaus tai muu samanaikainen lääkitys, jonka tiedetään voivan aiheuttaa maksavaikutuksia (ks. kohta 4.8). Antibiootteihin liittyvää koliittia on ilmoitettu melkein kaikkien antibakteeristen lääkkeiden, myös amoksisilliinin, käytön yhteydessä. Se voi vaihdella lievästä henkeä uhkaavaan (ks. kohta 4.8). Sen vuoksi tätä diagnoosia on tarkeää harkita potilailla, joilla ilmenee ripulia minkä tahansa antibiootihoidon aikana tai sen jälkeen. Jos antibioottihoitoon liittyvää koliittia esiintyy, amoksisilliini-klavulaanihappohoito on lopetettava heti, neuvoteltava lääkärin kanssa ja aloitettava asianmukainen hoito. Suolen peristaltiikkaa heikentävät lääkevalmisteet ovat vasta-aiheisia tässä tilanteessa. Pitkäkestoisen hoidon aikana on syytä seurata määräajoin elintoimintoja, mm. munuaisten, maksan ja hematopoieettisen järjestelmän toimintaa. Protrombiiniajan pidentymistä on ilmoitettu harvoin amoksisilliini-klavulaanihappoa saavilla potilailla. Samanaikaisesti antikoagulantteja käyttävien potilaiden tarpeellisesta seurannasta on huolehdittava. Peroraalisten antikoagulanttien annoksen muuttaminen saattaa olla tarpeen halutun antikoagulaatiotason säilyttämiseksi (ks. kohdat 4.5 ja 4.8). Potilailla, joilla on munuaisten vajaatoiminta, tulee annosta muuttaa vajaatoiminnan asteen mukaisesti (ks. kohta 4.2). Potilailla, joilla on pienentynyt virtsaneritys, on todettu hyvin harvoin kidevirtsaisuutta, pääasiassa parenteraalisen hoidon yhteydessä. Annettaessa suuria amoksisilliiniannoksia on syytä huolehtia riittävästä nesteen saannista ja virtsanerityksestä, jotta amoksisilliinin aiheuttamaa kidevirtsaisuuden 4
5 todennäköisyyttä voidaan pienentää. Potilailla, joilla on virtsakatetri, on säännöllisesti tarkistettava, ettei katetri ole tukkeutunut (ks. kohta 4.9). Kun amoksisilliinihoidon aikana tutkitaan virtsan glukoosia, tulisi käyttää entsymaattisia glukoosioksidaasimenetelmiä, koska vääriä positiivisia tuloksia saattaa esiintyä ei-entsymaattisilla menetelmillä. Augmentinissa oleva klavulaanihappo voi aiheuttaa IgG:n ja albumiinin ei-spesifisen sitoutumisen punasolujen kalvoille johtaen väärään positiiviseen Coombsin kokeeseen. Platelia Aspergillus EIA -menetelmällä (Bio-Rad Laboratories) on saatu positiivisia testituloksia amoksisilliini-klavulaanihappohoidon aikana, vaikka myöhemmin on todettu, ettei potilailla ole ollut Aspergillus -infektiota. Non-Aspergillus polysakkaridien ja polyfuranoosien ristireaktiota on raportoitu Platelia Aspergillus EIA -menetelmää (Bio-Rad Laboratories) käytettäessä. Siksi amoksisilliiniklavulaanihappohoitoa saavien potilaiden positiivisiin testituloksiin on suhtauduttava varauksella, ja ne on vahvistettava muilla diagnostisilla menetelmillä. 4.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset Oraaliset antikoagulantit Oraalisia antikoagulantteja ja penisilliiniantibiootteja on laajasti käytetty käytännössä ilman raportoituja interaktioita. Kuitenkin kirjallisuudesta löytyy tapauksia, joissa INR (International Normalized Ratio) on noussut potilailla, jotka käyttävät asenokumarolia tai varfariinia ja joille on määrätty amoksisilliinikuuri. Jos samanaikainen anto on välttämätöntä, protrombiiniaikaa tai INR-arvoa on tarkoin seurattava, kun hoitoon lisätään tai siitä poistetaan amoksisilliini. Lisäksi peroraalisten antikoagulanttien annoksen muuttaminen saattaa olla tarpeen (ks. kohdat 4.4 ja 4.8). Metotreksaatti Penisilliinit saattavat vähentää metotreksaatin erittymistä, mistä aiheutuu mahdollinen toksisuuden lisääntyminen. Probenesidi Probenesidin samanaikaista käyttöä ei suositella. Probenesidi vähentää amoksisilliinin erittymistä munuaistubulusten kautta. Amoksisilliinin, mutta ei klavulaanihapon, pitoisuus veressä voi suurentua ja pitkittyä probenesidin samanaikaisen käytön seurauksena. Mykofenolaattimofetiili Mykofenolaattimofetiilia saavilla potilailla on raportoitu mykofenolaattimofetiilin aktiivisen metaboliitin, mykofenolihapon (MPA), annosta edeltävän pitoisuuden pienenemistä noin 50 %:lla oraalisen amoksisilliini-klavulaanihappo yhdistelmän aloittamisen jälkeen. Annosta edeltävän pitoisuuden muutokset eivät välttämättä kuvasta tarkasti MPA:n kokonaisaltistuksessa tapahtuvaa muutosta. Tästä johtuen mykofenolaattimofetiilin annoksen muuttamisen ei yleensä pitäisi olla tarpeen ellei kliinistä osoitusta siirteen vajaatoiminnasta ole. Kuitenkin tarkka kliinien seuranta on tarpeen antibioottihoidon aikana ja lyhyen aikaa sen jälkeen. 5
6 4.6 Hedelmällisyys, raskaus ja imetys Raskaus Eläinkokeet eivät ole osoittaneet suoraa tai epäsuoraa vahingollista vaikutusta raskauteen, alkion/sikiönkehitykseen, synnytykseen eikä postnataaliseen kehitykseen (ks. kohta 5.3). Rajalliset tiedot amoksisilliini-klavulaanihapon raskaudenaikaisesta käytöstä eivät viittaa synnynnäisten epämuodostumien vaaran suurenemiseen. Yhdessä tutkimuksessa naisilla, joilla oli todettu ennennaikainen sikiökalvojen repeytyminen raportoitiin, että profylaktiseen amoksisilliiniklavulaanihappohoitoon saattaa vastasyntyneillä liittyä lisääntynyt nekrotisoivan enterokoliitin vaara. Käyttöä tulee välttää raskauden aikana, ellei hoitava lääkäri pidä sitä välttämättömänä. Imetys Molemmat vaikuttavat aineet erittyvät rintamaitoon (klavulaanihapon vaikutuksia imetettävään lapseen ei tunneta). Näin ollen imetettävän lapsen ripuli ja limakalvojen sieni-infektio ovat mahdollisia, joten imetys täytyy mahdollisesti lopettaa. Herkistymisen mahdollisuus pitäisi ottaa huomioon. Amoksisilliiniklavulaanihappoa tulee käyttää imetyksen aikana ainoastaan lääkärin tekemän hyöty/riski-arvion jälkeen. 4.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn Tutkimuksia valmisteen vaikutuksesta ajokykyyn tai koneiden käyttökykyyn ei ole tehty. Sellaisia haittavaikutuksia voi kuitenkin esiintyä (esim. allergisia reaktioita, huimausta, kouristuksia), jotka voivat vaikuttaa ajokykyyn tai kykyyn käyttää koneita (ks. kohta 4.8). 4.8 Haittavaikutukset Yleisimmin raportoidut haittavaikutukset ovat ripuli, pahoinvointi ja oksentelu. Alla luetellaan Augmentinin kliinisissä tutkimuksissa ja markkinoille tulon jälkeisessä seurannassa esiin tulleet haittavaikutukset elinryhmittäin MedDRA-luokituksen mukaan. Seuraavia termejä on käytetty haittavaikutusten esiintymistiheyden luokittelussa: hyvin yleinen (1/10) yleinen (1/100, <1/10) melko harvinainen (1/1000, <1/100) harvinainen (1/10,000, <1/1000) hyvin harvinainen (<1/10,000) tuntematon (koska saatavissa oleva tieto ei riitä arviointiin) Infektiot Mukokutaaninen kandidiaasi Resistenttien mikrobien lisääntyminen Veri ja imukudos Korjautuva leukopenia (myös neutropenia) Trombosytopenia Korjautuva agranulosytoosi Hemolyyttinen anemia Vuotoajan ja protrombiiniajan pidentyminen 1 Yleinen Harvinainen Harvinainen Immuunijärjestelmä 10 6
7 Angioneuroottinen ödeema Anafylaksi Seerumisairauden kaltainen oireyhtymä Allerginen vaskuliitti Hermosto Huimaus Päänsärky Korjautuva hyperaktiivisuus Kouristukset 2 Aseptinen meningiitti Ruoansulatuselimistö Ripuli Pahoinvointi 3 Oksentelu Ruoansulatushäiriöt Antibioottihoidon yhteydessä esiintyvä suolitulehdus 4 Musta nukkainen kieli Maksa ja sappi ASAT- ja/tai ALAT-arvojen nousu 5 Hepatiitti 6 Kolestaattinen keltaisuus 6 Iho ja ihonalainen kudos 7 Ihottuma Kutina Urtikaria Erythema multiforme Stevens-Johnsonin oireyhtymä Toksinen epidermaalinen nekrolyysi Rakkulainen kesivä ihottuma Akuutti yleistynyt märkärakkulainen eksanteema 9 Melko harvinainen Melko harvinainen Hyvin yleinen Yleinen Yleinen Melko harvinainen Melko harvinainen Melko harvinainen Melko harvinainen Melko harvinainen Harvinainen Munuaiset ja virtsatiet Interstitiaalinefriitti Kidevirtsaisuus 8 1 Ks. kohta Ks. kohta Pahoinvointi liittyy useimmiten suuriin peroraalisiin annoksiin. Mahdollisia ruoansulatuskanavan reaktioita voidaan vähentää ottamalla amoksisilliini-klavulaanihappo aterian yhteydessä. 4 Mukaan lukien pseudomembranoottinen suolitulehdus ja vuotava suolitulehdus (ks. kohta 4.4) 5 Kohtalaista ASAT- ja/tai ALAT-arvojen nousua on todettu potilailla, joita on hoidettu beetalaktaamiantibiooteilla, mutta näiden löydösten merkitystä ei tunneta. 6 Näitä tapahtumia on todettu muilla penisilliineillä ja kefalosporiineilla (ks. kohta 4.4). 7 Jos yliherkkyyteen viittaavia ihoreaktioita esiintyy, hoito tulee lopettaa (ks. kohta 4.4). 8 Ks. kohta Ks. kohta Ks. kohta 4.3 ja 4.4 Epäillyistä haittavaikutuksista ilmoittaminen 7
8 On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteenhyöty-haitta tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle: www-sivusto: Lääkealan turvallisuus- ja kehittämiskeskus Fimea Lääkkeiden haittavaikutusrekisteri PL FIMEA 4.9 Yliannostus Yliannostuksen oireet ja merkit Yliannostukseen voi liittyä ruoansulatuskanavan oireita sekä neste- ja elektrolyyttitasapainon häiriöitä. Amoksisilliinista johtuvaa kidevirtsaisuutta, joka on joissakin tapauksissa johtanut munuaisten vajaatoimintaan, on todettu (ks. kohta 4.4 ). Kouristuksia voi ilmetä munuaisten vajaatoimintaa sairastavilla tai suuria annoksia saavilla potilailla. Amoksisilliinin on raportoitu saostuvan virtsakatetreihin, pääasiassa suurten laskimonsisäisten annosten jälkeen. On tarkistettava säännöllisesti, ettei katetri ole tukkeutunut (ks. kohta 4.4). Myrkytyksen hoito Gastrointestinaalioireet voidaan hoitaa oireenmukaisesti, kiinnittäen huomiota neste- ja elektrolyttitasapainoon. Amoksisilliini-klavulaanihappo voidaan poistaa verenkierrosta hemodialyysillä. 5. FARMAKOLOGISET OMINAISUUDET 5.1 Farmakodynamiikka Farmakoterapeuttinen ryhmä: Penisilliinien yhdistelmävalmisteet, mukaan lukien beetalaktamaasiinhibiittorit; ATC-koodi: J01CR02. Vaikutusmekanismi Amoksisilliini on puolisynteettinen penisilliini (beetalaktaamiantibiootti), joka ehkäisee yhtä tai useampaa entsyymiä (kutsutaan usein penisilliiniä sitoviksi proteiineiksi, PBP) bakteerin peptidoglykaanin biosynteesissä. Peptidoglykaani on bakteerin soluseinämän keskeinen rakenneosa. Peptidoglykaanin synteesin esto johtaa bakteerin soluseinämän heikkenemiseen, jota yleensä seuraa solun hajoaminen ja kuolema. Amoksisilliini on herkkä resistenttien bakteerien tuottamien beetalaktamaasien hajottavalle vaikutukselle, ja sen vuoksi amoksisilliinin vaikutuskirjo ei yksinään kata organismeja, jotka tuottavat näitä entsyymejä. Klavulaanihappo on beetalaktaami, joka on rakenteellisesti sukua penisilliinille. Se inaktivoi joitakin beetalaktamaasientsyymejä estäen siten amoksisilliinin inaktivaation. Klavulaanihapolla yksinään ei ole kliinisesti hyödyllistä antibakteerista tehoa. 8
9 Farmakokineettiset/farmakodynaamiset suhteet Aika, jona pitoisuus seerumissa pysyy MIC-arvon yläpuolella (T>MIC), on tärkeimpiä amoksisilliinin tehon mittareita. Resistenssimekanismit Kaksi pääasiallista resistenssimekanismia amoksisilliini-klavulaanihapolle: Inaktivaatio, jonka aiheuttaa sellaiset bakteeribeetalaktamaasit, joita klavulaanihappo ei inhiboi, mukaan lukien luokat B, C ja D. Penisilliiniä sitovien proteiinien muutokset, jotka vähentävät antibakteerisen lääkeaineen affiniteettia kohdekudokseen. Bakteerien läpäisemättömyys tai effluksipumppumekanismit voivat aiheuttaa tai myötävaikuttaa bakteerien resistenssiin erityisesti gram-negatiivisilla bakteereilla. Raja-arvot Amoksisilliini-klavulaanihapon MIC-raja-arvot ovat EUCAST:n (The European Committee on Antimicrobial Susceptibility Testing) antamia Mikro-organismi Raja-arvot (mikrog/ml) Herkkä Kohtalaisen herkkä Resistentti Haemophilus influenzae > 1 Moxarella catarrhalis > 1 Staphylococcus aureus Koagulaasi-negatiiviset 0,25 0,25 stafylokokit 2 Enterococcus Streptococcus A, B, C, G 5 0,25-0,25 Streptococcus pneumoniae 3 0, Enterobacteriaceae 1,4-8 Gram-negatiiviset anaerobit Gram-positiiviset anaerobit Lajeista riippumattomat rajaarvot Raportoidut arvot tarkoittavat amoksisilliinipitoisuuksia. Herkkyystestejä varten klavulaanihappopitoisuus on vakioitu tasolle 2 mg/l. 2 Raportoidut arvot tarkoittavat oksasilliinipitoisuuksia. 3 Taulukon raja-arvot perustuvat ampisilliinin raja-arvoihin. 4 Resistenttiyden raja-arvo R>8 mg/l varmistaa, että kaikki kannat, joilla on resistenssimekanismeja raportoidaan resistenteiksi. 5 Taulukon raja-arvot perustuvat bentsyylipenisilliinin raja-arvoihin. Joidenkin lajien resistenssin esiintyvyys saattaa vaihdella maantieteellisesti ja ajallisesti, joten paikallinen tietous resistenssistä on toivottavaa, etenkin silloin kun hoidetaan vaikeita infektioita. Tarpeen mukaan 9
10 on syytä hakea asiantuntijan neuvoa silloin kun paikallinen resistenssi on sellainen, että lääkkeen teho on ainakin joihinkin infektioihin kyseenalainen. Yleisesti herkät lajit Gram-positiiviset aerobiset mikro-organismit Enterococcus faecalis Gardnerella vaginalis Staphylococcus aureus (metisilliinille herkkä) koagulaasinegatiiviset stafylokokit (metisilliinille herkät) Streptococcus agalactiae Streptococcus pneumoniae 1 Streptococcus pyogenes ja muut beetahemolyyttiset streptokokit Streptococcus viridans ryhmä Gram-negatiiviset aerobiset mikro-organismit Capnocytophaga spp. Eikenella corrodens Haemophilus influenzae 2 Moxarella catarrhalis Pasteurella multocida Anaerobiset mikro-organismit Bacteroides fragilis Fusobacterium nucleatum Prevotella spp. Lajit, joiden hankittu resistenssi saattaa aiheuttaa ongelmia Gram-positiiviset aerobiset mikro-organismit Enterococcus faecium $ Gram-negatiiviset aerobiset mikro-organismit Escherichia coli Klebsiella oxytoca Klebsiella pneumoniae Proteus mirabilis Proteus vulgaris Luonnostaan resistentit mikro-organismit Gram-negatiiviset aerobiset mikro-organismit Acinetobacter sp. Citrobacter freundii Enterobacter sp. Legionella pneumophila Morganella morganii Providencia spp. Pseudomonas sp. Serratia sp. Stenotrophomonas maltophilia Muut mikro-organismit Chlamydophila pneumoniae Chlamydophila psittaci Coxiella burnetti 10
11 Mycoplasma pneumoniae $ Luonnostaan kohtalainen herkkyys ilman hankittua resistenssimekanismia Kaikki metisilliinille resistentit stafylokokit ovat resistenttejä amoksisilliini-klavulaanihapolle. 1 Streptococcus pneumoniae -kantoja, jotka ovat resistenttejä penisilliinille, ei pidä hoitaa tällä amoksisilliini-klavulaanihappovalmisteella (ks. kohdat 4.2 ja 4.4). 2 Eräissä EU-maissa kantoja, joiden herkkyys on heikentynyt, on raportoitu esiintyvän yli 10 %. 5.2 Farmakokinetiikka Imeytyminen Amoksisilliini ja klavulaanihappo liukenevat täydellisesti vesiliuoksiin fysiologisessa ph:ssa. Molemmat aineet imeytyvät nopeasti ja hyvin suun kautta annettaessa. Suun kautta annettaessa amoksisilliinin ja klavulaanihapon biologinen hyötyosuus on noin 70 %. Molempien komponenttien plasmaprofiilit ovat samanlaiset ja huippupitoisuuden saavuttamiseen kuluva aika (t max ) on molempien kohdalla noin yksi tunti. Farmakokineettiset tulokset tutkimuksesta, jossa amoksisilliini-klavulaanihappoa (875 mg/125 mg tabletit kaksi kertaa vuorokaudessa) annettiin paastotilanteessa terveille vapaaehtoisille, esitetään oheisessa taulukossa. Farmakokineettiset parametrit, keskiarvo ( SD) Annettu vaikuttava aine Annos C max t max * AUC (0-24 h) t ½ (mg) (mikrog/ml) (h) (mikrog.h/ml) (h) AMX/CA 875 mg/125 mg AMX/CA 875 mg/125 mg AMX amoksisilliini, CA - klavulaanihappo * Mediaani (vaihteluväli) Amoksisilliini ,64 1,50 2,78 (1,0 2,5) Klavulaanihappo 125 2,18 1,25 0,99 (1,0 2,0) 53,52 12,31 10,16 3,04 1,19 0,21 0,96 0,12 Amoksisilliini-klavulaanihappovalmisteella saavutetut amoksisilliini- ja klavulaanihappopitoisuudet seerumissa ovat samat kuin annettaessa pelkkää amoksisilliinia tai klavulaanihappoa suun kautta vastaavina annoksina. Jakautuminen Noin 25 % plasman koko klavulaanihappopitoisuudesta ja 18 % plasman koko amoksisilliinipitoisuudesta on sitoutuneena proteiiniin. Amoksisilliinin laskettu jakautumistilavuus on noin 0,3 0,4 l/kg ja klavulaanihapon noin 0,2 l/kg. Laskimonsisäisen annon jälkeen sekä amoksisilliinia että klavulaanihappoa on mitattu sappirakosta, vatsan kudoksista, ihosta, rasva- ja lihaskudoksesta, nivel- ja peritoneaalinesteestä, sapesta ja märkäeritteestä. Amoksisilliini ei jakaudu aivo-selkäydinnesteeseen riittävässä määrin. Eläinkokeissa ei ole havaittu kummankaan yhdisteen kertyvän merkittävästi mihinkään elimeen. Amoksisilliinia, kuten useimpia penisilliinejä, voidaan todeta rintamaidossa. Myös klavulaanihappoa voi esiintyä rintamaidossa hyvin vähäisinä määrinä (ks. kohta 4.6). 11
12 Sekä amoksisilliini että klavulaanihappo läpäisevät istukan (ks. kohta 4.6). Biotransformaatio Osa amoksisilliinista erittyy virtsaan inaktiivisena penisilloiinihappona määrinä, jotka vastaavat % alkuannoksesta. Suuri osa klavulaanihaposta metaboloituu ihmiselimistössä ja eliminoituu virtsan ja ulosteen mukana sekä uloshengityksen mukana hiilidioksidina. Eliminaatio Amoksisilliini eliminoituu pääasiassa munuaisten kautta, kun taas klavulaanihapon eliminoituminen noudattaa sekä munuaisista riippuvaa että riippumatonta mekanismia. Amoksisilliini-klavulaanihapon kskimääräinen eliminaation puoliintumisaika on yksi tunti ja keskimääräinen kokonaispuhdistuma noin 25 l/h terveillä henkilöillä. Noin % amoksisilliinista ja noin % klavulaanihaposta erittyy muuttumattomana virtsaan ensimmäisten kuuden tunnin kuluessa yhden 250/125 mg:n tai 500/125 mg:n Augmentin-tabletin kerta-annoksen jälkeen. Eri tutkimuksissa on todettu, että virtsaan erittyy 24 tunnin kuluessa % amoksisilliinista ja % klavulaanihaposta. Klavulaanihaposta suurin osa erittyy 2 ensimmäisen tunnin aikana lääkkeen annosta. Probenesidin samanaikainen anto pitkittää amoksisilliinin, mutta ei klavulaanihapon erittymistä munuaisten kautta (ks. kohta 4.5). Ikä Amoksisilliinin eliminaation puoliintumisaika on noin 3 kuukauden 2 vuoden ikäisillä lapsilla samanlainen kuin vanhemmilla lapsilla ja aikuisilla. Vastasyntyneiden lasten (myös ennenaikaisesti syntyneiden) ensimmäisen elinviikon aikana annostiheys ei saisi ylittää kahta kertaa vuorokaudessa munuaisista riippuvan poistumisreitin kypsymättömyyden vuoksi. Koska iäkkäillä potilailla on todennäköisemmin heikentynyt munuaistoiminta, annoksen valinnassa on noudatettava varovaisuutta. Munuaistoiminnan seuranta saattaa myös olla hyödyllistä. Sukupuoli Annettaessa amoksisilliini-klavulaanihappoa suun kautta terveille miehille ja naisille sukupuolella ei ole merkittävää vaikutusta amoksisilliinin eikä klavulaanihapon farmakokinetiikkaan. Munuaisten vajaatoiminta Amoksisilliini-klavulaanihapon kokonaispuhdistuma seerumista pienenee samassa suhteessa kuin munuaistoiminta heikkenee. Lääkkeen puhdistuman pienentyminen on huomattavampaa amoksisilliinin kuin klavulaanihapon osalta, koska suurempi osa amoksisilliinista erittyy munuaisten kautta. Kun harkitaan annosta potilaille, joiden munuaistoiminta on heikentynyt, on vältettävä amoksisilliinin kumuloitumista, mutta turvattava riittävät klavulaanihappopitoisuudet (ks. kohta 4.2). Maksan vajaatoiminta Maksan vajaatoimintaa sairastaville potilaille on annettava lääkevalmistetta varoen, ja maksan toimintaa tulee seurata säännöllisin väliajoin. 12
13 5.3 Prekliiniset tiedot turvallisuudesta Farmakologista turvallisuutta, geenitoksisuutta sekä reproduktiotoksisuutta koskevien tutkimusten eikliiniset tiedot eivät viittaa erityiseen vaaraan ihmisille. Amoksisilliini-klavulaanihapolla tehdyt toistuvan annostelun toksisuutta tarkastelevat tutkimukset koirilla osoittivat mahaärsytystä ja oksentelua sekä kielen värjäytymistä. Karsinogeenisuustutkimuksia ei ole tehty amoksisilliini-klavulaanihapolla eikä sen komponenteilla. 6. FARMASEUTTISET TIEDOT 6.1 Apuaineet Tabletin ydin Magnesiumstearaatti Natriumtärkkelysglykolaatti, tyyppi A Piidioksidi, kolloidinen, vedetön Mikrokiteinen selluloosa. Tabletin kalvopäällyste Titaanidioksidi (E171) Hypromelloosi Makrogoli (4000, 6000) Dimetikoni. 6.2 Yhteensopimattomuudet Ei oleellinen. 6.3 Kestoaika 2 vuotta. Kuivattavaa ainetta sisältäviin pusseihin pakatut tabletit tulee käyttää 30 päivän kuluessa avaamisesta. 6.4 Säilytys Säilytä alle 25 C. Säilytä alkuperäispakkauksessa. Herkkä kosteudelle. 6.5 Pakkaustyyppi ja pakkauskoko (pakkauskoot) PVC/Alumiini/Polyamidilaminaatti, jossa on alumiinipinnoite eli kylmämuovattu alumiiniläpipainopakkaus, jossa on 2, 4, 10,12, 14, 16, 20, 24, 30, 100 tai 500 tablettia. Alumiini PVC/PVdC läpipainopakkaus, joka on suljettu alumiinilaminaattipussin sisälle, joka sisältää kuivattavaa ainetta sisältävän pussin, eli kuivattavaa ainetta sisältävä pussipakkaus, jossa on 14 tablettia. Kaikkia pakkauskokoja ei välttämättä ole myynnissä. 13
14 6.6 Erityiset varotoimet hävittämiselle ja muut käsittelyohjeet Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti. 7. MYYNTILUVAN HALTIJA SmithKline Beecham Ltd. 980 Great West Road Brentford, Middlesex TW8 9GS Iso-Britannia 8. MYYNTILUVAN NUMERO(T) MYYNTILUVAN MYÖNTÄMISPÄIVÄMÄÄRÄ/UUDISTAMISPÄIVÄMÄÄRÄ Myyntiluvan myöntämisen päivämäärä: Viimeisimmän uudistamisen päivämäärä: TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
VALMISTEYHTEENVETO. 875 mg/125 mg: Amoksisilliinitrihydraatti, joka vastaa 875 mg amoksisilliinia ja kaliumklavulanaatti,
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion Comp 500 mg/125 mg tabletti, kalvopäällysteinen Amorion Comp 875 mg/125 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 500 mg/125
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion Comp 500 mg/125 mg tabletti, kalvopäällysteinen Amorion Comp 875 mg/125 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 500 mg/125
LIITE III VALMISTEYHTEENVETO, MYYNTIPÄÄLLYSMERKINNÄT JA PAKKAUSSELOSTE
 LIITE III VALMISTEYHTEENVETO, MYYNTIPÄÄLLYSMERKINNÄT JA PAKKAUSSELOSTE Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste olivat ajantasaisia komission päätöstä annettaessa. Komission
LIITE III VALMISTEYHTEENVETO, MYYNTIPÄÄLLYSMERKINNÄT JA PAKKAUSSELOSTE Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste olivat ajantasaisia komission päätöstä annettaessa. Komission
VALMISTEYHTEENVETO. Amoksisilliinitrihydraatti, joka vastaa 80 mg/ml amoksisilliinia ja kaliumklavulanaatti, joka vastaa 11,4 mg/ml klavulaanihappoa.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion Comp 80 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Amoksisilliinitrihydraatti, joka vastaa 80 mg/ml amoksisilliinia ja
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion Comp 80 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Amoksisilliinitrihydraatti, joka vastaa 80 mg/ml amoksisilliinia ja
VALMISTEYHTEENVETO. Augmentin on tarkoitettu seuraavien infektioiden hoitoon aikuisille ja lapsille (ks. kohdat 4.2, 4.4 ja 5.1):
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Augmentin Fruit 80/11,4 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista oraalisuspensiota sisältää
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Augmentin Fruit 80/11,4 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista oraalisuspensiota sisältää
Annokset ilmaistaan kauttaaltaan amoksisilliinina/klavulaanihappona paitsi silloin, kun annokset ilmoitetaan yksittäisinä komponentteina.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxin comp 50 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml käyttövalmista oraalisuspensiota (vast. 0,125 g jauhetta) sisältää:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxin comp 50 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml käyttövalmista oraalisuspensiota (vast. 0,125 g jauhetta) sisältää:
Yksi kalvopäällysteinen tabletti sisältää 500 mg amoksisilliinia (amoksisilliinitrihydraattina) ja 125 mg klavulaanihappoa (kaliumklavulanaattina).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Betaklav 500 mg/125 mg kalvopäällysteiset tabletit Betaklav 875 mg/125 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Betaklav 500 mg/125
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Betaklav 500 mg/125 mg kalvopäällysteiset tabletit Betaklav 875 mg/125 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Betaklav 500 mg/125
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI SYNULOX vet 40 mg/10 mg tabletti, koiralle ja kissalle SYNULOX vet 200 mg/50 mg tabletti, koiralle ja kissalle SYNULOX vet 400 mg/100 mg tabletti, koiralle 2. LAADULLINEN
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI SYNULOX vet 40 mg/10 mg tabletti, koiralle ja kissalle SYNULOX vet 200 mg/50 mg tabletti, koiralle ja kissalle SYNULOX vet 400 mg/100 mg tabletti, koiralle 2. LAADULLINEN
CLAVUBACTIN 50/12,5 mg tabletti koirille ja kissoille. 500/125 mg tabletti koirille Amoksisilliini
 1. ELÄINLÄÄKKEEN NIMI CLAVUBACTIN 50/12,5 mg tabletti koirille ja kissoille CLAVUBACTIN 250/62,5 mg tabletti koirille CLAVUBACTIN 500/125 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat
1. ELÄINLÄÄKKEEN NIMI CLAVUBACTIN 50/12,5 mg tabletti koirille ja kissoille CLAVUBACTIN 250/62,5 mg tabletti koirille CLAVUBACTIN 500/125 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat
VALMISTEYHTEENVETO. 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg jauhe oraalisuspensiota varten, annospussi 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg jauhe oraalisuspensiota varten, annospussi 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita,
VALMISTEYHTEENVETO. Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia, joka vastaa 2,68 mg bentsydamiinia.
 1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
VALMISTEYHTEENVETO. Yksi tabletti sisältää amoksisilliinitrihydraattia vastaten amoksisilliinia 375 mg, 500 mg tai 750 mg.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion 375 mg tabletti, kalvopäällysteinen Amorion 500 mg tabletti, kalvopäällysteinen Amorion 750 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion 375 mg tabletti, kalvopäällysteinen Amorion 500 mg tabletti, kalvopäällysteinen Amorion 750 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN
VALMISTEYHTEENVETO. Aikuiset (myös iäkkäät): Suositeltu annos on 800 mg eli 2 kapselia vuorokaudessa kerta-annoksena kolmen kuukauden ajan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745. Apuaineet,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745. Apuaineet,
VALMISTE YHT E ENVET O
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
VALMISTEYHTEENVETO. Mesillinaamille herkkien gramnegatiivisten bakteerien aiheuttamat virtsatieinfektiot.
 1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Selexid 200 mg tabletti, kalvopäällysteinen Selexid 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti
1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Selexid 200 mg tabletti, kalvopäällysteinen Selexid 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fusidic Acid Orifarm 20 mg/g, emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää fusidiinihappoa hemihydraattina, joka vastaa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fusidic Acid Orifarm 20 mg/g, emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää fusidiinihappoa hemihydraattina, joka vastaa
VALMISTEYHTEENVETO. Tabletti. Vaaleanpunainen, pyöreä tabletti, toisella puolella jakouurre, toisella puolella painettu numero 500.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amoxiclav vet 400 mg/100 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina) Klavulaanihappo
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amoxiclav vet 400 mg/100 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina) Klavulaanihappo
1. LÄÄKEVALMISTEEN NIMI. Lyngonia kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 1. LÄÄKEVALMISTEEN NIMI Lyngonia kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää: 361-509 mg Arctostaphylos uva-ursi (L.) Spreng. folium (sianpuolukan
1. LÄÄKEVALMISTEEN NIMI Lyngonia kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää: 361-509 mg Arctostaphylos uva-ursi (L.) Spreng. folium (sianpuolukan
VALMISTEYHTEENVETO. Yksi millilitra käyttövalmista oraalisuspensiota sisältää amoksisilliinitrihydraattia vastaten amoksisilliinia 50 mg.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amovet vet 50 mg/ml jauhe oraalisuspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi millilitra käyttövalmista oraalisuspensiota sisältää
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amovet vet 50 mg/ml jauhe oraalisuspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi millilitra käyttövalmista oraalisuspensiota sisältää
VALMISTEYHTEENVETO. Valmistetta ei saa antaa kanille, marsulle, hamsterille, gerbiilille eikä muille pienille jyrsijöille.
 1. ELÄINLÄÄKKEEN NIMI Amovet vet 150 mg/ml injektioneste, suspensio VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Amoksisilliinitrihydraatti (172,1 mg) vastaten
1. ELÄINLÄÄKKEEN NIMI Amovet vet 150 mg/ml injektioneste, suspensio VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Amoksisilliinitrihydraatti (172,1 mg) vastaten
Vaaleankeltainen, opalisoiva piparmintun tuoksuinen ja makuinen suspensio.
 1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
VALMISTEYHTEENVETO. Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia 20 mg (2 %).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
VALMISTEYHTEENVETO. Yksi kalvopäällysteinen tabletti sisältää amoksisilliinitrihydraattia määrän, joka vastaa 750 mg amoksisilliinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxicillin Mylan 750 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää amoksisilliinitrihydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxicillin Mylan 750 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää amoksisilliinitrihydraattia
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO. Vaikuttava aine: Kefaleksiini (kefaleksiinimonohydraattina)
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Tsefalen 1000 mg tabletti, kalvopäällysteinen koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi kalvopäällysteinen tabletti sisältää: Vaikuttava aine: Kefaleksiini
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Tsefalen 1000 mg tabletti, kalvopäällysteinen koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi kalvopäällysteinen tabletti sisältää: Vaikuttava aine: Kefaleksiini
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. Amoxiclav vet 40 mg/10 mg tabletti kissalle ja koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amoxiclav vet 40 mg/10 mg tabletti kissalle ja koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina)
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Amoxiclav vet 40 mg/10 mg tabletti kissalle ja koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina)
1. ELÄINLÄÄKKEEN NIMI. Amoxibactin vet 250 mg tabletit koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Amoxibactin vet 250 mg tabletit koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 tabletti sisältää: Vaikuttava aine: Amoksisilliini 250 mg (vastaa 287,50 mg:aa amoksisilliinitrihydraattia)
1. ELÄINLÄÄKKEEN NIMI Amoxibactin vet 250 mg tabletit koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 tabletti sisältää: Vaikuttava aine: Amoksisilliini 250 mg (vastaa 287,50 mg:aa amoksisilliinitrihydraattia)
VALMISTEYHTEENVETO. Akrivastiinia ei pidä määrätä potilaille, joiden munuaistoiminta on merkittävästi heikentynyt.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO. Apuaine, jonka vaikutus tunnetaan: aspartaami 1,7 mg/ml oraalisuspensiota.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion 50 mg/ml jauhe oraalisuspensiota varten Amorion 100 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amorion 50 mg/ml jauhe oraalisuspensiota varten Amorion 100 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista
VALMISTEYHTEENVETO. Bakteerilääkkeiden tarkoituksenmukaista käyttöä koskevat viralliset ohjeet on otettava huomioon.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxicillin MIP Pharma 500 mg tabletit Amoxicillin MIP Pharma 1000 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää amoksisilliinitrihydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxicillin MIP Pharma 500 mg tabletit Amoxicillin MIP Pharma 1000 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää amoksisilliinitrihydraattia
VALMISTEYHTEENVETO. Huom. Emätinpuikko tulee työntää syvälle emättimeen, ei mielellään kuukautisten aikana.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.1 Käyttöaiheet. 4.2 Annostus ja antotapa
 1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
Bakteerilääkkeiden asianmukaista käyttöä koskevat viranomaisohjeet tulee ottaa huomioon.
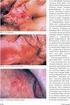 1. LÄÄKEVALMISTEEN NIMI Bioclavid 500 mg/125 mg kalvopäällysteinen tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää: Amoksisilliinia 500,00 mg vastaten 574 mg amoksisilliinitrihydraattia
1. LÄÄKEVALMISTEEN NIMI Bioclavid 500 mg/125 mg kalvopäällysteinen tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää: Amoksisilliinia 500,00 mg vastaten 574 mg amoksisilliinitrihydraattia
VALMISTEYHTEENVETO. Valmisteen kuvaus: pyöreä, merkintä BEPANTHEN kehässä, halkaisija n. 18 mm, paksuus n. 3,5 mm, harmaankeltainen, sitruunan tuoksu.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Penisilliiniyliherkkyys. Ei sovi kaneille, marsuille, hamstereille tai muille pikkujyrsijöille.
 1. ELÄINLÄÄKKEEN NIMI VALMISTEYHTEENVETO Synulox vet 40 mg/ml jauhe oraalisuspensiota varten koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliinitrihydraatti
1. ELÄINLÄÄKKEEN NIMI VALMISTEYHTEENVETO Synulox vet 40 mg/ml jauhe oraalisuspensiota varten koiralle ja kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliinitrihydraatti
VALMISTEYHTEENVETO. Tabletit ovat pyöreitä, harmaansinisiä ja sokeripäällysteisiä, halkaisija n. 11 mm.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
LIITE VALMISTEYHTEENVETO
 LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
Histadin- valmisteen tehoa ja turvallisuutta ei ole osoitettu alle 2-vuotiailla lapsilla.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO. Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia vastaten 1,5 g glukosamiinisulfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
1. ELÄINLÄÄKKEEN NIMI. AMOXIVAL VET 200 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Vaikuttava aine:
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI AMOXIVAL VET 200 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Amoksisilliini... 200,00 mg Vastaten amoksisilliinitrihydraattia...
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI AMOXIVAL VET 200 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Amoksisilliini... 200,00 mg Vastaten amoksisilliinitrihydraattia...
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. XEDEN vet 50 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI XEDEN vet 50 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää: Enrofloksasiini... 50,0 mg Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI XEDEN vet 50 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää: Enrofloksasiini... 50,0 mg Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. BiQi 3 g jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BiQi 3 g jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 3 grammaa diosmektiittiä. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BiQi 3 g jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 3 grammaa diosmektiittiä. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO. Ruiskeina annettavien jauheiden, konsentraattien ja liuosten liuottamiseen ja laimentamiseen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Fresenius Kabi 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9,0 mg/ml Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Fresenius Kabi 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9,0 mg/ml Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI V-penisilliini ratiopharm 1000 1 milj. IU tabletti, kalvopäällysteinen V-penisilliini ratiopharm 1500 1,5 milj. IU tabletti, kalvopäällysteinen 2. VAIKUTTAVAT
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI V-penisilliini ratiopharm 1000 1 milj. IU tabletti, kalvopäällysteinen V-penisilliini ratiopharm 1500 1,5 milj. IU tabletti, kalvopäällysteinen 2. VAIKUTTAVAT
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. CLAVUBACTIN 500/125 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Vaikuttavat aineet:
 1. ELÄINLÄÄKKEEN NIMI CLAVUBACTIN 500/125 mg tabletti koirille VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina) Klavulaanihappo
1. ELÄINLÄÄKKEEN NIMI CLAVUBACTIN 500/125 mg tabletti koirille VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Amoksisilliini (amoksisilliinitrihydraattina) Klavulaanihappo
Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Basiron AC 5 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Basiron AC 5 % geeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi g sisältää bentsoyyliperoksidia, vesipitoinen, vastaten vedetöntä bentsoyyliperoksidia 50 mg.
VALMISTEYHTEENVETO. Yksi gramma emulsiovoidetta sisältää: 21,5 mg mupirosiinikalsiumia vastaten 20,0 mg mupirosiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bactroban 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää: 21,5 mg mupirosiinikalsiumia vastaten 20,0 mg mupirosiinia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bactroban 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää: 21,5 mg mupirosiinikalsiumia vastaten 20,0 mg mupirosiinia.
VALMISTEYHTEENVETO. Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml. Valmisteen kuvaus: miedosti tuoksuva, väritön tai hieman kellertävä liuos
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
VALMISTEYHTEENVETO. Vaaleanpunainen pyöreä tabletti, jonka toisella puolella on jakouurre ja toisella merkintä 500.
 1. ELÄINLÄÄKKEEN NIMI CLAMOVET 400 mg/100 mg tabletti koiralle VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: 1 tabletti sisältää amoksisilliinitrihydraattia 459 mg, joka
1. ELÄINLÄÄKKEEN NIMI CLAMOVET 400 mg/100 mg tabletti koiralle VALMISTEYHTEENVETO 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: 1 tabletti sisältää amoksisilliinitrihydraattia 459 mg, joka
Carepen vet 600 mg intramammaarisuspensio lypsävälle lehmälle.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Carepen vet 600 mg intramammaarisuspensio lypsävälle lehmälle. 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ruiskullinen (= 10 g) valmistetta sisältää: Vaikuttava
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Carepen vet 600 mg intramammaarisuspensio lypsävälle lehmälle. 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ruiskullinen (= 10 g) valmistetta sisältää: Vaikuttava
VALMISTEYHTEENVETO. Yli 33 kg painavat lapset (noin 11-vuotiaat), alle 50 kg painavat nuoret ja aikuiset:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO. Lievän tai kohtalaisen vaikean polven nivelrikon oireiden lievittäminen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Metronidatsoli 0,75 paino-%, 7,5 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO. Yliherkkyys vaikuttavalle aineelle, muille imidatsolijohdoksille tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 20 mg mikonatsolinitraattia. Apuaineet, joiden vaikutus
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 20 mg mikonatsolinitraattia. Apuaineet, joiden vaikutus
VALMISTEYHTEENVETO. Neste- ja elektrolyyttihukka esim. leikkauksen, trauman tai palovammojen yhteydessä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ringer-acetat Fresenius Kabi, infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml infuusionestettä sisältää: Natr. chlorid. 5,9 g Natr. acet.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ringer-acetat Fresenius Kabi, infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 000 ml infuusionestettä sisältää: Natr. chlorid. 5,9 g Natr. acet.
VALMISTEYHTEENVETO. Shampoo Viskoosi liuos, joka on väriltään kirkkaan oljenkeltainen tai vaaleanoranssi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO. Harmaapilkullinen, pyöreä, kuperapintainen tabletti, halkaisija 13 mm
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI CARBO MEDICINALIS 250 mg -tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Aktiivihiili, 250 mg Täydellinen apuaineluettelo, ks. kohta 6.1 3. LÄÄKEMUOTO Tabletti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI CARBO MEDICINALIS 250 mg -tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Aktiivihiili, 250 mg Täydellinen apuaineluettelo, ks. kohta 6.1 3. LÄÄKEMUOTO Tabletti
VALMISTEYHTEENVETO. Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä penisilliineille, kefalosporiineille tai apuaineille.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI KEFAVET VET 50 mg/ml rakeet oraalisuspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Kefaleksiinimonohydraatti vastaten
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI KEFAVET VET 50 mg/ml rakeet oraalisuspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava aine: Kefaleksiinimonohydraatti vastaten
VALMISTEYHTEENVETO. Kapseli, kova Valmisteen kuvaus: Kapseli on valkoinen, merkintä 7658, halk 8 mm, pituus 21 mm.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Diclocil 500 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Dikloksasilliininatriummonohydraatti vastaten dikloksasilliiniä 500 mg Apuaineet, ks. 6.1.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Diclocil 500 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Dikloksasilliininatriummonohydraatti vastaten dikloksasilliiniä 500 mg Apuaineet, ks. 6.1.
1. ELÄINLÄÄKKEEN NIMI. Quiflox vet 80 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Yksi tabletti sisältää:
 1. ELÄINLÄÄKKEEN NIMI Quiflox vet 80 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: Vaikuttava aine: Marbofloksasiini.80 mg Apuaineet: Täydellinen apuaineluettelo,
1. ELÄINLÄÄKKEEN NIMI Quiflox vet 80 mg tabletti koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: Vaikuttava aine: Marbofloksasiini.80 mg Apuaineet: Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Ensisijaisesti ripulin ja ilmavaivojen hoito. Voidaan käyttää myös akuuttien lääkeaine- ja muiden myrkytysten ensiapuun.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Carbo Medicinalis 250 mg -tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 250 mg aktiivihiiltä. Apuaine, jonka vaikutus tunnetaan: 1 tabletti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Carbo Medicinalis 250 mg -tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 250 mg aktiivihiiltä. Apuaine, jonka vaikutus tunnetaan: 1 tabletti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Ginkgomax kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ginkgomax kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kaps.: Ginkgonis (Ginkgo biloba L., fol.) extr. aceton. sicc. raffinat. et quantificat. (35-45:1)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ginkgomax kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kaps.: Ginkgonis (Ginkgo biloba L., fol.) extr. aceton. sicc. raffinat. et quantificat. (35-45:1)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Dalacin 10 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dalacin 10 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg klindamysiiniä (klindamysiinifosfaattina). Täydellinen
1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dalacin 10 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg klindamysiiniä (klindamysiinifosfaattina). Täydellinen
Silmäinfektiot kuten keratiitti, konjunktiviitti, meibomiitti, blefariitti ym., jotka johtuvat fusidiinille herkistä bakteereista.
 1. LÄÄKEVALMISTEEN NIMI Fucithalmic 10 mg/g silmätipat 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma silmätippoja sisältää 10 mg fusidiinihappoa. Apuaine, jonka vaikutus tunnetaan: bentsalkoniumkloridi
1. LÄÄKEVALMISTEEN NIMI Fucithalmic 10 mg/g silmätipat 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma silmätippoja sisältää 10 mg fusidiinihappoa. Apuaine, jonka vaikutus tunnetaan: bentsalkoniumkloridi
VALMISTEYHTEENVETO. 1 g nenävoidetta sisältää mupirosiinikalsiumia vastaten 20 mg (2 % w/w) mupirosiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bactroban Nasal 2 % nenävoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 g nenävoidetta sisältää mupirosiinikalsiumia vastaten 20 mg (2 % w/w) mupirosiinia. Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bactroban Nasal 2 % nenävoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 g nenävoidetta sisältää mupirosiinikalsiumia vastaten 20 mg (2 % w/w) mupirosiinia. Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg karmelloosinatriumia. Yksi tippa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Celluvisc 1,0 % silmätipat, liuos kerta-annossäiliössä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra sisältää 10 mg karmelloosinatriumia. Yksi tippa
VALMISTEYHTEENVETO. Päänahan seborrooinen ekseema ja muu päänahan hilseily (pityriasis capitis). Pityriasis versicolor.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Yksi tabletti sisältää amoksisilliinitrihydraattia vastaten amoksisilliinia 500 mg. Apuaineet, ks. 6.1.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI AMORION 500 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää amoksisilliinitrihydraattia vastaten amoksisilliinia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI AMORION 500 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää amoksisilliinitrihydraattia vastaten amoksisilliinia
Vaaleankeltainen, opalisoiva piparmintun tuoksuinen ja makuinen suspensio.
 1. LÄÄKEVALMISTEEN NIMI Nystatin Orifarm 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet, joiden vaikutus tunnetaan: - metyyliparahydroksibentsoaatti
1. LÄÄKEVALMISTEEN NIMI Nystatin Orifarm 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet, joiden vaikutus tunnetaan: - metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO. Yksi tabletti sisältää natriumfluoridia määrän, joka vastaa 0,25 mg:aa fluoridia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fludent 0,25mg F- imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää natriumfluoridia määrän, joka vastaa 0,25 mg:aa fluoridia. Yksi
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fludent 0,25mg F- imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää natriumfluoridia määrän, joka vastaa 0,25 mg:aa fluoridia. Yksi
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Penomax 200 mg tabletti, kalvopäällysteinen Penomax 400 mg tabletti, kalvopäällysteinen
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Penomax 200 mg tabletti, kalvopäällysteinen Penomax 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää pivmesillinaamihydrokloridia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Penomax 200 mg tabletti, kalvopäällysteinen Penomax 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää pivmesillinaamihydrokloridia
Kissa: Leikkauksen jälkeisen kivun lievitys kohdun ja munasarjojen poistoleikkauksen sekä pienten pehmytkudoskirurgisten toimenpiteiden jälkeen.
 1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Amoxin comp 875 mg / 125 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxin comp 875 mg / 125 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää: Amoksisilliinitrihydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Amoxin comp 875 mg / 125 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää: Amoksisilliinitrihydraattia
VALMISTEYHTEENVETO. Valkoinen, pyöreä, kummaltakin puolelta litteä viistoreunainen tabletti, jossa jakouurre toisella puolella.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni. 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine:
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg kalsiumia. Täydellinen apuaineluettelo, ks. kohta 6.
 1. LÄÄKEVALMISTEEN NIMI Kalcipos 500 mg tabletti, kalvopäällysteinen VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg
1. LÄÄKEVALMISTEEN NIMI Kalcipos 500 mg tabletti, kalvopäällysteinen VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg
VALMISTEYHTEENVETO. Hiuspohja pestään Ketoconazol ratiopharm shampoolla, jonka annetaan vaikuttaa 3-5 minuutin ajan ennen huuhtelua.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
VALMISTEYHTEENVETO. Valmisteen kuvaus: Valkoinen tai melkein valkoinen talkkimainen jauhe.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Sisältää natriumia yhdessä injektiopullossa 33 mg (A-Pen 500 mg) ja 66 mg (A-Pen 1 g).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI A-Pen 500 mg injektio-/infuusiokuiva-aine, liuosta varten A-Pen 1 g injektio-/infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Injektio-/infuusiokuiva-aine,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI A-Pen 500 mg injektio-/infuusiokuiva-aine, liuosta varten A-Pen 1 g injektio-/infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Injektio-/infuusiokuiva-aine,
VALMISTEYHTEENVETO. Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112 mg feksofenadiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
VALMISTEYHTEENVETO. Kapseli, kova Norsunluunvalkoiset kapselit. Koko 2, sisältää valkoista rikinhajuista jauhetta.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hidrasec 100 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 100 mg rasekadotriilia. Apuaineet: Yksi kapseli sisältää 41 mg laktoosia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hidrasec 100 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 100 mg rasekadotriilia. Apuaineet: Yksi kapseli sisältää 41 mg laktoosia
1. LÄÄKEVALMISTEEN NIMI. Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg.
 1. LÄÄKEVALMISTEEN NIMI Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan: Yksi millilitra
1. LÄÄKEVALMISTEEN NIMI Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan: Yksi millilitra
1.3.1 Valmisteyhteenveto
 1.3.1 Valmisteyhteenveto 1 1. LÄÄKEVALMISTEEN NIMI Donaxyl 10 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 10 mg dekvaliniumkloridia. Täydellinen apuaineluettelo,
1.3.1 Valmisteyhteenveto 1 1. LÄÄKEVALMISTEEN NIMI Donaxyl 10 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 10 mg dekvaliniumkloridia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Penomax 200 mg kalvopäällysteiset tabletit Penomax 400 mg kalvopäällysteiset tabletit
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Penomax 200 mg kalvopäällysteiset tabletit Penomax 400 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää pivmesillinaamihydrokloridia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Penomax 200 mg kalvopäällysteiset tabletit Penomax 400 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää pivmesillinaamihydrokloridia
VALMISTEYHTEENVETO. Augmentin on tarkoitettu seuraavien infektioiden hoitoon aikuisille ja lapsille (ks. kohdat 4.2, 4.4 ja 5.1).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Augmentin 80/11,4 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista oraalisuspensiota sisältää amoksisilliinitrihydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Augmentin 80/11,4 mg/ml jauhe oraalisuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra käyttövalmista oraalisuspensiota sisältää amoksisilliinitrihydraattia
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI. THERIOS VET 750 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI THERIOS VET 750 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää: Kefaleksiini (kefaleksiinimonohydraattina)
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI THERIOS VET 750 mg tabletti koiralle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Yksi tabletti sisältää: Kefaleksiini (kefaleksiinimonohydraattina)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Galieve Peppermint purutabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Galieve Peppermint purutabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi purutabletti sisältää: Natriumalginaatti 250 mg Natriumvetykarbonaatti 133,5 mg Kalsiumkarbonaatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Galieve Peppermint purutabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi purutabletti sisältää: Natriumalginaatti 250 mg Natriumvetykarbonaatti 133,5 mg Kalsiumkarbonaatti
Silmäinfektiot, kuten keratiitti, konjunktiviitti, meibomiitti, blefariitti ym., jotka johtuvat fusidiinille herkistä bakteereista.
 1. LÄÄKEVALMISTEEN NIMI Fucithalmic 10 mg/g silmätipat, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma silmätippoja sisältää 10 mg fusidiinihappoa. Apuaine, jonka vaikutus tunnetaan: bentsalkoniumkloridi
1. LÄÄKEVALMISTEEN NIMI Fucithalmic 10 mg/g silmätipat, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma silmätippoja sisältää 10 mg fusidiinihappoa. Apuaine, jonka vaikutus tunnetaan: bentsalkoniumkloridi
VALMISTEYHTEENVETO 1/7 1. ELÄINLÄÄKEVALMISTEEN NIMI
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKEVALMISTEEN NIMI Clavaseptin 40 mg/10 mg tabletit koiralle ja kissalle Clavaseptin 50 mg/12,5 mg tabletit koiralle ja kissalle Clavaseptin 200 mg/50 mg tabletit koiralle
VALMISTEYHTEENVETO 1. ELÄINLÄÄKEVALMISTEEN NIMI Clavaseptin 40 mg/10 mg tabletit koiralle ja kissalle Clavaseptin 50 mg/12,5 mg tabletit koiralle ja kissalle Clavaseptin 200 mg/50 mg tabletit koiralle
PAKKAUSSELOSTE. Kesium vet 400 mg / 100 mg purutabletti koirille
 PAKKAUSSELOSTE Kesium vet 400 mg / 100 mg purutabletti koirille 1. MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI Myyntiluvan
PAKKAUSSELOSTE Kesium vet 400 mg / 100 mg purutabletti koirille 1. MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI Myyntiluvan
Jokainen ml sisältää 50 mg d-alfa-tokoferolia tokofersolaanin muodossa, vastaten 74,5 IU tokoferolia.
 1. LÄÄKEVALMISTEEN NIMI Vedrop 50 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml sisältää 50 mg d-alfa-tokoferolia tokofersolaanin muodossa, vastaten 74,5 IU tokoferolia. Apuaineet:
1. LÄÄKEVALMISTEEN NIMI Vedrop 50 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen ml sisältää 50 mg d-alfa-tokoferolia tokofersolaanin muodossa, vastaten 74,5 IU tokoferolia. Apuaineet:
VALMISTEYHTEENVETO. Kaikki hengitystiesairaudet, joissa esiintyy sitkeän liman kertymistä keuhkoputkiin.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bisolvon 8 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi 8 mg Apuaineet, joiden vaikutus tunnetaan: Yksi tabletti sisältää laktoosimonohydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bisolvon 8 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi 8 mg Apuaineet, joiden vaikutus tunnetaan: Yksi tabletti sisältää laktoosimonohydraattia
VALMISTEYHTEENVETO. Purutabletti Pitkänomainen, jakouurrettu, beige tabletti. Tabletti voidaan puolittaa kahteen yhtäsuureen osaan.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Kesium vet 50 mg / 12,5 mg purutabletti kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: Vaikuttavat aineet: Amoksisilliini
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Kesium vet 50 mg / 12,5 mg purutabletti kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi tabletti sisältää: Vaikuttavat aineet: Amoksisilliini
VALMISTEYHTEENVETO. Kroonisen ummetuksen hoito Kuivuneen, kovan ulostemassan (koprostaasin) pehmentäminen ja hajottaminen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ColonSoft jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra valmista oraaliliuosta sisältää Natriumkloridia 1,46 mg Vedetöntä
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ColonSoft jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra valmista oraaliliuosta sisältää Natriumkloridia 1,46 mg Vedetöntä
Yksi dispergoituva tabletti sisältää amoksisilliinitrihydraattia määrän, joka vastaa 750 mg amoksisilliinia.
 1. LÄÄKEVALMISTEEN NIMI Amoxicilin DSM Sinochem 750 mg dispergoituva tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi dispergoituva tabletti sisältää amoksisilliinitrihydraattia määrän, joka vastaa
1. LÄÄKEVALMISTEEN NIMI Amoxicilin DSM Sinochem 750 mg dispergoituva tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi dispergoituva tabletti sisältää amoksisilliinitrihydraattia määrän, joka vastaa
VALMISTEYHTEENVETO. Kaikki hengitystiesairaudet, joissa esiintyy sitkeän liman kertymistä keuhkoputkiin.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bisolvon 8 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi 8 mg Apuaineet, joiden vaikutus tunnetaan: Yksi tabletti sisältää laktoosimonohydraattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bisolvon 8 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi 8 mg Apuaineet, joiden vaikutus tunnetaan: Yksi tabletti sisältää laktoosimonohydraattia
