VALMISTEYHTEENVETO. Opaali, vaaleanpunainen, pitkänomainen (50 mg:n kapseli noin 20 x 8 mm), pehmeä liivatekapseli.
|
|
|
- Marjut Mäkelä
- 9 vuotta sitten
- Katselukertoja:
Transkriptio
1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 50 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää: 50 mg etoposidia. Apuaineet, joiden vaikutus tunnetaan: natriumetyyliparahydroksibentsoaatti (E215), natriumpropyyliparahydroksibentsoaatti (E217) Täydellinen apuaineluettelo, ks. kohta LÄÄKEMUOTO Kapseli, pehmeä Opaali, vaaleanpunainen, pitkänomainen (50 mg:n kapseli noin 20 x 8 mm), pehmeä liivatekapseli. 4. KLIINISET TIEDOT 4.1 Käyttöaiheet Keuhkokarsinooma: Pienisoluinen keuhkosyöpä tai okasolusyöpä. Alustavien tulosten mukaan etoposidilla voi olla tehoa myös muuta solutyyppiä olevaan keuhkokarsinoomaan. Akuutti leukemia: Nonlymfoblastinen leukemia, akuutti monosyyttileukemia, akuutti myelomonosyyttileukemia, akuutti myelooinen leukemia. Maligni lymfooma: Hodgkinin tauti, retikkelisolusarkooma, lymfosarkooma. Kivessyöpä: Yhdistelmähoitona muiden syöpälääkkeiden kanssa erityisesti potilailla, joiden kivessyöpä on aikaisemmasta kirurgisesta hoidosta, kemoterapiasta tai sädehoidosta huolimatta uusiutunut. 4.2 Annostus ja antotapa Annostus mg/m 2 päivässä viiden päivän ajan (päivät 1 5) tai 200 mg/m 2 päivässä kolmen päivän ajan (1, 3 ja 5) 3 4 viikon välein yhdistelmähoitona muiden sytostaattien kanssa. Vepesid-kapseleiden biologinen hyötyosuus minkä tahansa suuruisen oraalisen annoksen jälkeen vaihtelee potilaittain. Tämä on otettava huomioon lääkettä määrättäessä. Koska vaihtelu on merkittävää samallakin potilaalla, annosta on ehkä muutettava halutun hoitovaikutuksen saavuttamiseksi. Jos vuorokausiannos on yli 200 mg, on se annettava jaettuna (kahteen osa-annokseen päivässä). Antotapa Kapselit otetaan tyhjään mahaan. Annoksen muuttaminen 1
2 Annostusta on muutettava ottaen huomioon muiden samanaikaisesti annettavien lääkkeiden mahdolliset myelosuppressiiviset vaikutukset tai aiemmasta sädehoidosta tai kemoterapiasta johtuva luuydinreservin mahdollinen heikkeneminen. Potilaalle ei saa aloittaa uutta Vepesid-hoitokuuria, jos neutrofiilimäärä on alle solua/mm 3 tai verihiutalemäärä on alle solua/mm 3, paitsi jos tämä johtuu pahanlaatuisesta syövästä. Tavallisesti vaaditaan kolme tai neljä hoitokuuria ennen kuin etoposidihoidon tehoa voidaan arvioida. Lääkeannosta ja hoitokuurien lukumäärää voidaan lisätä tai vähentää luuytimen toiminnan tai hoitovasteen mukaan. Aloitusannoksen jälkeistä annosta on muutettava, jos neutrofiilimäärä on alle 500 solua/mm 3 yli viiden päivän ajan tai jos siihen liittyy kuumetta tai infektio; jos verihiutalemäärä on alle solua/mm 3 ; jos potilaalle kehittyy jokin muu luokan 3 tai 4 toksisuus tai jos munuaispuhdistuma on alle 50 ml/min. Heikentynyt munuaistoiminta Jos potilaan munuaistoiminta on heikentynyt, aloitusannoksen muuttamista on harkittava seuraavan kreatiniinipuhdistumaan perustuvan taulukon mukaisesti. Mitattu kreatiniinipuhdistuma Etoposidiannostus > 50 ml/min 100 % annoksesta ml/min 75 % annoksesta Aloitusannoksen jälkeisen annostuksen on perustuttava potilaan sietokykyyn ja kliiniseen vaikutukseen. Saatavilla ei ole tietoa potilaista, joiden kreatiniinipuhdistuma on < 15 ml/min; näille potilaille on harkittava annoksen pienentämistä vieläkin suuremmassa määrin. 4.3 Vasta-aiheet Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille. Keltakuumerokotetta tai muita eläviä taudinaiheuttajia sisältäviä rokotteita ei saa antaa immuunipuutteisille potilaille (ks. kohdat 4.4 ja 4.5). 4.4 Varoitukset ja käyttöön liittyvät varotoimet Vepesidiä saa antaa vain syövän kemoterapian antoon perehtyneen lääkärin valvonnassa. Potilaalla voi ilmetä vaikea myelosuppressio ja siihen liittyvä infektio tai verenvuoto. Etoposidin annon jälkeen on ilmoitettu kuolemaan johtanutta myelosuppressiota. Vepesid-hoitoa saavia potilaita on seurattava myelosuppression varalta tarkoin ja tiheään sekä ennen hoitoa että sen jälkeen. Vepesid-hoidon merkittävin annosta rajoittava toksisuus on myelosuppressio. Seuraavat tutkimukset on tehtävä hoitoa aloitettaessa ja sen jälkeen ennen jokaista Vepesid-annosta: verihiutalemäärä, hemoglobiini, valkosolumäärä ja erittelylaskenta. Jos potilas on saanut sädehoitoa tai kemoterapiaa ennen etoposidihoitoa, luuytimelle on annettava riittävästi toipumisaikaa ennen etoposidin antoa. Vepesidiä ei saa antaa potilaalle, jonka neutrofiilimäärä on alle solua/mm 3 tai verihiutalemäärä alle solua/mm 3, paitsi jos tämä johtuu pahanlaatuisesta syövästä. Leukosyytit on määritettävä ennen jokaista lääkekuuria. Hoidon aloittaminen edellyttää, että leukosyyttien määrä on normaali tai nousemassa. Mikäli leukosyyttien määrä on alle 2 x 10 9 /l etoposidihoidon aikana, hoito on keskeytettävä, kunnes leukosyyttien määrä on normaali, mikä tavallisesti tapahtuu 10 päivässä. Säännöllinen verenkuvan seuranta, mukaan lukien trombosyyttilaskenta, on välttämätön. Jos trombosyyttiarvo on < 50 x 10 9 /l tai neutrofiiliarvo < 0,5 x 10 9 /l, on hoito keskeytettävä, kunnes veriarvot ovat toipuneet riittävästi. Mikäli potilas on 2
3 saanut sädehoitoa tai muuta systostaattia ennen etoposidia, on muista hoidoista kuluneen ajan oltava riittävän pitkä luuytimen toipumiseen. Aloitusannoksen jälkeistä annosta on muutettava, jos neutrofiilimäärä on alle 500 solua/mm 3 yli 5 päivän ajan tai jos siihen liittyy kuumetta tai infektio; jos verihiutalemäärä on alle solua/mm 3 ; jos potilaalle kehittyy jokin muu luokan 3 tai 4 toksisuus tai jos munuaispuhdistuma on alle 50 ml/min. Annostusta on muutettava niin, että otetaan huomioon muiden yhdistelmähoidossa annettavien lääkkeiden myelosuppressiivinen vaikutus tai aiemmasta sädehoidosta tai kemoterapiasta johtuva luuydinreservin mahdollinen heikkeneminen. Etoposidia sisältävää kemoterapiaa saavilla potilailla on kuvattu akuutti leukemia, johon voi liittyä myelodysplastinen oireyhtymä. Kumulatiivinen kokonaisannostus (etoposidi > mg/m 2 ) suurentaa sekundaarisen akuutin nonlymfoblastisen leukemian riskiä. Kumulatiivista riskiä ja sekundaariselle leukemialle altistavia tekijöitä ei tunneta. Sekä etoposidin antoaikataulun että sen kumulatiivisten annosten on arveltu vaikuttavan asiaan mutta varmuutta tästä ei ole. Sekundaarista leukemiaa on raportoitu harvoin potilailla, joita on hoidettu etoposidilla yhdessä muiden antineoplastisten aineiden kanssa. Joillakin sekundaarista leukemiaa sairastaneilla ja epipodofyllotoksiineja saaneilla potilailla on todettu 11q23-kromosomipoikkeavuus. Sama poikkeavuus on todettu myös potilailla, joille sekundaarinen leukemia on kehittynyt epipodofyllotoksiineja sisältämättömän kemoterapian jälkeen tai de novo -leukemian jälkeen. Toinen piirre sekundaarisessa leukemiassa, jota ilmaantuu epipodofyllotoksiineja saaneille potilaille, näyttäisi olevan latenssivaiheen lyhyys: leukemia kehittyy keskimäärin (mediaani) noin 32 kuukaudessa. Anafylaktisissa reaktioissa, joissa on oireina vilunväreet, kuume, takykardia, bronkospasmi, dyspnea ja hypotensio ja jotka voivat olla kuolemaan johtavia, on lääkärin harkinnan mukaan keskeytettävä etoposidin anto ja aloitettava tarvittaessa oireenmukainen hoito verenpainetta nostavilla aineilla, kortikosteroideilla, antihistamiineilla tai plasmanlaajentajilla. Pahoinvointi ja oksentelu ovat yleensä hoidettavissa antiemeeteillä. Bakteeri-infektiot tulee olla hallinnassa ennen etoposidihoitoa. Varovaisuutta on noudatettava potilailla, joilla on munuaisten tai maksan vajaatoiminta. Harkittaessa Vepesidin käyttöä kemoterapiassa lääkärin on aina punnittava lääkkeen tarvetta ja hyödyllisyyttä haittavaikutusriskiä vasten. Suurin osa haittavaikutuksista korjaantuu, jos ne havaitaan varhain. Jos vaikeita reaktioita ilmenee, annosta on pienennettävä tai hoito lopetettava ja ryhdyttävä asianmukaisiin korjaaviin toimenpiteisiin lääkärin kliinisen arvioinnin mukaan. Vepesid-hoidon uudelleen aloittamisessa on oltava varovainen ja harkittava riittävän perusteellisesti lääkkeen käytön jatkamistarvetta. Potilasta on seurattava tarkoin toksisuuden mahdollisen uusiutumisen varalta. Jos seerumin albumiinimäärä on pieni, etoposidiin liittyvä toksisuusriski saattaa olla suurentunut. Jos potilaan munuaistoiminta on heikentynyt, munuaisten ja maksan toimintaa on seurattava säännöllisesti lääkkeen kertymisriskin vuoksi. Bakteeri-infektiot on saatava hallintaan ennen Vepesid-hoidon aloittamista. Koska etoposidi on mahdollisesti mutageeninen, sekä mies- että naispotilaiden on käytettävä luotettavaa ehkäisymenetelmää hoidon aikana ja 6 kuukauden ajan hoidon päättymisestä. Perinnöllisyysneuvontaa suositellaan, jos potilas haluaa hankkia lapsia hoidon jälkeen. Koska etoposidi voi heikentää miehen hedelmällisyyttä, lapsia myöhemmin haluava miespotilas voi harkita siittiöiden pakastamista (ks. kohta 4.6). Vepesid-valmisteen käyttö yhtä aikaa eläviä viruksia sisältävän rokotteen kanssa voi johtaa rokotevirusten replikoitumiseen ja/tai lisätä rokotevirusten aiheuttamia haittavaikutuksia, sillä Vepesid saattaa heikentää normaalia puolustusmekanismia. Vepesid-valmistetta käyttävien potilaiden 3
4 rokottaminen eläviä viruksia sisältävällä rokotteella voi johtaa vaikeaan infektioon. Potilaan vastaainevaste rokotteille voi olla heikentynyt. Eläviä viruksia sisältävien rokotteiden käyttöä tulee välttää ja yksittäisissä tapauksissa on konsultoitava erikoislääkäriä. Ks. kohdat 4.3 ja 4.5. Pediatriset potilaat Valmisteen turvallisuutta ja tehoa lapsilla ei ole tutkittu järjestelmällisesti. 4.5 Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset Oraalisen etoposidin kanssa otetut suuret siklosporiiniannokset, joista saatava pitoisuus on yli ng/ml, ovat suurentaneet etoposidialtistusta (AUC) 80 % ja pienentäneet etoposidin kokonaispuhdistumaa 38 % verrattuna pelkän etoposidin antoon. Samanaikaiseen sisplatiinihoitoon liittyy etoposidin kokonaispuhdistuman pienentyminen. Samanaikaiseen fenytoiinihoitoon liittyy etoposidipuhdistuman suureneminen ja tehon heikkeneminen. Samanaikaiseen muuhun epilepsialääkehoitoon voi liittyä etoposidin suurentunut puhdistuma ja heikentynyt teho. Vepesidin ja epilepsialääkkeiden samanaikainen anto voi johtaa heikentyneeseen kohtausten hallintaan johtuen lääkkeiden farmakokineettisistä yhteisvaikutuksista. Samanaikainen varfariinihoito voi suurentaa INR-arvoa (international normalized ratio). INR-arvon tarkkaa seurantaa suositellaan. Keltakuumerokotteeseen liittyy kuolemaan johtavan systeemisen rokotusoireyhtymän riskin suureneminen. Immuunipuutteisille potilaille ei saa antaa eläviä taudinaiheuttajia sisältäviä rokotteita. (Ks. kohdat 4.3 ja 4.4). Jos potilas on saanut aiemmin tai saa nyt samanaikaisesti etoposidin kanssa sellaisia muita lääkkeitä, joilla on etoposidin/etoposidifosfaatin kaltainen myelosuppressiivinen vaikutus, voi niillä olla additiivisia tai synergistisiä vaikutuksia (ks. kohta 4.4). Etoposidi sitoutuu plasman proteiineihin 97-prosenttisesti in vitro. Fenyylibutatsoni, natriumsalisylaatti ja asetyylisalisyylihappo saattavat syrjäyttää etoposidin plasman proteiineihin sitoutumisessa. Eläintutkimuksissa on raportoitu ristiresistenssiä antrasykliinien ja etoposidin välillä. 4.6 Hedelmällisyys, raskaus ja imetys Raskaus Etoposidin epäillään vaurioittavan sikiötä, jos sitä käytetään raskauden aikana. Vepesidiä ei pidä käyttää raskauden aikana ennen kuin äidille mahdollisesti koituva hyöty on punnittu suhteessa sikiölle koituvaan vaaraan. Vepesid on osoitettu teratogeeniseksi hiirille ja rotille. Ei ole olemassa tietoja tai on vain vähän tietoja etoposidin käytöstä raskaana oleville naisille. Hedelmällisessä iässä olevia naisia on kehotettava välttämään raskautta. Jos Vepesidin kaltaisia lääkkeitä käytetään raskaana olevalle tai jos potilas tulee raskaaksi niiden käytön aikana, potilaalle on kerrottava sikiölle mahdollisesti koituvasta vaarasta. Imetys Vepesid on vasta-aiheista rintaruokinnan aikana. Ei ole riittävästi tietoa, etoposidin erittymisestä ihmisen rintamaitoon. Koska monet lääkkeet erittyvät ihmisen rintamaitoon ja koska Vepesid voi aiheuttaa rintaruokintaa saaville imeväisille vakavia haittavaikutuksia, on päätettävä lopetetaanko rintaruokinta vai lopetetaanko Vepesid-hoito ottaen huomioon rintaruokinnasta aiheutuvat hyödyt lapselle ja hoidosta koituvat hyödyt äidille. 4
5 Hedelmällisyys Etoposidin mahdollisen mutageenisuuden vuoksi sekä mies- että naispotilaiden on käytettävä tehokasta ehkäisyä hoidon aikana ja 6 kuukauden ajan hoidon päättymisen jälkeen. Perinnöllisyysneuvontaa suositellaan, jos potilas haluaa hankkia lapsia hoidon jälkeen. Koska etoposidi voi heikentää miehen hedelmällisyyttä, lapsia myöhemmin haluava miespotilas voi harkita siittiöiden pakastamista. 4.7 Vaikutus ajokykyyn ja koneiden käyttökykyyn Tutkimuksia valmisteen vaikutuksesta ajokykyyn tai koneiden käyttökykyyn ei ole tehty. Jos potilaalla ilmenee haittavaikutuksia, kuten uupumusta ja uneliaisuutta, hänen on vältettävä autolla ajamista ja koneiden käyttämistä. 4.8 Haittavaikutukset Seuraavassa taulukossa on lueteltu haittatapahtumat elinjärjestelmittäin ja esiintymistiheyksittäin. Esiintymistiheyksien määritelmät ovat: hyvin yleiset ( 1/10); yleiset ( 1/100, < 1/10); melko harvinaiset ( 1/1 000, < 1/100); harvinaiset ( 1/10 000, < 1/1 000); hyvin harvinaiset (< 1/10 000) ja tuntematon (koska saatavilla oleva markkinoille tulon jälkeinen tieto ei riitä arviointiin). Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä. Taulukko 2. Etoposidilla ja etoposidifosfaatilla raportoidut lääkkeeseen liittyvät haittatapahtumat Hyvän- ja pahanlaatuiset kasvaimet (mukaan lukien kystat ja polyypit) Yleiset Akuutti leukemia, johon voi liittyä preleukeeminen vaihe, yhdistelmähoidossa muiden antineoplastisten lääkkeiden kanssa. Veri ja imukudos* Hyvin yleiset Myelosuppressio*, annoksesta riippuvainen leukopenia, neutropenia, trombosytopenia, anemia Immuunijärjestelmä Anafylaktistyyppiset reaktiot** Aineenvaihdunta ja ravitsemus Tuntematon Tuumorilyysioireyhtymä Hermosto Yleiset Heitehuimaus Melko harvinaiset Hyvin harvinaiset Perifeerinen neuropatia Kouristuskohtaus***, näköhermon tulehdus, ohimenevä kortikaalinen sokeus, neurotoksisuudet (esim. uneliaisuus, uupumus), pyörtyminen Parestesia Sydän Yleiset Sydäninfarkti, rytmihäiriöt Verisuonisto Yleiset Kohonnut verenpaine Hengityselimet, rintakehä ja välikarsina Keuhkofibroosi, interstitiaalinen pneumoniitti Ruoansulatuselimistö Hyvin yleiset Vatsakipu, ummetus, pahoinvointi ja oksentelu, ruokahaluttomuus 5
6 Yleiset Limakalvotulehdus (mukaan lukien suutulehdus ja ruokatorvitulehdus), ripuli Nielemishäiriö, makuhäiriö Maksa ja sappi Hyvin yleiset Hepaattinen toksisuus Hyvin harvinaiset Kohonneet maksaentsyymipitoisuudet Iho ja ihonalainen kudos Hyvin yleiset Korjaantuva hiustenlähtö, pigmentaatio Yleisoireet ja antopaikassa todettavat haitat Yleiset Hyvin yleiset Hyvin harvinaiset * Kuolemaan johtanutta myelosuppressiota on raportoitu. Ihottuma, nokkosihottuma, kutina, punoitus Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi, säteilyihottuma Voimattomuus, huonovointisuus Kuume, jälkimaku Apnea ** Anafylaktistyyppiset reaktiot voivat olla kuolemaan johtavia. *** Kouristuskohtauksiin liittyy toisinaan allergisia reaktioita. Seuraavissa kappaleissa mainittujen haittatapahtumien ilmaantuvuudet (ilmaistu keskiarvoprosentteina) perustuvat tutkimuksiin, joissa etoposidia/etoposidifosfaattia annettiin yksinään. Hematologinen toksisuus Etoposidin annon jälkeen on raportoitu kuolemaan johtanutta myelosuppressiota. Myelosuppressio on useimmiten annosta rajoittava. Luuydin toipuu yleensä täysin 20 päivässä, eikä kumulatiivista toksisuutta ole raportoitu. Granulosyytti- ja verihiutalearvot ovat yleensä pienimmillään noin päivää etoposidin tai etoposidifosfaatin annon jälkeen antotavasta tai hoito-ohjelmasta riippuen. Arvot laskevat pienimmilleen yleensä nopeammin laskimonsisäisessä kuin oraalisessa annossa. Etoposidia/etoposidifosfaattia saaneista potilaista %:lla todettiin leukopenia ja 7 17 %:lla vaikea leukopenia (alle solua/mm 3 ). Etoposidia/etoposidifosfaattia saaneista potilaista %:lla todettiin trombosytopenia ja 4 20 %:lla vaikea trombosytopenia (alle verihiutaletta/mm 3 ). Ilmoitusten mukaan myös kuume ja infektiot olivat hyvin yleisiä etoposidilla/etoposidifosfaatilla hoidetuilla potilailla, joilla oli neutropenia. Maha-suolikanavan toksisuus Etoposidin ja etoposidifosfaatin tärkeimmät maha-suolikanavaan kohdistuvat toksisuudet ovat pahoinvointi ja oksentelu. Ne saadaan yleensä hallintaan antiemeeteillä. Niitä on havaittu %:lla etoposidia laskimoon saaneista potilaista. Ruokahaluttomuutta on todettu %:lla ja suutulehdusta 1 6 %:lla etoposidia laskimoon saaneista potilaista. Ripulia on todettu 1 13 %:lla näistä potilaista. Hiustenlähtö Korjaantuvaa hiustenlähtöä, joka toisinaan etenee täydelliseksi kaljuudeksi, on todettu enimmillään 6
7 66 %:lla etoposidia saaneista potilaista. Verenpaineen muutokset Kohonnut verenpaine Etoposidin ja etoposidifosfaatin kliinisissä tutkimuksissa on raportoitu verenpaineen kohoamista. Jos etoposidia saavan potilaan verenpaine kohoaa kliinisesti merkittävästi, on aloitettava asianmukainen tukihoito. Allergiset reaktiot Etoposidin tai etoposidifosfaatin aloitusannoksen yhteydessä voi ilmetä anafylaktistyyppisiä reaktioita. Etoposidin käytön yhteydessä on raportoitu akuutteja, kuolemaan johtaneita reaktioita, joihin on liittynyt bronkospasmi. Etoposidifosfaattia saaneista potilaista 2 %:lla on raportoitu kasvojen punoitusta ja 3 %:lla ihottumia. Aineenvaihdunnan komplikaatiot Kun etoposidia on käytetty yhdessä muiden kemoterapia-aineiden kanssa, on raportoitu tuumorilyysioireyhtymä (toisinaan kuolemaan johtava). Epäillyistä haittavaikutuksista ilmoittaminen On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty haitta-tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle: www-sivusto: Lääkealan turvallisuus- ja kehittämiskeskus Fimea Lääkkeiden haittavaikutusrekisteri PL FIMEA 4.9 Yliannostus Kokonaisannokset 2,4 3,5 g/m 2 annettuna laskimoon kolmen päivän aikana ovat aiheuttaneet vaikeaa mukosiittia ja myelotoksisuutta. Metabolista asidoosia ja vakavaa hepaattista toksisuutta on raportoitu potilailla, jotka ovat saaneet suositeltuja annoksia suurempia annoksia. Spesifistä vastalääkettä ei ole. Siksi hoidon on oltava oireenmukaista ja elintoimintoja tukevaa ja potilasta on tarkkailtava tiiviisti. 5. FARMAKOLOGISET OMINAISUUDET 5.1 Farmakodynamiikka Farmakoterapeuttinen ryhmä: Kasvialkaloidit ja muut luonnontuotteet; podofyllotoksiinijohdokset, ATC-koodi: L01CB01 Etoposidi on podofyllotoksiinin puolisynteettinen johdos. Etoposidin päävaikutus näyttää olevan DNA:n kaksoisrihmakatkosten aiheuttaminen reaktiossa DNA-topoisomeraasi II:n kanssa, tai vapaiden radikaalien muodostumisen tuloksena. 5.2 Farmakokinetiikka Suun kautta otettavan kapselin keskimääräinen biologinen hyötyosuus on noin 50 % (25 75 %). 7
8 Vepesid-kapseliannos perustuu laskimoon annettavaan suositusannokseen, joka huomioi Vepesidkapselien annoksesta riippuvaisen biologisen hyötyosuuden. 100 mg:n oraalinen annos on verrattavissa 75 mg:n laskimonsisäiseen annokseen, ja 400 mg:n oraalinen annos on verrattavissa 200 mg:n laskimonsisäiseen annokseen. Laskimonsisäisen annostelun jälkeen plasmapitoisuus laskee kaksivaiheisena prosessina, jossa terminaalinen puoliintumisaika on 4 11 tuntia. Kokonaispuhdistuma on ml/min/m 2, ja kuten puoliintumisaika, se on annoksesta riippumaton alueella mg/m 2. Etoposidi ei kumuloidu plasmaan annettaessa 100 mg/m 2 päivässä 4 6 päivän ajan. Keskimääräinen jakautumistilavuus on 7-17 l/m 2. Etoposidi pääsee likvoriin huonosti. In vitro, etoposidi sitoutuu suuressa määrin ihmisen plasman proteiineihin (97 %). Tutkimuksessa, jossa selvitettiin muiden vaikuttavien aineiden vaikutuksia 14 C-etoposidin sitoutumiseen ihmisen seerumin proteiineihin in vitro, vain fenyylibutatsoni, natriumsalisylaatti ja asetyylisalisyylihappo syrjäyttivät proteiineihin sitoutuneen etoposidin pitoisuuksilla, jotka yleensä saavutetaan in vivo. Etoposidi poistuu elimistöstä siis sekä renaalisten että muiden prosessien kautta eli metaboloitumalla ja erittymällä sappeen. Annettaessa 3 H-etoposidia ( mg/m 2 ) laskimonsisäisesti keskimääräinen radioaktiivisuus virtsassa oli % ja ulosteessa 0 16 % annoksesta % annoksesta erittyi virtsaan muuttumattomana etoposidina 24 tunnin aikana. Etoposidin ei-renaalinen eliminaatio tapahtuu pääasiassa metaboloitumalla. Korkeintaan 6 % annoksesta erittyy sappeen. Pediatriset potilaat Lapsilla noin 55 % annoksesta erittyy virtsaan etoposidina 24 tunnissa. Munuaissairauden vaikutusta lapsen plasman etoposidipuhdistumaan ei tiedetä. Lapsilla suurentuneeseen ALAT-pitoisuuteen liittyy lääkkeen kokonaispuhdistuman pieneneminen. Lapsilla plasman albumiinipitoisuuden ja etoposidin munuaispuhdistuman välillä on käänteinen suhde. Lapsilla etoposidin kokonaispuhdistumaa elimistöstä voi pienentää myös aiempi sisplatiinin käyttö. Heikentynyt munuaistoiminta Etoposidia saavilla potilailla, joiden munuaistoiminta on heikentynyt, elimistön kokonaispuhdistuma on pienentynyt, AUC-arvo suurentunut ja vakaan tilan jakautumistilavuus suurentunut. 5.3 Prekliiniset tiedot turvallisuudesta Karsinogeenisuustutkimuksia etoposidilla ei ole tehty. Vaikutusmekanismin perusteella mahdolliset geenitoksiset ja karsinogeeniset vaikutukset ihmiseen tulee ottaa huomioon. 6. FARMASEUTTISET TIEDOT 6.1 Apuaineet Vedetön sitruunahappo Glyseroli 85 % Puhdistettu vesi Makrogoli 400 Liivate Natriumetyyliparahydroksibentsoaatti (E215) Natriumpropyyliparahydroksibentsoaatti (E217) Punainen rautaoksidi (E172) Titaanidioksidi (E171) 6.2 Yhteensopimattomuudet Ei oleellinen. 8
9 6.3 Kestoaika 3 vuotta. 6.4 Säilytys Säilytä alle 25 C. 6.5 Pakkaustyyppi ja pakkauskoko Läpipainopakkaus (PVC/Aclar ja alumiinifolio) 20 kapselia. 6.6 Erityiset varotoimet hävittämiselle ja muut käsittelyohjeet Solunsalpaajien ja sytostaattien käsittely- ja hävittämisohjeita on noudatettava. Solunsalpaajien käsittelyssä on aina noudatettava varovaisuutta. Altistuminen on pyrittävä estämään asianmukaisin toimenpitein. Näihin kuuluvat asianmukaiset suojavarusteet, kuten suojakäsineiden käyttö, sekä käsien peseminen saippualla ja vedellä tällaisten valmisteiden käsittelyn jälkeen. 7. MYYNTILUVAN HALTIJA Bristol-Myers Squibb AB Box Solna Ruotsi 8. MYYNTILUVAN NUMERO MYYNTILUVAN MYÖNTÄMISPÄIVÄMÄÄRÄ/UUDISTAMISPÄIVÄMÄÄRÄ Myyntiluvan myöntämisen päivämäärä: Viimeisimmän uudistamisen päivämäärä: TEKSTIN MUUTTAMISPÄIVÄMÄÄRÄ
VALMISTEYHTEENVETO. Opaali, vaaleanpunainen, pitkänomainen (50 mg:n kapseli noin 20 x 8 mm), pehmeä liivatekapseli.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 50 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää: 50 mg etoposidia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 50 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää: 50 mg etoposidia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Malignit lymfooma:. Hodgkinin tauti, retikkelisolusarkooma, lymfosarkooma.
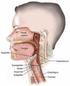 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 20 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidi 20 mg/ml Apuaineet, ks 6.1 3. LÄÄKEMUOTO Infuusiokonsentraatti,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Vepesid 20 mg/ml infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidi 20 mg/ml Apuaineet, ks 6.1 3. LÄÄKEMUOTO Infuusiokonsentraatti,
VALMISTEYHTEENVETO. Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia vastaten 1,5 g glukosamiinisulfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Orifarm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää glukosamiinisulfaattinatriumkloridikompleksia
VALMISTEYHTEENVETO. Lievän tai kohtalaisen vaikean polven nivelrikon oireiden lievittäminen.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin ratiopharm 1,5 g jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää 1,5 g glukosamiinisulfaattia glukosamiinisulfaattinatriumkloridina
VALMISTEYHTEENVETO. Aikuiset (myös iäkkäät): Suositeltu annos on 800 mg eli 2 kapselia vuorokaudessa kerta-annoksena kolmen kuukauden ajan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Chondroitin Sulphate Rovi 400 mg, kovat kapselit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiinisulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
Hoito: Yksilöllinen annos, joka säädetään seerumin kaliumarvojen mukaan.
 1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
1. LÄÄKEVALMISTEEN NIMI Kaliumklorid Orifarm 750 mg depottabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi depottabletti sisältää 750 mg kaliumkloridia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
Vaaleankeltainen, opalisoiva piparmintun tuoksuinen ja makuinen suspensio.
 1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
1. LÄÄKEVALMISTEEN NIMI Nystimex, 100 000 IU/ml oraalisuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 100 000 IU nystatiinia. Apuaineet: metyyliparahydroksibentsoaatti 1 mg natrium1,2 mg/ml,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Metronidatsoli 0,75 paino-%, 7,5 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Zidoval 7,5 mg/g emätingeeli 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Metronidatsoli 0,75 paino-%, 7,5 mg/g Apuaineet, joiden vaikutus tunnetaan: Metyyliparahydroksibentsoaatti
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 400 mg emätinpuikko, kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 400 mg/emätinpuikko Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Glucosamin Pharma Nord 400 mg kapselit. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 400 mg glukosamiinia, joka vastaa 509 mg glukosamiinisulfaattia, vastaten 676 mg
VALMISTEYHTEENVETO. Etopofos infuusiokuiva-aine laimennetaan ennen käyttöä kohdassa 6.6 olevan ohjeen mukaan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ETOPOFOS 100 mg infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidifosfaatti 113,6 mg (vastaa 100 mg etoposidia) Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ETOPOFOS 100 mg infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Etoposidifosfaatti 113,6 mg (vastaa 100 mg etoposidia) Täydellinen apuaineluettelo,
Hivenaineiden perustarpeen sekä hiukan lisääntyneen tarpeen tyydyttämiseen laskimoravitsemuksen yhteydessä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Gyno-Daktarin 2 % emätinvoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mikonatsolinitraatti 20 mg/g Apuaineet, joiden vaikutus tunnetaan: bentsoehappo, butyylihydroksianisoli.
VALMISTEYHTEENVETO. Valkoinen, pyöreä, kummaltakin puolelta litteä viistoreunainen tabletti, jossa jakouurre toisella puolella.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 30 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 30 mg ambroksolihydrokloridia. Apuaineet: 40 mg laktoosimonohydraattia (ks.
Yksi kapseli sisältää estramustiininatriumfosfaattimonohydraattia vastaten 140 mg estramustiinifosfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ESTRACYT 140 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää estramustiininatriumfosfaattimonohydraattia vastaten 140 mg estramustiinifosfaattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ESTRACYT 140 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää estramustiininatriumfosfaattimonohydraattia vastaten 140 mg estramustiinifosfaattia.
Histadin- valmisteen tehoa ja turvallisuutta ei ole osoitettu alle 2-vuotiailla lapsilla.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Histadin 10 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Yksi tabletti sisältää 94 mg laktoosimonohydraattia.
VALMISTEYHTEENVETO. Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112 mg feksofenadiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nefoxef 120 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 120 mg feksofenadiinihydrokloridia, mikä vastaa 112
VALMISTEYHTEENVETO. Tabletit ovat pyöreitä, harmaansinisiä ja sokeripäällysteisiä, halkaisija n. 11 mm.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Songha Yö/Natt tabletti, päällystetty 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää: Valerianae (Valeriana officinalis L. s.l.) rad. extr. spir.
Kissa: Leikkauksen jälkeisen kivun lievitys kohdun ja munasarjojen poistoleikkauksen sekä pienten pehmytkudoskirurgisten toimenpiteiden jälkeen.
 1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
1. ELÄINLÄÄKKEEN NIMI Acticam 5 mg/ml injektioneste, liuos koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Acticam 5 mg/ml injektionesteliuosta sisältää: Vaikuttavat aineet Meloksikaami
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 9 mg natriumkloridia. 100 ml sisältää 15,4 mmol (vastaten 354 mg) natriumia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Phybag 9 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 9 mg natriumkloridia. 100 ml sisältää 15,4 mmol (vastaten 354 mg) natriumia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää: Glukoosi, vedetön 6,75 g Natriumkloridi 1,30 g Natriumsitraatti
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rehydron Optim jauhe oraaliliuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annospussi sisältää: Glukoosi, vedetön 6,75 g Natriumkloridi 1,30 g Natriumsitraatti
VALMISTEYHTEENVETO. Yli 33 kg painavat lapset (noin 11-vuotiaat), alle 50 kg painavat nuoret ja aikuiset:
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PERFALGAN 10 mg/ml, infuusioneste, liuos. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 10 mg parasetamolia 1 infuusiopullo sisältää 50 ml vastaten 500
VALMISTEYHTEENVETO. 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 2,5 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 2,5 mg kapseli, pehmeä 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää natriumpikosulfaattimonohydraattia 2,593 mg, joka vastaa 2,5 mg natriumpikosulfaattia.
Eläimiä koskevat erityiset varotoimet Jos haittavaikutuksia ilmenee, tulee hoito keskeyttää ja ottaa yhteys eläinlääkäriin.
 1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
1. ELÄINLÄÄKKEEN NIMI Meloxoral 0,5 mg/ml oraalisuspensio kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Meloksikaami 0,5 mg Apuaine: Natriumbentsoaatti 1,75 mg Täydellinen
LIITE VALMISTEYHTEENVETO
 LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
LIITE VALMISTEYHTEENVETO 4 1. LÄÄKEVALMISTEEN NIMI Mizollen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Mitsolastiini (INN) 10 mg 3. LÄÄKEMUOTO Depottabletti. 4. KLIINISET TIEDOT 4.1. Terapeuttiset indikaatiot
4.1 Käyttöaihe Akuutteihin tai kroonisiin keuhko- ja keuhkoputkisairauksiin liittyvän limaa erittävän yskän limaa irrottava hoito.
 V A LMIS T EYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 60 mg poretabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi poretabletti sisältää 60 mg ambroksolihydrokloridia. Apuaineet: 110,00 mg vedetöntä
V A LMIS T EYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Flavamed 60 mg poretabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi poretabletti sisältää 60 mg ambroksolihydrokloridia. Apuaineet: 110,00 mg vedetöntä
1. LÄÄKEVALMISTEEN NIMI. Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg.
 1. LÄÄKEVALMISTEEN NIMI Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan: Yksi millilitra
1. LÄÄKEVALMISTEEN NIMI Picorion 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan: Yksi millilitra
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN OLEELLISET OSAT Huomautus: Nämä valmisteyhteenvedon ja pakkausselosteen muutokset ovat voimassa komission päätöksen ajankohtana. Komission päätöksen jälkeen
Metotreksaattihoidon toksisen vaikutuksen kumoaminen. Pitkälle edennyt kolorektaalisyöpä yhdessä 5- fluorourasiilin kanssa.
 1. LÄÄKEVALMISTEEN NIMI Isovorin 10 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Levofoliinihappo 10 mg/ml kalsiumlevofolinaattina Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
1. LÄÄKEVALMISTEEN NIMI Isovorin 10 mg/ml injektioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Levofoliinihappo 10 mg/ml kalsiumlevofolinaattina Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Jos ihoärsytystä, kosketusihottumaa tai yliherkkyyttä esiintyy, lopeta valmisteen käyttö.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BETADINE 75 mg/ml -ihonpuhdisteliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jodattu povidoni 75 mg/ml Täydellinen apuaineluettelo, ks. kohta 6.1 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BETADINE 75 mg/ml -ihonpuhdisteliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jodattu povidoni 75 mg/ml Täydellinen apuaineluettelo, ks. kohta 6.1 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Mesillinaamille herkkien gramnegatiivisten bakteerien aiheuttamat virtsatieinfektiot.
 1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Selexid 200 mg tabletti, kalvopäällysteinen Selexid 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti
1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Selexid 200 mg tabletti, kalvopäällysteinen Selexid 400 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti
VALMISTEYHTEENVETO. Päänahan seborrooinen ekseema ja muu päänahan hilseily (pityriasis capitis). Pityriasis versicolor.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Rennie Orange imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rennie Orange imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää: Kalsiumkarbonaatti 680 mg Magnesiumsubkarbonaatti, raskas
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Rennie Orange imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää: Kalsiumkarbonaatti 680 mg Magnesiumsubkarbonaatti, raskas
VALMISTEYHTEENVETO. Hammaslääkärin tai lääkärin määräyksestä: Pre- ja postoperatiivinen desinfiointi suukirurgiassa ja parodontaalisessa kirurgiassa.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Corsodyl 2 mg/ml liuos suuonteloon 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Klooriheksidiiniglukonaatti 2 mg/ml Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Corsodyl 2 mg/ml liuos suuonteloon 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Klooriheksidiiniglukonaatti 2 mg/ml Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Maksimivuorokausiannos 40 ml (120 mg dekstrometorfaania)
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resilar 3 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml sisältää 3 mg dekstrometorfaanihydrobromidia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resilar 3 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi ml sisältää 3 mg dekstrometorfaanihydrobromidia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO. Tämä lääkevalmiste on tarkoitettu vain IgE-välitteisen allergian spesifiseen diagnostiseen käyttöön.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI SOLUPRICK SQ hyönteismyrkyt, liuos ihopistotestiin - 801 Mehiläisen myrkky (Apis mellifera) - 802 Ampiaisen myrkky (Vespula spp.) 2. VAIKUTTAVAT AINEET JA NIIDEN
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI SOLUPRICK SQ hyönteismyrkyt, liuos ihopistotestiin - 801 Mehiläisen myrkky (Apis mellifera) - 802 Ampiaisen myrkky (Vespula spp.) 2. VAIKUTTAVAT AINEET JA NIIDEN
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. PAUSANOL 0,1 mg/g -emätinemulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PAUSANOL 0,1 mg/g -emätinemulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emätinemulsiovoidetta sisältää estriolia 0,1 mg. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI PAUSANOL 0,1 mg/g -emätinemulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emätinemulsiovoidetta sisältää estriolia 0,1 mg. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Akrivastiinia ei pidä määrätä potilaille, joiden munuaistoiminta on merkittävästi heikentynyt.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Benadryl 8 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Akrivastiini 8 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Kapseli, kova Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, ks. 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, ks. 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Vaaleankeltainen, kalvopäällysteinen, neliönmuotoinen tabletti, jossa on pallomainen kohouma molemmilla puolilla.
 1. LÄÄKEVALMISTEEN NIMI Ridaura 3 mg tabletti VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Auranofiini 3 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Tabletti, kalvopäällysteinen.
1. LÄÄKEVALMISTEEN NIMI Ridaura 3 mg tabletti VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Auranofiini 3 mg Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Tabletti, kalvopäällysteinen.
VALMISTEYHTEENVETO. Yliherkkyys mikonatsolille, muille imidatsolijohdannaisille tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 20 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää mikonatsolinitraattia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 20 mg/ml emulsio iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää mikonatsolinitraattia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1.
Apuaine, jonka vaikutus tunnetaan: yksi tabletti sisältää 43,3 mg laktoosimonohydraattia. Täydellinen apuaineluettelo, ks. kohta 6.
 1. LÄÄKEVALMISTEEN NIMI Levodonna 1,5 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 1,5 mg levonorgestreeliä. Apuaine, jonka vaikutus tunnetaan: yksi tabletti sisältää 43,3
1. LÄÄKEVALMISTEEN NIMI Levodonna 1,5 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 1,5 mg levonorgestreeliä. Apuaine, jonka vaikutus tunnetaan: yksi tabletti sisältää 43,3
1. ELÄINLÄÄKKEEN NIMI. Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS. Yksi millilitra sisältää: Vaikuttava aine:
 1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
1. ELÄINLÄÄKKEEN NIMI Loxicom 0,5 mg/ml oraalisuspensio kissalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra sisältää: Vaikuttava aine: Meloksikaami Apuaineet: Natriumbentsoaatti 0,5 mg 1,5
VALMISTEYHTEENVETO. Huom. Emätinpuikko tulee työntää syvälle emättimeen, ei mielellään kuukautisten aikana.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI GYNO-TROSYD 100 mg emätinpuikko, tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi emätinpuikko sisältää 100 mg tiokonatsolia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. 1 gramma voidetta sisältää 1 mg:n mometasonifuroaattia (1mg/g mometasonifuroaatti).
 1. LÄÄKEVALMISTEEN NIMI Mometasone furoate Auden Mckenzie 1mg/g voide VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 gramma voidetta sisältää 1 mg:n mometasonifuroaattia (1mg/g mometasonifuroaatti).
1. LÄÄKEVALMISTEEN NIMI Mometasone furoate Auden Mckenzie 1mg/g voide VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 gramma voidetta sisältää 1 mg:n mometasonifuroaattia (1mg/g mometasonifuroaatti).
VALMISTEYHTEENVETO. Valmisteen kuvaus: pyöreä, merkintä BEPANTHEN kehässä, halkaisija n. 18 mm, paksuus n. 3,5 mm, harmaankeltainen, sitruunan tuoksu.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO. Täydellisen parenteraalisen ravitsemuksen täydennyksenä vesiliukoisten vitamiinien päivittäisen tarpeen tyydyttämiseksi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
VALMISTEYHTEENVETO. Matkapahoinvoinnin ja merisairauden ehkäisyyn ja lievittämiseen aikuisille ja yli 12-vuotiaille nuorille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Postafen 25 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 25 mg meklotsiinihydrokloridia. Täydellinen apuaineluettelo, ks. kohta 6.1
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Postafen 25 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 25 mg meklotsiinihydrokloridia. Täydellinen apuaineluettelo, ks. kohta 6.1
VALMISTEYHTEENVETO. Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g
 1 LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen annospussi sisältää seuraavat määrät vaikuttavia
1 LÄÄKEVALMISTEEN NIMI VALMISTEYHTEENVETO Laxido Appelsiini jauhe oraaliliuosta varten, annospussi 13,8 g 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen annospussi sisältää seuraavat määrät vaikuttavia
1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.1 Käyttöaiheet. 4.2 Annostus ja antotapa
 1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
1. LÄÄKEVALMISTEEN NIMI Betahistin Orifarm 8 mg tabletit Betahistin Orifarm 16 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 tabletti sisältää 8 mg tai 16 mg betahistiinidihydrokloridia Täydellinen
VALMISTEYHTEENVETO. Valmisteen kuvaus: Valkoinen, läpikuultamaton emulsiovoide ja vaalean kellertävä peräpuikko.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Neoproct yhdistelmäpakkaus Rektaalivoide, creme ja peräpuikko 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 g rektaalivoidetta sisältää 1 mg fluokortoloni-21-pivalaattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Neoproct yhdistelmäpakkaus Rektaalivoide, creme ja peräpuikko 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 g rektaalivoidetta sisältää 1 mg fluokortoloni-21-pivalaattia
Valmisteyhteenveto. Deksametasonia (max 20 mg kerran vuorokaudessa) annetaan samanaikaisesti suun kautta.
 Valmisteyhteenveto 1. LÄÄKEVALMISTEEN NIMI Granisetron Bluefish 1 mg tabletti, kalvopäällysteinen Granisetron Bluefish 2 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 mg:n tabletti:
Valmisteyhteenveto 1. LÄÄKEVALMISTEEN NIMI Granisetron Bluefish 1 mg tabletti, kalvopäällysteinen Granisetron Bluefish 2 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 mg:n tabletti:
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin 38/46 A. Valmisteyhteenveto 4.1 Käyttöaiheet [tällä hetkellä hyväksytyt käyttöaiheet on poistettava ja korvattava seuraavilla]
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin 38/46 A. Valmisteyhteenveto 4.1 Käyttöaiheet [tällä hetkellä hyväksytyt käyttöaiheet on poistettava ja korvattava seuraavilla]
VALMISTEYHTEENVETO. Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia, joka vastaa 2,68 mg bentsydamiinia.
 1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
1 LÄÄKEVALMISTEEN NIMI Zyx Minttu 3 mg imeskelytabletti Zyx Sitruuna 3 mg imeskelytabletti VALMISTEYHTEENVETO 2 VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 3 mg bentsydamiinihydrokloridia,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Hydrea 500 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hydrea 500 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää hydroksikarbamidia (hydroksiurea) 500 mg. Apuaine, jonka vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hydrea 500 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää hydroksikarbamidia (hydroksiurea) 500 mg. Apuaine, jonka vaikutus tunnetaan:
VALMISTEYHTEENVETO. Valmisteen kuvaus: Valkoinen tai melkein valkoinen talkkimainen jauhe.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 10 mg/g puuteri 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma puuteria sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LAXOBERON 7,5 mg/ml tipat, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml tippoja sisältää natriumpikosulfaattia 7,5 mg. Apuaineet, joiden vaikutus tunnetaan:
VALMISTE YHT E ENVET O
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Dormiplant tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää:valerianae (Valeriana officinalis L.)
Farmakoterapeuttinen ryhmä: steroideihin kuulumaton anti-inflammatorinen lääkeaine, ATCvet-koodi QM01AE90
 VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Quadrisol 100 mg/ml oraaligeeli hevosille 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Quadrisol oraaligeeliä sisältää Vaikuttava(t) aine(et) Vedaprofeeni 100
VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Quadrisol 100 mg/ml oraaligeeli hevosille 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml Quadrisol oraaligeeliä sisältää Vaikuttava(t) aine(et) Vedaprofeeni 100
VALMISTEYHTEENVETO. 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745. Apuaineet,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kapseli sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745. Apuaineet,
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
VALMISTEYHTEENVETO. Bricanyl Turbuhaler 0,25 mg/annos ja 0,5 mg/annos inhalaatiojauheet
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bricanyl Turbuhaler 0,25 mg/annos ja 0,5 mg/annos inhalaatiojauheet 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bricanyl Turbuhaler 0,25 mg/annos: 1 annos sisältää
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Bricanyl Turbuhaler 0,25 mg/annos ja 0,5 mg/annos inhalaatiojauheet 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bricanyl Turbuhaler 0,25 mg/annos: 1 annos sisältää
VALMISTEYHTEENVETO. 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni. 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine:
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Canidryl 50 mg tabletti koirille Karprofeeni 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine: Karprofeeni 50 mg/tabletti Apuaineet Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Kestine 20 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Kestine 20 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 20 mg mikronisoitua ebastiinia. Apuaine, jonka vaikutus
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Kestine 20 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 20 mg mikronisoitua ebastiinia. Apuaine, jonka vaikutus
1. ELÄINLÄÄKKEEN NIMI. Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
VALMISTEYHTEENVETO. Valkoinen tai melkein valkoinen, tasainen, viistoreunainen, jakouurteellinen tabletti, halkaisija n. 9 mm, koodi ORN 276.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tyrazol 5 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 5 mg karbimatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tyrazol 5 mg tabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 5 mg karbimatsolia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Kapseli, kova Norsunluunvalkoiset kapselit. Koko 2, sisältää valkoista rikinhajuista jauhetta.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hidrasec 100 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 100 mg rasekadotriilia. Apuaineet: Yksi kapseli sisältää 41 mg laktoosia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Hidrasec 100 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 100 mg rasekadotriilia. Apuaineet: Yksi kapseli sisältää 41 mg laktoosia
KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman hoitoon.
 KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
KEYTRUDA (pembrolitsumabi) Terveydenhuollon ammattilaiset Usein kysytyt kysymykset KEYTRUDA monoterapiana on tarkoitettu aikuisille edenneen (leikkaukseen soveltumattoman tai metastasoituneen) melanooman
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 3. LÄÄKEMUOTO 4. KLIINISET TIEDOT. 4.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI TROSYD 1 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 10 mg tiokonatsolia. Täydellinen apuaineluettelo, ks. kohta
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. Granisetron Stada 1 mg kalvopäällysteiset tabletit Granisetron Stada 2 mg kalvopäällysteiset tabletit
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Granisetron Stada 1 mg kalvopäällysteiset tabletit Granisetron Stada 2 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen 1 mg:n kalvopäällysteinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Granisetron Stada 1 mg kalvopäällysteiset tabletit Granisetron Stada 2 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen 1 mg:n kalvopäällysteinen
Bakteerilääkkeiden asianmukaista käyttöä koskevat viranomaisohjeet tulee ottaa huomioon.
 1. LÄÄKEVALMISTEEN NIMI Cetraxal 2 mg/ml korvatipat, liuos, kerta-annospakkauksessa 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml liuosta sisältää 2 mg siprofloksasiinia hydrokloridina. Yhdestä kerta-annospipetistä
1. LÄÄKEVALMISTEEN NIMI Cetraxal 2 mg/ml korvatipat, liuos, kerta-annospakkauksessa 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml liuosta sisältää 2 mg siprofloksasiinia hydrokloridina. Yhdestä kerta-annospipetistä
Pakkausseloste: Tietoa käyttäjälle. Lomustine medac 40 mg kapselit, kova
 Pakkausseloste: Tietoa käyttäjälle Lomustine medac 40 mg kapselit, kova Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja. Säilytä
Pakkausseloste: Tietoa käyttäjälle Lomustine medac 40 mg kapselit, kova Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja. Säilytä
VALMISTEYHTEENVETO. Kerta-annos tulisi niellä yhdellä kertaa eikä sitä tulisi pitää suussa kovin pitkään.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI DUPHALAC 667 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra Duphalac-oraaliliuosta sisältää 667 mg laktuloosia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI DUPHALAC 667 mg/ml oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra Duphalac-oraaliliuosta sisältää 667 mg laktuloosia. Täydellinen apuaineluettelo,
Yliherkkyys vaikuttavalle aineelle tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fusidic Acid Orifarm 20 mg/g, emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää fusidiinihappoa hemihydraattina, joka vastaa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fusidic Acid Orifarm 20 mg/g, emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää fusidiinihappoa hemihydraattina, joka vastaa
VALMISTEYHTEENVETO. Valmisteen kuvaus. Vaaleanpunainen nelikulmainen tabletti, jonka kulmat on pyöristetty, halkaisija 7 mm, merkintä FA 10.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Pepcid 10 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 10 mg famotidiinia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Pepcid 10 mg tabletti, kalvopäällysteinen 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kalvopäällysteinen tabletti sisältää 10 mg famotidiinia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia 20 mg (2 %).
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Fucidin voideside 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Voideside sisältää Fucidin 2% voidetta noin 1,5 g/dm 2. 1 g voidetta sisältää vaikuttavaa ainetta: Natriumfusidaattia
Valmistetta ei tule käyttää tiineillä ja imettävillä nartuilla eikä koirilla, joilla on maksan vajaatoiminta.
 1. ELÄINLÄÄKKEEN NIMI Barbivet vet. 30 mg tabletti Barbivet vet. 60 mg tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine Yksi 30 mg tabletti sisältää fenobarbitaalia 30 mg. Yksi 60 mg tabletti
1. ELÄINLÄÄKKEEN NIMI Barbivet vet. 30 mg tabletti Barbivet vet. 60 mg tabletti 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttava aine Yksi 30 mg tabletti sisältää fenobarbitaalia 30 mg. Yksi 60 mg tabletti
VALMISTEYHTEENVETO. Yliherkkyys vaikuttavalle aineelle, muille imidatsolijohdoksille tai kohdassa 6.1 mainituille apuaineille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 20 mg mikonatsolinitraattia. Apuaineet, joiden vaikutus
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Daktarin 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi gramma emulsiovoidetta sisältää 20 mg mikonatsolinitraattia. Apuaineet, joiden vaikutus
a) Perusimmunisaatio: Perusimmunisaatio tulisi mieluimmin suorittaa kylmänä vuodenaikana.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Encepur lapset Puutiaisaivokuumerokote. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annos (0,25 ml suspensiota) sisältää: inaktivoitua TBE (puutiaisaivotulehdus)
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Encepur lapset Puutiaisaivokuumerokote. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annos (0,25 ml suspensiota) sisältää: inaktivoitua TBE (puutiaisaivotulehdus)
VALMISTEYHTEENVETO. Hiuspohja pestään Ketoconazol ratiopharm shampoolla, jonka annetaan vaikuttaa 3-5 minuutin ajan ennen huuhtelua.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Ketoconazol ratiopharm 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi millilitra shampoota sisältää 20 mg ketokonatsolia. Apuaineet: Täydellinen
VALMISTEYHTEENVETO 1
 VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Nootropil 1200 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Nootropil 1200 mg kalvopäällysteinen tabletti sisältää 1200 mg pirasetaamia.
VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Nootropil 1200 mg kalvopäällysteiset tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Nootropil 1200 mg kalvopäällysteinen tabletti sisältää 1200 mg pirasetaamia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI. NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT. Ketokonatsoli 20 mg/g
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ketokonatsoli 20 mg/g Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Emulsiovoide Valmisteen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI NIZORAL 2 % emulsiovoide 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Ketokonatsoli 20 mg/g Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO Emulsiovoide Valmisteen
VALMISTEYHTEENVETO. 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita, kanta CNCM I-745.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg jauhe oraalisuspensiota varten, annospussi 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Precosa 250 mg jauhe oraalisuspensiota varten, annospussi 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 annospussi sisältää 250 mg kylmäkuivattua Saccharomyces boulardiita,
VALMISTEYHTEENVETO. Lääkkeellinen hengitysilma on tarkoitettu lapsille, aikuisille ja vanhuksille.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI AIRAPY 100%, lääkkeellinen kaasu, puristettu 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hengitysilma lääkintäkäyttöön 100 % 200 baarin paineessa (15 C). 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI AIRAPY 100%, lääkkeellinen kaasu, puristettu 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Hengitysilma lääkintäkäyttöön 100 % 200 baarin paineessa (15 C). 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Alutard SQ:n biologinen aktiivisuus liittyy allergeenin pitoisuuteen, joka ilmaistaan SQ-U/ml. Pullo 3
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ALUTARD SQ siitepölyt, injektioneste, suspensio - 225 Timotei (Phleum pratense) 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Timoteiuute. Puhdistettuja ja vakioituja
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI ALUTARD SQ siitepölyt, injektioneste, suspensio - 225 Timotei (Phleum pratense) 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Timoteiuute. Puhdistettuja ja vakioituja
Annosta tulee muuttaa eläimillä, joilla on munuaisten tai maksan vajaatoiminta, koska haittavaikutusriski on suurentunut.
 1. ELÄINLÄÄKKEEN NIMI Metomotyl vet 2,5 mg/ml injektioneste, liuos kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 millilitra sisältää: Vaikuttava aine: metoklopramidi (hydrokloridimonohydraattina)
1. ELÄINLÄÄKKEEN NIMI Metomotyl vet 2,5 mg/ml injektioneste, liuos kissoille ja koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 millilitra sisältää: Vaikuttava aine: metoklopramidi (hydrokloridimonohydraattina)
VALMISTEYHTEENVETO. 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg kalsiumia. Täydellinen apuaineluettelo, ks. kohta 6.
 1. LÄÄKEVALMISTEEN NIMI Kalcipos 500 mg tabletti, kalvopäällysteinen VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg
1. LÄÄKEVALMISTEEN NIMI Kalcipos 500 mg tabletti, kalvopäällysteinen VALMISTEYHTEENVETO 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 kalvopäällysteinen tabletti sisältää kalsiumkarbonaattia vastaten 500 mg
Tuulix tabletit on tarkoitettu allergisen nuhan sekä kroonisen idiopaattisen urtikarian oireiden hoitoon.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tuulix 10 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Tuulix 10 mg tabletit 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää 10 mg loratadiinia. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO. Yksi tabletti sisältää natriumfluoridia vastaten 0,25 mg fluoridia ja omenahappoa 28,6 mg.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Xerodent 0,25 mg / 28,6 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää natriumfluoridia vastaten 0,25 mg fluoridia ja omenahappoa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Xerodent 0,25 mg / 28,6 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi tabletti sisältää natriumfluoridia vastaten 0,25 mg fluoridia ja omenahappoa
VALMISTEYHTEENVETO. Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml. Valmisteen kuvaus: miedosti tuoksuva, väritön tai hieman kellertävä liuos
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Mucovin 0,8 mg/ml -oraaliliuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Bromiheksiinihydrokloridi, 0,8 mg/ml Apuaineet, joiden vaikutus tunnetaan: etanoli 100 mg/ml
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
VALMISTEYHTEENVETO. Vero-soluissa kasvatetut poliovirukset tyyppi 1 (Brunhilde), tyyppi 2 (MEF-1) ja tyyppi 3 (Saukett) on puhdistettu ja inaktivoitu.
 1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI VeroPol Injektioneste, liuos, esitäytetty ruisku. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annos = 0,5 ml: Poliovirus tyyppi 1, inaktivoitu Poliovirus tyyppi
1 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI VeroPol Injektioneste, liuos, esitäytetty ruisku. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi annos = 0,5 ml: Poliovirus tyyppi 1, inaktivoitu Poliovirus tyyppi
VALMISTEYHTEENVETO. 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LIVOSTIN 0,5 mg/ml silmätipat, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI LIVOSTIN 0,5 mg/ml silmätipat, suspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää 0,54 mg levokabastiinihydrokloridia, joka vastaa 0,5 mg levokabastiinia.
VALMISTEYHTEENVETO. Annostus Aikuiset (myös iäkkäät): Suositeltu annos on 800 mg eli 2 kapselia vuorokaudessa kerta-annoksena kolmen kuukauden ajan.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Cartexan 400 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiininatriumsulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Cartexan 400 mg kapseli, kova 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi kapseli sisältää 400 mg kondroitiininatriumsulfaattia. Täydellinen apuaineluettelo,
VALMISTEYHTEENVETO. Kermanvärinen tai vaaleanruskea hieno jauhe, jolla tunnusomainen vaniljan tuoksu.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resonium jauhe oraalisuspensiota/peräruiskesuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumpolystyreenisulfonaatti 99,934 g/100 g jauhetta Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Resonium jauhe oraalisuspensiota/peräruiskesuspensiota varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumpolystyreenisulfonaatti 99,934 g/100 g jauhetta Täydellinen
Neste- ja NaCl- vajaus. Infuusioiden ja injektioiden valmistamiseen.
 1. LÄÄKEVALMISTEEN NIMI Natriumklorid Baxter 9 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9 mg/ml mmol/l: Na + 154 Cl - 154 Täydellinen apuaineluettelo, ks. kohta
1. LÄÄKEVALMISTEEN NIMI Natriumklorid Baxter 9 mg/ml infuusioneste, liuos 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Natriumkloridi 9 mg/ml mmol/l: Na + 154 Cl - 154 Täydellinen apuaineluettelo, ks. kohta
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos. 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
VALMISTEYHTEENVETO. Yksi Salofalk 4 g/60 ml peräruiskesuspensio (= 60 g suspensiota) sisältää 4 g mesalatsiinia.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Salofalk 4 g/60 ml peräruiskesuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Salofalk 4 g/60 ml peräruiskesuspensio (= 60 g suspensiota) sisältää 4 g mesalatsiinia.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Salofalk 4 g/60 ml peräruiskesuspensio 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Salofalk 4 g/60 ml peräruiskesuspensio (= 60 g suspensiota) sisältää 4 g mesalatsiinia.
