RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
|
|
|
- Elsa Mäkelä
- 6 vuotta sitten
- Katselukertoja:
Transkriptio
1 TISSEEL , Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Leikkaukset ovat maailmanlaajuisesti suuri sairauksiin liittyvä taakka. Euroopassa tehdään vuosittain noin sydänleikkausta, joissa voidaan tarvita verenvuotoa estävää lääkettä. Lisäksi vuosittain tehdään arviolta 2,5 miljoonaa suolistoleikkausta, joissa 48 %:ssa poistetaan osa suolta. Tämän lisäksi vuosittain tehdään 2,1 miljoonaa aivo- tai selkäydinleikkausta. Niihin voi sisältyä myös toimenpiteitä, joilla estetään aivoselkäydinnesteen vuoto selkäytimestä, nenästä, kurkusta tai silmästä. Tällaisissa leikkauksissa käytetään kudosliimoja tai fibriiniliimoja haavojen sulkemisen ja parantamisen apuna. Kudosliiman tarkoituksena on edistää haavojen paranemista niin, että ompeleita ja haavahakasia tarvitaan vähemmän kuin normaalisti tai ei lainkaan. Kudosliiman käyttö yksinään tai ompeleiden ja haavahakasten kanssa voi olla hyödyllinen vaihtoehto, jonka avulla haavat paranevat hyvin sekä entistä kivuttomammin ja nopeammin. TISSEEL on kudosliima, jossa vaikuttavien aineiden pitoisuudet ovat korkeita. TISSEEL - valmistetta voidaan käyttää: verenvuodon tyrehdyttämisen apuna leikkauksissa edistämään haavojen paranemista (ompeleiden kanssa tai ilman ompeleita) seuraavanlaisissa leikkauksissa: verenkiertojärjestelmän (suoniston) leikkaukset mahalaukun tai suoliston liittäminen takaisin yhteen selkäranka- tai aivoleikkaukset, joissa ollaan kosketuksessa aivoselkäydinnesteen tai aivojen/selkärangan ulkokerroksen kanssa (esimerkiksi korva-, nenä-, kurkku-, silmä- tai rankaleikkaukset) 13 avuksi kudospintojen sulkeutumisessa, kahden ihokappaleen kiinnittymisessä yhteen tai uuden ihokappaleen kiinnittämisessä alueelle, josta puuttuu ihoa. Vuosittain tehdään noin 1,2 miljoonaa sydänleikkausta, joissa voidaan tarvita verenvuotoa estävää lääkettä. Lisäksi arvioidaan, että vuosittain tehdään 2,5 miljoonaa
2 suolistoleikkausta, joissa 48 %:ssa poistetaan osa suolta. Tämän lisäksi vuosittain tehdään 2,1 miljoonaa aivo- tai selkäydinleikkausta. Niihin sisältyy myös toimenpiteitä, joilla estetään aivo-selkäydinnesteen vuoto selkäytimestä, nenään, kurkkuun tai silmään, sekä selkärangan toimenpiteitä Euroopan unionissa TISSEEL-valmisteen myyntilupa myönnetään joko kansallisessa menettelyssä tai tunnustamismenettelyssä. Kansallisissa myyntiluvissa käyttöaiheet vaihtelevat maittain. Käyttöaihe Kudosliimana edistämään haavan paranemista tai ommelten tukena neurokirurgiassa ja sellaisissa kirurgisissa toimenpiteissä, joissa voidaan olla kosketuksissa aivo-selkäydinnesteeseen (CSF) tai kovakalvoon (esim. korva-, nenä- ja kurkkukirurgiassa, silmä- ja spinaalikirurgiassa) ei ole hyväksytty kaikissa Euroopan unionin maissa. Yhteenveto hoidon hyödyistä Leikkaushaavojen sulkemiseen käytetään tavallisimmin ompeleita ja hakasia. Kudosliimojen tiedetään edistävän hyvin verenvuodon tyrehtymistä ja haavojen paranemista. Niiden tarkoituksena on saada haavat paranemaan hyvin sekä entistä nopeammin ja kivuttomammin. Hoidon hyötyihin liittyvät asiat, joita ei tunneta Kudosliimoja on tutkittu monilla ihmisillä eri ikäryhmissä ja eri etnisissä ryhmissä. On todennäköistä, että kudosliimat toimivat hyvin kaikissa etnisissä ryhmissä. Yhteenveto turvallisuustiedoista Taulukko 1. Tärkeät tunnistetut riskit Riski Mitä tiedetään Ehkäistävyys Yliherkkyys. Jos TISSEEL -valmistetta applikoidaan vahingossa verisuoneen, saattaa muodostua verisuonitukoksia, jotka voivat kulkeutua elimistössä toiseen paikkaan (Tromboemboliset tapahtumat tahattoman suonensisäisen annon seurauksena). TISSEEL voi aiheuttaa allergisia reaktioita. Niiden todennäköisyys voi kasvaa, jos TISSEEL -valmistetta applikoidaan vahingossa verisuoneen. TISSEELvalmisteen käytön yhteydessä on raportoitu allergisia reaktioita. Nämä ovat harvoin johtaneet kuolemaan. TISSEEL-valmisteen käytön yhteydessä on raportoitu verisuonitukoksia, kun hoitoalan ammattilainen on vahingossa applikoinut valmistetta verisuoneen. Valmisteen joutuminen verisuoneen voi olla hengenvaarallista. Jos olet aikaisemmin saanut allergisen reaktion kudosliimasta, liimaa ei saa käyttää uudestaan. Varmista, että lääkäri kertoo sinulle TISSEEL-valmisteen aiheuttamista mahdollisista allergisista reaktioista, kuten nokkosrokosta, kutinasta, ihottumasta, rinnanahdistuksesta, hengityksen vinkumisesta ja matalasta verenpaineesta. Hoitoalan ammattilaisia varoitetaan, että TISSEELvalmistetta ei saa koskaan antaa verisuoneen.
3 On mahdollista, ettei valmiste toimi, jos sitä ei käsitellä oikein, erityisesti silloin, kun käytetään vain pieniä määriä valmistetta. (Tehon puute annostelupoikkeaman vuoksi käytettäessä pientä määrää valmistetta). Jos ruiskutuslaitetta käytetään väärin, laitteesta tuleva ilma tai kaasu voi johtaa ilma- tai kaasukuplien muodostumiseen verenkierrossa (Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa) Sellaisten leikkausten yhteydessä, joissa käytetään vain pientä määrää valmistetta, lääke on sekoitettava kunnolla. Suurin osa tällaisista leikkauksista kohdistui silmiin. Vaikuttaa siltä, että ilma- tai kaasukuplat liittyvät ruiskutuslaitetten käyttöön suositeltua suuremmalla paineella ja/tai kudospinnan läheisyydessä. Hoitoalan ammattilaisia opastetaan poistamaan TISSEEL -ruiskusta tulevat ensimmäiset pisarat ennen valmisteen käyttöä. Kirurgien on noudatettava ruiskutuslaitteen käyttöohjeita. Kirurgi ei saa käyttää liikaa painetta eikä ruiskuttaa kudosliimaa liian läheltä, sillä muuten verenkiertoon voi muodostua ilma- tai kaasukuplia. Taulukko 2. Tärkeät mahdolliset riskit Riski Valmisteen käytöstä aiheutuvat infektiot (Infektioiden siirtymisen riski) Jos valmistetta käytetään liikaa, on mahdollista, että kudosta kiinnittyy eitoivottuihin kohtiin ja käyttökohtaan muodostuu liikaa kudosta tai arpeutumista (Kudoksen kiinnittyminen eitoivottuihin kohtiin ja granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta) TISSEEL-valmistetta voidaan käyttää väärin tyränkorjausleikkauksissa. (Puutteellinen lääkkeenantotekniikka tyrän korjauksessa) TISSEEL voi reagoida muiden lääkkeiden kanssa tai vaikuttaa niiden toimintaan, tai muut lääkkeet voivat vaikuttaa TISSEEL - valmisteen toimintaan (Yhteisvaikutukset/ yhteensopimattomuudet muiden lääkevalmisteiden kanssa) Mitä tiedetään Kudosliimat tehdään ihmisestä saatavista aineista (ihmisen plasmasta). Kaikki ihmisestä saatava plasma käy läpi hyvin tarkan seulontaprosessin. Infektioiden siirtymisen riskiä ei kuitenkaan pystytä koskaan täysin poistamaan. Kaikki kehonosat hoidettavaa aluetta lukuun ottamatta on peitettävä huolellisesti, jotta vältetään kudoksen kiinnittyminen ei-toivottuihin kohtiin. TISSEEL -valmistetta käytetään vain ohut kerros. Jos TISSEEL -valmistetta käytetään liian paksu kerros, liikaa kudosta tai arpikudosta voi muodostua, mikä saattaa häiritä valmisteen toimintaa ja elimistön kykyä parantua kunnolla. TISSEEL -valmistetta käytettäessä on aina tärkeää valita annos toimenpiteen tyypin, leikkausalueen koon, lääkkeen antotavan (suihke tai muu) ja tarvittavan määrän mukaan. Tietyt lääkkeet voivat reagoida TISSEEL -valmisteen kanssa tai häiritä sen toimintaa. Erityisesti tietyt kehon puhdistamiseen ennen leikkausta käytettävät lääkkeet sisältävät alkoholia ja voivat häiritä TISSEEL -valmisteen toimintaa.
4 Taulukko 3. Puuttuvat tiedot Riski Eläimillä ei ole tutkittu valmisteen keskipitkän tai pitkäaikaisen käytön aiheuttamia haittavaikutuksia, kykyä aiheuttaa syöpää eikä vaikutuksia raskauteen, sikiöön tai immuunijärjestelmään. (Prekliininen tieto, joka liittyy subakuuttiin ja krooniseen toksisuuteen, karsinogeenisuuteen, lisääntymis- ja kehitystoksisuuteen tai immuunistimulaatioon) Kliinisen tutkimustiedon puute raskauden tai imetyksen aikaisesta käytöstä ihmisellä Rajallisia tietoja pediatrisista potilaista Mitä tiedetään Eläimillä ei ole tutkittu haittavaikutuksia pitkäaikaisen käytön yhteydessä. Eläinkokeita ei ole tehty tiineillä tai imettävillä naarailla. TISSEEL -valmistetta ei suositella raskauden aikana. Kudosliimojen käytön turvallisuutta raskauden tai imetyksen aikana ei ole varmistettu kontrolloiduissa kliinisissä tutkimuksissa. TISSEEL -valmistetta ei suositella raskauden tai imetyksen aikana. Kudosliimojen käytön turvallisuutta pediatrisilla potilailla ei ole tarkoin varmistettu kontrolloiduissa kliinisissä tutkimuksissa. Yhteenveto toimenpiteistä riskien minimoimiseksi Kaikilla lääkkeillä on valmisteyhteenveto, josta lääkärit, apteekkihenkilökunta ja muut hoitoalan ammattilaiset saavat lisätietoa lääkkeiden käytöstä, riskeistä ja riskien minimointia koskevista suosituksista. Tästä on saatavilla selkokielinen lyhennelmä eli pakkausseloste. Näiden asiakirjojen toimenpiteitä kutsutaan yleisimpien riskien minimointitoimenpiteiksi. Tämän lääkkeen turvallista ja tehokasta käyttöä koskevat erityisehdot ja -rajoitukset (lisätoimenpiteet riskin minimoimiseksi). Nämä lisätoimenpiteet riskien minimoimiseksi koskevat seuraavaa riskiä: Taulukko 4. Jos ruiskutuslaitetta käytetään väärin, siitä tuleva ilma tai kaasu voi johtaa ilma- tai kaasukuplien muodostumiseen verenkierrossa (Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa) Toimenpiteet riskien minimoimiseksi: Terveydenhuollon ammattilaisia informoidaan ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riskistä, joka on vaarana käytettäessä ruiskutuslaitetta liian korkealla paineella tai liian lähellä antokohtaa. Baxterin myyntihenkilökunnalle ja hoitoalan ammattilaisille annetaan koulutusta laitteen oikeaan käyttöön. Tavoite ja perustelu: Alla mainittujen toimenpiteiden tavoitteena on lisätä tietoisuutta kudosliimojen käyttöön liittyvistä riskeistä, estää potilaille aiheutuvia vahinkoja, varmistaa, että käyttäjät ovat oikein koulutettuja kudosliimojen käyttöön, ja taata Baxterin kudosliimojen oikeanlainen käyttö. Pääasialliset lisätoimenpiteet riskin minimoimiseksi: Toimi 1: Myyntiluvan haltijoiden tiedotteet hoitoalan ammattilaisille
5 Toimi 2: Oikean paineen ja sumutusetäisyyden ilmaisevan symbolin näyttävän merkinnän/tarran lisääminen paineensäätölaitteeseen Toimi 3: EasySpray-ruiskutuslaitteen paineensäätölaitteen uudelleenmuotoilu niin, että suurin saatava paine pienenee. Toimi 4: Hoitoalan ammattilaisten ja Baxterin henkilökunnan koulutusmateriaalien päivittäminen Toimi 5: Hoitoalan ammattilaisten kouluttaminen Toimi 6: Baxterin henkilökunnan kouluttaminen Toimi 7: Koulutuksellisten nettisivujen luominen suihkutettavien tuotteiden käytöstä Kehityssuunnitelma myyntiluvan myöntämisen jälkeen TISSEEL-valmisteelle ei ole turvallisuutta koskevia kehityssuunnitelmia myyntiluvan myöntämisen jälkeen. Myyntiluvan ehdoissa mainitut tutkimukset TISSEEL-valmisteelle ei ole myyntiluvan ehdoissa mainittuja tutkimuksia. Yhteenveto riskienhallintasuunnitelman päivityksistä TISSEEL-valmisteen riskienhallintasuunnitelman päivitykset on merkitty alla olevaan taulukkoon.
6 Merkittävät riskienhallintasuunnitelman päivitykset Taulukko 5. Merkittävät riskienhallintasuunnitelman päivitykset Versio Päivämäärä Turvallisuustiedot Kommentti Muutettiin riski Ei ole. intravaskulaarinen käyttö riskiksi tromboemboliset tapahtumat tahattoman suonensisäisen annostelun seurauksena. Lisättiin lääkityspoikkeamat mahdolliseksi riskiksi kuvaamaan riskiä tehon puutteesta, kun ensimmäisiä pisaroita TISSEEL - valmisteesta ei poisteta. Lisättiin mahdollinen riski granulaatiokudoksen muodostuminen, ylimääräinen fibriini, inflammaatio ja vierasesinereaktio sekä ihon kovettuminen. Lisättiin puuttuva tieto yhteisvaikutukset muiden lääkevalmisteiden kanssa; yhteensopimattomuudet. Lisättiin puuttuva tieto prekliininen tieto, joka liittyy subakuuttiin ja krooniseen toksisuuteen, karsinogeenisuuteen, lisääntymis- ja kehitystoksisuuteen tai immunostimulaatioon Riskienhallintasuunnitelma päivitettiin sisältämään riski ilmaembolia, kudosrepeämä ja kaasutasku käytettäessä ruiskutuslaitetta paineella. Lisättiin mahdollinen riski puutteellinen lääkkeenantotekniikka tyrän korjauksessa Ei uusia turvallisuutta koskevia huolenaiheita. Riski yhteisvaikutukset/ yhteensopimattomuudet muiden lääkevalmisteiden kanssa siirrettiin puuttuvista Riskienhallintasuunnitelma päivitettiin vastaamaan turvallisuustietojen (CCSI) päivityksen päivän 59 kysymyksiin viimeisimmistä ilmatai kaasuemboliariskistä varoittavista sanamuodoista. Toimitettiin osana sitoumusta, jossa kansalliselle viranomaiselle (AGES) luvattiin toimittaa päivitetty RMP seuraavan
7 1.0 (Ensimmäinen versio uuden EU:n lääketurvalainsää dännön mukaan, yhteinen ARTISS - valmisteelle) tiedoista mahdolliseksi riskiksi vastaamaan näiden määritelmiä. Riski lääkityspoikkeamat muutettiin riskiksi Tehon puute annostelupoikkeaman vuoksi käytettäessä pientä määrää valmistetta ja siirrettiin mahdollisista riskeistä tunnistetuksi riskiksi, koska Baxterille ilmoitettiin näistä (vaikka mitään merkkejä ei ollut). Q1/2013 Ei uusia turvallisuutta koskevia huolenaiheita. Mahdollinen riski ilmaembolia, kudosrepeämä ja kaasutasku käytettäessä ruiskutuslaitetta paineella muutettiin selkeyden vuoksi riskiksi. Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa. määräaikaisen turvallisuuskatsauksen yhteydessä. Lisättiin myös tuloksia tutkimuksista ja Toimitettiin kansallisille terveysviranomaisille maissa, joissa TISSEEL- ja/tai ARTISS -valmiste on hyväksytty, kuten sovittiin artiklan 31 menettelyssä, joka koski ruiskutuslaitteilla annosteltavien kudosliimojen ilma- tai kaasuembolioita (EMEA/H/A-31/1337). Prosessinumero AT/H/0317/ /IB/026 Versio 1.0 päivitettiin PVAR:n mukaan Lisättiin lisätoimenpiteet riskien minimoimiseksi ilmaja kaasuemboliariskin suhteen ylimääräisenä lääketurvatoimena Lisättiin seuraava puuttuviin tietoihin: Kliinisen tutkimustiedon puute raskauden tai imetyksen aikaisesta käytöstä ihmisellä. 2.0 Q4/2013 Ei muutoksia turvallisuutta koskeviin huolenaiheisiin edellisen toimitetun version jälkeen. Muokkaukset tehty vastauksena tiettyihin terveysministeriön pyyntöihin: Päivitetty vastauksena Irlannin terveysministeriön päivättyihin kysymyksiin. Päivitetty vastauksena Suomen terveysministeriön
8 sitoutumispyyntöön riskienhallintasuunnite lman version 1.0 muokkaamisesta seuraavasti: osa VI.2.4 Yhteenveto turvallisuustiedoista nykyisen sanamuodon Lääkärin tulee varoa injektoimasta TISSEEL -valmistetta kudokseen. selkeämmäksi sanamuodoksi. 3.0 Q4/2015 Riskin ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa luokitus muutettiin tärkeästä mahdollisesta riskistä tärkeäksi tunnistetuksi riskiksi uuden EU:n lääketurvalainsäädännön määritelmien mukaan. Kuvastaa tilannetta, jossa TISSEEL - valmisteen indikaatio Kudosliimana parantamaan haavojen paranemista tai tukemaan ompeleita neurokirurgiassa ja kirurgisissa toimenpiteissä, joissa voidaan olla kosketuksessa aivoselkäydinnesteen (CSF) tai kovakalvon kanssa (esim. KNK-, silmä- ja rankaleikkaukset) ei ole hyväksytty kaikissa Euroopan unionin maissa. Riskienhallintasuunnitelma päivitettiin kuvastamaan lisäriskin minimoimistoimenpite iden täyttymistä. Täydennettiin lisätoimenpiteet riskien minimoimiseksi seuraavasti: Suora tiedote terveydenhuollon asiantuntijoille. Oikean paineen ja sumutusetäisyyden ilmaisevan
9 symbolin sisältävän merkinnän/tarran lisääminen paineensäätölaitteeseen on symboli, joka ilmaisee oikean paineen ja sumutusetäisyyden. EasySpray-ruiskutuslaitteen paineensäätölaitteen uudelleenmuotoilu niin, että suurin saatava paine pienenee. Hoitoalan ammattilaisten ja Baxterin henkilökunnan koulutusmateriaalien ja käyttöohjeiden päivittäminen. Hoitoalan ammattilaisten kouluttaminen. Baxterin henkilökunnan kouluttaminen. Koulutuksellisten nettisivujen luominen suihkutettavien tuotteiden käytöstä. Versio 3.0 päivitettiin PVAR:n mukaan: Tärkeä tunnistettu riski Allergiset reaktiot on muutettu muotoon Yliherkkyys. Tärkeä mahdollinen riski Kudoksen kiinnittyminen eitoivottuihin kohtiin ja granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta on muutettu muotoon Kudoksen kiinnittyminen ei-toivottuihin kohtiin ja granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta. Lisättiin puuttuvat tiedot Rajallisia tietoja pediatrisista potilaista (TISSEEL).
10 ARTISS , Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Leikkaukset ovat maailmanlaajuisesti suuri sairauksiin liittyvä taakka. Euroopassa tehdään vuosittain noin sydänleikkausta, joissa voidaan tarvita verenvuotoa estävää lääkettä. Lisäksi arvioidaan, että Euroopassa tehtiin kaiken kaikkiaan noin 3,9 miljoonaa plastiikkakirurgista toimenpidettä vuonna Noin 10 % näistä oli kasvoihin kohdistuvia leikkauksia. ARTISS -valmistetta mahdollisesti käyttävä populaatio vaihtelee hoidettavan tilan mukaan, mutta palovammojen hoidossa ARTISS -kudosliimaa käytetään useimmiten nuorille miehille ja lapsille. Tällaisissa leikkauksissa käytetään kudosliimoja tai fibriiniliimoja haavojen sulkemisen apuna. Kudosliiman tarkoituksena on edesauttaa kudospintojen kiinnittymistä tai sulkeutumista ja auttamalla tyrehdyttämään verenvuotoa. ARTISS on kudosliima, jossa vaikuttavien aineiden pitoisuudet ovat pieniä. ARTISS - valmistetta voidaan käyttää: kosmeettisissa ja korjaavissa leikkauksissa sekä palovammaleikkauksissa edistämään kudosten paranemista ja erillään olevien kudospintojen kiinnittymistä korvaamaan ja/tai tukemaan ommelten ja hakasten käyttöä leikkauksissa verenvuodon tyrehdyttämisen apuna ihonalaisilla kudospinnoilla. Vuosittain tehdään noin palovammaleikkausta. Vuosittain noin 1,5 miljoonaa ihmistä saa palovammoja, jotka vaativat hoitoa; puolet näistä on liekkien aiheuttamia vammoja. Tuleen liittyviä palovammoja saa maailmanlaajuisesti noin 1,1 ihmistä :ta ihmistä kohti. Palovammojen ilmaantuvuus pieni- ja keskituloisissa maissa on 1,3 ihmistä :ta ihmistä kohti, kun taas korkeatuloisissa maissa se on 0,14 ihmistä :ta ihmistä kohti. Euroopassa tehtiin arviolta kaiken kaikkiaan noin plastiikkakirurgista toimenpidettä vuonna Noin 10 % näistä oli kasvoihin kohdistuvia leikkauksia. Yhteenveto hoidon hyödyistä
11 Leikkaushaavojen sulkemiseen käytetään tavallisimmin ompeleita ja hakasia. Kudosliimojen tiedetään edistävän hyvin verenvuodon tyrehtymistä ja haavojen paranemista. Niiden tarkoituksena on saada haavat paranemaan hyvin sekä entistä nopeammin ja kivuttomammin. Hoidon hyötyihin liittyvät asiat, joita ei tunneta Kudosliimoja on tutkittu monilla ihmisillä eri ikäryhmissä ja eri etnisissä ryhmissä. Suurin osa tutkituista oli kaukasialaisia. Jonkin verran on tutkittu myös latinalaisamerikkalaisia, mustaihoisia, aasialaisia ja syntyperäisiä amerikkalaisia. On todennäköistä, että kudosliimat toimivat hyvin kaikissa etnisissä ryhmissä. Yhteenveto turvallisuustiedoista Taulukko 1. Tärkeät tunnistetut riskit Riski Mitä tiedetään Ehkäistävyys Yliherkkyys Jos ARTISS -valmistetta applikoidaan vahingossa verisuoneen, saattaa muodostua verisuonitukoksia, jotka voivat kulkeutua elimistössä toiseen paikkaan (Tromboemboliset tapahtumat tahattoman suonensisäisen annon seurauksena). On mahdollista, ettei valmiste toimi, jos sitä ei käsitellä oikein, erityisesti silloin, kun käytetään vain pieniä määriä valmistetta (Tehon puute annostelupoikkeaman vuoksi käytettäessä pientä määrää valmistetta). ARTISS voi aiheuttaa allergisia reaktioita. Niiden todennäköisyys voi kasvaa, jos ARTISS -valmistetta applikoidaan vahingossa verisuoneen. ARTISS - valmisteen käytön yhteydessä on raportoitu allergisia reaktioita. Nämä ovat harvoin johtaneet kuolemaan. ARTISS -valmisteen käytön yhteydessä on raportoitu verisuonitukoksia, kun hoitoalan ammattilainen on vahingossa applikoinut valmistetta verisuoneen. Valmisteen joutuminen verisuoneen voi olla hengenvaarallista. Sellaisten leikkausten yhteydessä, joissa käytetään vain pientä määrää valmistetta, lääke on sekoitettava kunnolla. Suurin osa tällaisista leikkauksista kohdistui silmiin. Jos olet aikaisemmin saanut allergisen reaktion kudosliimasta, liimaa ei saa käyttää uudestaan. Varmista, että lääkäri kertoo sinulle ARTISS -valmisteen aiheuttamista mahdollisista allergisista reaktioista, kuten nokkosrokosta, kutinasta, ihottumasta, rinnanahdistuksesta, hengityksen vinkumisesta ja matalasta verenpaineesta. Hoitoalan ammattilaisia varoitetaan, että ARTISS - valmistetta ei saa koskaan antaa verisuoneen. Hoitoalan ammattilaisia opastetaan poistamaan ARTISS - ruiskusta tulevat ensimmäiset pisarat ennen valmisteen käyttöä.
12 Jos ruiskutuslaitetta käytetään väärin, laitteesta tuleva ilma tai kaasu voi johtaa ilma- tai kaasukuplien muodostumiseen verenkierrossa (Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa) Vaikuttaa siltä, että ilma- tai kaasukuplat liittyvät ruiskutuslaitetteen käyttöön suositeltua suuremmalla paineella ja/tai kudospinnan läheisyydessä. Kirurgien on noudatettava ruiskutuslaitteen käyttöohjeita. Kirurgi ei saa käyttää liikaa painetta eikä ruiskuttaa kudosliimaa liian läheltä, sillä muuten verenkiertoon voi muodostua ilma- tai kaasukuplia.
13 Taulukko 2. Tärkeät mahdolliset riskit Riski Valmisteen käytöstä aiheutuvat infektiot (Infektioiden siirtymisen riski) Jos valmistetta käytetään liikaa, on mahdollista, että kudosta kiinnittyy eitoivottuihin kohtiin ja käyttökohtaan muodostuu liikaa kudosta tai arpeutumista (Kudoksen kiinnittyminen eitoivottuihin kohtiin ja granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta) ARTISS voi reagoida muiden lääkkeiden kanssa tai vaikuttaa niiden toimintaan, tai muut lääkkeet voivat vaikuttaa ARTISS - valmisteen toimintaan (Yhteisvaikutukset/ yhteensopimattomuudet muiden lääkevalmisteiden kanssa) Mitä tiedetään Kudosliimat tehdään ihmisestä saatavista aineista (ihmisen plasmasta). Kaikki ihmisestä saatava plasma käy läpi hyvin tarkan seulontaprosessin. Infektioiden siirtymisen riskiä ei kuitenkaan pystytä koskaan täysin poistamaan. Kaikki kehonosat hoidettavaa aluetta lukuun ottamatta on peitettävä huolellisesti, jotta vältetään kudoksen kiinnittyminen ei-toivottuihin kohtiin. ARTISS -valmistetta käytetään vain ohut kerros. Jos ARTISS -valmistetta käytetään liian paksu kerros, liikaa kudosta tai arpikudosta voi muodostua, mikä saattaa häiritä valmisteen toimintaa ja elimistön kykyä parantua kunnolla. Tietyt lääkkeet voivat reagoida ARTISS -valmisteen kanssa tai häiritä sen toimintaa. Erityisesti tietyt kehon puhdistamiseen ennen leikkausta käytettävät lääkkeet sisältävät alkoholia ja voivat häiritä ARTISS -valmisteen toimintaa. Taulukko 3. Puuttuvat tiedot Riski Eläimillä ei ole tutkittu valmisteen keskipitkän tai pitkäaikaisen käytön aiheuttamia haittavaikutuksia, kykyä aiheuttaa syöpää eikä vaikutuksia raskauteen, sikiöön tai immuunijärjestelmään. (Prekliininen tieto, joka liittyy subakuuttiin ja krooniseen toksisuuteen, karsinogeenisuuteen, lisääntymis- ja kehitystoksisuuteen tai immuunistimulaatioon) Kliinisen tutkimustiedon puute raskauden tai imetyksen aikaisesta käytöstä ihmisellä Mitä tiedetään Eläimillä ei ole tutkittu haittavaikutuksia pitkäaikaisen käytön yhteydessä. Eläinkokeita ei ole tehty tiineillä tai imettävillä naarailla. ARTISS -valmistetta ei suositella raskauden aikana. Kudosliimojen käytön turvallisuutta raskauden tai imetyksen aikana ei ole varmistettu kontrolloiduissa kliinisissä tutkimuksissa. ARTISS -valmistetta ei suositella raskauden tai imetyksen aikana. Yhteenveto lisätoimenpiteistä riskien minimoimiseksi Kaikilla lääkkeillä on valmisteyhteenveto, josta lääkärit, apteekkihenkilökunta ja muut hoitoalan ammattilaiset saavat lisätietoa lääkkeiden käytöstä, riskeistä ja niiden minimointia koskevista suosituksista. Tästä on saatavilla selkokielinen lyhennelmä eli
14 pakkausseloste. Näiden asiakirjojen toimenpiteitä kutsutaan yleisimpien riskien minimointitoimenpiteiksi. Tämän lääkkeen turvallista ja tehokasta käyttöä koskevat erityisehdot ja -rajoitukset (lisätoimenpiteet riskin minimoimiseksi). Nämä lisätoimenpiteet riskien minimoimiseksi koskevat seuraavaa riskiä: Taulukko 4. Jos ruiskutuslaitetta käytetään väärin, siitä tuleva ilma tai kaasu voi johtaa ilma- tai kaasukuplien muodostumiseen verenkierrossa (Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa) Toimet riskien minimoimiseksi: Lisätoimenpiteenä riskien minimoimiseksi terveydenhuollon ammattilaisia informoidaan ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riskistä, joka on vaarana käytettäessä ruiskutuslaitetta liian korkealla paineella tai liian lähellä antokohtaa. Baxterin myyntihenkilökunnalle ja hoitoalan ammattilaisille annetaan koulutusta laitteen oikeaan käyttöön. Tavoite ja perustelu: Alla mainittujen toimenpiteiden tavoitteena on lisätä tietoisuutta kudosliimojen käyttöön liittyvistä riskeistä, estää potilaille aiheutuvia vahinkoja, varmistaa, että käyttäjät ovat oikein koulutettuja kudosliimojen käyttöön, ja taata Baxterin kudosliimojen oikeanlainen käyttö. Pääasialliset lisätoimenpiteet riskin minimoimiseksi: Toimi 1: Myyntiluvan haltijoiden tiedotteet hoitoalan ammattilaisille Toimi 2: Oikean paineen ja sumutusetäisyyden ilmaisevan symbolin näyttävän merkinnän/tarran lisääminen paineensäätölaitteeseen Toimi 3: EasySpray -ruiskutuslaitteen paineensäätölaitteen uudelleenmuotoilu niin, että suurin saatava paine pienenee. Toimi 4: Hoitoalan ammattilaisten ja Baxterin henkilökunnan koulutusmateriaalien päivittäminen Toimi 5: Hoitoalan ammattilaisten kouluttaminen Toimi 6: Baxterin henkilökunnan kouluttaminen Toimi 7: Koulutuksellisten nettisivujen luominen suihkutettavien tuotteiden käytöstä Kehityssuunnitelma myyntiluvan myöntämisen jälkeen ARTISS -valmisteelle ei ole kehityssuunnitelmia myyntiluvan myöntämisen jälkeen. Myyntiluvan ehdoissa mainitut tutkimukset ARTISS -valmisteelle ei ole myyntiluvan ehdoissa mainittuja tutkimuksia.
15 Yhteenveto riskienhallintasuunnitelman päivityksistä ARTISS -valmisteen riskienhallintasuunnitelman päivitykset on merkitty alla olevaan taulukkoon. Taulukko 5. Merkittävät riskienhallintasuunnitelman päivitykset Versio Päivämäärä Turvallisuustiedot Kommentti Lisättiin mahdollinen riski Ei ole. granulaatiokudoksen muodostuminen, ylimääräinen fibriini, inflammaatio ja vierasesinereaktio sekä ihon kovettuminen. Lisättiin puuttuva tieto yhteisvaikutukset muiden lääkevalmisteiden kanssa; yhteensopimattomuudet. Lisättiin puuttuva tieto prekliininen tieto, joka liittyy subakuuttiin ja krooniseen toksisuuteen, karsinogeenisuuteen, lisääntymis- ja kehitystoksisuuteen tai immunostimulaatioon. Lisättiin lääkityspoikkeamat mahdolliseksi riskiksi kuvaamaan riskiä tehon puutteesta, kun ensimmäisiä pisaroita ARTISS - valmisteesta ei poisteta Ei turvallisuutta koskevia päivityksiä Muutettiin riski intravaskulaarinen käyttö riskiksi tromboemboliset tapahtumat tahattoman suonensisäisen annostelun seurauksena. Lisättiin tunnistettu riski tehon puute annostelupoikkeaman vuoksi. Lisättiin mahdollinen riski ilmaembolia, kudosrepeämä ja kaasutasku käytettäessä ruiskutuslaitetta. Lisättiin tuloksia tutkimuksesta Riskienhallintasuunnite lma päivitettiin vastaamaan turvallisuustietojen (CCSI) viimeisimpiä ilma- tai kaasuemboliariskistä varoittavia sanamuotoja. Lisättiin tuloksia tutkimuksesta Riski yhteisvaikutukset/ yhteensopimattomuudet muiden lääke-valmisteiden kanssa siirrettiin puuttuvista tiedoista mahdolliseksi riskiksi
16 vastaamaan näiden määritelmiä Lisättiin tunnistettu riski tehon puute annostelupoikkeaman vuoksi käytettäessä pientä määrää valmistetta. 1.0 (Ensimmäinen versio uuden EU:n lääketurvalainsää dännön mukaan, yhteinen TISSEEL-, ja ARTISS - valmisteelle) Q1/2013 Ei uusia turvallisuutta koskevia huolenaiheita. Riski ilmaembolia, kudosrepeämä ja kaasutasku käytettäessä ruiskutuslaitetta muutettiin selkeyden vuoksi riskiksi ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa. Versio 1.0 päivitettiin PVAR:n mukaan Lisättiin lisätoimenpiteet riskien minimoimiseksi ilmaja kaasuemboliariskin suhteen ylimääräisenä lääketurvatoimena. Lisättiin seuraava puuttuviin tietoihin: Kliinisen tutkimustiedon puute raskauden tai imetyksen aikaisesta käytöstä ihmisellä. 2.0 Q4/2013 Ei muutoksia turvallisuutta koskeviin huolenaiheisiin edellisen toimitetun version jälkeen. Toimitettiin osana sitoumusta, jossa kansalliselle viranomaiselle (AGES) luvattiin toimittaa päivitetty RMP seuraavan määräaikaisen turvallisuuskatsauksen yhteydessä. Lisättiin myös tuloksia tutkimuksesta Toimitettiin kansallisille terveysviranomaisille maissa, joissa TISSEEL- ja/tai ARTISS -valmiste on hyväksytty, kuten sovittiin artiklan 31 menettelyssä, joka koski ruiskutuslaitteilla annosteltavien kudosliimojen ilma- tai kaasuembolioita (EMEA/H/A-31/1337). Muokkaukset tehty vastauksena tiettyihin terveysministeriön pyyntöihin: Päivitetty vastauksena Irlannin terveysministeriön päivättyihin kysymyksiin
17 3.0 Q4/2015 Ilma- tai kaasuembolian, kudosrepeämän ja ilma- tai kaasutaskun riski käytettäessä ruiskutuslaitetta suositeltua korkeammilla paineilla ja lähellä kudospintaa luokiteltiin uudestaan tärkeästä mahdollisesta riskistä tärkeäksi tunnistetuksi riskiksi uuden EU:n lääketurvalainsäädännön määritelmien mukaan. Riskienhallintasuunnitelma päivitettiin kuvastamaan lisäriskin minimoimistoimenpite iden täyttymistä. Täydennettiin lisätoimenpiteet riskien minimoimiseksi seuraavasti: Suora tiedote terveydenhuollon asiantuntijoille. Oikean paineen ja sumutusetäisyyden ilmaisevan symbolin sisältävän merkinnän/tarran lisääminen paineensäätölaitteeseen on symboli, joka ilmaisee oikean paineen ja sumutusetäisyyden. EasySpray -ruiskutuslaitteen paineensäätölaitteen uudelleenmuotoilu niin, että suurin saatava paine pienenee Hoitoalan ammattilaisten ja Baxterin henkilökunnan koulutusmateriaalien ja käyttöohjeiden päivittäminen. Hoitoalan ammattilaisten kouluttaminen. Baxterin henkilökunnan kouluttaminen. Koulutuksellisten nettisivujen luominen suihkutettavien tuotteiden käytöstä Versio 3.0 päivitettiin PVAR:n mukaan: Tärkeä tunnistettu riski Allergiset reaktiot on muutettu muotoon Yliherkkyys. Tärkeä mahdollinen riski Kudoksen kiinnittyminen eitoivottuihin kohtiin ja
18 granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta on muutettu muotoon Kudoksen kiinnittyminen ei-toivottuihin kohtiin ja granulaatiokudoksen muodostuminen käytettäessä liikaa valmistetta.
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
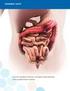 Tisseel 23.3.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Kudosliimoja tai fibriiniliimoja käytetään haavojen
Tisseel 23.3.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Kudosliimoja tai fibriiniliimoja käytetään haavojen
Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio)
 28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
28 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden epidemiologiasta (Enintään 150 sanaa per indikaatio) Parenteraalinen ravitsemus voi olla indikoitu suurelle määrälle sairauksia, kuten syöpä ja
Hoidon hyötyihin liittyvät asiat, joita ei tunneta (yksi lyhyt kappale kustakin käyttöaiheesta, enintään 50 sanaa)
 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Albiomin 5 % ja 20 % ovat laskimoon annettavia infuusioliuoksia, jotka on tarkoitettu kiertävän veritilavuuden palauttamiseen ja
Raplixan (ihmisen fibrinogeeni / ihmisen trombiini) riskienhallintasuunnitelman yhteenveto
 EMA/66782/2015 Raplixan (ihmisen fibrinogeeni / ihmisen trombiini) riskienhallintasuunnitelman yhteenveto Tämä asiakirja on Raplixa-lääkevalmisteen riskienhallintasuunnitelman yhteenveto. Siinä esitetään
EMA/66782/2015 Raplixan (ihmisen fibrinogeeni / ihmisen trombiini) riskienhallintasuunnitelman yhteenveto Tämä asiakirja on Raplixa-lääkevalmisteen riskienhallintasuunnitelman yhteenveto. Siinä esitetään
Propecia (finasteridi 0,2 ja 1 mg) tabletti , versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
Propecia (finasteridi 0,2 ja 1 mg) tabletti 25.4.2017, versio 4.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Miestyyppinen hiustenlähtö
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
10 maaliskuuta 2016 Mometasoni Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Nuha Allerginen nuha on ylähengitysteiden
Primovist (dinatriumgadoksetaatti) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Primovist (dinatriumgadoksetaatti) 05/2013, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 2. Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Magneettikuvaus (MK) on yksi useasta
Primovist (dinatriumgadoksetaatti) 05/2013, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 2. Julkisen yhteenvedon osiot 2.1 Tietoa sairauden esiintyvyydestä Magneettikuvaus (MK) on yksi useasta
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
CORTIMENT (budesonidi) 26.11.2013, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Haavainen paksusuolentulehdus (UC)
LIITE III MUUTOKSET VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN TARVITTAVIIN KOHTIIN
 LIITE III MUUTOKSET VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN TARVITTAVIIN KOHTIIN 1 Tisseel A. Valmisteyhteenveto Seuraavat muutokset on tehtävä Tisseel -valmisteen ja muilla myyntinimillä myytävien valmisteiden
LIITE III MUUTOKSET VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN TARVITTAVIIN KOHTIIN 1 Tisseel A. Valmisteyhteenveto Seuraavat muutokset on tehtävä Tisseel -valmisteen ja muilla myyntinimillä myytävien valmisteiden
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Mydrane 0,2 mg/ml + 3,1 mg/ml + 10 mg/ml injektioneste, liuos 3.7.2015, Versio 2.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Mydrane 0,2 mg/ml + 3,1 mg/ml + 10 mg/ml injektioneste, liuos 3.7.2015, Versio 2.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 11 maaliskuuta 2016 Desloratadiini Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Heinänuha Pohjoismaiset tutkimukset
11 maaliskuuta 2016 Desloratadiini Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Heinänuha Pohjoismaiset tutkimukset
Proscar. 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Proscar 7.8.2015, versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT VI.2.1 Tietoa sairauden esiintyvyydestä Eturauhanen on ainoastaan miehillä oleva rauhanen. Eturauhanen
Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa , Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa 6.7.2016, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden
Influvac 15 mikrog HA / 0,5 ml injektioneste, suspensio esitäytetyssä ruiskussa 6.7.2016, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0
 PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
PLENADREN RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VERSIO 3.0 VI.2 VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä PLENADREN-valmistetta käytetään lisämunuaisten vajaatoiminnan
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
TicoVac ja TicoVac Junior 29.12.2015, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Puutiaisaivotulehdus (TBE) on keskushermostoon
Käyttöopas. EasySpray- ja Duplospraypaineensäätölaitteiden. käyttö
 Käyttöopas EasySpray- ja Duplospraypaineensäätölaitteiden oikea käyttö EASYSPRAY- ja DUPLOSPRAY MIS -paineensäätölaite Ohjeet oikeasta käyttämisestä EASYSPRAY-paineensäätölaitteen käyttö (avoleikkauksiin)
Käyttöopas EasySpray- ja Duplospraypaineensäätölaitteiden oikea käyttö EASYSPRAY- ja DUPLOSPRAY MIS -paineensäätölaite Ohjeet oikeasta käyttämisestä EASYSPRAY-paineensäätölaitteen käyttö (avoleikkauksiin)
Liite II. Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle
 Liite II Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle 3 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä arvioinnista, joka koskee valmistetta nimeltä Quixil Taustatietoa
Liite II Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle 3 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä arvioinnista, joka koskee valmistetta nimeltä Quixil Taustatietoa
RMP section VI.2 Elements for Public Summary
 RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
RMP section VI.2 Elements for Public Summary Product: RMP: Atosiban Stragen, 6,75mg/0,9ml solution for injection Atosiban Stragen, 37,5mg/5ml concentrate for solution for infusion RMP-PID-ATO-v03 DLP:
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi)
 Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
Entyvio 300 mg kuiva aine välikonsentraatiksi infuusionestettä varten, liuos (vedolitsumabi) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO 27.6.2014, versio 1.0 VI.2 Julkisen yhteenvedon osiot VI.2.1
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
DUTASTERIDE RATIOPHARM 0,5 MG PEHMEÄT KAPSELIT Päivämäärä: 16.3.2016, Versio: 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Alteplaasi Versio 3.3
 Boehringer Ingelheim Sivu 1 / 5 OSA VI.2 Osa VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä Erilaiset sairaudet ja tilat edellyttävät laskimokatetrien eli laskimoon asetettavien ohuiden
Boehringer Ingelheim Sivu 1 / 5 OSA VI.2 Osa VI.2.1 JULKISEN YHTEENVEDON OSIOT Tietoa sairauden esiintyvyydestä Erilaiset sairaudet ja tilat edellyttävät laskimokatetrien eli laskimoon asetettavien ohuiden
innohep Päivämäärä: , Versio 5 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 innohep Päivämäärä: 27.2.2017, Versio 5 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Käyttöaihe: veritulppien hoito Jalkojen isoissa
innohep Päivämäärä: 27.2.2017, Versio 5 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Käyttöaihe: veritulppien hoito Jalkojen isoissa
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Paracetamol B. Braun 10 mg/ml infuusioneste, liuos 22.10.2014, versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Parasetamolia
Paracetamol B. Braun 10 mg/ml infuusioneste, liuos 22.10.2014, versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Parasetamolia
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Latanoprost Pfizer 4.2.2014, Versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Glaukooma on toiseksi yleisin sokeuden aiheuttaja
Latanoprost Pfizer 4.2.2014, Versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Glaukooma on toiseksi yleisin sokeuden aiheuttaja
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 BREVIBLOC 27.2.2015, Versio 6.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä BREVIBLOC kuuluu beetasalpaajien lääkeryhmään. Sitä
BREVIBLOC 27.2.2015, Versio 6.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä BREVIBLOC kuuluu beetasalpaajien lääkeryhmään. Sitä
Julkisen yhteenvedon osiot
 VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Hunterin oireyhtymä on harvinainen geneettinen sairaus, jota esiintyy pääasiallisesti miehillä kaikissa etnisissä ryhmissä. Esiintyvyys
VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Hunterin oireyhtymä on harvinainen geneettinen sairaus, jota esiintyy pääasiallisesti miehillä kaikissa etnisissä ryhmissä. Esiintyvyys
Ibandronat Stada 150 mg kalvopäällysteiset tabletit. 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Ibandronat Stada 150 mg kalvopäällysteiset tabletit 3.11.2014, versio V2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1b Tietoa sairauden esiintyvyydestä Vuonna
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu sovittelumenettelyssä. Direktiivin
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Telmisartan/ ratiopharm 4.12.2014, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Telmisartan/ ratiopharm on angiotensiini
Telmisartan/ ratiopharm 4.12.2014, Versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Telmisartan/ ratiopharm on angiotensiini
PLENADREN EU-Riskienhallintasuunnitelma, versio 3.2. Julkisen yhteenvedon osa-alueet. Katsaus taudin epidemiologiaan. Yhteenveto hoidon hyödyistä
 PLENADREN EU-Riskienhallintasuunnitelma, versio 3.2 VI.2 VI.2.1 Julkisen yhteenvedon osa-alueet Katsaus taudin epidemiologiaan PLENADREN sisältää hydrokortisonia ja sitä käytetään lisämunuaisten vajaatoiminnan
PLENADREN EU-Riskienhallintasuunnitelma, versio 3.2 VI.2 VI.2.1 Julkisen yhteenvedon osa-alueet Katsaus taudin epidemiologiaan PLENADREN sisältää hydrokortisonia ja sitä käytetään lisämunuaisten vajaatoiminnan
Abstral, EU:n riskienhallintasuunnitelma, versio 4.0
 Vaikuttavat aineet (kansainvälinen INN-nimi tai Fentanyyli (fentanyylisitraattina) yleinen nimi): Farmakoterapeuttinen ryhmä (ATC-koodi): Opioidianalgeetit, fenyylipiperidiinijohdannaiset, N02ABO3 Myyntiluvan
Vaikuttavat aineet (kansainvälinen INN-nimi tai Fentanyyli (fentanyylisitraattina) yleinen nimi): Farmakoterapeuttinen ryhmä (ATC-koodi): Opioidianalgeetit, fenyylipiperidiinijohdannaiset, N02ABO3 Myyntiluvan
Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/775985/2014 Viekirax-valmisteen (ombitasviiri/paritapreviiri/ritonaviiri) enhallintasuunnitelman yhteenveto Tämä on Viekirax-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT
 RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT ORION CORPORATION PÄIVÄMÄÄRÄ: 15-6-2015, VERSIO 2 VI.2 Julkisen yhteenvedon osiot VI.2.1
RISKINHALLINTASUUNNITELMAN JULKINEN YHTEENVETO PREGABALIN ORION 25, 50, 75, 100, 150, 225, 300 MG KOVAT KAPSELIT ORION CORPORATION PÄIVÄMÄÄRÄ: 15-6-2015, VERSIO 2 VI.2 Julkisen yhteenvedon osiot VI.2.1
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Akne Aikuisiän aknea esiintyy 25 prosentilla aikuisista miehistä ja 50 prosentilla
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Akne Aikuisiän aknea esiintyy 25 prosentilla aikuisista miehistä ja 50 prosentilla
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit , Versio 1.3
 Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
Emtricitabine / Tenofovir disoproxil Stada 200 mg/245 mg kalvopäällysteiset tabletit 30.5.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Emtricitabine
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Numeta G16E, Numeta G19E 2332015, Versio 30 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2 Julkisen yhteenvedon osiot VI21 Tietoa sairauden esiintyvyydestä Joillakin sairaalapotilailla ei välttämättä
Numeta G16E, Numeta G19E 2332015, Versio 30 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2 Julkisen yhteenvedon osiot VI21 Tietoa sairauden esiintyvyydestä Joillakin sairaalapotilailla ei välttämättä
Betaserc 24 mg suussa hajoavat tabletit , versio 2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Betaserc 24 mg suussa hajoavat tabletit 23.9.2014, versio 2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Betahistiini on tarkoitettu
Betaserc 24 mg suussa hajoavat tabletit 23.9.2014, versio 2.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Betahistiini on tarkoitettu
Nucala. 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EMA/671186/2015 Nucala 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Nucalan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
EMA/671186/2015 Nucala 01.02.2016 Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Nucalan riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Enstilar , Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Enstilar 21.1.2016, Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Psoriaasi on yleinen ihosairaus, jossa iholle ilmestyy
Enstilar 21.1.2016, Versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Psoriaasi on yleinen ihosairaus, jossa iholle ilmestyy
RMP section VI.2 Elements for Public Summary
 RMP section VI.2 Elements for Public Summary Product: Tranexamic acid Stragen 100 mg/ml solution for injection RMP: Version 4.0 DLP: 01-09-2012 MAH: Stragen Nordic A/S VI.2 VI.2.1 Julkisen yhteenvedon
RMP section VI.2 Elements for Public Summary Product: Tranexamic acid Stragen 100 mg/ml solution for injection RMP: Version 4.0 DLP: 01-09-2012 MAH: Stragen Nordic A/S VI.2 VI.2.1 Julkisen yhteenvedon
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Noviana 0,5 mg/0,1 mg kalvopäällysteiset tabletit 19.5.2014, Painos 3, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä
Symbicort Turbuhaler. Päivämäärä, Versio RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Symbicort Turbuhaler Päivämäärä, Versio RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Astma Astma on yleinen hengitysteiden tulehdussairaus,
Symbicort Turbuhaler Päivämäärä, Versio RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Astma Astma on yleinen hengitysteiden tulehdussairaus,
Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto
 EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
EMA/775515/2014 Cosentyx-valmisteen (sekukinumabi) riskienhallintasuunnitelman yhteenveto Tämä on Cosentyx-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan,
RMP section VI.2 Elements for Public Summary
 RMP section VI.2 Elements for Public Summary Product: Zarelle 75 microgram filmcoated tablet RMP: Version 1.0 DLP: 28-02-2013 MAH: Stragen Nordic A/S 32 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden
RMP section VI.2 Elements for Public Summary Product: Zarelle 75 microgram filmcoated tablet RMP: Version 1.0 DLP: 28-02-2013 MAH: Stragen Nordic A/S 32 VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 JAYDESS 13,5 mg, kohdunsisäinen ehkäisin 5/2014 versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2. VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Jaydess-hormonkierukkaa
JAYDESS 13,5 mg, kohdunsisäinen ehkäisin 5/2014 versio 2.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI2. VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Jaydess-hormonkierukkaa
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Elidel 10 mg/g emulsiovoide 8.12.2015, Versio 11 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ekseemaa esiintyy lähinnä lapsilla
Elidel 10 mg/g emulsiovoide 8.12.2015, Versio 11 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Ekseemaa esiintyy lähinnä lapsilla
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Physioneal 23.3.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Munuaisten toimintahäiriöitä esiintyy Euroopassa
Physioneal 23.3.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Munuaisten toimintahäiriöitä esiintyy Euroopassa
NeuroBloc B-tyypin botulinumtoksiini injektioneste, liuos U/ml
 NeuroBloc B-tyypin botulinumtoksiini injektioneste, liuos 5 000 U/ml Tärkeitä turvallisuutta koskevia tietoja lääkäreille Tämän käyttöoppaan tarkoitus on antaa NeuroBloc -valmisteen määräämiseen ja antamiseen
NeuroBloc B-tyypin botulinumtoksiini injektioneste, liuos 5 000 U/ml Tärkeitä turvallisuutta koskevia tietoja lääkäreille Tämän käyttöoppaan tarkoitus on antaa NeuroBloc -valmisteen määräämiseen ja antamiseen
Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen
 Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen Huom! Nämä muutokset sisällytetään voimassa oleviin valmisteyhteenvetoon, myyntipäällysmerkintöihin ja pakkausselosteeseen, jotka ovat koordinaatioryhmämenettelyssä
Liite III Muutoksia valmisteyhteenvetoon ja pakkausselosteeseen Huom! Nämä muutokset sisällytetään voimassa oleviin valmisteyhteenvetoon, myyntipäällysmerkintöihin ja pakkausselosteeseen, jotka ovat koordinaatioryhmämenettelyssä
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Extraneal peritoneaalidialyysineste 8.10.2015, Versio 6 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä On arvioitu, että yli 10 % Euroopan väestöstä
Extraneal peritoneaalidialyysineste 8.10.2015, Versio 6 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä On arvioitu, että yli 10 % Euroopan väestöstä
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Pregabalin Krka 17.2.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Täydellisyyden vuoksi, viitaten Direktiivin 2001/83 artiklaan 11, hakija varaa mahdollisuuden
Pregabalin Krka 17.2.2015, Versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Täydellisyyden vuoksi, viitaten Direktiivin 2001/83 artiklaan 11, hakija varaa mahdollisuuden
Käyttöopas. EasySpray- ja Duplospraypaineensäätölaitteiden. käyttö
 Käyttöopas EasySpray- ja Duplospraypaineensäätölaitteiden oikea käyttö b EASYSPRAY- ja DUPLOSPRAY EASYSPRAY-paineensäätölaitteen käyttö (avoleikkauksiin) Aseta 9 V:n paristo EASYSPRAYpaineensäätölaitteeseen
Käyttöopas EasySpray- ja Duplospraypaineensäätölaitteiden oikea käyttö b EASYSPRAY- ja DUPLOSPRAY EASYSPRAY-paineensäätölaitteen käyttö (avoleikkauksiin) Aseta 9 V:n paristo EASYSPRAYpaineensäätölaitteeseen
Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto
 EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/738120/2014 Ofev-valmisteen (nintedanibi) riskienhallintasuunnitelman yhteenveto Tämä on Ofev-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
Olysio (simepreviiri) RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Tämä on yhteenveto Olysio-valmisteen riskienhallintasuunnitelmasta (risk management plan, RMP), jossa esitetään yksityiskohtaisesti
, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
Entecavir STADA 0,5 mg ja 1 mg kalvopäällysteiset tabletit 14.6.2016, versio V1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Entecavir Stada 0,5 mg kalvopäällysteiset
NuvaRing. N.V. Organon. 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 NuvaRing N.V. Organon 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Etonogestreelia ja etinyyliestradiolia
NuvaRing N.V. Organon 20.1.2014, versio 6.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Etonogestreelia ja etinyyliestradiolia
Ethambutol Orion 500 mg tabletit Päivämäärä: , Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Ethambutol Orion 500 mg tabletit Päivämäärä: 21.10.2016, Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Etambutoli on
Ethambutol Orion 500 mg tabletit Päivämäärä: 21.10.2016, Versio 1.1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Etambutoli on
Olmesartan medoxomil STADA. 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
Olmesartan medoxomil STADA 10.11.2015, Versio V1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Olmesartan medoxomil STADA 10 mg kalvopäällysteiset tabletit Olmesartan
Morphine Orion. Pvm: , Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Morphine Orion Pvm: 19.12.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Tämä lääke on tarkoitettu voimakkaan kivun
Morphine Orion Pvm: 19.12.2016, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Tämä lääke on tarkoitettu voimakkaan kivun
Exviera-valmisteen (dasabuviiri) riskienhallintasuunnitelman yhteenveto
 EMA/775993/2014 Exviera-valmisteen (dasabuviiri) enhallintasuunnitelman yhteenveto Tämä on Exviera-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
EMA/775993/2014 Exviera-valmisteen (dasabuviiri) enhallintasuunnitelman yhteenveto Tämä on Exviera-valmisteen enhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet, joilla varmistetaan, että
19.2.2014, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Femoston 1/10 tabletti, kalvopäällysteinen Femoston 2/10 tabletti, kalvopäällysteinen Femoston Conti 1/5 tabletti, kalvopäällysteinen Femoston Conti 0,5/2,5 tabletti, kalvopäällysteinen 19.2.2014, versio
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos. 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
Calciumfolinat Fresenius Kabi 10 mg/ml injektio-/infuusioneste, liuos 11.8.2014, Versio 0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä
LIITE III. Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin
 HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
HUOM! LIITE III Muutokset valmisteyhteenvedon ja pakkausselosteen olennaisiin osiin Kansallisten viranomaisten on mahdollisesti jälkeenpäin päivitettävä valmisteyhteenvedot ja pakkausselosteet tarpeen
Skudex 75 mg / 25 mg kalvopäällysteinen tabletti , v. 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Skudex 75 mg / 25 mg kalvopäällysteinen tabletti 28.12.2015, v. 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Kivulla voi olla
Skudex 75 mg / 25 mg kalvopäällysteinen tabletti 28.12.2015, v. 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Kivulla voi olla
Praluent. 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Praluent 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Praluent-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Praluent 08-2015, Versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Tämä on Praluent-valmisteen riskienhallintasuunnitelman yhteenveto, jossa esitetään toimenpiteet,
Bimatoprosti. 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Bimatoprosti 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Kohonneen silmänpaineen alentaminen kroonista avokulmaglaukoomaa
Bimatoprosti 6.6.2014, versio 1 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Kohonneen silmänpaineen alentaminen kroonista avokulmaglaukoomaa
Pramipexol Stada. 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Pramipexol Stada 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Pramipexol STADA 0,088 mg tabletti Pramipexol STADA 0,18 mg tabletti Pramipexol STADA
Pramipexol Stada 18.10.2013, Versio V01 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot Pramipexol STADA 0,088 mg tabletti Pramipexol STADA 0,18 mg tabletti Pramipexol STADA
OSA VI: RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 EU RMP Lääkeaine Bikalutamidi Version numero 2 Päivämäärä 2 toukokuu 2014 OSA VI: RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT Bikalutamidi (CASODEX 1 ) on hormonaalinen
EU RMP Lääkeaine Bikalutamidi Version numero 2 Päivämäärä 2 toukokuu 2014 OSA VI: RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 JULKISEN YHTEENVEDON OSIOT Bikalutamidi (CASODEX 1 ) on hormonaalinen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 22 helmikuuta 2016 Drospirenoni/etinyyliestradioli Versionumero: 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Suun kautta
22 helmikuuta 2016 Drospirenoni/etinyyliestradioli Versionumero: 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Suun kautta
Remeron. 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Remeron 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Masennus on sairaus, jossa surullisuuden tunne ja
Remeron 13.11.2013, Versio 3.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Masennus on sairaus, jossa surullisuuden tunne ja
Litalgin-tabletti Litalgin-peräpuikko Litalgin-injektioneste, liuos (metamitsolinatrium ja pitofenonihydrokloridi) , versio 1.
 Litalgin-tabletti Litalgin-peräpuikko Litalgin-injektioneste, liuos (metamitsolinatrium ja pitofenonihydrokloridi) 21.6.2017, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen
Litalgin-tabletti Litalgin-peräpuikko Litalgin-injektioneste, liuos (metamitsolinatrium ja pitofenonihydrokloridi) 21.6.2017, versio 1.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen
Perusseikkoja julkista yhteenvetoa varten
 Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
Perusseikkoja julkista yhteenvetoa varten Yleiskatsaus taudin epidemiologiaan Elinajanodotteen kasvamisen ja väestön ikääntymisen oletetaan tekevän nivelrikosta neljänneksi suurimman työkyvyttömyyden syyn
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Ei oleellinen. Tämä on geneerinen hakemus. Valmisteyhteenveto noudattaa alkuperäisvalmisteen
Lipanthyl Penta 145 mg , versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Lipanthyl Penta 145 mg 15.9.2015, versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Fenofibraatti: Julkisen yhteenvedon osiot Fenofibraatti: Tietoa sairauden esiintyvyydestä Arviolta
Lipanthyl Penta 145 mg 15.9.2015, versio 3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Fenofibraatti: Julkisen yhteenvedon osiot Fenofibraatti: Tietoa sairauden esiintyvyydestä Arviolta
TÄRKEITÄ TURVALLISUUSTIETOJA RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE
 RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
RIXATHON (RITUKSIMABI) -HOITOA SAAVILLE POTILAILLE POTILASESITE MUIHIN KUIN ONKOLOGISIIN KÄYTTÖAIHEISIIN Tähän lääkkeeseen kohdistuu lisäseuranta. rituksimabi Fimean hyväksymä, heinäkuu/2018 2 3 TÄRKEÄÄ
ZAVEDOS , versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 1 (6) ZAVEDOS 9.6.2016, versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Akuuttia lymfaattista leukemiaa (ALL) esiintyy
1 (6) ZAVEDOS 9.6.2016, versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Akuuttia lymfaattista leukemiaa (ALL) esiintyy
Pronaxen 250 mg tabletti OTC , Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Pronaxen 250 mg tabletti OTC 25.9.2015, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Pronaxen 250 mg on tarkoitettu
Pronaxen 250 mg tabletti OTC 25.9.2015, Versio 1.3 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Pronaxen 250 mg on tarkoitettu
VALMISTEYHTEENVETO. Valmisteen kuvaus: pyöreä, merkintä BEPANTHEN kehässä, halkaisija n. 18 mm, paksuus n. 3,5 mm, harmaankeltainen, sitruunan tuoksu.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI BEPANTHEN 100 mg imeskelytabletti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi imeskelytabletti sisältää 100 mg dekspantenolia. Apuaineet, joiden vaikutus tunnetaan:
OSA VI: YHTEENVETO VALMISTEEN RISKIENHALLINTASUUNNITELMAAN SISÄLTYVISTÄ TOIMISTA
 OSA VI: YHTEENVETO VALMISTEEN RISKIENHALLINTASUUNNITELMAAN SISÄLTYVISTÄ TOIMISTA Tässä julkaistu osan VI sisältö koskee kaikkia tässä riskienhallintasuunnitelmassa mainittuja lääkevalmisteita, joita ovat:
OSA VI: YHTEENVETO VALMISTEEN RISKIENHALLINTASUUNNITELMAAN SISÄLTYVISTÄ TOIMISTA Tässä julkaistu osan VI sisältö koskee kaikkia tässä riskienhallintasuunnitelmassa mainittuja lääkevalmisteita, joita ovat:
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin
 Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
Liite III Muutokset valmistetietojen asianmukaisiin kohtiin Huom: Nämä muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin on laadittu lausuntopyyntömenettelyssä. Direktiivin 2001/83/EY
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO. Moventig-valmisteen (naloksegoli) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/611606/2014 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Moventig-valmisteen (naloksegoli) riskienhallintasuunnitelman (RMP) yhteenveto VI.2 Julkisen yhteenvedon osiot Tämä on Moventig-valmisteen
EMA/611606/2014 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO Moventig-valmisteen (naloksegoli) riskienhallintasuunnitelman (RMP) yhteenveto VI.2 Julkisen yhteenvedon osiot Tämä on Moventig-valmisteen
Liite III. Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin
 Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
Liite III Muutokset valmisteyhteenvedon ja pakkausselosteen asianmukaisiin kohtiin Huom: Tämä valmisteyhteenveto, myyntipäällysmerkinnät ja pakkausseloste on laadittu referral-menettelyn tuloksena. Jäsenvaltion
Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto
 EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
EMA/601943/2014 Trulicity-valmisteen (dulaglutidi) riskienhallintasuunnitelman (RMP) yhteenveto Tämä on Trulicity-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet,
Liite I. Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle
 Liite I Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1 Tieteelliset päätelmät Ottaen huomioon arviointiraportin, jonka lääketurvallisuuden riskinarviointikomitea (PRAC)
Liite I Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1 Tieteelliset päätelmät Ottaen huomioon arviointiraportin, jonka lääketurvallisuuden riskinarviointikomitea (PRAC)
Isotretinoin riskinhallintaohjelma. Isotretinoin Orion (isotretinoiini) Potilaan opas. Raskauden ja sikiöaltistuksen ehkäisy
 Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Isotretinoin riskinhallintaohjelma Isotretinoin Orion (isotretinoiini) Potilaan opas Raskauden ja sikiöaltistuksen ehkäisy TÄMÄN ESITTEEN TARKOITUS Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO ORION OYJ
 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO CANDESARTAN/HYDROCHLOROTHIAZIDE ORION 8 MG/12,5 MG, 16 MG/12,5 MG, 32 MG/12,5 MG, 32 MG/25 MG ORION OYJ PÄIVÄYS: 17.4.2015, versio 2 Sivu 1/6 VI.2 Julkisen
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO CANDESARTAN/HYDROCHLOROTHIAZIDE ORION 8 MG/12,5 MG, 16 MG/12,5 MG, 32 MG/12,5 MG, 32 MG/25 MG ORION OYJ PÄIVÄYS: 17.4.2015, versio 2 Sivu 1/6 VI.2 Julkisen
Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista
 Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista Diasesitys terveydenhuollon ammattilaisten koulutukseen 1 Benepali (etanersepti) Tähän lääkkeeseen kohdistuu lisäseuranta. On tärkeää
Benepali (etanersepti): Lyhyt koulutus riskien minimoinnin lisätoimista Diasesitys terveydenhuollon ammattilaisten koulutukseen 1 Benepali (etanersepti) Tähän lääkkeeseen kohdistuu lisäseuranta. On tärkeää
Tieteelliset johtopäätökset ja perusteet
 Liite IV Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle sekä yksityiskohtainen selvitys lääketurvallisuuden riskinarviointikomitean suositukseen liittyvistä eroista Tieteelliset
Liite IV Tieteelliset johtopäätökset ja perusteet myyntilupien ehtojen muuttamiselle sekä yksityiskohtainen selvitys lääketurvallisuuden riskinarviointikomitean suositukseen liittyvistä eroista Tieteelliset
Yleisen yhteenvedon osat. Tiivistelmä tautiepidemiologiasta
 VI.2 VI.2.1 Yleisen yhteenvedon osat Tiivistelmä tautiepidemiologiasta Gaucherin tauti on harvinainen geneettinen sairaus, joka johtuu määrätyn entsyymin puuttumisesta kehosta. Noin 30 000 henkilöllä maailmassa
VI.2 VI.2.1 Yleisen yhteenvedon osat Tiivistelmä tautiepidemiologiasta Gaucherin tauti on harvinainen geneettinen sairaus, joka johtuu määrätyn entsyymin puuttumisesta kehosta. Noin 30 000 henkilöllä maailmassa
Osio VI: Yhteenveto riskienhallintasuunnitelman toimista
 Osio VI: Yhteenveto riskienhallintasuunnitelman toimista VI.2 VI.2.1 Julkisen yhteenvedon osat Tietoa sairauden esiintyvyydestä Lääkevalmiste Dormix 12,5 mg ja 25 mg kalvopäällysteiset tabletit on tarkoitettu
Osio VI: Yhteenveto riskienhallintasuunnitelman toimista VI.2 VI.2.1 Julkisen yhteenvedon osat Tietoa sairauden esiintyvyydestä Lääkevalmiste Dormix 12,5 mg ja 25 mg kalvopäällysteiset tabletit on tarkoitettu
Kovaltry-valmisteen (oktokogialfa) riskienhallintasuunnitelman yhteenveto
 EMA/1560/2016 Kovaltry-valmisteen (oktokogialfa) riskienhallintasuunnitelman yhteenveto Tämä on Kovaltry-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet, joiden avulla
EMA/1560/2016 Kovaltry-valmisteen (oktokogialfa) riskienhallintasuunnitelman yhteenveto Tämä on Kovaltry-valmisteen riskienhallintasuunnitelman (RMP) yhteenveto, jossa esitetään toimenpiteet, joiden avulla
VALMISTEYHTEENVETO. Shampoo Viskoosi liuos, joka on väriltään kirkkaan oljenkeltainen tai vaaleanoranssi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Sebiprox 1,5 % shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g shampoota sisältää 1,5 g siklopiroksiolamiinia (1,5% w/w). Täydellinen apuaineluettelo, ks.
VALMISTEYHTEENVETO. Päänahan seborrooinen ekseema ja muu päänahan hilseily (pityriasis capitis). Pityriasis versicolor.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Nizoral 20 mg/ml shampoo 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml sisältää ketokonatsolia 20 mg. Täydellinen apuaineluettelo, ks. kohta 6.1. 3. LÄÄKEMUOTO
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS
 LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
LIITE III VALMISTEYHTEENVEDON JA PAKKAUSSELOSTEEN MUUTOS Nämä muutokset valmisteyhteenvetoon ja pakkausselosteeseen ovat voimassa Komission päätöksestä. Jäsenvaltioiden viranomaiset päivittävät valmistetiedot
RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Geloplasma, infuusioneste, liuos 13.9.2016, Versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Yhteenveto hoidon hyödyistä Nestetilavuus vähenee, kun soluvälitilasta
Geloplasma, infuusioneste, liuos 13.9.2016, Versio 4.0 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Yhteenveto hoidon hyödyistä Nestetilavuus vähenee, kun soluvälitilasta
Nexplanon. 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Nexplanon 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Implanon ja Implanon NXT/Nexplanon ovat pitkävaikutteisia
Nexplanon 30.3.2016, versio 5.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Implanon ja Implanon NXT/Nexplanon ovat pitkävaikutteisia
Liite I. Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle
 Liite I Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1 Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1. Pneumokefalus: Karmustiini-implantteihin
Liite I Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1 Tieteelliset päätelmät ja perusteet myyntiluvan (-lupien) ehtojen muuttamiselle 1. Pneumokefalus: Karmustiini-implantteihin
Lescol / Lescol Depot. 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Lescol / Lescol Depot 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Korkea kolesteroli tarkoittaa kolesterolin
Lescol / Lescol Depot 29.12.2014, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 Julkisen yhteenvedon osiot VI.2.1 Tietoa sairauden esiintyvyydestä Korkea kolesteroli tarkoittaa kolesterolin
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
