Reaktiokinetiikka katalyytin vaikutus reaktionopeuteen
|
|
|
- Olavi Karjalainen
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 Reaktiokinetiikka katalyytin vaikutus reaktionopeuteen Helsingin yliopisto Matemaattis-luonnontieteellinen tiedekunta Kemian laitos Kemian opettajankoulutusyksikkö Kandidaatintutkielma Tekijä: Ida Ståhle Pvm Ohjaaja: Maija Aksela Tarkastajat: Maija Aksela Raimo Timonen
2 Sisällysluettelo 1 Johdanto Katsaus reaktiokinetiikan tutkimuksen historiaan Reaktiokinetiikkaa Määritelmä Törmäysteoria Reaktionopeuteen vaikuttaminen Katalyytin vaikutus reaktiossa Yleistä Homogeeninen ja heterogeeninen katalyysi Entsyymit Yhteenveto LÄHTEET... 21
3 1 Johdanto Reaktiokinetiikka on merkittävä kemian osa-alue. Sitä on tutkittu jo 1700-luvulta lähtien (Hudson, 1995). Kemiallisten reaktioiden ymmärtäminen on yksi tärkeimmistä kemian aiheista. On tärkeää ymmärtää tekijöitä, jotka vaikuttavat reaktionopeuteen. (Laidler, 1969). Tässä tutkimuksessa esitellään joitain reaktionopeuteen vaikuttavia tekijöitä. Tämä tutkimus on rajattu tukemaan tekemääni pro gradu tutkielmaa, jossa käsitellään reaktiokinetiikan opetusta lukiossa. Tutkimuksen rajaamisessa on huomioitu lukion opetussuunnitelman perusteissa määritellyt reaktiokinetiikkaan liittyvät käsitteet ja teoriat (LOPS, 2003). Luvussa kaksi esitellään reaktiokinetiikan tutkimuksen historiaa. Reaktiokinetiikkaa on tutkittu yli 300 vuoden ajan ja edelleen tutkijat ovat osittain tyytymättömiä kehitettyihin malleihin ja teorioihin. (Laidler, 1969). Luvussa kolme määritellään ensin reaktiokinetiikka ja siihen liittyviä käsitteitä ja laskukaavoja. Käsitteiden ja kaavojen määrittely luo pohjan tutkimukselle. Kolmannessa luvussa esitellään myös törmäysteoria, joka on yksi tapa selittää miksi kemiallisia reaktioita tapahtuu. Törmäysteoria valittiin tähän tutkimukseen, koska se kuuluu lukion oppimäärään. Kolmannen luvun viimeisessä osassa esitellään reaktionopeuteen vaikuttavista tekijöistä konsentraatio ja lämpötila. Tutkimuksen neljännessä luvussa käsitellään katalyyttien vaikutusta reaktionopeuteen. Luvun alussa katalyytit esitellään yleisesti. Sen jälkeen luvussa 4.2 kerrotaan heterogeenisista ja homogeenisista katalyyteistä. Luvussa 4.3 esitellään entsyymit. 1
4 2 Katsaus reaktiokinetiikan tutkimuksen historiaan Luultavasti ensimmäisen reaktiokinetiikka- eli reaktionopeustutkimuksen teki Carl Wenzel ( ) vuonna Hänen teki tutkimuksen, jossa hän pyrki järjestämään metallit sen mukaan, kuinka nopeasti tietty määrä metallia liukenee happoon. Tutkimuksessaan hän vaihteli hapon väkevyyttä ja huomasi, että hapon konsentraation pienentyessä puoleen kaksinkertaistui liukenemisaika. (esim. Hudson, 1995). Wenzelin jälkeen Henrich Rose ( ) tutki bariumsulfaatin ja natriumkarbonaatin välistä reaktiota. Hän huomasi, että jos aineita oli yhtä paljon, alle 10 prosenttia niistä muuttui natriumsulfaatiksi ja bariumkarbonaatiksi. Jos natriumkarbonaattia oli 15-kertainen määrä, kaikki bariumsulfaatti muuttui bariumkarbonaatiksi. (esim. Hudson, 1995). Vuonna 1850 Ludwig Ferdinand Wilhelmy ( ) julkaisi ensimmäiset perusteelliset kinetiikantutkimustulokset. Wilhelmy tutki sukroosin hydrolyysiä ja huomasi, että sukroosikonsentraatio pieneni kaavan MZS (2-1) mukaan, jossa M on vakio, Z on sukroosin konsentraatio annetulla ajanhetkellä ja S on hapon konsentraatio. Hän havaitsi myös hapon konsentraation pysyvän samana koko reaktion ajan. Wilhelmyn työt tulivat tunnetuksi vasta kolmekymmentä vuotta myöhemmin. (Hudson, 1995). Tällä välillä reaktiokinetiikan tutkimusta jatkoivat muun muassa Marclin Berthelot ( ) ja Léon Péan de Saint-Gilles ( ), jotka tutkivat etikkahapon ja etanolin reaktiota. He huomasivat, että reaktionopeus oli suoraa verrannollinen reagoivien aineiden määriin ja kääntäen verrannollinen järjestelmän tilavuuteen. (esim. Hudson, 1995). Myös norjalaiset Cato Maximilian Guldberh ( ) ja Peter Waage ( ) tekivät omia tutkimuksiaan vuonna He kehittivät kaavan, jolle he antoivat nimeksi massavaikutuksen laki. Kaavan mukaan, jos aineiden A ja B reagoidessa keskenään muodostuu uusia aineita A ja B, vaikuttaa aineiden välillä voima kpq, (2-2) 2
5 jossa k on vakio, jota he nimittivät affiniteettikertoimeksi ja p ja q ovat reaktioon osallistuvien aineiden aktiiviset massat eli konsentraatiot. Lauseke kpq on yhtä suuri kuin aineiden A ja B massa, joka muuttuu aikayksikössä aineiksi A ja B. Tasapainossa reaktiota lähtöaineisiin ja tuotteisiin vievät voimat ovat yhtä suuret eli kpq=k p q. (2-3) Lopputulos muistuttaa modernia tasapainolakia. Guldbergin ja Waagen julkaisu vuonna 1864 oli norjankielinen eikä siksi saanut osakseen paljonkaan huomiota. Ranskankielinen versio julkaistiin kolme vuotta myöhemmin. Seuraavien vuosien aikana useat tutkijat saivat vastaavia tuloksia tasapainolain erikoistapauksista tietämättä norjalaisten töistä. Vuonna 1879 norjalaiset julkaisivat uudelleen tuloksensa ja esittivät, että muiden tutkijoiden työt vahvistivat heidän tuloksensa. (esim. Hudson, 1995) Samaan aikaan, kun norjalaiset julkaisivat työnsä ensimmäisen kerran, ranskassa Augustus Vernon Harcourt ( ) ja William Esson ( ) tekivät vastaavanlaisia tutkimuksia irreversiibeleillä reaktioilla. Näin he pystyivät keskittymään pelkästään kemiallisen kinetiikan tutkimiseen. He tutkivat kolmenkymmenen vuoden ajan hydrisen peroksidin ja hydrisen jodin reaktiota happamassa liuoksessa H 2 O 2 + 2HI 2 H 2 O + I2 (2-4) Tuhansissa huolellisissa kokeissaan Harcourt ja Essen havaitsivat reaktionopeuden riippuvan reaktioon osallistuvien aineiden konsentraatioista. He huomasivat myös, että lämpötila vaikutti reaktionopeuteen. 10 o C lämpötilannousu lähes kaksinkertaisti reaktionopeuden. Ekstrapoloimalla he päättelivät myös, ettei reaktioita tapahdu enää -272,6 celsiusasteen lämpötilassa. (esim. Hudson, 1995) 1800-luvun lopussa kemialliseen kinetiikkaa tarttui moni muukin tutkija. Jacobus Henricus van t Hoff ( ) oli heistä tunnetuin. Hän esitti kirjassaan Études de dynamique chimique katsauksen omiin töihinsä sekä muiden töihin vuonna Teos käsitteli reaktiokinetiikan, reaktiomekanismien ja reaktionopeuden lämpötilariippuvuuden välisiä suhteita. van t Hoff tutki kinetiikan lisäksi myös tasapainoja. Tutkimuksissaan hän huomasi, 3
6 että lämpötilan muuttaminen vaikutti reaktion tasapainotilaan. Hän kehitti tutkimuksiensa perusteella liikkuvan tasapainon periaatteen, jonka mukaan lämpötilan nousu suosii endotermisiä reaktioita. (esim. Hudson, 1995). van t Hoffin kirjan ilmestymisen aikoihin ranskalainen Henri Louis Le Châtelier ( ) esitti nimeään kantavan periaatteen. Le Châtelier n periaatteen mukaan, dynaamisessa tasapainossa olevan järjestelmän tilaa muutettaessa, se reagoi pyrkimällä pienentämään aiheutettua muutosta. van t Hoffin periaate on le Châtelier n periaatteen erikoistapaus. (esim. Hudson, 1995). Ruotsalainen Svante Arrhenius ( ) tutki vuonna 1889 syitä reaktionopeuden suureen kasvuun pienenkin lämpötilan nousun seurauksena. Kineettinen teoria ei hänen mukaansa riittänyt selittämään ilmiötä. Jo vuonna 1867 Leopold Pfaundler ( ) oli ehdottanut, että kemialliseen muutokseen osallistuvat ainoastaan kriittisen energian saaneet molekyylit. James Clerk Maxwell ( ) oli tutkinut molekyylien nopeuksia. Maxwell huomasi, että runsas energeettisten molekyylien lukumäärä kasvoi lämpötilan noustessa. Näiden tutkimusten perusteella Arrhenius ehdotti, että kemialliseen reaktioon pystyvät ainoastaan suuren energian molekyylit, ja että näiden molekyylien määrä on korkeissakin lämpötiloissa pieni molekyylien kokonaismäärään verrattuna. Arrhenius ehdotti lämpötiloissa T 0 ja T 1 olevien reaktiovakioiden k 0 ja k 1 väliseksi yhtälöksi kk 1 = kk 0 qq (TT1 TT0) 2TT1TT0 (2-5) Nykyisin tämä yhtälö esitetään yleensä muodossa kk = AA EE RRRR (2-6) ja tunnetaan nimellä Arrheniuksen yhtälö. (esim. Hudson, 1995). Arrheniuksen yhtälöstä kerrotaan lisää tämän tutkimuksen luvussa luvulla kinetiikan tutkimus on edistynyt merkittävästi. On pystytty määrittelemään muun muassa reaktiovakioita ja reaktioiden kertalukuja. Merkittävimpiä 1900-luvun löytöjä on myös törmäysteorian kehittäminen. Vuonna 1917 saksalainen Max Trautz ( ) ja 4
7 englantilainen William Lewis ( ) ehdottivat, toisistaan tietämättä, että molekyylien törmäystiheys määrittelee reaktionopeuden. (A Brief History of Chemical Kinetics, ) Vuonna 1935 yhdysvaltalainen Henry Eyring ( ) esitteli teorian nimeltä absoluuttinen reaktionopeus teoria (tai aktivoidun kompleksin teoria). Eyringin teorian mukaan reaktiot tapahtuvat kahdessa vaiheessa. Ensimmäisessä vaiheessa lähtöaineet muuttuvat aktivoiduksi kompleksiksi. Toisessa vaiheessa nämä kompleksit hajoavat määrätyllä nopeudella. Nykyisin teoria tunnetaan nimellä siirtymätilateoria. (A Brief History of Chemical Kinetics, ) 5
8 3 Reaktiokinetiikkaa Tässä luvussa määritellään ensin mitä reaktiokinetiikalla tarkoitetaan. Sen jälkeen luvussa 3.2 kerrotaan kemiallisen reaktion tapahtumisen edellytyksistä. Luvussa 3.3 tehdään vielä lyhyt katsaus reaktionopeuteen vaikuttaviin tekijöihin. 3.1 Määritelmä Kinetiikka voidaan jakaa fysikaaliseen ja kemialliseen kinetiikkaan. Fysikaalinen kinetiikka tutkii fysikaalisia ilmiöitä kuten diffuusiota ja viskositeettia. Kemiallinen kinetiikka tutkii kemiallisia ilmiöitä kuten kemiallisen reaktion nopeutta (Connors, 1990). Tässä tutkimuksessa keskitytään kemialliseen kinetiikkaan ja reaktionopeuteen. Kemiallinen kinetiikka käsittelee ajan kuluessa tapahtuvia kemiallisia muutoksia. Muutokset voivat tapahtua missä tahansa olomuodossa. Homogeenin reaktio on sellainen, jossa muutokset tapahtuvat yhdessä faasissa. Heterogeeninen reaktio puolestaan tapahtuu kahden faasin rajapinnalla. (esim. Steinfeld et al, 1998). Kemiallinen muutos, joka tapahtuu jonkin reaktion kautta, voidaan esittää esimerkiksi näin aa + bb cc + dd (3-1) jossa pienet kirjaimet (a, b, c ja d) kuvaavat reaktion stoikiometrisiä kertoimia. (esim. Steinfeld et al, 1998). Reaktionopeus, R, tarkoittaa reaktioseoksen koostumuksen muutosta ajan kuluessa. Reaktion (3-1) lähtöaineille reaktionopeus voidaan laskea seuraavasti 1 d R = a dt [ A] 1 d[ B] = b dt (3-2) 6
9 Hakasulkeita käytetään kuvaamaan aineen konsentraatiota eli [X] tarkoittaa aineen X konsentraatiota. Miinusmerkki yhtälössä tarkoittaa, että aineen konsentraatio pienenee reaktion edetessä. Plusmerkki kertoo, että aineen konsentraatio kasvaa reaktion edetessä. Reaktiotuotteille voidaan kirjoittaa kaava 1 d R = + c dt [ C] 1 d[ D] = + d dt (3-3) Kertoimet a, b, c ja d kaavoissa (3-2) ja (3-3) viittaavat reaktion (3-1) stoikiometrisiin kertoimiin. Lähtöaineiden ja tuotteiden konsentraatiot liittyvät reaktioyhtälöön (3-1), joten reaktion nopeus voidaan laskea, jos tiedetään yhdenkin aineen konsentraation muutos reaktion kuluessa. (esim. Steinfeld et al, 1998). Reaktionopeudelle on monia eri yksiköitä. Reaktionopeuden, R, yksikkö koostuu seuraavista osista tai [aineen määrä][tilavuus] -1 [aika] -1 [konsentraatio][aika] -1 SI-järjestelmän mukainen yksikkö konsentraatiolle on moolia per kuutiodesimetri (mol dm -3 ). (Steinfeld et al, 1998). Yleinen yksikkö reaktionopeudelle on moolia kuutiodesimetrissä sekunnissa (mol dm -3 s -1 ). Kaasufaasissa tapahtuville reaktioille voidaan käyttää yksikköä molekyyliä kuutiosenttimetrissä sekunnissa (molekyyli cm -3 s -1 ). Heterogeenisille reaktioille reaktionopeus ilmaistaan usein mooleina kuutiometrissä sekunnissa (mol m -3 s -1 ). (esim. Atkins & de Paula, 2010). Reaktionnopeuslaki reaktiolle (3-1) kirjoitetaan v = k r [A][B] (3-4) jossa k r on reaktionopeuskerroin. Reaktionopeuskerroin on konsentraatioriippumaton, mutta se riippuu lämpötilasta. Reaktionopeuskertoimen yksikkö määräytyy konsentraation yksikön 7
10 mukaan. Esimerkiksi kaavassa (3-4) reaktiovakion k r yksikkö on mol dm -3 s -1. (esim. Atkins & de Paula, 2010). Yleisesti reaktionopeuslaki kirjoitetaan muotoon v = k r [A] a [B] b (3-5) Tämä kaava kuvaa eri tekijöiden konsentraation vaikutuksen voimakkuutta reaktion nopeuteen. Tätä vaikutusta kutsutaan reaktion kertaluvuksi. Kemiallisilla reaktioilla voi olla erilaisia kertalukuja. Reaktion kertaluvun ei tarvitse olla kokonaisluku. Kaasufaasissa tapahtuvilla reaktioilla kertaluvut eivät usein ole kokonaislukuja. Nollannen kertaluvun reaktio ei ole lainkaan riippuvainen konsentraatiosta, jolloin sen nopeuslaki voidaan kirjoittaa v = k r (3-6) Entsyymireaktiot ovat usein nollannen kertaluvun reaktioita. Niissä entsyymille sopivaa reagenssia on läsnä ylimäärin, jolloin entsyymi määrittelee reaktionopeuden reagenssin sijaan. Jos reaktionnopeuslaki ei ole samaa muotoa kuin laki (3-5), reaktiolla ei ole kokonaiskertalukua. (esim. Atkins & de Paula, 2010). Konsentraation lisäksi monet muut tekijät, kuten paine, lämpötila ja katalyytti, voivat vaikuttaa nopeuteen, jolla reaktio tapahtuu. Näitä tekijöitä tarkastellaan lähemmin luvussa Törmäysteoria Tässä luvussa esitellään lyhyesti törmäysteoria, joka on yksinkertaisin tapa selittää, miksi kemialliset reaktiot tapahtuvat. Sitä voidaan käyttää yksinkertaisten hiukkasten kaasufaasissa tapahtuvien reaktioiden selittämiseen. (esim. Atkins & de Paula, 2010). Törmäysteoria perustuu siihen, että molekyylien on kohdattava ja reaktio tapahtuu vain, jos molekyyleillä on tietty minimienergia (esim. Atkins & de Paula, 2010). 8
11 Kuvassa 3.1 esitetään, miten väärässä suunnassa toisiinsa törmäävät molekyylit eivät reagoi keskenään. Kuva 3.1 Molekyylien on törmättävä oikeassa suunnassa toisiinsa, jota reaktio tapahtuu. (Talktalk, 2010) Molekyylien törmäyssuunta vaikuttaa siihen, tapahtuuko reaktio vai ei. Sen lisäksi molekyylien energia vaikuttaa siihen, reagoivatko molekyylit vai eivät luvulla Svante Arrhenius esitteli ensimmäisenä käsitteen aktivoitumisenergia. (esim. Zumdahl & Zumdahl, 2003). Kuvassa 3.2 on esitetty eksotermisen reaktion energiaprofiili. Kuva 3.2 Eksotermisen reaktion energiaprofiili. Reaktion potentiaalienergian muutos reaktion etenemisen funktiona (Pieniniemi, 2010) 9
12 Kuvassa 3.2 lähtöaineet ovat tietyllä energiatasolla ja tuotteet ovat toisella energiatasolla. Lähtöaineista tulee tuotteita siirtymäkompleksin kautta. Siirtymäkompleksin muodostuminen vaatii energiaa, jota kutustaan aktivoitumisenergiaksi. Yhteenvetona törmäysteoriasta voi sanoa, että reaktio vaatii tapahtuakseen energiamäärän, joka ylittää reaktion aktivoitumisenergian ja lisäksi reagoivien molekyylien on törmättävä toisiinsa oikeassa suunnassa. (esim. Zumdahl & Zumdahl, 2003). Kun nämä asiat huomioidaan, voidaan reaktionopeuskerroin esittää seuraavasti k E a / RT = zpe (3-7) jossa z on törmäystiheys, p on steerinen kerroin, joka kuvaa oikeassa suunnassa tapahtuvia törmäyksiä ja E a RT e / kuvaa sitä osaa törmäyksistä, joilla on riittävän suuri energia. 3.3 Reaktionopeuteen vaikuttaminen Tässä luvussa esitellään joitain reaktionopeuteen vaikuttavia tekijöitä. Esiteltäviksi tekijöiksi on valittu konsentraatio, lämpötila ja katalyytti. Katalyytin vaikutusta reaktionopeuteen käsitellään tarkemmin luvussa neljä. Näiden lisäksi reaktionopeuteen vaikuttaa muun muassa paine. Käytännössä kaikkien reaktioiden reaktionopeus riippuu yhden tai useamman aineen konsentraatiosta. Joissain tapauksissa reaktionopeus voi riippua myös jonkin reaktion välituotteena syntyvän aineen konsentraatiosta. Katalyytit ovat esimerkki aineesta, jota ei näy stoikiometrisessä reaktioyhtälössä, mutta niiden konsentraatio voi olennaisesti muuttaa reaktion nopeutta. (esim. Steinfeld et al, 1998). Luvussa 3.1 esiteltiin reaktionopeuden laskukaavoja (kaavat 3-2, 3-3, 3-4 ja 3-5), joissa konsentraatio on keskeinen tekijä. Kaavoista nähdään, että reaktionopeus riippuu reagoivien aineiden konsentraatioista. Useimpien kemiallisten reaktioiden nopeus on riippuvainen lämpötilasta. Svante Arrhenius esitti ensimmäisenä tämän riippuvuuden kvantitatiivisesti. Arrheniuksen kaavaa käytetään edelleen laajasti. Hän esitti seuraavaa riippuvuutta reaktiokertoimen k ja absoluuttisen lämpötilan T välillä (Amdur & Hammes, 1966) 10
13 k E a RT = Ae (3-4) jossa R on kaasuvakio, A lämpötilasta riippumaton taajuustekijä (törmäystekijä) ja E a tarkoittaa aktivoitumisenergiaa (vrt. kaava 3-7). Aktivoitumisenergia on pienin reaktion toteutumiseen vaadittava kineettinen energia. Mitä korkeampi reaktion aktivoitumisenergia on sitä, sitä enemmän reaktionopeus riippuu lämpötilasta. Jos aktivoitumisenergia on nolla, reaktio ei riipu lämpötilasta. Joissain tapauksissa aktivoitumisenergia on negatiivinen, mikä tarkoittaa, että reaktio hidastuu lämpötilan kasvaessa. (esim. Atkins & de Paula, 2010). Arrheniuksen yhtälö voidaan esittää myös kuvaajana, kuten kuvassa 3.3. Kuva 3.3. Jos reaktio noudattaa Arrheniuksen yhtälöä, on ln k ja 1/T välinen riippuvuus lineaarinen. (Atkins & de Paula, 2010) Kuvaajassa 3.3 esitetään tekijöiden ln k ja 1/T välinen riippuvuus. Kuvaajan ollessa suora on reaktio Arrheniuksen yhtälön mukainen. Suoran kulmakerroin on kaavassa (2-4) oleva termi E a /R ja kohta, jossa 1/T =0 on kaavan termi ln A. (esim. Atkins & de Paula, 2010). Lämpötilan vaikutus reaktionopeuteen voidaan selittää törmäysteorian avulla. Lämmittämällä reagensseja, niille annetaan lisää energiaa. Hiukkaset alkavat myös liikkua nopeammin. Näin ollen törmäyksiä tapahtuu enemmän ja niillä on tarpeeksi energiaa, jotta kemiallinen reaktio tapahtuisi. (esim. Zumdahl & Zumdahl, 2003). 11
14 4 Katalyytin vaikutus reaktiossa Tässä luvussa perehdytään katalyytin vaikutukseen kemiallisessa reaktiossa. Luvussa 4.1 määritellään katalyytit. Luvussa 4.2 tutustutaan heterogeeniseen ja homogeeniseen katalyysiin. Entsyymit on esitelty luvussa Yleistä Monilla reaktioilla on jokin reaktiota rajoittava vaihe. Rajoittavalla vaiheella tarkoitetaan vaihetta, joka on merkittävästi hitaampi kuin reaktion muut vaiheet ja hidastaa siksi kokonaisreaktion nopeutta. Useimmiten toivottu reaktionopeus on samalla suurin mahdollinen nopeus jollekin reaktiolle. Reaktionopeutta voidaan nostaa nostamalla lämpötilaa, mutta se ei aina ole järkevä ratkaisu. Suuri lämpötilan nosto saattaa aiheuttaa ei-toivottuja sivureaktioita tai aiheuttaa epäpuhtauksia saantoon. Tällaisissa tilanteissa katalyytti on käytännöllinen ratkaisu. Sana katalyytti on johdettu kahdesta kreikankielen sanasta, jotka tarkoittavat alas ja löystyä. Tällä viitataan katalyytin kykyyn alentaa aktivoitumisenergiaa sekä löysentää kemiallisia sidoksia. (Steinfeld et al, 1998). Katalyytti osallistuu reaktion siirtymätilaan ja vapautuu reaktion lähetessä loppuaan samassa muodossa kuin se oli reaktion alkaessa. Katalysoitu reaktio voidaan määritellä reaktiovaiheiden määrän tai luonteen muutoksena katalyytin vaikutuksesta. (Panchekov & Lebedev, 1976). Katalyytin C vaikutus hitaassa reaktiossa A B voidaan kirjoittaa seuraavasti A + C B + C (4-1) Kaavassa (4-1) katalyytti on samassa muodossa lähtöaineissa ja reaktiotuotteissa. Se ei muutu reaktion kuluessa. (esim. Steinfeld et al, 1998). Kuvassa 4.1 esitetään katalyytin vaikutusta reaktion kulkuun. 12
15 Kuva 4.1. Katalyytin vaikutus reaktion kulkuun. (Wayne s world, 2010) Kuvasta 4.1 nähdään, että ilman katalyyttia reaktion aktivoitumisenergia on korkea ja reaktio etenee hitaasti. Katalyytti muuttaa reaktion kulkureittiä siten, että aktivoitumisenergia pienenee ja reaktio nopeutuu. Katalyytti toimii tarjoamalla reaktiolle vähemmän energiaa vaativan reitin. (esim. Zumdahl & Zumdahl, 2003). Kuvassa 4.2 esitetään, kuinka katalyytti lisää reaktioon johtavien törmäysten määrää. Kun reaktio vaatii vähemmän energiaa tapahtuakseen, suurempi osa molekyylien välisistä tömäyksistä johtaa reaktioon. Katalyytti ei kuitenkaan vaikuta reaktion kokonaisenergiaan. (esim. Zumdahl & Zumdahl, 2003). 13
16 Kuva 4.2 Katalyytin vaikutus reaktioon johtavien törmäysten määrään (Zumdahl & Zumdahl, 2003) Ihminen tarvitsee biologisia katalyyttejä, entsyymejä, toimiakseen (ks. luku 4.3). Teollisuudessa katalyyttejä käytetään nopeuttamaan reaktioita ja siten pienentämään tuotantokustannuksia. Useiden teollisuudelle tärkeiden reaktioiden nopeuttaminen pelkästään lämpötilaa nostamalla olisi liian kallista. (esim. Zumdahl & Zumdahl, 2003). 4.2 Homogeeninen ja heterogeeninen katalyysi Katalyytit voidaan jakaa homogeenisiin ja heterogeenisiin katalyytteihin. Homogeeninen katalyytti on samassa faasissa kuin reagoivat aineet. Heterogeeninen katalyytti on eri faasissa kuin reagoivat aineet, yleensä kiinteänä aineena. (esim. Zumdahl & Zumdahl, 2003). Heterogeeninen katalyysi tapahtuu useimmiten siten, että reagoiva aine on kaasufaasissa ja absorboituu kiinteän katalyytin pinnalle. Esimerkki heterogeenisesti katalysoidusta reaktiosta on tyydyttymättömän hiilivedyn hydraus. Hydraus on tärkeä teollisuuden prosessi, jota käytetään muuttamaan tyydyttymättömät, öljynä esiintyvät, rasvat tyydyttyneiksi rasvoiksi, joissa hiili-hiili-kaksoissidokset on korvattu yksinkertaisilla hiili-hiili sidoksilla. Reaktio tapahtuu kaasufaasissa ja sen reaktioyhtälö on C 2 H 4 (g) + H 2 (g) C 2 H 6 (g) (4-2) Normaalilämpötilassa reaktio on melko hidas. Tämä johtuu pääasiallisesti vedyn voimakkaasta sidoksesta, joka nostaa reaktion aktivoitumisenergiaa. Reaktiota voidaan 14
17 nopeuttaa käyttämällä platinaa, palladiumia tai nikkeliä kiinteänä katalyyttinä. (esim. Zumdahl & Zumdahl, 2003). Kuvassa 4.3 esitetään eteenin heterogeenisesti katalysoitu hydrausreaktio. Kuva 4.3. Eteenin hydrausreaktio heterogeenisesti katalysoituna. (Zumdahl & Zumdahl, 2003) Kuvasta 4.3 nähdään, että alussa molekyylit ovat metallipinnan yläpuolella. Seuraavassa vaiheessa vety absorboituu metallin pinnalle, ja vetyatomien väliset sidokset katkeavat. Myös eteenin π-sidos katkeaa ja sen tilalle muodostuu metalli-hiili sidokset. Kolmannessa vaiheessa atomit liikkuvat toisiaan kohti metallin pinnalla ja muodostavat uusia hiili-vety-sidoksia. Viimeisessä vaiheessa etaani molekyyli irtoaa metallin pinnasta. Katalyytin päätehtävä tässä reaktiossa on heikentää voimakasta vety-vety-sidosta muodostamalla vety-metalli-sidoksia. (esim. Zumdahl & Zumdahl, 2003). 15
18 Heterogeenisessä katalyysissä on yleensä neljä vaihetta. Ensimmäisessä vaiheessa reagenssit absorboituvat katalyytin pinnalle ja aktivoituvat. Toisessa vaiheessa katalyytin pinnalla olevat reagenssit liikkuvat lähemmäs toisiaan. Kolmannessa vaiheessa reagenssit muodostavat uusia sidoksia keskenään. Viimeisessä vaiheessa tuotteet irrottautuvat katalyytin pinnasta. Homogeeninen katalyytti on samassa faasissa kuin reagoivat molekyylit. Reaktiot tapahtuvat yleensä neste- tai kaasufaaseissa. Homogeeninen katalyytti voi olla todella tehokas. Esimerkiksi vetyperoksidin hajoamisreaktion aktivoitumisenergia on 76 kj/mol ja huoneenlämmössä reaktio on hidas. Kun vetyperoksidiin lisätään vähän jodidi-ionia, aktivoitumisenergia putoaa 56 kj/mol ja reaktionnopeus kasvaa 2000-kertaisesksi. (esim. Atkins & de Paula, 2010). Yksi tunnetuimmista esimerkeistä homogeenisen katalyytin toiminnasta on otsonin muodostuminen troposfäärissä. Typpimonoksidia (NO) muodostuu luonnostaan ilmakehässä typpi- ja happimolekyylien reagoidessa keskenään. Reaktio on kuitenkin hyvin hidas normaalilämpötilassa, koska typpimolekyylien kolmoissidokset ja happimolekyylien kaksoissidokset ovat hyvin voimakkaita. Korkeissa lämpötiloissa, kuten autojen polttomoottoreissa, reaktio nopeutuu. Osa typpimonoksidista muutetaan typpikaasuksi auton katalysaattorissa, mutta osa siitä vapautuu ilmakehään. Typpimonoksidi reagoi hapen kanssa muodostaen typpidioksidia NO (g) + ½ O 2 (g) NO 2 (g) (4-3) Ilmakehässä typpidioksidi absorboi valoa ja hajoaa seuraavasti NO 2 (g) vvvvvvvvvv NO (g) + O (g) (4-4) Vapaa happiatomi on hyvin reaktiivinen. Se voi reagoida happimolekyylien kanssa muodostaen otsonia O (g) + O 2 (g) O 3 (g) (4-5) Otsoni voi edelleen reagoida muiden ilmansaasteiden kanssa muodostaen aineita, jotka ärsyttävät ihmisten silmiä ja keuhkoja. Otsoni on myrkyllistä myös itsekseen. Tässä 16
19 reaktiosarjassa typpimonoksidi toimii katalyyttinä, joka nopeuttaa otsonin muodostumista alailmakehässä. Typpimonoksidi ei kulu reaktiossa vaan vapautuu muuttumattomana, kuten reaktioyhtälöstä (4-4) nähdään. (esim. Zumdahl & Zumdahl, 2003). 17
20 4.3 Entsyymit Biologiset entsyymit ovat elämälle tärkeä katalyyttiluokka. Entsyymit ovat useimmiten proteiinimolekyylejä, jotka ovat evoluution myötä muuttuneet hyvin spesifeiksi ja tehokkaiksi biokemiallisten reaktioiden toteuttajiksi elävissä organismeissa. (esim. Steinfeld et al, 1998). Entsyymit voivat muuttaa molekyylien orientaatiota reaktiolle suotuisammaksi. Entsyymit myös stabiloivat reaktion transitiotilaa. Ilman entsyymejä monien elimistön biologisten reaktioiden nopeus olisi lähes olematon. Entsyymit nopeuttavat reaktioita vähintään tekijällä (Stryer, 1999). Kuvassa 4.4 esitetään entsyymin toimintaperiaate. Kuva 4.4. Entsyymin toiminta kaaviokuvana. Substraatti voi olla esimerkiksi yksinkertainen sokeri. (AP Biology, 2010) Kuvassa 4.2 esitetty entsyymin epätasainen muoto kuvaa entsyymien spesifistä rakennetta, johon sopii vain tietynlainen substraatti. Substraatti voi olla mitä tahansa proteiinista yksinkertaiseen sokeriin tai RNA:han tai jopa kokonaiseen soluun. Substraatti sitoutuu entsyymin pinnalle ja sen sidokset heikentyvät. Reaktion lopussa substraatti irtoaa entsyymistä ja hajoaa reaktiotuotteiksi. Reaktion tapahduttua entsyymi vapautuu muuttumattomana ja voi reagoida uuden substraatin kanssa. (esim. Steinfeld et al, 1998). 18
21 Kuvan 4.4 reaktio voidaan esittää reaktioyhtälönä seuraavasti (4-6) Reaktioyhtälössä entsyymi E muuttaa substraattia S entsyymin ja substraatin kompleksiksi, ES, reaktiovakiolla k 1. Entsyymin ja substraatin kompleksilla on kaksi mahdollisuutta, se voi hajota takaisin entsyymiksi ja substraatiksi reaktiovakiolla k -1 tai se voi muuttua entsyymiksi ja reaktiotuotteeksi P reaktiovakiolla k 3. (Stryer, 1999). Reaktiosta (4-6) voidaan laskea tuotteen muodostumisnopeus Michaelis-Mentenin yhtälöllä V [ S] [ S] + K M = V max (4-7) jossa V max tarkoittaa reaktionopeutta silloin, kun entsyymi toimii täydellä teholla ja K M on Michaelisin vakio. Michaelsin vakio ilmoittaa substraatin konsentraation silloin, kun reaktio nopeus on puolet maksimistaan. (Stryer, 1999). Entsyymit ovat usein lämpötilaherkkiä. Jos reaktion lämpötila nousee liian korkeaksi, entsyymin toiminta loppuu. Liian kylmässä lämpötilassa entsyymin vaikutus taas on merkityksettömän pieni. Entsyymin optimaalista lämpötilaa ei ole helppo määritellä, koska se vaihtelee entsyymin ja substraatin konsentraatioiden mukaan. (Laidler, 1987) Jotkut pienet molekyylit tai ionit voivat estää entsyymien toiminnan. Entsyymin toiminnan estäviä hiukkasia kutustaan inhibiittoreiksi. Inhibiittorit voivat olla irreversiibeleitä, jolloin ne kiinnittyvät entsyymiin tiukasti ja irtoavat hyvin hitaasti. Reversiibeli inhibiittori hidastaa entsyymin katalysoimaa reaktiota kiinnittymällä löysästi entsyymin aktiiviseen kohtaan, irtoamalla jonkin ajan kuluttua ja estämällä siten entsyymin täydellistä toimintaa. (Stryer, 1999). 19
22 5 Yhteenveto Reaktiokinetiikkaa ja siihen liittyviä ilmiöitä on tutkittu yli 300 vuoden ajan. Reaktiokinetiikka voidaan määritellä tieteenä, joka tutkii muun muassa kemiallisten reaktioiden nopeuksia. Nopeuksien tutkimiseen liittyy käsitys siitä, miksi kemialliset reaktiot tapahtuvat. Yksi selitysmalli on törmäysteoria, jonka mukaan kemiallisia reaktioita tapahtuu vain, jos hiukkaset törmäävät toisiinsa oikeassa suunnassa ja niillä on tarpeeksi energiaa reaktion tapahtumiseksi. Tällä mallilla voidaan selittää yksinkertaisia kaasufaasissa tapahtuvia reaktioita. Lukio-opetuksessa törmäysteoria on keskeinen malli kemiallisten reaktioiden selittämisessä. Reaktiokinetiikan tutkimiseen liittyy myös reaktiota nopeuttavien ja hidastavien tekijöiden määrittely. Tässä tutkimuksessa reaktiota nopeuttavista tekijöistä esiteltiin konsentraatio, lämpötila ja katalyytit. Hidastavana tekijänä mainittiin entsyymin toiminnan estävä tai sitä hidastava inhibiittori. Konsentraation lisäys lisää reaktion nopeutta, koska se lisää hiukkasten määrää tietyssä tilavuudessa. Mitä enemmän hiukkasia, sitä suuremmalla todennäköisyydellä ne törmäävät oikeassa asennossa ja tarpeeksi suurella energialla. Lämpötilan nostaminen antaa hiukkasille lisää energiaa ja lisää niiden liikettä. Tämä johtaa jälleen useampiin törmäyksiin ja siten useampiin kemiallisiin reaktioihin. Lämpötilan nostaminen ei ole aina taloudellisesti kannattavaa tai muuten mahdollista. Tällöin reaktiota voidaan nopeuttaa sopivalla katalyytillä. Katalyytti tarjoaa reaktiolle reitin, joka vaatii vähemmän energiaa, ja nopeuttaa näin reaktiota. Katalyytti ei kulu itse reaktiossa eikä se vaikuta reaktion kokonaisenergiaan. Entsyymit ovat luonnon katalyyttejä, joita ilman eliöissä tapahtuvat biologiset reaktiot olisivat liian hitaita ylläpitämään elämää. Laidler sanoi jo vuonna 1969, että reaktionopeuteen vaikuttavien tekijöiden osaaminen on keskeistä kemian ymmärtämisen kannalta. Tässä tutkimuksessa perehdyttiin joihinkin reaktionopeuteen vaikuttaviin tekijöihin, mutta moni tekijä jäi vielä käsittelemättä. 20
23 LÄHTEET Amdur, I. & Hammes, G. (1966). Chemical Kinetics Principles and Selected Topics (s ). McGraw-Hill Book Company. Atkins, P. & de Paula, J. (2010). Atkins Physical Chemistry (9. painos, luvut 21-23). Oxford University press Connors, K. A. (1990) Chemical kinetics the study of reaction rates in solution. VCH Publishers. ng%20reaction%20kinetics&lr&hl=fi&pg=pa1#v=onepage&q&f=false ( ) Hudson, J. (1995). Suurin tiede kemian historia (s ). Art House. Lukion opetussuunnitelman perusteet Nuorille tarkoitetun lukiokoulutuksen opetussuunnitelman perusteet. (LOPS) Opetushallitus. Laidler, K. J. (1969). Theories of Chemical Reaction Rates. McGraw-Hill Book Company. Laidler, K. J. (1987). Chemical Kinetics (3. painos, s ). Harper & Row Publishers. Panchenkov, G. M. & Lebedev, V. P. (1976). Chemical kinetics and catalysis (19-22, ). MIR Publishers. Steinfeld, J. I., Francisco J. S. & Hase, W. L. (1998). Chemical Kinetics and Dynamics. Prentice Hall. Stryer, L. (1999). Biochemistry (4. painos, luku 8). W. H. Freeman and Company. Zumdahl, S. S. & Zumdahl, S. A. (2003). Chemistry (6. painos, luku 12). Houghton Mifflin Company. 21
24 Internet-lähteet A Brief History of Chemical Kinetics, (viitattu ) Kuvalähteet Kuva 3.1. Molekyylien törmäyssuunta (viitattu ) Kuva Endotermisen reaktion energiaprofiili 20REAKTIOYHT%C4L%D6.html (viitattu ) Kuva 3.3. Arrheniuksen yhtälö Piirretty Atkins & de Paula (2010) mukaan, Fig , s.799 Kuva 4.1. Katalyytin vaikutus Piirretty mukaan (viitattu ) Kuva 4.2. Katalyytin vaikutus reaktioon johtavien törmäysten määrään Piirretty Zumdahl & Zumdahl (2003) mukaan Fig , s. 589 Kuva 4.3. Eteenin hydrausreaktio heterogeenisesti katalysoituna Piirretty Zumdahl & Zumdahl (2003) mukaan Fig , s. 590 Kuva 4.4. Entsyymin vaikutus reaktion kulkuun (viitattu ) 22
Tasapainotilaan vaikuttavia tekijöitä
 REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
REAKTIOT JA TASAPAINO, KE5 Tasapainotilaan vaikuttavia tekijöitä Fritz Haber huomasi ammoniakkisynteesiä kehitellessään, että olosuhteet vaikuttavat ammoniakin määrään tasapainoseoksessa. Hän huomasi,
Esimerkiksi ammoniakin valmistus typestä ja vedystä on tyypillinen teollinen tasapainoreaktio.
 REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
REAKTIOT JA TASAPAINO, KE5 REAKTIOTASAPAINO Johdantoa: Usein kemialliset reaktiot tapahtuvat vain yhteen suuntaan eli lähtöaineet reagoivat keskenään täydellisesti reaktiotuotteiksi, esimerkiksi palaminen
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Luku 8. Reaktiokinetiikka
 Luku 8 Reaktiokinetiikka 234 8.1 Reaktion nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista
Luku 8 Reaktiokinetiikka 234 8.1 Reaktion nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista
Luku 2. Kemiallisen reaktion tasapaino
 Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Luku 2 Kemiallisen reaktion tasapaino 1 2 Keskeisiä käsitteitä 3 Tasapainotilan syntyminen, etenevä reaktio 4 Tasapainotilan syntyminen 5 Tasapainotilan syntyminen, palautuva reaktio 6 Kemiallisen tasapainotilan
Törmäysteoria. Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa
 Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Törmäysteoria Törmäysteorian mukaan kemiallinen reaktio tapahtuu, jos reagoivat hiukkaset törmäävät toisiinsa tarpeeksi suurella voimalla ja oikeasta suunnasta. 1 Eksotermisen reaktion energiakaavio E
Luento 9 Kemiallinen tasapaino CHEM-A1250
 Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luento 9 Kemiallinen tasapaino CHEM-A1250 Kemiallinen tasapaino Kaksisuuntainen reaktio Eteenpäin menevän reaktion reaktionopeus = käänteisen reaktion reaktionopeus Näennäisesti muuttumaton lopputilanne=>
Luku 21. Kemiallisten reaktioiden nopeus
 Luku 21. Kemiallisten reaktioiden nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista tasapainoreaktiota:
Luku 21. Kemiallisten reaktioiden nopeus Reaktiokinetiikka tarkastelee reaktioiden nopeuksia (vrt. termodynamiikka) reaktionopeus = konsentraation muutos aikayksikössä Tarkastellaan yksinkertaista tasapainoreaktiota:
Reaktiokinetiikan opetus lukiossa
 Reaktiokinetiikan opetus lukiossa Ida Ståhle Pro gradu tutkielma 8/2010 Kemian opettajan suuntautumisvaihtoehto Kemian koulutusohjelma Matemaattis-luonnontieteellinen tiedekunta Helsingin yliopisto Ohjaaja:
Reaktiokinetiikan opetus lukiossa Ida Ståhle Pro gradu tutkielma 8/2010 Kemian opettajan suuntautumisvaihtoehto Kemian koulutusohjelma Matemaattis-luonnontieteellinen tiedekunta Helsingin yliopisto Ohjaaja:
Kemiallinen reaktio
 Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Kemiallinen reaktio REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa eli aineenvaihduntareaktioissa,
Teddy 2. välikoe kevät 2008
 Teddy 2. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Teddy 2. välikoe kevät 2008 Vastausaikaa on 2 tuntia. Kokeessa saa käyttää laskinta ja MAOL-taulukoita. Jokaiseen vastauspaperiin nimi ja opiskelijanumero! 1. Ovatko seuraavat väitteet oikein vai väärin?
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Perjantai VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN
 Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
Kemian koe, Ke3 Reaktiot ja energia RATKAISUT Kannaksen lukio Perjantai 26.9.2014 VASTAA YHTEENSÄ KUUTEEN TEHTÄVÄÄN 1. A. Selitä käsitteet ja määritelmät (lyhyesti), lisää tarvittaessa kemiallinen merkintätapa:
4) Törmäysten lisäksi rakenneosasilla ei ole mitään muuta keskinäistä tai ympäristöön suuntautuvaa vuorovoikutusta.
 K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
K i n e e t t i s t ä k a a s u t e o r i a a Kineettisen kaasuteorian perusta on mekaaninen ideaalikaasu, joka on matemaattinen malli kaasulle. Reaalikaasu on todellinen kaasu. Reaalikaasu käyttäytyy
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia)
 ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
ENTSYYMIKATA- LYYSIN PERUSTEET (dos. Tuomas Haltia) Elämän edellytykset: Solun täytyy pystyä (a) replikoitumaan (B) katalysoimaan tarvitsemiaan reaktioita tehokkaasti ja selektiivisesti eli sillä on oltava
kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin?
 Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Esimerkki: Mihin suuntaan etenee reaktio CO (g) + H 2 O (g) CO 2 (g) + H 2 (g), K = 0,64, kun hiilimonoksidia ja vettä oli 0,0200 M kumpaakin ja hiilidioksidia ja vetyä 0,0040 M kumpaakin? 1 Le Châtelier'n
Lämpö- eli termokemiaa
 Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
Lämpö- eli termokemiaa Endoterminen reaktio sitoo ympäristöstä lämpöenergiaa. Eksoterminen reaktio vapauttaa lämpöenergiaa ympäristöön. Entalpia H kuvaa systeemin sisäenergiaa vakiopaineessa. Entalpiamuutos
KOTITEKOINEN PALOSAMMUTIN (OSA II)
 Johdanto KOTITEKOINEN PALOSAMMUTIN (OSA II) Monet palosammuttimet, kuten kuvassa esitetty käsisammutin, käyttävät hiilidioksidia. Jotta hiilidioksidisammutin olisi tehokas, sen täytyy vapauttaa hiilidioksidia
Johdanto KOTITEKOINEN PALOSAMMUTIN (OSA II) Monet palosammuttimet, kuten kuvassa esitetty käsisammutin, käyttävät hiilidioksidia. Jotta hiilidioksidisammutin olisi tehokas, sen täytyy vapauttaa hiilidioksidia
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe
 Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Kemian koe kurssi KE5 Reaktiot ja tasapaino koe 1.4.017 Tee kuusi tehtävää. 1. Tämä tehtävä koostuu kuudesta monivalintaosiosta, joista jokaiseen on yksi oikea vastausvaihtoehto. Kirjaa vastaukseksi numero-kirjainyhdistelmä
Lukion kemia 3, Reaktiot ja energia. Leena Piiroinen Luento 2 2015
 Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos
 ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
ympäristö ympäristö 15.12.2016 REAKTIOT JA ENERGIA, KE3 Ekso- ja endotermiset reaktiot sekä entalpian muutos Kaikilla aineilla (atomeilla, molekyyleillä) on asema- eli potentiaalienergiaa ja liike- eli
Nimi sosiaaliturvatunnus. Vastaa lyhyesti, selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
1. a) Seoksen komponentit voidaan erotella toisistaan kromatografisilla menetelmillä. Mihin kromatografiset menetelmät perustuvat? (2p) Menetelmät perustuvat seoksen osasten erilaiseen sitoutumiseen paikallaan
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
ELEC-C2210 Molekyyli- ja solubiologia
 ELEC-C2210 Molekyyli- ja solubiologia Entsyymikatalyysi Vuento & Heino ss. 66-75 ECB: Luku 3, s. 90-93 & luku 4, s. 144- Dos. Tuomas Haltia, Biotieteiden laitos, biokemia ja biotekniikka Miten entsyymit
ELEC-C2210 Molekyyli- ja solubiologia Entsyymikatalyysi Vuento & Heino ss. 66-75 ECB: Luku 3, s. 90-93 & luku 4, s. 144- Dos. Tuomas Haltia, Biotieteiden laitos, biokemia ja biotekniikka Miten entsyymit
CHEM-A1110 Virtaukset ja reaktorit. Laskuharjoitus 9/2016. Energiataseet
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 9/2016 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa D406 Energiataseet Tehtävä 1. Adiabaattisen virtausreaktorin
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia
 Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
Erilaisia entalpian muutoksia REAKTIOT JA ENERGIA, KE3 Erilaisille kemiallisten reaktioiden entalpiamuutoksille on omat terminsä. Monesti entalpia-sanalle käytetään synonyymiä lämpö. Reaktiolämmöllä eli
L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle 1
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]
![KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille]](/thumbs/24/3803781.jpg) KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
KAASUJEN YLEISET TILANYHTÄLÖT ELI IDEAALIKAASUJEN TILANYHTÄLÖT (Kaasulait) [pätevät ns. ideaalikaasuille] A) p 1, V 1, T 1 ovat paine tilavuus ja lämpötila tilassa 1 p 2, V 2, T 2 ovat paine tilavuus ja
Biomolekyylit ja biomeerit
 Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
Biomolekyylit ja biomeerit Polymeerit ovat hyvin suurikokoisia, pitkäketjuisia molekyylejä, jotka muodostuvat monomeereista joko polyadditio- tai polykondensaatioreaktiolla. Polymeerit Synteettiset polymeerit
REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE
 REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE Essi Purhonen 1, Krista Iltanen 1 & Sini Hänninen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Opettajan ohje Aihe: Ihmiskehossa
REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE Essi Purhonen 1, Krista Iltanen 1 & Sini Hänninen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Opettajan ohje Aihe: Ihmiskehossa
L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle Oppimistavoitteet
CHEM-C2230 Pintakemia L7 Kaasun adsorptio kiinteän aineen pinnalle Monika Österberg Barnes&Gentle, 2005, luku 8 Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle Oppimistavoitteet
Teddy 10. harjoituksen malliratkaisu syksy 2011
 Teddy. harjoituksen malliratkaisu syksy 2. Tarkastellaan reaktioketjua k O 3 O2 +O () O 2 +O k O 3 (2) O 3 +O k 2 O 2 +O 2 (3) Vakiotilaolettamuksen mukaan välituotteen konsentraatio pysyy vakiona lyhyen
Teddy. harjoituksen malliratkaisu syksy 2. Tarkastellaan reaktioketjua k O 3 O2 +O () O 2 +O k O 3 (2) O 3 +O k 2 O 2 +O 2 (3) Vakiotilaolettamuksen mukaan välituotteen konsentraatio pysyy vakiona lyhyen
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio:
 Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
Liittymis- eli additioreaktio Määritelmä, liittymisreaktio: REAKTIOT JA ENERGIA, KE3 Liittymis- eli additioreaktiossa molekyyliin, jossa on kaksois- tai kolmoissidos, liittyy jokin toinen molekyyli. Reaktio
d) Klooria valmistetaan hapettamalla vetykloridia kaliumpermanganaatilla. (Syntyy Mn 2+ -ioneja)
 Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
Helsingin yliopiston kemian valintakoe: Mallivastaukset. Maanantaina 29.5.2017 klo 14-17 1 Avogadron vakio NA = 6,022 10 23 mol -1 Yleinen kaasuvakio R = 8,314 J mol -1 K -1 = 0,08314 bar dm 3 mol -1 K
Reaktioyhtälö. Sähköisen oppimisen edelläkävijä www.e-oppi.fi. Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava
 Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
Reaktioyhtälö Sähköisen oppimisen edelläkävijä www.e-oppi.fi Empiirinen kaava, molekyylikaava, rakennekaava, viivakaava Empiirinen kaava (suhdekaava) ilmoittaa, missä suhteessa yhdiste sisältää eri alkuaineiden
REAKTIOT JA ENERGIA, KE3. Kaasut
 Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
Kaasut REAKTIOT JA ENERGIA, KE3 Kaasu on yksi aineen olomuodosta. Kaasujen käyttäytymistä kokeellisesti tutkimalla on päädytty yksinkertaiseen malliin, ns. ideaalikaasuun. Määritelmä: Ideaalikaasu on yksinkertainen
vetyteknologia Polttokennon tyhjäkäyntijännite 1 DEE-54020 Risto Mikkonen
 DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
DEE-5400 olttokennot ja vetyteknologia olttokennon tyhjäkäyntijännite 1 DEE-5400 Risto Mikkonen 1.1.014 g:n määrittäminen olttokennon toiminta perustuu Gibbsin vapaan energian muutokseen. ( G = TS) Ideaalitapauksessa
Tehtävä 1. Tasapainokonversion laskenta Χ r G-arvojen avulla Alkyloitaessa bentseeniä propeenilla syntyy kumeenia (isopropyylibentseeniä):
 CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
CHEM-A1110 Virtaukset ja reaktorit Laskuharjoitus 10/017 Lisätietoja s-postilla reetta.karinen@aalto.fi tai tiia.viinikainen@aalto.fi vastaanotto huoneessa E409 Kemiallinen tasapaino Tehtävä 1. Tasapainokonversion
1.1 Homogeeninen kemiallinen tasapaino
 1.1 Homogeeninen kemiallinen tasapaino 1. a) Mitä tarkoittaa käsite kemiallinen tasapaino? b) Miten kemiallinen tasapaino ilmaistaan reaktioyhtälössä? c) Mistä tekijöistä tasapainossa olevan reaktioseoksen
1.1 Homogeeninen kemiallinen tasapaino 1. a) Mitä tarkoittaa käsite kemiallinen tasapaino? b) Miten kemiallinen tasapaino ilmaistaan reaktioyhtälössä? c) Mistä tekijöistä tasapainossa olevan reaktioseoksen
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Reaktiosarjat
 Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
Reaktiosarjat Usein haluttua tuotetta ei saada syntymään yhden kemiallisen reaktion lopputuotteena, vaan monen peräkkäisten reaktioiden kautta Tällöin edellisen reaktion lopputuote on seuraavan lähtöaine
REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE
 REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE Essi Purhonen 1, Krista Iltanen 1 & Sini Hänninen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Oppilaan ohje 1.1 LÄMPÖTILAN
REAKTIONOPEUS IHMISKEHOSSA TUTKIMUKSELLINEN TYÖ YLÄKOULULAISILLE Essi Purhonen 1, Krista Iltanen 1 & Sini Hänninen 1 1 Kemian opettajankoulutusyksikkö, Helsingin yliopisto Oppilaan ohje 1.1 LÄMPÖTILAN
T F = T C ( 24,6) F = 12,28 F 12,3 F T K = (273,15 24,6) K = 248,55 K T F = 87,8 F T K = 4,15 K T F = 452,2 F. P = α T α = P T = P 3 T 3
 76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
76628A Termofysiikka Harjoitus no. 1, ratkaisut (syyslukukausi 2014) 1. Muunnokset Fahrenheit- (T F ), Celsius- (T C ) ja Kelvin-asteikkojen (T K ) välillä: T F = 2 + 9 5 T C T C = 5 9 (T F 2) T K = 27,15
kertausta Boltzmannin jakauma infoa Ideaalikaasu kertausta Maxwellin ja Boltzmannin vauhtijakauma
 infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
infoa kertausta Boltzmannin jakauma Huomenna itsenäisyyspäivänä laitos on kiinni, ei luentoa, ei laskareita. Torstaina laboratoriossa assistentit neuvovat myös laskareissa. Ensi viikolla tiistaina vielä
Nimi sosiaaliturvatunnus. Vastaa lyhyesti, selkeällä käsialalla. Vain vastausruudun sisällä olevat tekstit, kuvat jne huomioidaan
 1. Valitse listasta kunkin yhdisteen yleiskielessä käytettävä ei-systemaattinen nimi. (pisteet yht. 5p) a) C-vitamiini b) glukoosi c) etikkahappo d) salisyylihappo e) beta-karoteeni a. b. c. d. e. ksylitoli
1. Valitse listasta kunkin yhdisteen yleiskielessä käytettävä ei-systemaattinen nimi. (pisteet yht. 5p) a) C-vitamiini b) glukoosi c) etikkahappo d) salisyylihappo e) beta-karoteeni a. b. c. d. e. ksylitoli
Reaktiotekniikka. Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää
 Reaktiotekniikka Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää Luennon sisältö Johdanto ja termejä Reaktiotekniikka Kemiallinen prosessitekniikka Kemialliset reaktiot Reaktioiden jaottelu
Reaktiotekniikka Prosessi- ja ympäristötekniikan perusta Teema 4 Kaisa Lamminpää Luennon sisältö Johdanto ja termejä Reaktiotekniikka Kemiallinen prosessitekniikka Kemialliset reaktiot Reaktioiden jaottelu
Hiilen ja vedyn reaktioita (1)
 Hiilen ja vedyn reaktioita (1) Hiilivetyjen tuotanto alkaa joko säteilevällä yhdistymisellä tai protoninvaihtoreaktiolla C + + H 2 CH + 2 + hν C + H + 3 CH+ + H 2 Huom. Reaktio C + + H 2 CH + + H on endoterminen,
Hiilen ja vedyn reaktioita (1) Hiilivetyjen tuotanto alkaa joko säteilevällä yhdistymisellä tai protoninvaihtoreaktiolla C + + H 2 CH + 2 + hν C + H + 3 CH+ + H 2 Huom. Reaktio C + + H 2 CH + + H on endoterminen,
Teddy 7. harjoituksen malliratkaisu syksy 2011
 Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Teddy 7. harjoituksen malliratkaisu syksy 2011 1. Systeemin käyttäytymistä faasirajalla kuvaa Clapeyronin yhtälönä tunnettu keskeinen relaatio dt = S m. (1 V m Koska faasitasapainossa reaktion Gibbsin
Kondensaatio ja hydrolyysi
 Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
Kondensaatio ja hydrolyysi REAKTIOT JA ENERGIA, KE3 Määritelmä, kondensaatioreaktio: Kondensaatioreaktiossa molekyylit liittyvät yhteen muodostaen uuden funktionaalisen ryhmän ja samalla molekyylien väliltä
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta Insinöörivalinnan kemian koe MALLIRATKAISUT
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT 1 a) Vaihtoehto B on oikein. Elektronit sijoittuvat atomiorbitaaleille kasvavan
Luku 5: Diffuusio kiinteissä aineissa
 Luku 5: Diffuusio kiinteissä aineissa Käsiteltävät aiheet... Mitä on diffuusio? Miksi sillä on tärkeä merkitys erilaisissa käsittelyissä? Miten diffuusionopeutta voidaan ennustaa? Miten diffuusio riippuu
Luku 5: Diffuusio kiinteissä aineissa Käsiteltävät aiheet... Mitä on diffuusio? Miksi sillä on tärkeä merkitys erilaisissa käsittelyissä? Miten diffuusionopeutta voidaan ennustaa? Miten diffuusio riippuu
 KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
KULJETUSSUUREET Kuljetussuureilla tai -ominaisuuksilla tarkoitetaan kaasumaisen, nestemäisen tai kiinteän väliaineen kykyä siirtää ainetta, energiaa, tai jotain muuta fysikaalista ominaisuutta paikasta
Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen
 KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
KEMA221 2009 PUHTAAN AINEEN FAASIMUUTOKSET ATKINS LUKU 4 1 PUHTAAN AINEEN FAASIMUUTOKSET Esimerkkejä faasimuutoksista? Tässä luvussa keskitytään faasimuutosten termodynaamiseen kuvaukseen Faasi = aineen
Puhtaat aineet ja seokset
 Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
Puhtaat aineet ja seokset KEMIAA KAIKKIALLA, KE1 Määritelmä: Puhdas aine sisältää vain yhtä alkuainetta tai yhdistettä. Esimerkiksi rautatanko sisältää vain Fe-atomeita ja ruokasuola vain NaCl-ioniyhdistettä
Kvanttifysiikan perusteet 2017
 Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Kvanttifysiikan perusteet 207 Harjoitus 2: ratkaisut Tehtävä Osoita hyödyntäen Maxwellin yhtälöitä, että tyhjiössä magneettikenttä ja sähkökenttä toteuttavat aaltoyhtälön, missä aallon nopeus on v = c.
Reaktiot ja tasapaino
 Reaktiot ja tasapaino Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä): Reaktiot ja tasapaino Tunnit (45min ja 1,5h): ma 14:10 14:55, ke 08:00 09:50, to 11:20 12:05 ja 14:10 14:55 pe 14:10 14:55
Reaktiot ja tasapaino Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä): Reaktiot ja tasapaino Tunnit (45min ja 1,5h): ma 14:10 14:55, ke 08:00 09:50, to 11:20 12:05 ja 14:10 14:55 pe 14:10 14:55
Henkilötunnus: - KOULUTUSOHJELMA Sukunimi: 27.5.2014 Etunimet: Nimikirjoitus: KEMIA. Kemian kuulustelu klo 9.00
 TERVEYDE BITIETEIDE enkilötunnus: - KULUTUSJELMA Sukunimi: 27.5.2014 Etunimet: imikirjoitus: KEMIA Kemian kuulustelu klo 9.00 YLEISET JEET 1. Tarkista, että saamassasi tehtävänipussa on sivut 1-10. Paperinippua
TERVEYDE BITIETEIDE enkilötunnus: - KULUTUSJELMA Sukunimi: 27.5.2014 Etunimet: imikirjoitus: KEMIA Kemian kuulustelu klo 9.00 YLEISET JEET 1. Tarkista, että saamassasi tehtävänipussa on sivut 1-10. Paperinippua
Reaktiot ja tasapaino
 Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä/ohjattu tenttiminen*): Tunnit (ohjausajat ja labrat 1,5h): labrat: ke 12:15 14:00, ohjausajat: ti 14-15 ja pe 10-11 sopiiko? Kurssikirja: Reaktio
Kurssi 5, KE5 Kurssin yleiset tiedot Kurssi 5 (syventävä/ohjattu tenttiminen*): Tunnit (ohjausajat ja labrat 1,5h): labrat: ke 12:15 14:00, ohjausajat: ti 14-15 ja pe 10-11 sopiiko? Kurssikirja: Reaktio
Bensiiniä voidaan pitää hiilivetynä C8H18, jonka tiheys (NTP) on 0,703 g/ml ja palamislämpö H = kj/mol
 Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Kertaustehtäviä KE3-kurssista Tehtävä 1 Maakaasu on melkein puhdasta metaania. Kuinka suuri tilavuus metaania paloi, kun täydelliseen palamiseen kuluu 3 m 3 ilmaa, jonka lämpötila on 50 C ja paine on 11kPa?
Atomin elektronikonfiguraatiot (1)
 Atomin elektronikonfiguraatiot (1) Atomiin sidotun elektronin tilaa kuvataan neljällä kvanttiluvulla: n pääkvattiluku - aaltofunktion eli orbitaalin energia, keskimääräinen etäisyys ytimestä, saa arvot
Atomin elektronikonfiguraatiot (1) Atomiin sidotun elektronin tilaa kuvataan neljällä kvanttiluvulla: n pääkvattiluku - aaltofunktion eli orbitaalin energia, keskimääräinen etäisyys ytimestä, saa arvot
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA
 PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
PHYS-C0220 TERMODYNAMIIKKA JA STATISTINEN FYSIIKKA Kevät 2016 Emppu Salonen Lasse Laurson Arttu Lehtinen Toni Mäkelä Luento 8: Kemiallinen potentiaali, suurkanoninen ensemble Pe 18.3.2016 1 AIHEET 1. Kanoninen
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2½ p. = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 2015 Insinöörivalinnan kemian koe 27.5.2015 MALLIRATKAISUT JA PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei
TKK, TTY, LTY, OY, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 31.5.2006
 TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut
 Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
Astrokemia Kevät 2011 Harjoitus 1, Massavaikutuksen laki, Ratkaisut 1 a Kaasuseoksen komponentin i vapaa energia voidaan kirjoittaa F i (N,T,V = ln Z i (T,V missä on ko hiukkasten lukumäärä tilavuudessa
YLEINEN KEMIA. Alkuaineiden esiintyminen maailmassa. Alkuaineet. Alkuaineet koostuvat atomeista. Atomin rakenne. Copyright Isto Jokinen
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
1. van der Waalsin tilanyhtälö: 2 V m RT. + b2. ja C = b2. Kun T = 273 K niin B = cm 3 /mol ja C = 1200 cm 6 mol 2
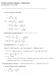 FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
FYSIKAALINEN KEMIA KEMA22) Laskuharjoitus 2, 28..2009. van der Waalsin tilanyhtälö: p = RT V m b a Vm V 2 m pv m = RT V m b = RT = RT a ) V m RT a b/v m V m RT ) [ b/v m ) a V m RT Soveltamalla sarjakehitelmää
Puhtaan kaasun fysikaalista tilaa määrittävät seuraavat 4 ominaisuutta, jotka tilanyhtälö sitoo toisiinsa: Paine p
 KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
KEMA221 2009 KERTAUSTA IDEAALIKAASU JA REAALIKAASU ATKINS LUKU 1 1 IDEAALIKAASU Ideaalikaasu Koostuu pistemäisistä hiukkasista Ei vuorovaikutuksia hiukkasten välillä Hiukkasten liike satunnaista Hiukkasten
= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]
![= P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ] = P 0 (V 2 V 1 ) + nrt 0. nrt 0 ln V ]](/thumbs/62/46694692.jpg) 766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
766328A Termofysiikka Harjoitus no. 7, ratkaisut (syyslukukausi 2014) 1. Sylinteri on ympäristössä, jonka paine on P 0 ja lämpötila T 0. Sylinterin sisällä on n moolia ideaalikaasua ja sen tilavuutta kasvatetaan
Yhdisteiden nimeäminen
 Yhdisteiden nimeäminen Binääriyhdisteiden nimeäminen 1. Ioniyhdisteet 2. Epämetallien väliset yhdisteet Kompleksiyhdisteiden nimeäminen Kemiallinen reaktio 1. Reaktioyhtälö 2. Määrälliset laskut 3. Reaktionopeuteen
Yhdisteiden nimeäminen Binääriyhdisteiden nimeäminen 1. Ioniyhdisteet 2. Epämetallien väliset yhdisteet Kompleksiyhdisteiden nimeäminen Kemiallinen reaktio 1. Reaktioyhtälö 2. Määrälliset laskut 3. Reaktionopeuteen
CHEM-C2230 Pintakemia Barnes & Gentle: luku 8 L7 Kaasun adsorptio kiinteän aineen pinnalle
 CHEM-C2230 Pintakemia Barnes & Gentle: luku 8 L7 Kaasun adsorptio kiinteän aineen pinnalle Prof. Monika Österberg Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle
CHEM-C2230 Pintakemia Barnes & Gentle: luku 8 L7 Kaasun adsorptio kiinteän aineen pinnalle Prof. Monika Österberg Aikaisemmin käsitellyt Adsorptio kiinteälle pinnalle nesteessä Adsorptio nestepinnalle
KEMA221 2009 KEMIALLINEN TASAPAINO ATKINS LUKU 7
 KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
KEMIALLINEN TASAPAINO Määritelmiä Kemiallinen reaktio A B pyrkii kohti tasapainoa. Yleisessä tapauksessa saavutetaan tasapainoa vastaava reaktioseos, jossa on läsnä sekä lähtöaineita että tuotteita: A
P = kv. (a) Kaasun lämpötila saadaan ideaalikaasun tilanyhtälön avulla, PV = nrt
 766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
766328A Termofysiikka Harjoitus no. 2, ratkaisut (syyslukukausi 204). Kun sylinterissä oleva n moolia ideaalikaasua laajenee reversiibelissä prosessissa kolminkertaiseen tilavuuteen 3,lämpötilamuuttuuprosessinaikanasiten,ettäyhtälö
PHYS-A0120 Termodynamiikka syksy 2016
 PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
PHYS-A0120 Termodynamiikka syksy 2016 Emppu Salonen Prof. Peter Liljeroth Viikko 6: Faasimuutokset Maanantai 5.12. Kurssin aiheet 1. Lämpötila ja lämpö 2. Työ ja termodynamiikan 1. pääsääntö 3. Lämpövoimakoneet
Ainemäärien suhteista laskujen kautta aineiden määriin
 REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
REAKTIOT JA ENERGIA, KE3 Ainemäärien suhteista laskujen kautta aineiden määriin Mitä on kemia? Kemia on reaktioyhtälöitä, ja niiden tulkitsemista. Ollaan havaittu, että reaktioyhtälöt kertovat kemiallisen
Lämpöoppi. Termodynaaminen systeemi. Tilanmuuttujat (suureet) Eristetty systeemi. Suljettu systeemi. Avoin systeemi.
 Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Lämpöoppi Termodynaaminen systeemi Tilanmuuttujat (suureet) Lämpötila T (K) Absoluuttinen asteikko eli Kelvinasteikko! Paine p (Pa, bar) Tilavuus V (l, m 3, ) Ainemäärä n (mol) Eristetty systeemi Ei ole
Reaktiolämpö KINEETTINEN ENERGIA POTENTIAALI- ENERGIA
 POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
POTENTIAALI- ENERGIA KINEETTINEN ENERGIA Reaktiolämpö REAKTIOT JA ENERGIA, KE3 Johdantoa: Syömme elääksemme, emme elä syödäksemme! sanonta on totta. Kun elimistömme hyödyntää ravintoaineita metaboliassa
Reaktiot ja energia. Kurssin yleiset tiedot. (työt to-pe!!! Ehkä ma-ti) Kurssi 3 (syventävä): Reaktiot ja energia, Ke3 Tunnit (45min):
 Reaktiot ja energia Kurssi 3, Ke3 Kurssin yleiset tiedot Kurssi 3 (syventävä): Tunnit (45min): ma 8:00-8:45 ja 14:10 14:55, ti, ke ja pe 8:00 8:45 ja to 14:10 14:55 (työt to-pe!!! Ehkä ma-ti) Kurssikirja:
Reaktiot ja energia Kurssi 3, Ke3 Kurssin yleiset tiedot Kurssi 3 (syventävä): Tunnit (45min): ma 8:00-8:45 ja 14:10 14:55, ti, ke ja pe 8:00 8:45 ja to 14:10 14:55 (työt to-pe!!! Ehkä ma-ti) Kurssikirja:
KE03. Kurssikalvot. Tuomas Hentunen. Kevät Tuomas Hentunen KE03 Kevät / 26
 KE03 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE03 Kevät 2016 1 / 26 Reaktioyhtälöt ja niiden tasapainottaminen Kemiallista reaktiota kuvataan reaktioyhtälöllä reaktioyhtälöstä selviää:
KE03 Kurssikalvot Tuomas Hentunen Kevät 2016 Tuomas Hentunen KE03 Kevät 2016 1 / 26 Reaktioyhtälöt ja niiden tasapainottaminen Kemiallista reaktiota kuvataan reaktioyhtälöllä reaktioyhtälöstä selviää:
Näiden aihekokonaisuuksien opetussuunnitelmat ovat luvussa 8.
 9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
9. 11. b Oppiaineen opetussuunnitelmaan on merkitty oppiaineen opiskelun yhteydessä toteutuva aihekokonaisuuksien ( = AK) käsittely seuraavin lyhentein: AK 1 = Ihmisenä kasvaminen AK 2 = Kulttuuri-identiteetti
POHDITTAVAKSI ENNEN TYÖTÄ
 MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
MUSTIKKATRIO KOHDERYHMÄ: Työ voidaan suorittaa kaikenikäisten kanssa, jolloin teoria sovelletaan osaamistasoon. KESTO: n. 1h MOTIVAATIO: Arkipäivän ruokakemian ilmiöiden tarkastelu uudessa kontekstissa.
REAKTIOT JA TASAPAINO, KE5 KERTAUSTA
 KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KERTAUSTA REAKTIOT JA TASAPAINO, KE5 Aineiden ominaisuudet voidaan selittää niiden rakenteen avulla. Aineen rakenteen ja ominaisuuksien väliset riippuvuudet selittyvät kemiallisten sidosten avulla. Vahvat
KEMIA. Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista.
 KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
KEMIA Kemia on tiede joka tutkii aineen koostumuksia, ominaisuuksia ja muuttumista. Kemian työturvallisuudesta -Kemian tunneilla tutustutaan aineiden ominaisuuksiin Jotkin aineet syttyvät palamaan reagoidessaan
782630S Pintakemia I, 3 op
 782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
782630S Pintakemia I, 3 op Ulla Lassi Puh. 0400-294090 Sposti: ulla.lassi@oulu.fi Tavattavissa: KE335 (ma ja ke ennen luentoja; Kokkolassa huone 444 ti, to ja pe) Prof. Ulla Lassi Opintojakson toteutus
Kaikki ympärillämme oleva aine koostuu alkuaineista.
 YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
YLEINEN KEMIA Yleinen kemia käsittelee kemian perusasioita kuten aineen rakennetta, alkuaineiden jaksollista järjestelmää, kemian peruskäsitteitä ja kemiallisia reaktioita. Alkuaineet Kaikki ympärillämme
KEMIAN MIKROMAAILMA, KE2 VESI
 VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
VESI KEMIAN MIKROMAAILMA, KE2 Johdantoa: Vesi on elämälle välttämätöntä. Se on hyvä liuotin, energian ja aineiden siirtäjä, lämmönsäätelijä ja se muodostaa vetysidoksia, jotka tekevät siitä poikkeuksellisen
ENERGIAA! ASTE/KURSSI AIKA 1/5
 1/5 ASTE/KURSSI Yläasteelle ja lukioon elintarvikkeiden kemian yhteydessä. Sopii myös alaasteryhmille opettajan avustaessa poltossa, sekä laskuissa. AIKA n. ½ tuntia ENERGIAA! Vertaa vaahtokarkin ja cashewpähkinän
1/5 ASTE/KURSSI Yläasteelle ja lukioon elintarvikkeiden kemian yhteydessä. Sopii myös alaasteryhmille opettajan avustaessa poltossa, sekä laskuissa. AIKA n. ½ tuntia ENERGIAA! Vertaa vaahtokarkin ja cashewpähkinän
= 84. Todennäköisin partitio on partitio k = 6,
 S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
S-435, Fysiikka III (ES) entti 43 entti / välikoeuusinta I Välikokeen alue Neljän tunnistettavissa olevan hiukkasen mikrokanonisen joukon mahdolliset energiatasot ovat, ε, ε, 3ε, 4ε,, jotka kaikki ovat
Kertaustehtävien ratkaisut LUKU 2
 Kertaustehtävien ratkaisut LUKU 1. Neutraoitumisen reaktioyhtäö: H (aq) NaOH(aq) Na (aq) H O(). Lasketaan NaOH-iuoksen konsentraatio, kun V(NaOH) 150 m 0,150, m(naoh),40 ja M(NaOH) 39,998. n m Kaavoista
Kertaustehtävien ratkaisut LUKU 1. Neutraoitumisen reaktioyhtäö: H (aq) NaOH(aq) Na (aq) H O(). Lasketaan NaOH-iuoksen konsentraatio, kun V(NaOH) 150 m 0,150, m(naoh),40 ja M(NaOH) 39,998. n m Kaavoista
Sähkökemian perusteita, osa 1
 Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
1 WKB-approksimaatio. Yleisiä ohjeita. S Harjoitus
 S-114.1427 Harjoitus 3 29 Yleisiä ohjeita Ratkaise tehtävät MATLABia käyttäen. Kirjoita ratkaisut.m-tiedostoihin. Tee tuloksistasi lyhyt seloste, jossa esität laskemasi arvot sekä piirtämäsi kuvat (sekä
S-114.1427 Harjoitus 3 29 Yleisiä ohjeita Ratkaise tehtävät MATLABia käyttäen. Kirjoita ratkaisut.m-tiedostoihin. Tee tuloksistasi lyhyt seloste, jossa esität laskemasi arvot sekä piirtämäsi kuvat (sekä
Lukion kemian OPS 2016
 Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
Lukion kemian OPS 2016 Tieteellisen maailmankuvan rakentuminen on lähtökohtana. muodostavat johdonmukaisen kokonaisuuden (ao. muutoksien jälkeen). Orgaaninen kemia pois KE1-kurssilta - yhdisteryhmät KE2-kurssiin
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA!
 ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
ENY-C2001 Termodynamiikka ja lämmönsiirto TERVETULOA! Luento 14.9.2015 / T. Paloposki / v. 03 Tämän päivän ohjelma: Aineen tilan kuvaaminen pt-piirroksella ja muilla piirroksilla, faasimuutokset Käsitteitä
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017
 PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
PHYS-C0220 Termodynamiikka ja statistinen fysiikka Kevät 2017 Emppu Salonen Lasse Laurson Toni Mäkelä Touko Herranen Luento 2: kineettistä kaasuteoriaa Pe 24.2.2017 1 Aiheet tänään 1. Maxwellin ja Boltzmannin
Kuva 1: Yksinkertainen siniaalto. Amplitudi kertoo heilahduksen laajuuden ja aallonpituus
 Kuva 1: Yksinkertainen siniaalto. Amplitudi kertoo heilahduksen laajuuden ja aallonpituus värähtelytiheyden. 1 Funktiot ja aallot Aiemmin käsiteltiin funktioita ja miten niiden avulla voidaan kuvata fysiikan
Kuva 1: Yksinkertainen siniaalto. Amplitudi kertoo heilahduksen laajuuden ja aallonpituus värähtelytiheyden. 1 Funktiot ja aallot Aiemmin käsiteltiin funktioita ja miten niiden avulla voidaan kuvata fysiikan
AUTON LIIKETEHTÄVIÄ: KESKIKIIHTYVYYS ak JA HETKELLINEN KIIHTYVYYS a(t) (tangenttitulkinta) sekä matka fysikaalisena pinta-alana (t,
 AUTON LIIKETEHTÄVIÄ: KESKIKIIHTYVYYS ak JA HETKELLINEN KIIHTYVYYS a(t) (tangenttitulkinta) sekä matka fysikaalisena pinta-alana (t, v)-koordinaatistossa ruutumenetelmällä. Tehtävä 4 (~YO-K97-1). Tekniikan
AUTON LIIKETEHTÄVIÄ: KESKIKIIHTYVYYS ak JA HETKELLINEN KIIHTYVYYS a(t) (tangenttitulkinta) sekä matka fysikaalisena pinta-alana (t, v)-koordinaatistossa ruutumenetelmällä. Tehtävä 4 (~YO-K97-1). Tekniikan
- Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka: kappaleiden liike)
 KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
KEMA221 2009 TERMODYNAMIIKAN 1. PÄÄSÄÄNTÖ ATKINS LUKU 2 1 1. PERUSKÄSITTEITÄ - Termodynamiikka kuvaa energian siirtoa ( dynamiikkaa ) systeemin sisällä tai systeemien kesken (vrt. klassinen dynamiikka:
arvioinnin kohde
 KEMIA 8-lk Merkitys, arvot ja asenteet T2 Oppilas asettaa itselleen tavoitteita sekä työskentelee pitkäjänteisesti. Oppilas kuvaamaan omaa osaamistaan. T3 Oppilas ymmärtää alkuaineiden ja niistä muodostuvien
KEMIA 8-lk Merkitys, arvot ja asenteet T2 Oppilas asettaa itselleen tavoitteita sekä työskentelee pitkäjänteisesti. Oppilas kuvaamaan omaa osaamistaan. T3 Oppilas ymmärtää alkuaineiden ja niistä muodostuvien
l 1 2l + 1, c) 100 l=0
 MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
MATEMATIIKAN PERUSKURSSI I Harjoitustehtäviä syksy 5. Millä reaaliluvun arvoilla a) 9 =, b) 5 + 5 +, e) 5?. Kirjoita Σ-merkkiä käyttäen summat 4, a) + + 5 + + 99, b) 5 + 4 65 + + n 5 n, c)
Luento 2: Lämpökemiaa, osa 1 Keskiviikko klo Termodynamiikan käsitteitä
 Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Luento 2: Lämpökemiaa, osa 1 Keskiviikko 12.9. klo 8-10 477401A - ermodynaamiset tasapainot (Syksy 2018) ermodynamiikan käsitteitä - Systeemi Eristetty - suljettu - avoin Homogeeninen - heterogeeninen
Solun toiminta. II Solun toiminta. BI2 II Solun toiminta 7. Fotosynteesi tuottaa ravintoa eliökunnalle
 Solun toiminta II Solun toiminta 7. Fotosynteesi tuottaa ravintoa eliökunnalle 1. Avainsanat 2. Fotosynteesi eli yhteyttäminen 3. Viherhiukkanen eli kloroplasti 4. Fotosynteesin reaktiot 5. Mitä kasvit
Solun toiminta II Solun toiminta 7. Fotosynteesi tuottaa ravintoa eliökunnalle 1. Avainsanat 2. Fotosynteesi eli yhteyttäminen 3. Viherhiukkanen eli kloroplasti 4. Fotosynteesin reaktiot 5. Mitä kasvit
