MT Korroosionestotekniikan perusteet. KORROOSIOYMPÄRISTÖT, Korroosio vedessä. Trends in metal use KORROOSIOYMPÄRISTÖT
|
|
|
- Kaarina Majanlahti
- 7 vuotta sitten
- Katselukertoja:
Transkriptio
1 KORROOSIOYMPÄRISTÖT MT Korroosionestotekniikan perusteet KORROOSIOYMPÄRISTÖT, Korroosio vedessä Ennen 1800-lukua käytettyjen metallien luku oli pieni ja korroosioympäristöt, eli ilma, maaperä ja vesi olivat suhteellisen puhtaita. Suhteellisesti noin 80% teräsrakenteista on alttiina ilmastorasitukselle, 10% syöpyy vedessä ja 10% maaperässä. 2 Trends in metal use KORROOSIOYMPÄRISTÖT Metal/element use intensity in products Metal Recycling, UNEP, 2013 Korroosion perusreaktiot ilmassa, vedessä ja maassa ovat samat. Ympäristöstä riippuen perusreaktioiden, eli katodisen reaktion ja anodisen liukenemisreaktion luonne ja nopeus muuttuvat. Esimerkiksi ympäristön happipitoisuus erot ilmastorasituksessa ovat merkityksettömiä korroosion aiheuttajia kun taas maaperässä happipitoisuuserojen merkitys on materiaalin korroosion kanalta ratkaisevin tekijä
2 KORROOSIOKENNO KORROOSIOKENNO Vesiliuos elektrolyyttinä O 2 O 2 O 2 O 2 Anodi Katodi Hapetin adsorboituu liuoksesta O 2 Fe Fe 4 e - Anodi Katodi Fe = Fe e- O 2 + H 2 O + 4e - = 4 OH - Varauksensiirtoreaktio, elektronit siirtyvät anodialueelta katodille. Fe 2+ Fe 2+ OH- OH- OH - OH - Fe Fe Anodi Katodi Reaktiotuotteet poistuvat liuokseen 5 6 KORROOSIOYMPÄRISTÖT Liuosolosuhteet PUHTAAN VEDEN OLOTILAT 2.0 Hapan ja hapettava Emäksinen ja hapettava Liuosolosuhteet vaikuttavat sähkökemiallisten reaktioiden todennäköisyyteen ja nopeuteen. Tärkeimmät liuosmuuttujat ovat happamuus, redox-potentiaali, lämpötila sekä ionien konsentraatiot. 2 H 2 O = O H e - E = 0,81-0,059pH V 2 H e - = H 2 E / V vs. SHE Hapen kehitys Veden stabiilisuusalueen yläraja Veden stabiilisuusalueen alaraja Vedyn kehitys -1.0 Hapan ja pelkistävä Emäksinen ja pelkistävä ph 7 8 2
3 HAPETTIMET JA PELKISTIMET HAPETTIMET JA PELKISTIMET Hapettimet hapettavat muita aineita, ottavat vastaan elektroneja ja pelkistyvät samalla itse. Pelkistimet pelkistävät muita aineita, luovuttavat elektroneja ja hapettuvat itse. Aineen kykyä toimia hapettimena tai pelkistimenä voidaan arvioida sen standardielektrodipotentiaalin avulla. Periaatteessa, mitä korkeampi E o niin sitä voimakkaampi hapetin ja mitä alhaisempi E o niin sitä voimakkaampi pelkistin. Liuoksen kykyä hapettaa tai pelkistää kuvataan redoxpotentiaalin avulla. Redox-potentiaali on liuokseen upotetun reagoimattoman elektrodin (Pt, Au tms.) potentiaali jonkin referenssielektrodin suhteen. Liuoksen redox-potentiaali riippuu siihen liuenneiden hapettimien ja pelkistimien pitoisuuksista. Jos liuoksessa on useita hapettimia tai pelkistimiä, redox-potentiaalin mittaus ei kykene erottamaan niiden vaikutuksia. MT , luento MT , luento HAPETTIMET JA PELKISTIMET HAPETTIMET JA PELKISTIMET REDOX-POTENTIAALI, mv vs. SCE Hapetin on katodisen reaktion lähtöaine, tavallisesti vety-ioni, jokin liuennut kaasu (O 2, Cl 2 ), hapettava yhdiste (ClO 2 ) tai metalli-ioni. Perinteisesti puhutaan korroosiosta hapettavissa ja pelkistävissä olosuhteissa. Pelkistävissä olosuhteissa redox-potentiaali on matala ja korroosio on vedynkehitysreaktion aiheuttamaa. Hapettavissa olosuhteissa redox-potentiaali on korkea ja katodireaktio on joku muu kuin vedynkehitys, kuten esimerkiksi luonnonvesissä liuenneen hapen pelkistyminen. O 3 -PITOISUUS, ppm MT , luento MT , luento
4 Sähkönjohtavuus LIUOSTEN RAKENNE JA OMINAISUUDET Veden sähkönjohtavuus tai ominaisvastus kuvaavat veteen liuenneiden suolojen määrää. Johtavuudesta ei voi päätellä mitä suoloja vedessä on. Osa suoloista on korroosioneston kannalta edullisia ja osa haitallisia, joten johtavuus ei kerro syövyttävyydestä. Liuos Johtokyky, µs/cm 3.5% NaCl-liuos Valtameren vesi M NaCl M NaCl ,1 M NaCl Käsittelemätön luonnonvesi >200 Pehmeä vesijohtovesi Ionivaihdettu vesi Täyssuolanpoistettu vesi noin 2 Ionivaihdettu ja ultrasuodatettu noin MT , luento LIUOSTEN RAKENNE JA OMINAISUUDET Meriveden johtokyky paranee kun lämpötila ja suolapitoisuus kasvavat. Johtokyky k [ms/cm] Saliniteetti [, g/dm 3 NaCl] 30 C 25 C 20 C 15 C 10 C 5 C 0 C Liuosmuuttujien vaikutus korroosioon Tärkeimmät ympäristön syövyttävyyteen vaikuttavat liuosmuuttujat ovat : Liuotin eli liuoksen pääkomponentti, johon muut aineet ovat liuenneet. Liuotin voi olla vesi, orgaaninen yhdiste tai niiden seos. ph eli liuoksen happamuus vaikuttaa sekä reaktionopeuksiin että passivoitumiseen. Redox-potentiaali, eli liuoksen kyky hapettaa vaikuttaa myös reaktionopeuksiin ja passivoitumiseen. Lämpötila vaikuttaa reaktionopeuksiin. Liuenneet suolat vaikuttavat reaktiotuotekerrosten muodostumiseen ja tuhoutumiseen. Liuoksen virtaus vaikuttaa reaktionopeuksiin ja reaktiotuotekerrosten pysyvyyteen. Virtaus tai sen puuttuminen muuttaa myös liuoksen koostumusta paikallisesti. MT , luento
5 VEDEN SYÖVYTTÄVYYS Synteettinen pohjavesi Pyhäsalmen kaivoksen pohjavesi KORROOSIO VEDESSÄ KORROOSIO VEDESSÄ Vedessä liuennutta happea on vain rajoitetusti. Korroosio vedessä riippuu siitä nopeudesta, jolla happea kulkeutuu metallin pinnalle. Korroosiotuotteet ovat usein huokoisia ja irrallisia, eivätkä ne muodosta tiivistä suojaavaa kalvoa. Korroosio vedessä tapahtuu yleensä paikallisena, jolloin esimerkiksi vesijohtoputket saattavat syöpyä puhki ennen kuin korroosio on aiheuttanut edes 5% painonmuutosta
6 KORROOSIO VEDESSÄ HAPETTIMET JA PELKISTIMET Korroosio luonnonvedessä eroaa oleellisesti korroosiosta ilmassa, sillä vedessä liuennutta happea on vain rajoitetusti. Yhdessä kuutiometrissä (1 tonnissa) vettä on noin 8 grammaa happea, joka kykenee syövyttämään noin 60 g rautaa. Korroosio vedessä riippuu siitä nopeudesta, jolla happea kulkeutuu metallin pinnalle, eli korroosionopeus on hapen aineensiirron rajoittama. Hapen liukoisuus meriveteen: liuenneen kaasun pitoisuus laskee kun lämpötila tai suolapitoisuus kasvavat. O 2 [ml/l] C 5 C 10 C 15 C 20 C 25 C 30 C Saliniteetti [, g/dm 3 NaCl] 21 MT , luento Liuoksen happamuus vaikuttaa korroosionopeuteen katodisen reaktion nopeuden ja suojaavien reaktiotuotekerrosten kautta. Jalometallien korroosioon ph ei vaikuta. Amfoteeriset metallit, kuten alumiinin ja sinkki, syöpyvät ioneina kun ph on liian matala ja komplekseina kun ph on liian korkea. Useimmat metallit syöpyvät happamissa liuoksissa vedynkehityksen takia. Tällöin ei myöskään suojaavia kerroksia muodostu. Hyvin emäksiset liuokset voivat myös estää suojaavien kerrosten muodostumisen. Useimmat metallit kestävät neutraaleissa tai lievästi emäksisissä liuoksissa
7 CORROSION RATE, mm/year Acid Hydrogen evolution begins Alkaline T = 40 o C T = 20 o C ph Redox-potentiaali on mitta liuoksen kyvystä hapettaa. Hapetin käynnistää katodisen reaktion, johon tarvittavat elektronit saadaan anodisesta reaktiosta. Hapetin on tavallisesti vety-ioni, jokin liuennut kaasu (O 2, Cl 2 ), hapettava yhdiste (ClO 2 ) tai metalli-ioni. Perinteisesti puhutaan korroosiosta hapettavissa ja pelkistävissä olosuhteissa. Pelkistävissä olosuhteissa redox-potentiaali on matala ja korroosio on vedynkehitysreaktion aiheuttamaa. Hapettavissa olosuhteissa redox-potentiaali on korkea ja katodireaktio on joku muu kuin vedynkehitys, kuten esimerkiksi luonnonvesissä liuenneen hapen pelkistyminen Redox-potentiaalien arvoja HAPETTIMET JA PELKISTIMET O H e - = 2 H 2 O E 0 = pH log(pO 2 ) O H e - = 4 OH - E 0 = pOH log(pO 2 ) = pH log(pO 2 ) O H e - = 3 H 2 O E 0 = pH + 9.8log(pO 3 ) H 2 O H e - = 2 H 2 O E 0 = pH log(H 2 O 2 ) ClO H e - = Cl H 2 O E 0 = pH log(pClO 2 )/(Cl - ) Cl e - = 2 Cl - E 0 = log(Cl 2 )/(Cl - ) 2 ClO - + H 2 O + 2 e - = Cl OH - E 0 = pH log(ClO - )/(Cl - ) Fe 3+ + e - = Fe 2+ E 0 = log(Fe 2+ )/(Fe 3+ ) S 2 O H e - = 2 S + 3 H 2 O E 0 = pH log(S 2 O 2-3 ) Cu 2+ + e - = Cu + E 0 = log(Cu + )/(Cu 2+ ) 2 H e - = H 2 E 0 = 0-59pH log(pH 2 ) 27 Liuoksen lämpötila vaikuttaa suoraan reaktionopeuteen. Reaktiomekanismista riippuen korroosionopeus kasvaa kaksinkertaiseksi, kun lämpötila nousee o C. Lämpötila vaikuttaa reaktionopeuksien lisäksi reaktioiden käynnistymiseen. Kun reaktio on kerran käynnistynyt, niin se ei välttämättä pysähdy vaikka lämpötila laskisikin, esimerkiksi rakokorroosio. Toistuva lämpötilan muutos aiheuttaa tavallisesti liuoksen väkevöitymistä. Lämpötilan muutos saattaa aiheuttaa muutoksia rakenteen jännitystilassa ja käynnistää jännityskorroosion. 28 7
8 Jos johtokyky on huono, yleinen korroosio tapahtuu pieninä toistensa lähellä olevina syöpyminä ja korroosio näyttää tasaiselta. Johtokyvyn kasvaessa korroosiovauriot muuttuvat suuremmiksi ja ne ovat kauempana toisistaan. Jos liuoksen johtokyky on hyvä, galvaaninen korroosio tapahtuu laajalla alueella matalana syöpymänä materiaalien liitoskohdan ympärillä. Jos johtokyky on huono, galvaaninen korroosio keskittyy liitoskohdan lähelle aiheuttaen syviä syöpymiä Liuenneilla suoloilla on voimakas vaikutus passivoituvien metallien korroosionkestävyyteen. Esimerkiksi ruostumattomien terästen pistekorroosio alkaa, kun kloridipitoisuus on liian korkea. Kloridien vaikutusta voidaan inhiboida toisilla suoloilla. Emäksisissä liuoksissa voi olla enemmän klorideja kuin happamissa, koska OH - -ionit kumoavat kloridien vaikutusta. Muita ioneja, jotka voivat kumota kloridien aiheuttamaa pistesyöpymää ruostumattomille teräksille ovat SO 4 2-, ClO 3-, CO 3 2-, ja CrO Virtaus parantaa aina aineensiirtoa. Hapen kulkeutuminen metallin pinnalle on virtaavassa vedessä voimakkaampaa kuin seisovassa vedessä. Liian hidas virtaus saattaa johtaa sakan keräytymiseen pinnalle, joka taas aiheuttaa paikallista korroosiota mm. happipitoisuuserojen kautta. Liian hidas virtaus saattaa myös aiheuttaa sen, että katodinen reaktio ei ole riittävän voimakas passivoitumisen käynnistämiseksi. Virtaus aiheuttaa myös mekaanista rasitusta metallin pintaan. Virtausnopeuden kasvaessa metallit voivat syöpyä, koska suojaava kerros tuhoutuu
9 KORROOSIONOPEUS Aineensiirto kontrolloi Kriittinen leikkausvoima ylitetään Suojakerros hajoaa Ei suojaavaa kerrosta Stern-Bishop-diagrammi, hapettava-pelkistävä + klorideja-ei klorideja Hastelloy C Hastelloy G 304 ruostumaton Alumiini 316 haponkestävä Incoloy Nikkeli Zirkoni Monel Alloy 20 CB-3 Inconel Monel Titaani Hastelloy G Superausteniittinen teräs Hastelloy C Pd-seostettu titaani Hastelloy B Zirkoni Grafiitti Fluorimuovit Tantaali Lasivuorattu teräs Ei klorideja Klorideja VIRTAUSNOPEUS Hapettavat olosuhteet Pelkistävät olosuhteet KÄYTTÖVESI KÄYTTÖVESI Euroopan Unionin neuvoston direktiivissä 98/83/EY ihmisten käyttöön tarkoitetun veden laadusta on määritetty eräitä arvoja, joilla on merkitystä materiaalien korroosiolle: Alumiini 200 µg/l Ammonium 0,50 mg/l Kloridi 250 mg/l Johtavuus 2500 µs/cm, T = 25 C. Vetyionipitoisuus, ph = 6,5-9,5 Sulfaatti 250 mg/l ph:n, johtavuuden sekä kloridi- ja sulfaatti-pitoisuuden kohdalla todetaan erikseen, että vesi ei saa olla syövyttävää. Soveltamisopas talousvesiasetukseen (2000) antaa ohjeelliset vedenlaadun ohjearvot korroosion estämiseksi: ph > 7,5 Alkaliteetti yli 0,6 mval/l (HCO 3 pitoisuus) Kalsium yli 10 mg/l (0,25 mmol/l) Happi yli 2 mg/l HCO 3 /(SO 4 +Cl) 1,5 (ekvivalenttisuhde)
10 ph-arvon vaikutus sinkin syöpymiseen VEDEN ALKALITEETTI Alkaliteetti kuva veden puskurikapasiteettia. Mitä pienempi on alkaliteetti, sitä helpommin ph laskee, kun veteen lisätään happoa. Jos alkaliteetti on alle 0,5 mmol/l, vesi happamoituu helposti. Yli 1,0 mmol/l alkaliteettia sisältävä vesi pysyy yleensä korroosioneston kannalta riittävän emäksisenä. Alkaliteetti vähentää liuenneiden suolojen syövyttävää vaikutusta KÄYTTÖVESI KÄYTTÖVESI Kokonaiskovuus on kalsiumin ja magnesiumin määrän summa. Veden kovuus, ph ja liuennut hiilidioksidi liittyvät toisiinsa ja niiden muodostamaa kalkkitasapainoa on pidetty veden syövyttävyyttä kuvaavana tekijänä. Jos vedessä on enemmän hiilidioksidia kuin mitä hiilidioksidin ja bikarbonaatin välinen tasapaino edellyttää, niin liukenemattomat karbonaatit voivat muuttua liukoisiksi bikarbonaateiksi. SUHTEELLINEN OSUUS, % Hiilihappo H 2 CO 3 HCO 3 - CO 3 2- Bikarbonaatti Karbonaatti ph 10
11 Karbonaattikerroksen muodostuminen KALKKISAOSTUMAN MUODOSTUMINEN O 2 O 2 O 2 Fe 2+ Fe 2+ Suojakalvon voi muodostua kun vesi on riittävän kovaa, lähellä kalkkitasapainoa, happea on riittävästi eikä vedessä ole suojakalvon syntymistä estäviä aineita. Korroosion tapahtuessa kalkkitasapaino häiriintyy paikallisesti kun metallin pinnalla ph kasvaa katodisilla alueilla. Karbonaattikerros ei ilmesty yhdessä hetkessä koko pinnalle. Se saostuu pinnan katodialueille, joista se saattaa edelleen levitä peittämään koko pinnan. Hapettomassa tai niukkahappisessa vedessä suojakalvoa ei muodostu. Anodi Katodi 1 Happi adsorboituu vedestä katodialueelle. Fe Fe Anodi 4 e - Fe = Fe e - O 2 + H 2 O + 4e - = 4 OH - 2 Varauksensiirtoreaktiot: happi pelkistyy, rauta hapettuu. OH O OH- - 2 OH - OH- Fe Fe Katodi O 2 Anodi Katodi 3 Liuenneet rautaionit poistuvat liuokseen, katodialueella ph kasvaa paikallisesti. Anodi CaCO 3 Katodi 4 Katodialueella kalkkihiilidioksiditasapaino häiriintyy, ja metallin pinnalle saostuu karbonaattia VEDEN OMINAISUUDET KALKKISAOSTUMIA TERÄKSELLÄ Jos veden vapaan hiilihapon määrä on suurempi kuin tasapainotilassa, niin vesi liuottaa kalkkia eikä suojaavia kerroksia muodostu. Jos vapaan hiilihapon määrä on tasapainoa pienempi, niin kalkkikerroksia saostuu. Suojakalvon muodostumisen edellytykset ovat, että vesi on riittävän kovaa, yli 20 mg/l CaO, vesi on lähellä kalkkitasapainoa, vedessä on riittävästi happea eikä vedessä ole suojakalvon syntymistä estäviä aineita. Teräsnäytteet, upotusaika 1 viikko, peitattu rikkihapossa
12 KÄYTTÖVESI Miten kuvata veden syövyttävyyttä, eli koska korroosio on niin nopeaa, että se vaurioittaa järjestelmää tai pilaa veden laadun. Yleistä arviointiperustaa ei ole! Ei voida sanoa onko esimerkiksi teräksen ohenema 30 mm vuodessa liikaa veden laadun kannalta. Käytettyjä kyllä/ei -syövyttävyysindeksejä ovat olleet: Kalkkitasapainoon liittyvät Alkaliteetti ja suolat Joukko muuttujien sallittuja rajoja Näiden lisäksi vielä monimutkaisia analyysiin perustuvia, jotka antavat jonkin korroosionopeuden VEDEN OMINAISUUDET Merivesi Kloridien taipumus estää suojakalvojen muodostuminen ja suhteellisen korkean happipitoisuus tekevät merivesistä erään syövyttävimmistä luonnon korroosioympäristöistä. Galvaaniset parit ovat merkittäviä. Suojakalvoja ei yleensä muodostu, ja korroosionopeus pysyy merivesissä tasaisena. Tavallisimpien käyttömetallien korroosionopeudet vaihtelevat välillä 0,01-0,2 mm/a. VEDEN OMINAISUUDET Merivesi Murtovesissä teräksen korroosionopeus on noin kaksi kertaa suurempi kuin valtameren vesissä suuremman hapen liukoisuuden takia. Lämpötilan nousu ja virtausnopeuden kasvu kasvattavat myös korroosionopeutta. Voimakkaasti virtaavassa vedessä korroosionopeus voi olla yli 1,2 mm vuodessa ja partikkelieroosio voi kasvattaa korroosionopeuden 10 mm:iin vuodessa
13 VEDEN OMINAISUUDET Korroosio on voimakkainta ilman ja veden rajapinnalla eli roiskevyöhykkeellä ja upotusvyöhykkeen yläosassa. Noustessa ylöspäin vedenpinnan tasosta korroosio muuttuu upotusrasituksesta ilmastorasitukseksi. Samoin laskeuduttaessa alaspäin vedenpinnasta korroosio hidastuu
14 m/year KORROOSIONOPEUKSIA ISOSAARESSA Multimetal immersion tests in Isosaari, one year test sets. Loss of thickness calculated from weight loss st set 4th set th set Al Cu Brass Steel Galvanized Zn -20 Metals Grafiitti Titaani "haponkestävä" Monel "ruostumaton" 70/30 CuNi Lyijy 90/10 CuNi Piipronssi Kupari Messinki Alumiinipronssi Hiiliteräs, valurauta Alumiiniseokset Sinkki Magnesium Korroosiopotentiaali [V vs. Ag/AgCl]
KORROOSIO KORROOSIOKENNO
 MT-0.3301 Korroosionestotekniikan perusteet osa 1 Perusideoiden kertausta Yleinen ja paikallinen korroosio Yleinen tai tasainen korroosio Eroosiokorroosio 2 KORROOSIO KORROOSIOKENNO Korroosio fysikaalis-kemiallinen
MT-0.3301 Korroosionestotekniikan perusteet osa 1 Perusideoiden kertausta Yleinen ja paikallinen korroosio Yleinen tai tasainen korroosio Eroosiokorroosio 2 KORROOSIO KORROOSIOKENNO Korroosio fysikaalis-kemiallinen
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä
 Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
Voimalaitoksen vesikemian yleiset tavoitteet ja peruskäsitteitä Susanna Vähäsarja ÅF-Consult 4.2.2016 1 Sisältö Vedenkäsittelyn vaatimukset Mitä voimalaitoksen vesikemialla tarkoitetaan? Voimalaitosten
Korroosion estäminen KORROOSIOKENNO KORROOSIONESTO KORROOSIONESTO. MT Korroosionestotekniikan teoreettiset perusteet
 Korroosion estäminen MT-0.3301 Korroosionestotekniikan teoreettiset perusteet KORROOSIOKENNO Anodi - Hapetusreaktio - Hapettuneiden aineiden siirtyminen liuokseen e - Johde Elektronit siirtyvät anodilta
Korroosion estäminen MT-0.3301 Korroosionestotekniikan teoreettiset perusteet KORROOSIOKENNO Anodi - Hapetusreaktio - Hapettuneiden aineiden siirtyminen liuokseen e - Johde Elektronit siirtyvät anodilta
Epäpuhtaudet vesi-höyrypiirissä lähteet ja vaikutukset
 Epäpuhtaudet vesihöyrypiirissä lähteet ja vaikutukset Susanna Vähäsarja ÅFConsult 11.2.2016 1 Sisältö Epäpuhtauksien lähteet ja kulkeutuminen vesihöyrypiirissä Korroosiovauriot ja muodot vesihöyrypiirissä
Epäpuhtaudet vesihöyrypiirissä lähteet ja vaikutukset Susanna Vähäsarja ÅFConsult 11.2.2016 1 Sisältö Epäpuhtauksien lähteet ja kulkeutuminen vesihöyrypiirissä Korroosiovauriot ja muodot vesihöyrypiirissä
Käytännön esimerkkejä on lukuisia.
 PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
PROSESSI- JA Y MPÄRISTÖTEKNIIK KA Ilmiömallinnus prosessimet allurgiassa, 01 6 Teema 4 Tehtävien ratkaisut 15.9.016 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA Yleistä Tämä dokumentti sisältää
Kemian opetuksen keskus Helsingin yliopisto Veden kovuus Oppilaan ohje. Veden kovuus
 Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
Huomaat, että vedenkeittimessäsi on valkoinen saostuma. Päättelet, että saostuma on peräisin vedestä. Haluat varmistaa, että vettä on turvallista juoda ja viet sitä tutkittavaksi laboratorioon. Laboratoriossa
METALLITEOLLISUUDEN PINTAKÄSITTELYN PERUSTEET - KORROOSIO
 METALLITEOLLISUUDEN PINTAKÄSITTELYN PERUSTEET - KORROOSIO 25.9.2014 Juha Kilpinen Tekninen Palvelu 1 METALLIN KORROOSIO Metallin korroosiolla tarkoitetaan sen syöpymistä ympäristön kanssa tapahtuvissa
METALLITEOLLISUUDEN PINTAKÄSITTELYN PERUSTEET - KORROOSIO 25.9.2014 Juha Kilpinen Tekninen Palvelu 1 METALLIN KORROOSIO Metallin korroosiolla tarkoitetaan sen syöpymistä ympäristön kanssa tapahtuvissa
Käsitteitä. Hapetusluku = kuvitteellinen varaus, jonka atomi saa elektronin siirtyessä
 Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Sähkökemia Nopea kertaus! Mitä seuraavat käsitteet tarkoittivatkaan? a) Hapettuminen b) Pelkistyminen c) Hapetusluku d) Elektrolyytti e) Epäjalometalli f) Jalometalli Käsitteitä Hapettuminen = elektronin
Ilmastollinen korroosio
 Ilmastollinen korroosio MT-0.3301 Korroosionestotekniikan perusteet Ilmastollinen korroosio Ilmastollinen korroosio yleisin korroosiotapahtuma osuus kaikista korroosiotapahtumista yli 80 % Ilmastollisella
Ilmastollinen korroosio MT-0.3301 Korroosionestotekniikan perusteet Ilmastollinen korroosio Ilmastollinen korroosio yleisin korroosiotapahtuma osuus kaikista korroosiotapahtumista yli 80 % Ilmastollisella
Elektrolyysi Anodilla tapahtuu aina hapettuminen ja katodilla pelkistyminen!
 Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
Elektrolyysi MATERIAALIT JA TEKNOLOGIA, KE4 Monet kemialliset reaktiot ovat palautuvia eli reversiibeleitä. Jo sähkökemian syntyvaiheessa oivallettiin, että on mahdollista rakentaa kahdenlaisia sähkökemiallisia
MT KORROOSIONESTOTEKNIIKAN PERUSTEET
 LUENNON PÄÄASIAT MT-0.3301 KORROOSIONESTOTEKNIIKAN PERUSTEET Korroosiokenno Evansin diagrammi E-pH diagrammi Passivoituminen 3. luento, lisää sähkökemiaa 2 Merivesi Anodi Katodi Teräs Veteen liuennut happi
LUENNON PÄÄASIAT MT-0.3301 KORROOSIONESTOTEKNIIKAN PERUSTEET Korroosiokenno Evansin diagrammi E-pH diagrammi Passivoituminen 3. luento, lisää sähkökemiaa 2 Merivesi Anodi Katodi Teräs Veteen liuennut happi
Sähkökemiaa. Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio
 Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio Hapettuminen ja pelkistyminen 1. Hapetin ja pelkistin 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi
Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Faradayn laki Korroosio Hapettuminen ja pelkistyminen 1. Hapetin ja pelkistin 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi
MT KORROOSIONESTOTEKNIIKAN PERUSTEET
 LUENNON PÄÄASIAT MT0.330 KORROOSIONESTOTEKNIIKAN PERUSTEET Korroosion termejä Faradayn laki ja korroosionopeus Sähkökemiallinen potentiaali Korroosiokenno 2. luento, sähkökemiaa 2 KORROOSIOILMIÖT KORROOSIOILMIÖT
LUENNON PÄÄASIAT MT0.330 KORROOSIONESTOTEKNIIKAN PERUSTEET Korroosion termejä Faradayn laki ja korroosionopeus Sähkökemiallinen potentiaali Korroosiokenno 2. luento, sähkökemiaa 2 KORROOSIOILMIÖT KORROOSIOILMIÖT
Normaalipotentiaalit
 Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
Normaalipotentiaalit MATERIAALIT JA TEKNOLOGIA, KE4 Yksittäisen elektrodin aiheuttaman jännitteen mittaaminen ei onnistu. Jännitemittareilla voidaan havaita ja mitata vain kahden elektrodin välinen potentiaaliero
Workshop: Tekniikan kemia OAMK:ssa
 1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
1 Oulun seudun ammattikorkeakoulu Kemian opetuksen päivät Tekniikan yksikkö OULU 2012 Workshop: Tekniikan kemia OAMK:ssa Miksi betonissa rauta ruostuu ulkopuolelta ja puussa sisäpuolelta? Rautatanko betonissa:
Sähkökemian perusteita, osa 1
 Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Sähkökemian perusteita, osa 1 Ilmiömallinnus prosessimetallurgiassa Syksy 2015 Teema 4 - Luento 1 Teema 4: Suoritustapana oppimispäiväkirja Tehdään yksin tai pareittain Tehtävät/ohjeet löytyvät kurssin
Sähkökemia. Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali
 Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Sähkökemia Sähkökemiallinen jännitesarja, galvaaninen kenno, normaalipotentiaali Esimerkki 1 Pohdi kertauksen vuoksi seuraavia käsitteitä a) Hapettuminen b) Pelkistin c) Hapetusluku d) Elektrolyytti e)
Vesi. Pintajännityksen Veden suuremman tiheyden nesteenä kuin kiinteänä aineena Korkean kiehumispisteen
 Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Vesi Hyvin poolisten vesimolekyylien välille muodostuu vetysidoksia, jotka ovat vahvimpia molekyylien välille syntyviä sidoksia. Vetysidos on sähköistä vetovoimaa, ei kovalenttinen sidos. Vesi Vetysidos
Evansin diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 4
 Evansin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 4 Tavoite Oppia hyödyntämään Evansin diagrammeja esimerkiksi hydrometallurgisissa tai korroosiotarkasteluissa 1 Termodynamiikka
Evansin diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 4 Tavoite Oppia hyödyntämään Evansin diagrammeja esimerkiksi hydrometallurgisissa tai korroosiotarkasteluissa 1 Termodynamiikka
Sähkökemiaa. Hapettuminen Jännitesarja Elektrolyysi Korroosio
 Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Korroosio Hapettuminen ja pelkistyminen 1. Määritelmät 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi ja sen sovelluksia
Sähkökemiaa Hapettuminen Jännitesarja Elektrolyysi Korroosio Hapettuminen ja pelkistyminen 1. Määritelmät 2. Hapetusluku Sähkökemiaa 1. Sähköpari 2. Metallien jännitesarja 3. Elektrolyysi ja sen sovelluksia
17VV VV Veden lämpötila 14,2 12,7 14,2 13,9 C Esikäsittely, suodatus (0,45 µm) ok ok ok ok L. ph 7,1 6,9 7,1 7,1 RA2000¹ L
 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, elokuu Näytteenottopvm: 22.8.2017 Näyte saapui: 23.8.2017 Näytteenottaja: Eerikki Tervo Analysointi
17VV VV 01021
 Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Pvm: 4.5.2017 1/5 Boliden Kevitsa Mining Oy Kevitsantie 730 99670 PETKULA Tutkimuksen nimi: Kevitsan vesistötarkkailu 2017, huhtikuu Näytteenottopvm: 4.4.2017 Näyte saapui: 6.4.2017 Näytteenottaja: Mika
Lkm keski- maksimi Lkm keski- maksimi. Lkm keski- maksimi Lkm keski- maksimi
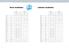 Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
Firan vesilaitos Lahelan vesilaitos Lämpötila C 12 9,5 14,4 12 7,9 8,5 ph-luku 12 6,6 6,7 12 8,0 8,1 Alkaliteetti mmol/l 12 0,5 0,5 12 1,1 1,1 Happi mg/l 12 4,2 5,3 12 11,5 13,2 Hiilidioksidi mg/l 12 21
MT Sähkökemialliset tutkimusmenetelmät
 .9. MT-. Sähkökemialliset tutkimusmenetelmät POTENTIO- JA GALVANOSTAATTISET MITTAUKSET Potentiostaattisissa menetelmissä näytettä pidetään vakiopotentiaalissa ja samalla mitataan kennosysteemin läpi kulkevaa
.9. MT-. Sähkökemialliset tutkimusmenetelmät POTENTIO- JA GALVANOSTAATTISET MITTAUKSET Potentiostaattisissa menetelmissä näytettä pidetään vakiopotentiaalissa ja samalla mitataan kennosysteemin läpi kulkevaa
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 5 25.1.2017 Hapettuminen ja pelkistyminen Alun perin hapettumisella tarkoitettiin aineen yhtymistä happeen l. palamista: 2 Cu + O 2 -> 2
Korroosiomuodot KORROOSIOMUODOT 11/6/2015. MT Korroosionestotekniikan perusteet KORROOSIOMUODOT osa 2 KORROOSIO
 MT-0.3301 Korroosionestotekniikan perusteet osa 2 Yleinen ja paikallinen korroosio Piste- ja rakokorroosio Raerajakorroosio Valikoiva liukeneminen Jännityskorroosio ja korroosioväsyminen Vetyhauraus 2
MT-0.3301 Korroosionestotekniikan perusteet osa 2 Yleinen ja paikallinen korroosio Piste- ja rakokorroosio Raerajakorroosio Valikoiva liukeneminen Jännityskorroosio ja korroosioväsyminen Vetyhauraus 2
Hapettuminen ja pelkistyminen: RedOx -reaktiot. CHEM-A1250 Luento
 Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
Hapettuminen ja pelkistyminen: RedOx -reaktiot CHEM-A1250 Luento 9 Sisältö ja oppimistavoitteet Johdanto sähkökemiaan Hapetusluvun ymmärtäminen Hapetus-pelkistys reaktioiden kirjoittaminen 2 Hapetusluku
Kuparin korroosio hapettomissa olosuhteissa
 Kuparin korroosio hapettomissa olosuhteissa Olof Forsén, Antero Pehkonen, Jari Aromaa Aalto-yliopisto Timo Saario VTT 1 Kuparin korroosio hapettomissa olosuhteissa Taustaa Aikaisemmat tutkimukset Tutkimuksen
Kuparin korroosio hapettomissa olosuhteissa Olof Forsén, Antero Pehkonen, Jari Aromaa Aalto-yliopisto Timo Saario VTT 1 Kuparin korroosio hapettomissa olosuhteissa Taustaa Aikaisemmat tutkimukset Tutkimuksen
Hapetus-pelkistymisreaktioiden tasapainottaminen
 Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
Hapetus-pelkistymisreaktioiden tasapainottaminen hapetuslukumenetelmällä MATERIAALIT JA TEKNO- LOGIA, KE4 Palataan hetkeksi 2.- ja 3.-kurssin asioihin ja tarkastellaan hapetus-pelkistymisreaktioiden tasapainottamista.
luku2 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen
 Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
Kappale 2 Hapettumis pelkistymisreaktioiden ennustaminen ja tasapainottaminen 1 Ennakkokysymyksiä 2 Metallien reaktioita ja jännitesarja Fe(s) + CuSO 4 (aq) Cu(s) + AgNO 3 (aq) taulukkokirja s.155 3 Metallien
Seokset ja liuokset. 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen
 Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Seokset ja liuokset 1. Seostyypit 2. Aineen liukoisuus 3. Pitoisuuden yksiköt ja mittaaminen Hapot, emäkset ja ph 1. Hapot, emäkset ja ph-asteikko 2. ph -laskut 3. Neutralointi 4. Puskuriliuokset Seostyypit
Liukeneminen 31.8.2016
 Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
Liukeneminen KEMIAN MIKROMAAILMA, KE2 Kertausta: Kun liukenevan aineen rakenneosasten väliset vuorovaikutukset ovat suunnilleen samanlaisia kuin liuottimen, niin liukenevan aineen rakenneosasten välisiä
c) Nimeä kaksi alkuainetta, jotka kuuluvat jaksollisessa järjestelmässä samaan ryhmään kalsiumin kanssa.
 Kurssikoe KE1.2, Ihmisen ja elinympäristön kemia, ke 6.4. 2016 Vastaa vain kuuteen tehtävään. Jokaisessa tehtävässä maksimi pistemäärä on kuusi pistettä (paitsi tehtävässä 7 seitsemän pistettä). Voit vapaasti
Kurssikoe KE1.2, Ihmisen ja elinympäristön kemia, ke 6.4. 2016 Vastaa vain kuuteen tehtävään. Jokaisessa tehtävässä maksimi pistemäärä on kuusi pistettä (paitsi tehtävässä 7 seitsemän pistettä). Voit vapaasti
Oppikirjan tehtävien ratkaisut
 Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
Oppikirjan tehtävien ratkaisut Liukoisuustulon käyttö 10. a) Selitä, mitä eroa on käsitteillä liukoisuus ja liukoisuustulo. b) Lyijy(II)bromidin PbBr liukoisuus on 1,0 10 mol/dm. Laske lyijy(ii)bromidin
MOOLIMASSA. Vedyllä on yksi atomi, joten Vedyn moolimassa M(H) = 1* g/mol = g/mol. ATOMIMASSAT TAULUKKO
 MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
MOOLIMASSA Moolimassan symboli on M ja yksikkö g/mol. Yksikkö ilmoittaa kuinka monta grammaa on yksi mooli. Moolimassa on yhden moolin massa, joka lasketaan suhteellisten atomimassojen avulla (ATOMIMASSAT
Firan vesilaitos. Laitosanalyysit. Lkm keski- maksimi Lkm keski- maksimi
 Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
Laitosanalyysit Firan vesilaitos Lämpötila C 3 8,3 8,4 4 8,4 9 ph-luku 3 6,5 6,5 4 7,9 8,1 Alkaliteetti mmol/l 3 0,53 0,59 4 1 1,1 Happi 3 2,8 4 4 11,4 11,7 Hiilidioksidi 3 23,7 25 4 1 1,9 Rauta Fe 3
vi) Oheinen käyrä kuvaa reaktiosysteemin energian muutosta reaktion (1) etenemisen funktiona.
 3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
3 Tehtävä 1. (8 p) Seuraavissa valintatehtävissä on esitetty väittämiä, jotka ovat joko oikein tai väärin. Merkitse paikkansapitävät väittämät rastilla ruutuun. Kukin kohta voi sisältää yhden tai useamman
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa
 Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa Jari Aromaa, Lotta Rintala Teknillinen korkeakoulu Materiaalitekniikan laitos 1. Taustaa, miksi kupari syöpyy ja kuinka
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa Jari Aromaa, Lotta Rintala Teknillinen korkeakoulu Materiaalitekniikan laitos 1. Taustaa, miksi kupari syöpyy ja kuinka
AKKU- JA PARISTOTEKNIIKAT
 AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
AKKU- JA PARISTOTEKNIIKAT H.Honkanen Kemiallisessa sähköparissa ( = paristossa ) ylempänä oleva, eli negatiivisempi, metalli syöpyy liuokseen. Akussa ei elektrodi syövy pois, vaan esimerkiksi lyijyakkua
Vesijohtoverkostosta ja -laitteista talousveteen liukenevat metallit
 1.5.217 Vesijohtoverkostosta ja -laitteista talousveteen liukenevat metallit Vesihuoltopäivät Jyväskylä 1.5.217 8.5.217 Page 1 Hankkeen tausta Juomavesidirektiivin muutos (liite II D) Talousveden valvontanäytteet
1.5.217 Vesijohtoverkostosta ja -laitteista talousveteen liukenevat metallit Vesihuoltopäivät Jyväskylä 1.5.217 8.5.217 Page 1 Hankkeen tausta Juomavesidirektiivin muutos (liite II D) Talousveden valvontanäytteet
1. Malmista metalliksi
 1. Malmista metalliksi Metallit esiintyvät maaperässä yhdisteinä, mineraaleina Malmiksi sanotaan kiviainesta, joka sisältää jotakin hyödyllistä metallia niin paljon, että sen erottaminen on taloudellisesti
1. Malmista metalliksi Metallit esiintyvät maaperässä yhdisteinä, mineraaleina Malmiksi sanotaan kiviainesta, joka sisältää jotakin hyödyllistä metallia niin paljon, että sen erottaminen on taloudellisesti
kemiallisesti puhdas vesi : tislattua vettä käytetään mm. höyrysilitysraudoissa (saostumien ehkäisy)
 Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
Pesukemian perusteet Veden pesuominaisuudet 1. kostuttaa 2. liuottaa (dipoli) 3. laimentaa 4. liikkuva vesi tekee mekaanista työtä 5. kuljettaa kemiallisesti puhdas vesi : tislattua vettä käytetään mm.
2.1 Sähköä kemiallisesta energiasta
 2.1 Sähköä kemiallisesta energiasta Monet hapettumis ja pelkistymisreaktioista on spontaaneja, jolloin elektronien siirtyminen tapahtuu itsestään. Koska reaktio on spontaani, vapautuu siinä energiaa, yleensä
2.1 Sähköä kemiallisesta energiasta Monet hapettumis ja pelkistymisreaktioista on spontaaneja, jolloin elektronien siirtyminen tapahtuu itsestään. Koska reaktio on spontaani, vapautuu siinä energiaa, yleensä
Johdantoa. Kemia on elektronien liikkumista/siirtymistä. Miksi?
 Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Mitä on kemia? Johdantoa REAKTIOT JA ENERGIA, KE3 Kemia on elektronien liikkumista/siirtymistä. Miksi? Kaikissa kemiallisissa reaktioissa tapahtuu energian muutoksia, jotka liittyvät vanhojen sidosten
Määritelmät. Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin
 Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Hapot ja emäkset Määritelmät Happo = luovuttaa protonin H + Emäs = vastaanottaa protonin Happo-emäsreaktioita kutsutaan tästä johtuen protoninsiirto eli protolyysi reaktioiksi Protolyysi Happo Emäs Emäs
Kestääkö kuparikapseli
 Kestääkö kuparikapseli korroosiota 100 000 vuotta? Olof Forsén Materiaalitekniikan laitos KUPARIN KORROOSIONKESTÄVYYS Yleistä Kuparin korroosionkestävyys k on hyvä maassa, vedessä ja ilmassa maassa kuparin
Kestääkö kuparikapseli korroosiota 100 000 vuotta? Olof Forsén Materiaalitekniikan laitos KUPARIN KORROOSIONKESTÄVYYS Yleistä Kuparin korroosionkestävyys k on hyvä maassa, vedessä ja ilmassa maassa kuparin
Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu ylöspäin, esim. 2 1/2 p = 2 p.
 Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Diplomi-insinöörien ja arkkitehtien yhteisvalinta dia-valinta 014 Insinöörivalinnan kemian koe 8.5.014 MALLIRATKAISUT ja PISTEET Lasku- ja huolimattomuusvirheet ½ p. Loppupisteiden puolia pisteitä ei korotettu
Jännittävät metallit
 Jännittävät metallit Tästä alkaa tutkimusmatkamme sähkön syntymiseen! Varmaan tiedätkin, että sähköä saadaan sekä pistorasioista että erilaisista paristoista. Pistorasioista saatava sähkö tuotetaan fysikaalisesti,
Jännittävät metallit Tästä alkaa tutkimusmatkamme sähkön syntymiseen! Varmaan tiedätkin, että sähköä saadaan sekä pistorasioista että erilaisista paristoista. Pistorasioista saatava sähkö tuotetaan fysikaalisesti,
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo. Luento 8 CHEM-A1250
 Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Kemiallinen tasapaino 3: Puskuriliuokset Liukoisuustulo Luento 8 CHEM-A1250 Puskuriliuokset Puskuriliuos säilyttää ph:nsa, vaikka liuosta väkevöidään tai laimennetaan tai siihen lisätään pieniä määriä
Seoksen pitoisuuslaskuja
 Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
Seoksen pitoisuuslaskuja KEMIAA KAIKKIALLA, KE1 Analyyttinen kemia tutkii aineiden määriä ja pitoisuuksia näytteissä. Pitoisuudet voidaan ilmoittaa: - massa- tai tilavuusprosentteina - promilleina tai
SAIPPUALIUOKSEN SÄHKÖKEMIA 09-2009 JOHDANTO
 SAIPPUALIUOKSEN SÄHKÖKEMIA 09-009 JOHDANTO 1 lainaus ja kuvat lähteestä: Työssä tutkitaan johtokyky- ja ph-mittauksilla tavallisen palasaippuan kemiallista koostumusta ja misellien ja aggregaattien muodostumista
SAIPPUALIUOKSEN SÄHKÖKEMIA 09-009 JOHDANTO 1 lainaus ja kuvat lähteestä: Työssä tutkitaan johtokyky- ja ph-mittauksilla tavallisen palasaippuan kemiallista koostumusta ja misellien ja aggregaattien muodostumista
METALLITASE, KOKONAISLIUOTUSSAANTI JA KANNATTAVUUS
 METALLITASE, KOKONAISLIUOTUSSAANTI JA KANNATTAVUUS Document name: METALLITASE, Version: 1 KOKONAISLIUOTUSSAANTI JA KANNATTAVUUS Creation time: Virhe. Tuntematon asiakirjan ominaisuuden nimi. Date: Virhe.
METALLITASE, KOKONAISLIUOTUSSAANTI JA KANNATTAVUUS Document name: METALLITASE, Version: 1 KOKONAISLIUOTUSSAANTI JA KANNATTAVUUS Creation time: Virhe. Tuntematon asiakirjan ominaisuuden nimi. Date: Virhe.
Metallien ominaisuudet ja rakenne
 Metallien Kemia 25 Metallien ominaisuudet ja rakenne Metallit ovat käyttökelpoisia materiaaleja. Niiden ominaisuudet johtuvat metallin rakennetta koossa pitävästä metallisidoksesta. Metalleja käytetään
Metallien Kemia 25 Metallien ominaisuudet ja rakenne Metallit ovat käyttökelpoisia materiaaleja. Niiden ominaisuudet johtuvat metallin rakennetta koossa pitävästä metallisidoksesta. Metalleja käytetään
125,0 ml 0,040 M 75,0+125,0 ml Muodostetaan ionitulon lauseke ja sijoitetaan hetkelliset konsentraatiot
 4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
4.4 Syntyykö liuokseen saostuma 179. Kirjoita tasapainotettu nettoreaktioyhtälö olomuotomerkintöineen, kun a) fosforihappoliuokseen lisätään kaliumhydroksidiliuosta b) natriumvetysulfaattiliuokseen lisätään
 PROSESSI - JA YM P ÄRI STÖTEKNII K AN OS ASTO I lmi ömalli nnus prosessi metallurgi assa, 201 2 Teema 4 Tehtävänanto ja työselostusohje 21.9.2012 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA
PROSESSI - JA YM P ÄRI STÖTEKNII K AN OS ASTO I lmi ömalli nnus prosessi metallurgi assa, 201 2 Teema 4 Tehtävänanto ja työselostusohje 21.9.2012 SÄHKÖKEMIALLISTEN REAKTIOIDEN TERMODYNAMIIKKA JA KINETIIKKA
Veden kovuus. KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi.
 KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi. KESTO: n. 60 min. Työn kesto riippuu käsittelylaajuudesta ja ryhmän koosta. MOTIVAATIO: Huomaat,
KOHDERYHMÄ: Työ on suunniteltu lukiolaisille. Se voidaan tehdä esimerkiksi kursseilla KE5 ja työkurssi. KESTO: n. 60 min. Työn kesto riippuu käsittelylaajuudesta ja ryhmän koosta. MOTIVAATIO: Huomaat,
MT Korroosionestotekniikan perusteet
 Kurssin sisältö MT-0.3301 Korroosionestotekniikan perusteet dosentti Jari Aromaa Materiaalien, erityisesti metallien korroosioilmiöt sähkökemiallisen teorian pohjalta. Metallien liukenemisen perusteet
Kurssin sisältö MT-0.3301 Korroosionestotekniikan perusteet dosentti Jari Aromaa Materiaalien, erityisesti metallien korroosioilmiöt sähkökemiallisen teorian pohjalta. Metallien liukenemisen perusteet
Kuparikapselin korroosio
 Kuparikapselin korroosio Ydinjätteen loppusijoituksen mikrobiologia KYT2018-seminaari April 24, 2018 Pauliina Rajala VTT Technical Research Centre of Finland Ltd. Mikrobit Mikrobeilla tarkoitetaan mikroskooppisen
Kuparikapselin korroosio Ydinjätteen loppusijoituksen mikrobiologia KYT2018-seminaari April 24, 2018 Pauliina Rajala VTT Technical Research Centre of Finland Ltd. Mikrobit Mikrobeilla tarkoitetaan mikroskooppisen
Ioniselektiivinen elektrodi
 ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
ELEC-A8510 Biologisten ilmiöiden mittaaminen Ioniselektiivinen elektrodi Luento 2 h: menetelmän teoria ja laboratoriotyön esittely Itsenäinen työskentely 2 h: materiaaliin tutustuminen Laboratoriotyöskentely
TUTKIMUSTODISTUS. Jyväskylän Ympäristölaboratorio. Sivu: 1(1) Päivä: 09.10.14. Tilaaja:
 Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Jyväskylän Ympäristölaboratorio TUTKIMUSTODISTUS Päivä: 09.10.14 Sivu: 1(1) Tilaaja: PIHTIPUTAAN LÄMPÖ JA VESI OY C/O SYDÄN-SUOMEN TALOUSHAL. OY ARI KAHILAINEN PL 20 44801 PIHTIPUDAS Näyte: Verkostovesi
Kemia ja ympäristö opintojakso
 1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
1 FILE:\EVTEK_Kemia ja ymparisto_luku5 ja 6_03102005 Opettaja: Pekka Lehtonen GSM: 050-3595099 E-mail: pekka.lehtonen@evtek.fi opintojakso Tiivistelmä oppikrjan luvuista 5 ja 6 LUKU 5: SEOKSET - Liuokset
b) Reaktio Zn(s) + 2 Ag + (aq) Zn 2+ (aq) + 2 Ag (s) tapahtuu galvaanisessa kennossa. Kirjoita kennokaavio eli kennon lyhennetty esitys.
 KE4-KURSSIN KOE Kastellin lukio 2013 Vastaa kuuteen (6) kysymykseen. Tee pisteytysruudukko. 1. Tarkastele jaksollista järjestelmää ja valitse siitä a) jokin jalometalli. b) jokin alkuaine, joka reagoi
KE4-KURSSIN KOE Kastellin lukio 2013 Vastaa kuuteen (6) kysymykseen. Tee pisteytysruudukko. 1. Tarkastele jaksollista järjestelmää ja valitse siitä a) jokin jalometalli. b) jokin alkuaine, joka reagoi
Tehtäviä sähkökemiasta
 Tehtäviä sähkökemiasta 1. Millainen on sähkökemiallinen jännitesarja? Mitä sen avulla voidaan kuvata? Jännitesarjalla kuvataan metallien taipumusta muodostaa kemiallisia yhdisteitä. Metallit on järjestetty
Tehtäviä sähkökemiasta 1. Millainen on sähkökemiallinen jännitesarja? Mitä sen avulla voidaan kuvata? Jännitesarjalla kuvataan metallien taipumusta muodostaa kemiallisia yhdisteitä. Metallit on järjestetty
Rauta-hiili tasapainopiirros
 Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Rauta-hiili tasapainopiirros Teollisen ajan tärkein tasapainopiirros Tasapainon mukainen piirros on Fe-C - piirros, kuitenkin terästen kohdalla Fe- Fe 3 C -piirros on tärkeämpi Fe-Fe 3 C metastabiili tp-piirrosten
Liitetaulukko 1/11. Tutkittujen materiaalien kokonaispitoisuudet KOTIMAINEN MB-JÄTE <1MM SAKSAN MB- JÄTE <1MM POHJAKUONA <10MM
 Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Liitetaulukko 1/11 Tutkittujen materiaalien kokonaispitoisuudet NÄYTE KOTIMAINEN MB-JÄTE
Osio 1. Laskutehtävät
 Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
Osio 1. Laskutehtävät Nämä palautetaan osion1 palautuslaatikkoon. Aihe 1 Alkuaineiden suhteelliset osuudet yhdisteessä Tehtävä 1 (Alkuaineiden suhteelliset osuudet yhdisteessä) Tarvitset tehtävään atomipainotaulukkoa,
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
Kuumasinkittyjen teräsrakenteiden käyttöikä
 Kuumasinkittyjen teräsrakenteiden käyttöikä Teräs on aikamme käytetyin materiaali ja 100 % kierrätettävä. Teräs kuitenkin syöpyy hapen ja kosteuden vaikutuksesta, jonka takia se on suojattava ruostumista
Kuumasinkittyjen teräsrakenteiden käyttöikä Teräs on aikamme käytetyin materiaali ja 100 % kierrätettävä. Teräs kuitenkin syöpyy hapen ja kosteuden vaikutuksesta, jonka takia se on suojattava ruostumista
Dislokaatiot - pikauusinta
 Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Dislokaatiot - pikauusinta Ilman dislokaatioita Kiteen teoreettinen lujuus ~ E/8 Dislokaatiot mahdollistavat deformaation Kaikkien atomisidosten ei tarvitse murtua kerralla Dislokaatio etenee rakeen läpi
Kemia 3 op. Kirjallisuus: MaoL:n taulukot: kemian sivut. Kurssin sisältö
 Kemia 3 op Kirjallisuus: MaoL:n taulukot: kemian sivut Kurssin sisältö 1. Peruskäsitteet ja atomin rakenne 2. Jaksollinen järjestelmä,oktettisääntö 3. Yhdisteiden nimeäminen 4. Sidostyypit 5. Kemiallinen
Kemia 3 op Kirjallisuus: MaoL:n taulukot: kemian sivut Kurssin sisältö 1. Peruskäsitteet ja atomin rakenne 2. Jaksollinen järjestelmä,oktettisääntö 3. Yhdisteiden nimeäminen 4. Sidostyypit 5. Kemiallinen
Ohjeita opetukseen ja odotettavissa olevat tulokset
 Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Ohjeita opetukseen ja odotettavissa olevat tulokset Ensimmäinen sivu on työskentelyyn orientoiva johdatteluvaihe, jossa annetaan jotain tietoja ongelmista, joita happamat sateet aiheuttavat. Lisäksi esitetään
Näytenumero Näytetunnus Tunnus Ottopvm. Näytteenottaja Saapunut pvm. Tutkimus alkoi Tutkimus valmis
 Tutkimustodistus '1.RA03' Kierros: elo 26.09.2018 Ranuan Infra Oy Keskustie 11 97700 Ranua Tulokset hyväksynyt Hanna Kemppe Laboratoriokemisti 040 704 0528 22569 (26.09.2018), 22570 (21.09.2018), 22571
Tutkimustodistus '1.RA03' Kierros: elo 26.09.2018 Ranuan Infra Oy Keskustie 11 97700 Ranua Tulokset hyväksynyt Hanna Kemppe Laboratoriokemisti 040 704 0528 22569 (26.09.2018), 22570 (21.09.2018), 22571
a) Puhdas aine ja seos b) Vahva happo Syövyttävä happo c) Emäs Emäksinen vesiliuos d) Amorfinen aine Kiteisen aineen
 1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
1. a) Puhdas aine ja seos Puhdas aine on joko alkuaine tai kemiallinen yhdiste, esim. O2, H2O. Useimmat aineet, joiden kanssa olemme tekemisissä, ovat seoksia. Mm. vesijohtovesi on liuos, ilma taas kaasuseos
Testausseloste 2009-2611-1 1(1) Vesinäyte 31.07.2009
 Testausseloste 2009-2611-1 1(1) Vesinäyte 31.07.2009 Ulvilan Näytetiedot Näyte Näyte otettu 28.07.2009 Näytteen ottaja Haanpää Saapunut 28.07.2009 Näytteenoton syy Jatkuva valvonta Tutkimus alkoi 28.07.2009
Testausseloste 2009-2611-1 1(1) Vesinäyte 31.07.2009 Ulvilan Näytetiedot Näyte Näyte otettu 28.07.2009 Näytteen ottaja Haanpää Saapunut 28.07.2009 Näytteenoton syy Jatkuva valvonta Tutkimus alkoi 28.07.2009
VILJAVUUSTUTKIMUS s-posti: neuvonta@viljavuuspalvelu.fi Päivämäärä Asiakasnro Tutkimusnro
 1/8 Näytteen numero 1 2 3 4 5 6 7 Peruslohkotunnus 754-07722- 19 754-07334- 19 Pintamaan maalaji a) HeS HeS HeS HeS HsS HsS HeS Multavuus a) rm rm rm rm rm rm rm 0,8 1,0 0,7 0,5 0,4 0,6 0,5 Happamuus ph
1/8 Näytteen numero 1 2 3 4 5 6 7 Peruslohkotunnus 754-07722- 19 754-07334- 19 Pintamaan maalaji a) HeS HeS HeS HeS HsS HsS HeS Multavuus a) rm rm rm rm rm rm rm 0,8 1,0 0,7 0,5 0,4 0,6 0,5 Happamuus ph
KaiHali. Järvisedimentin ja suoturpeen luontainen kyky poistaa kaivosveden sulfaatti- ja metallikuormitusta
 KaiHali Järvisedimentin ja suoturpeen luontainen kyky poistaa kaivosveden sulfaatti- ja metallikuormitusta Lehtoranta J., Ekholm P., Laamanen T. Taustaa Suot ja sulfaatti Palviainen, M., Lehtoranta, J.,
KaiHali Järvisedimentin ja suoturpeen luontainen kyky poistaa kaivosveden sulfaatti- ja metallikuormitusta Lehtoranta J., Ekholm P., Laamanen T. Taustaa Suot ja sulfaatti Palviainen, M., Lehtoranta, J.,
MT Sähkökemialliset tutkimusmenetelmät
 MT-.66 Sähkökemialliset tutkimusmenetelmät VOLTAMETRIA Voltametriassa tutkitaan mittaussysteemissä kulkevan virran muutoksia ulkoisen jännitesignaalin muuttuessa. Voltametriassa virtaa pidetään funktiona
MT-.66 Sähkökemialliset tutkimusmenetelmät VOLTAMETRIA Voltametriassa tutkitaan mittaussysteemissä kulkevan virran muutoksia ulkoisen jännitesignaalin muuttuessa. Voltametriassa virtaa pidetään funktiona
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa
 Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa TkT Jari Aromaa Teknillinen korkeakoulu Korroosion ja materiaalikemian laboratorio TAUSTAA Kuparin yleinen korroosio voi
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa TkT Jari Aromaa Teknillinen korkeakoulu Korroosion ja materiaalikemian laboratorio TAUSTAA Kuparin yleinen korroosio voi
METSÄTAIMITARHAPÄIVÄT 2016 KEKKILÄ PROFESSIONAL
 METSÄTAIMITARHAPÄIVÄT 2016 KEKKILÄ PROFESSIONAL Superex - kastelulannoitteet Vesiliukoiset Superex lannoitteet Puhtaita ja täysin vesiliukoisia ph 4,5-4,8 Kastelusuuttimet pysyvät auki Voidaan sekoittaa
METSÄTAIMITARHAPÄIVÄT 2016 KEKKILÄ PROFESSIONAL Superex - kastelulannoitteet Vesiliukoiset Superex lannoitteet Puhtaita ja täysin vesiliukoisia ph 4,5-4,8 Kastelusuuttimet pysyvät auki Voidaan sekoittaa
MT Korroosionestotekniikan perusteet
 MT-0.330 Korroosionestotekniikan perusteet. 2. Yksinkertaistetut korroosiojärjestelmät 3. Ilmastollinen korroosio 4. Sähkökemialliset mittaukset 5. Sähkökemian laitteisto 2 Ensimmäinen korroosiotutkimus
MT-0.330 Korroosionestotekniikan perusteet. 2. Yksinkertaistetut korroosiojärjestelmät 3. Ilmastollinen korroosio 4. Sähkökemialliset mittaukset 5. Sähkökemian laitteisto 2 Ensimmäinen korroosiotutkimus
CHEM-A1410 Materiaalitieteen perusteet, 4. luento, muut ominaisuudet
 CHEM-A1410, luento 4 CHEM-A1410 Materiaalitieteen perusteet, 4. luento, muut ominaisuudet Jari Aromaa, Kemian tekniikan ja metallurgian laitos 4. luento, sisällys Kiinteän materiaalin ominaisuudet ovat:
CHEM-A1410, luento 4 CHEM-A1410 Materiaalitieteen perusteet, 4. luento, muut ominaisuudet Jari Aromaa, Kemian tekniikan ja metallurgian laitos 4. luento, sisällys Kiinteän materiaalin ominaisuudet ovat:
Luku 3. Protolyysireaktiot ja vesiliuoksen ph
 Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Luku 3 Protolyysireaktiot ja vesiliuoksen ph 1 MIKÄ ALKUAINE? Se ei ole metalli, kuten alkalimetallit, se ei ole jalokaasu, vaikka onkin kaasu. Kevein, väritön, mauton, hajuton, maailmankaikkeuden yleisin
Pourbaix-diagrammit. Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 3
 Pourbaix-diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 3 Tavoite Oppia hyödyntämään Pourbaix-piirroksia esimerkiksi hydrometallurgisissa tai korroosiotarkasteluissa 1 Mikä
Pourbaix-diagrammit Ilmiömallinnus prosessimetallurgiassa Syksy 2016 Teema 4 - Luento 3 Tavoite Oppia hyödyntämään Pourbaix-piirroksia esimerkiksi hydrometallurgisissa tai korroosiotarkasteluissa 1 Mikä
www.ruukki.com MINERAALI- TUOTTEET Kierrätys ja Mineraalituotteet
 www.ruukki.com MINERAALI- TUOTTEET Kierrätys ja Mineraalituotteet Masuunihiekka stabiloinnit (sideaineena) pehmeikkörakenteet sidekivien alusrakenteet putkijohtokaivannot salaojan ympärystäytöt alapohjan
www.ruukki.com MINERAALI- TUOTTEET Kierrätys ja Mineraalituotteet Masuunihiekka stabiloinnit (sideaineena) pehmeikkörakenteet sidekivien alusrakenteet putkijohtokaivannot salaojan ympärystäytöt alapohjan
Happamat sulfaattimaat ja niiden tunnistaminen. Mirkka Hadzic Suomen ympäristökeskus, SYKE Vesistökunnostusverkoston vuosiseminaari 2018
 Happamat sulfaattimaat ja niiden tunnistaminen Mirkka Hadzic Suomen ympäristökeskus, SYKE Vesistökunnostusverkoston vuosiseminaari 2018 Kuva: https://commons.wikimedia.org/wiki/file:litorinameri_5000_eaa.svg
Happamat sulfaattimaat ja niiden tunnistaminen Mirkka Hadzic Suomen ympäristökeskus, SYKE Vesistökunnostusverkoston vuosiseminaari 2018 Kuva: https://commons.wikimedia.org/wiki/file:litorinameri_5000_eaa.svg
Liite 1. Saimaa. Immalanjärvi. Vuoksi. Mellonlahti. Joutseno. Venäjä
 Liite 1 Saimaa Immalanjärvi Vuoksi Mellonlahti Joutseno Venäjä Liite 2 1 5 4 3 2 Liite 3 puron patorakennelma Onnelan lehto Onnelan lehto Mellonlahden ranta Liite 4 1/7 MELLONLAHDEN TILAN KEHITYS VUOSINA
Liite 1 Saimaa Immalanjärvi Vuoksi Mellonlahti Joutseno Venäjä Liite 2 1 5 4 3 2 Liite 3 puron patorakennelma Onnelan lehto Onnelan lehto Mellonlahden ranta Liite 4 1/7 MELLONLAHDEN TILAN KEHITYS VUOSINA
Kangasalan Vesi, valvojana Ins. Kimmo Suonperä
 TAMPEREEN AMMATTIKORKEAKOULU Kemiantekniikan koulutusohjelma Opinnäytetyö KALKKIKIVIROUHEELLA SUORITETTAVAN ALKALOINNIN OPTIMOIMINEN Työn ohjaaja Työn teettäjä Tampere 2007 DI Esa Väliaho Kangasalan Vesi,
TAMPEREEN AMMATTIKORKEAKOULU Kemiantekniikan koulutusohjelma Opinnäytetyö KALKKIKIVIROUHEELLA SUORITETTAVAN ALKALOINNIN OPTIMOIMINEN Työn ohjaaja Työn teettäjä Tampere 2007 DI Esa Väliaho Kangasalan Vesi,
Tutkimusmateriaalit -ja välineet: kaarnan palaset, hiekan murut, pihlajanmarjat, juuripalat, pakasterasioita, vettä, suolaa ja porkkananpaloja.
 JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
JIPPO-POLKU Jippo-polku sisältää kokeellisia tutkimustehtäviä toteutettavaksi perusopetuksessa, kerhossa tai kotona. Polun tehtävät on tarkoitettu suoritettavaksi luonnossa joko koulun tai kerhon lähimaastossa,
EPÄORGAANINEN KEMIA HARJOITUKSIA. Jaksollinen järjestelmä
 EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
EPÄORGAANINEN KEMIA HARJOITUKSIA Jaksollinen järjestelmä Mitkä alkuaineet ovat oheisesta jaksollisesta järjestelmästä peitetyt A ja B? Mitkä ovat A:n ja B:n muodostamien kloridien stoikiometriat? Jos alkuaineita
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
KE5 Kurssikoe Kastellin lukio 2012 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko.
 KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
KE5 Kurssikoe Kastellin lukio 01 Valitse kuusi (6) tehtävää. Piirrä pisteytystaulukko. 1. a) Selvitä, mitä tarkoitetaan seuraavilla käsitteillä lyhyesti sanallisesti ja esimerkein: 1) heikko happo polyproottinen
Liuos voi olla hapan, emäksinen tai neutraali
 Hapot ja emäkset 19 Liuos voi olla hapan, emäksinen tai neutraali happamuuden aiheuttavat oksoniumionit Monet marjat, hedelmät ja esimerkiksi piimä maistuvat happamilta. Happamuus seuraa siitä kun happo
Hapot ja emäkset 19 Liuos voi olla hapan, emäksinen tai neutraali happamuuden aiheuttavat oksoniumionit Monet marjat, hedelmät ja esimerkiksi piimä maistuvat happamilta. Happamuus seuraa siitä kun happo
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka
 Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
Kaikenlaisia sidoksia yhdisteissä: ioni-, kovalenttiset ja metallisidokset Fysiikan ja kemian perusteet ja pedagogiikka Kari Sormunen Kevät 2012 Kertausta IONIEN MUODOSTUMISESTA Jos atomi luovuttaa tai
TERRAFAME OY TERRAFAMEN KAIVOKSEN VELVOITETARKKAILU 2015 OSA IX: POHJAVEDET
 Vastaanottaja Terrafame Oy Asiakirjatyyppi Vuosiraportti Päivämäärä 2.5.2016 Viite 1510016678 ja 1510021110 TERRAFAME OY TERRAFAMEN KAIVOKSEN VELVOITETARKKAILU 2015 OSA IX: POHJAVEDET TERRAFAME OY TERRAFAMEN
Vastaanottaja Terrafame Oy Asiakirjatyyppi Vuosiraportti Päivämäärä 2.5.2016 Viite 1510016678 ja 1510021110 TERRAFAME OY TERRAFAMEN KAIVOKSEN VELVOITETARKKAILU 2015 OSA IX: POHJAVEDET TERRAFAME OY TERRAFAMEN
PERTUNMAAN JA HEINOLAN JÄRVITUTKIMUKSET VUONNA 2007
 PERTUNMAAN JA HEINOLAN JÄRVITUTKIMUKSET VUONNA 27 Kymijoen vesi ja ympäristö ry:n tutkimusraportti no 91/27 Anne Åkerberg SISÄLLYS sivu 1 Johdanto 1 2 Näytteenotto ja sääolot 1 3 Tulokset 2 3.1 Lämpötila
PERTUNMAAN JA HEINOLAN JÄRVITUTKIMUKSET VUONNA 27 Kymijoen vesi ja ympäristö ry:n tutkimusraportti no 91/27 Anne Åkerberg SISÄLLYS sivu 1 Johdanto 1 2 Näytteenotto ja sääolot 1 3 Tulokset 2 3.1 Lämpötila
TUTKIMUSSELOSTE. Tutkimuksen lopetus pvm. Näkösyv. m
 TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 3 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
TUTKIMUSSELOSTE Tarkkailu: Talvivaaran prosessin ylijäämävedet 2012 Jakelu: pirkko.virta@poyry.com Tarkkailukierros: vko 3 hanna.kurtti@poyry.com Tilaaja: Pöyry Finland Oy Havaintopaikka Tunnus Näytenumero
Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta.
 Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Helsingin yliopiston kemian valintakoe 10.5.2019 Vastaukset ja selitykset Tehtävä 1. Avaruussukkulan kiihdytysvaiheen kiinteänä polttoaineena käytetään ammonium- perkloraatin ja alumiinin seosta. Reaktio
Kontroll över surheten i Perho ås nedre del (PAHAprojektet) Juhani Hannila & Mats Willner PAHA-loppuseminaari Kokkola 30.10.2014
 Kontroll över surheten i Perho ås nedre del (PAHAprojektet) Juhani Hannila & Mats Willner PAHA-loppuseminaari Kokkola 30.10.2014 PAHA-hanke Perhonjoen alaosan happamuuden hallinta (PAHA- hanke) toteutetaan
Kontroll över surheten i Perho ås nedre del (PAHAprojektet) Juhani Hannila & Mats Willner PAHA-loppuseminaari Kokkola 30.10.2014 PAHA-hanke Perhonjoen alaosan happamuuden hallinta (PAHA- hanke) toteutetaan
