[B] (11) (45)Patentti myönnetty Patent m-2ddelat (51) Kvik.'/Int.C1. 1 A 61 K 37/24. (21) Patenttlhakemus PatentansöknIng
|
|
|
- Pasi Lattu
- 8 vuotta sitten
- Katselukertoja:
Transkriptio
1 [B] (11) KUULUTUSJULKAISU c)1997 UTLÄGGNINGSSKRIFT,J" SUOMI FINLAND (F I) Patentti- ja rekisterihallitus Patent- och registerstyrelsen (45)Patentti myönnetty Patent m-2ddelat (51) Kvik.'/Int.C1. 1 A 61 K 37/24 C 7 C 13/52 C 7 G 7/ (21) Patenttlhakemus PatentansöknIng (22) Hakemispålvä Ansökningsdag (23) Alkupalvi GlItighetsdag (41) Tullut julkiseksi Blivit offentlig (44) Nit~lksipancm ja ktml.lulltmsun pvm. Ansökan utlagd och utl.skriften publicerad (32)(33)(31) Pyydetty etuoikeus Begard prioritet USA(US) Toteennäytetty-Styrkt (71)All India Institute of Medical Sciences, New Delhi, 1116, Intia-Indien(IN) (72)Gursaran Parshad Talwar, New Delhi, Intia-Indien(IN) (74) Antti Impola. (54) Menetelmä rokotteen valmistamiseksi raskauden estämistä varten - Förfarande för framställning av ett vaccin för förhindrande av graviditet Esillä oleva keksintö koskee menetelmää rokotteen valmistamiseksi raskauden estämistä varten. Tunnetaan erilaisia menetelmiä hedelmöittymisen kontrolloimiseksi ja raskauden estämiseksi ja lopettamiseksi. Lukuisia keinoja, kuten kondomeja, mekaanisia välineitä, spermisidaalisia voiteita ja hyytelöitä, vaahtotabletteja, suun kautta annettavia pillereitä jne, ovat saatavissa ehkäisynä raskautta vastaan. Näillä menetelmillä, vaikkakin ne ovat tehokkaita vaihtelevassa määrässä, on myös rajoituksensa. Useimmat niistä vaativat jatkuvaa perustelua käyttäjän o- salta. Toiset vaativat spesialisoitua lääkärintutkimusta. Immunologisten menetelmien kehittäminen hedelmöittymisen säätämiseksi on ollut tutkimuksen kohteena tämän vuosisadan alusta alkaen. Albert Tyler on kuvannut useita tapoja julkaisussa "Approaches to the Control of Fertility Based on Immunological Phenomena", Journal of Reproduction and Fertility, (1961)2, sivut " Tavoista, joita tutkijat ovat viimevuosina seuranneet, mainittakoon immunoiminen istukka-, sikiö- tai hormooniaineksilla. Tähän saakka ei ole kuitenkaan voitu kehittää mitään tehokasta rokotetta hedelmöittymistä vastaan. Esillä oleva keksintö perustuu vasta-aineeseen, joka aktiivisesti immunoi hormoonin, joka on kriitillinen raskauden alkuunsaattamiseksi ja ylläpitämiseksi.
2 Keksinnön kohteena on aikaansaada menetelmä rokotteen valmistamiseksi raskauden estämiseksi, joka rokote aikaansaa vasta-aineita, jotka mandollisimman vähän reagoivat muiden sisäsyntyisten hormoonien kanssa fysiologisissa pitoisuuksissa. Nyt on todettu, että aikaansaadaan rokote raskauden estämiseksi muodostamalle yhteensopivan immunogeenisen kantajan ja HCG:n (ihmissikiönsuonikalvo-gonadotropiini) /g-alayksikön reaktiotuotteesta valmista, joka on vapaa tekijöistä, jotka voivat reagoida voi- makkaasti anti-lh-seerumien kanssa (LH lutenisoiva hormooni). Keksinnön mukaisesti valmistetaan rokotteita raskauden estämiseksi siten, että (a) HCG:n -alayksikkö puhdistetaan kemiallisesti, (b) mainittu kemiallisesti puhdas /g-alayksikkö puhdistetaan immunokemiallisesti valmisteen vapauttamiseksi tekijöistä, jotka voivat reagoida voimakkaasti anti-lutenisoivahormooni(lh)-seerumin kanssa, (c) kemiallisesti ja immunokemiallisesti puhdistettu -alayksikkö kondensoidaan jäykkäkouristustoksoidi-kantajan kanssa, (d) saadusta konjugaatista valmistetaan rokote käyttäen sinänsä tunnettuja lisäaineita. Sanonta immunokemiallisesti puhdistettu tarkoittaa käsittelyä, joka poistaa /3 -alayksikkö-valmisteesta komponentit, jotka ollessaan läsnä voisivat aiheuttaa vasta-aineiden muodostumista, jotka voisivat reagoida sisäsyntyisen LH:n kanssa. Keksinnön mukainen rokote on olennaisesti vapaa reaktiosta muiden sisäsyntyisten hormoonien kanssa, kuten aivolisäkesyntyisten hormoonien kanssa, jotka ovat tarpeellisia lisääntymistä välittävien elimien normaalia toimintaa varten. Keksinnön edullisen suoritusmuodon mukaan 73 -alayksikkö eroitetaan ihmis-sikiönsuonikalvo-gonadotropiinin (,-alayksiköstä tunnettujen menetelmien mukaan ja sen jälkeen kemiallisesti puhdistetaan tunnetulla tavalla ja sitten puhdistetaan immunokemiallisesti käyttämällä vieraslajista anti-lh-immunosorbenttia. Rokote on edullisessa muodossaan ihmis-sikiönsuonikalvo-gonadotropiinin /3 -alayksikön kemiallisesti ja immunokemiallisesti puhdistetun muodon ja jäykkäkouristus-toksoidin reaktiotuote moolisuhteen ollessa alueella noin 1:5...1:2. Reaktio tapahtuu kondensoimisaineen kuten glutaraldehydin tai etyyliaminopropyylikarbodi-imidin läsnäollessa, jolloin saadaan kovalenttisesti sitoutunut konjugaatti. Reaktiotuote saatetaan senjälkeen tavanomaiseen dialysoimiseen, steriliteetti-kontrolliin ja saostukseen rokotteen muodostamiseksi.
3 Kuten tunnettua on istukka kudos, joka kehittyy ainoastaan raskauden yhteydessä; se ei ole ei-raskaan naisen normaaliosa. Keksinnön mukaisesti valmistettu rokote voi vaikuttaa raskauden syntymistä ja ylläpysymistä vastaan. Esine. ihmisissä kriitillistä hormoonia, ihmissikiönsuonikalvo-gonadotropiinia muodostuu istukan suonikalvoissa noin 8. päivänä hedelmöittymisen jälkeen. Tämä hormooni ylläpitää tässä vaiheessa keltarauhasen toimintaa ja varmistaa kohdun vastaanottavuuden. Hormooni voi myös suojella rakkula-alkiota muulla tavoin. Sen neutraloituminen johtaa kuukautisten alkamiseen siten estäen raskauden pysymisen. Ihmis-sikiönsuonikalvo-gonadotropiini (nimitetään myöhemmin lyhennyksellä HCG) on glyko-proteiini.hormooni, koostuen' kandesta alayksiköstä: alfasta ja beetasta. Alfa-alayksikkö on melkein identtinen sellaisten hormoonien kuin kilpirauhesta stimuloivan hormoonin (TSH), munarakkulaa stimuloivan hormoonin (FSH) ja lutenisoivan hormoonin (LH) vastaavien alfa-alayksiköiden kanssa. Hormoonin beta-alayksikkö kussakin tapauksessa määrää hormoonin spesifisyyden. Ihmis-sikiönsuonikalvo-gonadotropiinin /3 -alayksikkö on aminohappojen polypeptidi, jossa kolme viidestä hiilihydraattitähteestä on C-ketjun päässä. Osassa /3-alayksikköä on LH:n /3 -alayksikön aminohappo-homologeja. Dissosioimalla erittäin puhdasta HCG: tä saadaan /5-HCG, joka osoittaa melkoista mikroheterogenisyyttä jakautumalla elektroforeesissa 8 nauhaan käytettäessä analyyttisiä polyakryyliamidi-geelejä. Tämä mikroheterogeenisuus todetaan kaupallisesti saatavissa HCG:ssä, joka valmistetaan raskausajan virtsasta. Mikroheterogenisuus voi johtua molekyylin lohkeamisen ja/tai modifioitumisen vaihtelevasta asteesta molekyylin kulkiessa erilaisten kudoksien lävitse. HCG kokonaismolekyylinä tai HCG:n (3-alayksikkö injektoituna naiseen ei aiheuta vasta-aineiden muodostumista, jotka voivat neutraloida HCG:n aktiivisuuden. Se voidaan kuitenkin tehdä antigeeniseksi yhdistämällä se voimakkaasti antigeenisten hapteenien kanssa. Diatsotoituja sulfaniliinihappo-johdannaisia on tutkittu tässä tarkoituksessa ja tällöin on todettu, että anti-hcg-vasta-aineita muodostuu vaihdevuodet sivuuttaneissa naisissa. Tämä on kuvattu Stevens'in suomalaisessa hakemuksessa no 1383/74 ja hänen tieteellisessä kirjoituksessaan: " Effects of Immunization with Hapten-Coupled HCG on the Human Menstrual Cycle", Obstetrics and Gynecology, Vol. 42, No. 4, lokakuu Kuitenkin tutkituissa tapauksissa esiintyi keskijakso- LH-huippujen alenemista tai häviämistä, minkä mukaan tutkijat katso-
4 vat, että vasta-aineet ovat reagoineet ristiin in vivo sisäsyntyisen LH:n kanssa. Sellainen reaktio aivolisäkesyntyisen hormoonin kanssa, jota vaaditaan lisääntymistä välittävien elimien normaalia toimintaa varten, ei ole haluttu ja on mandollisesti vaarallinen. Verrattuna edellä mainittuun Stevens'in suomalaiseen hakemukseen koskee esillä oleva keksintö erilaista menetelmää, valmistettu tuote on erilainen ja sillä on erilaiset biologiset ominaisuudet. Keksinnön mukaisesti annetaan HCG:n kemiallisesti ja immunokemiallisesti puhdistetun, -alayksikön reagoida immunogeenisen kantajan jäykkäkouristustoksoidin kanssa. Sensijaan Stevens'in mukaan HCG tai sen /5-alayksikkö modifioidaan hapteenilla kuten sulfaniilihapolla. Saadun tuotteen kokonaisrakenne on tärkeä ja niinpä modifiointi Stevens'in mukaan aikaansaa molekyyliin täysin erilaisia ominaisuuksia. Toisaalta esillä olevan keksinnön mukaisesti immunogeeniset ominaisuudet ovat johdettavissa kokonaisrakenteesta eikä yksistään HCG:n /3-alayksiköstä. Keksinnön mukaisesti HCG:n -alayksikkö puhdistetaan ei vain kemiallisesti vaan myös immunokemiallisesti. Tällä tekniikalla poistetaan jäljet HCG-kokonaismolekyylistä ja sen oe-alayksiköstä, jotka rokotteessa voivat johtaa vasta-aineen muodostukseen muita hormooneja kuten LH:ta vastaan. Lisäpuhdistuksella poistetaan rokotteen synnyttämien vasta-aineiden ristiinreaktio muiden hormoonien kuin HCG:n kanssa. Eroavaisuudet oheisen keksinnön mukaisen tuotteen ja Stevens'in valmistavan tuotteen ominaisuuksissa ja biologisessa käytössä ovat o- lennaisia. Stevens'in mukaan valmistetun tuotteen annosmäärät vastaaineiden synnyttämiseksi ovat paljon suurempia kuin keksinnön mukaisesti valmistetulla tuotteella. Viimeksimainitun yhteydessä tyypilliset annosyksiköt anti-hcg-vasta-aineiden synnyttämiseksi ihmisessa ovat alle 1 /ug (Contraception, 13(2), 237, 1976), kun taas Stevens'in mukaan annostellaan rokotettaessa neljä injektiota 1 mg annosyksiköitä. Keksinnön mukaisesti valmistettu rokote eroaa selvästi (mikä myös on tärkeintä) biologisilta ominaisuuksiltaan Stevens'in rokotteesta. Ensiksi mainittu on hyvin immunogeenisen ja reaktiota ristiin ei tapandu LH:n ja muiden hormoonien kanssa, kun taas Stevens'in rokote on vain vähän immunogeeninen ja voidaan todeta reaktiota ristiin LH:n ja muiden hormoonien kanssa. Muista eroavaisuuksista voidaan mainita, että Stevens'in rokote aiheuttaa paikallista reaktiota injektiokohdassa tai muuta sivu-
5 54997 _ vaikutusta (kuumetta), kun taas keksinnön mukaisesti valmistetulla rokotteella ei ole mitään sivuvaikutuksia. Lisäksi keksinnön mukaisesti valmistettu rokote aikaansaa pienemmillä annoksina lyhyemmässä ajassa vasta-aineen muodostusta kuin Stevensin rokote. Keksinnön mukaisesti on tärkeätä, että reaktioseoksessa käytetty HCG:n /3-alayksikkö on hyvin puhdistettu sekä kemiallisesti että immunokemiallisesti. /T-alayksikön kemiallinen puhdistaminen voidaan suorittaa millä sinänsä tunnetulla tavalla tahansa, kuten menetelmällä, jonka ovat kuvanneet Morgan, F.J. ja R.E. Canfield: Endocrinology 88, 145, 1974 ja F.J. Morgan, R.E. Canfield, J.K. Vaitukaitis ja G.T. Ross: Endocrinology 24 1 sivut , Toisen sopivan menetelmän HCG:n kemiallisesti puhtaan /5 -alayksikön saamiseksi ovat kuvanneet Swaminathan, N. ja Bahi,.P.: "Dissosiation and Recombination of Subunits of Human Chorionic Gonadotropin", Biochem. Biophys. Res. Commun., Vol. 4, sivu 422, (197). Kuitenkaan nämä kemialliset puhdistusmenetelmät eivät ole riittäviä tekijöiden poistamiseksi, jotka voivat reagoida suurella tehokkuudella anti-lh-seerumin kanssa. Immunokemiallisen puhdistusvaiheen mukaisesti HCG:n kemiallisesti puhdistettu /5-alayksikkö liuotetaan fysiologiseen liuottimeen, kuten fosfaatilla puskuroituun suolaliuokseen ja liuosta sekoitetaan huoneenlämpötilassa valvotun ajan immunologisen sorbentin, kuten kaniinin anti-lammas-lh:n kanssa. Käsittely vieraslajisella anti-lhimmuno-sorbentilla huolellisesti valvotuissa olosuhteissa poistaa sellaiset osat valmisteesta, joissa on tekijöitä, jotka voivat reagoida voimakkaasti anti-lh-seerumin kanssa. Keksinnön mukaisessa menetelmässä käytetty immunosorbentti voi olla mikä tahansa vieraslajinen LH-antiseerumi, kuten kaniinin anti-lammas-lh, apinan anti-lammastai anti-nauta-lh. Sekoittaminen suoritetaan lämpötilassa esim. 25 C:ssa minuuttia tai kauemmin riippuen lämpötilasta, HCG:n alayksikön panoksen luonteesta ja käytetyn immunosorbentin voimakkuudesta. Optimiolosuhteet voidaan määrätä kunkin 73 -alayksikkövalmisteen näytteen mukaan ja kunkin immunosorbentin mukaan.sen jälkeen valmiste saatetaan sentrifugoimisvaiheeseen; sakka hylätään. Suodos sisältää kemiallisesti ja immunokemiallisesti puhdistettua HCG:ng - alayksikköä. Edellä käytetty sanonta "voimakkaasti anti-lh-seerumin kanssa reagoiva" tarkoittaa sellaisten yksiköiden reaktiokykyä, jotka yhdistyvät anti-lh-seerumin kanssa hyvin nopeasti käytetyssä lämpötilassa. Anti-LH-seerumi tätä tarkoitusta varten on edullisesti vieraslajinen LH.
6 HCG:n /3-alayksikön valmiste, joka on vapaa tekijöistä, jotka voivat reagoida voimakkaasti anti-lh-seerumin kanssa, saatetaan sen jälkeen reagoimaan yhteensopivan, immunogeenisen kantajan, nimittäin jäykkäkouristus-toksoidin kanssa halutuissa suhteissa käyttämällä kondensoimisainetta, joka konjugoi /g-alayksikön kantajan kanssa. Keksinnön edullisen suoritusmuodon mukaisesti reaktiotuote on jäykkäkouristus-toksoidin ja HCG:n kemiallisesti ja immunokemiallisesti puhdistetun /3-alayksikön kompleksi-polymeeri, joka on konjugoitu kovalenttisesti moolisuhteessa noin 1:5...1:2 kondensoimistai kytkemisaineen, kuten glutaraldehydin tai 1-etyyli-3-(3-dimetyyliaminopropyyli)-karbodi-imidin läsnäollessa. Kun kondensoimisaineena on 1-etyyli-3-(3-dimetyyli-aminopropyyli)-karbodi-imidi sekoitetaan puhdistettu jäykkäkouristus-toksoidi ja HCG:n 4 -alayksikkö edellä esitetyssä moolisuhteessa yhdessä kondensoimisaineen kanssa ja seosta pidetään sen jälkeen lämpötilassa korkeintaan 25 C korkeintaan 6 tunnin ajan lämpötilasta riippuen. On edullista, että reaktio suoritetaan lämpötilassa korkeintaan 1 C ja aikana tuntia. Kun kondensoimisaineena on glutaraldehydi, puhdistettu jäykkäkouristus-toksoidi ja HCG:n -alayksikkö sekoitetaan halutussa moolisuhteessa kondensoimisaineen kanssa ja sen jälkeen seosta pidetään lämpötilassa korkeintaan 37 C korkeintaan 6 tuntia. Edullisesti tämä vaihe suoritetaan lämpötilassa noin C ja aikana tuntia. Sen jälkeen saatu yhdiste dialysoidaan hyvin fosfaatilla puskuroitua suolaliuosta, ph 7,2,,5 N vastaan kylmässä, esim. 5 C:ssa ja otetaan talteen steriiliin putkeen käyttämällä membraanisuodatinta ja ruiskulaitteeseen käyttämällä suolaliuosta siirtoa varten. Sen jälkeen valmiste saatetaan steriliteettitutkimukseen sinänsä tunnetulla tavalla mikro-organismien poissaolon varmistamiseksi. Steriloimisvaiheen jälkeen valmiste saostetaan alunalle käyttäen steriilejä kalialuna-zå1k (SO4 ) 2. 12H27 ja steriilejä natriumkarbonaattiliuoksia. Alunan asemesta voidaan käyttää mitä tahansa muuta sopivaa lisäainetta. Kuitenkin on todettu, että saostaminen alunalle suojaa aktiivista ainetta adsorboitumasta lasisäiliöihin ja myös aikaansaa pidemmän kestoajan. Rokotetta käytetään edullisesti emulsiona kasviöljyjen kanssa injektiota varten ja tämä edelleen parantaa antigeenisuutta. Keksinnön muut kohteet ja edut ilmenevät seuraavista esimerkeistä, joissa on kuvattu rokotteen valmistus ja käyttö.
7 ESIMERKKI 1 Rokote raskauden estämiseksi valmistettiin seuraavalla menetelmällä: A. HCG:n -alayksikön kemiallinen puhdistaminen Puhdistettu HCG valmistettiin raa'asta HCG:stä menetelmällä, jonka on kuvannut Canfield et al: Recent Progr. Horm. Res. El; 124, Sitä viljeltiin 4 C:ssa 1 tunti juuri valmistetun 81"1 virtsaaineliuoksen kanssa, joka oli puhdistettu käyttäen seka-ioninvaihtohartsipylvästä, erikoisesti kerrosta, jolla oli yhtäsuuret määrät Dowex-1 X-8 ja Dowex-5 X-4 meshin ollessa 2. Pylvään koko oli 2 x 4 cm. Virtsa-aineen läsnäollessa /5-alayksiköt dissosioituivat ja senjälkeen ne erotettiin menetelmällä, jonka on kuvanneet Morgan ja Canfield: Endocrinology 88, 145, Tämän menetelmän mukaisesti seos johdettiin toistuvasti ioninvaihtokolonnin lävitse ja Sephadexkolonnien lävitse dissosioituneen (5-alayksikön saamiseksi, jossa oli mandollisimman vähän HCG:n kokonaismolekyyliä tai sen oc-alayksikköä. B. HCG:n rs -alayksikön immunokemiallinen puhdistaminen Vaiheessa A valmistetusta HCG:n /3-alayksiköstä otettiin 1 ug:n näytteitä määrältään 5 kappaletta ja kukin liuotettiin,1 ml:aan 1 mm natriumfosfaatilla (NaH 2PO4 ja Na 2HPO4 ) puskuroitua suolaliuosta (,85 % NaC1) (ph 7,2), mistä liuoksesta käytetään myöhemmin lyhennystä PBS-liuos. Jokaista näytettä sekoitettiin huoneenlämpötilassa (25 C) kaniinin anti-lammas-lh:n immunosorbentin kanssa, joka oli valmistettu kohdassa C kuvatulla tavalla. Sekoitusajat olivat 1, 5, 1, 2 ja 3 minuuttia. Sekoittamisen jälkeen putkia sentrifugoitiin 1 minuuttia...4 C:ssa. Jokaisen putken pinnalla olevaa nestettä tutkittiin sen reaktiokyvyn määräämiseksi anti-hcg:ta ja anti-lh:ta vastaan. Tämän kokeen avulla todettiin, että tarkoituksenmukaiset olosuhteet kohdassa A valmistetun HCG:n, -alayksikön koko panoksen puhdistamiseksi vastasivat sekoitusaikaa 3 minuuttia 25 C:ssa. Sekoitusaika 3 minuuttia perustui siihen havaintoon, että tällöin näytteen pinnalla olevalla nesteellä oli mandollisimman pieni reaktiokyky LH:n kanssa. Kohdassa A valmistetun HCG:n puhdistetun /3 -alayksikön - HCG:n ominaisuuksia verrattiin immunokemiallisesti puhdistetun alayksikkö-valmisteen kanssa, joka oli valmistettu kohdan B mukaisesti. Piirustusten kuviot 1 ja 2 osoittavat vastaavien valmisteiden
8 reaktiokyvyn anti-hcg:n ja anti-lh-seerumin kanssa ennen (kuvio 1) ja immunosorbtio-puhdistusvaiheen jälkeen (kuvio 2). Absorptiovaihe parantaa myös valmisteen mikro-heterogeenisuutta. Viitaten kuvioihin 1 ja 2 /3 -HCG-valmisteet saatettiin elektroforeesiin 7,5 %:ssa analyyttisissä polyakryyli-amidi-geeleissä ph-arvossa 9,. Sarjasta geelejä suoritettiin densitometriset mittaukset ja toinen identtinen sarja leikattiin pituussuuntaa vastaan kohtisuoraan noin 2,5 mm paksuiksi segmenteiksi. Proteiinit kustakin segmentistä eluoitiin,9 %:seen natriumkloridiliuokseen. Sekä kuviossa 1 että kuviossa 2 käyrä ) kuvaa proteiineja mitattuna densitometrisesti; käyrä ( ) kuvaa proteiineja, jotka kilpailevat /3-HCG 1251 kanssa anti- /3-HCG-seerumin sitomiseksi; ja käyrä kuvaa proteiineja, jotka kilpailevat HLH 1251 kanssa anti-hlh-seerumin sitomiseksi. Todetaan, että immunokemiallisesti puhdistetulla valmisteella on olennaisesti pienempi reaktiokyky anti-hlh-seerumin kanssa. Voidaan todeta, että sekoittamisen ja lämpötilan optimiolosuhteet määräytyvät -alayksikön käytetyn panoksen luonteesta ja käytetyn immunosorbentin voimakkuudesta. Voitiin todeta, että viimeksimainittu vaihtelee käytetyn antiseerumin tiitterien mukaan ja immunosorbentin varastointiajan mukaan. C. Iamunosorbentin valmistus 1 ml antiseerumia (kaniinin anti-lammas-lh), joka oli saatu käsittelemällä kaniinia lammas-lh:11a, dialysoitiin PBS:ää vastaan...4 C:ssa ja ph säädettiin arvoon 5 1M natriumasetaatti-puskurilla. Lisättiin varovaisesti samalla sekoittaen 3 ml glutaraldehydin 2,5 %:sta vesiliuosta. Reaktioseoksen annettiin seistä huoneenlämpötilassa (25 C) 3 tuntia. Polymeroitu aine homogenoitiin Potter ElveJhem-homogenisoimislaitteessa, jossa oli Teflon-sekoitin. Se pestiin toistuvasti PBS-liuoksella siihen saakka kunnes se oli vapaa 28 m/u absorboivasta aineesta (ei-polymeroitunut vapaa proteiini). Senjälkeen se pestiin 2 mm glysiini-hc1-puskurilla ph 2,2 ja neutraloitiin 2M K 2 HPO 4 -liuoksella ja lopuksi tasapainoitettiin PBS:llä. Immunosorbenttia varastoitiin 4 C:ssa käyttäen,1 %:sta Na-atsidia säilöntäaineena glysiini-hc1-puskurissa. D 1 Rokotteen valmistus käyttämällä 1-etyyli-3-(3-dimetyyliaminopropyyli)-karbodi-imidiä kondensoimisaineena Valmistus (4 annosta varten) 3,2 mg kohdan B mukaan valmistettua HCG:n /3 -alayksikköä sekoitettiin 4 Lf:n kanssa jäykkäkouristus-toksoidia (15 Lf/mg pro-
9 54997 teiinia N) ja 16 mg:n kanssa l-etyyli-3-(3-dimetyyliaminopropyyli)- karboni-imidiä 6,5 mi:ssa PBS-liuosta ja liuosta pidettiin 1 C:ssa 5 tuntia välillä ravistellen. Jäykkäkouristus-toksoidin moolisuhde HCG:n -alayksikköön oli noin 1:1. Reaktiotuote dialysoitiin fosfaattipuskurisuolaliuosta vastaan ph-arvossa 7,2,,5 M kylmässä. Tuote otettiin talteen steriiliin putkeen käyttäen membraanisuodatinta ja ruiskulaitetta ja käyttäen suolaliuosta siirtoa varten. Tuotteen steriilisyyttä tutkittiin tioglykolaatti-väliaineessa 7 päivää. Sen jälkeen se adsorboitiin aluminiumhydroksidille käyttäen steriiliä 1 %:sta kalialuna-ja 1 %:sta natriumkarbonaatti-liuosta. Sen jälkeen rokote jaettiin ampulleihin ja otettiin näytteitä pyrolyysi- ja steriliteetti-tutkimuksia varten. D 2 Rokotteen valmistaminen käyttäen glutaraldehydiä kondensoimisaineena - Yhden annoksen valmistus 8 /ug kohdan B mukaan valmistettua HCG:n -alayksikköä sekoitettiin 1 annoksen kanssa jäykkäkouristus-toksoidia (1 Lf-yksikköä) ja 5 /u1:n kanssa 1 %:sta glutaraldehydivesiliuosta. Seosta pidettiin 3 C:ssa välillä sekoittaen 3 tuntia ja senjälkeen dialysoitiin PBS:ää, ph 7,2,5 Ni vastaan. Sen jälkeen meneteltiin e- delleen samalla tavalla kuin mitä on kuvattu valmistuksessa D 1. Ominaisuudet: Kohdan D 1 mukaan valmistettu rokote, jota seuraavassa nimitetään /3-HCG-TT:ksi, aiheutti immuniteettia hiiressä, kaniinissa, vuohessa, apinoissa samoin kuin naispuolisissa ihmisissä. Kohdassa D 2 kuvatulla rokotteella todettiin olevan samankaltaiset immunogeeniset ominaisuudet apinoissa. Molemmilla vasta-ainereaktio kesti erittäin kauan. Yksinkertainen ruiske rokotetta D 1 annettuna Freund'in lisäaineen kanssa useihin kohtiin vuohta aikaansai vasta-aineen suurenevat pitoisuudet noin 9 kuukauden aikana, minkä jälkeen saavutettiin ylätaso. Sen jälkeen seurasi aleneva suuntaus. Toinen lisäruiske a- lenevassa faasissa johti vasta-aineen pitoisuuksien jyrkkään nousuun. Tämä on esitetty kuviossa 3. Reaktiotulokset 1 kokeessa käyttäen reesusapinaa koe-eläimenä todettiin olevan samankaltaisia, vaikkakin esiintyi yksilöllisiä vaihteluita. Tämä on myös esitetty kuviossa 3.
10 Tutkittaessa anti-seerumin (beta-hcg-tt) immunologisia ominaisuuksia todettiin, että vuohessa tai apinassa kehitetty seerumi reagoi immunologisesti kokonaisten HCG-molekyylien kanssa. Anti-seerumi ei reagoinut ihmisen kasvuhormoonin (HCG), ihmisen prolaktiinin ja ihmisen istukka-laktogeenin (HPL), FSH, TSH tai LH kanssa kun niitä tutkittiin fysiologisina pitoisuuksina. Taulukko I kuvaa tuloksia.
11 TAULUKKO I Anti /3-HCG-T.T.-seerumin spesifisyys apinassa ja vuohessa Hormooni Väkevyys % sidottu vasta-aineeseen Apina (1:5) Vuohi (1:4) Täydellisyys-% Apina Vuohi Suurin väkevyys kilpailun esiintyessä /5-HCG HCG HLH EFSH ETSII HPL HGH 1 ng ng ng ng ng xx ng.4 ngx ngxx ng.3 ngx ngxx 1 1»1 ng 12.5 ngxx 1 1 >>1 ug.25 ngxx 1 1 >>1 ug _. x xx Perus- tai lisäväkevyys Suurin fysiologinen väkevyys
12 Anti-seerumin (beta-hcg-tt) biologisia ominaisuuksia vuohessa ja apinoissa ja seerumin kykyä neutraloida HCG:tä tutkittiin useilla järjestelmillä. Sen todettiin estävän tehokkaasti HCG:llä aikaansaatua vatsanpuoleisten eturauhasten painon kasvua rotissa, jotka eivät olleet sukukypsiä. Tästä työstä saadut koetulokset on esitetty yhteenvetona kuviossa 4. Se esti myös in vitro HCG:llä aikaansaatua progesteronin muodostumisen kasvua keltarauhasessa. Tulokset on esitetty taulukossa II. TAULUKKO II Anti /5 -HCG-TT vaikutus keltarauhasen progesteronisynteesiin Lisäykset 1. Ei 2. + HCG (.1 ug/ml) 3. + HCG + anti -TT 4. + anti -TT P4ug/g kudostax ± X Keskiarvo + S.E. 6 kokeesta Anti-seerumi esti myös HCG:n sitoutumisen reseptoreihin membraanivalmisteissa, jotka on tehty kiveksistä ja munasarjoista. Tätä osoittavat koetulokset on esitetty yhteenvetona kuvioss 5. Kaikki nämä kokeet osoittavat, että yhdiste beta-hcg-tt:tä vastaan muodostuneilla vasta-aineilla ei ole ainoastaan kyky reagoida immunologisesti kokonaisten HCG-molekyylien kanssa, vaan ne myös neutraloivat niiden biologisen aktiviteetin. (beta-hcg-tt)-rokotevalmistetta D 1 tutkittiin brittiläisen farmakopean vaatimusten mukaisesti ja todettiin, ettei se aiheuttanut yhtään kuolemaa mersuissa 4 viikon tutkimusaikana. Siltä puuttui myöskin akuuttinen ja subakuuttinen myrkyllisyys tutkittuna kandella lajilla, nimittäin jyrsijöillä ja apinalla. Sen siedettävyyttä tutkittiin myös 65 hiirellä, 7 kaniinilla ja 13 apinalla aikana, joka ulottui yhteen vuoteen ja vielä pidemmäksi ajaksi. Immunoitujen eläinten eloonjääminen oli 1 %. Muut parametrit kuten hematologia Lfiemoglobiini, leukosyyttien kokonaislaskenta ja leukosyyttien erottelulaskenta (TLC/DLC), sullottu solutilavuus (PCV), verihiutaleiden ja retikulosyyttien pintasivelytutkimus7, maksatoiminnat (seerumi-bilirubiini, alkaalinen fosfataasi, transaminaasit GOT ja GPT, LDH-isoent- '.r
13 syymit, koliiniesteraasi), munuaistoimintakokeet, veren glukoosi, seerumin lipidit, kolesteroli, triglyseridit, vapaat rasvahapot ja kilpirauhasen toiminta olivat normaaleja immunoiduissa apinoissa. Immunoidut apinat eivät kehittäneet välitöntä (Arthus) tai myöhäisempää yliherkkyyttä HCG:hen nähden. Kliiniset tutkimukset: 6 naispuolista vapaehtoista, jotka olivat 2-32 vuotta vanhoja, injektoitiin joko rokotevalmisteella, joka oli tehty kohdan D l mukaan, tai he saivat tehottomia ruiskeita sokeakokeina. Koska näiden kokeiden tarkoituksena oli määritellä keksinnön mukaisesti valmistetun rokotteen immunogeenisyys,oli kokeeseen valituille naisille aikaisemmin suoritettu munajohtimen sidonta. Tehottomat ruiskeet eivät antaneet missään kokeessa reagointia. Kolmessa koehenkilössä, jotka saivat rokotetta, muodostui vasta-ainetta, joka reagoi sekä jäykkäkouristus-toksoidia että HCG:tä vastaan. Hitaan alkuvaiheen jälkeen, jota kesti 4-6 viikkoa vaihdellen koehenkilöstä koehenkilöön, seurasi vasta-aineen tiitterien progressiivinen kasvu. Vasta-aineita muodostui samanaikaisesti myös jäykkäkouristusta vastaan. Kuviot 6, 7 ja 8 kuvaavat kolmen vapaehtoisen naisen, jotka saivat rokotetta, reagointia. Rouva K. V., kuvio 8, oli 3 vuotta vanha 5 raskautta takanapäin ja hänellä oli 4 elävää lasta. HCG:tä vastaan reagoivien vasta-aineiden kasvua esittää käyrä (o o) ja anti-jäykkäkouristus-vasta-ainetta käyrä Anti- HOG-tiitterit saavuttivat ylätason ja pysyivät tässä tasossa noin 9 kuukautta injektion jälkeen. Kokeita jatkettiin. Kuukautispäivä merkittiin X merkillä kuvion yläosaan. Koehenkilöllä oli ollut säännölliset kuukautiset. Kohdun limakalvon koepalan tarkastus, joka otettiin 15 päivänä, osoitti munasolun irtoamisen, mikä vahvistettiin emättimen soluopin ja progesteroni-pitoisuuksien avulla jakson eritysfaasissa. Toinen koehenkilö rouva A. M., kuvio 7, oli 32 vuotta vanha, 3 raskautta ja 2 elävää lasta. Kuvio 7 osoittaa samankaltaista immunoreaktiota kuin rouva A. M. yhteydessä. Kohdun limakalvon koepalan tarkastus samoin kuin emättimen soluoppi ja progesteroni-pitoisuudet osoittivat hänenkin tapauksessaan munasolun irtoamista. Kolmas koehenkilö rouva N. D. (kuvio 6) oli 3 vuotta vanha, 5 raskautta ja 3 elävää lasta. Rouva N. D. oli syöttänyt lasta noin 5 ensimmäisen päivän aikana tutkimuksessa, mikä osoittaa kuukautisten puuttuminen tänä aikana. Immunoiminen rokotevalmisteella ei ai
14 kaansaanut mitään häiriötä maidon erityksessä huolimatta erittäin hyvästä immuno-reagoimisesta. Siten hänellä olivat alkaneet kuukautiset ja hänellä oli ollut normaalit kuukautisvälit. Libido ja muu suvunjatkamiseen liittyvä, toiminta oli kaikilla kolmella koehenkilöllä täydellisen normaaleja. Kliininen tutkimus ei osoittanut mitään epänormaalisuutta missään suhteessa. Muut parametrit kuten hematologia (hemoglobiini, TLC/DLC, PCV, verihiutaleiden ja retikulosyyttien pintasivelytutkimus), maksatoiminnat (seerumibilirubiini, alkaalinen fosfataasi, transaminaasit GOT ja GPT, LDHisoentsyymit, koliiniesteraasi), munuaistoimintakokeet, veren glukoosi, seerumin lipoidit, kolesteroli, triglyseridit, vapaat rasvahapot ja kilpirauhasen toiminta olivat normaaleja ja immunoiminen ei ollut aikaansaanut mitään muutosta elinten toiminnoissa ja aineenvaihdunnassa. Koehenkilöt osoittivat myös normaalia reagointia insuliiniverensokeriniukkuuskokeessa, jossa muodostui kortisolia ja kasvuhormonia. Näiden immunoitujen naisten seerumi samoin kuin apinoiden ja vuohien, jotka oli immunoitu beta-hcg-tt-valmisteella, seerumit tutkittiin erilaisilla kokeilla mandollisten autoimmunoreaktioiden poissulkemiseksi ruumiin elimiä vastaan. Ne todettiin negatiivisiksi antituma-vasta-aineiden ja antimikrosomi-vasta-aineiden suhteen ja niiltä puuttui reumafaktorireaktiokyky. Tämä on esitetty yhteenvetona taulukossa II.
15 TAULUKKO II Immunopatologiatutkimukset immunoiduilla koehenkilöillä Koehenkilön verihaara Tutkimukset Havainnot N.D. 3 kuv N.D N.D A.M. 32 kuv K.W. 3 kuv K.W Ei-immunoitu kontrolli 1. Antituma-vastaaineet 2. Antimikrosomi-vastaaineet 3. Lateksi-agglutanaatio reumafaktorille Mitään reaktiota ei todettu millään tutkituista veriheroista
16 Ne todettiin myös negatiivisiksi reaktiokyvyltään ihmisen kilpirauhasta, lisäkilpirauhasta, lisämunuaisia, munuaisia, kiveksiä ja munasarjoja vastaan. Nämä tiedot on esitetty yhteenvetona taulukossa
17 TAULUKKO III Anti- / 5 -TT-seerumin reaktiokyky ihmisen elimiä vastaan Verihera Tutkitut elimet Havainnot Normaali naispuolinen ihminen Kiplirauhanen Mitään immunofluoresenssilla havaittavaa Immunoitu ihminen Lisäkilpirauhanen reaktiota ei todettu (N.D.) Kuv. 6 Lisämunuaisen millään seerumeista Normaali apina Munuainen Immunoitu apina Kivekset Munaserja
18 Ne olivat myöskin negatiivisia reaktiokyvyltään hiirestä, kaniinista ja paviaaniapinasta otettuja kudossubstraatteja vastaan, kuten on esitetty yhteenvetona taulukossa IV.
19 TAULUKKO IV Anti- /5 -HCG-TT-seerumin reaktiokyky eri lajeista otettujen kudossubstraattien kanssa Tutkittu verhera Kudossubstraatit Suoritetut kokeet Havainnot Normaali ihminen Hiiri a) Epäsuora immuno- 1) Ei todettu kufluoresenssi dosten kanssa reagoivia vast-aineita Immunoitu nainen Kaniini b) Anti-IINA-vasta- 2) Ei todettu Pavianiapina aineet anti-dna-vastaaineita Normaali apina Immunoitu apina
20 Vapaaehtoisissa koeihmisissä muodostuneiden vasta-aineiden todettiin olevan tehokkaita kokonaisen HCG-molekyylin biologisen aktiviteetin neutraloimiseksi. Kuvio 9 osoittaa näiden vasta-aineiden kyvyn koehenkilössä rouva N. D. estää HCG:n sitoutuminen keltarauhasvalmis teisiin radioreseptori-kokeessa. Näiden vasta-aineiden kyky sitoutua HCG:n kanssa in vivo osoittaa määräykset, jotka on kuvattu kuviossa 1. HCG:hen kohdistuvan immunoreaktion kokonaisaika ihmisissä, joille on annettu primäärisenä immunoimisena neljä ruisketta rokotetta 14 päivän välein, oletetaan olevan yli 1 vuosi, vaikkakin yksilöllisiä vaihteluita voi esiintyä. Aktiivinen immunointi ei ole aiheuttanut haitallisia sivureaktioita. Koehenkilöillä on ollut normaalit kuukautiskierrot. Heillä on todettu munasolun irtoaminen. Munuaiaen, maksan, aivolisäkkeen, sydänverisuonten, kilpirauhasen ja muiden e- linten toiminnat ovat normaaleja ja häiriintymättömiä.
(B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT. - (51) Kv.lk.4 "-' A 61K 39/12. (24) Alkupäivä Löpdag 01.06.84
 (B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT C (45) PAÖntti Myörinetty Paten't - beviljats - (51) Kv.lk.4 "-' A 61K 39/12 (21) Patenttihakemus Patentansökning 842215 SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus
(B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT C (45) PAÖntti Myörinetty Paten't - beviljats - (51) Kv.lk.4 "-' A 61K 39/12 (21) Patenttihakemus Patentansökning 842215 SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus
[B] 111 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 55 1 9 0. C (45) Patentti cl» -_,'nnetty li 06 1979 Patent medde1.t (51) K~.C1.
![[B] 111 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 55 1 9 0. C (45) Patentti cl» -_,'nnetty li 06 1979 Patent medde1.t (51) K~.C1. [B] 111 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 55 1 9 0. C (45) Patentti cl» -_,'nnetty li 06 1979 Patent medde1.t (51) K~.C1.](/thumbs/26/7417528.jpg) [B] 111 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 55 1 9 0 (45) Patentti cl» -_,'nnetty li 06 1979 Patent medde1.t (51) K~.1. 1 07 D 213/79 SUOMI FINLAND (F I) Patentti- ja rekisterlhallitus Patent- och registerstyrelsen
[B] 111 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 55 1 9 0 (45) Patentti cl» -_,'nnetty li 06 1979 Patent medde1.t (51) K~.1. 1 07 D 213/79 SUOMI FINLAND (F I) Patentti- ja rekisterlhallitus Patent- och registerstyrelsen
Adrenaliini Mistä erittyy? Miten/Mihin vaikuttaa? Muita huomioita?
 Hormonitaulukko Adrenaliini Lisämunuainen Erittyy suorituskykyä vaativissa stressitilanteissa. Vaikuttaa moniin elintoimintoihin fyysistä suorituskykyä lisäten, kuten kiihdyttää sydämen toimintaa, laajentaa
Hormonitaulukko Adrenaliini Lisämunuainen Erittyy suorituskykyä vaativissa stressitilanteissa. Vaikuttaa moniin elintoimintoihin fyysistä suorituskykyä lisäten, kuten kiihdyttää sydämen toimintaa, laajentaa
S UOM 1 FI N LAN D 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 4 5 7 6 6
 S UOM 1 FI N LAN D 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 4 5 7 6 6 Kv. lk./int. Cl. C 12 k 5/00 (5:» Uc./KI. 30 h 6 Patentti myönnetty Patent meddelat 11 IX 1972 Patenttihakemus Patentansökning 547 /6 9
S UOM 1 FI N LAN D 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 4 5 7 6 6 Kv. lk./int. Cl. C 12 k 5/00 (5:» Uc./KI. 30 h 6 Patentti myönnetty Patent meddelat 11 IX 1972 Patenttihakemus Patentansökning 547 /6 9
PAKKAUSSELOSTE. VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa
 PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
PAKKAUSSELOSTE VPRIV 200 yksikköä infuusiokuiva-aine, liuosta varten VPRIV 400 yksikköä infuusiokuiva-aine, liuosta varten velagluseraasi alfa Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat
BI4 IHMISEN BIOLOGIA
 BI4 IHMISEN BIOLOGIA 5 HORMONIT OVAT ELIMISTÖN TOIMINTAA SÄÄTELEVIÄ VIESTIAINEITA Avainsanat aivolisäke hormoni hypotalamus kasvuhormoni kortisoli palautesäätely rasvaliukoinen hormoni reseptori stressi
BI4 IHMISEN BIOLOGIA 5 HORMONIT OVAT ELIMISTÖN TOIMINTAA SÄÄTELEVIÄ VIESTIAINEITA Avainsanat aivolisäke hormoni hypotalamus kasvuhormoni kortisoli palautesäätely rasvaliukoinen hormoni reseptori stressi
GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA. Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva
 GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva Gluteenittomuus Gluteenittomia tuotteita koskevan standardin on asettanut Codex Alimentarius
GLUTEENIANALYTIIKKA KELIAKIAN KANNALTA Viljateknologien Helmikollokvio Hartwall, Lahti 8.2.2008 Päivi Kanerva Gluteenittomuus Gluteenittomia tuotteita koskevan standardin on asettanut Codex Alimentarius
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1/16 1. ELÄINLÄÄKKEEN NIMI Equilis injektioneste, suspensio, hevoselle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Annos (1 ml) sisältää: Vaikuttava(t) aine(et) Hevosen influenssaviruksien
LIITE I VALMISTEYHTEENVETO 1/16 1. ELÄINLÄÄKKEEN NIMI Equilis injektioneste, suspensio, hevoselle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Annos (1 ml) sisältää: Vaikuttava(t) aine(et) Hevosen influenssaviruksien
c) Tasapainota seuraava happamassa liuoksessa tapahtuva hapetus-pelkistysreaktio:
 HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
HTKK, TTY, LTY, OY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 26.05.2004 1. a) Kun natriumfosfaatin (Na 3 PO 4 ) ja kalsiumkloridin (CaCl 2 ) vesiliuokset sekoitetaan keske- nään, muodostuu
Steroidihormonimääritykset lapsettomuuden hoidossa ja diagnostiikassa
 Steroidihormonimääritykset lapsettomuuden hoidossa ja diagnostiikassa Helena Tinkanen LT Synnytys- ja naistentautien ja gynekologisen endokrinologian erikoislääkäri TAYS Raskauden alkamiseen tarvitaan
Steroidihormonimääritykset lapsettomuuden hoidossa ja diagnostiikassa Helena Tinkanen LT Synnytys- ja naistentautien ja gynekologisen endokrinologian erikoislääkäri TAYS Raskauden alkamiseen tarvitaan
Patentti myönnetty' Patent medelat 10 V 191
 3 UO M I-FI N LAN D 11 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 4 3 6 2 5 Kv.11(11M.C1 C 12 k 5/00 UJXL 30 h 6 Patentti myönnetty' Patent medelat 10 V 191 Patenttihakemus Patentansökning 2788/67 Hakemispäivä
3 UO M I-FI N LAN D 11 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFT 4 3 6 2 5 Kv.11(11M.C1 C 12 k 5/00 UJXL 30 h 6 Patentti myönnetty' Patent medelat 10 V 191 Patenttihakemus Patentansökning 2788/67 Hakemispäivä
Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi
 Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
Liite II Euroopan lääkeviraston esittämät muutokset valmisteyhteenvedon ja pakkausselosteen muuttamiseksi Tämä valmisteyhteenveto ja pakkausseloste on laadittu viitemaamenettelyssä. Jäsenvaltioiden toimivaltaiset
Adrenaliini. Mistä erittyy? Miten/Mihin vaikuttaa? Muita huomioita?
 Hormonitaulukko Adrenaliini Lisämunuaisesta kortikotropiinin aktivoimana Parantaa suorituskykyä laajentamalla keuhkoputkea. Kiihdyttää aineenvaihduntaa ja happi kulkee nopeammin. Nostaa verenpainetta Toimii
Hormonitaulukko Adrenaliini Lisämunuaisesta kortikotropiinin aktivoimana Parantaa suorituskykyä laajentamalla keuhkoputkea. Kiihdyttää aineenvaihduntaa ja happi kulkee nopeammin. Nostaa verenpainetta Toimii
Adrenaliini. -lisämunuainen -stressitilanteet. -käytetään lääkkeenä mm. sydänkohtaukset, äkilliset allergiset reaktiot.
 Hormonitaulukko Adrenaliini -lisämunuainen -stressitilanteet -Kohottaa verenpainetta, supistaa pintaverisuonia ja laajentaa lihasten verisuonia. -lisää keuhkojen toimintakapasiteettia. -vaikuttaa sitoutumalla
Hormonitaulukko Adrenaliini -lisämunuainen -stressitilanteet -Kohottaa verenpainetta, supistaa pintaverisuonia ja laajentaa lihasten verisuonia. -lisää keuhkojen toimintakapasiteettia. -vaikuttaa sitoutumalla
Uutta lääkkeistä: Ulipristaali
 Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
Page 1 of 5 JULKAISTU NUMEROSSA 3/2012 UUTTA LÄÄKKEISTÄ Uutta lääkkeistä: Ulipristaali Annikka Kalliokoski Esmya, 5 mg tabletti, PregLem France SAS. Ulipristaaliasetaattia voidaan käyttää kohdun myoomien
b) Laske prosentteina, paljonko sydämen keskimääräinen teho muuttuu suhteessa tilanteeseen ennen saunomista. Käytä laskussa SI-yksiköitä.
 Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Lääketieteellisten alojen valintakokeen 009 esimerkkitehtäviä Tehtävä 4 8 pistettä Aineistossa mainitussa tutkimuksessa mukana olleilla suomalaisilla aikuisilla sydämen keskimääräinen minuuttitilavuus
Istukkagonadotropiini (hcg) - enemmän kuin raskaushormoni. Kristina Hotakainen, LT. Kliinisen kemian yksikkö Helsingin yliopisto ja HUSLAB
 Istukkagonadotropiini (hcg) - enemmän kuin raskaushormoni Kristina Hotakainen, LT. Kliinisen kemian yksikkö Helsingin yliopisto ja HUSLAB Istukkagonadotropiini (Human Chorionic Gonadotropin, hcg) Kuuluu
Istukkagonadotropiini (hcg) - enemmän kuin raskaushormoni Kristina Hotakainen, LT. Kliinisen kemian yksikkö Helsingin yliopisto ja HUSLAB Istukkagonadotropiini (Human Chorionic Gonadotropin, hcg) Kuuluu
Määräys STUK SY/1/ (34)
 Määräys SY/1/2018 4 (34) LIITE 1 Taulukko 1. Vapaarajat ja vapauttamisrajat, joita voidaan soveltaa kiinteiden materiaalien vapauttamiseen määrästä riippumatta. Osa1. Keinotekoiset radionuklidit Radionuklidi
Määräys SY/1/2018 4 (34) LIITE 1 Taulukko 1. Vapaarajat ja vapauttamisrajat, joita voidaan soveltaa kiinteiden materiaalien vapauttamiseen määrästä riippumatta. Osa1. Keinotekoiset radionuklidit Radionuklidi
I1111111 111111111IlIl 11111111111111111111181111111111i
 I1111111 111111111IlIl 11111111111111111111181111111111i F I00008 111111 il I I Ill (B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 91688. L.-*, 1.-Lu-..IC " _ b./ n * I. - A I... I. 1. n!. : :,.:. (17) :-
I1111111 111111111IlIl 11111111111111111111181111111111i F I00008 111111 il I I Ill (B) (11) KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 91688. L.-*, 1.-Lu-..IC " _ b./ n * I. - A I... I. 1. n!. : :,.:. (17) :-
LIUOTTAMISEEN, ANNOSTELUUN JA ANTAMISEEN
 Tärkeää tietoa lääkevalmisteen LIUOTTAMISEEN, ANNOSTELUUN JA ANTAMISEEN VELCADE (bortetsomibi) 3,5 mg injektiopullo ihon alaiseen tai laskimon sisäiseen käyttöön OIKEA LIUOTTAMINEN, KUN VALMISTE ANNETAAN
Tärkeää tietoa lääkevalmisteen LIUOTTAMISEEN, ANNOSTELUUN JA ANTAMISEEN VELCADE (bortetsomibi) 3,5 mg injektiopullo ihon alaiseen tai laskimon sisäiseen käyttöön OIKEA LIUOTTAMINEN, KUN VALMISTE ANNETAAN
LASTEN VIITEARVOISTA. Esa Hämäläinen, oyl, dos HUSLAB Lasten ja Nuorten sairaala
 LASTEN VIITEARVOISTA Esa Hämäläinen, oyl, dos HUSLAB Lasten ja Nuorten sairaala Meites et al. 1989 Soldin et al. 1999 Lapset eivät ole pieniä aikuisia Lapsuuden aikana maksan, munuaisten ja keuhkojen toiminta
LASTEN VIITEARVOISTA Esa Hämäläinen, oyl, dos HUSLAB Lasten ja Nuorten sairaala Meites et al. 1989 Soldin et al. 1999 Lapset eivät ole pieniä aikuisia Lapsuuden aikana maksan, munuaisten ja keuhkojen toiminta
RECEPTAL vet 4 mikrog/ml
 VALMISTEYHTEENVETO 1 ELÄINLÄÄKEVALMISTEEN KAUPPANIMI Receptal vet 4 mikrog/ml 2 VAIKUTTAVAT AINEET JA APUAINEET JA NIIDEN MÄÄRÄT 1 millilitra injektionestettä sisältää: Vaikuttavat aineet: Busereliiniasetaatti
VALMISTEYHTEENVETO 1 ELÄINLÄÄKEVALMISTEEN KAUPPANIMI Receptal vet 4 mikrog/ml 2 VAIKUTTAVAT AINEET JA APUAINEET JA NIIDEN MÄÄRÄT 1 millilitra injektionestettä sisältää: Vaikuttavat aineet: Busereliiniasetaatti
KEMIA HYVÄN VASTAUKSEN PIIRTEET
 BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
BILÄÄKETIETEEN enkilötunnus: - KULUTUSJELMA Sukunimi: 20.5.2015 Etunimet: Nimikirjoitus: KEMIA Kuulustelu klo 9.00-13.00 YVÄN VASTAUKSEN PIIRTEET Tehtävämonisteen tehtäviin vastataan erilliselle vastausmonisteelle.
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Nobivac L4 injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttavat aineet: Inaktivoidut Leptospira
LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Nobivac L4 injektioneste, suspensio koirille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttavat aineet: Inaktivoidut Leptospira
SUOMI-FINLAND 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFt43094
 SUOMI-FINLAND 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFt Kv. lk./int. Cl. C 1 2 k 7/00 Lk./KI. 30 h 6 CO Patentti myönnetty 11 11971 Patent meddetat Patenttihakemus Patentansökning 2099/66 Hakemispkiivä Ansökningsdag
SUOMI-FINLAND 0 KUULUTUSJULKAISU UTLÄGGNINGSSKRIFt Kv. lk./int. Cl. C 1 2 k 7/00 Lk./KI. 30 h 6 CO Patentti myönnetty 11 11971 Patent meddetat Patenttihakemus Patentansökning 2099/66 Hakemispkiivä Ansökningsdag
NIMI: Luokka: c) Atomin varaukseton hiukkanen on nimeltään i) protoni ii) neutroni iii) elektroni
 Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
Peruskoulun kemian valtakunnallinen koe 2010-2011 NIMI: Luokka: 1. Ympyröi oikea vaihtoehto. a) Ruokasuolan kemiallinen kaava on i) CaOH ii) NaCl iii) KCl b) Natriumhydroksidi on i) emäksinen aine, jonka
5 LIUOKSEN PITOISUUS Lisätehtävät
 LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
LIUOKSEN PITOISUUS Lisätehtävät Esimerkki 1. a) 100 ml:ssa suolaista merivettä on keskimäärin 2,7 g NaCl:a. Mikä on meriveden NaCl-pitoisuus ilmoitettuna molaarisuutena? b) Suolaisen meriveden MgCl 2 -pitoisuus
1 Tehtävät. 2 Teoria. rauta(ii)ioneiksi ja rauta(ii)ionien hapettaminen kaliumpermanganaattiliuoksella.
 1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
1 Tehtävät Edellisellä työkerralla oli valmistettu rauta(ii)oksalaattia epäorgaanisen synteesin avulla. Tätä sakkaa tarkasteltiin seuraavalla kerralla. Tällä työ kerralla ensin valmistettiin kaliumpermanganaatti-
Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille
 1. ELÄINLÄÄKKEEN NIMI Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra injektionestettä sisältää: Vaikuttava
1. ELÄINLÄÄKKEEN NIMI Veterelin vet 4 mikrog/ml injektioneste, liuos naudalle, hevoselle, sialle ja kanille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi millilitra injektionestettä sisältää: Vaikuttava
11 11111111 111 11111 11 1110111! 11 11191911 1 11111111 111 111111
 11 11111111 111 11111 11 1110111! 11 11191911 1 11111111 111 111111 (12) PATENTTIJULKAISU PATENTSKRIFT (10) FI 107515B (45) Patentti myönnetty - Patent beviljats 31.08.2001 SUOMI - FINLAND (FI) PATENTTI-
11 11111111 111 11111 11 1110111! 11 11191911 1 11111111 111 111111 (12) PATENTTIJULKAISU PATENTSKRIFT (10) FI 107515B (45) Patentti myönnetty - Patent beviljats 31.08.2001 SUOMI - FINLAND (FI) PATENTTI-
TKK, TTY, LTY, OY, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 31.5.2006
 TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
TKK, TTY, LTY, Y, TY, VY, ÅA / Insinööriosastot Valintakuulustelujen kemian koe 1.5.006 1. Uraanimetallin valmistus puhdistetusta uraanidioksidimalmista koostuu seuraavista reaktiovaiheista: (1) U (s)
Varhainen Raskaustesti Tikku
 FI Varhainen Raskaustesti Tikku Käyttöopas Kotikäyttöön. Version 1.0 FI 17012017 Cat.No. W1-S 10mIU Babyplan varhainen raskaustestin voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
FI Varhainen Raskaustesti Tikku Käyttöopas Kotikäyttöön. Version 1.0 FI 17012017 Cat.No. W1-S 10mIU Babyplan varhainen raskaustestin voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
SARAN JA TUOMAKSEN TARINA
 SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
SARAN JA TUOMAKSEN TARINA Opettajalle Sara on 15-vuotias ja Tuomas 17. He ovat seurustelleet parisen kuukautta. He olivat olleet yhdynnässä ensimmäistä kertaa eräissä bileissä, joissa he olivat myös juoneet
VALMISTEYHTEENVETO. Hygieeninen käsien desinfektio: Vähintään 3 ml STERILLIUM-liuosta hierotaan kuiviin käsiin 30 sekunnin ajan. Ei huuhdella.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI STERILLIUM, liuos iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g liuosta sisältää: Isopropanoli N-propanoli Mesetroniumetyylisulfaatti 45 g 30 g 0,2 g Täydellinen
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI STERILLIUM, liuos iholle 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 100 g liuosta sisältää: Isopropanoli N-propanoli Mesetroniumetyylisulfaatti 45 g 30 g 0,2 g Täydellinen
Säteilyturvakeskuksen määräys turvallisuusluvasta ja valvonnasta vapauttamisesta
 1 (33) LUONNOS 2 -MÄÄRÄYS STUK SY/1/2017 Säteilyturvakeskuksen määräys turvallisuusluvasta ja valvonnasta vapauttamisesta Säteilyturvakeskuksen päätöksen mukaisesti määrätään säteilylain ( / ) 49 :n 3
1 (33) LUONNOS 2 -MÄÄRÄYS STUK SY/1/2017 Säteilyturvakeskuksen määräys turvallisuusluvasta ja valvonnasta vapauttamisesta Säteilyturvakeskuksen päätöksen mukaisesti määrätään säteilylain ( / ) 49 :n 3
VALMISTEYHTEENVETO. Vaikuttava(t) aine(et): Hevosen puhdistettua antiseerumia, jonka vaikuttava aine on tetanusantitoksiini.
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Equilis Tetanus-Serum vet injektioneste, liuos 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava(t) aine(et): Hevosen puhdistettua antiseerumia,
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Equilis Tetanus-Serum vet injektioneste, liuos 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml sisältää: Vaikuttava(t) aine(et): Hevosen puhdistettua antiseerumia,
Toctino (alitretinoiini)
 POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
POTILASESITE Toctino (alitretinoiini) Raskaudenehkäisyohjelma TOC-FI-004-051208-D Tästä esitteestä Tässä esitteessä on tärkeää tietoa Toctino-hoidostanne ja lääkkeen käyttöön liittyvästä mahdollisesta
30 RYHMÄ FARMASEUTTISET TUOTTEET
 30 RYHMÄ FARMASEUTTISET TUOTTEET Huomautuksia 1. Tähän ryhmään eivät kuulu: a) ravintovalmisteet ja juomat (kuten dieettiset, diabeettiset tai "vahvistetut" ravintovalmisteet, lisäravinteet, vahvistavat
30 RYHMÄ FARMASEUTTISET TUOTTEET Huomautuksia 1. Tähän ryhmään eivät kuulu: a) ravintovalmisteet ja juomat (kuten dieettiset, diabeettiset tai "vahvistetut" ravintovalmisteet, lisäravinteet, vahvistavat
RASKAUDEN EHKÄISY SYNNYTYKSEN JÄLKEEN
 RASKAUDEN EHKÄISY SYNNYTYKSEN JÄLKEEN Anneli Kivijärvi LKT, naistentautien ja synnytysten erikoislääkäri, vastaava lääkäri Turun Hyvinvointitoimiala 11.05.2016 Turku, Yleislääkäripäivät Mitkä asiat otetaan
RASKAUDEN EHKÄISY SYNNYTYKSEN JÄLKEEN Anneli Kivijärvi LKT, naistentautien ja synnytysten erikoislääkäri, vastaava lääkäri Turun Hyvinvointitoimiala 11.05.2016 Turku, Yleislääkäripäivät Mitkä asiat otetaan
TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU
 Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Oulun Seudun Ammattiopisto Raportti Page 1 of 6 Turkka Sunnari & Janika Pietilä 23.1.2016 TITRAUKSET, KALIBROINNIT, SÄHKÖNJOHTAVUUS, HAPPOJEN JA EMÄSTEN TARKASTELU PERIAATE/MENETELMÄ Työssä valmistetaan
Vinkkejä opettajille ja odotetut tulokset SIVU 1
 Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Vinkkejä opettajille ja odotetut tulokset SIVU 1 Konteksti palautetaan oppilaiden mieliin käymällä Osan 1 johdanto uudelleen läpi. Kysymysten 1 ja 2 tarkoituksena on arvioida ovatko oppilaat ymmärtäneet
Raskaustesti Puikko. Käyttöopas. Version 1.0 FI Cat.No. W1-M(5.0mm)
 FI Raskaustesti Puikko Käyttöopas Version 1.0 FI 18102017 Cat.No. W1-M(5.0mm) Babyplan raskaustesti on nopea raskaustesti, jonka voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
FI Raskaustesti Puikko Käyttöopas Version 1.0 FI 18102017 Cat.No. W1-M(5.0mm) Babyplan raskaustesti on nopea raskaustesti, jonka voit helposti suorittaa itse. Se havaitsee virtsasta ihmisen koriongonadotropiinin
VALMISTEYHTEENVETO. Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti. Osmolaliteetti: noin 4 000 mosm/kg vettä ph: noin 4
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Kaliumkloridia sisältää: Kaliumkloridi 150 mg/ml, joka vastaa
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addex-Kaliumklorid 150 mg/ml infuusiokonsentraatti 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT 1 ml Addex-Kaliumkloridia sisältää: Kaliumkloridi 150 mg/ml, joka vastaa
Otoskoko 107 kpl. a) 27 b) 2654
 1. Tietyllä koneella valmistettavien tiivisterenkaiden halkaisijan keskihajonnan tiedetään olevan 0.04 tuumaa. Kyseisellä koneella valmistettujen 100 renkaan halkaisijoiden keskiarvo oli 0.60 tuumaa. Määrää
1. Tietyllä koneella valmistettavien tiivisterenkaiden halkaisijan keskihajonnan tiedetään olevan 0.04 tuumaa. Kyseisellä koneella valmistettujen 100 renkaan halkaisijoiden keskiarvo oli 0.60 tuumaa. Määrää
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I
 Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Kemialliset reaktiot ja reaktorit Prosessi- ja ympäristötekniikan perusta I Juha Ahola juha.ahola@oulu.fi Kemiallinen prosessitekniikka Sellaisten kokonaisprosessien suunnittelu, joissa kemiallinen reaktio
Osa A. Täytetään kaikkien naispotilaiden kohdalla
 Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
Tarkastuslista määrättäessä isotretinoiinia naispotilaille: Isotretinoin Actavis (isotretinoiini) 10 mg:n ja 20 mg:n pehmeät kapselit Raskauden ja sikiöaltistuksen ehkäisyohjelma Isotretinoiini on erittäin
KUULUTUSjULKAISU UTLÄGGNINGSSKRIFT 409_22 30. 1;), 10 VII 1969 : Pat,3:it IrL3ddelat. Patenffihakemus Patentansökning 2303/63
 SUOMI FINLAND Patentti- ja rekisterihallitus Patent- och registerstyrelsen KUULUTUSjULKAISU UTLÄGGNINGSSKRIFT 409_22 Kv. IkJlnt. Cl. A 61 k 3/60 Uc/KI. 30. 1;), 10 VII 1969 : Pat,3:it IrL3ddelat Patenffihakemus
SUOMI FINLAND Patentti- ja rekisterihallitus Patent- och registerstyrelsen KUULUTUSjULKAISU UTLÄGGNINGSSKRIFT 409_22 Kv. IkJlnt. Cl. A 61 k 3/60 Uc/KI. 30. 1;), 10 VII 1969 : Pat,3:it IrL3ddelat Patenffihakemus
KUULUTUSJULKAISU r 7. Patentti MY'jnr1.2'_ ty 10 Cl 193 (45) 1i. (go) KvA?mit.a3. (21) Patenttlhakemus Patemensökning (n) HaltemispIllvi AmoöknIquelag
 SUOMI FINLAND (F I) Patentti- ja rekisterihallitus Patent- och registerstyreisen (B]. KUULUTUSJULKAISU r 7 C UTLAGGNINGSSKRIFT 0 Patentti MY'jnr1.2'_ ty 10 Cl 193 (45) 1i (go) KvA?mit.a3 (21) Patenttlhakemus
SUOMI FINLAND (F I) Patentti- ja rekisterihallitus Patent- och registerstyreisen (B]. KUULUTUSJULKAISU r 7 C UTLAGGNINGSSKRIFT 0 Patentti MY'jnr1.2'_ ty 10 Cl 193 (45) 1i (go) KvA?mit.a3 (21) Patenttlhakemus
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa
 Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa TkT Jari Aromaa Teknillinen korkeakoulu Korroosion ja materiaalikemian laboratorio TAUSTAA Kuparin yleinen korroosio voi
Kuparin korroosionopeuden mittaaminen kaasufaasissa loppusijoituksen alkuvaiheessa TkT Jari Aromaa Teknillinen korkeakoulu Korroosion ja materiaalikemian laboratorio TAUSTAA Kuparin yleinen korroosio voi
VALMISTEYHTEENVETO. Busol vet 0,004 mg/ml injektioneste, liuos naudalle, hevoselle, kanille (FI)
 1. ELÄINLÄÄKKEEN NIMI VALMISTEYHTEENVETO Busol vet 0,004 mg/ml injektioneste, liuos naudalle, hevoselle, kanille (FI) 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml injektionestettä sisältää Vaikuttava aine:
1. ELÄINLÄÄKKEEN NIMI VALMISTEYHTEENVETO Busol vet 0,004 mg/ml injektioneste, liuos naudalle, hevoselle, kanille (FI) 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 ml injektionestettä sisältää Vaikuttava aine:
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma. (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Potilaan opas (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä
VALMISTEYHTEENVETO. Täydellisen parenteraalisen ravitsemuksen täydennyksenä vesiliukoisten vitamiinien päivittäisen tarpeen tyydyttämiseksi.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Soluvit infuusiokuiva-aine, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Yksi Soluvit-injektiopullo sisältää: Yksi pullo sisältää vaikuttavia aineita:
Lukion kemia 3, Reaktiot ja energia. Leena Piiroinen Luento 2 2015
 Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Lukion kemia 3, Reaktiot ja energia Leena Piiroinen Luento 2 2015 Reaktioyhtälöön liittyviä laskuja 1. Reaktioyhtälön kertoimet ja tuotteiden määrä 2. Lähtöaineiden riittävyys 3. Reaktiosarjat 4. Seoslaskut
Geeliputkien lähetys ja säilyttäminen
 Geeliputkien lähetys ja säilyttäminen Laboratoriolääketiede 2014 Riitta Tähtelä, FT, sairaalakemisti Mehiläinen Oy Laboratoriopalvelut 1 Verinäytteiden käsittely Suositusten mukaan Näytteet otetaan lisäaineelliseen
Geeliputkien lähetys ja säilyttäminen Laboratoriolääketiede 2014 Riitta Tähtelä, FT, sairaalakemisti Mehiläinen Oy Laboratoriopalvelut 1 Verinäytteiden käsittely Suositusten mukaan Näytteet otetaan lisäaineelliseen
SUO M 1-FI N LAN D 0 KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 43624
 SUO M 1-FI N LAN D 0 KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 43624 Kv. lk./int. Cl. A 61 k 23/02 C 12 k 5/00 30 h 6 Pat.hak. peruutettu Pat.ans. återtagen 3 V 1971 Patenttihakemus Patentansökning 1977/67 Hakemispäivä
SUO M 1-FI N LAN D 0 KUULUTUSJULKAISU UTLAGGNINGSSKRIFT 43624 Kv. lk./int. Cl. A 61 k 23/02 C 12 k 5/00 30 h 6 Pat.hak. peruutettu Pat.ans. återtagen 3 V 1971 Patenttihakemus Patentansökning 1977/67 Hakemispäivä
KEMIALLISET ANALYYSIT TURUN YLIOPISTOSSA
 Biokemian ja elintarvikekemian laitos RAPORTTI 1 (8) Projekti: Siian laatu kalan tarjontaketjussa Dnro: 4682/3516/05 Hankenro: 534589 Raportin laatija: Jukka Pekka Suomela KEMIALLISET ANALYYSIT TURUN YLIOPISTOSSA
Biokemian ja elintarvikekemian laitos RAPORTTI 1 (8) Projekti: Siian laatu kalan tarjontaketjussa Dnro: 4682/3516/05 Hankenro: 534589 Raportin laatija: Jukka Pekka Suomela KEMIALLISET ANALYYSIT TURUN YLIOPISTOSSA
Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe Tehtävä 1 Pisteet / 15
 Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Tampereen yliopisto Henkilötunnus - Lääketieteen ja biotieteiden tiedekunta Sukunimi Bioteknologia tutkinto-ohjelma Etunimet valintakoe pe 18.5.2018 Tehtävä 1 Pisteet / 15 1. Alla on esitetty urheilijan
Lääkealan turvallisuus- ja kehittämiskeskuksen määräys
 Määräys pp.kk.vvvv Dnro 002646/00.01.00/2014 /2014 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys PITKÄLLE KEHITETYSSÄ TERAPIASSA KÄY- TETTÄVIEN LÄÄKKEIDEN (ATMP) VALMISTA- MINEN YKSITTÄISEN POTILAAN
Määräys pp.kk.vvvv Dnro 002646/00.01.00/2014 /2014 Lääkealan turvallisuus- ja kehittämiskeskuksen määräys PITKÄLLE KEHITETYSSÄ TERAPIASSA KÄY- TETTÄVIEN LÄÄKKEIDEN (ATMP) VALMISTA- MINEN YKSITTÄISEN POTILAAN
(12) PATENTTIJULKAISU PATENTSKRIFT. (10) Fl 110234 B. (45) Patentti myönnetty - Patent beviljats 31.12.2002. (51) Kv.lk.7 - Int.kl.
 1111111111 1111111111 1111 11111111 11111 1111 11111111 F1000B (12) PATENTTIJULKAISU PATENTSKRIFT (10) Fl B (45) Patentti myönnetty - Patent beviljats 31.12.2002 SUOMI - FINLAND (FI) PATENTTI- JA REKISTERIHALLITUS
1111111111 1111111111 1111 11111111 11111 1111 11111111 F1000B (12) PATENTTIJULKAISU PATENTSKRIFT (10) Fl B (45) Patentti myönnetty - Patent beviljats 31.12.2002 SUOMI - FINLAND (FI) PATENTTI- JA REKISTERIHALLITUS
2CHEM-A1210 Kemiallinen reaktio Kevät 2017 Laskuharjoitus 7.
 HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
HEM-A0 Kemiallinen reaktio Kevät 07 Laskuharjoitus 7.. Metalli-ioni M + muodostaa ligandin L - kanssa : kompleksin ML +, jonka pysyvyysvakio on K ML + =,00. 0 3. Mitkä ovat kompleksitasapainon vapaan metalli-ionin
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
COLAJUOMAN HAPPAMUUS Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAUSTA Cola-juomien voimakas happamuus johtuu pääosin niiden sisältämästä fosforihaposta. Happamuus saattaa laskea jopa ph
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana
 Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Angitensiiniä konvertoivan entsyymin (ACE:n) estäjät ja angiotensiini II -reseptorin salpaajat: Käyttö raskauden ja imetyksen aikana Valmisteyhteenvedon ja pakkausselosteen hyväksytyt sanoitukset, PhVWP
Raskauden ehkäisy. Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää.
 Raskauden ehkäisy Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää. Jokaisella on oikeus saada oikeaa tietoa ja neuvontaa raskauden ehkäisyn keinoista sekä niiden hyödyistä,
Raskauden ehkäisy Jokaisella on oikeus raskauden ehkäisyyn. Siihen on monta keinoa eli menetelmää. Jokaisella on oikeus saada oikeaa tietoa ja neuvontaa raskauden ehkäisyn keinoista sekä niiden hyödyistä,
ja piirrä sitä vastaavat kaksi käyrää ja tarkista ratkaisusi kuvastasi.
 Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
Harjoituksia yhtälöryhmistä ja matriiseista 1. Ratkaise yhtälöpari (F 1 ja F 2 ovat tuntemattomia) cos( ) F 1 + cos( ) F 2 = 0 sin( ) F 1 + sin( ) F 2 = -1730, kun = -50 ja = -145. 2. Ratkaise yhtälöpari
1. Muunna seuraavat yksiköt. Ammatillisen koulutuksen kaikkien alojen yhteinen matematiikan valmiuksien kilpailu. Oppilaitos:.. Koulutusala:...
 MATEMATIIKAN KOE Ammatillisen koulutuksen kaikkien alojen yhteinen matematiikan valmiuksien kilpailu Nimi: Oppilaitos:.. Koulutusala:... Luokka:.. Sarjat: LAITA MERKKI OMAAN SARJAASI. Tekniikka ja liikenne:..
MATEMATIIKAN KOE Ammatillisen koulutuksen kaikkien alojen yhteinen matematiikan valmiuksien kilpailu Nimi: Oppilaitos:.. Koulutusala:... Luokka:.. Sarjat: LAITA MERKKI OMAAN SARJAASI. Tekniikka ja liikenne:..
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Purevax Rabies injektioneste, suspensio 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttava aine: Rabies rekombinantti canarypox-virus
LIITE I VALMISTEYHTEENVETO 1 1. ELÄINLÄÄKKEEN NIMI Purevax Rabies injektioneste, suspensio 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi 1 ml:n annos sisältää: Vaikuttava aine: Rabies rekombinantti canarypox-virus
PAKKAUSSELOSTE. Addex-Natriumklorid 235 mg/ml infuusiokonsentraatti, liuosta varten. Natriumkloridi
 PAKKAUSSELOSTE Addex-Natriumklorid 235 mg/ml infuusiokonsentraatti, liuosta varten Natriumkloridi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste. Voit tarvita
PAKKAUSSELOSTE Addex-Natriumklorid 235 mg/ml infuusiokonsentraatti, liuosta varten Natriumkloridi Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen. - Säilytä tämä seloste. Voit tarvita
joka voidaan määrittää esim. värinmuutosta seuraamalla tai lukemalla
 REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
REAKTIOT JA TASAPAINO, KE5 Happo-emästitraukset Määritelmä, titraus: Titraus on menetelmä, jossa tutkittavan liuoksen sisältämä ainemäärä määritetään lisäämällä siihen tarkkaan mitattu tilavuus titrausliuosta,
Hivenaineiden perustarpeen sekä hiukan lisääntyneen tarpeen tyydyttämiseen laskimoravitsemuksen yhteydessä.
 VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
VALMISTEYHTEENVETO 1. LÄÄKEVALMISTEEN NIMI Addaven infuusiokonsentraatti, liuosta varten 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Addaven sisältää: 1 ml 1 ampulli (10 ml) Kromikloridi 6 H 2 O 5,33 mikrog
Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus.
 Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus. 2012 Envitop Oy Riihitie 5, 90240 Oulu Tel: 08375046 etunimi.sukunimi@envitop.com www.envitop.com 2/5 KUUSAKOSKI OY Janne Huovinen Oulu 1 Tausta Valtioneuvoston
Kuusakoski Oy:n rengasrouheen kaatopaikkakelpoisuus. 2012 Envitop Oy Riihitie 5, 90240 Oulu Tel: 08375046 etunimi.sukunimi@envitop.com www.envitop.com 2/5 KUUSAKOSKI OY Janne Huovinen Oulu 1 Tausta Valtioneuvoston
niin monta nisäkäs-siirtoktilkua, ettei niiden hengitystien epiteelissä
 SUOMI-FINLAND (I» KUULUTUSJOLKAISU UTLÄGGNINGSSKRIFT 41428 Kv. lk./int. Cl. A 61 k 23/00 30 h 6 ;inn3tt:r 10 ZI 1?(.) Patenttihakemus Patentansökning 983/65 Qit Hakemispäivä Ansökningsdag 22 IV 1965 Alkupäivä
SUOMI-FINLAND (I» KUULUTUSJOLKAISU UTLÄGGNINGSSKRIFT 41428 Kv. lk./int. Cl. A 61 k 23/00 30 h 6 ;inn3tt:r 10 ZI 1?(.) Patenttihakemus Patentansökning 983/65 Qit Hakemispäivä Ansökningsdag 22 IV 1965 Alkupäivä
Elintarviketeollisuuden hapan vaahtopesuneste
 P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
P3-topax 56 Elintarviketeollisuuden hapan vaahtopesuneste OMINAISUUDET Erinomainen poistamaan mineraalisaostumia Poistaa hyvin rasvaa ja proteiinia Erittäin tehokas matalissa konsentraateissa Parannellut
Uusi ejektoripohjainen hiilidioksidin talteenotto-menetelmä. BioCO 2 -projektin loppuseminaari elokuuta 2018, Jyväskylä.
 Uusi ejektoripohjainen hiilidioksidin talteenotto-menetelmä BioCO 2 -projektin loppuseminaari - 30. elokuuta 2018, Jyväskylä Kristian Melin Esityksen sisältö Haasteet CO 2 erotuksessa Mitä uutta ejektorimenetelmässä
Uusi ejektoripohjainen hiilidioksidin talteenotto-menetelmä BioCO 2 -projektin loppuseminaari - 30. elokuuta 2018, Jyväskylä Kristian Melin Esityksen sisältö Haasteet CO 2 erotuksessa Mitä uutta ejektorimenetelmässä
VALMISTEYHTEENVETO. Duramune DAPPi injektiokuiva-aine, kylmäkuivattu ja liuotin suspensiota varten
 VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Duramune DAPPi injektiokuiva-aine, kylmäkuivattu ja liuotin suspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 annos (1 ml) sisältää: Vaikuttavat aineet:
VALMISTEYHTEENVETO 1. ELÄINLÄÄKKEEN NIMI Duramune DAPPi injektiokuiva-aine, kylmäkuivattu ja liuotin suspensiota varten 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS 1 annos (1 ml) sisältää: Vaikuttavat aineet:
Potilaan opas. Acitretin Orifarm 10 mg ja 25 mg. Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/FI/66949
 Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
Potilaan opas Acitretin Orifarm 10 mg ja 25 mg Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma 03/2018/ Tämän esitteen tarkoitus Tämä esite sisältää tärkeitä tietoja etenkin hedelmällisessä iässä
HSC-ohje laskuharjoituksen 1 tehtävälle 2
 HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
HSC-ohje laskuharjoituksen 1 tehtävälle 2 Metanolisynteesin bruttoreaktio on CO 2H CH OH (3) 2 3 Laske metanolin tasapainopitoisuus mooliprosentteina 350 C:ssa ja 350 barin paineessa, kun lähtöaineena
LIITE I VALMISTEYHTEENVETO
 LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Ganireliksi SUN 0,25 mg/0,5 ml injektioneste, liuos esitäytetty ruisku. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen esitäytetty ruisku sisältää
LIITE I VALMISTEYHTEENVETO 1 1. LÄÄKEVALMISTEEN NIMI Ganireliksi SUN 0,25 mg/0,5 ml injektioneste, liuos esitäytetty ruisku. 2. VAIKUTTAVAT AINEET JA NIIDEN MÄÄRÄT Jokainen esitäytetty ruisku sisältää
KALIUMPERMANGANAATIN KULUTUS
 sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
sivu 1/6 Kohderyhmä: Työ on suunniteltu lukiolaisille Aika: n. 1h + laskut KALIUMPERMANGANAATIN KULUTUS TAUSTATIEDOT tarkoitaa veden sisältämien kemiallisesti hapettuvien orgaanisten aineiden määrää. Koeolosuhteissa
Dermovat scalp 0,5 mg/ml liuos iholle Klobetasolipropionaatti
 PAKKAUSSELOSTE Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos sinulla on lisäkysymyksiä, käänny lääkärisi tai apteekin
PAKKAUSSELOSTE Lue tämä seloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen - Säilytä tämä seloste. Voit tarvita sitä myöhemmin. - Jos sinulla on lisäkysymyksiä, käänny lääkärisi tai apteekin
Tausta. Materiaalit ja menetelmät
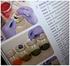 1 Liisa Manner 12.12.2007 Valio Oy T&K, PL 30, 00039 Valio Tuula Sontag Strohm Kari Thessler Elintarviketeknologian laitos, Agnes Sjöbergin katu 2, 00014 Helsingin yliopisto Tausta Työn tavoitteena oli
1 Liisa Manner 12.12.2007 Valio Oy T&K, PL 30, 00039 Valio Tuula Sontag Strohm Kari Thessler Elintarviketeknologian laitos, Agnes Sjöbergin katu 2, 00014 Helsingin yliopisto Tausta Työn tavoitteena oli
COLAJUOMAN HAPPAMUUS
 COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
COLAJUOMAN HAPPAMUUS KOHDERYHMÄ: Työ soveltuu lukion viidennelle kurssille KE5. KESTO: 90 min MOTIVAATIO: Juot paljon kolajuomia, miten ne vaikuttavat hampaisiisi? TAVOITE: Opiskelija pääsee titraamaan.
( B ) (11) KUULUTUSJ'ULKÅISU UTLAGGNINGSSKRIFT 89172. .. - (51) Kv.lk.5 - Int.c1.5 C 07H 15/04, C 07K 3/08, A 61K 39/385 // C 07H 11/04
 ( B ) (11) KUULUTUSJ'ULKÅISU UTLAGGNINGSSKRIFT 89172 C /1:3) P3,',y.. - (51) Kv.lk.5 - Int.c1.5 C 7H 15/4, C 7K 3/8, A 61K 39/385 // C 7H 11/4 -- SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus Patent-
( B ) (11) KUULUTUSJ'ULKÅISU UTLAGGNINGSSKRIFT 89172 C /1:3) P3,',y.. - (51) Kv.lk.5 - Int.c1.5 C 7H 15/4, C 7K 3/8, A 61K 39/385 // C 7H 11/4 -- SUOMI-FINLAND (FI) Patentti- ja rekisterihallitus Patent-
PAKKAUSSELOSTE. Fertavid 600 IU/0,72 ml injektioneste, liuos follitropiini beeta
 PAKKAUSSELOSTE Fertavid 600 IU/0,72 ml injektioneste, liuos follitropiini beeta Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen. Säilytä tämä pakkausseloste. Voit tarvita
PAKKAUSSELOSTE Fertavid 600 IU/0,72 ml injektioneste, liuos follitropiini beeta Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen. Säilytä tämä pakkausseloste. Voit tarvita
MYYNTILUVAN HALTIJA FERRING LÄÄKKEET OY, PL 23, 02241 Espoo, puhelin 0207 401 440
 PAKKAUSSELOSTE MINIRIN 0,1 mg/ml nenätipat, liuos MINIRIN SISÄLTÄÄ: 1 ml nenätippoja sisältää: desmopressiiniasetaattia 0,1 mg vastaten desmopressiinia 0,089 mg sekä apuaineina klooributanolihemihydraattia
PAKKAUSSELOSTE MINIRIN 0,1 mg/ml nenätipat, liuos MINIRIN SISÄLTÄÄ: 1 ml nenätippoja sisältää: desmopressiiniasetaattia 0,1 mg vastaten desmopressiinia 0,089 mg sekä apuaineina klooributanolihemihydraattia
Kemikaalien EU-riskinarviointi ja vähennys
 Kemikaalien EU-riskinarviointi ja vähennys 4 -tert-butyyli-2,6 -dimetyyli-3,5 -dinitroasetofenoni Päivitetty 16.9.2009 CAS nro 81-14-1 Synonyymejä Myskiketoni Musk ketone 3,5-dinitro-2,6-dimetyyli-4-tert-butyyliasetofenoni
Kemikaalien EU-riskinarviointi ja vähennys 4 -tert-butyyli-2,6 -dimetyyli-3,5 -dinitroasetofenoni Päivitetty 16.9.2009 CAS nro 81-14-1 Synonyymejä Myskiketoni Musk ketone 3,5-dinitro-2,6-dimetyyli-4-tert-butyyliasetofenoni
Liite II. Euroopan lääkeviraston tieteelliset johtopäätökset ja myönteisen lausunnon perusteet
 Liite II Euroopan lääkeviraston tieteelliset johtopäätökset ja myönteisen lausunnon perusteet 4 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä arvioinnista, joka koskee valmistetta nimeltä Seasonique
Liite II Euroopan lääkeviraston tieteelliset johtopäätökset ja myönteisen lausunnon perusteet 4 Tieteelliset johtopäätökset Tiivistelmä tieteellisestä arvioinnista, joka koskee valmistetta nimeltä Seasonique
Myös normaali sadevesi on hieman hapanta (ph n.5,6) johtuen ilman hiilidioksidista, joka liuetessaan veteen muodostaa hiilihappoa.
 sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
sivu 1/5 Kohderyhmä: Aika: Työ sopii sekä yläasteelle, että lukion biologiaan ja kemiaan käsiteltäessä ympäristön happamoitumista. Lukion kemiassa aihetta voi myös käsitellä typen ja rikin oksideista puhuttaessa.
Naproxen Orion 25 mg/ml oraalisuspensio. 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO
 Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Naproxen Orion 25 mg/ml oraalisuspensio 26.10.2015, Versio 1.2 RISKIENHALLINTASUUNNITELMAN JULKINEN YHTEENVETO VI.2 VI.2.1 Julkisen yhteenvedon osiot Tietoa sairauden esiintyvyydestä Naproxen Orion on
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille
 Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
Raskauden- ja sikiöaikaisen altistuksen ehkäisyohjelma Tarkastuslista määrättäessä asitretiinia naispotilaille (asitretiini) 10 mg:n ja 25 mg:n kovat kapselit Asitretiini on erittäin teratogeenistä ja
PLUSET vet 500 IU / 500 IU injektiokuiva-aine ja liuotin liuosta varten naudalle
 1. ELÄINLÄÄKKEEN NIMI PLUSET vet 500 IU / 500 IU injektiokuiva-aine ja liuotin liuosta varten naudalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi injektiopullo kylmäkuivattua valmistetta sisältää: Vaikuttavat
1. ELÄINLÄÄKKEEN NIMI PLUSET vet 500 IU / 500 IU injektiokuiva-aine ja liuotin liuosta varten naudalle 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi injektiopullo kylmäkuivattua valmistetta sisältää: Vaikuttavat
Actinobacillus pleuropneumoniae, serotyyppi 2, kanta RP 1*
 1. ELÄINLÄÄKEVALMISTEEN NIMI Hyobac App Multi Vet., injektioneste, emulsio 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Annosta kohti (1,0 ml) Actinobacillus pleuropneumoniae, serotyyppi
1. ELÄINLÄÄKEVALMISTEEN NIMI Hyobac App Multi Vet., injektioneste, emulsio 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Vaikuttavat aineet: Annosta kohti (1,0 ml) Actinobacillus pleuropneumoniae, serotyyppi
ZOELY -käyttäjäopas. nomegestroliasetaatti estradioli 2,5 mg/1,5 mg kalvopäällysteisiä tabletteja
 ZOELY -käyttäjäopas nomegestroliasetaatti estradioli 2,5 mg/1,5 mg kalvopäällysteisiä tabletteja SISÄLLYS Tietoja ZOELY-valmisteesta... 2 Miten ZOELY toimii?... 3 ZOELY on tehty sinua varten... 4 5 Lisätietoja
ZOELY -käyttäjäopas nomegestroliasetaatti estradioli 2,5 mg/1,5 mg kalvopäällysteisiä tabletteja SISÄLLYS Tietoja ZOELY-valmisteesta... 2 Miten ZOELY toimii?... 3 ZOELY on tehty sinua varten... 4 5 Lisätietoja
NOBIVAC RABIES VET. Adjuvantti: Alumiinifosfaatti (2 %) 0,15 ml (vastaten alumiinifosfaattia 3 mg)
 VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Nobivac RABIES Vet 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Per annos (1 ml): Vaikuttava aine: BHK-21-soluviljelmässä kasvatettua ja beeta-propionilaktonilla inaktivoitua
VALMISTEYHTEENVETO 1 ELÄINLÄÄKKEEN NIMI Nobivac RABIES Vet 2 LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Per annos (1 ml): Vaikuttava aine: BHK-21-soluviljelmässä kasvatettua ja beeta-propionilaktonilla inaktivoitua
Luento 8 6.3.2015. Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit
 Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Luento 8 6.3.2015 1 Entrooppiset voimat Vapaan energian muunoksen hyötysuhde Kahden tilan systeemit Entrooppiset voimat 3 2 0 0 S k N ln VE S, S f ( N, m) 2 Makroskooppisia voimia, jotka syntyvät pyrkimyksestä
Clinical impact of serum proteins on drug delivery Felix Kratz, Bakheet Elsadek Journal of Controlled Release 161 (2012)
 Clinical impact of serum proteins on drug delivery Felix Kratz, Bakheet Elsadek Journal of Controlled Release 161 (2012) 429 445 Sampo Kurvonen 25.10.2017 Sisältö Plasmaproteiineista Albumiini Transferriini
Clinical impact of serum proteins on drug delivery Felix Kratz, Bakheet Elsadek Journal of Controlled Release 161 (2012) 429 445 Sampo Kurvonen 25.10.2017 Sisältö Plasmaproteiineista Albumiini Transferriini
JÄTEHUOLLON ERIKOISTYÖ
 Jari-Jussi Syrjä 1200715 JÄTEHUOLLON ERIKOISTYÖ Typpioksiduulin mittaus GASMET-monikaasuanalysaattorilla Tekniikka ja Liikenne 2013 1. Johdanto Erikoistyön tavoitteena selvittää Vaasan ammattikorkeakoulun
Jari-Jussi Syrjä 1200715 JÄTEHUOLLON ERIKOISTYÖ Typpioksiduulin mittaus GASMET-monikaasuanalysaattorilla Tekniikka ja Liikenne 2013 1. Johdanto Erikoistyön tavoitteena selvittää Vaasan ammattikorkeakoulun
1. ELÄINLÄÄKKEEN NIMI. Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS
 1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
1. ELÄINLÄÄKKEEN NIMI Carprofelican vet 50 mg/ml injektioneste, liuos, koirille ja kissoille 2. LAADULLINEN JA MÄÄRÄLLINEN KOOSTUMUS Yksi ml sisältää: Vaikuttava aine: Karprofeeni Apuaineet: Bentsyylialkoholi
VAKOLA Koetusselostus 415
 VAKOLA 101 Helsinki Rukkila Helsinki 43 41 6/ ld Pitäjänmäki O VALTION MAATALOUSKONEIDEN TUTKIMUSLAITOS Finnish Research Institute of Agricultural Engineering 1962 Koetusselostus 415 BUHL-MAIDONJÄÄHDYTIN
VAKOLA 101 Helsinki Rukkila Helsinki 43 41 6/ ld Pitäjänmäki O VALTION MAATALOUSKONEIDEN TUTKIMUSLAITOS Finnish Research Institute of Agricultural Engineering 1962 Koetusselostus 415 BUHL-MAIDONJÄÄHDYTIN
